Тест с ответами по теме «Юношеский артрит с системным началом. Общая диагностика (по утвержденным клиническим рекомендациям)»
Тыльное сгибание в лучезапястном суставе в норме должно составлять 70°.
- артрит
- бесплатно
- Диагностика
- клиническим
- медицинские
- на
- началом
- нмо
- общая
- ответами
- по
- рекомендациям
- с
- системным
- теме
- Тест
- утвержденным
- Юношеский
Тыльное сгибание в лучезапястном суставе в норме должно составлять 70°.
1. «Утиная» похода развивается при поражении
1) Голеностопных суставов;
2) Коленных суставов;
3) Тазобедренных суставов;+
4) Тазобедренных, коленных, голеностопных суставов.
2. Боковое сгибание в шейном отделе позвоночника в норме должно составлять
1) 24°;
2) 40°;+
3) 45°;
4) 50°.
3. В настоящее время, системный юношеский артрит рассматривается как
1) Аутовоспалительное заболевание;+
2) Аутогенеративное заболевание;
3) Аутоиммунное заболевание;
4) Ауторецессивное заболевание.
4. В норме пронацию и супинация в локтевом суставе должен составлять
1) 100°;
2) 70°;
3) 85°;
4) 90°.+
5. В норме угол разгибания в локтевом суставе должен составлять не менее
1) 150°;
2) 170°;
3) 180°;+
4) 190°.
6. В норме угол сгибания в локтевом суставе должен составлять не более
1) 10°;
2) 15°;
3) 20°;+
4) 30°.
7. Варианты походки при поражении суставов при сЮИА?
1) «Походка пьяного»;
2) «Утиная походка»;+
3) «походку Тодда»;
4) Перонеальнуа походка, или степпаж;
5) С быстрым переносом массы тела с больной ноги на здоровую. +
+
8. Внутренняя и наружная ротация в тазобедренном суставе в норме должна составлять не менее
1) 30-35 о;
2) 35-40 о;
3) 40-45 о;+
4) 45-50 о.
9. Где чаще всего локализуются локальные ангионевротические отеки?
1) В области кисти;+
2) В области коленного сустава;
3) В области плеча;
4) В области стопы.
10. Геморрагическая сыпь появляется при
1) Гемафагоцитарном синдроме;+
2) Нунан синдроме;
3) Синдроме Уотерхауса-фридериксена;
4) Синдроме циклической рвоты.
11. Длительность эпизода перикардита составляет
1) 1-2 года;
2) 1-8 месяцев;
3) 1-8 недель;+
4) 6 месяцев.
12. Для сЮА характерно отсутствие связи с главным комплексом гистосовместимости класса
1) Класса I;+
2) Класса II;
3) Класса III;
4) Класса IV.
13. Как внешне выглядят высыпания на коже?
1) Пятна диаметром >10 мм, возвышающиеся или западающие по сравнению с уровнем окружающей кожи;
2) Пятна обычно окружены бледным ободком, в центре элементов более крупного размера формируется очаг просветления;+
3) Пятна представляют собой заполненные прозрачной жидкостью полостные элементы диаметром >10 мм;
4) Пятна представляют собой участки изменения цвета, не возвышающиеся и не западающие по сравнению с окружающей кожей.
14. Какие жалобы при сЮА?
1) Боль в мышцах;+
2) Высыпания на коже, уменьшающиеся на высоте лихорадки;
3) Высыпания на коже, усиливающиеся на высоте лихорадки;+
4) Головная боль;
5) Повышение температуры тела до 38-40°С;+
6) Слабость;+
7) Снижение температуры тела 34°С.
15. Какие урогенитальные инфекции могут быть выяснены при акушерском и гинекологическом анамнезе матери?
1) Вирус Эпштейна-Барр;+
2) Пневмококковая;
3) Протозойная;
4) Хламидийной;+
5) Цитомегаловирусной. +
+
16. Какую информацию нужно выяснить у матери о предыдущих беременностях?
1) Имели ли место внутриутробная гибель плода;+
2) Поздние роды;
3) Преждевременные роды;+
4) Хроническое не вынашивание беременности.+
17. Ладонное сгибание в лучезапястном суставе в норме должно составлять
1) 100°;
2) 70°;
3) 85°;
4) 90°.+
18. Место развития капиллярита при васкулите
1) В подмышечных областях;
2) На ладонной поверхности;+
3) На подошвенной поверхности;+
4) На ягодичных областях.
19. На высоте лихорадки общее состояние детей
1) Среднее;
2) Среднетяжелое;+
3) Стабильное;
4) Тяжелое.+
20. Наличие лихорадки при сЮИА сопровождается подъёмом температуры тела до
1) ≤ 39°C;
2) ≥ 37°C;
3) ≥ 38°C;
4) ≥ 39°C. +
+
21. Отведение в тазобедренных суставах должно быть не менее
1) 120 о;
2) 130 о;
3) 140 о;+
4) 150 о.
22. Перикардит может сопровождаться
1) Болью в области сердца;+
2) Головной болью;
3) Одышкой;+
4) Онемением верхних конечностей;
5) Цианотичностью нижних конечностей.
23. Подошвенное разгибание в голеностопном суставе в норме должно составлять
1) 10°;
2) 15°;
3) 20°;+
4) 25°.
24. При заболеваниях тазобедренных суставов в первую очередь изменяется
1) Внутренняя и наружная ротация;
2) Внутренняя ротация;+
3) Наружная ротация.
25. При лимфаденопатии лимфатические узлы увеличиваются в диаметре до
1) 2-3 см;
2) 3-4 см;
3) 4-6 см;+
4) 5-8 см.
26. При пальпации, лимфатические узлы, как правило
1) Безболезненны;+
2) Болезенные;
3) Мягко- или плотноэластической консистенции;+
4) Не спаянные между собой и с подлежащими тканями;+
5) Неподвижные;
6) Подвижные;+
7) Спаянные между собой и с подлежащими тканями.
27. При поражение каких суставов, больной ходит перемежаясь с больной ноги на здоровую?
1) Коленные суставы;+
2) Локтевые суставы;
3) Лучезапястные суставы;
4) Тазобедренные суставы.+
28. При развитие какого синдрома лимфаденопатия резко нарастает?
1) Гемафагоцитарный синдром;+
2) Нунан синдроме;
3) Синдром Уотерхауса-фридериксена;
4) Синдром циклической рвоты.
29. При физикальном обследовании больного с перикардитом выявляются
1) Выпадение сердечного тона;
2) Приглушенность сердечных тонов;+
3) Расширение границ относительной сердечной тупости;+
4) Ритм галопа;
5) Тахикардия;+
6) Уменьшение границ относительной сердечной тупости;
7) Шум трения перикарда;+
8) Шум трения плевры.
30. При юношеском артрите с системным началом наиболее часто в процесс вовлекаются
1) Голеностопные суставы;+
2) Коленные суставы;+
3) Локтевые суставы;
4) Лучезапястные суставы;+
5) Тазобедренные суставы.
31. Пронация в голеностопном суставе в норме должно составлять
1) 10°;
2) 15°;
3) 20°;+
4) 30°.
32. Развитие гипохромной анемии связывают с гиперпродукцией какого интерлейкина?
1) Интерлейкина 2;
2) Интерлейкина 3;
3) Интерлейкина 4;
4) Интерлейкина 6.+
33. Разгибание в шейном отделе позвоночника в норме должно составлять
1) 10-30°;
2) 30-40°;
3) 30-60°;
4) 50-60°.+
34. Размер пятен достигает
1) 1-3 мм;
2) 2-5 мм;+
3) 3-4 мм;
4) 5-7 мм.
35. Рекомендуется провести осмотр кожных покровов на наличие кого заболевания?
1) Васкулит;+
2) Псориаз;
3) Себорея;
4) Туберкулез кожи.
36. Рекомендуется провести перкуссию границ и аускультацию сердца, для выявления какого заболевания?
1) Миокардит;
2) Перикардит;+
3) Эндокардит.
37. С гиперпродукцией провоспалительных цитокинов связывают развитие клинических проявлений
1) Гепатоспленомегалия;+
2) Лихорадка;+
3) Остеопороз;+
4) Перикардит;
5) Полиморфная сыпь;+
6) Цистит.
38. С гиперпродукцией провоспалительных цитокинов связывают развитие патологических изменений лабораторных показателей
1) Гиперпродукция амилоида А;+
2) Лейкопения;
3) Лейкоцитоз;+
4) С-реактивного белка;+
5) Тромбоцитоз;+
6) Эритроцитоз.
39. Сгибание в шейном отделе позвоночника в норме должно составлять
1) 30-50°;
2) 40-80°;
3) 50-60°;
4) 60-80°.+
40. Сгибание в шейном отделе позвоночника в норме должно составлять
1) 24°;
2) 33°;
3) 45°;+
4) 50°.
41. Супинация в голеностопном суставе в норме должно составлять
Супинация в голеностопном суставе в норме должно составлять
1) 10°;
2) 15°;
3) 20°;
4) 30°.+
42. Тыльное сгибание в голеностопном суставе в норме должно составлять
1) 40 о;
2) 45 о;+
3) 50 о;
4) 55 о.
43. Тыльное сгибание в лучезапястном суставе в норме должно составлять
1) 100°;
2) 70°;+
3) 85°;
4) 90°.
44. Угол разгибания в коленном суставе должен составлять
1) 100 о;
2) 150 о;
3) 170 о;
4) 180 о.+
45. Характер сыпи приюношеском артрите с системным началом
1) Линейная;+
2) Петехиальная;
3) Пятнистая;+
4) Уртикарная;+
5) Эритематозная.
46. Что играет центральную роль в патогенезе сЮИА?
1) Активация врожденной иммунной системы;+
2) Активация приобретённой иммунной системы;
3) Продукция макрофагов;
4) Продукция провоспалительных цитокинов. +
+
47. Что такое юношеский артрит с системным началом?
1) Артрит одного и более суставов, который сопровождается подтвержденной перемежающейся лихорадкой продолжительностью не менее 3-х дней в течение минимум 2-х недель в сочетании с одним или более из перечисленных признаков;+
2) Артрит одного и более суставов, который сопровождается подтвержденной перемежающейся лихорадкой продолжительностью не менее 3-х дней в течение минимум 6-х недель в сочетании с одним или более из перечисленных признаков;
3) Артрит одного и более суставов, который сопровождается подтвержденной перемежающейся лихорадкой продолжительностью не менее 6-х дней в течение минимум 2-х недель в сочетании с одним или более из перечисленных признаков;
4) Артрит одного, который не сопровождается подтвержденной перемежающейся лихорадкой продолжительностью не менее 3-х дней в течение минимум 2-х недель в сочетании с одним или более из перечисленных признаков.
48. Что является причиной развития дефицита железа при сЮА?
Что является причиной развития дефицита железа при сЮА?
1) Секреция гаппоглондина;
2) Секреция гепсидина;+
3) Секреция трансаминазы;
4) Секреция ферритина.
← Тест с ответами по теме «Диагностика и внутрипросветное эндоскопическое удаление неэпителиальных опухолей верхних отделов пищеварительного тракта»↑ Тесты НМО Тест с ответами по теме «Колостома: помощь в психологическом преодолении» →
причины, симптомы, лечение — Онлайн-диагностика
болезнь Стилла- Описание
- Куда обратиться
Описание
Юношеский артрит с системным началом (ЮАС) (МКБ-10: М08.2) является одной из разновидностей (примерно пятая часть) ювенильного артрита, но выделяется среди них более неблагоприятным прогнозом. Данная форма заболевания характеризуется множественными внесуставными поражениями и в половине случаев приводит к инвалидизации, а без адекватного лечения может закончиться летально. ЮАС поражает детей в возрасте младше 16 лет, им с одинаковой частотой болеют лица мужского и женского пола. Примерно девять детей из 100 тысяч страдают этим заболеванием.
ЮАС поражает детей в возрасте младше 16 лет, им с одинаковой частотой болеют лица мужского и женского пола. Примерно девять детей из 100 тысяч страдают этим заболеванием.
Причина заболевания доподлинно не известна. Однако замечено, что дебют заболевания провоцируется рядом возбудителей инфекционных болезней, травмированием сустава, психоэмоциональным стрессовым воздействием, а также может быть детерминирован генетически. СЮА считается особой формой ювенильного артрита, потому что в отличие от него является аутовоспалительным заболеванием, при котором активируется врожденный иммунитет, а главными эффекторными клетками являются моноциты и нейтрофилы, а не лимфоциты. Именно высокие уровни белков S100, продуцируемых этими клетками, отличают СЮА от других заболеваний, протекающих с лихорадочным синдромом. При СЮА период ремиссии может продолжаться несколько лет, но в большинстве случаев течение заболевания заканчивается формированием функциональной суставной недостаточности.
Симптомы юношеского артрита с системным началом
- острое начало;
- интермиттирующая лихорадка;
- пятнисто-папулезная, линейная сыпь на коже, не сопровождающаяся зудом;
- сыпь нестойкая, усиливающаяся на высоте лихорадки;
- нарушение частоты, глубины и ритма дыхания;
- боли в прекардиальной области;
- чувство тяжести в нижних отделах грудной клетки;
- частые пневмонии;
- отечность кистей рук;
- акроцианоз;
- мраморность кожного покрова;
- увеличение регионарных лимфоузлов;
- гепатоспленомегалия;
- артралгии;
- миалгии;
- олиго- и полиартриты;
- стойкие деформации и контрактуры суставов;
- иридоциклит.

Состояние здоровья пациентов с СЮА, в конечном счете, определяется артритом, который у части больных переходит в хроническую форму и персистирует уже после исчезновения системных проявлений и в редких случаях приводит к деструкции суставов и стойкой их деформации.
Диагностика
Помимо характерной клинической симптоматики, которая должна наблюдаться не менее трех месяцев подряд, характерны следующие изменения по данным лабораторных и инструментальных методов исследования:
- Иммунный статус: повышение уровня СРБ, IgM и IgG в сыворотке крови.
- ЭКГ: признаки перегрузки отделов сердца и нарушения коронарного кровообращения
- УЗИ органов брюшной полости: гепатоспленомегалия, паренхиматозные изменения.
- ЭхоКГ: дилатация ЛЖ, снижение фракции выброса ЛЖ, недостаточность митрального, трехстворчатого клапанов, экссудативный перикардит.

- Рентгенография суставов: околосуставной остеопороз, периостальная костная пролиферация.
Лечение юношеского артрита с системным началом
Направлено, в первую очередь, на сохранение функции суставов и минимизацию системных проявлений. Назначаются НПВС, системные кортикостероиды, иммунодепрессанты, генноинженерные биологические препараты, внутрисуставное введение глюкокортикоидов. Важное значение имеют ЛФК и трудотерапия. Всем детям оформляется инвалидность, при необходимости проводится обучение на дому; противопоказано введение вакцин, γ-глобулина, иммуномодуляторов. Большинство детей с СЮА, на фоне адекватной терапии, способны вести нормальный образ жизни.
Основные лекарственные препараты
ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. ПРОКОНСУЛЬТИРУЙТЕСЬ С ВРАЧОМ.
- Адалимумаб (селективный иммунодепрессант). Режим дозирования: вводится подкожно; детям с 13 до 17 лет 40 мг 1 раз в 2 недели, детям с 4 до 12 лет препарат назначают в дозе 24 мг/м2 площади поверхности тела.
 Продолжительность лечения не менее 12 недель.
Продолжительность лечения не менее 12 недель. - Тоцилизумаб (антитела моноклональные). Режим дозирования: детям с массой тела 30 кг в/в из расчета 8 мг/кг; детям с массой тела более 30 кг в/в из расчета 12 мг/кг. Частота введения — 1 раз в 2 недели.
Рекомендации
- Консультация офтальмолога.
- Консультация эндокринолога.
- Консультация отоларинголога.
- Консультация гематолога.
- Консультация ортопеда-травматолога.
- Консультация медицинского генетика.
- Консультация иммунолога.
Тест с ответами по теме «Юношеский артрит с системным началом. Обследование пациентов с подтвержденным диагнозом юношеский артрит в системным началом с стадии активной и неактивной болезни»
psiholog 0 Комментариев артрит, обследование, пациент, подтвержденный диагноз, тест, тест с ответами, юношеский артрит
Юношеский артрит с системным началом (ЮАС) (МКБ-10: М08. 2) является одной из разновидностей (примерно пятая часть) ювенильного артрита, но выделяется среди них более неблагоприятным прогнозом. Данная форма заболевания характеризуется множественными внесуставными поражениями и в половине случаев приводит к инвалидизации, а без адекватного лечения может закончиться летально. ЮАС поражает детей в возрасте младше 16 лет, им с одинаковой частотой болеют лица мужского и женского пола. Примерно девять детей из 100 тысяч страдают этим заболеванием. Причина заболевания доподлинно не известна. Однако замечено, что дебют заболевания провоцируется рядом возбудителей инфекционных болезней, травмированием сустава, психоэмоциональным стрессовым воздействием, а также может быть детерминирован генетически. СЮА считается особой формой ювенильного артрита, потому что в отличие от него является аутовоспалительным заболеванием, при котором активируется врожденный иммунитет, а главными эффекторными клетками являются моноциты и нейтрофилы, а не лимфоциты. Именно высокие уровни белков S100, продуцируемых этими клетками, отличают СЮА от других заболеваний, протекающих с лихорадочным синдромом.
2) является одной из разновидностей (примерно пятая часть) ювенильного артрита, но выделяется среди них более неблагоприятным прогнозом. Данная форма заболевания характеризуется множественными внесуставными поражениями и в половине случаев приводит к инвалидизации, а без адекватного лечения может закончиться летально. ЮАС поражает детей в возрасте младше 16 лет, им с одинаковой частотой болеют лица мужского и женского пола. Примерно девять детей из 100 тысяч страдают этим заболеванием. Причина заболевания доподлинно не известна. Однако замечено, что дебют заболевания провоцируется рядом возбудителей инфекционных болезней, травмированием сустава, психоэмоциональным стрессовым воздействием, а также может быть детерминирован генетически. СЮА считается особой формой ювенильного артрита, потому что в отличие от него является аутовоспалительным заболеванием, при котором активируется врожденный иммунитет, а главными эффекторными клетками являются моноциты и нейтрофилы, а не лимфоциты. Именно высокие уровни белков S100, продуцируемых этими клетками, отличают СЮА от других заболеваний, протекающих с лихорадочным синдромом.
1. Что играет центральную роль в патогенезе сЮИА?
1) Активация приобретённой иммунной системы;
2) Продукция провоспалительных цитокинов; +
3) Активация врожденной иммунной системы; +
4) Продукция макрофагов.
2. Протеинурия у пациентов сЮИА может быть проявлением
1) Мочекаменной болезни;
2) Гломерулонефрита;
3) Амилоидоза почек; +
4) Тромбоза почечных сосудов.
3. Исследование коагуляционного гемостаза рекомендуется при проявлении
1) Синдрома Уотерхауса-фридериксена;
2) Гемафагоцитарного синдрома; +
3) Васкулита; +
4) Псориазе;
5) Нунан синдроме.
4. Причиной повышения креатинина в анализе крови пациентов с сЮА может быть
1) Лечение НПВП; +
2) Лечение метотрексатом; +
3) Прием нифедипина;
4) Лечение иммуномодуляторами.
5. При развитии гемафагоцитарного синдрома развиваются
1) Увелечение СОЭ;
2) Лейкоцитоз;
3) Лейкопения; +
4) Снижается СОЭ; +
5) Тромбоцитоз;
6) Тромбоцитопения; +
7) Эритропения. +
6. Определение иммунофенотипа лимфоцитов проводится пациентам, часто болеющим
1) Микоплазменными инфекциями;
2) Бактериальными инфекциями; +
3) Гнойными инфекциями; +
4) Вирусными инфекциями; +
5) Кишечными инфекциями.
7. При сЮА без инфекционных осложнений прокальцитониновый тест
1) Слабоположительный;
2) Положительный;
3) Отрицательный. +
8. Что является причиной развития дефицита железа при сЮА?
1) Секреция трансаминазы;
2) Секреция гаппоглондина;
3) Секреция ферритина;
4) Секреция гепсидина. +
+
9. С гиперпродукцией провоспалительных цитокинов связывают развитие патологических изменений лабораторных показателей
1) Лейкоцитоз; +
2) Эритроцитоз;
3) Лейкопения;
4) С-реактивного белка; +
5) Тромбоцитоз; +
6) Гиперпродукция амилоида А. +
10. Рекомендуется проведение эзофагогастродуоденоскопии с биопсией каких структур?
1) Слизистой оболочки желудка; +
2) Слизистой оболочки пищевода;
4) Слизистой оболочки тощей кишки.
11. В настоящее время, системный юношеский артрит рассматривается как
1) Аутовоспалительное заболевание; +
2) Аутогенеративное заболевание;
3) Ауторецессивное заболевание;
4) Аутоиммунное заболевание.
12. Что такое юношеский артрит с системным началом?
1) Артрит одного и более суставов, который сопровождается подтвержденной перемежающейся лихорадкой продолжительностью не менее 3-х дней в течение минимум 2-х недель в сочетании с одним или более из перечисленных признаков; +
2) Артрит одного и более суставов, который сопровождается подтвержденной перемежающейся лихорадкой продолжительностью не менее 3-х дней в течение минимум 6-х недель в сочетании с одним или более из перечисленных признаков;
3) Артрит одного и более суставов, который сопровождается подтвержденной перемежающейся лихорадкой продолжительностью не менее 6-х дней в течение минимум 2-х недель в сочетании с одним или более из перечисленных признаков;

13. С какой целью проводят биопсию слизистой оболочки желудка при cЮИА?
1) Для определения, наличия опухолевых процессов в желудке;
2) Для определения язвенных процессов в желудке;
3) Для определения, наличия Helicobacter pylori; +
4) Для оценки состояния желудочной стенки.
14. Клинический анализ крови пациентам с сЮА проводится с целью выявления
1) Нейтропении;
2) Тромбоцитоза; +
3) Лейкоцитоза; +
4) Гипохромной анемии. +
15. С гиперпродукцией провоспалительных цитокинов связывают развитие клинических проявлений
1) Полиморфная сыпь; +
2) Остеопороз; +
3) Цистит;
4) Гепатоспленомегалия; +
5) Перикардит;
6) Лихорадка. +
16. Пациентам с сЮА рекомендуется проводить исследование кала на
1) Стеркобилин;
2) Амиак;
3) Кальпротектин. +
+
17. Какой материал используют для проведения молекулярно-биологического исследования на вирусы герпетической группы?
1) Моча; +
2) Мокрота;
3) Слюна; +
4) Кал;
5) Кровь. +
18. Для сЮА характерно отсутствие связи с главным комплексом гистосовместимости класса
1) Класса II; +
2) Класса IV;
3) Класса III;
4) Класса I.
19. В иммунологическом анализе крови при сЮИА, концентрации IgМ, IgG и СРБ, как правило
1) Не меняются;
2) Повышены; +
3) Понижены.
Системный ЮИА: Новые разработки в понимании патофизиологии и терапии
1. Стилл Г.Ф. О форме хронической болезни суставов у детей. Мед-Чир Транс. 1897; 80: 47–59. Сообщил Proc R Med-Chir Soc 1898; 9: 10–15. [Бесплатная статья PMC] [PubMed] [Google Scholar]
2. Schneider R, Laxer RM. Ювенильный ревматоидный артрит с системным началом. Baillieres Clin Rheumatol. 1998; 12: 245–271. [PubMed] [Google Scholar]
Baillieres Clin Rheumatol. 1998; 12: 245–271. [PubMed] [Google Scholar]
3. Lang BA, et al. Рентгенологические признаки системного ювенильного ревматоидного артрита. J Ревматол. 1995;22:168–173. [PubMed] [Google Scholar]
4. Hadchouel M, Prieur AM, Griscelli C. Острые геморрагические, печеночные и неврологические проявления при ювенильном ревматоидном артрите: возможная связь с лекарствами или инфекцией. J Педиатр. 1985 г., апрель; 106 (4): 561–566. [PubMed] [Google Scholar]
5. Раманан А.В., Шнайдер Р. Синдром активации макрофагов — что в названии! J Ревматол. 2003;30:2513–2516. [PubMed] [Google Scholar]
6. Атрея Б.Х. Является ли синдром активации макрофагов новой сущностью? Клин Эксперт Ревматол. 2002; 20: 121–123. [PubMed] [Академия Google]
7. Гром А.А. Дисфункция NK: общий путь системного начала ювенильного ревматоидного артрита, синдрома активации макрофагов и гемофагоцитарного лимфогистиоцитоза. Ревмирующий артрит. 2004; 50: 689–698. [PubMed] [Google Scholar]
8. Филипович Х.А. Гемофагоцитарный лимфогистиоцитоз. Иммунол Аллергия Клин Н Ам. 2002; 22: 281–300. [Google Scholar]
Филипович Х.А. Гемофагоцитарный лимфогистиоцитоз. Иммунол Аллергия Клин Н Ам. 2002; 22: 281–300. [Google Scholar]
9. Henter JI, Horne A, Arico M, Egeler RM, Filipovich AH, Imashuku S, Ladisch S, McClain K, Webb D, Winiarski J, Janka G. HLH-2004: Диагностические и терапевтические рекомендации по гемопагогоцитарный лимфогистиоцитоз. Педиатр. Рак крови. 2007; 48: 124–131. [PubMed] [Академия Google]
10. Pascual V, Allantaz F, Arce E, Punaro M, Banchereau J. Роль интерлейкина-1 (IL-1) в патогенезе системного ювенильного идиопатического артрита и клинического ответа на блокаду IL-1. J Эксперт Мед. 2005; 201:1479–1486. [Бесплатная статья PMC] [PubMed] [Google Scholar]
11. Раманан А.В., Гром А.А. Относится ли ювенильный идиопатический артрит с системным началом к ювенильному идиопатическому артриту? Ревматология (Оксфорд) 2005;44:1350–1353. [PubMed] [Google Scholar]
12. Fall N, Barnes M, Thornton S, Luyrink L, Olson J, Ilowite NT, et al. Профилирование экспрессии генов в периферической крови пациентов с нелеченным впервые выявленным системным ювенильным идиопатическим артритом выявляет молекулярную гетерогенность, которая может предсказывать синдром активации макрофагов. Ревмирующий артрит. 2007;56:3793–3804. [PubMed] [Google Scholar]
Ревмирующий артрит. 2007;56:3793–3804. [PubMed] [Google Scholar]
13. Ogilvie EM, Khan A, Hubank M, Kellam P, Woo P. Профили экспрессии специфических генов при системном ювенильном идиопатическом артрите. Ревмирующий артрит. 2007; 56: 1954–1965. [PubMed] [Google Scholar]
14. Фрош М., Рот Дж. Новое понимание системного ювенильного идиопатического артрита — от патофизиологии до лечения. Ревматология (Оксфорд) 2008;47:121–125. [PubMed] [Google Scholar]
15. Барнс М.Г., Гром А.А., Томпсон С.Д., Иловите Н.Т., Олсон Дж.С., Шерри Д.Д., Готлиб Б.С., Аронов Б.Дж., Павлидис П., Хинце С., Торнтон С., Гриффин Т.А., Колберт К.А., Стекло ДН. Сигнатуры экспрессии генов при новом начале нелеченного ювенильного идиопатического артрита. Ревмирующий артрит. 2009 г.;60:2101–2112. [Бесплатная статья PMC] [PubMed] [Google Scholar]
16. Allantaz F, Chaussabel D, Stichweh D, Bennett L, Allman W, Mejias A, et al. Микрочипы лейкоцитов крови для диагностики ювенильного идиопатического артрита с системным началом и наблюдения за реакцией на блокаду IL-1.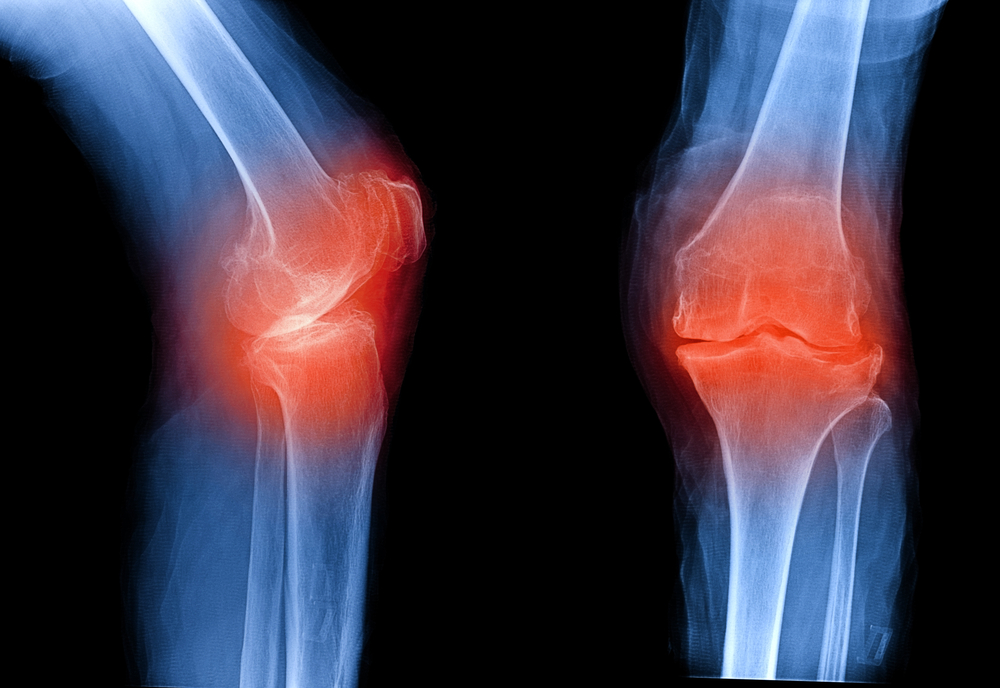 J Эксперт Мед. 2007; 204:2131–2144. [Бесплатная статья PMC] [PubMed] [Google Scholar]
J Эксперт Мед. 2007; 204:2131–2144. [Бесплатная статья PMC] [PubMed] [Google Scholar]
17. Beutler B. Выводы, вопросы и возможности передачи сигналов Toll-подобных рецепторов. Природа. 2004; 430: 257–263. [PubMed] [Академия Google]
18. Халл К.М., Шохам Н., Че Дж.Дж., Аксентиевич И., Кастнер Д.Л. Расширяющийся спектр системных аутовоспалительных заболеваний и их ревматических проявлений. Курр Опин Ревматол. 2003; 15:61–69. [PubMed] [Google Scholar]
19. Church LD, Cook GP, McDermott MF. Праймер: инфламмасомы и интерлейкин 1β при воспалительных заболеваниях. Nature Clin Практика Rheumatol. 2008; 4:34–42. [PubMed] [Google Scholar]
20. Непом Б.Г., Гласс Д.Н. Ювенильный ревматоидный артрит и HLA: отчет семинара Park City III. Дж. Ревматол. 1992;33 приложение:70–74. [PubMed] [Google Scholar]
21. Thompson SD, et al. Полногеномное сканирование на наличие ювенильного ревматоидного артрита в пораженных семьях родственных пар свидетельствует о сцеплении. Ревмирующий артрит. 2004;50(9):2920–2930. [PubMed] [Google Scholar]
Ревмирующий артрит. 2004;50(9):2920–2930. [PubMed] [Google Scholar]
22. Date Y, et al. Выявление генетического фактора риска системного ювенильного ревматоидного артрита в 5′-фланкирующей области гена TNF-альфа и генов HLA. Ревмирующий артрит. 1999;42:2577–2582. [PubMed] [Академия Google]
23. Фишман Д. и соавт. Влияние новых полиморфизмов гена интерлейкина-6 (IL-6) на транскрипцию IL-6 и уровни IL-6 в плазме, а также связь с ювенильным хроническим артритом с системным началом. Джей Клин Инвест. 1998; 102:1369–1376. [Бесплатная статья PMC] [PubMed] [Google Scholar]
24. Ogilvie EM, et al. Аллель -174G гена интерлейкина-6 придает предрасположенность к системному артриту у детей: многоцентровое исследование с использованием семей с простым и множественным ювенильным идиопатическим артритом. Ревмирующий артрит. 2003;48:3202–3206. [PubMed] [Академия Google]
25. Донн Р.П. и соавт. Новый полиморфизм 5′-фланкирующей области фактора, ингибирующего миграцию макрофагов, связан с ювенильным идиопатическим артритом с системным началом. Ревмирующий артрит. 2001; 44: 1782–1785. [PubMed] [Google Scholar]
Ревмирующий артрит. 2001; 44: 1782–1785. [PubMed] [Google Scholar]
26. De Benedetti F, et al. Функциональная и прогностическая значимость полиморфизма -173 гена ингибирующего фактора миграции макрофагов при ювенильном идиопатическом артрите с системным началом. Ревмирующий артрит. 2003; 48: 1398–1407. [PubMed] [Академия Google]
27. Wittkowski H, Frosch M, Wulffraat N, Goldbach-Mansky R, Kallinich T, Kuemmerle-Deschner J, et al. S100A12 представляет собой новый молекулярный маркер, отличающий ювенильный идиопатический артрит с системным началом от других причин лихорадки неизвестного происхождения. Ревмирующий артрит. 2008;58:3924–3931. [Бесплатная статья PMC] [PubMed] [Google Scholar]
28. Frosch M, Ahlmann M, Vogl T, Wittkowski H, Wulffraat N, Foell D, et al. Комплекс миелоидных белков 8 и 14, новый лиганд толл-подобного рецептора 4 и интерлейкин-1бета образуют механизм положительной обратной связи при ювенильном идиопатическом артрите с системным началом. Ревмирующий артрит. 2009 г.;60:883–891. [PubMed] [Google Scholar]
2009 г.;60:883–891. [PubMed] [Google Scholar]
29. Vogl T, Tenbrock K, Ludwig S, Leukert N, Ehrhardt C, van Zoelen MA, et al. Mrp8 и Mrp14 являются эндогенными активаторами Toll-подобного рецептора 4, способствуя летальному шоку, индуцированному эндотоксином. Нат Мед. 2007; 13:1042–1049. [PubMed] [Google Scholar]
30. Maeno N, Takei S, Imanaka H, Yamamoto K, Kuriwaki K, Kawano Y, et al. Повышенная экспрессия интерлейкина-18 в костном мозге пациента с системным ювенильным идиопатическим артритом и нераспознанным синдромом активации макрофагов. Ревмирующий артрит. 2004 июнь; 50 (6): 1935–1938. [PubMed] [Google Scholar]
31. Де Бенедетти Ф., Мартини А. Является ли системный ювенильный ревматоидный артрит заболеванием, опосредованным интерлейкином 6? J Ревматол. 1998; 25: 203–207. [PubMed] [Google Scholar]
32. Де Бенедетти Ф., Масса М., Роббиони П., Равелли А., Бурджио Г.Р., Мартини А. Корреляция уровней интерлейкина-6 в сыворотке с поражением суставов и тромбоцитозом при системном ювенильном ревматоидном артрите. Ревмирующий артрит. 1991; 34: 1158–1163. [PubMed] [Google Scholar]
Ревмирующий артрит. 1991; 34: 1158–1163. [PubMed] [Google Scholar]
33. De Benedetti F, Meazza C, Oliveri M, Pignatti P, Vivarelli M, Alonzi T, et al. Влияние ИЛ-6 на ИФР-связывающий белок-3: исследование на мышах, трансгенных по ИЛ-6, и у пациентов с системным ювенильным идиопатическим артритом. Эндокринология. 2001; 142:4818–4826. [PubMed] [Академия Google]
34. Cazzola M, Ponchio L, De BF, Ravelli A, Rosti V, Beguin Y, et al. Дефектное обеспечение железом для эритропоэза и адекватная продукция эндогенного эритропоэтина при анемии, связанной с системным началом ювенильного хронического артрита. Кровь. 1996; 87: 4824–4830. [PubMed] [Google Scholar]
35. Вербский Дж. В., Уайт А. Дж. Эффективное применение рекомбинантного антагониста рецептора интерлейкина 1 анакинры при резистентном к терапии ювенильном ревматоидном артрите с системным началом. J Ревматол. 2004;31:2071–2075. [PubMed] [Академия Google]
36. Иригойен П.И., Олсон Дж., Хом С., Иловите Н.Т. Лечение системного ювенильного ревматоидного артрита анакинрой. Ревмирующий артрит. 2004; 50 приложение: S437. [Google Scholar]
Ревмирующий артрит. 2004; 50 приложение: S437. [Google Scholar]
37. Хенриксон М. Эффективность анакинры при рефрактерном системном артрите. Ревмирующий артрит. 2004; 50 приложение: S438. [Google Scholar]
38. Prieur AM, et al. Специфический ингибитор интерлейкина-1 в сыворотке крови и моче детей с системным ювенильным хроническим артритом. Ланцет. 1987; 2 (8570): 1240–1242. [PubMed] [Академия Google]
39. Gattorno M, Piccini A, Lasiglie D, Tassi S, Brisca G, Carta S, et al. Характер ответа на лечение антиинтерлейкином-1 различает две подгруппы пациентов с ювенильным идиопатическим артритом с системным началом. Ревмирующий артрит. 2008; 58: 1505–1515. [PubMed] [Google Scholar]
40. Behrens EM, Beukelman T, Paessler M, Cron RQ. Синдром скрытой активации макрофагов у больных системным ювенильным идиопатическим артритом. J Ревматол. 2007; 34:1133–1138. [PubMed] [Академия Google]
41. Bleesing J, Prada A, Siegel DM, Villanueva J, Olson J, Ilowite NT, et al. Диагностическое значение растворимого CD163 и альфа-цепи растворимого рецептора интерлейкина-2 при синдроме активации макрофагов и нелеченом новом начале системного ювенильного идиопатического артрита. Ревмирующий артрит. 2007; 56: 965–971. [PubMed] [Google Scholar]
Диагностическое значение растворимого CD163 и альфа-цепи растворимого рецептора интерлейкина-2 при синдроме активации макрофагов и нелеченом новом начале системного ювенильного идиопатического артрита. Ревмирующий артрит. 2007; 56: 965–971. [PubMed] [Google Scholar]
42. Авчин Т., Це С.М.Л., Шнайдер Р., Нган Б., Сиверман Э.Д. Синдром активации макрофагов как клиническое проявление ревматических заболеваний в детском возрасте. J Педиатр. 2006; 148: 683–686. [PubMed] [Академия Google]
43. Schaer DJ, Schleiffenbaum B, Kurrer M, Imhof A, Bachli E, Fehr J, Moller HJ, Moestrup SK, Schaffner A. Растворимый гемоглобин-гаптоглобиновый поглотитель рецептора CD163 как линейно-специфический маркер реактивного гемофагоцитарного синдрома. Евр Дж Гемотол. 2005; 74: 6–10. [PubMed] [Google Scholar]
44. Kristiansen M, Graversen JH, Jacobsen, Sonne O, Hoffman HJ, Law S, Moestrup SK. Идентификация рецептора поглотителя гемоглобина. Природа. 2001; 409:198–201. [PubMed] [Академия Google]
45. Поршерей Ф., Вио С., Риманиол А.С., Леоне Б., Самах Н., Дереуддре-Боске Д., Гра Д.Г. Переключение активации макрофагов: актив для разрешения воспаления. Клин Эксп Иммунол. 2005; 142: 481–489. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Поршерей Ф., Вио С., Риманиол А.С., Леоне Б., Самах Н., Дереуддре-Боске Д., Гра Д.Г. Переключение активации макрофагов: актив для разрешения воспаления. Клин Эксп Иммунол. 2005; 142: 481–489. [Бесплатная статья PMC] [PubMed] [Google Scholar]
46. Мантовани А., Соццани С., Локати М., Аллавена П., Сика А. Поляризация макрофагов: ассоциированные с опухолью макрофаги как парадигма для поляризованных мононуклеарных фагоцитов М2. Тренды Иммунол. 2002; 23: 549–555. [PubMed] [Академия Google]
47. Такахаши А., Мори М., Наруто Т., Накадзима С., Миямаэ Т., Имагава Т., Ёкота С. Роль гемоксигеназы-1 в системном начале ювенильного идиопатического артрита. Мод Ревматол. 2009; 19: 302–308. [PubMed] [Google Scholar]
48. Stepp SE, Dufourcq-Lagelouse R, Le DF, Bhawan S, Certain S, Mathew PA, et al. Дефекты гена перфорина при семейном гемофагоцитарном лимфогистиоцитозе. Наука. 1999; 286:1957–1959. [PubMed] [Google Scholar]
49. Feldmann J, Callebaut I, Raposo G, Certain S, Bacq D, Dumont C, et al. Munc13-4 необходим для слияния цитолитических гранул и мутирует в форме клетки семейного гемофагоцитарного лимфогистиоцитоза (FHL3). 2003; 115: 461–473. [PubMed] [Академия Google]
Munc13-4 необходим для слияния цитолитических гранул и мутирует в форме клетки семейного гемофагоцитарного лимфогистиоцитоза (FHL3). 2003; 115: 461–473. [PubMed] [Академия Google]
50. Zur Stadt U, Schmidt S, Kasper B, Beutel K, Diler AS, Henter JI, et al. Связывание семейного гемофагоцитарного лимфогистиоцитоза (FHL) 4-го типа с хромосомой 6q24 и идентификация мутаций синтаксин 11. Hum Mol Genet. 2005 г., 15 марта; 14 (6): 827–834. [PubMed] [Google Scholar]
51. Menasche G, Pastural E, Feldman J, et al. Мутации в Rab27a вызывают синдром Гришелли, связанный с гемофагоцитарным синдромом. Нат Генетика. 2000; 25: 173–176. [PubMed] [Академия Google]
52. Барбоза М.Д., Нгуен К.А., Чернев В.Т., и соавт. Идентификация гомологичных генов бежевого и синдрома Чедиака-Хигаси (LYST) Природа. 1996; 382: 262–265. [Бесплатная статья PMC] [PubMed] [Google Scholar]
53. Coffey AJ, Brooksbank RA, Brandau O, et al. Реакция хозяина на инфекцию EBV при Х-сцепленном лимфопролиферативном заболевании является результатом мутаций в гене, кодирующем Sh3-домен.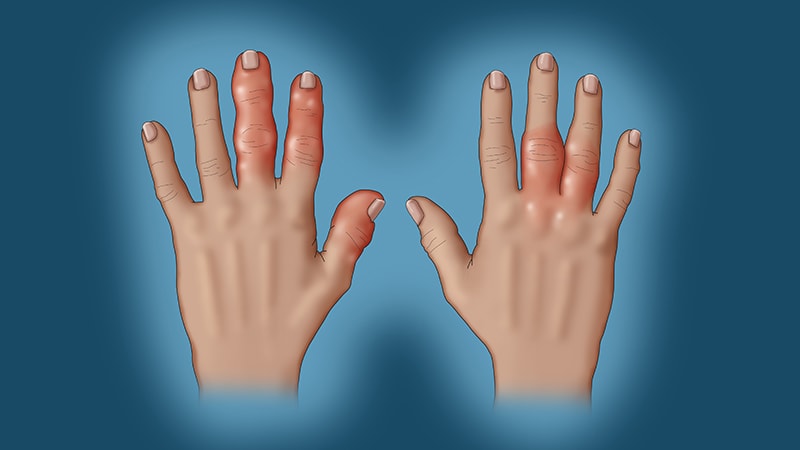 Нат Жене. 1998;20:129. [PubMed] [Google Scholar]
Нат Жене. 1998;20:129. [PubMed] [Google Scholar]
54. Воскобойник И., Смит М.Дж., Трапани Дж.А. Опосредованная перфорином гибель клеток-мишеней и иммунный гомеостаз. Нат Рев Иммунол. 2006; 6:940–952. [PubMed] [Google Scholar]
55. Stepp SE, Dufourcq-Lagelouse R, Le DF, Bhawan S, Certain S, Mathew PA, et al. Дефекты гена перфорина при семейном гемофагоцитарном лимфогистиоцитозе. Наука. 1999; 286:1957–1959. [PubMed] [Google Scholar]
56. Wulffraat NM, Rijkers GT, Elst E, Brooimans R, Kuis W. Снижение экспрессии перфорина при системном ювенильном идиопатическом артрите восстанавливается путем трансплантации аутологичных стволовых клеток. Ревматология (Оксфорд) 2003;42:375–379. [PubMed] [Академия Google]
57. Гром А.А., Вильянуэва Дж., Ли С., Гольдмунц Э.А., Пассо М.Х., Филипович А. Дисфункция естественных клеток-киллеров у пациентов с системным ювенильным ревматоидным артритом и синдромом активации макрофагов. J Педиатр. 2003; 142: 292–296. [PubMed] [Google Scholar]
58. Zhang K, Biroschak J, Glass DN, Thompson SD, Finkel T, Passo MH, et al. Синдром активации макрофагов у пациентов с системным ювенильным идиопатическим артритом связан с полиморфизмом MUNC13-4. Ревмирующий артрит. 2008;58:2892–2896. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Zhang K, Biroschak J, Glass DN, Thompson SD, Finkel T, Passo MH, et al. Синдром активации макрофагов у пациентов с системным ювенильным идиопатическим артритом связан с полиморфизмом MUNC13-4. Ревмирующий артрит. 2008;58:2892–2896. [Бесплатная статья PMC] [PubMed] [Google Scholar]
59. de Jager W, Hoppenreijs EP, Wulffraat NM, Wedderburn LR, Kuis W, Prakken BJ. Признаки цитокинов крови и синовиальной жидкости у пациентов с ювенильным идиопатическим артритом: перекрестное исследование. Энн Реум Дис. 2007; 66: 589–598. [Бесплатная статья PMC] [PubMed] [Google Scholar]
60. Iannello A, Samarani S, Debbeche O, Ahmad R, Boulassel MR, Tremblay C, et al. Возможная роль интерлейкина-18 в иммунопатогенезе СПИДа: участие в братоубийственном уничтожении NK-клеток. Дж Вирол. 2009 г.Июнь; 83 (12): 5999–6010. [Бесплатная статья PMC] [PubMed] [Google Scholar]
61. Ву П. Системный ювенильный идиопатический артрит: диагностика, лечение и исход. Nature Clinical Practice Ревматология.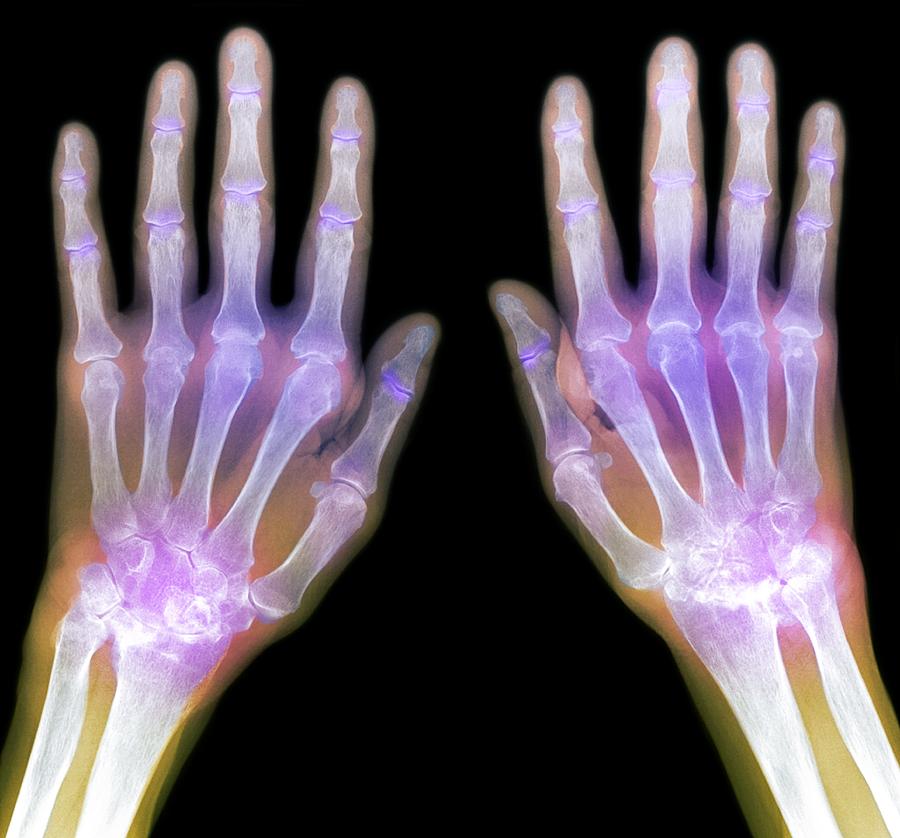 2006; 2: 28–34. [PubMed] [Google Scholar]
2006; 2: 28–34. [PubMed] [Google Scholar]
62. Lehman TJ, Schechter SJ, Sundel RP, Oliveira SK, Huttenlocher A, Onel KB. Талидомид для лечения тяжелого системного омсета ювенильного ревматоидного артрита: многоцентровое исследование. J Педиатр. 2004; 145:856–857. [PubMed] [Google Scholar]
63. Уоллес К.А., Шерри Д.Д. Испытание внутривенного пульс-циклофосфамида и метилпреднизолона при лечении тяжелого системного ювенильного ревматоидного артрита. Ревмирующий артрит. 1997;40:1852–1855. [PubMed] [Google Scholar]
64. Wulffraat NM, van Rooijen EM, Tewarie R, Brinkman D, Prakken B, Kuis W. Современные перспективы трансплантации аутологичных стволовых клеток при тяжелом ювенильном идиопатическом артрите. Аутоиммунитет. 2008; 41: 632–638. [PubMed] [Google Scholar]
65. Halle F, Prieur AM. Оценка метотрексата при лечении ювенильного хронического артрита в зависимости от подтипа. Клин Эксперт Ревматол. 1991; 9: 297–302. [PubMed] [Google Scholar]
66. Speckmaier M, et al.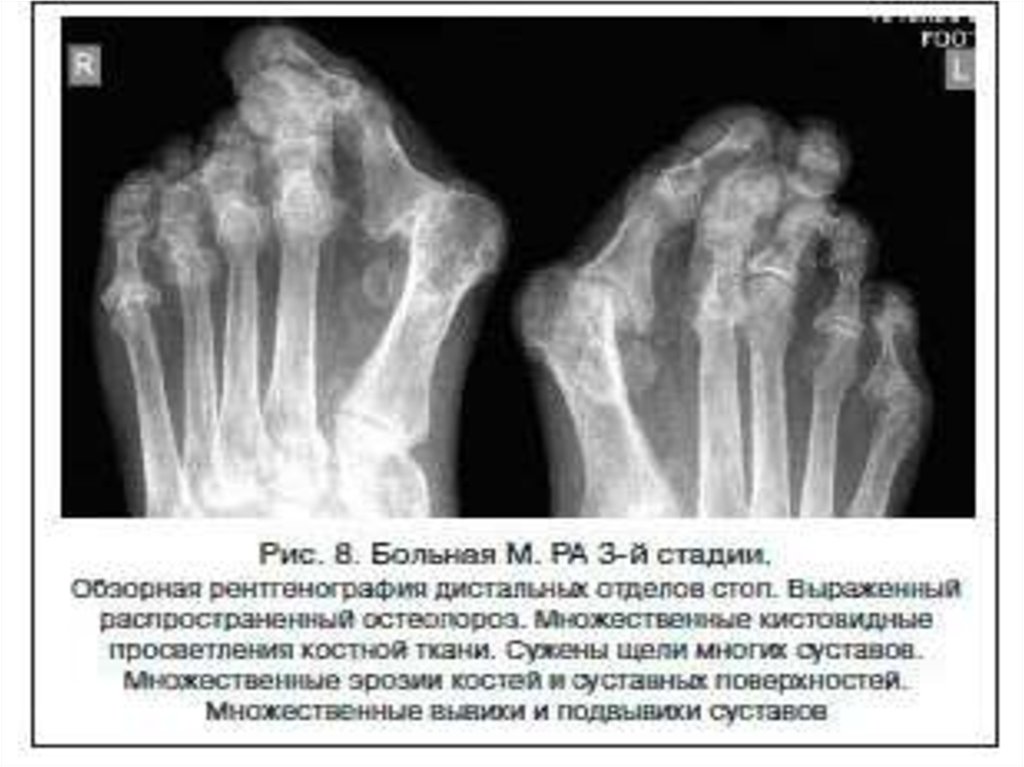 Низкие дозы метотрексата при ювенильном хроническом артрите с системным началом. Клин Эксперт Ревматол. 1989;7:647–650. [PubMed] [Google Scholar]
Низкие дозы метотрексата при ювенильном хроническом артрите с системным началом. Клин Эксперт Ревматол. 1989;7:647–650. [PubMed] [Google Scholar]
67. Woo P, et al. Рандомизированное, плацебо-контролируемое, перекрестное исследование низких доз перорального метотрексата у детей с распространенным олигоартикулярным или системным артритом. Ревмирующий артрит. 2000; 43: 1849–1857. [PubMed] [Google Scholar]
68. Lovell DJ, Reiff A, Ilowite NT, Wallace CA, Chon Y, Lin SL, et al. Безопасность и эффективность непрерывной терапии этанерцептом в течение восьми лет у пациентов с ювенильным ревматоидным артритом. Ревмирующий артрит. 2008;58:1496–1504. [PubMed] [Google Scholar]
69. Quartier P, Taupin P, Bourdeaut F, Lemelle I, Pillet P, Bost M, et al. Эффективность этанерцепта при лечении ювенильного идиопатического артрита в зависимости от типа дебюта. Ревмирующий артрит. 2003;48:1093–1101. [PubMed] [Google Scholar]
70. Horneff G, Schmeling H, Biedermann T, Foeldvari I, Ganser G, Girschick HJ, et al. Немецкий регистр этанерцепта для лечения ювенильного идиопатического артрита. Энн Реум Дис. 2004; 63: 1638–1644. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Немецкий регистр этанерцепта для лечения ювенильного идиопатического артрита. Энн Реум Дис. 2004; 63: 1638–1644. [Бесплатная статья PMC] [PubMed] [Google Scholar]
71. Kimura Y, Pinho P, Walco G, Higgins G, Hummell D, Szer I, et al. Терапия этанерцептом у пациентов с рефрактерным системным началом ювенильного ревматоидного артрита. J Ревматол. 2005; 32: 935–942. [PubMed] [Google Scholar]
72. Руссо Р.А., Кацикас М.М. Клиническая ремиссия у больных системным ювенильным идиопатическим артритом, получавших препараты против фактора некроза опухоли. J Ревматол. 2009; 36: 1078–1082. [PubMed] [Google Scholar]
73. Lequerre T, Quartier P, Rosellini D, Alaoui F, De Bandt M, Mejjad O, et al. Лечение антагонистом рецептора интерлейкина-1 (анакинра) у пациентов с ювенильным идиопатическим артритом с системным началом или болезнью Стилла у взрослых: предварительный опыт во Франции. Энн Реум Дис. 2008; 67: 302–308. [PubMed] [Академия Google]
74. Ву П. Анакинра лечение системного ювенильного идиопатического артрита и болезни Стилла у взрослых. Энн Реум Дис. 2008; 67: 281–282. [PubMed] [Google Scholar]
Энн Реум Дис. 2008; 67: 281–282. [PubMed] [Google Scholar]
75. Динарелло, Калифорния. Терапевтические стратегии по снижению активности IL-1 при лечении местного и системного воспаления. Курр Опин Фармакол. 2004; 4: 378–385. [PubMed] [Google Scholar]
76. Goldbach-Mansky, et al. Пилотное исследование по оценке безопасности и эффективности ингибитора интерлейкина-1 длительного действия рилонацепта (ловушка интерлейкина-1) у пациентов с семейным холодовым аутовоспалительным синдромом. Ревмирующий артрит. 2008; 58: 2432–2442. [Бесплатная статья PMC] [PubMed] [Google Scholar]
77. Ву П., Уилкинсон Н., Приер А. М., Саутвуд Т., Леоне В., Ливермор П. и соавт. Открытое исследование фазы II однократных возрастающих доз MRA у детей европеоидной расы с тяжелым системным ювенильным идиопатическим артритом: доказательство принципа эффективности блокады рецепторов IL6 при этом типе артрита и демонстрация длительного клинического улучшения. Артрит Res Ther. 2005; 7: Р1281–Р1288. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [Google Scholar]
78. Yokota S, Imagawa T, Mori M, Miyamae T, Aihara Y, Takei S, et al. Эффективность и безопасность тоцилизумаба у пациентов с ювенильным идиопатическим артритом с системным началом: рандомизированное двойное слепое плацебо-контролируемое исследование III фазы отмены. Ланцет. 2008;371:998–1006. [PubMed] [Google Scholar]
Относится ли ювенильный идиопатический артрит с системным началом к ювенильному идиопатическому артриту? | Ревматология
Журнальная статья
А.В.Раманан,
А. В. Раманан
Ищите другие работы этого автора на:
Оксфордский академический
пабмед
Google ученый
А. А. Гром
А. А. Гром
Ищите другие работы этого автора на:
Оксфордский академический
пабмед
Google ученый
Ревматология , том 44, выпуск 11, ноябрь 2005 г.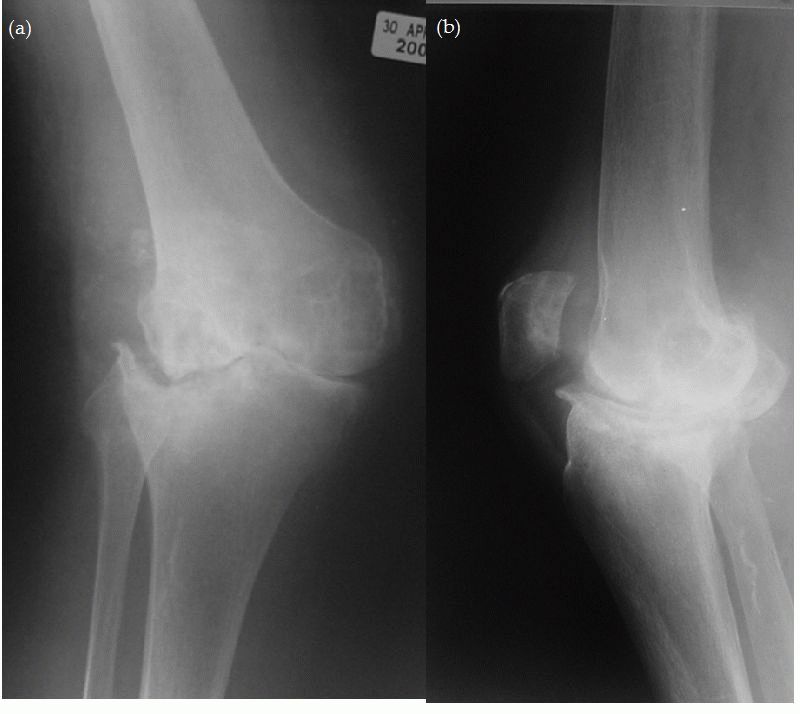 , страницы 1350–1353, https://doi.org/10.1093/rheumatology/keh710
, страницы 1350–1353, https://doi.org/10.1093/rheumatology/keh710
Опубликовано:
14 июня 2005 г.
История статьи
Получено:
11 мая 2005 г.
Получена редакция:
13 мая 2005 г.
Опубликовано:
14 июня 2005 г. PDF
- Содержание статьи
- Рисунки и таблицы
- видео
- Аудио
- Дополнительные данные
Цитировать
Cite
А. В. Раманан, А. А. Гром, Относится ли ювенильный идиопатический артрит с системным началом к ювенильному идиопатическому артриту?, Rheumatology , том 44, выпуск 11, ноябрь 2005 г., страницы 1350–1353, https://doi.org /10.1093/ревматология/keh710
В. Раманан, А. А. Гром, Относится ли ювенильный идиопатический артрит с системным началом к ювенильному идиопатическому артриту?, Rheumatology , том 44, выпуск 11, ноябрь 2005 г., страницы 1350–1353, https://doi.org /10.1093/ревматология/keh710
Выберите формат Выберите format.ris (Mendeley, Papers, Zotero).enw (EndNote).bibtex (BibTex).txt (Medlars, RefWorks)
Закрыть
Разрешения
- Электронная почта
- Твиттер
- Фейсбук
- Подробнее
Фильтр поиска панели навигации РевматологияЭтот выпускЖурналы Британского общества ревматологииРевматологияКнигиЖурналыOxford Academic Термин поиска мобильного микросайта
Закрыть
Фильтр поиска панели навигации РевматологияЭтот выпускЖурналы Британского общества ревматологииРевматологияКнигиЖурналыOxford Academic Термин поиска на микросайте
Advanced Search
Abstract
«Наука есть систематическая классификация опыта»
Джордж Генри Льюис (1817–1878 гг. ), английский философ, критик, драматург, ученый.
), английский философ, критик, драматург, ученый.
Ювенильный идиопатический артрит (ЮИА) встречается примерно у 1 из 1000 детей. Самое раннее официальное описание этого заболевания было сделано сэром Джорджем Фредериком Стиллом в 1897 году [1]. Эта работа была проделана, когда он был регистратором в больнице для больных детей на Грейт-Ормонд-стрит в Лондоне [2]. В этом первоначальном описании 19 пациентов он определил три типа артрита, один из которых стал известен позже как болезнь Стилла [теперь известный как ювенильный идиопатический артрит с системным началом (ЮИА)]. В течение следующих нескольких десятилетий стало понятно, что одна форма артрита у детей сильно отличается и преобладает наличием системных проявлений. За последние два десятилетия несколько детских ревматологов объединились для классификации ювенильного артрита в целях лучшей идентификации и исследования заболевания. Все это время системная форма ювенильного артрита всегда выделялась в отдельную группу; фактически в течение нескольких десятилетий (и даже сейчас в некоторых странах) системная форма ювенильного артрита называлась болезнью Стилла. В этой статье мы попытаемся выделить причины, по которым мы считаем, что SoJIA, возможно, не лучше всего сохраняется в компании JIA.
В этой статье мы попытаемся выделить причины, по которым мы считаем, что SoJIA, возможно, не лучше всего сохраняется в компании JIA.
ЮИА с системным началом, синдром активации макрофагов, гемофагоцитарный лимфогистиоцитоз
Эпидемиология
СоЮИА составляет 10–20% всех ЮИА [3]. Однако две трети смертности при ЮИА связаны с СоЮИА [4, 5]. Мы считаем, что между SoJIA и другими JIA больше различий, чем сходств. Считается, что заболеваемость SoJIA составляет около 0,4–0,8 на 100 000. В отличие от 2-3-кратного преобладания женского пола для всех ювенильных хронических артритов, существует почти одинаковая половая заболеваемость при системном начале заболевания. СоЮИА может возникнуть в любом возрасте от периода новорожденности до подросткового возраста. Заболевание также наблюдается у взрослых и известно как болезнь Стилла у взрослых (AOSD). Хотя этот диагноз был популяризирован в 1971 согласно отчету сэра Эрика Байуотерса, подобные случаи спорадически регистрировались на протяжении прошлого столетия. Внесуставные системные особенности СоЮИА делают привлекательной возможность вирусной этиологии, но нет никаких доказательств, подтверждающих эту гипотезу. Хотя есть некоторые сообщения, предполагающие сезонное распространение СоЮИА, это не подтверждается другими сообщениями [6–9].
Внесуставные системные особенности СоЮИА делают привлекательной возможность вирусной этиологии, но нет никаких доказательств, подтверждающих эту гипотезу. Хотя есть некоторые сообщения, предполагающие сезонное распространение СоЮИА, это не подтверждается другими сообщениями [6–9].
Клиническая картина
В отличие от других пациентов с ЮИА, у которых поражение суставов обычно затмевает более общую симптоматику, при ЮИА наиболее выражены внесуставные проявления, такие как пиковая лихорадка, гепатоспленомегалия и васкулопатия [1, 3, 10]. Характерны типичная мимолетная розовая макулярная сыпь, плеврит или перикардит. Типично также генерализованное увеличение лимфатических узлов, особенно в подмышечных впадинах. У этих больных часто отмечаются выраженный полиморфно-ядерный лейкоцитоз и тромбоцитоз. Поражение суставов, как и сыпь, может быть более выраженным во время подъема температуры, а иногда может полностью отсутствовать, когда лихорадка исчезает.
Клиническое течение на более поздних стадиях СоЮИА сильно варьирует. Системные признаки, такие как лихорадка, сыпь и полисерозит, как правило, исчезают в течение первых месяцев или лет болезни. Около половины детей с СоЮИА выздоравливают почти полностью, часто после олигоартикулярной болезни. Другая половина продолжает демонстрировать прогрессирующее поражение все большего числа суставов. Заболевание суставов, наблюдаемое при ЮИА, в некоторых отношениях сильно отличается от других подтипов ЮИА. Вовлечение тазобедренного сустава встречается почти у 50% пациентов, обычно двустороннее и наблюдается у пациентов с полиартритом. Болезнь среднего отдела стопы с анкилозом чаще наблюдается у детей с СоЮИА, чем с другими подтипами. Анкилоз шейного отдела позвоночника также чаще наблюдается при ЮИА по сравнению с другими подтипами ЮИА. Ранние рентгенологические изменения, в том числе деструктивные изменения, достаточно характерны для СоЮИА, в одной серии у трети пациентов были выявлены эрозии и сужение суставной щели, у 8% — подвывих бедра, у одного больного в течение 2 лет от начала заболевания развился анкилоз [11].
Патогенез
Несколько линий доказательств указывают на то, что отчетливые клинические особенности системного ЮИА также связаны с уникальными иммунологическими аномалиями. Например, на геномном уровне отличительной особенностью системной формы является отсутствие сильных ассоциаций главного комплекса гистосовместимости (MHC) класса II [12]. Это сильно отличается от других клинических форм ЮИА, в которых вклад генов MHC весьма значителен. Фактически, недавно завершенный полногеномный скрининг показал, что большая часть генетической предрасположенности к олиго-ЮИА обусловлена локусами MHC [13]. Напротив, при системном ЮИА генетические эффекты, о которых чаще всего сообщалось, ограничивались главным образом умеренным влиянием полиморфизмов генов цитокинов/хемокинов. Особенно важны ассоциации с полиморфизмами промоторных элементов и генов, кодирующих фактор некроза опухоли-альфа (TNF-α), интерлейкин-6 (IL-6) [14–16] и фактор, ингибирующий миграцию макрофагов (MIF) [17, 18]. . Связь с однонуклеотидным полиморфизмом в промоторной области гена IL-6 особенно интригует. Два зарегистрированных генотипа предрасполагают к более высокой и более низкой продукции IL-6 соответственно. Исследования в двух разных популяциях показали, что генотип с низкой реакцией менее распространен при ювенильном хроническом артрите с системным началом, особенно у детей, у которых заболевание дебютирует в возрасте до 6 лет [15].
. Связь с однонуклеотидным полиморфизмом в промоторной области гена IL-6 особенно интригует. Два зарегистрированных генотипа предрасполагают к более высокой и более низкой продукции IL-6 соответственно. Исследования в двух разных популяциях показали, что генотип с низкой реакцией менее распространен при ювенильном хроническом артрите с системным началом, особенно у детей, у которых заболевание дебютирует в возрасте до 6 лет [15].
Цитокины, играющие решающую роль в поддержании воспалительного процесса при системной форме ЮИА, также отличаются от таковых при других подтипах ЮИА. Действительно, многие клинические признаки СоЮИА, в том числе характерные скачкообразные лихорадки, кожная сыпь, гипергаммаглобулинемия, гипоальбуминемия, повышенная скорость оседания эритроцитов и фибриноген, могут быть объяснены иммунным ответом с участием цитокинов ИЛ-1 и ИЛ-6 и ФНО-α [19]. –23]. Однако лечебные стратегии, направленные на нейтрализацию TNF-α, имели довольно ограниченную эффективность при системном ЮИА [24, 25]. Это резко контрастирует с отличным ответом на это лечение при других клинических формах заболевания, что позволяет предположить, что роль TNF-α при системном ЮИА может быть более ограниченной. Напротив, уровни экспрессии IL-6 намного выше при системном ЮИА и, по-видимому, коррелируют с общей клинической активностью заболевания и такими отличительными клиническими признаками, как тромбоцитоз, микроцитарная анемия, задержка роста и остеопения [21, 26]. Кроме того, исследования уникального характера ежедневной лихорадки системного ювенильного хронического артрита показывают, что концентрации IL-6 повышаются и падают в соответствии со скачками температуры и снижением температуры [20, 27]. В соответствии с этими наблюдениями предварительный клинический опыт с биологическим агентом, нейтрализующим активность IL-6, является очень многообещающим [28]. Кинерет, биологический агент, направленный на нейтрализацию цитокина IL-1, также показывает большие перспективы [29].–31]. Кинерет является растворимым антагонистом рецептора IL-1, сходным с встречающимся в природе IL1ra.
Это резко контрастирует с отличным ответом на это лечение при других клинических формах заболевания, что позволяет предположить, что роль TNF-α при системном ЮИА может быть более ограниченной. Напротив, уровни экспрессии IL-6 намного выше при системном ЮИА и, по-видимому, коррелируют с общей клинической активностью заболевания и такими отличительными клиническими признаками, как тромбоцитоз, микроцитарная анемия, задержка роста и остеопения [21, 26]. Кроме того, исследования уникального характера ежедневной лихорадки системного ювенильного хронического артрита показывают, что концентрации IL-6 повышаются и падают в соответствии со скачками температуры и снижением температуры [20, 27]. В соответствии с этими наблюдениями предварительный клинический опыт с биологическим агентом, нейтрализующим активность IL-6, является очень многообещающим [28]. Кинерет, биологический агент, направленный на нейтрализацию цитокина IL-1, также показывает большие перспективы [29].–31]. Кинерет является растворимым антагонистом рецептора IL-1, сходным с встречающимся в природе IL1ra. Интересно, что в первом отчете, описывающем существование встречающихся в природе ингибиторов ИЛ-1 (которые в конечном итоге оказались ИЛ-1ра), эти факторы были обнаружены в образце мочи лихорадящего пациента с системным ЮИА [32]. Совсем недавно Banchereau и его коллеги представили новые данные об участии дендритных клеток в патогенезе SoJIA [33]. В этом отчете экспансия дендритных клеток была связана с повышенной активностью IL-1, что дает еще одно возможное объяснение высокой чувствительности к Кинерету в этой конкретной клинической группе.
Интересно, что в первом отчете, описывающем существование встречающихся в природе ингибиторов ИЛ-1 (которые в конечном итоге оказались ИЛ-1ра), эти факторы были обнаружены в образце мочи лихорадящего пациента с системным ЮИА [32]. Совсем недавно Banchereau и его коллеги представили новые данные об участии дендритных клеток в патогенезе SoJIA [33]. В этом отчете экспансия дендритных клеток была связана с повышенной активностью IL-1, что дает еще одно возможное объяснение высокой чувствительности к Кинерету в этой конкретной клинической группе.
Сильная связь с так называемым синдромом активации макрофагов (MAS) может дать еще один ключ к пониманию отличительных патогенетических особенностей системной формы ЮИА. MAS является тяжелым, потенциально опасным для жизни осложнением, характеризующимся чрезмерной активацией высокодифференцированных макрофагов, что приводит к лихорадке, гепатоспленомегалии, лимфаденопатии, тяжелой цитопении, серьезному заболеванию печени, внутрисосудистому свертыванию крови и неврологическому поражению. MAS обычно наблюдается при SoJIA и очень редко при других подтипах JIA.
MAS обычно наблюдается при SoJIA и очень редко при других подтипах JIA.
MAS объясняет значительную заболеваемость и смертность, наблюдаемую при SoJIA. В патогенезе MAS, связанного с SoJIA, участвуют различные триггеры, включая вирусные инфекции, терапию нестероидными противовоспалительными препаратами, солями золота, сульфасалазином, метотрексатом и этанерцептом [34–36]. MAS при SoJIA можно увидеть при первоначальном диагнозе, во время обострения заболевания или даже когда заболевание находится в стадии ремиссии [37–39]. Точная частота этого состояния у детей с ЮИА неизвестна. В одном ретроспективном исследовании, проведенном высшим учебным заведением, у семи из 103 детей с диагнозом СоЮИА за 20-летний период развился МАС (6,7%) [35]. Авторы, однако, признали, что истинная частота MAS может быть намного выше, поскольку легкие случаи MAS не всегда диагностируются. Действительно, многие детские ревматологи все чаще признают наличие легкого САМ у пациентов с ЮИА, часто даже не требующего специфического лечения. Некоторые даже предполагают, что MAS и SoJIA — это просто «разные концы одного и того же спектра». Наличие нарушений свертывания крови [40] и значительно повышенного уровня ферритина в сыворотке крови, двух отличительных признаков САМ, у большинства пациентов с активным ЮИА, безусловно, согласуется с этим представлением. Неудивительно, что плохое определение того, что представляет собой истинный MAS, сильно усложнило разработку диагностических критериев MAS. Однако в настоящее время все чаще признается, что MAS имеет близкое сходство с гистиоцитарным заболеванием, вторичным гемофагоцитарным лимфогистиоцитозом (HLH), более четко определенным состоянием, наблюдаемым в гетерогенной группе заболеваний, включая инфекции, новообразования, гематологические состояния и аутоиммунные заболевания [41, 42]. Фактически было предложено заменить термин «MAS» на «реактивный HLH, связанный с аутоиммунным заболеванием (ReHLH)» [41, 42]. С другой стороны, в недавнем обзоре всех случаев ReHLH в условиях больницы для взрослых около 40% зарегистрированных пациентов соответствовали критериям болезни Стилла с началом во взрослом возрасте, что побудило авторов подвергнуть сомнению различную природу этих двух состояний.
Некоторые даже предполагают, что MAS и SoJIA — это просто «разные концы одного и того же спектра». Наличие нарушений свертывания крови [40] и значительно повышенного уровня ферритина в сыворотке крови, двух отличительных признаков САМ, у большинства пациентов с активным ЮИА, безусловно, согласуется с этим представлением. Неудивительно, что плохое определение того, что представляет собой истинный MAS, сильно усложнило разработку диагностических критериев MAS. Однако в настоящее время все чаще признается, что MAS имеет близкое сходство с гистиоцитарным заболеванием, вторичным гемофагоцитарным лимфогистиоцитозом (HLH), более четко определенным состоянием, наблюдаемым в гетерогенной группе заболеваний, включая инфекции, новообразования, гематологические состояния и аутоиммунные заболевания [41, 42]. Фактически было предложено заменить термин «MAS» на «реактивный HLH, связанный с аутоиммунным заболеванием (ReHLH)» [41, 42]. С другой стороны, в недавнем обзоре всех случаев ReHLH в условиях больницы для взрослых около 40% зарегистрированных пациентов соответствовали критериям болезни Стилла с началом во взрослом возрасте, что побудило авторов подвергнуть сомнению различную природу этих двух состояний. нарушения [43]. Чтобы решить эту проблему, в настоящее время проводятся исследования с использованием новых технологий микрочипов, чтобы определить степень сходства между SoJIA, MAS и «классическим» ReHLH.
нарушения [43]. Чтобы решить эту проблему, в настоящее время проводятся исследования с использованием новых технологий микрочипов, чтобы определить степень сходства между SoJIA, MAS и «классическим» ReHLH.
Общество гистиоцитов классифицировало гистиоцитарные нарушения на три основные группы: (1) нарушения, связанные с дендритными клетками; (2) нарушения, связанные с макрофагами, и (3) злокачественные заболевания [44]. ГЛГ относится к категории заболеваний, связанных с макрофагами, и составляет большинство пациентов этой категории (гистиоцитоз класса II). Существует два различных типа ГЛГ: (1) первичная ГЛГ, семейная и спорадическая форма, обычно провоцируемая вирусной инфекцией; семейная форма первичной ГЛГ (СГЛГ) представляет собой аутосомно-рецессивное заболевание, которое, как показано, обусловлено рядом различных генетических мутаций [45] и (2) вторичная ГЛГ; это также было названо вирус-ассоциированным гемофагоцитарным синдромом (VAHS) и злокачественным гемофагоцитарным синдромом (MAHS) в литературе [46].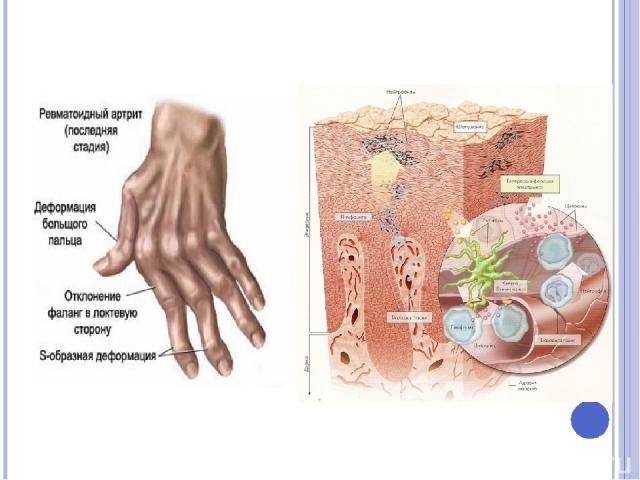
Наиболее стойким иммунологическим отклонением, о котором сообщалось у пациентов с СГЛГ, было нарушение цитотоксических функций. Таким образом, было продемонстрировано, что большинство пациентов с СГЛГ имеют нормальное количество В-лимфоцитов и нормальный уровень сывороточного иммуноглобулина [47]. Большинство этих пациентов имеют удивительно нормальное абсолютное количество лимфоцитов и нормальное распределение субпопуляций зрелых Т-клеток. Напротив, функция естественных киллеров (NK) заметно снижена или отсутствует практически у всех пациентов [47, 48]. Цитотоксическая активность клеток CD8+ также нарушена. Примерно у 40% пациентов с СГЛГ эти иммунологические аномалии были связаны с мутациями в гене, кодирующем перфорин, белок, который опосредует цитотоксическую активность NK- и Т-клеток. Другие мутации, недавно связанные с FHLH, по-видимому, влияют на белки, участвующие в доставке перфорина на клеточную поверхность [49].–51]. Из-за этого, несмотря на нормальное количество перфорина, цитотоксические клетки не могут индуцировать лизис клеток-мишеней. Примечательно, что аналогичные иммунологические аномалии, то есть низкая цитолитическая активность NK-клеток, часто связанная с аномальными уровнями экспрессии перфорина, также отличают системный ЮИА от других клинических форм детского артрита [52–54].
Примечательно, что аналогичные иммунологические аномалии, то есть низкая цитолитическая активность NK-клеток, часто связанная с аномальными уровнями экспрессии перфорина, также отличают системный ЮИА от других клинических форм детского артрита [52–54].
Точные механизмы, которые связывают недостаточность функций NK-клеток и цитотоксических Т-лимфоцитов с экспансией активированных макрофагов, неясны. В литературе были предложены два альтернативных объяснения. Один из них связан с тем фактом, что у пациентов с ГЛГ/МАС снижена способность контролировать некоторые инфекции [55, 56]. Более конкретно, NK-клетки и цитотоксические Т-лимфоциты не способны убить инфицированные клетки и, таким образом, устранить источник антигенной стимуляции. Такая постоянная антигенная стимуляция, в свою очередь, приводит к постоянной антиген-зависимой активации и пролиферации Т-клеток, связанной с возрастающей продукцией цитокинов, которые стимулируют макрофаги. Однако во многих случаях MAS попытки определить инфекционный триггер не увенчались успехом, и некоторые эпизоды, по-видимому, вызваны изменениями в лекарственной терапии, а не инфекцией. Кроме того, важность NK-клеток и систем на основе перфорина в подавлении клеточных иммунных ответов была продемонстрирована в экспериментальных системах животных, где иммунные ответы вызывались анти-CD3-антителами или стафилококковыми токсинами вместо вирусов [57, 58]. . Некоторые авторы выдвинули гипотезу о том, что аномальные цитотоксические клетки могут быть не в состоянии обеспечить соответствующие апоптотические сигналы для удаления антиген-презентирующих клеток и/или активированных Т-клеток после устранения инфекции. Такие Т-клетки могут продолжать секретировать цитокины, включая интерферон-гамма (IFN-γ) и гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF), два важных активатора макрофагов. Впоследствии устойчивая активация макрофагов приводит к инфильтрации тканей и продукции высоких уровней TNF-α, IL-1 и IL-6, которые играют важную роль в различных клинических симптомах и повреждении тканей. Обе гипотезы согласуются с наблюдениями на животных моделях ГЛГ, в которых нейтрализация IFN-γ приводит к почти полному купированию синдрома, в то время как нейтрализация TNFα, IL-1 или IL-6 обеспечивает лишь умеренное облегчение симптомов.
Кроме того, важность NK-клеток и систем на основе перфорина в подавлении клеточных иммунных ответов была продемонстрирована в экспериментальных системах животных, где иммунные ответы вызывались анти-CD3-антителами или стафилококковыми токсинами вместо вирусов [57, 58]. . Некоторые авторы выдвинули гипотезу о том, что аномальные цитотоксические клетки могут быть не в состоянии обеспечить соответствующие апоптотические сигналы для удаления антиген-презентирующих клеток и/или активированных Т-клеток после устранения инфекции. Такие Т-клетки могут продолжать секретировать цитокины, включая интерферон-гамма (IFN-γ) и гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF), два важных активатора макрофагов. Впоследствии устойчивая активация макрофагов приводит к инфильтрации тканей и продукции высоких уровней TNF-α, IL-1 и IL-6, которые играют важную роль в различных клинических симптомах и повреждении тканей. Обе гипотезы согласуются с наблюдениями на животных моделях ГЛГ, в которых нейтрализация IFN-γ приводит к почти полному купированию синдрома, в то время как нейтрализация TNFα, IL-1 или IL-6 обеспечивает лишь умеренное облегчение симптомов. 59].
59].
Связь с дефектным апоптозом может быть дополнительно подтверждена ассоциацией MAS и болезни Кикучи, некротизирующего лимфаденита, у пациентов с SoJIA. В литературе имеются сообщения по крайней мере о девяти пациентах с ЮИА, AOSD или системной красной волчанкой (СКВ) с патологией лимфатических узлов, предполагающей болезнь Кикучи, у которых позже развился СМА, и возможно, что эти два заболевания представляют собой основные дефекты апоптотического пути и имеют общие патогенетические механизмы [52, 60–64]. Важность выявления основных дефектов заключается не только в потенциальной ранней диагностике САМ, но также и в способности идентифицировать этих детей во время диагностики их ревматического заболевания, когда другое лечение потенциально может предотвратить развитие САМ.
В совокупности эти наблюдения позволяют предположить, что роль адаптивных иммунных реакций при системном ЮИА может быть довольно ограниченной по сравнению с другими клиническими формами заболевания. Напротив, вклад врожденного компонента иммунной системы, включая линию моноцитов/макрофагов/гистиоцитов и NK-клетки, может быть гораздо более заметным.
Напротив, вклад врожденного компонента иммунной системы, включая линию моноцитов/макрофагов/гистиоцитов и NK-клетки, может быть гораздо более заметным.
Реакция на другие виды лечения
ЮИА действительно реагирует на стероиды и, возможно, ни на какие другие терапевтические средства, как на пациентов с другими клиническими формами ЮИА. Даже у тех детей с СоЮИА, системное заболевание которых достигло стадии ремиссии и у которых осталось чисто суставное заболевание, артрит не поддается лечению обычными противоревматическими препаратами, модифицирующими заболевание, как другие подтипы ЮИА. Внутрисуставные стероиды, которые достаточно успешно используются при лечении других подтипов ЮИА, по-видимому, не столь эффективны при СоЮИА [65]. Метотрексат, препарат второго ряда при ЮИА, признан менее эффективным как при системных, так и при суставных проявлениях ЮИА [66–68]. В контролируемых исследованиях биологической терапии (этанерцепт) подгруппа пациентов с ЮИА давала гораздо более слабый ответ, чем пациенты с другими подтипами ЮИА.
Таким образом, учитывая различия между ЮИА и другими типами ЮИА, возможно, что ЮИА является другим заболеванием, таким как СКВ и ювенильный дерматомиозит, одним из клинических признаков которого является артрит. Важно отметить это различие, поскольку оно должно позволить нам заглянуть дальше от современных терапевтических стратегий и этиопатофизиологических механизмов. Возможно, что SoJIA, учитывая сходство с вторичным HLH, может быть даже формой гистиоцитарного расстройства!
AAG поддерживается грантами NIH AR050828 и AR048928. Другой автор заявил об отсутствии конфликта интересов.
Каталожные номера
1
Все еще GF. О форме хронической болезни суставов у детей.
Мед Чир Транс
1897
;
80
:
47
–59.
2
Байуотерс Э. Г. Джордж Фредерик Стилл (1868–1941): его жизнь и творчество.
Г. Джордж Фредерик Стилл (1868–1941): его жизнь и творчество.
Дж Мед Биогр
1994
;
2
:
125
–31.
3
Шнайдер Р., Лаксер Р.М. Ювенильный ревматоидный артрит с системным началом.
Baillieres Clin Rheumatol
1998
;
12
:
245
–71.
4
Уоллес К.А., Левинсон Дж.Е. Ювенильный ревматоидный артрит: исход и лечение в 1990-е гг.
Rheum Dis Clin North Am
1991
;
17
:
891
–905.
5
Шнайдер Р., Лаксер Р.М.
Ювенильный идиопатический артрит с системным началом
. В: Isenberg DA, Maddison PJ, Woo P, Glass D, Breedveld FC, eds, Оксфордский учебник ревматологии. Оксфорд: Oxford University Press,
В: Isenberg DA, Maddison PJ, Woo P, Glass D, Breedveld FC, eds, Оксфордский учебник ревматологии. Оксфорд: Oxford University Press,
2004
:
798
–809.
6
Линдсли CB. Сезонные вариации системного начала ювенильного ревматоидного артрита.
Ревматоидный артрит
1987
;
30
:
838
–9.
7
Фельдман Б.М., Берди Н., Бун Дж.Е. и др. . Сезонное начало системного ювенильного ревматоидного артрита.
J Педиатр
1996
;
129
:
513
–18.
8
Oen K, Fast M, Postl B.![]() Эпидемиология ювенильного ревматоидного артрита в Манитобе, Канада, 1975–92: циклы заболеваемости.
Эпидемиология ювенильного ревматоидного артрита в Манитобе, Канада, 1975–92: циклы заболеваемости.
J Ревматол
1995
;
22
:
745
–50.
9
Узиэль Ю., Померанц А., Брик Р. и др. . Сезонные вариации ювенильного ревматоидного артрита с системным началом в Израиле.
J Ревматол
1999
;
26
:
1187
–9.
10
Lomater C, Gerloni V, Gattinara M, Mazzotti J, Cimaz R, Fantini F. Ювенильный идиопатический артрит с системным началом: ретроспективное исследование 80 последовательных пациентов, наблюдаемых в течение 10 лет.
J Ревматол
2000
;
27
:
491
–6.
11
Ланг Б.А., Шнайдер Р., Рейли Б.Дж., Сильверман Э.Д., Лаксер Р.М. Рентгенологические признаки системного ювенильного ревматоидного артрита.
J Ревматол
1995
;
22
:
168
–73.
12
Непом BG, Стекло DN. Ювенильный ревматоидный артрит и HLA: отчет семинара Park City III.
J Ревматол
1992
;
33 (дополнение)
:
70
–4.
13
Томпсон С.Д., Морольдо М.Б., Гайер Л. и др. . Полногеномное сканирование на наличие ювенильного ревматоидного артрита в пораженных семьях родственных пар свидетельствует о сцеплении.
Ревматоидный артрит
2004
;
50
:
2920
–30.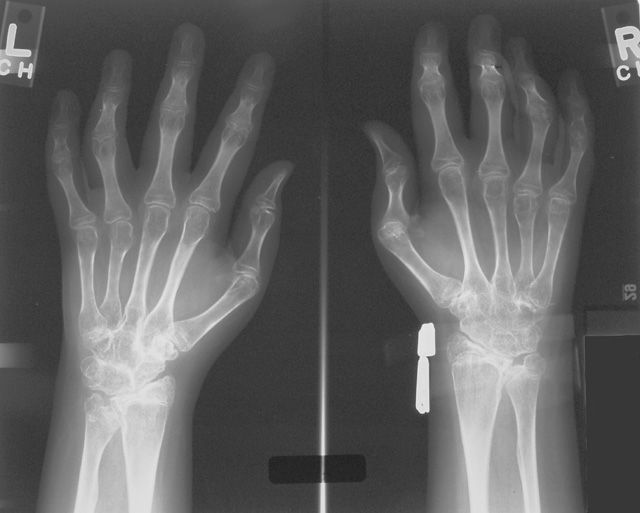
14
Дата Y, Seki N, Kamizono S и др. . Выявление генетического фактора риска системного ювенильного ревматоидного артрита в 5′-фланкирующей области гена TNF-альфа и генов HLA.
Ревматоидный артрит
1999
;
42
:
2577
–82.
15
Фишман Д., Фолдс Г., Джеффри Р. и др. . Влияние новых полиморфизмов гена интерлейкина-6 (IL-6) на транскрипцию IL-6 и уровни IL-6 в плазме, а также связь с ювенильным хроническим артритом с системным началом.
Дж. Клин Инвест
1998
;
102
:
1369
–76.
16
Огилви Э.М., Файф М.С., Томпсон С.Д. и др. . Аллель -174G гена интерлейкина-6 придает предрасположенность к системному артриту у детей: многоцентровое исследование с использованием семей с простым и множественным ювенильным идиопатическим артритом.
Аллель -174G гена интерлейкина-6 придает предрасположенность к системному артриту у детей: многоцентровое исследование с использованием семей с простым и множественным ювенильным идиопатическим артритом.
Ревматоидный артрит
2003
;
48
:
3202
–6.
17
Донн Р.П., Шелли Э., Оллиер В.Е., Томсон В., Британская исследовательская группа по детской ревматологии. Новый полиморфизм 5′-фланкирующей области фактора, ингибирующего миграцию макрофагов, связан с ювенильным идиопатическим артритом с системным началом.
Ревматоидный артрит
2001
;
44
:
1782
–5.
18
Де Бенедетти Ф., Меацца С., Виварелли М. и др. . Функциональная и прогностическая значимость полиморфизма -173 гена фактора, ингибирующего миграцию макрофагов, при ювенильном идиопатическом артрите с системным началом.
. Функциональная и прогностическая значимость полиморфизма -173 гена фактора, ингибирующего миграцию макрофагов, при ювенильном идиопатическом артрите с системным началом.
Ревматоидный артрит
2003
;
48
:
1398
–407.
19
Keul R, Heinrich PC, Muller-Newen G, Muller K, Woo P. Возможная роль растворимого рецептора IL-6 в патогенезе системного ювенильного хронического артрита.
Цитокин
1998
;
10
:
729
–34.
20
Руни М., Дэвид Дж., Саймонс Дж., Ди Джовин Ф., Варсани Х., Ву П. Воспалительные реакции цитокинов при ювенильном хроническом артрите.
BrJ Ревматол
1995
;
34
:
454
–60.
21
Pignatti P, Vivarelli M, Meazza C, Rizzolo MG, Martini A, De Benedetti F. Аномальная регуляция интерлейкина 6 при системном ювенильном идиопатическом артрите.
J Ревматол
2001
;
28
:
1670
–6.
22
Музаффер М.А., Дайер Дж.М., Фельдман Б.М. и др. . Различия в профилях циркулирующих уровней растворимых рецепторов фактора некроза опухоли и антагониста рецептора интерлейкина-1 отражают гетерогенность подгрупп ювенильного ревматоидного артрита.
J Ревматол
2002
;
29
:
1071
–8.
23
Мангге Х., Кензиан Х., Галлистл С. и др. . Цитокины сыворотки при ювенильном ревматоидном артрите. Корреляция с обычными параметрами воспаления и клиническими подтипами.
Цитокины сыворотки при ювенильном ревматоидном артрите. Корреляция с обычными параметрами воспаления и клиническими подтипами.
Ревматоидный артрит
1995
;
38
:
211
–20.
24
Quartier P, Taupin P, Bourdeaut F и др. . Эффективность этанерцепта при лечении ювенильного идиопатического артрита в зависимости от типа дебюта.
Ревматоидный артрит
2003
;
48
:
1093
–101.
25
Кимура Ю.П., Хиггинс Г. Лечение системного ЮИА этанерцептом: последующее исследование.
Ревматоидный артрит
2002
;
46
:
S481
.
26
De Benedetti F, Martini A. Является ли системный ювенильный ревматоидный артрит заболеванием, опосредованным интерлейкином 6?
J Ревматол
1998
;
25
:
203
–7.
27
Приер А.М., Ру-Ломбар П., Дайер Дж.М. Динамика лихорадки и цитокиновая сеть при системном ювенильном артрите.
Rev Rhum Engl Ed
1996
;
63
:
163
–70.
28
Yokota SM, Imagawa T. Испытание фазы II антитела к рецептору IL-6 (MRA) для детей с системным началом ювенильного идиопатического артрита.
Ревматоидный артрит
2003
;
48
:
S429
.
29
Вербский Ю.В., Уайт А.Дж. Эффективное применение рекомбинантного антагониста рецептора интерлейкина 1 анакинры при резистентном к терапии ювенильном ревматоидном артрите с системным началом.
J Ревматол
2004
;
31
:
2071
–5.
30
Иригойен П.И., Олсен Дж., Хом С., Иловите Н.Т. Лечение системного ювенильного ревматоидного артрита анакинрой.
Ревматоидный артрит
2004
;
50
:
S437
.
31
Henrickson M. Эффективность анакинры при рефрактерном системном артрите.
Ревматоидный артрит
2004
;
50
:
S438
.
32
Приер А.М., Кауфманн М.Т., Гришелли С., Дайер Дж.М. Специфический ингибитор интерлейкина-1 в сыворотке крови и моче детей с системным ювенильным хроническим артритом.
Ланцет
1987
;
2
:
1240
–2.
33
Кузин Дж. Совещание по базовой и клинической иммунологии. И действие! Дендритные клетки оживают.
Наука
2004
;
305
:
772
–3.
34
Ramanan AV, Schneider R. Синдром активации макрофагов после начала лечения этанерцептом у ребенка с системным началом ювенильного ревматоидного артрита.
J Ревматол
2003
;
30
:
401
–3.
35
Сони С., Ву П., Мюррей К.Дж. Синдром активации макрофагов: потенциально фатальное осложнение ревматических заболеваний.
Arch Dis Child
2001
;
85
:
421
–6.
36
Стефан Дж.Л., Коне-Паут И., Галамбрун С., Муи Р., Бадер-Менье Б., Приер А.М. Реактивный гемофагоцитарный синдром у детей с воспалительными заболеваниями. Ретроспективное исследование 24 пациентов.
Ревматология
2001
;
40
:
1285
–92.
37
Дэвис С.В., Дин Д.Д., Уордроп, Калифорния и др. . Гемофагоцитарный синдром, ассоциированный с вирусом Эпштейна-Барр, у больного ювенильным хроническим артритом.
BrJ Ревматол
1994
;
33
:
495
–7.
38
Cuende E, Vesga JC, Perez LB, Ardanaz MT, Гвинея J. Синдром активации макрофагов как начальное проявление системного ювенильного идиопатического артрита.
Clin Exp Rheumatol
2001
;
19
:
764
–5.
39
Прахалад С., Бове К.Е., Диккенс Д., Ловелл Д.Дж., Гром А.А. Этанерцепт в лечении синдрома активации макрофагов.
J Ревматол
2001
;
28
:
2120
–4.
40
Блум Б. Дж., Такер Л.Б., Миллер Л.С., Шаллер Дж.Г. Фибрин-D-димер как маркер активности заболевания при системном ювенильном ревматоидном артрите.
Дж., Такер Л.Б., Миллер Л.С., Шаллер Дж.Г. Фибрин-D-димер как маркер активности заболевания при системном ювенильном ревматоидном артрите.
J Ревматол
1998
;
25
:
1620
–5.
41
Атрея Б.Х. Является ли синдром активации макрофагов новой сущностью?
Clin Exp Rheumatol
2002
;
20
:
121
–3.
42
Раманан А.В., Шнайдер Р. Синдром активации макрофагов — что в названии!
J Ревматол
2003
;
30
:
2513
–16.
43
Эмменеггер У.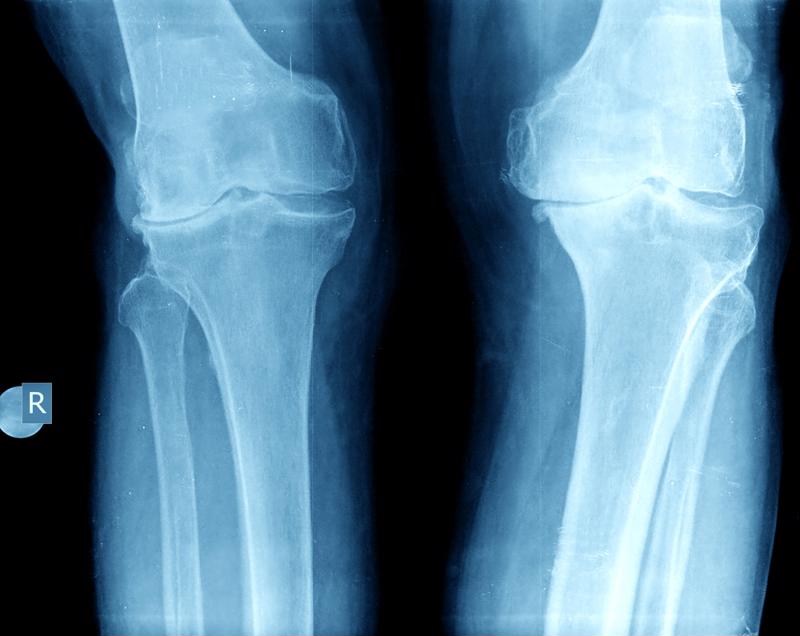 , Реймерс А., Фрей У. и др. . Синдром реактивной активации макрофагов: простая стратегия скрининга и ее потенциал в раннем начале лечения.
, Реймерс А., Фрей У. и др. . Синдром реактивной активации макрофагов: простая стратегия скрининга и ее потенциал в раннем начале лечения.
Swiss Med Wkly
2002
;
132
:
230
–6.
44
Фавара Б.Э., Феллер А.С., Паули М. и др. . Современная классификация гистиоцитарных нарушений. Комитет ВОЗ по пролиферации гистиоцитарных/ретикулярных клеток. Рабочая группа по реклассификации Общества гистиоцитов.
Мед Педиатр Онкол
1997
;
29
:
157
–66.
45
Горансдоттер Эриксон К., Фадил Б., Нильсон-Арднор С. и др. . Спектр мутаций гена перфорина при семейном гемофагоцитарном лимфогистиоцитозе.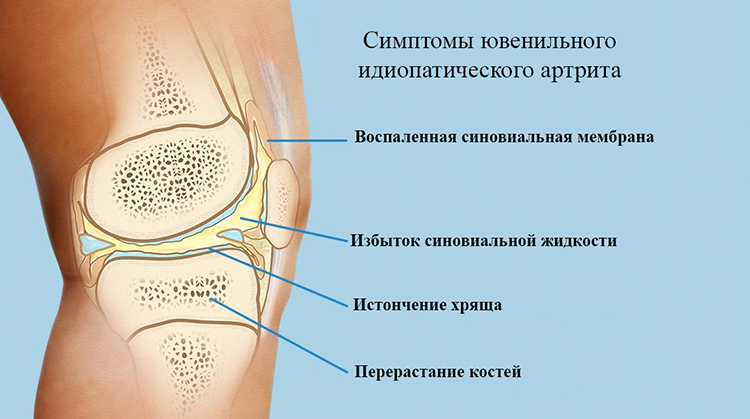
Am J Hum Genet
2001
;
68
:
590
–7.
46
Янка Г., Имашуку С., Элиндер Г., Шнайдер М., Хентер Дж.-И. Инфекционно- и злокачественно-ассоциированные гемофагоцитарные синдромы. Вторичный гемофагоцитарный лимфогистиоцитоз.
Hematol Oncol Clin North Am
1998
;
12
:
435
–44.
47
Эгелер Р.М., Шапиро Р., Лехельт Б., Филипович А. Характерные иммунные нарушения при гемофагоцитарном лимфогистиоцитозе.
J Pediatr Hematol Oncol
1996
;
18
:
340
–5.
48
Салливан К.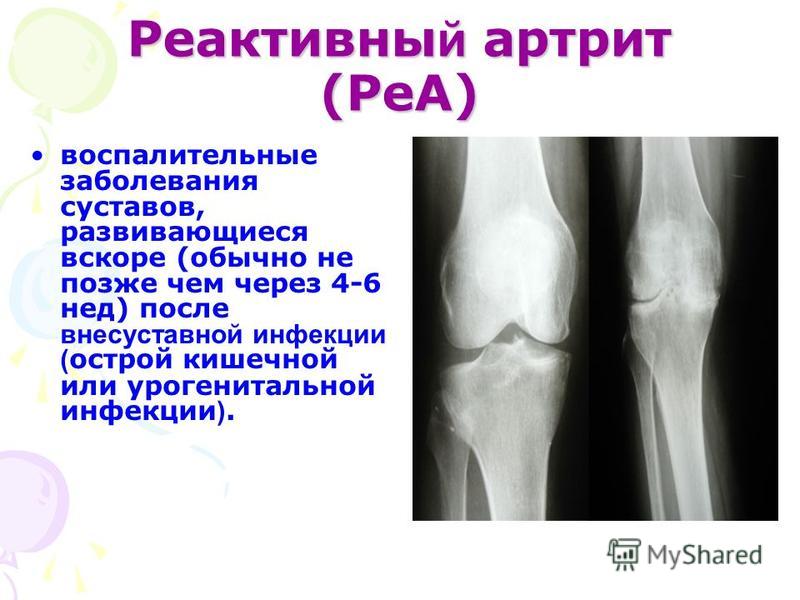 Е., Делаат К.А., Дуглас С.Д., Филипович А.Х. Дефектная функция естественных киллеров у больных гемофагоцитарным лимфогистиоцитозом и у родственников первой степени родства.
Е., Делаат К.А., Дуглас С.Д., Филипович А.Х. Дефектная функция естественных киллеров у больных гемофагоцитарным лимфогистиоцитозом и у родственников первой степени родства.
Педиатр Рез
1998
;
44
:
465
–8.
49
Neeft M, Wieffer M, de Jong AS и др. . Munc13-4 является эффектором rab27a и контролирует секрецию лизосом в гемопоэтических клетках.
Мол Биол Селл
2005
;
16
:
731
–41.
50
Feldmann J, Callebaut I, Raposo G и др. . Munc13-4 необходим для слияния цитолитических гранул и мутирует в форме семейного гемофагоцитарного лимфогистиоцитоза (FHL3).
Сотовый
2003
;
115
:
461
–73.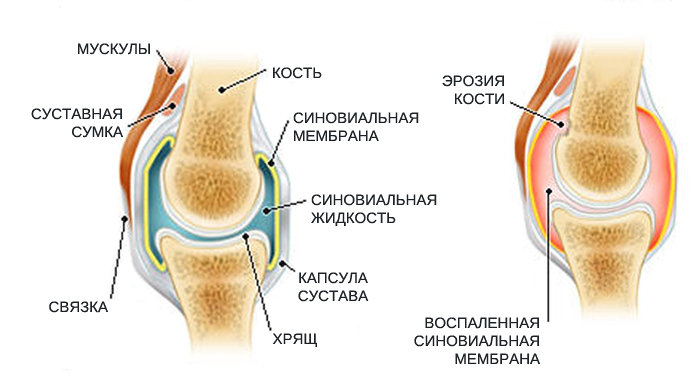
51
Feldmann J, Le Deist F, Fischer A, de Saint Basile G. [Munc13-4 необходим для слияния цитолитических гранул].
Med Sci (Париж)
2004
;
20
:
144
–6.
52
Гром А.А., Вильянуэва Дж., Ли С., Гольдмунц Э.А., Пассо М.Х., Филипович А. Дисфункция естественных клеток-киллеров у пациентов с системным ювенильным ревматоидным артритом и синдромом активации макрофагов.
J Педиатр
2003
;
142
:
292
–6.
53
Wulffraat NM, Rijkers GT, Elst E, Brooimans R, Kuis W. Снижение экспрессии перфорина при системном ювенильном идиопатическом артрите восстанавливается путем аутологичной трансплантации стволовых клеток.
Ревматология
2003
;
42
:
375
–9.
54
Вильянуэва Дж., Ли С., Джаннини Э.Х. и др. . Дисфункция естественных клеток-киллеров является отличительной чертой ювенильного ревматоидного артрита с системным началом и синдрома активации макрофагов.
Артрит Рес Тер
2005
;
7
:
10
.
55
Арнаут Р.А. Дефицит перфорина: сражаться без оружия?
Иммунол Сегодня
2000
;
21
:
592
(ответ автора 593–4).
56
Arico M, Danesino C, Pende D, Moretta L. Патогенез гемофагоцитарного лимфогистиоцитоза.
Патогенез гемофагоцитарного лимфогистиоцитоза.
BrJ Гематол
2001
;
114
:
761
–9.
57
Каги Д., Одерматт Б., Мак Т.В. Гомеостатическая регуляция CD8+ Т-клеток перфорином.
Eur J Immunol
1999
;
9
:
3262
–72.
58
Stepp SE, Mathew PA, Bennett M, de Saint Basile G, Kumar V. Перфорин: больше, чем просто эффекторная молекула.
Иммунол Сегодня
2000
;
21
:
254
–6.
59
Jordan MB, Hildeman D, Kappler J, Marrack P. Животная модель гемофагоцитарного лимфогистиоцитоза (HLH): CD8+ T-клетки и гамма-интерферон необходимы для заболевания.
Животная модель гемофагоцитарного лимфогистиоцитоза (HLH): CD8+ T-клетки и гамма-интерферон необходимы для заболевания.
Кровь
2004
;
104
:
735
–43.
60
Раманан А.В., Винн Р.Ф., Келси А., Бейлдам Э.М. Системный ювенильный идиопатический артрит, болезнь Кикучи и гемофагоцитарный лимфогистиоцитоз — есть ли связь? Отчет о клиническом случае и обзор литературы.
Ревматология
2003
;
42
:
596
–8.
61
Охта А., Мацумото Ю., Охта Т., Канеока Х., Ямагути М. Болезнь Стилла, связанная с некротическим лимфаденитом (болезнь Кикучи): отчет о 3 случаях.
J Ревматол
1988
;
15
:
981
–3.
62
Oliveira S, Destri UBW, Vasquez LCO, Ferman S, Romano S, Sztajnbok FR. Системный ювенильный идиопатический артрит, ассоциированный с болезнью Кикучи.
Энн Реум Дис
2000
;
59 (дополнение)
:
731
.
63
Кузен Ф., Грезард П., Рот Б., Бальме Б., Грегуар-Бардель М., Перро Х. Болезнь Кикучи, связанная с болезнью Стилла.
Int J Dermatol
1999
;
38
:
464
–7.
64
Вонг К.Ф., Хуэй П.К., Чан Дж.К. и др. . Острый волчаночный гемофагоцитарный синдром.
Энн Интерн Мед
1991
;
114
:
387
–90.
65
Breit W, Frosch M, Meyer U, Heinecke A, Ganser G. Специфическая для подгруппы оценка эффективности внутрисуставного триамцинолона гексацетонида при ювенильном хроническом артрите.
J Ревматол
2000
;
27
:
2696
–702.
66
Галле Ф., Приер А.М. Оценка метотрексата при лечении ювенильного хронического артрита в зависимости от подтипа.
Clin Exp Rheumatol
1991
;
9
:
297
–302.
67
Спекмайер М., Финдейзен Дж., Ву П. и др. . Низкие дозы метотрексата при ювенильном хроническом артрите с системным началом.
Clin Exp Rheumatol
1989
;
7
:
647
–50.
68
Woo P, Southwood TR, Prieur AM и др. . Рандомизированное, плацебо-контролируемое, перекрестное исследование низких доз перорального метотрексата у детей с распространенным олигоартикулярным или системным артритом.
Ревматоидный артрит
2000
;
43
:
1849
–57.
Примечания автора
Отделение детской ревматологии, NHS Trust и Королевская национальная больница ревматических заболеваний в Северном Бристоле, Бат, Великобритания и 1 Отделение ревматологии Уильяма С. Роу, Медицинский центр детской больницы Цинциннати, Цинциннати, Огайо, США.
© Автор, 2005 г. Опубликовано Oxford University Press от имени Британского общества ревматологов. Все права защищены. Для получения разрешений обращайтесь по электронной почте: journals. [email protected]
[email protected]
© Автор, 2005 г. Опубликовано Oxford University Press от имени Британского общества ревматологов. Все права защищены. Чтобы получить разрешения, отправьте электронное письмо по адресу: [email protected]
Раздел выпуска:
Обзоры
Скачать все слайды
Реклама
Цитаты
Альтметрика
Дополнительная информация о метриках
Оповещения по электронной почте
Оповещение об активности статьи
Предварительные уведомления о статьях
Оповещение о новой проблеме
Оповещение о теме
Получайте эксклюзивные предложения и обновления от Oxford Academic
Ссылки на статьи по телефону
Последний
Самые читаемые
Самые цитируемые
Эффективность системы оценки МРТ для воспаления суставов и энтезисов при периферическом СпА: ретроспективный анализ исследования CRESPA
Возвращаясь к идиопатическому эозинофильному миозиту: к клинико-патологическому континууму от мышц к фасциям и коже
Новая мутация и расширение фенотипа при дефиците IRF2BP2
Текстовая шея ошибочно диагностирована как фибромиалгия
Сравнение использования медицинских услуг, затрат и качества жизни, связанного со здоровьем, в подгруппах, определенных с помощью Keele START MSK Tool
.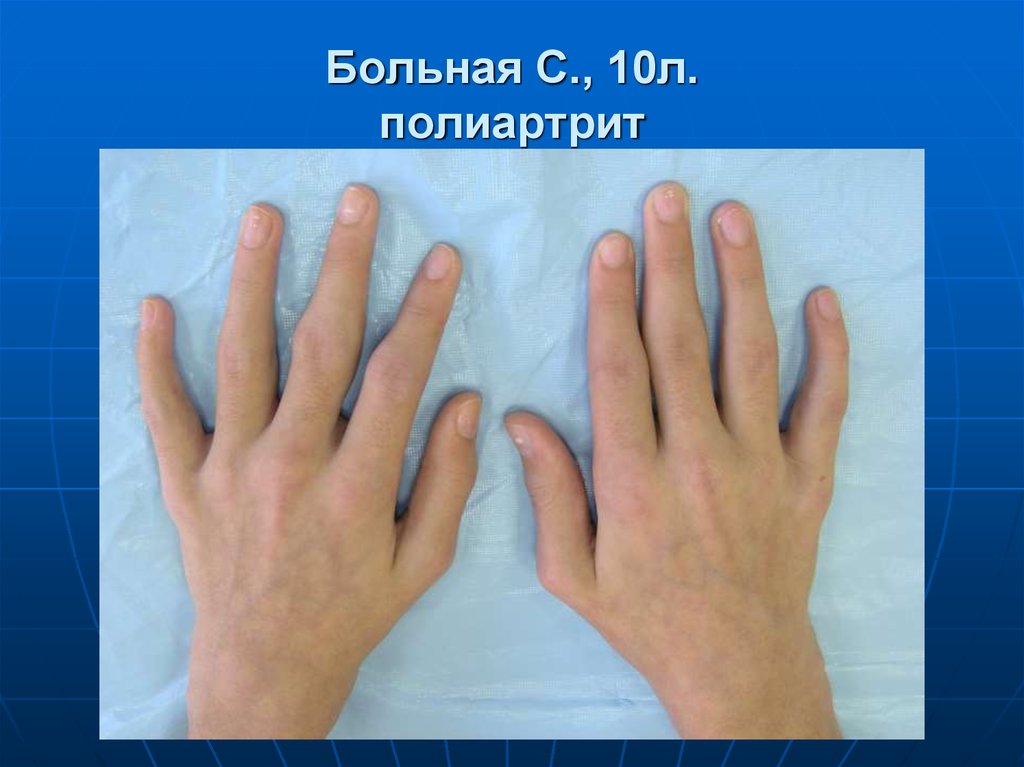
Реклама
Ювенильный ревматоидный артрит с системным началом неуточненной локализации
- Коды МКБ-10-СМ ›
- М00-М99 Заболевания опорно-двигательного аппарата и соединительной ткани ›
- М05-М1А Воспалительные полиартропатии ›
- М08- Ювенильный артрит ›
- 2023 Код диагноза по МКБ-10-CM M08.20
Ювенильный ревматоидный артрит с системным началом неуточненной локализации
- 2016 2017 2018 2019 2020 2021 2022 2023 Платежный/специальный код
- M08.20 — это оплачиваемый/специальный код МКБ-10-CM, который можно использовать для обозначения диагноза в целях возмещения расходов.
- Краткое описание: Ювенильный ревматоидный артрит с системным началом, сайт unsp
- Редакция МКБ-10-КМ M08.
 20 2023 г. вступила в силу 1 октября 2022 г.
20 2023 г. вступила в силу 1 октября 2022 г. - Это американская версия М08.20 МКБ-10-СМ. Другие международные версии МКБ-10 М08.20 могут отличаться.
Следующие коды выше M08.20 содержат обратные ссылки на аннотации
обратные ссылки на аннотации
В этом контексте обратные ссылки на аннотации относятся к кодам, которые содержат: , или
, которые могут быть применимы к M08.20:
- M00-M99
2023 МКБ-10-СМ Диапазон M00-M99
Заболевания опорно-двигательного аппарата и соединительной ткани причина заболевания опорно-двигательного аппарата
Тип 2 Исключая
- артропатический псориаз (L40.
 5-)
5-) - некоторые состояния, возникающие в перинатальном периоде (P04-P96)
- некоторые инфекционные и паразитарные болезни (A00-B99)
- компартмент-синдром (травматический) (T79.A-)
- осложнения беременности, родов и послеродового периода ( O00-O9A)
- врожденные пороки развития, деформации и хромосомные аномалии (Q00-Q99)
- эндокринные, алиментарные и метаболические заболевания (E00-E88)
- травмы, отравления и некоторые другие последствия внешних причин (S00-T88)
- новообразования (C00-D49)
- симптомы, признаки и аномальные клинические и лабораторные данные, не классифицированные в других рубриках (R00-R94)
Код диагноза по МКБ-10-СМ M08
Ювенильный артрит
- 2016 2017 2018 2019 2020 2021 2022 2023 НЕБОЛОБИТЕЛЬНЫЙ/НЕПРЕДЕЛИЧЕСКИЙ КОД
Код также
- Любое связанное сопутствующее состояние, такое как:
- Региональный энтегит [Cron’s Hebite] (K50] (K50] (K50] (K50] )
- Язвенный колит (K51.
 -)
-)
Тип 1 исключает
- Артропатия при болезни Уиппла (M14.8)
- Фелти Синдром (M05.0)
- Juvenile Dermatysite (M33.0-). Артротропатия (L40,54)
Код диагностики ICD-10-CM M08.2
Ювенильный ревматоидный артрит с системным началом
- 2016 2016 2018 2018 2019 2020 2021 2022233333. нет. Специальный код
Применимо к
- Болезнь Стилла БДУ
Тип 1 Исключая
- Болезнь Стилла с началом у взрослых (M06.1-)
- Ювенильный идиопатический артрит
- Болезнь Стилла
- Болезнь Стилла с началом в юношеском возрасте и/или во взрослом возрасте
- Ювенильный хронический артрит с системным началом
- Ювенильный идиопатический артрит с системным началом
- Ювенильный ревматоидный артрит с системным началом
МКБ-10-CM M08. 20 сгруппирована в группе (группах), связанной с диагностикой (MS-DRG v40.0):
20 сгруппирована в группе (группах), связанной с диагностикой (MS-DRG v40.0):
- 545 Заболевания соединительной ткани с mcc
- 546 Болезни соединительной ткани с cc
- 547 Заболевания соединительной ткани без cc/mcc
Преобразование M08.20 в ICD-9-CM
История кода
- 2016 (действует с 01.10.2015) : Новый код (первый год непроектной МКБ-10-CM)
- 2017 (действует с 01.10.2016) : Без изменений
- 2018 (действует с 01.10.2017) : без изменений
- 2019 (действует с 01.10.2018) : Без изменений
- 2020 (действует с 01.10.2019) : без изменений
- 2021 (действует с 01.10.2020) : Без изменений
- 2022 (действует с 01.
 10.2021) : без изменений
10.2021) : без изменений - 2023 (действует с 01.10.2022) : Без изменений
Записи указателя диагнозов, содержащие обратные ссылки на M08.20:
- Болезнь или синдром Стилла (юношеский) M08.20
Коды МКБ-10-СМ, соседние с M08.20
M08.069 Ювенильный ревматоидный артрит коленного сустава неуточненный неуточненный
M08.07 Неуточненный ювенильный ревматоидный артрит голеностопного сустава и стопы
M08. 071 Неуточненный ювенильный ревматоидный артрит правой лодыжки и стопы
071 Неуточненный ювенильный ревматоидный артрит правой лодыжки и стопы
M08.072 Неуточненный ювенильный ревматоидный артрит левой голени и стопы
M08.079 Неуточненный ювенильный ревматоидный артрит голеностопного сустава и стопы неуточненный
M08.08 …… позвонки
M08. 09 …… несколько сайтов
09 …… несколько сайтов
M08.0A …… другое указанное место
M08.1 Ювенильный анкилозирующий спондилит
M08.2 Ювенильный ревматоидный артрит с системным началом
М08.20 …… неуказанный сайт
M08. 21 Ювенильный ревматоидный артрит с системным началом, поражение плечевого сустава
21 Ювенильный ревматоидный артрит с системным началом, поражение плечевого сустава
M08.211 Ювенильный ревматоидный артрит с системным началом, правое плечо
M08.212 Ювенильный ревматоидный артрит с системным началом, поражение левого плеча
M08.219 Ювенильный ревматоидный артрит с системным началом, поражение плечевого сустава неуточненное
M08. 22 Ювенильный ревматоидный артрит с системным началом, поражение локтевого сустава
22 Ювенильный ревматоидный артрит с системным началом, поражение локтевого сустава
M08.221 Ювенильный ревматоидный артрит с системным началом, поражение правого локтевого сустава
M08.222 Ювенильный ревматоидный артрит с системным началом, поражение левого локтя
M08.229 Ювенильный ревматоидный артрит с системным началом, локтевой сустав неуточненный
M08.

 Продолжительность лечения не менее 12 недель.
Продолжительность лечения не менее 12 недель. 20 2023 г. вступила в силу 1 октября 2022 г.
20 2023 г. вступила в силу 1 октября 2022 г. 5-)
5-)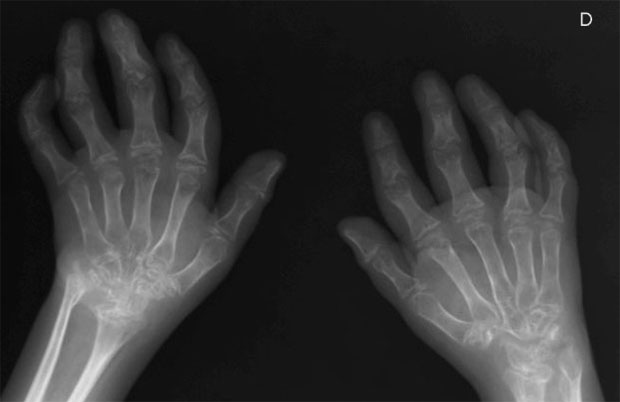 -)
-) 10.2021) : без изменений
10.2021) : без изменений