Формула Линолевой кислоты структурная химическая
- Жирная кислота
Структурная формула
Истинная, эмпирическая, или брутто-формула: C18H32O2
Рациональная формула: С17Н31COOH
Химический состав Линолевой кислоты
| Символ | Элемент | Атомный вес | Число атомов | Процент массы |
|---|---|---|---|---|
| C | Углерод | 12,011 | 18 | 77,1% |
| H | Водород | 1.008 | 32 | 11,5% |
| O | Кислород | 15.999 | 2 | 11,4% |
Молекулярная масса: 280,452
Не следует путать с линоленовой кислотой.
Линолевая кислота — одноосновная карбоновая кислота с двумя изолированными двойными связями CH3(CH2)3-(CH2CH=CH)2(CH2)7COOH. Относится к омега-6-ненасыщенным жирным кислотам.
История
Формула линолевой кислоты С17Н31COOH была установлена в 1889 г. профессором А. Н. Реформатским.
Свойства
Линолевая кислота — светло-жёлтая маслянистая жидкость, нерастворимая в воде, но хорошо растворимая во многих органических растворителях. Tпл −11 °C, tkип 182 °C (532 н/м², или 4 мм рт. ст.), плотность 0,903 г/см³ (20 °C). В натуральных жирах линолевая кислота находится в виде геометрического цис-изомера. Она имеет неразветвлённую цепь углеродных атомов и две изолированные (не сопряжённые) двойные связи, одна из которых расположена между 9-м и 10-м, а вторая между 12-м и 13-м углеродными атомами (9,12-уноктадиеновая кислота).
Нахождение в природе
Содержится в меньшей степени в животных жирах. Широко распространена в растительных маслах.
Биохимическое значение
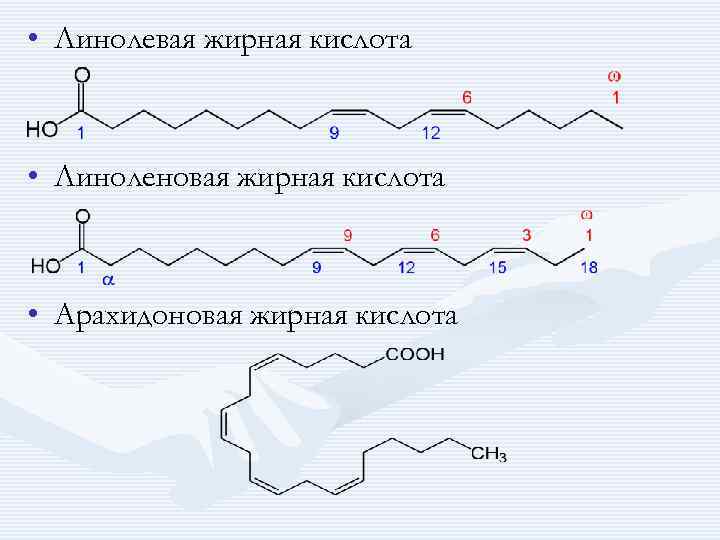
Линолевая кислота вместе с линоленовой кислотой относится к так называемым незаменимым жирным кислотам, необходимым для нормальной жизнедеятельности; в организм человека и животных эти кислоты поступают с пищей, главным образом в виде сложных липидов — триглицеридов и фосфатидов. Линолевая кислота относится к классу омега-6-ненасыщенных жирных кислот, поэтому организм человека способен синтезировать из неё относящуюся к этому же классу четырежды ненасыщенную арахидоновую жирную кислоту. В клеточных мембранах человека линолевой кислоты содержится в среднем в 10 раз раз больше, чем омега-3-ненасыщенной α-линоленовой жирной кислоты, что доказывает критическую важность линолевой кислоты и всего класса омега-6-ненасыщенных жирных кислот для нормального функционирования клеточных и субклеточных мембран.
Этиловый эфир линолевой кислоты, структурная формула, химические свойства, получение
1
H
ВодородВодород
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
ГелийГелий
4,0026
1s 2
Бесцветный газ
t°кип=-269°C
3
Li
ЛитийЛитий
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
БериллийБериллий
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
БорБор
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
УглеродУглерод
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
t°кип=4830°C
7
N
АзотАзот
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
КислородКислород
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
ФторФтор
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
НеонНеон
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
НатрийНатрий
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
МагнийМагний
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
АлюминийАлюминий
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t° кип=2467°C
14
Si
КремнийКремний
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
ФосфорФосфор
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
СераСера
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
ХлорХлор
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
АргонАргон
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
КалийКалий
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
КальцийКальций
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
СкандийСкандий
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
ТитанТитан
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
ВанадийВанадий
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
ХромХром
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t° кип=2482°C
25
Mn
МарганецМарганец
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
ЖелезоЖелезо
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
КобальтКобальт
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
НикельНикель
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
МедьМедь
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
ЦинкЦинк
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
ГаллийГаллий
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
ГерманийГерманий
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
МышьякМышьяк
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
СеленСелен
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
БромБром
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
КриптонКриптон
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
РубидийРубидий
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
СтронцийСтронций
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
ИттрийИттрий
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
ЦирконийЦирконий
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
НиобийНиобий
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
МолибденМолибден
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
ТехнецийТехнеций
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
РутенийРутений
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
РодийРодий
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
ПалладийПалладий
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
СереброСеребро
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
КадмийКадмий
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
ИндийИндий
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
ОловоОлово
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
СурьмаСурьма
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
ТеллурТеллур
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
ИодИод
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
КсенонКсенон
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
ЦезийЦезий
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
БарийБарий
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
ЛантанЛантан
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
ЦерийЦерий
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
ПразеодимПразеодим
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
НеодимНеодим
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
ПрометийПрометий
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
СамарийСамарий
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
ЕвропийЕвропий
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
ГадолинийГадолиний
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
ТербийТербий
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
ДиспрозийДиспрозий
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
ГольмийГольмий
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
ЭрбийЭрбий
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
ТулийТулий
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
ИттербийИттербий
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
ЛютецийЛютеций
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
ГафнийГафний
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
ТанталТантал
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
ВольфрамВольфрам
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
РенийРений
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
ОсмийОсмий
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
ИридийИридий
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
ПлатинаПлатина
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
ЗолотоЗолото
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
РтутьРтуть
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
ТаллийТаллий
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
СвинецСвинец
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
ВисмутВисмут
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
ПолонийПолоний
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
АстатАстат
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
РадонРадон
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
ФранцийФранций
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
РадийРадий
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
АктинийАктиний
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
ТорийТорий
232,04
f-элемент
Серый мягкий металл
91
Pa
ПротактинийПротактиний
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
УранУран
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
НептунийНептуний
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
ПлутонийПлутоний
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
АмерицийАмериций
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
КюрийКюрий
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
БерклийБерклий
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
КалифорнийКалифорний
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
ЭйнштейнийЭйнштейний
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
ФермийФермий
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
МенделевийМенделевий
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
НобелийНобелий
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
ЛоуренсийЛоуренсий
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
РезерфордийРезерфордий
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
ДубнийДубний
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
СиборгийСиборгий
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
БорийБорий
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
ХассийХассий
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
МейтнерийМейтнерий
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
ДармштадтийДармштадтий
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.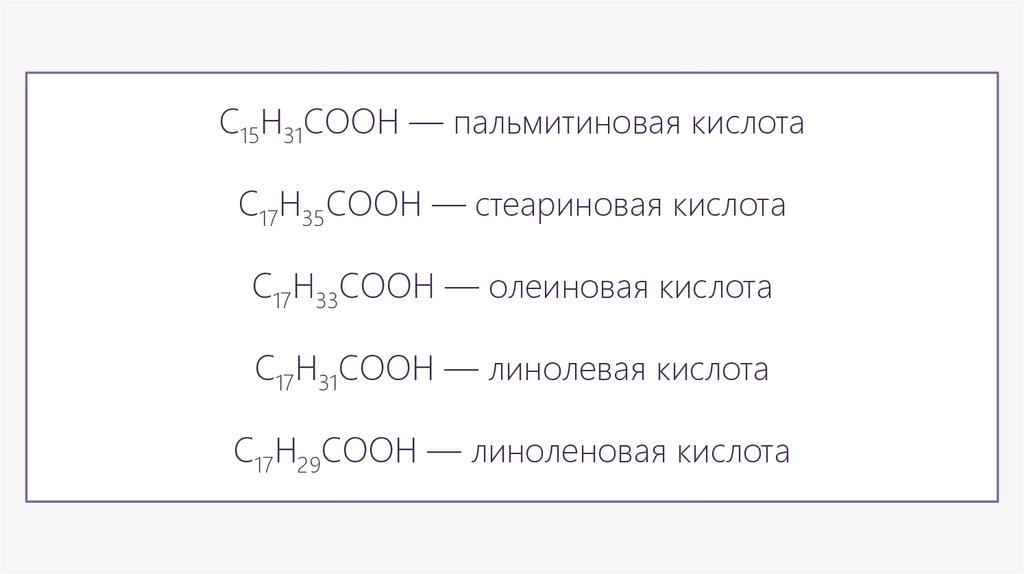
Чтобы получить подробное описание элемента, кликните по его названию.
Линолевая кислота — Тосканская диета
Линолевая кислота или LA или 18:2n-6 относится к группе липидов, известных как ненасыщенные жирные кислоты. Он имеет 18 атомов углерода и две двойные связи цис в положениях 9 и 12. Поскольку первая двойная связь по отношению к метильному концу расположена в положении 6, это полиненасыщенная жирная кислота омега-6 (ПНЖК) или омега-6 жирная кислота.
Линолевая кислота, от латинского linon , что означает лен, плюс олеиновая, что означает масло, была выделена Сакком Ф. в 1844 году из льняного масла, структура была уточнена Hilditch T.P. и другие. в 1939, и был синтезирован Рафаэлем Р.А. и Sondheimer F. в 1950 году.
Многие животные, включая человека, не могут ее синтезировать. Для этих животных линолевая кислота и альфа-линоленовая кислота или АЛК, которая является предшественником омега-3 полиненасыщенных жирных кислот или омега-3 жирных кислот, являются незаменимыми жирными кислотами, то есть жирными кислотами, которые необходимо получать из рациона. Кроме того, в отсутствие диетической LA другие омега-6 ПНЖК гамма-линоленовая кислота, дигомо-гамма-линоленовая кислота, арахидоновая кислота или ARA и адренокислота также становятся незаменимыми, поскольку она является их предшественником. По этой причине они определены как условно незаменимые жирные кислоты.
Кроме того, в отсутствие диетической LA другие омега-6 ПНЖК гамма-линоленовая кислота, дигомо-гамма-линоленовая кислота, арахидоновая кислота или ARA и адренокислота также становятся незаменимыми, поскольку она является их предшественником. По этой причине они определены как условно незаменимые жирные кислоты.
Как и другие жирные кислоты, редко встречается в свободной форме; чаще всего он связан сложноэфирными связями с органическими молекулами, такими как стеролы, глицерин и глицерол-3-фосфат, с образованием более сложных липидов, таких как сложные эфиры стеролов, например эфиры холестерина, триглицериды и фосфолипиды.
У людей он в изобилии содержится в жировой ткани и липопротеинах плазмы.
Он выполняет множество функций как прямо, так и косвенно через свои метаболиты. Его можно использовать для получения энергии. Это структурный компонент клеточных мембран. Он участвует в поддержании трансэпидермального водного барьера. Он служит предшественником для синтеза полиненасыщенных жирных кислот омега-6. Он может денасыщаться до альфа-линоленовой кислоты в сосудистых наземных растениях и фитопланктоне. Подобно ARA и докозагексаеновой кислоте или DHA, жирной кислоте омега-3, линолевая кислота служит предшественником для синтеза биоактивных липидных медиаторов. Наконец, было показано, что потребление LA с пищей обратно пропорционально риску ишемической болезни сердца.
Он может денасыщаться до альфа-линоленовой кислоты в сосудистых наземных растениях и фитопланктоне. Подобно ARA и докозагексаеновой кислоте или DHA, жирной кислоте омега-3, линолевая кислота служит предшественником для синтеза биоактивных липидных медиаторов. Наконец, было показано, что потребление LA с пищей обратно пропорционально риску ишемической болезни сердца.
Это самая распространенная ПНЖК в западной диете и единственная, потребление которой значительно увеличилось, в то время как потребление других жирных кислот омега-6 и омега-3 оставалось относительно постоянным с начала 1900-х годов, что соответствует меньшему менее 1% от суточной калорийности. Высокое потребление LA изменило соотношение омега-6 к омега-3 с 4:1 до 20:1.
Дефицит линолевой кислоты приводит к задержке роста и заживлению ран, дерматиту, репродуктивным проблемам, ожирению печени и полидипсии. Однако его дефицит встречается крайне редко из-за его обилия в западной диете и, следовательно, в грудном молоке, а также из-за его присутствия в детских смесях.
Основными пищевыми источниками являются соевое, кукурузное, подсолнечное, рапсовое и сафлоровое масла.
СВОЙСТВА, НАЗВАНИЯ И ИДЕНТИФИКАТОРЫ
Молекулярная масса: 280,447 г/моль
Молекулярная формула: C 18 H 32 O 2
точка: 230 °C (446 °F, 503,15 K) при 16 мм рт. Номер Европейского сообщества (ЕС): 200-470-9
В очищенном виде представляет собой бесцветное масло.
СОДЕРЖАНИЕ
- Синтез линолевой кислоты
- Распределение линолевой кислоты
- Метаболиты линолевой кислоты
- Роль линолевой кислоты
- Источники пищи
- Новые сорта
- Ссылки
Синтез линолевой кислоты
Линолевая кислота синтезируется из олеиновой кислоты, ненасыщенной жирной кислоты с цепью из 18 атомов углерода и двойной связью цис- в положении 9по отношению к метильному концу, поэтому омега-9 жирная кислота.
Реакция, катализируемая дельта-12-десатуразой (EC 1. 14.19.6), вводит вторую цис- двойную связь между атомами углерода 12 и 13 и является критическим этапом биосинтеза ПНЖК омега-6. .
14.19.6), вводит вторую цис- двойную связь между атомами углерода 12 и 13 и является критическим этапом биосинтеза ПНЖК омега-6. .
Следует подчеркнуть, что дельта-12-десатураза катализирует переход от омега-9 жирных кислот к омега-6 жирным кислотам.
Долгое время считалось, что этот фермент присутствует только в бактериях, простейших и растениях и что только эти организмы способны синтезировать линолевую кислоту. Однако в 1961 было показано, что насекомое, американский таракан Periplaneta americana , способно синтезировать линолевую кислоту. Впоследствии синтез МА был обнаружен у других насекомых и других беспозвоночных, в том числе у некоторых нематод, ракообразных и клещей.
Распределение линолевой кислоты
Линолевая кислота вместе с пальмитиновой и олеиновой кислотами является одной из наиболее распространенных жирных кислот в триглицеридах жировой ткани и липопротеинах плазмы, где ее концентрация отражает потребление с пищей. В США значительное увеличение потребления LA с пищей сопровождалось увеличением ее содержания в жировой ткани, которое оценивается >130%. Из-за своего обилия и подверженности окислению линолевая кислота является жирной кислотой, которая чаще всего окисляется в ЛПНП. А окисление липидов ЛПНП является фактором риска ишемической болезни сердца.
В США значительное увеличение потребления LA с пищей сопровождалось увеличением ее содержания в жировой ткани, которое оценивается >130%. Из-за своего обилия и подверженности окислению линолевая кислота является жирной кислотой, которая чаще всего окисляется в ЛПНП. А окисление липидов ЛПНП является фактором риска ишемической болезни сердца.
Хотя он необходим для развития нервной системы плода, он присутствует в мозге в низких концентрациях, менее 2% от общего количества жирных кислот, что намного ниже, чем у пальмитиновой кислоты, стеариновой кислоты, олеиновой кислоты, ДГК и АРК, которые составляют более 84% мозга. жирные кислоты.
Это самая распространенная ПНЖК в эпидермисе.
Метаболиты линолевой кислоты
Линолевая кислота является предшественником всех омега-6 жирных кислот.
Его можно десатурировать до альфа-линоленовой кислоты, предшественника омега-3 ПНЖК. Реакцию катализирует дельта-15-десатураза (КФ 1.14.19.25), который присутствует только в пластидах и в эндоплазматическом ретикулуме фитопланктона и сосудистых наземных растений.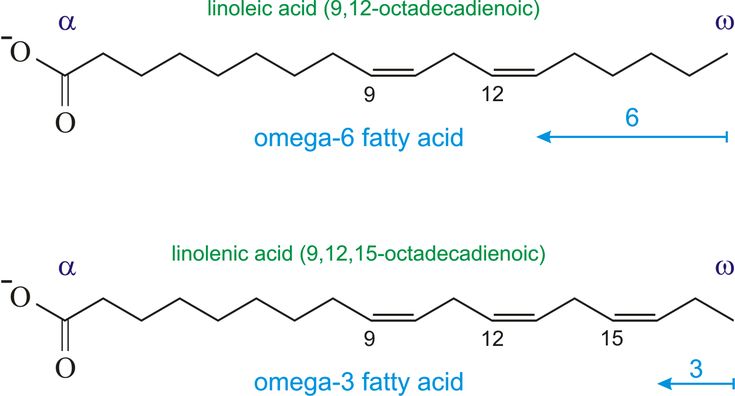 Следует подчеркнуть, что дельта-15-десатураза катализирует переход от омега-6 жирных кислот к омега-3 жирным кислотам.
Следует подчеркнуть, что дельта-15-десатураза катализирует переход от омега-6 жирных кислот к омега-3 жирным кислотам.
Является предшественником биоактивных липидных медиаторов с аутокринным и паракринным действием, которые участвуют в регуляции многих клеточных процессов. Подобно арахидоновой и докозагексаеновой кислотам, при высвобождении из фосфолипидов мембраны она может окисляться в реакциях, катализируемых такими ферментами, как 12-липоксигеназа (КФ 1.13.11.31), 15-липоксигеназа (КФ 1.13.11.33), циклооксигеназы (КФ 1.14. 99.1), растворимой эпоксигидролазой (КФ 3.3.2.10) и ферментами семейства цитохромов Р450, а именно теми же ферментами, которые участвуют в метаболизме АРК и ДГК. Он также может быть окислен свободными радикалами. Продуцируемые медиаторы, такие как эпокси- и моно-, ди- и тригидроксипроизводные, называемые метаболитами окисленной линолевой кислоты (OXLAM), участвуют в передаче клеточных сигналов и регуляции боли и воспаления.
Поскольку линолевая кислота может быть преобразована в арахидоновую кислоту, которая является предшественником биоактивных липидных медиаторов, некоторые из которых обладают противовоспалительной активностью или способны способствовать разрешению воспалительных повреждений, другие обладают провоспалительной активностью, было высказано предположение, что уровни ARA можно уменьшить, уменьшив потребление LA. Однако, по крайней мере, у субъектов, придерживающихся типичной западной диеты, этого, по-видимому, не происходит, поскольку преобразование LA в ARA очень скромное, от 0,3% до 0,6%, аналогично тому, что происходит при преобразовании ALA в DHA. Кроме того, было высказано предположение, что на профиль липидных медиаторов, а также на воспалительную реакцию на диету, богатую линолевой кислотой, влияют генотип FADS1 , где ген FADS1 кодирует дельта-5-десатуразу (КФ 1.14.19.44), фермент, катализирующий вторую реакцию десатурации пути синтеза арахидоновой кислоты, то есть десатурацию дигомо-гамма-линоленовой кислоты до АРА.
Однако, по крайней мере, у субъектов, придерживающихся типичной западной диеты, этого, по-видимому, не происходит, поскольку преобразование LA в ARA очень скромное, от 0,3% до 0,6%, аналогично тому, что происходит при преобразовании ALA в DHA. Кроме того, было высказано предположение, что на профиль липидных медиаторов, а также на воспалительную реакцию на диету, богатую линолевой кислотой, влияют генотип FADS1 , где ген FADS1 кодирует дельта-5-десатуразу (КФ 1.14.19.44), фермент, катализирующий вторую реакцию десатурации пути синтеза арахидоновой кислоты, то есть десатурацию дигомо-гамма-линоленовой кислоты до АРА.
Роль линолевой кислоты
Для большинства животных, включая человека, линолевая кислота является незаменимой жирной кислотой и играет важную роль, действуя напрямую или через свои метаболиты.
- Может использоваться как источник энергии. Например, он поступает в мозг со скоростью, сравнимой со скоростью ДГК, АРК и других жирных кислот.
 ARA и DHA в основном входят в состав мембранных фосфолипидов, тогда как почти 60% линолевой кислоты окисляется по пути бета-окисления. Кроме того, часть произведенного ацетата используется для синтеза холестерина в головном мозге.
ARA и DHA в основном входят в состав мембранных фосфолипидов, тогда как почти 60% линолевой кислоты окисляется по пути бета-окисления. Кроме того, часть произведенного ацетата используется для синтеза холестерина в головном мозге. - В качестве компонента мембранных фосфолипидов он участвует в поддержании текучести мембран.
- В составе мембранных сфинголипидов участвует в формировании и поддержании водопроницаемого барьера кожи.
- Он может связываться с PPARα и активировать его.
Этот фактор транскрипции играет важную роль в регуляции метаболизма. Например, он ингибирует транскрипцию генов, кодирующих ферменты, участвующие в липогенезе, и активирует транскрипцию генов, кодирующих ферменты, участвующие в липолизе, а также в митохондриальном и лизосомальном бета-окислении. Таким образом, линолевая кислота может снижать уровень общего холестерина и холестерина ЛПНП в плазме, тем самым способствуя снижению сердечно-сосудистого риска.
Источники пищи
В двадцатом веке потребление растительных масел, богатых линолевой кислотой, в Соединенных Штатах увеличилось в 20 раз.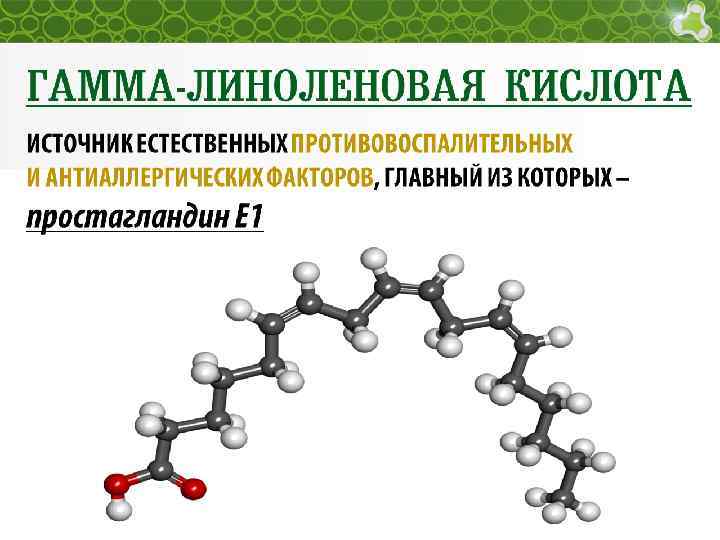 Это увеличение произошло из-за:
Это увеличение произошло из-за:
- разработки сортов, дающих семена с высоким содержанием LA, особенно сои и кукурузы;
- повышенная коммерческая доступность производных масел;
- диетических рекомендаций по увеличению его потребления в качестве средства для снижения уровня холестерина в крови, рекомендации, полученные в результате исследований американского физиолога Анселя Киза в середине 19-го века.50-е годы.
Это привело к нынешнему уровню потребления LA, составляющему около 6% от общей калорийности рациона, по сравнению со значениями до 1930-х годов, которые варьировались от 1 до 2% от общей калорийности рациона.
В диете США соевое масло является основным диетическим источником LA, на долю которого приходится около 45% его пищевого потребления.
Другими продуктами, богатыми линолевой кислотой, являются кислое кукурузное, подсолнечное, сафлоровое и рапсовое масла и соответствующие семена, а также грецкие орехи, арахис, семена хлопка и кунжута.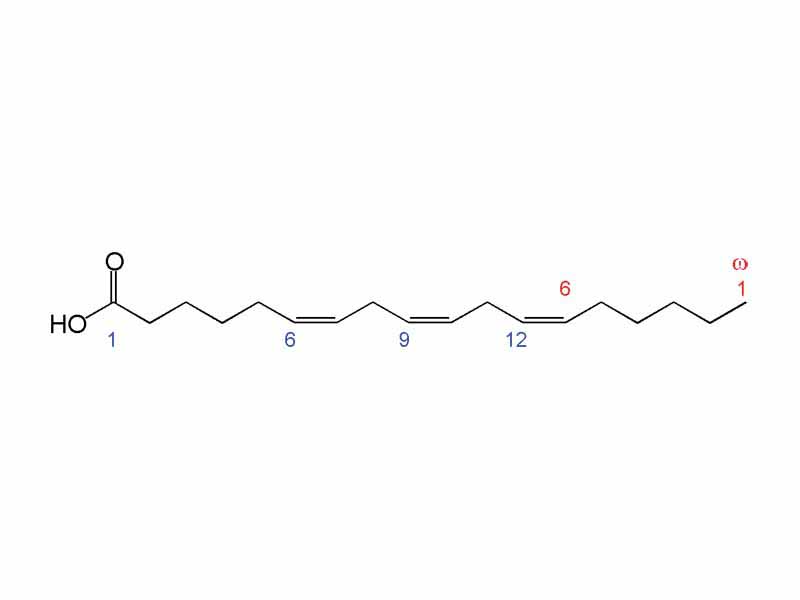
Животные, получающие пищу, богатую линолевой кислотой, также могут быть хорошим источником.
Это самая распространенная ПНЖК в пищевых продуктах. Самые высокие значения снова обнаружены в соевом масле, где оно составляет до 88% от общего количества ПНЖК и превышает 70% от общего количества ПНЖК в наиболее часто потребляемых продуктах питания. Например, в свинине, говядине и курятине она составляет от 75 до 85% от общего количества ПНЖК, а в яйцах превышает 80%. Более того, это основная ПНЖК в овощах, фруктах и злаках, то есть в продуктах с низким содержанием жира. Исключение составляет фасоль, где на ее долю приходится 40-50% от общего количества ПНЖК.
Новые сорта
В природе линолевая кислота синтезируется в концентрациях, сравнимых с концентрациями альфа-линоленовой кислоты.
Хотя в 1930-х годах были отобраны сорта, дающие семена с высоким содержанием LA, в последние годы эта тенденция меняется, поскольку были выбраны новые сорта, дающие семена с более низким содержанием LA.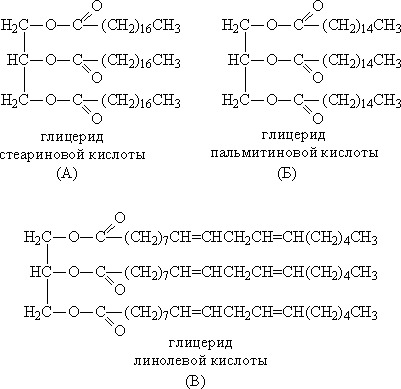 Более того, по большей части линолевая кислота заменена олеиновой кислотой. Это позволило получить не только подсолнечное и сафлоровое масла с высоким содержанием олеиновой кислоты вместо высокого содержания МК, но и соевые бобы с высоким содержанием олеиновой кислоты. И поскольку новые сорта заменят традиционные сорта, предположительно произойдет сокращение потребления линолевой кислоты в пользу олеиновой. Это может привести к тому, что уровни потребления МА вернутся к уровням, сопоставимым с теми, что были в начале 19 века.00с. Этот переход может принести пользу для здоровья, поскольку потребление олеиновой кислоты связано с улучшением уровня холестерина ЛПВП. Следует подчеркнуть, что хорошее потребление олеиновой кислоты с пищей в виде оливкового масла первого холодного отжима является особенностью средиземноморской диеты.
Более того, по большей части линолевая кислота заменена олеиновой кислотой. Это позволило получить не только подсолнечное и сафлоровое масла с высоким содержанием олеиновой кислоты вместо высокого содержания МК, но и соевые бобы с высоким содержанием олеиновой кислоты. И поскольку новые сорта заменят традиционные сорта, предположительно произойдет сокращение потребления линолевой кислоты в пользу олеиновой. Это может привести к тому, что уровни потребления МА вернутся к уровням, сопоставимым с теми, что были в начале 19 века.00с. Этот переход может принести пользу для здоровья, поскольку потребление олеиновой кислоты связано с улучшением уровня холестерина ЛПВП. Следует подчеркнуть, что хорошее потребление олеиновой кислоты с пищей в виде оливкового масла первого холодного отжима является особенностью средиземноморской диеты.
Каталожные номера
- Akoh C.C. и Мин Д.Б. Пищевые липиды: химия, питание и биотехнология. 3-е издание. CRC Press, Taylor & Фрэнсис Групп, 2008
- Blasbalg T.
 L., Hibbeln J.R., Ramsden C.E., Majchrzak S.F. & Rawlings R.R. Изменения в потреблении омега-3 и омега-6 жирных кислот в Соединенных Штатах в течение 20-го века. Ам Дж. Клин Нутр 2011; 93(5):950-962. doi:10.3945/ajcn.110.006643
L., Hibbeln J.R., Ramsden C.E., Majchrzak S.F. & Rawlings R.R. Изменения в потреблении омега-3 и омега-6 жирных кислот в Соединенных Штатах в течение 20-го века. Ам Дж. Клин Нутр 2011; 93(5):950-962. doi:10.3945/ajcn.110.006643 - Чоу Чинг К. Жирные кислоты в пищевых продуктах и их значение для здоровья. 3-е издание. CRC Press, Taylor & Фрэнсис Групп, 2008
- Фарвид М.С., Дин М., Пан А., Сунь К., Чиуве С.Е., Штеффен Л.М., Уиллетт В.К., Ху Ф.Б. Пищевая линолевая кислота и риск ишемической болезни сердца: систематический обзор и метаанализ проспективных когортных исследований. Тираж 2014; 130:1568-1578. doi:10.1161/РАСПИСАНИЕAHA.114.010236
- Гиене С.Дж., Карлсон С.Е. Увеличение содержания линолевой кислоты в жировой ткани взрослых людей США за последние полвека. Adv Nutr 2015;6(6):660-664. дои: https://DOI.org/10.3945/ан.115.009944
- Яндачек Р.Дж. Линолевая кислота: проблемы с питанием. Здравоохранение 2017;5(2):25. doi:10.3390/здравоохранение5020025
- Lankinen M.
 A., Fauland A., Shimizu B., Agren J., Wheelock CE, Laakso M., Schwab U. и Pihlajamaki J. Воспалительная реакция на пищевую линолевую кислоту зависит от генотипа FADS1 . Ам Дж. Клин Нутр 2019; 109: 165–175. дои: 10.1093/ajcn/nqy287
A., Fauland A., Shimizu B., Agren J., Wheelock CE, Laakso M., Schwab U. и Pihlajamaki J. Воспалительная реакция на пищевую линолевую кислоту зависит от генотипа FADS1 . Ам Дж. Клин Нутр 2019; 109: 165–175. дои: 10.1093/ajcn/nqy287 - Мальцицка М., Виссер Б., Эллерс Дж. Эволюционный взгляд на синтез линолевой кислоты у животных. Эвол Биол 2018;45:15-26. дои: 10.1007/s11692-017-9436-5
- Шустер С. Джонсон С.Д., Хеннебель М., Холтманн Т., Таха А.Ю., Кирпич И.А., Эгучи А., Рамсден С.Е., Папучадо Б.Г., Макклейн С.Дж., Фельдштейн А.Е. Окисленные метаболиты линолевой кислоты вызывают дисфункцию митохондрий печени, апоптоз и активацию NLRP3 в мышей. J Lipid Res 2018;59(9):1597-1609. дои: 10.1194/jlr.M083741
- Таха А.Ю. Линолевая кислота — полезная или вредная для мозга? NPJ Sci Food 2020; 4:1. дои: 10.1038/s41538-019-0061-9
- Уилан Дж. и Фриче К. Линолевая кислота. Ад Нутр 2013;4(3): 311-312. Дои: 10.3945/ан.113.003772
Линолевая кислота.
 Что такое линолевая кислота? О его науке, химии и структуре
Что такое линолевая кислота? О его науке, химии и структуреЛинолевая кислота (ЛК) представляет собой ненасыщенную жирную кислоту омега-6. Слово линолевая происходит от греческого слова linon (лен). Олеиновый означает, относящийся к нефти или полученный из нефти, или относящийся к олеиновой кислоте. Линолевая кислота — полиненасыщенная жирная кислота, используемая в биосинтезе простагландинов. Он содержится в липидах клеточных мембран. Его много во многих растительных маслах, особенно в сафлоровом и подсолнечном. Жирные кислоты представляют собой карбоновые кислоты с длинным неразветвленным алифатическим хвостом (цепью), которые бывают либо насыщенными, либо ненасыщенными. Можно предположить, что жирные кислоты, полученные из натуральных жиров и масел, имеют по меньшей мере 8 атомов углерода. Большинство природных жирных кислот имеют четное число атомов углерода, потому что в их биосинтезе участвует ацетил-КоА, кофермент, несущий группу из двух атомов углерода.
Ненасыщенные жирные кислоты имеют одну или несколько алкенильных функциональных групп вдоль цепи.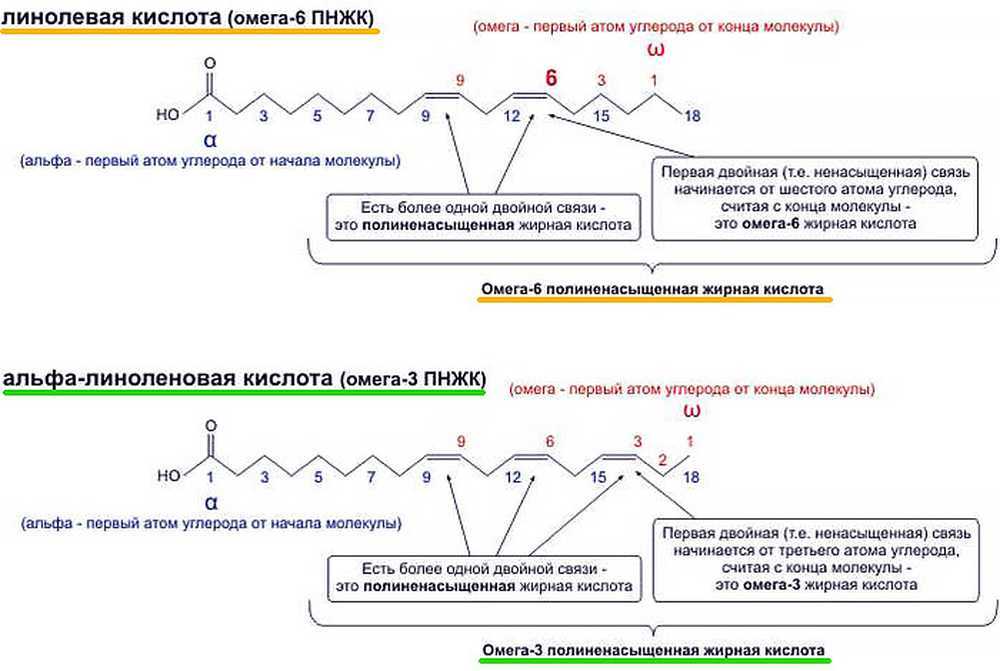 Два следующих атома углерода в цепи, связанные с любой стороной двойной связи, могут находиться в цис- или транс-конфигурации. Цис-конфигурация означает, что соседние атомы углерода находятся по одну сторону от двойной связи. Жесткость двойной связи замораживает ее конформацию, а в случае цис-изомера вызывает изгиб цепи и ограничивает конформационную свободу жирной кислоты. Чем больше двойных связей в цис-конфигурации цепи, тем меньше ее гибкость. Когда в цепи много цис-связей, она становится весьма искривленной в своих наиболее доступных конформациях. Например, олеиновая кислота с одной двойной связью имеет «перегиб», а линолевая кислота с двумя двойными связями имеет более выраженный изгиб. Альфа-линоленовая кислота с тремя двойными связями способствует крюкообразной форме. Эффект этого заключается в том, что в ограниченных средах, например, когда жирные кислоты являются частью фосфолипида в липидном бислое или триглицеридов в липидных каплях, цис-связи ограничивают способность жирных кислот плотно упаковываться и, следовательно, может влиять на температуру плавления мембраны или жира.
Два следующих атома углерода в цепи, связанные с любой стороной двойной связи, могут находиться в цис- или транс-конфигурации. Цис-конфигурация означает, что соседние атомы углерода находятся по одну сторону от двойной связи. Жесткость двойной связи замораживает ее конформацию, а в случае цис-изомера вызывает изгиб цепи и ограничивает конформационную свободу жирной кислоты. Чем больше двойных связей в цис-конфигурации цепи, тем меньше ее гибкость. Когда в цепи много цис-связей, она становится весьма искривленной в своих наиболее доступных конформациях. Например, олеиновая кислота с одной двойной связью имеет «перегиб», а линолевая кислота с двумя двойными связями имеет более выраженный изгиб. Альфа-линоленовая кислота с тремя двойными связями способствует крюкообразной форме. Эффект этого заключается в том, что в ограниченных средах, например, когда жирные кислоты являются частью фосфолипида в липидном бислое или триглицеридов в липидных каплях, цис-связи ограничивают способность жирных кислот плотно упаковываться и, следовательно, может влиять на температуру плавления мембраны или жира.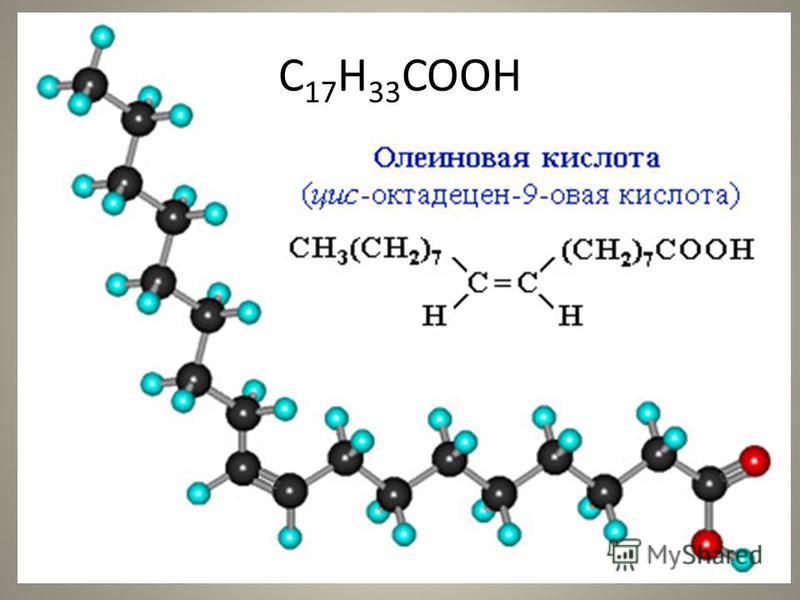 Транс-конфигурация, напротив, означает, что следующие два атома углерода связаны с противоположными сторонами двойной связи. В результате они не вызывают сильного изгиба цепи, а их форма похожа на прямые насыщенные жирные кислоты. В большинстве встречающихся в природе ненасыщенных жирных кислот каждая двойная связь имеет после себя 3n атомов углерода для некоторого n, и все они являются цис-связями. Большинство жирных кислот в транс-конфигурации (трансжиры) не встречаются в природе и являются результатом обработки человеком (например, гидрогенизации).
Различия в геометрии между различными типами ненасыщенных жирных кислот, а также между насыщенными и ненасыщенными жирными кислотами играют важную роль в биологических процессах и в построении биологических структур (например, клеточных мембран).
Транс-конфигурация, напротив, означает, что следующие два атома углерода связаны с противоположными сторонами двойной связи. В результате они не вызывают сильного изгиба цепи, а их форма похожа на прямые насыщенные жирные кислоты. В большинстве встречающихся в природе ненасыщенных жирных кислот каждая двойная связь имеет после себя 3n атомов углерода для некоторого n, и все они являются цис-связями. Большинство жирных кислот в транс-конфигурации (трансжиры) не встречаются в природе и являются результатом обработки человеком (например, гидрогенизации).
Различия в геометрии между различными типами ненасыщенных жирных кислот, а также между насыщенными и ненасыщенными жирными кислотами играют важную роль в биологических процессах и в построении биологических структур (например, клеточных мембран).
Организм человека может производить все необходимые ему жирные кислоты, кроме двух. Эти два вещества, линолевая кислота (LA) и альфа-линоленовая кислота (LNA), широко распространены в растительных маслах.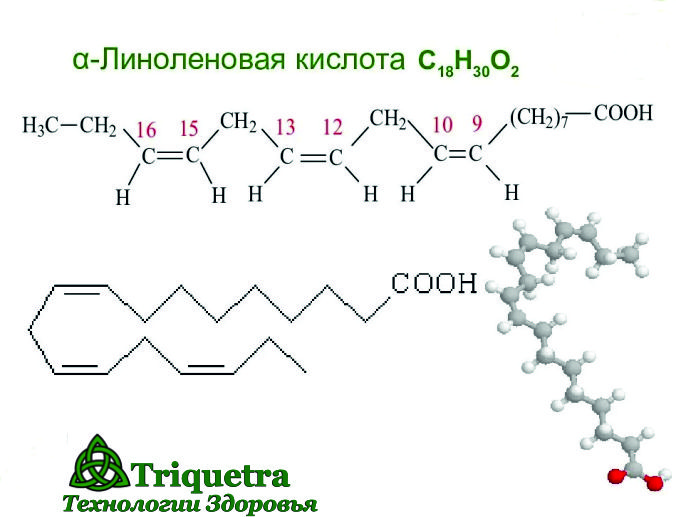 Кроме того, рыбий жир содержит длинноцепочечные омега-3 жирные кислоты эйкозапентаеновую кислоту (ЭПК) и докозагексаеновую кислоту (ДГК). Поскольку они не могут образовываться в организме из других субстратов и должны поступать с пищей, их называют незаменимыми жирными кислотами. У млекопитающих отсутствует способность вводить двойные связи в жирные кислоты за пределами углерода 9.и 10. Следовательно, линолевая кислота и линоленовая кислота являются незаменимыми жирными кислотами для человека. В организме незаменимые жирные кислоты в основном используются для производства гормоноподобных веществ, которые регулируют широкий спектр функций, включая артериальное давление, свертываемость крови, уровень липидов в крови, иммунный ответ и воспалительную реакцию на инфекцию.
Кроме того, рыбий жир содержит длинноцепочечные омега-3 жирные кислоты эйкозапентаеновую кислоту (ЭПК) и докозагексаеновую кислоту (ДГК). Поскольку они не могут образовываться в организме из других субстратов и должны поступать с пищей, их называют незаменимыми жирными кислотами. У млекопитающих отсутствует способность вводить двойные связи в жирные кислоты за пределами углерода 9.и 10. Следовательно, линолевая кислота и линоленовая кислота являются незаменимыми жирными кислотами для человека. В организме незаменимые жирные кислоты в основном используются для производства гормоноподобных веществ, которые регулируют широкий спектр функций, включая артериальное давление, свертываемость крови, уровень липидов в крови, иммунный ответ и воспалительную реакцию на инфекцию.
Официальное химическое название (IUPAC)
(9Z,12Z)-октадека-9,12-диеновая кислота
Ссылки
http://en.wikipedia.org/wiki/Unsaturated_fatty_acid
нажмите на изображение линолевой кислоты выше, чтобы взаимодействовать
с 3D-моделью
Структура линолевой кислоты
(откроется новое окно браузера)
C18 h42 O2
Обновление Карла Харрисона
(Молекула месяца для
август 2007 г.
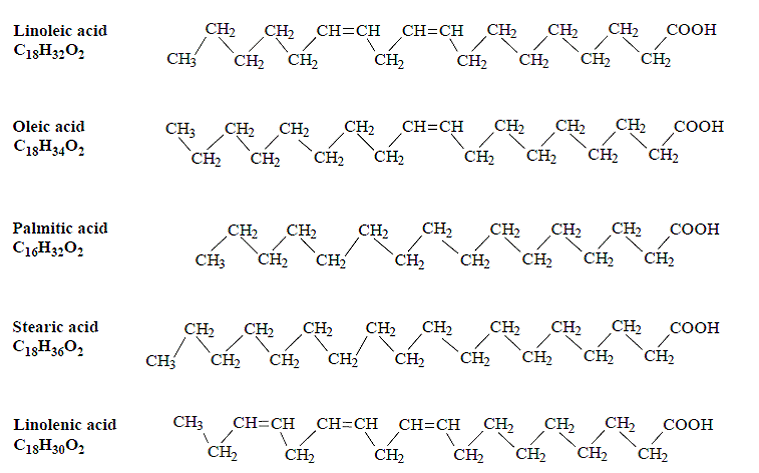 ARA и DHA в основном входят в состав мембранных фосфолипидов, тогда как почти 60% линолевой кислоты окисляется по пути бета-окисления. Кроме того, часть произведенного ацетата используется для синтеза холестерина в головном мозге.
ARA и DHA в основном входят в состав мембранных фосфолипидов, тогда как почти 60% линолевой кислоты окисляется по пути бета-окисления. Кроме того, часть произведенного ацетата используется для синтеза холестерина в головном мозге. L., Hibbeln J.R., Ramsden C.E., Majchrzak S.F. & Rawlings R.R. Изменения в потреблении омега-3 и омега-6 жирных кислот в Соединенных Штатах в течение 20-го века. Ам Дж. Клин Нутр 2011; 93(5):950-962. doi:10.3945/ajcn.110.006643
L., Hibbeln J.R., Ramsden C.E., Majchrzak S.F. & Rawlings R.R. Изменения в потреблении омега-3 и омега-6 жирных кислот в Соединенных Штатах в течение 20-го века. Ам Дж. Клин Нутр 2011; 93(5):950-962. doi:10.3945/ajcn.110.006643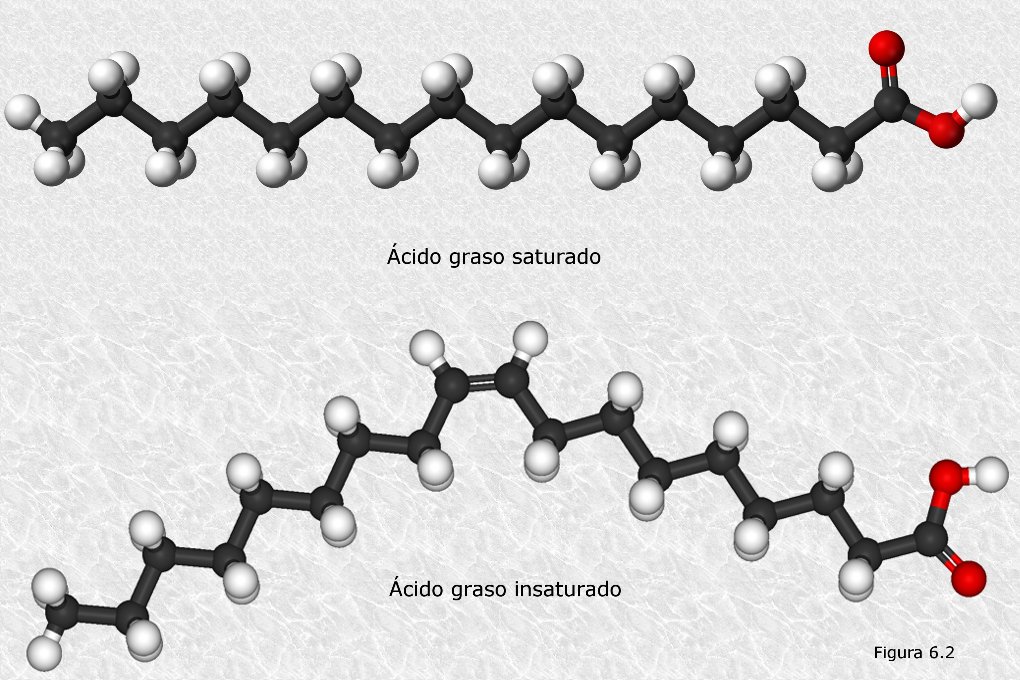 A., Fauland A., Shimizu B., Agren J., Wheelock CE, Laakso M., Schwab U. и Pihlajamaki J. Воспалительная реакция на пищевую линолевую кислоту зависит от генотипа FADS1 . Ам Дж. Клин Нутр 2019; 109: 165–175. дои: 10.1093/ajcn/nqy287
A., Fauland A., Shimizu B., Agren J., Wheelock CE, Laakso M., Schwab U. и Pihlajamaki J. Воспалительная реакция на пищевую линолевую кислоту зависит от генотипа FADS1 . Ам Дж. Клин Нутр 2019; 109: 165–175. дои: 10.1093/ajcn/nqy287