Лекарство Редуксин Лайт — инструкция по применению, отзывы
Раздел предназначен исключительно для медицинских и фармацевтических работников! Если Вы не являетесь медицинским и фармацевтическим работником — покиньте раздел! Условия использования
ЛЕКАРСТВЕННОЕ СРЕДСТВО
Купить Редуксин Лайт
В аптеках Санкт-Петербурга и Ленинградской области
от 2 025
КупитьВ других регионахОтзывы 93
Инструкция к лекарству Редуксин Лайт, противопоказания и способы применения, побочные эффекты и отзывы об этом препарате. Мнения врачей и возможность обсудить на форуме.
Редуксин Лайт
Состав
1 капсула содержит конъюгированная линолевая кислота — 500 мг, витамин Е; вспомогательные вещества: желатин, глицерин, вода очищенная, лимонная кислота
Фармакологические действие
Редуксин-лайт – биологически активная добавка к пище – средство для контроля веса и формирования подтянутого и привлекательного силуэта. Конъюгированная линолевая кислота (КЛК) – это полиненасыщенная жирная кислота природного происхождения, первоначально найденная в мясе крупного рогатого скота и молочных продуктах, в которых она содержится в ничтожных количествах. В настоящее время в промышленных масштабах конъюгированную линолевую кислоту преимущественно получают из растительных источников, например, из сафлорового масла.
КЛК (CLA) оказывает благоприятное влияние на обмен веществ в организме. КЛК (CLA) препятствует работе фермента, который задерживает жир в организме, и активирует ферментные системы, которые перерабатывают жир. Это приводит к уменьшению подкожного жира и к укреплению мышечной ткани за счет использования высвободившейся энергии, которая идет на белковый синтез.
Таким образом, КЛК (CLA) помогает организму человека использовать жир в качестве источника энергии и моделировать подтянутый и привлекательный силуэт!
Конъюгированная линолевая кислота (КЛК) – это полиненасыщенная жирная кислота природного происхождения, первоначально найденная в мясе крупного рогатого скота и молочных продуктах, в которых она содержится в ничтожных количествах. В настоящее время в промышленных масштабах конъюгированную линолевую кислоту преимущественно получают из растительных источников, например, из сафлорового масла.
КЛК (CLA) оказывает благоприятное влияние на обмен веществ в организме. КЛК (CLA) препятствует работе фермента, который задерживает жир в организме, и активирует ферментные системы, которые перерабатывают жир. Это приводит к уменьшению подкожного жира и к укреплению мышечной ткани за счет использования высвободившейся энергии, которая идет на белковый синтез.
Таким образом, КЛК (CLA) помогает организму человека использовать жир в качестве источника энергии и моделировать подтянутый и привлекательный силуэт!
Способ применения и дозы
Принимать взрослым по 1-2 капсулы в сутки во время еды. Продолжительность приема 1-2 месяца. Прием рекомендуется повторять 3-4 раза в год.
Оптимальное количество КЛК для достижения максимальной эффективности по моделированию фигуры составляет от 2 до 3 г в сутки (в пересчете на содержание КЛК в Редуксине-лайт – 4-6 капсул в сутки).
Продолжительность приема 1-2 месяца. Прием рекомендуется повторять 3-4 раза в год.
Оптимальное количество КЛК для достижения максимальной эффективности по моделированию фигуры составляет от 2 до 3 г в сутки (в пересчете на содержание КЛК в Редуксине-лайт – 4-6 капсул в сутки).
Условия хранения
Хранить в сухом, недоступном для детей месте при температуре не выше 30°С.
Показания к применению
Рекомендуется в качестве биологически активной добавки к пище — источника конъюгированной линолевой кислоты (КЛК).
Противопоказания
Индивидуальная непереносимость компонентов, беременность, кормление грудью, детский возраст до 18 лет. Перед применением рекомендуется проконсультироваться с врачом.
Перед применением рекомендуется проконсультироваться с врачом.
Актуализация
Информация предоставлена справочником лекарственных средств «Видаль». Последняя актуализация описания 28.09.2011
Срок годности
3 года.
Отзывы 93
Укажите e-mail на который будут приходить уведомления о новых сообщениях
Средство для похудения «Редуксин Лайт». Инструкция по применению и противопоказания
Как можно дольше все нормальные люди на Земле желают оставаться молодыми и красивыми. «Редуксин Лайт» — новая инновационная разработка на рынке активных биологически активных добавок, способная помочь в реализации стремлений человека к оздоровлению.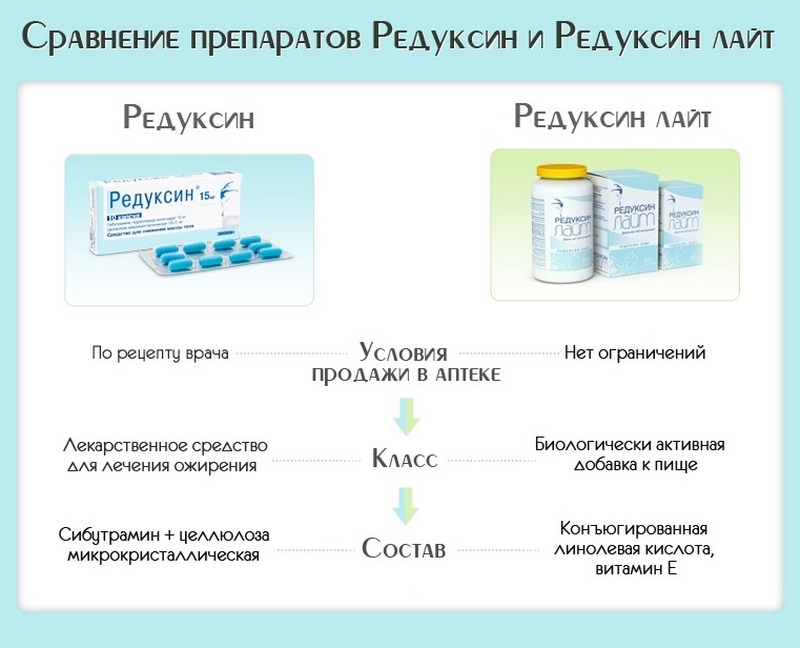
Основной формой выпуска препарата «Редуксин Лайт» инструкция по применению называет капсулы, которые содержат действующее вещество – конъюгированную лимонную кислоту (КЛК) с витамином Е. Вспомогательные вещества представлены в виде глицерина, желатина, лимонной кислоты. и очищенная вода. В одной упаковке лекарственного средства содержится 30 или 90 капсул.
Биологически активная добавка к пище, которой является Редуксин Лайт, аннотация представляет как средство контроля веса, формирования привлекательного силуэта. Ранее основной компонент препарата в виде CLA в небольших количествах обнаруживался в мясе животных и молочных продуктах. В промышленности его теперь получают из источников растительного происхождения (сафлоровое масло). Благоприятное действие препарата «Редуксин Лайт» инструкция по применению относится к его активной стимуляции обменных процессов. CLC минимизирует выработку ферментов, влияющих на удержание жира в организме, и, наоборот, стимулирует выработку других систем, активно перерабатывающих жир. За счет высвобождаемой энергии укрепляется мышечная масса, а это, в свою очередь, уменьшает жировые отложения.
За счет высвобождаемой энергии укрепляется мышечная масса, а это, в свою очередь, уменьшает жировые отложения.
Таким образом, CLC заставляет накопленный в организме жир выступать в качестве источника энергии и придает фигуре привлекательность и стройность.
В качестве основных показаний к применению активной БАД «Редуксин Лайт» инструкция по применению называет алиментарное ожирение, сопряженное, в том числе с факторами риска, нарушением жирового обмена в организме.
Отмечено комплексное действие препарата «Редуксин Лайт», описание применения БАД разделено на три направления:
- 1. В качестве меры по исправлению положения. Рекомендуется включать Редуксин Лайт в качестве добавки к питанию при иммунных, эндокринных, желудочно-кишечных заболеваниях, а также в качестве профилактики при развитии атеросклероза.
- 2. Как средство для похудения. В этом качестве выделяют несколько направлений действия препарата «Редуксин Лайт», инструкция по применению рекомендует данную пищевую добавку для:
— сжигание жира, не прибегая к уменьшению мышечной массы.
— Препятствие повторяющимся жировым скоплениям в подкожном слое и превращение их в источник энергии;
— активное воздействие на проблемные зоны тела (область бедер, живота) и установление пропорциональности фигуры человека.
3. В качестве стимулятора для поддержания спортивного телосложения. Здесь действие препарата обеспечивает:
— ускорение обменных процессов;
— действует как антиоксидант;
— Повышение мышечного тонуса;
— улучшение спортивных результатов.
Наряду с благотворным действием БАД «Редуксин Лайт» имеется ряд противопоказаний к средству:
— почечные и печеночные обострения;
— психические заболевания;
— инсульт:
— артериальная гипертензия;
Анорексия, булимия;
— медикаментозная, наркотическая, алкогольная зависимость;
— ИБС, инфаркт, тахикардия, аритмия, пороки сердца;
— беременность и лактация;
— ограничения по возрасту (подростки и лица старше 65 лет).
Известны единичные случаи побочных эффектов при применении препарата Редуксин Лайт, к ним относятся чувство сухости во рту и резкая потеря аппетита, иногда могут быть бессонница, головная боль, некоторые люди отличаются особой раздражительностью и тревожностью. «Редуксин Лайт» назначается только в том случае, если немедикаментозные методы похудения не принесли ожидаемого эффекта. При покупке пищевой добавки «Редуксин Лайт» следует обратить внимание на наличие внутри упаковки инструкции по применению препарата.
Информация о продукте RITUXAN HYCELA
Показания
RITUXAN HYCELA ® (ритуксимаб/гиалуронидаза человека) показан для лечения взрослых пациентов с:
- Рецидивирующим или рефрактерным, фолликулярная лимфома (ФЛ) в качестве монотерапии
- Ранее не леченная фолликулярная лимфома в комбинации с химиотерапией первой линии и у пациентов, достигших полного или частичного ответа на ритуксимаб в комбинации с химиотерапией, в качестве монотерапии поддерживающей терапии
- Непрогрессирующая (включая стабильное заболевание) фолликулярная лимфома в качестве монотерапии после первой линии химиотерапии циклофосфамидом, винкристином и преднизоном (CVP)
- Ранее не леченная диффузная крупноклеточная В-клеточная лимфома (ДВККЛ) в комбинации с циклофосфамидом, доксорубицином, винкристином, преднизоном (СНОР) или другими схемами химиотерапии на основе антрациклинов
- Ранее нелеченный и ранее леченный хронический лимфолейкоз (ХЛЛ) в комбинации с флударабином и циклофосфамидом (ФК)
Ограничения по применению
- Начинайте лечение препаратом РИТУКСАН ХАЙСЕЛА только после того, как пациенты получили по крайней мере одну полную дозу ритуксимаба путем внутривенной инфузии
- RITUXAN HYCELA не показан для лечения доброкачественных заболеваний
ПРЕДУПРЕЖДЕНИЯ В КОРОБКЕ: Тяжёлые кожно-слизистые реакции, реактивация вируса гепатита В и прогрессирующая мультифокальная лейкоэнцефалопатия
- кожно-слизистые реакции могут возникать у пациентов, получающих препараты, содержащие ритуксимаб, включая RITUXAN HYCELA
- Реактивация вируса гепатита B (HBV): Реактивация HBV может происходить у пациентов, получавших препараты, содержащие ритуксимаб, включая RITUXAN HYCELA, что в некоторых случаях приводило к фульминантному гепатиту, печеночной недостаточности и смерти.
 Проведите скрининг всех пациентов на инфекцию ВГВ до начала лечения и наблюдайте за пациентами во время и после лечения препаратом РИТУКСАН ХИСЕЛА. Прекратить прием РИТУКСАН HYCELA и сопутствующих препаратов в случае реактивации ВГВ
Проведите скрининг всех пациентов на инфекцию ВГВ до начала лечения и наблюдайте за пациентами во время и после лечения препаратом РИТУКСАН ХИСЕЛА. Прекратить прием РИТУКСАН HYCELA и сопутствующих препаратов в случае реактивации ВГВ - Прогрессирующая мультифокальная лейкоэнцефалопатия (ПМЛ), включая ПМЛ с летальным исходом, может возникать у пациентов, получающих препараты, содержащие ритуксимаб, включая RITUXAN HYCELA
ПРЕДУПРЕЖДЕНИЯ И МЕРЫ ПРЕДОСТОРОЖНОСТИ
Тяжелые кожно-слизистые реакции. Эти реакции включают паранеопластическую пузырчатку, синдром Стивенса-Джонсона, лихеноидный дерматит, везикулобуллезный дерматит и токсический эпидермальный некролиз
Реактивация вируса гепатита В
- Реактивация вируса гепатита В (ВГВ), в некоторых случаях приводящая к фульминантному гепатиту, печеночной недостаточности и смерти, может возникать у пациентов, получающих цитолитические антитела против CD20, включая препараты, содержащие ритуксимаб
- Реактивация HBV определяется как резкое увеличение репликации HBV, проявляющееся быстрым повышением уровня ДНК HBV в сыворотке или обнаружением HBsAg у человека, который ранее был HBsAg-отрицательным и анти-HBc-положительным.
 Реактивация репликации HBV часто сопровождается гепатитом, то есть повышением уровня трансаминаз. В тяжелых случаях может наступить повышение уровня билирубина, печеночная недостаточность и смерть
Реактивация репликации HBV часто сопровождается гепатитом, то есть повышением уровня трансаминаз. В тяжелых случаях может наступить повышение уровня билирубина, печеночная недостаточность и смерть - Перед началом лечения препаратом, содержащим ритуксимаб, проводят скрининг всех пациентов на инфекцию ВГВ путем измерения HBsAg и анти-HBc. Для пациентов, у которых есть признаки предыдущей инфекции гепатита В (HBsAg-положительный [независимо от статуса антител] или HBsAg-отрицательный, но анти-HBc-положительный), проконсультируйтесь с врачами, имеющими опыт лечения гепатита B, относительно мониторинга и рассмотрения противовирусной терапии HBV до и / или во время лечения препаратом, содержащим ритуксимаб. Мониторинг пациентов с признаками текущей или предшествующей инфекции ВГВ на наличие клинических и лабораторных признаков гепатита или реактивации ВГВ во время и в течение нескольких месяцев после приема препарата РИТУКСАН HYCELA. Сообщалось о реактивации ВГВ в течение 24 месяцев после завершения терапии, содержащей ритуксимаб 9.

- У пациентов, у которых развивается реактивация ВГВ во время приема РИТУКСАН HYCELA, немедленно прекратите лечение и любую сопутствующую химиотерапию и начните соответствующее лечение. Недостаточно данных относительно безопасности возобновления лечения RITUXAN HYCELA у пациентов, у которых развивается реактивация HBV. Возобновление лечения RITUXAN HYCELA у пациентов, у которых разрешается реактивация HBV, следует обсудить с врачами, имеющими опыт лечения HBV
Прогрессирующая многоочаговая лейкоэнцефалопатия (ПМЛ)
- Вирусная инфекция JC, приводящая к ПМЛ и смерти, наблюдалась у пациентов, получавших препараты, содержащие ритуксимаб, включая RITUXAN HYCELA
- Рассмотрите диагноз ПМЛ у любого пациента с впервые возникшими неврологическими проявлениями. Оценка ПМЛ включает, помимо прочего, консультацию невролога, МРТ головного мозга и люмбальную пункцию .
- Прекратить прием РИТУКСАН HYCELA и рассмотреть вопрос о прекращении или сокращении любой сопутствующей химиотерапии или иммуносупрессивной терапии у пациентов с развитием ПМЛ
Гиперчувствительность и другие реакции на введение
Системные реакции
- Пациенты должны получить по крайней мере одну полную дозу РИТУКСАНА перед введением РИТУКСАН HYCELA из-за более высокого риска гиперчувствительности и других острых реакций во время первой инфузии.
 Начало терапии РИТУКСАНОМ позволяет управлять гиперчувствительностью и другими реакциями на введение путем замедления или прекращения внутривенной инфузии
Начало терапии РИТУКСАНОМ позволяет управлять гиперчувствительностью и другими реакциями на введение путем замедления или прекращения внутривенной инфузии - Продукты, содержащие ритуксимаб, включая RITUXAN HYCELA, связаны с гиперчувствительностью и другими реакциями на введение, которые могут быть связаны с высвобождением цитокинов и/или других химических медиаторов. Синдром высвобождения цитокинов может быть клинически неотличим от острых реакций гиперчувствительности. Этот набор реакций, включающий синдром высвобождения цитокинов, синдром лизиса опухоли, анафилактические реакции и реакции гиперчувствительности, описан ниже. Они не связаны конкретно с путем введения препарата, содержащего ритуксимаб
- Сообщалось о тяжелых инфузионных реакциях с летальным исходом при использовании РИТУКСАН, с началом от 30 минут до 2 часов после начала первой внутривенной инфузии. Они характеризовались легочными явлениями в дополнение к лихорадке, ознобу, ознобу, гипотензии, крапивнице, ангионевротическому отеку и другим симптомам.
 Также могут возникать анафилактические и другие реакции гиперчувствительности. В отличие от синдрома высвобождения цитокинов истинные реакции гиперчувствительности обычно возникают в течение нескольких минут после начала инфузии
Также могут возникать анафилактические и другие реакции гиперчувствительности. В отличие от синдрома высвобождения цитокинов истинные реакции гиперчувствительности обычно возникают в течение нескольких минут после начала инфузии - Тяжелый синдром высвобождения цитокинов характеризуется сильной одышкой, часто связанной с бронхоспазмом и гипоксией, в дополнение к лихорадке, ознобу, ознобу, крапивнице и ангионевротическому отеку. Этот синдром может быть связан с острой дыхательной недостаточностью и летальным исходом. Синдром высвобождения цитокинов может развиться в течение 1-2 часов после начала инфузии. Пациенты с легочной недостаточностью в анамнезе или пациенты с легочной инфильтрацией опухоли могут подвергаться большему риску неблагоприятного исхода. Применение ритуксимаба следует немедленно прекратить и начать активное симптоматическое лечение
- Во время введения RITUXAN HYCELA инъекцию следует немедленно прервать при появлении признаков тяжелой реакции и начать агрессивное симптоматическое лечение.
 Внимательно следите за следующими пациентами: пациентами с ранее существовавшими сердечными или легочными заболеваниями, пациентами, перенесшими ранее сердечно-легочные побочные реакции, и пациентами с большим количеством циркулирующих злокачественных клеток (≥25 000/мкл 3 )
Внимательно следите за следующими пациентами: пациентами с ранее существовавшими сердечными или легочными заболеваниями, пациентами, перенесшими ранее сердечно-легочные побочные реакции, и пациентами с большим количеством циркулирующих злокачественных клеток (≥25 000/мкл 3 ) - Премедикация пациентов антигистаминными препаратами и ацетаминофеном перед каждым введением RITUXAN HYCELA. Также следует рассмотреть возможность премедикации глюкокортикоидами. Наблюдайте за пациентами в течение не менее 15 минут после введения RITUXAN HYCELA. Более длительный период может быть целесообразен у пациентов с повышенным риском реакций гиперчувствительности
Местные кожные реакции
- У пациентов, получавших RITUXAN HYCELA, сообщалось о местных кожных реакциях, включая реакции в месте инъекции. Симптомы включали боль, отек, уплотнение, кровоизлияние, эритему, зуд и сыпь. Некоторые местные кожные реакции возникали более чем через 24 часа после введения RITUXAN HYCELA.
 Частота местных кожных реакций после введения RITUXAN HYCELA составила 16%. Реакции были легкими или умеренными и разрешались без какого-либо специфического лечения. Местные кожные реакции любой степени тяжести были наиболее распространены во время первого цикла RITUXAN HYCELA (цикл 2: 5%), с уменьшением частоты при последующих инъекциях
Частота местных кожных реакций после введения RITUXAN HYCELA составила 16%. Реакции были легкими или умеренными и разрешались без какого-либо специфического лечения. Местные кожные реакции любой степени тяжести были наиболее распространены во время первого цикла RITUXAN HYCELA (цикл 2: 5%), с уменьшением частоты при последующих инъекциях
Синдром лизиса опухоли (СЛО)
- СЛО может возникнуть в течение 12–24 часов после введения препарата, содержащего ритуксимаб, включая РИТУКСАН HYCELA
- Большое количество циркулирующих злокачественных клеток (≥25 000/мм 3 ) или высокая опухолевая нагрузка повышают риск СЛО. Администрирование агрессивной внутривенной гидратации и антигиперурикемической терапии у пациентов с высоким риском СЛО. Коррекция нарушений электролитного баланса, мониторинг функции почек и водного баланса, назначение поддерживающей терапии, включая диализ, по показаниям
Инфекции
- Серьезные, в том числе фатальные, бактериальные, грибковые и новые или реактивированные вирусные инфекции могут возникать во время и после завершения терапии препаратами, содержащими ритуксимаб, включая RITUXAN HYCELA.
 Частота инфекций при применении RITUXAN HYCELA по сравнению с RITUXAN составила 56% и 49% соответственно у пациентов с ХЛЛ и 46% и 41% соответственно у пациентов с ФЛ/ДВККЛ в сочетании с химиотерапией. Сообщалось об инфекциях у некоторых пациентов с длительной гипогаммаглобулинемией (определяемой как гипогаммаглобулинемия >11 месяцев после применения ритуксимаба)
Частота инфекций при применении RITUXAN HYCELA по сравнению с RITUXAN составила 56% и 49% соответственно у пациентов с ХЛЛ и 46% и 41% соответственно у пациентов с ФЛ/ДВККЛ в сочетании с химиотерапией. Сообщалось об инфекциях у некоторых пациентов с длительной гипогаммаглобулинемией (определяемой как гипогаммаглобулинемия >11 месяцев после применения ритуксимаба) - Новые или реактивированные вирусные инфекции, включая цитомегаловирус, вирус простого герпеса, парвовирус B19, вирус ветряной оспы, вирус Западного Нила и гепатиты B и C. Прекратите прием препарата RITUXAN HYCELA при серьезных инфекциях и начните соответствующую противоинфекционную терапию
Побочные реакции со стороны сердечно-сосудистой системы
- Побочные реакции со стороны сердечно-сосудистой системы, включая фибрилляцию желудочков, инфаркт миокарда и кардиогенный шок, могут возникать при приеме препаратов, содержащих ритуксимаб, включая RITUXAN HYCELA
- Прекратите прием RITUXAN HYCELA при серьезных или угрожающих жизни сердечных аритмиях.
 Проводите кардиомониторинг во время и после всех введений RITUXAN HYCELA у пациентов, у которых развиваются клинически значимые аритмии или у которых в анамнезе аритмия или стенокардия
Проводите кардиомониторинг во время и после всех введений RITUXAN HYCELA у пациентов, у которых развиваются клинически значимые аритмии или у которых в анамнезе аритмия или стенокардия
Почечная токсичность
- После введения препаратов, содержащих ритуксимаб, включая RITUXAN HYCELA, может возникнуть тяжелая, в том числе смертельная, почечная токсичность. Почечная токсичность наблюдалась у пациентов с синдромом лизиса опухоли и у пациентов, получавших сопутствующую терапию цисплатином во время клинических исследований. Комбинация цисплатина и RITUXAN HYCELA не является утвержденной схемой лечения. Внимательно следите за признаками почечной недостаточности и прекратите прием РИТУКСАН HYCELA у пациентов с повышением уровня креатинина в сыворотке крови или олигурией
Непроходимость и перфорация кишечника
- Боли в животе, непроходимость кишечника и перфорация, в некоторых случаях приводящие к смерти, могут возникать у пациентов, получающих препараты, содержащие ритуксимаб, включая RITUXAN HYCELA, в сочетании с химиотерапией.
 В постмаркетинговых отчетах среднее время до документированной перфорации желудочно-кишечного тракта составляло 6 (диапазон 1–77) дней. Оцените наличие симптомов обструкции, таких как боль в животе или повторная рвота
В постмаркетинговых отчетах среднее время до документированной перфорации желудочно-кишечного тракта составляло 6 (диапазон 1–77) дней. Оцените наличие симптомов обструкции, таких как боль в животе или повторная рвота
Иммунизация
- Безопасность иммунизации живыми вирусными вакцинами после препаратов, содержащих ритуксимаб, включая RITUXAN HYCELA, не изучалась, и вакцинация живыми вирусными вакцинами не рекомендуется до или во время лечения
Эмбриофетальная токсичность
- На основании данных о людях, продукты, содержащие ритуксимаб, могут причинять вред плоду из-за В-клеточной лимфоцитопении у младенцев, подвергшихся воздействию ритуксимаба внутриутробно. Консультировать беременных женщин риска для плода. Женщины детородного возраста должны использовать эффективные методы контрацепции во время приема РИТУКСАН HYCELA и в течение 12 месяцев после последней дозы ритуксимаб-содержащих продуктов, включая РИТУКСАН HYCELA
- Подтвердить статус беременности у женщин с репродуктивным потенциалом до начала приема RITUXAN HYCELA
ПОБОЧНЫЕ РЕАКЦИИ
- Наиболее частыми побочными реакциями (≥20%) RITUXAN HYCELA, наблюдаемыми у пациентов с ФЛ в SABRINA, были: инфекции, нейтропения, тошнота, запор, кашель и утомляемость
- Наиболее частыми побочными реакциями (≥20%) RITUXAN HYCELA, наблюдаемыми у пациентов с ДВККЛ в MabEASE, были: инфекции, нейтропения, алопеция, тошнота и анемия
- Наиболее частыми побочными реакциями (≥20%) RITUXAN HYCELA, наблюдаемыми у пациентов с ХЛЛ в части 2 SAWYER, были: инфекции, нейтропения, тошнота, тромбоцитопения, лихорадка, рвота и эритема в месте инъекции
- За исключением местных кожных реакций, частота и профиль побочных реакций, о которых сообщалось для RITUXAN HYCELA, были сопоставимы с таковыми для RITUXAN.
 Общая частота побочных реакций на РИТУКСАН в сочетании с химиотерапией по сравнению с РИТУКСАНОМ HYCELA в сочетании с химиотерапией при ФЛ/ДВККЛ составила 9.3 % против 95 % (ППТ ≤ 1,73 м 2 ), 89 % против 93 % (1,73 < ППТ ≤ 1,92 м 2 ) и 94 % против 94 % (ППТ > 1,92 м 2 ) . Общая частота побочных реакций для РИТУКСАНа по сравнению с РИТУКСАНОМ HYCELA при ХЛЛ составила 89% против 100% (ППТ ≤ 1,81 м 2 ), 97% против 88% (1,82 < ППТ ≤ 1,99 м 2 ), и 88 % против 93 % (BSA > 2,00 м 2 )
Общая частота побочных реакций на РИТУКСАН в сочетании с химиотерапией по сравнению с РИТУКСАНОМ HYCELA в сочетании с химиотерапией при ФЛ/ДВККЛ составила 9.3 % против 95 % (ППТ ≤ 1,73 м 2 ), 89 % против 93 % (1,73 < ППТ ≤ 1,92 м 2 ) и 94 % против 94 % (ППТ > 1,92 м 2 ) . Общая частота побочных реакций для РИТУКСАНа по сравнению с РИТУКСАНОМ HYCELA при ХЛЛ составила 89% против 100% (ППТ ≤ 1,81 м 2 ), 97% против 88% (1,82 < ППТ ≤ 1,99 м 2 ), и 88 % против 93 % (BSA > 2,00 м 2 )
БЕРЕМЕННОСТЬ И ЛАКТАЦИЯ
- На основании данных о людях, продукты, содержащие ритуксимаб, могут вызывать неблагоприятные исходы развития, включая В-клеточную лимфоцитопению у младенцев, подвергшихся воздействию ритуксимаба внутриутробно. Нет доступных данных об использовании RITUXAN HYCELA беременными женщинами для информирования о риске серьезных врожденных дефектов и выкидыша, связанного с приемом препарата.

 Проведите скрининг всех пациентов на инфекцию ВГВ до начала лечения и наблюдайте за пациентами во время и после лечения препаратом РИТУКСАН ХИСЕЛА. Прекратить прием РИТУКСАН HYCELA и сопутствующих препаратов в случае реактивации ВГВ
Проведите скрининг всех пациентов на инфекцию ВГВ до начала лечения и наблюдайте за пациентами во время и после лечения препаратом РИТУКСАН ХИСЕЛА. Прекратить прием РИТУКСАН HYCELA и сопутствующих препаратов в случае реактивации ВГВ  Реактивация репликации HBV часто сопровождается гепатитом, то есть повышением уровня трансаминаз. В тяжелых случаях может наступить повышение уровня билирубина, печеночная недостаточность и смерть
Реактивация репликации HBV часто сопровождается гепатитом, то есть повышением уровня трансаминаз. В тяжелых случаях может наступить повышение уровня билирубина, печеночная недостаточность и смерть
 Начало терапии РИТУКСАНОМ позволяет управлять гиперчувствительностью и другими реакциями на введение путем замедления или прекращения внутривенной инфузии
Начало терапии РИТУКСАНОМ позволяет управлять гиперчувствительностью и другими реакциями на введение путем замедления или прекращения внутривенной инфузии Также могут возникать анафилактические и другие реакции гиперчувствительности. В отличие от синдрома высвобождения цитокинов истинные реакции гиперчувствительности обычно возникают в течение нескольких минут после начала инфузии
Также могут возникать анафилактические и другие реакции гиперчувствительности. В отличие от синдрома высвобождения цитокинов истинные реакции гиперчувствительности обычно возникают в течение нескольких минут после начала инфузии  Внимательно следите за следующими пациентами: пациентами с ранее существовавшими сердечными или легочными заболеваниями, пациентами, перенесшими ранее сердечно-легочные побочные реакции, и пациентами с большим количеством циркулирующих злокачественных клеток (≥25 000/мкл 3 )
Внимательно следите за следующими пациентами: пациентами с ранее существовавшими сердечными или легочными заболеваниями, пациентами, перенесшими ранее сердечно-легочные побочные реакции, и пациентами с большим количеством циркулирующих злокачественных клеток (≥25 000/мкл 3 ) Частота местных кожных реакций после введения RITUXAN HYCELA составила 16%. Реакции были легкими или умеренными и разрешались без какого-либо специфического лечения. Местные кожные реакции любой степени тяжести были наиболее распространены во время первого цикла RITUXAN HYCELA (цикл 2: 5%), с уменьшением частоты при последующих инъекциях
Частота местных кожных реакций после введения RITUXAN HYCELA составила 16%. Реакции были легкими или умеренными и разрешались без какого-либо специфического лечения. Местные кожные реакции любой степени тяжести были наиболее распространены во время первого цикла RITUXAN HYCELA (цикл 2: 5%), с уменьшением частоты при последующих инъекциях  Частота инфекций при применении RITUXAN HYCELA по сравнению с RITUXAN составила 56% и 49% соответственно у пациентов с ХЛЛ и 46% и 41% соответственно у пациентов с ФЛ/ДВККЛ в сочетании с химиотерапией. Сообщалось об инфекциях у некоторых пациентов с длительной гипогаммаглобулинемией (определяемой как гипогаммаглобулинемия >11 месяцев после применения ритуксимаба)
Частота инфекций при применении RITUXAN HYCELA по сравнению с RITUXAN составила 56% и 49% соответственно у пациентов с ХЛЛ и 46% и 41% соответственно у пациентов с ФЛ/ДВККЛ в сочетании с химиотерапией. Сообщалось об инфекциях у некоторых пациентов с длительной гипогаммаглобулинемией (определяемой как гипогаммаглобулинемия >11 месяцев после применения ритуксимаба) Проводите кардиомониторинг во время и после всех введений RITUXAN HYCELA у пациентов, у которых развиваются клинически значимые аритмии или у которых в анамнезе аритмия или стенокардия
Проводите кардиомониторинг во время и после всех введений RITUXAN HYCELA у пациентов, у которых развиваются клинически значимые аритмии или у которых в анамнезе аритмия или стенокардия 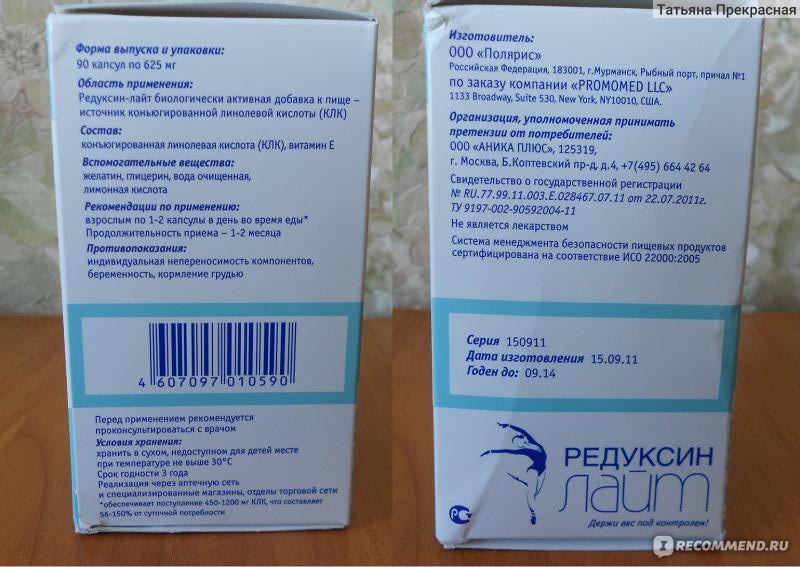 В постмаркетинговых отчетах среднее время до документированной перфорации желудочно-кишечного тракта составляло 6 (диапазон 1–77) дней. Оцените наличие симптомов обструкции, таких как боль в животе или повторная рвота
В постмаркетинговых отчетах среднее время до документированной перфорации желудочно-кишечного тракта составляло 6 (диапазон 1–77) дней. Оцените наличие симптомов обструкции, таких как боль в животе или повторная рвота  Общая частота побочных реакций на РИТУКСАН в сочетании с химиотерапией по сравнению с РИТУКСАНОМ HYCELA в сочетании с химиотерапией при ФЛ/ДВККЛ составила 9.3 % против 95 % (ППТ ≤ 1,73 м 2 ), 89 % против 93 % (1,73 < ППТ ≤ 1,92 м 2 ) и 94 % против 94 % (ППТ > 1,92 м 2 ) . Общая частота побочных реакций для РИТУКСАНа по сравнению с РИТУКСАНОМ HYCELA при ХЛЛ составила 89% против 100% (ППТ ≤ 1,81 м 2 ), 97% против 88% (1,82 < ППТ ≤ 1,99 м 2 ), и 88 % против 93 % (BSA > 2,00 м 2 )
Общая частота побочных реакций на РИТУКСАН в сочетании с химиотерапией по сравнению с РИТУКСАНОМ HYCELA в сочетании с химиотерапией при ФЛ/ДВККЛ составила 9.3 % против 95 % (ППТ ≤ 1,73 м 2 ), 89 % против 93 % (1,73 < ППТ ≤ 1,92 м 2 ) и 94 % против 94 % (ППТ > 1,92 м 2 ) . Общая частота побочных реакций для РИТУКСАНа по сравнению с РИТУКСАНОМ HYCELA при ХЛЛ составила 89% против 100% (ППТ ≤ 1,81 м 2 ), 97% против 88% (1,82 < ППТ ≤ 1,99 м 2 ), и 88 % против 93 % (BSA > 2,00 м 2 )