Стероидные и нестероидные противовоспалительные лекарственные средства : Farmf
Стероидные и нестероидные противовоспалительные лекарственные средства
1. Основные эффекты нестероидных противовоспалительных лекарственных средств:
— иммунодепрессивный;
+ противовоспалительный;
— пермиссивный;
+ жаропонижающий;
+ анальгетический.
2. Антиагрегантной активностью обладает:
— нимесулид;
— целекоксиб;
+ ацетилсалициловая кислота в низких дозировках;
— ацетилсалициловая кислота в высоких дозировках;
— кеторолак.
3. Наименее выраженным ульцерогенным эффектом обладают:
— селективные ингибиторы ЦОГ-1;
— индометацин;
+ селективные ингибиторы ЦОГ-2;
— пироксикам;
— диклофенак;
4. Для профилактики ульцерогенного действия НПВС рекомендуется назначать с:
— антацидами;
— сукральфатом;
— М-холинолитиками;
+ блокаторами протоновой помпы;
+ мизопростолом.
5. В отличие от нестероидных противовоспалительных лекарственных средств, глюкокортикоиды не обладают эффектом:
— иммунодепрессивным;
— противовоспалительным;
— противоаллергическим;
+ жаропонижающим;
+ анальгетическим.
6. Пермиссивный эффект глюкокортикоидов заключается в:
+ повышением чувствительности клеток к адреналину;
+ увеличением количества адренорецепторов;
— повышением чувствительности клеток к ацетилхолину;
— увеличением количества холинорецепторов;
— уменьшением количества холинорецепторов;
7. Показания к применению глюкокортикостероидов:
+ бронхиальная астма;
+ ревматоидный артрит;
— инсулиннезависимый сахарный диабет;
+ шок;
— стероидные язвы;
8. Влияние глюкокортикостероидов на углеводный обмен:
+ стимуляция глюконеогенеза в печени;
— увеличение проницаемости мембран для глюкозы;
— угнетение глюконеогенеза в печени;
+ уменьшение проницаемости мембран для глюкозы;
— уменьшение содержания глюкозы в крови.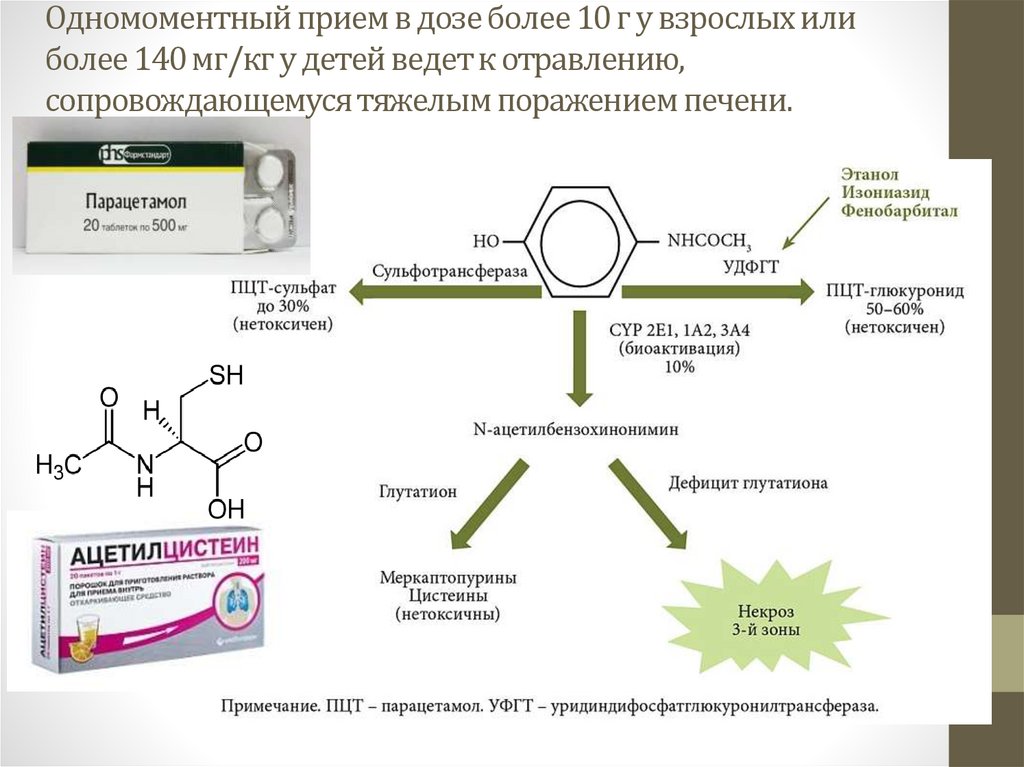
9. Влияние глюкокортикостероидов на водно-электролитный и минеральный обмен:
+ увеличение реабсорбции натрия;
+ усиление экскреции кальция;
+ усиление экскреции калия;
— задержка калия;
— увеличение выведения воды.
10. Нежелательные лекарственные реакции, развивающиеся при системной глюкокортикоидной терапии:
— кальцификация тканей;
+ гипертензия;
+ язвы желудка;
— стимуляция гипоталамо-гипофизарно-надпочечниковой системы;
+ активация инфекций.
11. Лекарственные средства для базисной терапии ревматоидного артрита:
+ соединения золота;
— рисперидон;
+ D-пеницилламин;
+ производные 5-аминосалициловой кислоты;
+ аминохинолиновые препараты.
12. Базисные препараты, в отличие от НПВС и глюкокортикоидов:
— действуют быстро;
+ замедляют суставную деструкцию;
— оказывают симптоматическое действие;
+ сохраняют действие несколько месяцев после отмены;
— обладают меньшим количеством побочных эффектов.
13. Группы препаратов, применяемые для фармакотерапии диффузных заболеваний соединительной ткани:
+ моноклональные антитела к цитокинам;
+ цитостатики;
+ глюкокортикостероиды;
— ингибиторы нейронального захвата серотонина;
+ аминохинолиновые препараты.
14. Препараты, используемые при лечении ревматоидного артрита:
+ преднизолон;
+ лефлунамид;
+ инфликсимаб;
+ метотрексат;
— триазолам.
15. Цитостатики, используемые в качестве иммуносупрессивных препаратов:
— моклобемид;
+ циклоспорин;
+ циклофосфамид;
+ метотрексат;
+ азатиоприн.
16. Отметить основные показания к применению ненаркотических анальгетиков:
+ Невралгии
+ Боли а мышцах и суставах воспалительного характера
+ Ревматические болезни
— Боли при злокачественных опухолях
+ Снижение повышенной температуры
17. С чем связывают болеутоляющий эффект анальгетиков (салицилаты и производные пиразолона)?
+ Угнетают синтез простагландинов в периферических тканях, в связи с этим понижают чувствительность ноцицепторов
— Нарушают меж нейронную передачу болевых импульсов на разных уровнях ЦНС
— Изменяют эмоциональную оценку болевого ощущения
+ Устраняют механические факторы (уменьшение отека, инфильтрации ткани), что снижает давление на рецепторные окончания
18. Жаропонижающее действие нестероидных противовоспалительных средств проявляется:
Жаропонижающее действие нестероидных противовоспалительных средств проявляется:
— При пониженной температуре тела
— При нормальной температуре тела
+ При повышенной температуре тела
19. В основе действия НПВС лежит:
— Угнетение фосфолипазы А2
— Угнетение синтеза арахидоновой кислоты
— Угнетение липооксигеназы
+ Угнетение циклооксигеназы
20. Назовите селективный ингибитор циклооксигеназы 2:
— Аспирин
+ Мелоксикам
— Ибупрофен
— Диклофенак — натрий
21. Укажите не наркотические анальгетики:
— Морфина гидрохлорид
+ Анальгин
— Промедол
+ Кеторолак
— Лоперамид
22. Указать механизм жаропонижающего действия анальгетиков
— Снижают тепло продукцию
+ Усиливают теплоотдачу за счет расширения сосудов кожи и стимуляции потоотделения
+ Обладают антисеротониновым действием
23. Отметить основные механизмы противовоспалительного эффекта анальгетиков
+ Тормозят синтез простагландинов, снижая повреждение ткани и экссудацию
+ Тормозят образование антител
+ Снижают образование и высвобождение медиаторов воспаления
+ За счет антиагрегантного действия улучшают кровоток в очаге воспаления
+ Тормозят синтез кислых мукополисахаридов и тем самым угнетают фазу пролиферации
— Подавляют митотическую активность и созревание фибробластов
24. Отметить побочные эффекты, характерные для салицилатов
Отметить побочные эффекты, характерные для салицилатов
+ Нарушение слуха
+ Аллергические реакции
+ Изъязвление слизистой ЖКТ
+ Желудочные и кишечные кровотечения
— Угнетение дыхания
— Развитие лекарственной зависимости
— Лейкопения
25. Отметить побочные эффекты, характерные для производных пиразолона
+ Аллергические реакции
— Нарушение слуха
+ Лейкопения
+ Изъязвление слизистой ЖКТ
— Угнетение дыхания
— Развитие лекарственной зависимости
26. Назовите ЛС из нестероидных противовоспалительных средств, являющееся специфическим блокатором ЦОГ2:
— мелоксикам
+ целекоксиб
— кеторолак
— диклофенак
— нимесулид
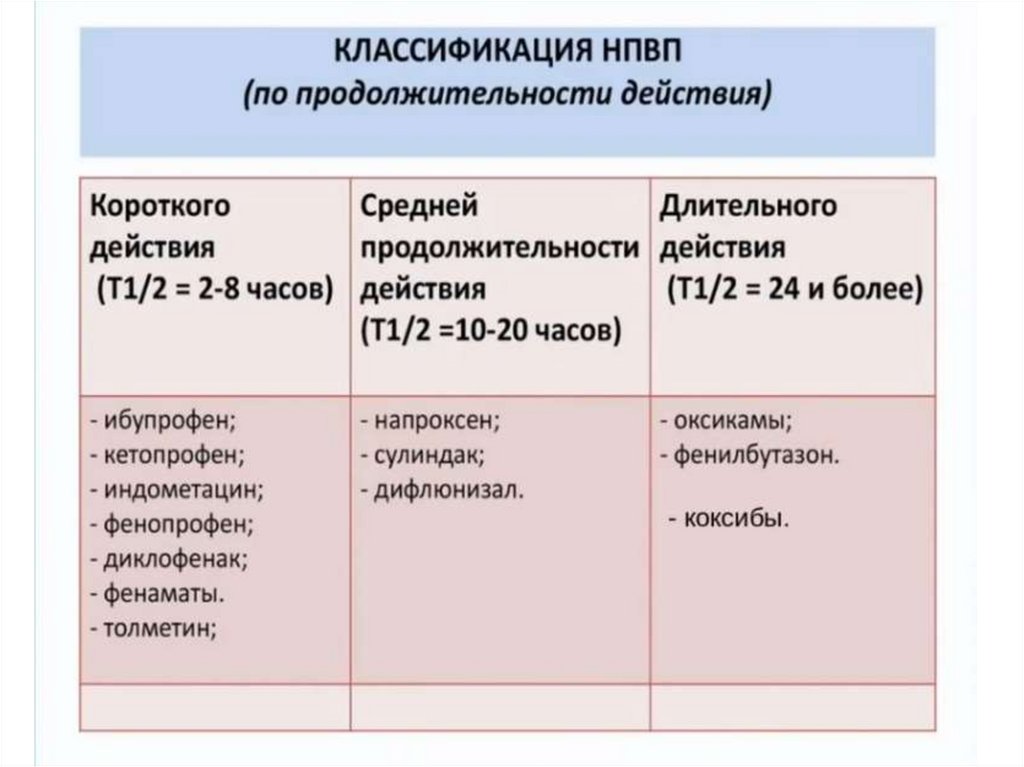
27. Назовите противовоспалительное средство пролонгированного действия:
— аспирин
— анальгин
— ортофен
— индометацин
+ нимесулид
+ пироксикам
28. Наиболее рационально для вторичной профилактики НПВС-гастропатии использовать:
— мизопростол
+ омепразол
— ранитидин
— алмагель
— гевискон
29. У детей в качестве жаропонижающего средства препаратом выбора является:
У детей в качестве жаропонижающего средства препаратом выбора является:
— индометацин
— аспирин
+ парацетамол
— анальгин
— диклофенак
30. Такие побочные эффекты как ульцерогенный, развитие геморрагического синдрома, нарушение почечного кровотока обусловлены:
— ингибирование ЦОГ2
+ ингибирование ЦОГ1
— ингибирование ЦОГ3
— ингибирование ЦОГ1 и ЦОГ2
Механизм развития ульцерогенного эффекта нестероидных противовоспалительных средств является:
— повышение кислотности желудочного сока
— снижение образования слизи
+ снижение синтеза простагландинов в слизистой оболочке желудка
— снижение репарации слизистой оболочки
— увеличение образования гастрина
Основным механизмом действия нестероидных противовоспалительных средств является:
+ антипростагландиновый
— антилейкотриеновый
— антибактериальный
— антигистаминный
— стабилизация мембран тучных клеток
Основным побочным эффектом нестероидных противовоспалительных средств является:
+ гастротоксический
— гепатотоксический
— нефротоксический
— кардиотоксический
— ототоксический
У детей в случае отсутствия эффекта от парацетамола, в качестве жаропонижающего средства рационально использовать:
— индометацин
— аспирин
+ ибупрофен
— анальгин
— диклофенак
Назовите селективный ингибитор циклооксигеназы 2:
— Аспирин
+ Мелоксикам
— Ибупрофен
После приема нестероидных противовоспалительных средств быстрее развивается эффект:
— противовоспалительный
+ анальгетический
— антикоагуляционный
Механизмом развития ульцерогенного эффекта неспецифических противовоспалительных средств является:
— повышение кислотности желудочного сока;
— снижение образования слизи;
+ снижение синтеза простагландинов в слизистой оболочке желудка;
— снижением репарации слизистой оболочки;
— увеличение образования гастрина.
Наиболее выраженным противовоспалительным свойством обладает:
+ фенилбутазон
— метамизол
— пироксикам
— парацетамол
— ибупрофен
Наиболее выраженными противовоспалительными свойствами обладает:
— бутадион;
— анальгин;
— пироксикам;
— кетопрофен;
+ вольтарен.
Нестероидные противовоспалительные средства
Существуют ли различия между нестероидными противовоспалительными препаратами? В центре внимания нимесулид | #10/16
Распространенность заболеваний, сопровождающихся острой болью и требующих применения обезболивающих препаратов, в современном мире постоянно растет. К ним относятся, в частности, ревматические болезни, воспалительные и дегенеративные заболевания опорно-двигательного аппарата, головная боль. Примерно 40% визитов к врачу общей практики обусловлены слабой и умеренной острой болью, а более 70% посещений отделений неотложной помощи происходит из-за наличия у пациента интенсивной острой боли [1]. В структуре общей заболеваемости населения Российской Федерации болезни костно-мышечной системы и соединительной ткани (БКМС) занимают 3-е место после болезней системы кровообращения и органов дыхания [2]. Агентство National Health Interview Survey демонстрирует следующие данные: в 2011 г. 28,4% взрослых американцев сообщали о боли в нижней части спины (БНС) в течение предыдущих опросу 3 месяцев [3].
В структуре общей заболеваемости населения Российской Федерации болезни костно-мышечной системы и соединительной ткани (БКМС) занимают 3-е место после болезней системы кровообращения и органов дыхания [2]. Агентство National Health Interview Survey демонстрирует следующие данные: в 2011 г. 28,4% взрослых американцев сообщали о боли в нижней части спины (БНС) в течение предыдущих опросу 3 месяцев [3].
Эффективность нестероидных противовоспалительных препаратов (НПВП) при острой боли не подвергается сомнению. НПВП обладают противовоспалительной, обезболивающей и жаропонижающей активностью. Входящие в состав НПВП вещества относятся к различным химическим классам, поэтому обладают разными фармакокинетическими и фармакодинамическими свойствами.
Обзор клинической эффективности НПВП показывает, что различные препараты данной группы обладают примерно схожей терапевтической активностью. В данной работе будут представлены различия НПВП и особое внимание будет уделено представителю НПВП нимесулиду.
Фармакологические свойства НПВП
Ингибирование синтеза простагландинов
В начале 70-х годов Vane высказал предположение, что в основе противовоспалительного действия Аспирина и аналогичных ему препаратов лежит способность ингибировать биосинтез простагладинов, путем ингибирования ответственного за их синтез фермента циклооксигеназы (ЦОГ). Лишь 20 лет спустя эта гипотеза получила свое подтверждение, и стало известно, что за синтез простагландинов отвечают две изоформы ЦОГ (ЦОГ-1 и ЦОГ-2), а НПВП можно разделять с учетом селективности в отношении разных изоформ ЦОГ.
ЦОГ-1 отвечает в основном за синтез простагландинов, участвующих в процессах гомеостаза в жизненно важных органах. Именно с ингибированием ЦОГ-1 связывают хорошо известные желудочно-кишечные побочные эффекты традиционных неселективных НПВП.
Ингибирование ЦОГ-2 обеспечивает противовоспалительный эффект НПВП, так как она участвует в синтезе воспалительных простагландинов.
Неселективные НПВП ингибируют обратимо или необратимо как ЦОГ-1, так и ЦОГ-2. Большинство токсических эффектов этих препаратов связано с их способностью блокировать синтез физиологических простагландинов, необходимых для обеспечения гомеостаза в почках, желудке и тромбоцитах за счет ингибирования ЦОГ-1.
Появление на рынке в конце 90-х годов селективных ингибиторов ЦОГ-2 (коксибов) давало клиницистам надежду на то, что эта группа НПВП обеспечит высокую фармакологическую эффективность при более низком уровне желудочно-кишечных осложнений. Однако ожидания были оправданы не в полной мере, в частности, получены доказательства того, что применение коксибов сопровождается увеличением частоты тромбоэмболических осложнений, что привело к выводу с рынка во всем мире таких препаратов, как рпсиофекоксиб и валдекоксиб. Кроме того, применение валдекоксиба связывают с частым развитием нежелательных кожных реакций. Кардиотоксичность коксибов объясняют блокированием синтеза простациклинов, опосредованного ЦОГ-2, что нивелирует их защитные эффекты в отношении тромбогенеза, гипертензии и атерогенеза in vivo.
НПВП классифицируют по степени селективности в отношении изоформ ЦОГ (рис. 1). Селективность в отношении ЦОГ определяется химической структурой НПВП. Аминокислотная структура ЦОГ-1 и ЦОГ-2 является достаточно стабильной, однако рентгеновские кристаллографические исследования ЦОГ показали, что активная область связывания с НПВП у ЦОГ-2 позволяет связываться с большим количеством субстратов, чем центр связывания у ЦОГ-1. Этот активный канал является гидрофобным, у ЦОГ-2 возможно открытие бокового гидрофильного кармана, который у ЦОГ-1 закрыт изолейцином.
Так, флурбипрофен, который относят к неселективным НПВП, взаимодействует с ЦОГ-1 посредством связывания фенильной группы с гидрофобным каналом и карбоксильной группы с аргинином в 120-м положении. Взаимодействие флурбипрофена с ЦОГ-2 сходно с вышеописанным, однако, связываясь с аргинином в 120-м положении, карбоксильная группа блокирует активный центр ЦОГ-2, не позволяя ему взаимодействовать с субстратом. Напротив, селективные ингибиторы ЦОГ-2 не могут войти в активный канал ЦОГ-1 и не имеют карбоксильной группы для связывания с аргинином в 120-м положении.
Нимесулид — единственный представитель класса сульфонанилидов, преимущественно ингибирующим ЦОГ-2. Активность нимесулида в отношении ЦОГ-2 в 5–50 раз превосходит активность в отношении ЦОГ-1. В исследованиях in vivo использование нимесулида в терапевтической дозе (100 мг 2 раза в сутки) продемонстрировало значительное снижение концентрации простагландина E2 в плазме крови. Нимесулид не оказывает влияния на агрегацию тромбоцитов, что было доказано при оценке индуцированной активности ЦОГ-1, и не влияет на образование в желудке простагландина E2 и простагландина I2, а также ЦОГ-1 зависимых эффектов.
Фармакокинетический профиль
На основании периода полувыведения НПВП могут быть разделены на две большие группы: с коротким периодом полувыведения (менее 6 часов) и с длительным периодом полувыведения (более 10 часов). Группа НПВП с коротким периодом полувыведения включает Аспирин, диклофенак, ибупрофен, флурбипрофен, индометацин, лумиракоксиб* и нимесулид. Группа препаратов с длительным периодом полувыведения включает целекоксиб, напроксен, сулиндак, рофекоксиб, оксапрозин*, пироксикам. Достижение равновесной концентрации препарата в плазме крови происходит после его применения в течение периода, превосходящего период полувыведения в 3–5 раз, поэтому достижение пиковой концентрации в плазме крови и максимального клинического эффекта НПВП с коротким периодом полувыведения происходит быстрее, чем препаратов с длительным периодом полувыведения.
Группа препаратов с длительным периодом полувыведения включает целекоксиб, напроксен, сулиндак, рофекоксиб, оксапрозин*, пироксикам. Достижение равновесной концентрации препарата в плазме крови происходит после его применения в течение периода, превосходящего период полувыведения в 3–5 раз, поэтому достижение пиковой концентрации в плазме крови и максимального клинического эффекта НПВП с коротким периодом полувыведения происходит быстрее, чем препаратов с длительным периодом полувыведения.
Нимесулид: фармакологический профиль
Нимесулид оказывает быстрое обезболивающее действие, что подтверждают следующие исследования. Применение нимесулида у пациентов с острым артритом характеризуется быстрым началом действия и ранним ингибированием образования простагландина E2 (маркера активности ЦОГ-2). В клинических исследованиях у пациентов с остеоартритом коленных суставов были получены доказательства быстрого начала действия нимесулида. У данной категории больных нимесулид вызывал достоверно более значимое облегчение боли, связанной с ходьбой, и эффект наступал быстрее, чем при применении целекоксиба и рофекоксиба. Начало обезболивающего действия нимесулида фиксировалось уже через 15 минут после приема. Согласно недавним исследованиям, эффективные концентрации нимесулида в плазме крови и синовиальной жидкости обнаруживаются уже через 30 минут после его приема.
Начало обезболивающего действия нимесулида фиксировалось уже через 15 минут после приема. Согласно недавним исследованиям, эффективные концентрации нимесулида в плазме крови и синовиальной жидкости обнаруживаются уже через 30 минут после его приема.
НПВП могут обладать противовоспалительными свойствами, которые не зависят от ЦОГ. Было показано, что нимесулид, помимо периферического ингибирующего воздействия на ЦОГ, может ингибировать высвобождение фактора некроза опухолей (ФНО), гистамина, образования активных форм кислорода (АФК), высвобождения матриксных металлопротеаз (ММП) и гибели хондроцитов (рис. 2).
Влияние нимесулида на медиаторы воспаления
ФНО-α играет ведущую роль в воспалительном процессе, что делает его идеальной целью при терапии ревматоидного артрита. В исследованиях на крысах, которым вводили липополисахариды для увеличения уровня ФНО-α, нимесулид эффективно ингибировал его высвобождение.
Выработка фагоцитами супероксида и высвобождение лактоферрина из нейтрофилов были исследованы у восьми добровольцев до и после приема нимесулида внутрь.
В ходе воспалительной реакции для предупреждения повреждения тканей требуется поддержание баланса между протеиназами (преимущественно эластазами, выделяемыми мигрировавшими в очаг нейтрофилами) и антипротеазами (в основном эластаз-специфическим альфа-1-ингибитором протеиназ; A1PI). Нейтрофильные клетки способны инактивировать A1PI с помощью серии окислительных реакций с участием хлорноватистой кислоты, что позволяет эластазе свободно разрушать соединительную ткань.
В другом исследовании морским свинкам предварительно вводили нимесулид или индометацин, после чего ацетальдегидом провоцировали выброс гистамина и бронхоспазм (рис. 4). В контрольной группе, получавшей только ацетальдегид, концентрация гистамина в крови была равна 195 ± 12 мг/л, в группе, получавшей нимесулид, при использовании дозы 0,1 мг/кг она была равна 154 ± 10 мг/л (p < 0,05 по сравнению с контрольной группой), дозы 0,3 мг/кг — 116 ± 13 мг/л (p < 0,01 по сравнению с контрольной группой), 63 ± 8 мг/л при использовании дозы 1 мг/кг (p < 0,01 по сравнению с контрольной группой) и 222 ± 16 мг/л у животных, получавших индометацин в дозе 1 мг/кг.
Данное исследование демонстрирует наличие дозозависимого блокирования нимесулидом высвобождения гистамина и развития бронхоспазма, что может иметь терапевтическое значение для пациентов с воспалительным процессом в дыхательных путях и аллергическим бронхоспазмом в анамнезе.
Влияние нимесулида на костную и хрящевую ткань
При остеоартрите ММП-1, ММП-8 и ММП-13 играют ведущую роль в разрушении коллагена второго типа, фрагменты которого в дальнейшем разрушаются ММП-3.
У пациентов с остеоартритом нимесулид вызывает снижение сывороточной концентрации ММП, что было показано в открытом пилотном исследовании, в которое вошли 20 пациентов с остеоартритом коленных или тазобедренных суставов с выраженными болями. Все больные получали нимесулид в дозе 100 мг 2 раза в сутки в течение 3 недель, при этом 22 здоровых добровольца (контрольная группа) лечения не получали. В сравнении с контрольной группой, терапия нимесулидом у пациентов с остеоартритом приводила к уменьшению боли и уменьшению средних сывороточных концентраций ММП-3 (от исходных 21,1 нг/мл до 14,7 нг/мл; p < 0,01) и ММП-8 (от 14,5 нг/мл до 10,0 нг/мл; p < 0,05). Таким образом, был сделан вывод, что нимесулид может блокировать разрушение межклеточного вещества за счет снижения концентраций ММП-8 и ММП-3.
Гиалуронан является маркером воспаления синовиальных оболочек, а С-телопептид коллагена II типа (CTX-II) является маркером разрушения коллагена хряща, высокие концентрации этих веществ являются неблагоприятными прогностическими факторами при остеоартрите. Было показано, что у пациентов с обострением остеоартрита нимесулид в большей степени, чем ибупрофен, снижал уровень CTX-II в моче и уровни гиалуронана, ММП-3 и ММП-13. В рандомизированном проспективном простом слепом исследовании 90 пациентов получали нимесулид в дозе 100 мг 2 раза в сутки (n = 45) или ибупрофен замедленного высвобождения по 800 мг 2 раза в сутки (n = 45) в течение 4 недель. К моменту окончания лечения в группе нимесулида было отмечено значимое снижение средней сывороточной концентрации гиалуронана (с 59 до 42 нг/мл; p < 0,05), в группе ибупрофена снижение было незначимым (с 62 до 52 нг/мл). Аналогично, средний уровень CTX-II в моче был значимо снижен в группе нимесулида (с 0,42 до 0,31 мг/моль креатинина; p < 0,001), но не в группе ибупрофена (с 0,42 до 0,38 мг/моль креатинина). Также нимесулид вызывал значимое снижение сывороточных концентраций ММП-3 (с 37 до 27 нг/мл; p < 0,05) и ММП-13 (с 92 до 58 пг/мл; p < 0,001), в то время как в группе ибупрофена значимого влияния на эти показатели не отмечалось. Кроме того, наблюдалась выраженная корреляция между отмеченным в группе нимесулида снижением концентраций CTX-II со снижением концентраций гиалуронана и ММП-13.
Также нимесулид вызывал значимое снижение сывороточных концентраций ММП-3 (с 37 до 27 нг/мл; p < 0,05) и ММП-13 (с 92 до 58 пг/мл; p < 0,001), в то время как в группе ибупрофена значимого влияния на эти показатели не отмечалось. Кроме того, наблюдалась выраженная корреляция между отмеченным в группе нимесулида снижением концентраций CTX-II со снижением концентраций гиалуронана и ММП-13.
Нимесулид может оказывать защитное действие при остеоартрозе посредством ЦОГ-независимых механизмов, например, ингибирования апоптоза хондроцитов (клеток, ответственных за восстановление хряща). Для оценки влияния различных НПВП на хондроциты клеточная линия хондроцитов была подвергнута воздействию стауроспорина для индуцирования апоптоза. Культуры были предварительно обработаны нимесулидом, ибупрофеном или селективным ингибитором ЦОГ-2 NS 398. Через 4 часа индуцированный стауроспорином апоптоз был значимо менее выражен в хондроцитах, предварительно обработанных нимесулидом (рис. 5) или ибупрофеном, эффект носил дозозависимый характер (10–12–10–6 моль/л).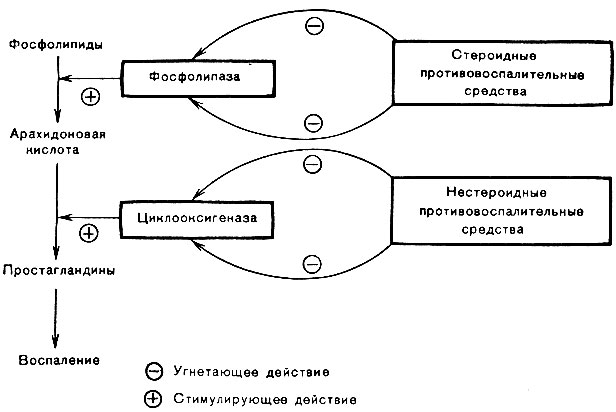 Однако NS 398 не оказывал такого защитного действия. Гибель клеток, по-видимому, связана с изменением экспрессии гена BCL-2 и активацией каспазы-3.
Однако NS 398 не оказывал такого защитного действия. Гибель клеток, по-видимому, связана с изменением экспрессии гена BCL-2 и активацией каспазы-3.
Таким образом, многочисленные механизмы действия нимесулида, не связанные с ингибированием фермента ЦОГ-2, могут оказывать благоприятное влияние на прогрессирование болезни у пациентов с ревматологическими заболеваниями.
Заключение
Нимесулид относится к числу препаратов, оказывающих ингибирующее действие преимущественно на ЦОГ-2, но при этом он обладает и другими механизмами действия. Нимесулид влияет на активность матриксных металлопротеаз, уменьшает высвобождение АФК и других токсических веществ нейтрофилами и снижает образование провоспалительных цитокинов.
В Вене 4 ноября 2014 г. проходила международная консенсусная встреча. Целью встречи было обсуждение вопросов патофизиологии и лечения острой боли с особым акцентом на применение нимесулида. В частности, обсуждались механизмы возникновения острой боли и эффективность и безопасность нимесулида у пациентов, страдающих различными формами такой боли. Обсуждались результаты новых эпидемиологических данных и обширного клинического опыта, подтверждающие положительный профиль польза/риск нимесулида в лечении некоторых форм острой боли. Члены этой встречи признали, что нимесулид является высокоэффективным НПВП (вследствие быстрого наступления обезболивающего эффекта) при лечении многих болезней, сопровождающихся острым воспалением, включая БНЧ, головную боль и первичную дисменорею [8].
Обсуждались результаты новых эпидемиологических данных и обширного клинического опыта, подтверждающие положительный профиль польза/риск нимесулида в лечении некоторых форм острой боли. Члены этой встречи признали, что нимесулид является высокоэффективным НПВП (вследствие быстрого наступления обезболивающего эффекта) при лечении многих болезней, сопровождающихся острым воспалением, включая БНЧ, головную боль и первичную дисменорею [8].
Литература
- Coda B. A., Bonica J. J. General considerations of acute pain. In: Loeser J. D., Butler S. H., Chapman C. R., Turk D. C. eds. Bonica’s Management of Pain. 3 rd ed. Hagerstown, MD: Lippincott Williams & Wilkins; 2001: 222–240.
- Болезни нервной системы. Руководство для врачей / Под ред. Н. Н. Яхно, Д. Р. Штульмана. М., 2001. Т. 1.
- Health, United States, 2012: with special feature on emergency care. Hyattsville, MD: National Center for Health Statistics; 2013.
- Warner T.
 D., Giuliano F., Vojnovic I. et al. Nonsteroid drug selectivities for cyclo-oxygenase-1 rather than cyclooxygenase-2 are associated with human gastrointestinal toxicity: a full in vitro analysis // Proc. Natl. Acad. Sci. USA 1999; 96: 7563–7568.
D., Giuliano F., Vojnovic I. et al. Nonsteroid drug selectivities for cyclo-oxygenase-1 rather than cyclooxygenase-2 are associated with human gastrointestinal toxicity: a full in vitro analysis // Proc. Natl. Acad. Sci. USA 1999; 96: 7563–7568. - Ottonello L., Dapino P., Pastorino G. et al. Inhibition of the neutrophil oxidative response induced by the oral administration of nimesulide in normal volunteers // J. Clin. Lab. Immunol. 1992; 37: 91–96.
- Rossoni G., Berti F., Buschi A. et al. New data concerning the antianaphylactic and antihistaminic activity of nimesulide // Drugs. 1993; 46 (Suppl. 1): 22–28.
- Mukherjee P., Rachita C., Aisen P. S. et al. Non-steroidal antiinflammatory drugs protect against chondrocyte apoptotic death // Clin. Exp. Rheumatol. 2001; 19 (1 Suppl. 22): S7–11.
- Kress H. G., Baltov A., Basinski A. et al. Acute pain: a multifaceted challenge — the role of nimesulide // Curr Med Res Opin.
 2016 Jan; 32 (1): 23–36.
2016 Jan; 32 (1): 23–36.
О. В. Котова, кандидат медицинских наук
ГБОУ ВПО Первый МГМУ им. И. М. Сеченова МЗ РФ, Москва
Контактная информация: [email protected]
* Препарат в РФ не зарегистрирован.
Чем отличаются нестероидные противовоспалительные препараты от стероидов
- Дом
- Подготовка org/ListItem»> Травмы
- В чем разница между нестероидными противовоспалительными препаратами и стероидами?
Нестероидные противовоспалительные препараты (НПВП) — это группа препаратов, которые обычно используются для уменьшения боли и отека. Наиболее узнаваемыми из них являются ибупрофен, напроксен и диклофенак.
Ибупрофен и напроксен — это повседневные болеутоляющие средства, которые можно купить без рецепта в любой аптеке. Они могут ослабить и помочь облегчить симптомы, возникающие во время кратковременных приступов боли, таких как мышечные напряжения, растяжения связок, боли в спине или головные боли или общий дискомфорт после травмы.
Растяжение и растяжение связок: в чем разница?
Как отличить травму мягких тканей от стрессового перелома?
В чем разница между мышцами, сухожилиями и связками?
Сразу после травмы высвобождаются простагландины как часть защитного механизма организма.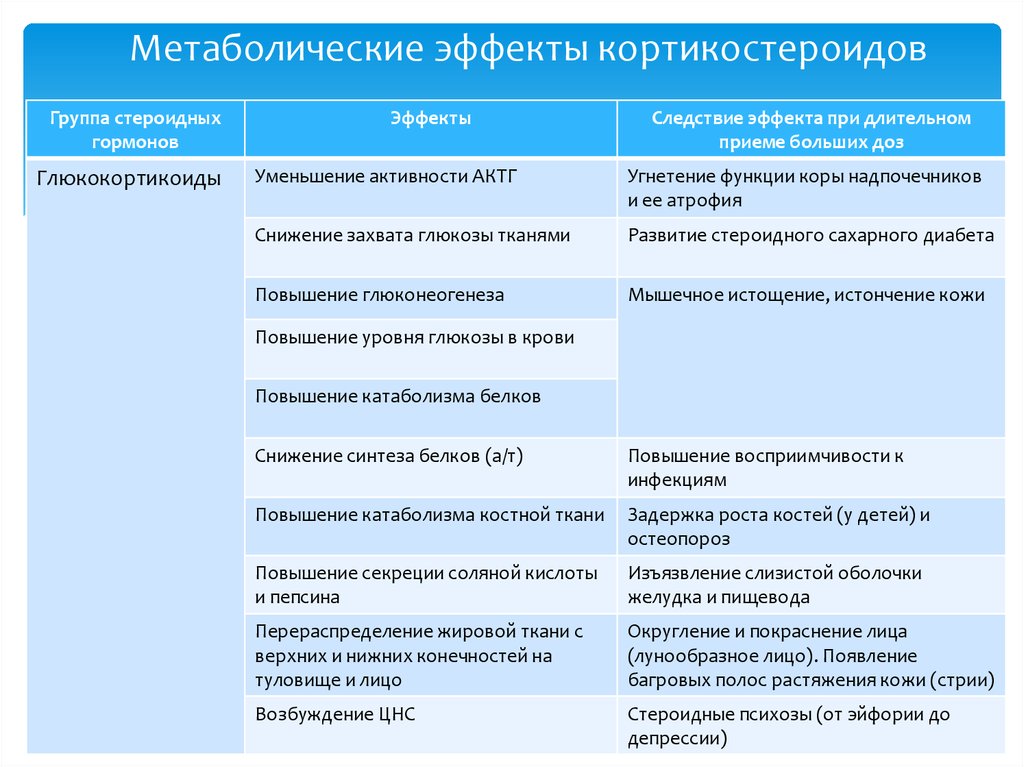 Они вызывают отек поврежденных участков тела, а также усиливают болевые сигналы. Это жизненно важная часть процесса заживления, но слишком сильный отек вызывает боль и угнетение мышц. НПВС работают, подавляя высвобождение этих простагландинов, тем самым уменьшая отек и боль.
Они вызывают отек поврежденных участков тела, а также усиливают болевые сигналы. Это жизненно важная часть процесса заживления, но слишком сильный отек вызывает боль и угнетение мышц. НПВС работают, подавляя высвобождение этих простагландинов, тем самым уменьшая отек и боль.
Хотя все три препарата имеют схожий эффект, лучше не смешивать их, так как это может привести к повышенному риску побочных эффектов. Длительное использование НПВП может вызвать дискомфорт в животе, запор и тошноту. Ибупрофен нельзя принимать на голодный желудок.
Стероиды, с другой стороны, являются гораздо более сильными препаратами, они более эффективны для уменьшения воспаления, но они также имеют гораздо более серьезные побочные эффекты. Поэтому их должен назначать и контролировать врач. Это синтетические гормоны, которые используются в основном для уменьшения воспаления при длительных состояниях, таких как астма, бронхит, колит и системный артрит.
Общие примеры стероидов включают; Преднизолон, кортизон и гидрокортизон. Они работают, подавляя иммунную систему, что приводит к уменьшению количества воспалений, возникающих в организме в ответ на болезнь или травму. Однако побочным эффектом этого является то, что с подавлением иммунной системы возникает повышенный риск заражения, если принимать его в течение длительного периода времени. Для людей с хроническими воспалительными заболеваниями стероиды являются высокоэффективным средством лечения.
Они работают, подавляя иммунную систему, что приводит к уменьшению количества воспалений, возникающих в организме в ответ на болезнь или травму. Однако побочным эффектом этого является то, что с подавлением иммунной системы возникает повышенный риск заражения, если принимать его в течение длительного периода времени. Для людей с хроническими воспалительными заболеваниями стероиды являются высокоэффективным средством лечения.
Таким образом, если вы испытываете незначительную боль или покалывание, короткий курс НПВП может помочь уменьшить боль и быстро вернуть вас к тренировкам. Однако их не следует использовать, чтобы помочь вам тренироваться с болью, и если вам нужно принимать обезболивающие, чтобы иметь возможность тренироваться, рекомендуется обратиться к местному физиотерапевту или врачу общей практики, чтобы определить причину вашей боли.
Если у вас есть какие-либо сомнения относительно того, следует ли вам принимать противовоспалительные препараты, ваш фармацевт или врач общей практики смогут вам помочь.
Если у вас есть какие-либо опасения, например, проблемы со здоровьем, обратитесь за медицинской помощью к квалифицированному практикующему врачу, будь то врач или физиотерапевт.
A lex Howarth – старший физиотерапевт в Capitalphysio.com
Кто такой физиотерапевт и чем он занимается?
В чем разница между расколотой голенью и стрессовым переломом?
Как снять боль в мышцах после тяжелой тренировки
Почему у меня опухают лодыжки и ноги после триатлона Ironman?
Могу ли я продолжать тренировки с остеоартрозом стопы?
Авторы
Команда 220 Triathlon состоит из опытных спортсменов, спортивных журналистов, обозревателей экипировки и тренеров. Словом, то, чего мы не знаем о мультиспорте, откровенно говоря, и знать не стоит! Говоря это, мы любим расширять наши спортивные знания и повышать наш опыт в этом феноменальном виде спорта.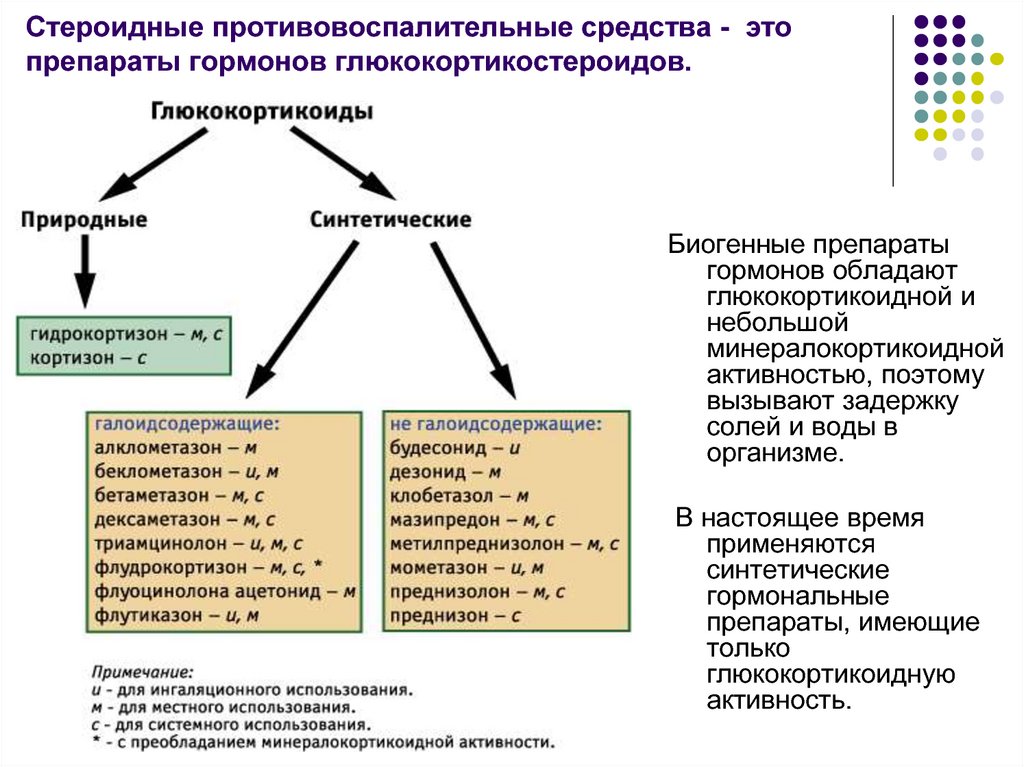
В чем разница между стероидными и нестероидными противовоспалительными препаратами
Ключевое различие между стероидными и нестероидными противовоспалительными препаратами заключается в том, что стероидные противовоспалительные препараты ингибируют фермент фосфолипазу А2, чтобы блокировать воспалительный каскад, в то время как нестероидные противовоспалительные препараты ингибируют фермент циклооксигеназу, чтобы блокировать воспалительный каскад.
Стероидные и нестероидные противовоспалительные препараты представляют собой два различных типа препаратов, доступных на рынке для уменьшения воспаления в организме человека, вызванного различными причинами. Они широко используются в медицине. Более того, обе эти молекулы блокируют действие присущих организму химических веществ, называемых простагландинами, которые способствуют воспалению, лихорадке и боли.
СОДЕРЖАНИЕ
1. Обзор и основные различия
2. Что такое стероидные противовоспалительные препараты
Что такое стероидные противовоспалительные препараты
3. Что такое нестероидные противовоспалительные препараты
4. Сходства – стероидные и нестероидные противовоспалительные препараты
5. Стероидные и нестероидные противовоспалительные препараты -воспалительные препараты в табличной форме
6. Резюме — стероидные и нестероидные противовоспалительные препараты
Что такое стероидные противовоспалительные препараты?
Стероидные противовоспалительные препараты — это тип противовоспалительных препаратов, используемых для уменьшения воспаления в организме человека. Эти препараты ингибируют фермент фосфолипазу А2, блокируя воспалительный каскад. Фосфолипазы, одно из основных веществ, высвобождаемых при воспалении, быстро превращаются в арахидоновую кислоту под действием фосфолипазы А2. Позже арахидоновая кислота может попасть в два разных ответвления воспалительного каскада. Следуя этому пути, он может быть преобразован в простагландины ферментом циклооксигеназой.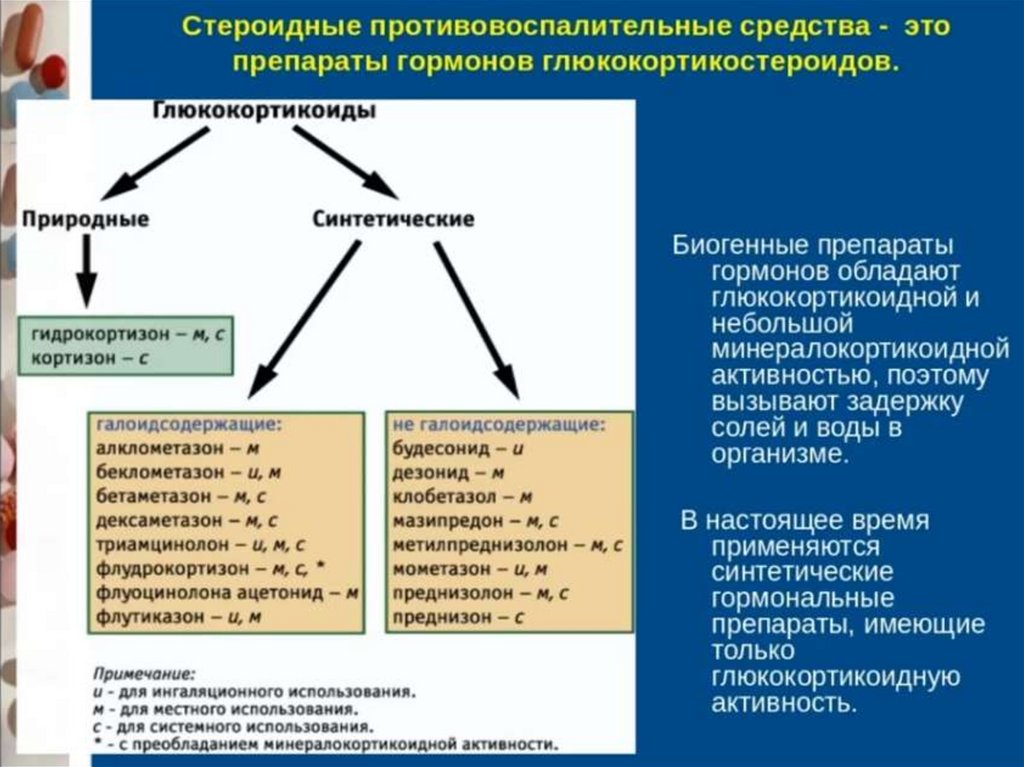 Следуя другим путем, он может быть преобразован в лейкотриены с помощью фермента липооксигеназы. Стероидные противовоспалительные препараты блокируют оба плеча воспалительного каскада.
Следуя другим путем, он может быть преобразован в лейкотриены с помощью фермента липооксигеназы. Стероидные противовоспалительные препараты блокируют оба плеча воспалительного каскада.
Рисунок 01: Стероидные противовоспалительные препараты
Стероидные противовоспалительные препараты уменьшают проницаемость сосудов, покраснение, отек и боль. Кроме того, они имеют дополнительное преимущество, так как удерживают лейкоциты изолированными от очага воспаления, блокируя липоксигеназное звено воспалительного каскада. Стероиды противовоспалительные препараты могут поступать из животных, растений и человека. Они могут состоять из половых стероидов, кортикостероидов и анаболических стероидов. Что касается кортикостероидов, то они используются при различных состояниях, включая кожные заболевания, гормональную недостаточность и опухоли. Кортикостероиды также в основном используются для лечения болей и воспалений в суставах. Однако они обладают наркотическим эффектом и могут вызывать сильную зависимость у пациентов.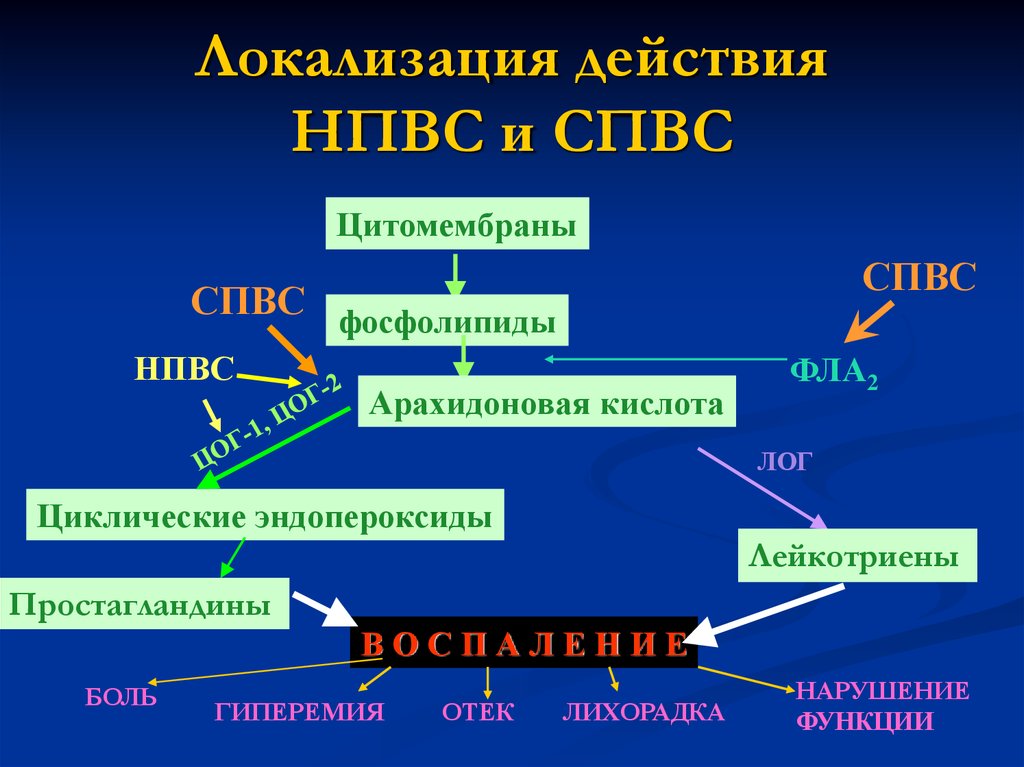
Что такое нестероидные противовоспалительные препараты?
Нестероидные противовоспалительные препараты (НПВП) ингибируют ферменты циклооксигеназы от блокирования воспалительного каскада. Они блокируют только одно звено воспалительного каскада. Нестероидные противовоспалительные препараты относятся к классу противовоспалительных препаратов, которые уменьшают боль, воспаление и лихорадку, а также предотвращают образование тромбов. НПВП действуют путем ингибирования ферментативной активности циклооксигеназы (ЦОГ-1 и ЦОГ-2). В клетках этот фермент участвует в синтезе ключевых биологических медиаторов, известных как простагландины и тромбоксаны, которые участвуют в воспалении и свертывании крови соответственно.
Рисунок 02: Нестероидные противовоспалительные препараты
Побочными эффектами нестероидных противовоспалительных препаратов являются тошнота, рвота, аллергические реакции, язвы желудочно-кишечного тракта, кровотечения, анемия, сердечный приступ и заболевание почек. Некоторыми из наиболее известных НПВП являются аспирин, ибупрофен и напроксен. Все они доступны без рецепта в большинстве стран.
Некоторыми из наиболее известных НПВП являются аспирин, ибупрофен и напроксен. Все они доступны без рецепта в большинстве стран.
Каковы сходства между стероидными и нестероидными противовоспалительными препаратами?
- Стероидные и нестероидные противовоспалительные препараты представляют собой два различных типа препаратов, доступных на рынке для уменьшения воспаления в организме человека, вызванного различными причинами.
- Оба класса препаратов могут уменьшать воспаление, боль и лихорадку.
- Имеют побочные эффекты.
- Они легко доступны на рынке.
В чем разница между стероидными и нестероидными противовоспалительными препаратами?
Стероидные противовоспалительные препараты ингибируют фермент фосфолипазу А2 от блокирования воспалительного каскада, в то время как нестероидные противовоспалительные препараты ингибируют фермент циклооксигеназу от блокирования воспалительного каскада. Таким образом, в этом ключевое различие между стероидными и нестероидными противовоспалительными препаратами.
 D., Giuliano F., Vojnovic I. et al. Nonsteroid drug selectivities for cyclo-oxygenase-1 rather than cyclooxygenase-2 are associated with human gastrointestinal toxicity: a full in vitro analysis // Proc. Natl. Acad. Sci. USA 1999; 96: 7563–7568.
D., Giuliano F., Vojnovic I. et al. Nonsteroid drug selectivities for cyclo-oxygenase-1 rather than cyclooxygenase-2 are associated with human gastrointestinal toxicity: a full in vitro analysis // Proc. Natl. Acad. Sci. USA 1999; 96: 7563–7568. 2016 Jan; 32 (1): 23–36.
2016 Jan; 32 (1): 23–36.