Роль УГЛЕРОДА в организме человека действие содержание источники (Таблица)
Углерод – важнейший биогенный элемент, составляющий основу жизни на Земле, структурная единица огромного числа органических соединений, участвующих в построении организмов и обеспечении их жизнедеятельности (биополимеры, а также многочисленные низкомолекулярные биологически активные вещества — витамины, гормоны, медиаторы и другие). Значительная часть необходимой организмам энергии образуется в клетках за счёт окисления углерода. Возникновение жизни на Земле рассматривается в современной науке как сложный процесс эволюции углеродистых соединений.
В организм человека углерод поступает с пищей (в норме около 300г в сутки). Общее содержание углерода достигает около 21% (15кг на 70кг общей массы тела). Углерод составляет 2/3 массы мышц и 1/3 массы костной ткани. Выводится из организма преимущественно с выдыхаемым воздухом (углекислый газ) и мочой (мочевина).
Таблица роль УГЛЕРОДА (С) в организме человека его содержание потребность источники
|
Содержание Углерода в человеческом организме: |
Содержание в человеческом организме: 21% от массы тела; костная ткань — 36%; мышечная ткань — 67% |
|
Биологическая роль Углерода: |
Главной функцией углерода является формирование разнообразия органических соединений, тем самым, обеспечивая биологическое разнообразие, участие во всех функциях и проявлениях живого. Играет очень важную биологическую роль для всех форм жизни: — входит в состав белков, жиров, углеводов, нуклеиновых кислот, гормонов, ферментов, витаминов и другие; — углекислота крови возбуждает дыхательный центр, расширяет мозговые сосуды, повышает возбудимость сердечной мышцы; — гидрокарбонаты калия и натрия входят в состав буферных систем крови и тканей, поддерживающих рН организма; — уксусная кислота принимает участие в синтезе холестерина |
|
Источники C: |
Источники: пищевые продукты, воздух, минеральные воды |
|
Суточная потребность: |
Суточная потребность составляет 300г с пищей |
|
Недостаток: |
При недостатоке в пище — общее истощение организма, снижение мозговой деятельности |
|
Избыток С: |
Избыток вызывает при повышенном содержании СО2 — кислородное голодание |
|
Токсичность углерода: |
Углерод в свободном виде не токсичен, токсичны соединения (СО, СN, СО2, HCN, CS2, COCl2 и другие) |
|
Лекарственные препараты, содержащие углерод |
Уголь активированный, Натрия гидрокарбонат |
_______________
Источник информации:
1. Химические элементы в организме человека./ Архангельск.: 2001.
Химические элементы в организме человека./ Архангельск.: 2001.
2. Роль биогенных элементов в организме человека и применение их в медицине и фармации./ Майкоп.: 2016.
Физиологическая роль углерода и кремния и их свойства в организме человека
МИНЕСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ
ФЕДЕРАЦИИ
Федеральное государственное
бюджетное образовательное
высшего профессионального образования
«Московский государственный университет пищевых производств»
Институт ветеринарной экспертизы, санитарии и экологии
Кафедра неорганической и аналитической химии
Реферат по химии
Тема: »Физиологическая роль углерода и кремния
и их свойства в организме человека»
 , 2 п.гр
, 2 п.гр
Москва 2013
Оглавление
1. Введение. 3
2. Физиологическая роль углерода. 4
2.1. Некоторые свойства углерода. 4
3. Физиологическая роль кремния. 5
3.1. «Пожиратели» кремния, дефицит. 6
3.2. Разновидности кремния. 6
3.2.1. Кремний – биокатализатор. 8
4. Вывод. 8
1. Введение.
Углерод (лат. Carboneum), С – химический элемент IV группы периодической системы Менделеева.
Углерод известен с глубокой древности.
Древесный уголь служил для восстановления
металлов из руд, алмаз – как драгоценный
камень. Значительно позднее стал применяться
графит для изготовления тиглей и карандашей.
Значительно позднее стал применяться
графит для изготовления тиглей и карандашей.
В 1778 году К. Шелле, нагревая графит с селитрой, обнаружил, что при этом, как и при нагревании угля с селитрой, выделяется углекислый газ. Химический состав алмаза был установлен в результате опытов А. Лавуазье (1772) по изучениям горени алмаза на воздухе и исследований С. Теннанта (1797), доказавшего, что одинаковые количества алмаза и угля дают при окислении равные количества углекислого газа. Угларод как химический элемент был признан только в 1789 А. Лавуазье. Латинское название carboneum углерод получил от carbo – уголь.
Ближайший аналог углерода – кремний
– является 3-им (после кислорода
и водорода) по распространенности
элементом: на его долю приходится 16,7%
от общего числа атомов земной коры.
Если углерод можно рассматривать
как основной элемент для всей
органической жизни, то кремний играет
подобную же роль по отношению к
твердой земной коре, так как главная
часть её массы состоит из силикатных
пород, обычно представляющих собой
смеси различных соединений кремния
с кислородом и рядом других элементов.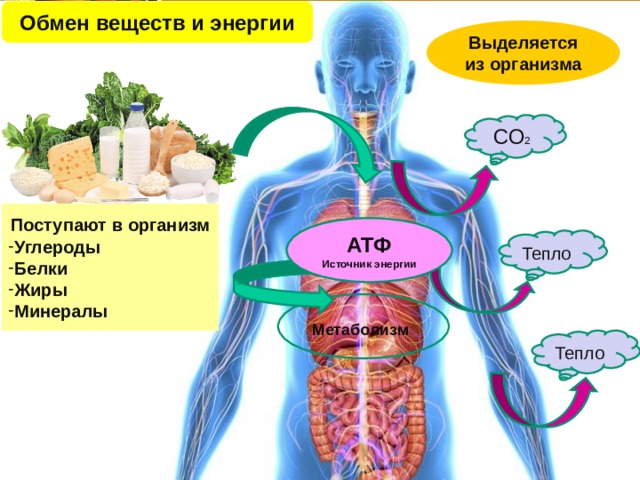 Весьма часто встречается и свободная
двуокись кремния (SiO2), главным образом
в виде обычного песка.
Весьма часто встречается и свободная
двуокись кремния (SiO2), главным образом
в виде обычного песка.
Свободный кремний впервые получен в 1823г. Природный элемент слагается из трёх изотопов – 28Si (92.2%), 29Si (4.7) и 30Si (3.1).
2. Физиологическая роль углерода.
Углерод имеет очень большое значение из-за его исключительно важной роли в живой природе. Соединения углерода являются основой растительных и живых организмов, то есть углерод является главным элементом жизни. Чем сложнее организм, тем, как правило, выше в нем содержание углерода (от 0,1 до 30 %). В организме человека на долю углерода приходится 21,15%. Он входит в состав всех тканей и клеток в форме белков, жиров, углеводов, витаминов и гормонов.
В организм человека углерод поступает
с пищей (около 300 г в сутки). Углерод
составляет 2/3 массы мышц и 1/3 массы
костной ткани. Выводится из организма
преимущественно с выдыхаемым воздухом
(углекислый газ) и мочой (мочевина).
В биомолекулах углерод образует полимерные цепи и прочно соединяется с водородом, кислородом, азотом и другими элементами. Физиологическая роль углерода определяется тем, что этот элемент входит в состав всех органических соединений и принимает участие практически во всех биохимических процессах в организме. Окисление соединений углерода под действием кислорода приводит к образованию воды и углекислого газа; этот процесс служит для организма источником энергии. Двуокись углерода СО2 (углекислый газ) образуется в процессе обмена веществ и является стимулятором дыхательного центра, играет важную роль в регуляции дыхания и кровообращения.
В свободном виде углерод не токсичен,
но многие его соединения обладают
значительной токсичностью: окись углерода
СО (угарный газ), четыреххлористый углерод
СС14, сероуглерод CS2, соли цианистой
кислоты HCN, бензол C6H8 и ряд
других. Углекислый газ в концентрации
свыше 10% вызывает ацидоз (снижение рН
крови), одышку и паралич дыхательного
центра.
Длительное вдыхание каменноугольной пыли может привести к антракозу — заболеванию, которое сопровождается отложением угольной пыли в ткани легких и лимфатических узлах, склеротическими изменениями легочной ткани. Токсическое действие углеводородов и других соединений нефти у рабочих, занятых в нефтедобывающей промышленности может проявиться в огрубении кожи, появлении трещин и язв, развитии хронических дерматитов.
2.1. Некоторые свойства углерода.
- Суточное поступление с продукт
ами питания: 300 г - Суточное поступление с воздухом: 3,7 г
- Резорбция (%): 10%
- Суточное выведение с воздухом: -300 г
- Период полувыведения из организма: 37 суток
- Число атомов в теле человека: 6,4 х 10
- Число атомов в одной клетке: 6.4 х 10
- Среднее содержание в человеческом организме:
кг/70 кг :16
кровь: 25000 мг/л
кости: 280000 мг/кг
- Токсичная доза для человека может быть в форме CO или цианидов.

3. Физиологическая роль кремния.
Великий русский ученый В. Вернадский
писал, что ни один живой организм
не может нормально развиваться
при дефиците кремния. Ведь соединения
кремния присутствуют в тканях практически
всех наших внутренних органов. Дефицит
кремния является одной из причин
патологического изменения
Кремний – это маленькая, но жизненно
важная часть всех соединительных тканей,
костей, сосудов и хрящей. Дефицит
кремния, нередко проявляющийся
с возрастом у человека, становится
причиной снижения эластичности сосудов,
особенно артерий крупного и среднего
диаметра. На этом фоне повышается склонность
к формированию в них атеросклеротических
бляшек. Кремний, содержащийся в тканях
стенок сосудов, препятствует проникновению
холестерина в плазму и отложению
липидов на стенках сосудов. С
возрастом может снизиться  Это
обстоятельство приводит к атеросклерозу,
так как стенки сосудов утрачивают
свою эластин-ткань, богатую кремнием,
ответственную за упругость сосудов.
В крови же обычно больших изменений
не происходит. Однако на стенках сосудов
образуются холестериновые бляшки — это
липиды на кальциевой основе и колонии
трихомонад — что приводит к сужению
сосудов.
Это
обстоятельство приводит к атеросклерозу,
так как стенки сосудов утрачивают
свою эластин-ткань, богатую кремнием,
ответственную за упругость сосудов.
В крови же обычно больших изменений
не происходит. Однако на стенках сосудов
образуются холестериновые бляшки — это
липиды на кальциевой основе и колонии
трихомонад — что приводит к сужению
сосудов.
3.1. «Пожиратели» кремния, дефицит.
Самыми страшными пожирателями
кремния в организме человека
являются глисты и грибки. Размножаясь
в огромных масштабах, они заселяют
практически все ткани  На смену
здорового экологического порядка приходит
хаос.
На смену
здорового экологического порядка приходит
хаос.
Если кремния не хватает, 70 других необходимых микроэлементов вообще не усваиваются. При недостатке кремния падает уровень лейкоцитов в крови, плохо заживают раны и царапины, снижаются аппетит и иммунитет, могут развиться остеопороз, артрит, атеросклероз, гипертония, язва желудка, туберкулез, стенокардия, аритмия, инфаркт миокарда и инсульт. При его дефиците ногти и волосы становятся ломкими и сухими, а кожа – дряблой. Большое количество бородавок на коже также может быть вызвано недостатком кремния в организме. Могут возникать и некоторые нарушения функций головного мозга, так как он играет важную роль в осуществлении нормальной деятельности мозжечка. На фоне дефицита кремния в организме нарушается координация движений, появляется пошатывание при ходьбе, общая слабость, нарастает раздражительность, растерянность.
Беременные женщины, кормящие
матери и дети особенно нуждаются
в продукта содержащих кремний. Необходимость
в кремнии у них в несколько
раз выше, чем у взрослого человека.
Ведь у растущего организма
Необходимость
в кремнии у них в несколько
раз выше, чем у взрослого человека.
Ведь у растущего организма
3.2. Разновидности кремния.
Кремний бывает темно — серого (такой
кремень содержит в себе магний) и красноватого
цвета (содержит железо). Для лечебных
целей используется только темно — серый
(черный) кремень. Происхождение его органогенное,
то есть он образовался на Земле при отмирании
колоний живых организмов, сохраняя в
своем составе раковины и скелеты. Он зарождался
в теплых водоемах Мелового периода, когда
появились привычные нам формы жизни.
Черный камень донес до нас «память» о
воде той эпохи. Камень в воде начинает
вырабатывать кремниевую кислоту в гомеопатических
дозах, но этого достаточно, чтобы при
попадании в организм она могла растворять
шлаки, отложения солей в различных органах. Он способен создавать условия, необходимые
для восстановления здоровых, жизнеобеспечивающих
процессов.
Он способен создавать условия, необходимые
для восстановления здоровых, жизнеобеспечивающих
процессов.
3.2.1. Кремний – биокатализатор.
Ученые утверждают, что органические остатки в кремнии — это уникальные биокатализаторы (устроители), способные перерабатывать энергию света и в десятки раз ускорять окислительно-восстановительные реакции в водных растворах нашего тела. Эти биологические вещества являются основой для построения сложных органических соединений — основ живого организма — хлорофилла и гемоглобина. Эти водные растворы, образующиеся вокруг кремния, играют огромнейшую роль в развитии всего живого и благотворно воздействуют на организм. В кремниевой воде происходит образование структурной водной системы с электрической решеткой жидких кристаллов кремния так, что в ней нет места патогенным, несимбиотным микроорганизмам и чужеродным химическим элементам. Эти чужеродные примеси вытесняются из воды и выпадают в осадок.
4. Вывод.
Кремний — микроэлемент, постоянно содержащийся
в организме человека. Наибольшее его
количество содержится в лимфоузлах, соединительной
ткани аорты, трахеи, в волосах и коже.
Кремний необходим для построения эпителиальных
клеток, участвует в процессах оссификации
совместно с магнием и фтором.
Наибольшее его
количество содержится в лимфоузлах, соединительной
ткани аорты, трахеи, в волосах и коже.
Кремний необходим для построения эпителиальных
клеток, участвует в процессах оссификации
совместно с магнием и фтором.
Кремний играет важную роль в процессе минерализации костной ткани; необходим для поддержания эластичности стенки артерий, оказывает положительное влияние на иммунитет и замедляет процессы старения в тканях организма человека.
Источниками кремния являются бурый рис, свёкла, соевые бобы,
Углерод — важнейший биогенный элемент, составляющий основу жизни на Земле. Значительная часть необходимой организмам энергии образуется в клетках за счет окисления Углерода. Уникальная роль Углерода в живой природе обусловлена его свойствами, которыми в совокупности не обладает ни один элемент периодической системы. Всего три элемента — С, О и Н — составляют 98% общей массы живых организмов.
2
3
7
Из каких химических элементов состоит тело человека?
Картографирование самых высоких гор мира по континентам
От заснеженных Гималаев в Азии до спящего Мауна-Кеа на Гавайях горы издавна привлекали людей.
Это геологические чудеса, священные места и венец славы природы и народов. И хотя горные хребты есть по всему миру, некоторые пики буквально выделяются среди остальных.
На этом рисунке Arijit Gupta использует данные из различных источников, включая Википедию, Peakbagger и EarthENV, чтобы выделить три горы, которые венчают каждый из континентов мира.
1. Азия
С тремя самыми высокими вершинами, каждая из которых превышает 8000 метров, Азия имеет самые высокие горы в мире с точки зрения абсолютной высоты.
| Гора | Диапазон | Высота |
|---|---|---|
| Эверест | Гималаи | 8 845 м |
| К2 | Каракорум | 8 609 м |
| Канченджанга | Гималаи | 8 586 м |
Возвышаясь над Гималаями, знаменитая гора Эверест на границе Китая и Непала является самой высокой горной вершиной на Земле по высоте.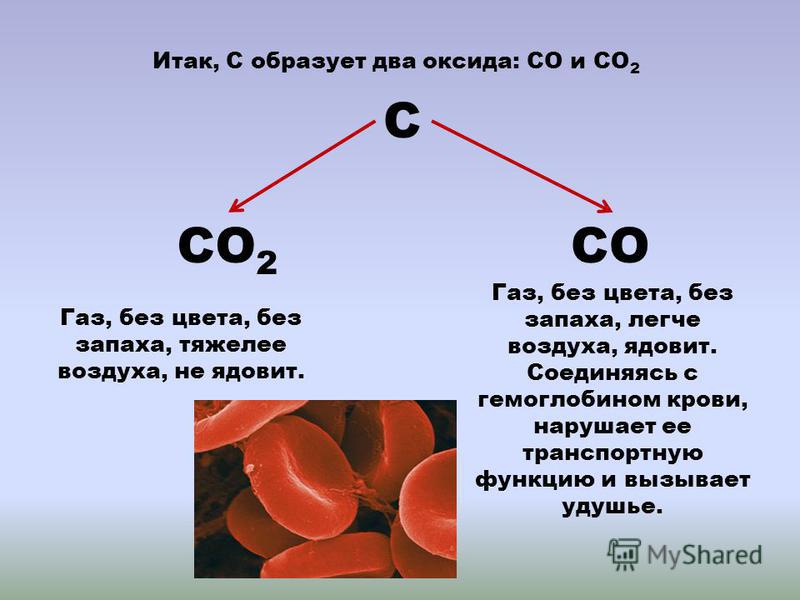 Альпинисты тренируются месяцами, а иногда и годами, чтобы покорить эту сложную вершину.
Альпинисты тренируются месяцами, а иногда и годами, чтобы покорить эту сложную вершину.
Недалеко от Эвереста находится Каракорумский хребет K2 между Пакистаном и Китаем. Хотя его вершина чуть более чем на 200 метров короче, чем у Эвереста, говорят, что более ненастная погода на местном уровне делает его намного более опасным для альпинистов.
Главный пик Канченджанга , другой гималайской горы между Индией и Непалом, имеет высоту 8586 метров. Хотя этот пик является третьим по высоте в мире, его диапазон включает четыре других пика, которые не сильно отстают.
2. Южная Америка
Вершины Южной Америки видны вдоль горной цепи Анд, начиная с самой высокой горной вершины в Южном полушарии— Аконкагуа .
| Гора | Диапазон | Высота |
|---|---|---|
| Аконкагуа | Анды | 6 961 м |
| Охос-дель-Саладо | Анды | 6893 м |
| Монте-Писсис | Анды | 6793 м |
Расположенный в Аргентине, Аконкагуа стоит на ошеломляющей высоте 6 961 метр над уровнем моря.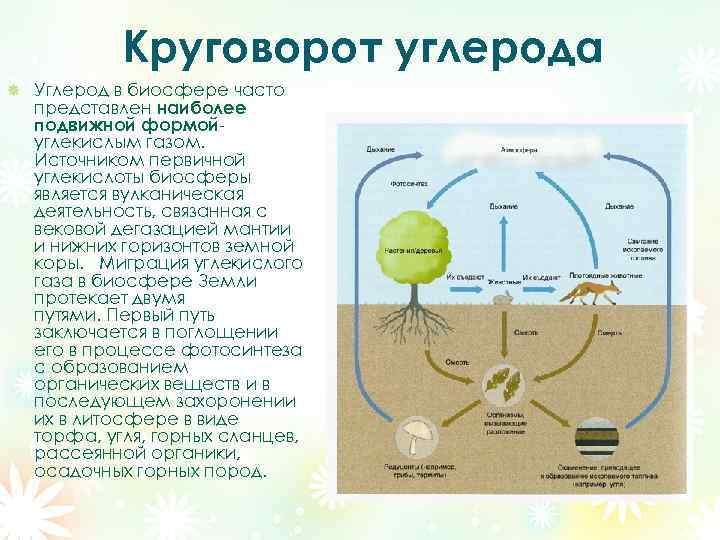 Это также самая высокая горная вершина в Америке.
Это также самая высокая горная вершина в Америке.
Охос-дель-Саладо на границе Аргентины и Чили занимает второе место по высоте. Этот пик считается самым высоким вулканом в мире, его верхние части содержат купола лавы, потоки лавы и вулканические кратеры.
Другая аргентинская гора, Monte Pissis , стоит всего на 100 метров ниже Охос-дель-Саладо. На высоте 6793 метра она по-прежнему является третьей по высоте горой в Западном полушарии.
3. Северная Америка
В отличие от вышеперечисленных континентов, самые высокие горы в Северной Америке расположены на нескольких различных горных хребтах.
| Гора | Диапазон | Высота |
|---|---|---|
| Денали | Аляска | 6 190 м |
| Гора Логан | Сент-Элиас | 5959 м |
| Пико де Орисаба | Трансмексиканский вулканический пояс | 5 636 м |
Гора Денали в США на Аляске — самая высокая гора в Северной Америке высотой 6190 метров. Говорят, что Денали, ранее называвшаяся горой Мак-Кинли, благодаря субарктическому расположению и высоте является самой холодной горой в мире.
Говорят, что Денали, ранее называвшаяся горой Мак-Кинли, благодаря субарктическому расположению и высоте является самой холодной горой в мире.
Расположенная на канадской территории Юкон, Гора Логан является второй по высоте горой в Северной Америке. Благодаря процессу, известному как тектоническое поднятие, он все еще увеличивается в высоту примерно на 0,35 мм каждый год.
Мексиканский спящий вулкан Пико-де-Орисаба занимает третье место. Хотя он является частью далекого Трансмексиканского вулканического пояса, все крупнейшие горы континента являются частью Североамериканских Кордильер соединенных горных хребтов.
4. Африка
В Африке находятся три высочайшие вершины мира, а окружающие их горные склоны отличаются одним из самых разнообразных климатических условий.
| Гора | Диапазон | Высота |
|---|---|---|
| Гора Килиманджаро | Восточный разлом | 5895 м |
| Гора Кения | Восточный разлом | 5199 м |
| Маунт Стэнли | Рувензори | 5 109 м |
Танзания Гора Килиманджаро — высочайшая вершина Африки и самая высокая отдельно стоящая гора в мире.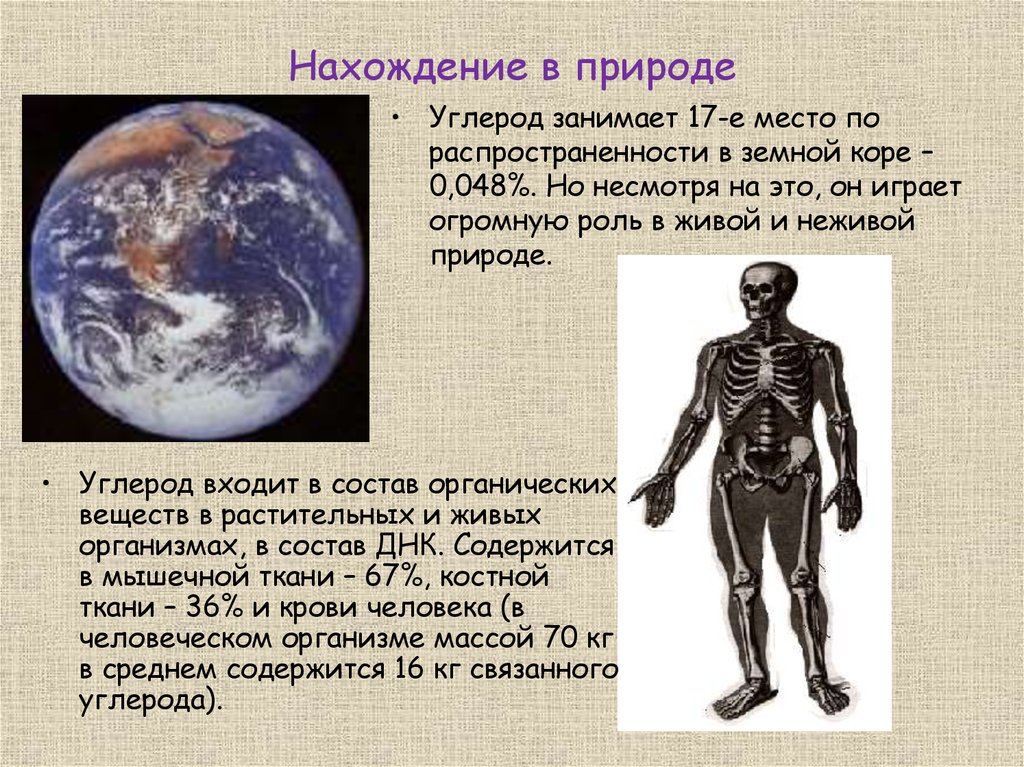 Восхождение на Килиманджаро — это уникальный опыт, поскольку он проведет вас через пять различных экологических зон, включая тропические леса, вересковые пустоши, альпийские пустыни и ледники.
Восхождение на Килиманджаро — это уникальный опыт, поскольку он проведет вас через пять различных экологических зон, включая тропические леса, вересковые пустоши, альпийские пустыни и ледники.
Между тем, вторая по высоте вершина Африки в Кении, ее тезка Гора Кения , на самом деле имеет три отдельные вершины. Это объект Всемирного наследия ЮНЕСКО, где обитают различные виды диких животных, в том числе слоны и гиены.
Рядом находится гора Стэнли хребта Рувензори. Расположенный на границе между Угандой и Демократической Республикой Конго, он считается священным местом, где на вершинах гор проживают предки.
5. Европа
В Кавказских горах на краю Восточной Европы расположены самые высокие горы континента.
| Гора | Диапазон | Высота |
|---|---|---|
| Гора Эльбрус | Кавказские горы | 5642 м |
| Гора Дых-Тау | Кавказские горы | 5,205м |
| Шхара | Кавказские горы | 5 193 м |
Гора Эльбрус занимает первое место в России с высотой 5642 м. Гора представляет собой спящий вулкан с симметричной формой двойного конуса, но, поскольку его последний взрыв произошел около 50 г. н.э., в настоящее время он покрыт снегом и ледниками.
Гора представляет собой спящий вулкан с симметричной формой двойного конуса, но, поскольку его последний взрыв произошел около 50 г. н.э., в настоящее время он покрыт снегом и ледниками.
Рядом Гоа Дых-Тау — вторая по высоте гора в Европе. Он имеет острую пирамидальную вершину, резко возвышающуюся над его основанием, и расположен всего в нескольких километрах к северу от границы с Грузией.
Сразу за границей с южной стороны находится Шхара , третья по высоте вершина на европейском континенте. Он известен характерной двойной вершиной, причем западная вершина немного выше восточной.
6. Океания
В то время как на многих из вышеперечисленных континентов есть горные вершины высокого ранга, расположенные в разных странах, все Океании полностью находятся в Индонезии на острове Новая Гвинея.
| Гора | Диапазон | Высота |
|---|---|---|
| Пунчак Джая | Судирман | 4 884 м |
| Сумантри | Судирман | 4870 м |
| Пунчак Мандала | Джаявиджая | 4 760 м |
Самая высокая вершина Океании — Пунчак-Джая , также известная под другими местными названиями, включая Пирамида Карстенса , вершиной которой является Пунчак-Джая.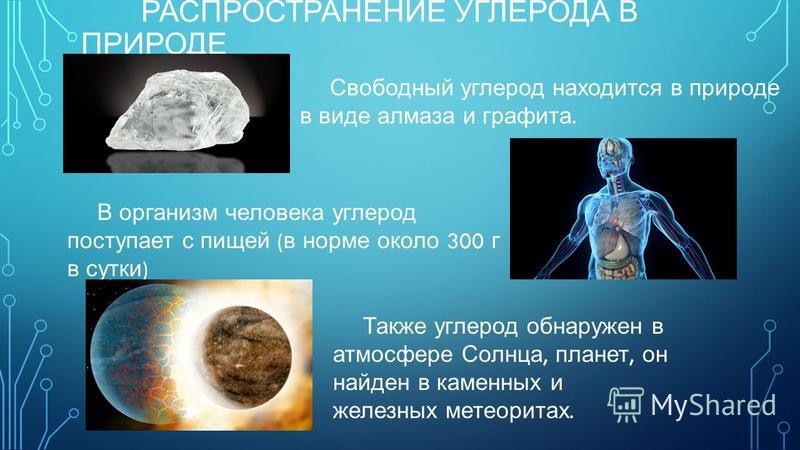 Это самая высокая гора в мире на острове, и восхождение на ее вершину представляет собой сложную задачу из-за ее удаленности и труднопроходимой местности.
Это самая высокая гора в мире на острове, и восхождение на ее вершину представляет собой сложную задачу из-за ее удаленности и труднопроходимой местности.
Десятилетия назад занявший второе место Сумантри был известен как Нгга Пулу и был выше, чем Пунчак Джая. Однако это изменилось из-за таяния ледников с 1850-х годов, что помогло изолировать и прояснить местные вершины пирамиды Карстенс. Сегодня Сумантри возвышается на 4870 метров и является вторым по высоте на континенте.
К востоку от хребта Джаявиджайя, Пунчак Мандала занимает третье место в этом списке. Но как отдельно стоящая гора она иногда считается второй по высоте вершиной в Океании, в то время как Сумантри не считается ответвлением пирамиды Карстенс.
Бонус: Антарктида
Хотя они не были нанесены на карту, Гупта также включил данные о горах Антарктиды, которые не похожи ни на какие другие горы на Земле.
Эти горы расположены относительно низко и часто полностью покрыты льдом и снегом.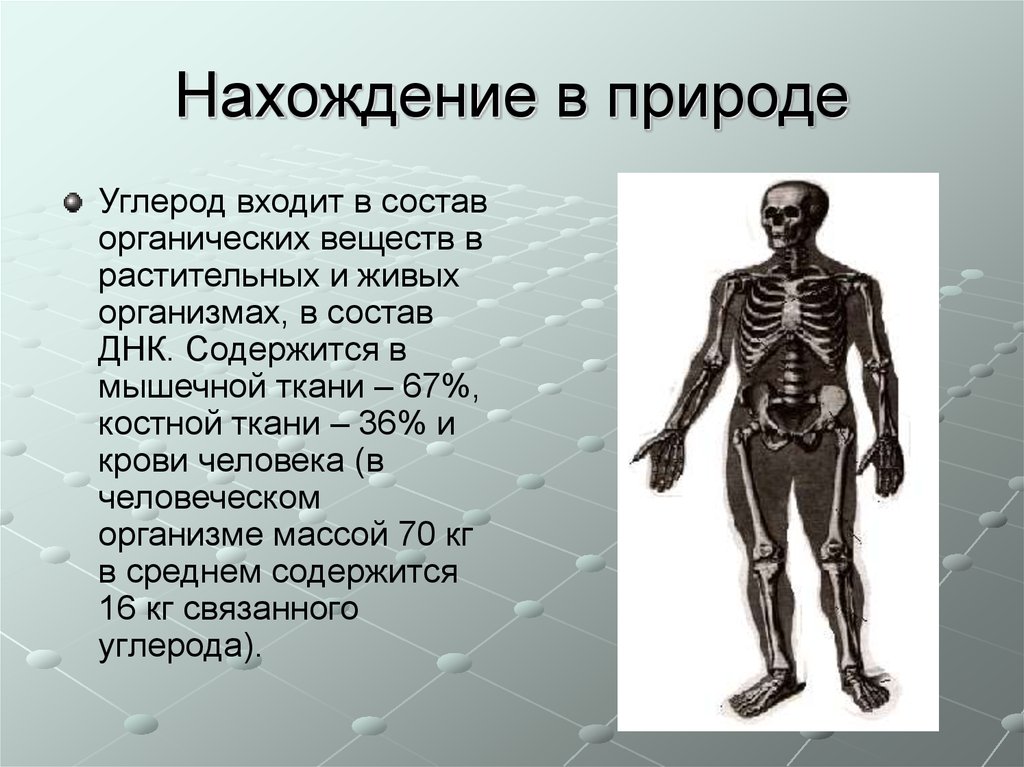
| Гора | Диапазон | Высота |
|---|---|---|
| Массив Винсон | Сентинел | 4892 м |
| Гора Тайри | Sentinel | 4852 м |
| Гора Шинн | Страж | 4661 м |
Массив Винсон содержит самую высокую вершину Антарктиды, известную как гора Винсон. Обнаруженная в 1958 году гора представляет собой сложное восхождение с большим количеством ледяной местности и была последней из семи вершин, на которую впервые поднялись в 19 году.66.
Гора Тайри является второй по высоте на континенте и находится всего в 13 километрах от Винсона. Он имеет высоту всего на 40 метров короче, но также труднодоступен.
Для сравнения, Гора Шинн — третья по высоте вершина на континенте — иногда также покоряется опытными альпинистами, которые приезжают в Антарктиду, чтобы подняться на гору Винсон.
Углерод | Факты, использование и свойства
углерод
Посмотреть все СМИ
- Ключевые люди:
- Август Кекуле фон Страдониц Сэр Гарольд В. Крото Роберт Керл Джон Ульрик Неф Чарльз Гловер Баркла
- Связанные темы:
- фуллерен графен алмаз графит аморфный углерод
Просмотреть весь связанный контент →
Последние новости
5 апреля 2023 г., 13:07 по восточному времени (AP)
Оспаривание политики Байдена в отношении «стоимости углерода» отклонено
Федеральный апелляционный суд отклонил возражение, которое Луизиана и другие республиканские штаты подали против экологической политики администрации Байдена
углерод (C) , неметаллический химический элемент в Группа 14 (IVa) периодической таблицы. Хотя углерод широко распространен в природе, его не так много — он составляет всего около 0,025 процента земной коры, — однако он образует больше соединений, чем все остальные элементы вместе взятые. В 1961 изотоп углерода-12 был выбран вместо кислорода в качестве эталона, относительно которого измеряются атомные массы всех других элементов. Углерод-14, который является радиоактивным, является изотопом, используемым для радиоуглеродного датирования и радиоактивной маркировки.
В 1961 изотоп углерода-12 был выбран вместо кислорода в качестве эталона, относительно которого измеряются атомные массы всех других элементов. Углерод-14, который является радиоактивным, является изотопом, используемым для радиоуглеродного датирования и радиоактивной маркировки.
| атомный номер | 6 | |
|---|---|---|
| атомный вес | от 12,0096 до 12,01389 432 точка плавления | 3550 °C (6420 °F) |
| температура кипения | 4827 °C (8721 °F) | |
| плотность | ||
| алмаз | 3,52 г/см | 3 |
| графит | 2,25 г/см 3 | |
| аморфный | 1,9 г/см 3 | |
| степени окисления | +2, +3, +4 | |
| 2 электронная конфигурация | 0328 2 2 с 2 2 p 2
Свойства и применение
По весу углерод занимает 19-е место по распространенности элементов в земной коре, и, по оценкам, в 3,5 раза больше атомов углерода. как атомы кремния во Вселенной. Только водорода, гелия, кислорода, неона и азота атомарно больше в космосе, чем углерода. Углерод — это космический продукт «сгорания» гелия, при котором три ядра гелия с атомным весом 4 сливаются, образуя ядро углерода с атомным весом 12,9.0005
как атомы кремния во Вселенной. Только водорода, гелия, кислорода, неона и азота атомарно больше в космосе, чем углерода. Углерод — это космический продукт «сгорания» гелия, при котором три ядра гелия с атомным весом 4 сливаются, образуя ядро углерода с атомным весом 12,9.0005
Знать об углероде и почему его называют элементом жизни
Посмотреть все видео к этой статье В земной коре элементарный углерод является второстепенным компонентом. Однако соединения углерода (то есть карбонаты магния и кальция) образуют обычные минералы (например, магнезит, доломит, мрамор или известняк). Кораллы и раковины устриц и моллюсков в основном состоят из карбоната кальция. Углерод широко распространен в виде угля и органических соединений, составляющих нефть, природный газ и все ткани растений и животных. Естественная последовательность химических реакций, называемая углеродным циклом, включающая превращение атмосферного углекислого газа в углеводы путем фотосинтеза в растениях, потребление этих углеводов животными и их окисление посредством метаболизма с образованием двуокиси углерода и других продуктов, а также возврат углерода. двуокиси в атмосферу — один из важнейших биологических процессов.
двуокиси в атмосферу — один из важнейших биологических процессов.
Углерод как элемент был открыт первым человеком, который достал древесный уголь из огня. Таким образом, наряду с серой, железом, оловом, свинцом, медью, ртутью, серебром и золотом углерод был одним из небольшой группы элементов, хорошо известных в древнем мире. Современная углеродная химия восходит к разработке углей, нефти и природного газа в качестве топлива и к выяснению синтетической органической химии, которые существенно развились с 1800-х годов.
Викторина Британика
Материал, из которого сделаны вещи
Элементарный углерод существует в нескольких формах, каждая из которых имеет свои физические характеристики. Две его четко определенные формы, алмаз и графит, имеют кристаллическую структуру, но различаются по физическим свойствам, поскольку расположение атомов в их структурах неодинаково. Третья форма, называемая фуллереном, состоит из множества молекул, полностью состоящих из углерода. Сфероидальные фуллерены с закрытой клеткой называются бакерминстерфуллеренами, или «бакиболами», а цилиндрические фуллерены называются нанотрубками. Четвертая форма, называемая Q-углеродом, является кристаллической и магнитной. Еще одна форма, называемая аморфным углеродом, не имеет кристаллической структуры. Другие формы — сажа, древесный уголь, ламповая сажа, уголь, кокс — иногда называют аморфными, но рентгенологическое исследование показало, что эти вещества действительно обладают низкой степенью кристалличности. Алмаз и графит встречаются на Земле в природе, но их также можно производить синтетическим путем; они химически инертны, но соединяются с кислородом при высоких температурах, как это делает аморфный углерод. Фуллерен был случайно открыт в 1985 в качестве синтетического продукта в ходе лабораторных экспериментов по моделированию химии атмосферы звезд-гигантов. Позже было обнаружено, что он встречается в природе в крошечных количествах на Земле и в метеоритах. Q-углерод также является синтетическим, но ученые предполагают, что он может образовываться в горячих средах некоторых планетарных ядер.
Сфероидальные фуллерены с закрытой клеткой называются бакерминстерфуллеренами, или «бакиболами», а цилиндрические фуллерены называются нанотрубками. Четвертая форма, называемая Q-углеродом, является кристаллической и магнитной. Еще одна форма, называемая аморфным углеродом, не имеет кристаллической структуры. Другие формы — сажа, древесный уголь, ламповая сажа, уголь, кокс — иногда называют аморфными, но рентгенологическое исследование показало, что эти вещества действительно обладают низкой степенью кристалличности. Алмаз и графит встречаются на Земле в природе, но их также можно производить синтетическим путем; они химически инертны, но соединяются с кислородом при высоких температурах, как это делает аморфный углерод. Фуллерен был случайно открыт в 1985 в качестве синтетического продукта в ходе лабораторных экспериментов по моделированию химии атмосферы звезд-гигантов. Позже было обнаружено, что он встречается в природе в крошечных количествах на Земле и в метеоритах. Q-углерод также является синтетическим, но ученые предполагают, что он может образовываться в горячих средах некоторых планетарных ядер.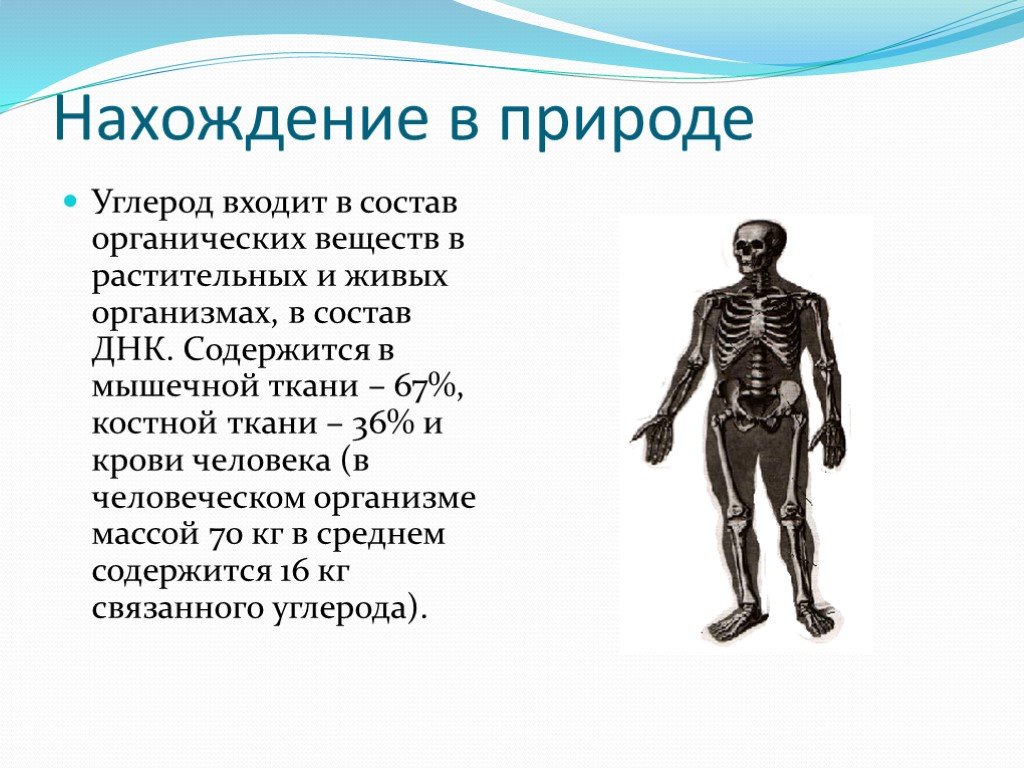
Слово углерод , вероятно, происходит от латинского карбо , означающего по-разному «уголь», «древесный уголь», «угли». Срок бриллиант , искаженное греческое слово adamas , «непобедимый», точно описывает постоянство этой кристаллизованной формы углерода, точно так же, как графит , название другой кристаллической формы углерода, происходящее от греческого глагола графеин , «писать», отражает его свойство оставлять темный след при трении о поверхность. До открытия в 1779 году, что графит при сгорании на воздухе образует углекислый газ, графит путали как с металлическим свинцом, так и с внешне похожим веществом, минералом молибденитом.
Оформите подписку Britannica Premium и получите доступ к эксклюзивному контенту. Подпишитесь сейчас
Чистый алмаз — самое твердое известное природное вещество, которое плохо проводит электричество. Графит, с другой стороны, представляет собой мягкое скользкое твердое вещество, которое является хорошим проводником как тепла, так и электричества. Углерод, как и алмаз, является самым дорогим и блестящим из всех природных драгоценных камней и самым твердым из встречающихся в природе абразивов. Графит используется в качестве смазки. В микрокристаллическом и почти аморфном виде используется как черный пигмент, как адсорбент, как горючее, как наполнитель для каучука, а в смеси с глиной — как «грифель» карандашей. Поскольку он проводит электричество, но не плавится, графит также используется для электродов в электрических печах и сухих камерах, а также для изготовления тиглей, в которых плавятся металлы. Молекулы фуллерена перспективны в ряде приложений, включая материалы с высокой прочностью на растяжение, уникальные электронные устройства и устройства хранения энергии, а также безопасную герметизацию горючих газов, таких как водород. Q-углерод, который создается путем быстрого охлаждения образца элементарного углерода, температура которого была повышена до 4000 К (3727 °C [6740 °F]), тверже алмаза, и его можно использовать для изготовления алмазных структур (таких как в виде алмазных пленок и микроигл) внутри его матрицы.
Углерод, как и алмаз, является самым дорогим и блестящим из всех природных драгоценных камней и самым твердым из встречающихся в природе абразивов. Графит используется в качестве смазки. В микрокристаллическом и почти аморфном виде используется как черный пигмент, как адсорбент, как горючее, как наполнитель для каучука, а в смеси с глиной — как «грифель» карандашей. Поскольку он проводит электричество, но не плавится, графит также используется для электродов в электрических печах и сухих камерах, а также для изготовления тиглей, в которых плавятся металлы. Молекулы фуллерена перспективны в ряде приложений, включая материалы с высокой прочностью на растяжение, уникальные электронные устройства и устройства хранения энергии, а также безопасную герметизацию горючих газов, таких как водород. Q-углерод, который создается путем быстрого охлаждения образца элементарного углерода, температура которого была повышена до 4000 К (3727 °C [6740 °F]), тверже алмаза, и его можно использовать для изготовления алмазных структур (таких как в виде алмазных пленок и микроигл) внутри его матрицы. Элементарный углерод нетоксичен.
Элементарный углерод нетоксичен.
Каждая из «аморфных» форм углерода имеет свою специфику и, следовательно, имеет свои особенности применения. Все они являются продуктами окисления и других форм разложения органических соединений. Уголь и кокс, например, широко используются в качестве топлива. Древесный уголь используется в качестве абсорбирующего и фильтрующего агента, а также в качестве топлива, а когда-то широко использовался в качестве ингредиента пороха. (Угли представляют собой элементарный углерод, смешанный с различным количеством углеродных соединений. Кокс и древесный уголь представляют собой почти чистый углерод.) Помимо использования в производстве чернил и красок, технический углерод добавляется в резину, используемую в шинах, для улучшения ее износостойкости. Костяная сажа или древесный уголь животных может поглощать газы и красящие вещества из многих других материалов.
Углерод, элементарный или связанный, обычно определяют количественно путем преобразования в газообразный диоксид углерода, который затем может поглощаться другими химическими веществами с получением взвешиваемого продукта или раствора с кислотными свойствами, который можно титровать.
Производство элементарного углерода
До 1955 г. все алмазы добывались из природных месторождений, наиболее значительных на юге Африки, но встречающихся также в Бразилии, Венесуэле, Гайане и Сибири. Единственный известный источник в США, в Арканзасе, не имеет коммерческого значения; и Индия, которая когда-то была источником чистых алмазов, в настоящее время не является важным поставщиком. Первичным источником алмазов является мягкая голубоватая перидотическая порода, называемая кимберлитом (в честь знаменитого месторождения Кимберли, Южная Африка), обнаруженная в вулканических структурах, называемых трубками, но многие алмазы встречаются в аллювиальных отложениях, предположительно образовавшихся в результате выветривания первичных источников. Единичные находки по всему миру в регионах, где не указаны источники, не были редкостью.
Природные месторождения разрабатывают дроблением, гравитационной и флотационной сепарацией, а также удалением алмазов путем прилипания их к слою смазки на подходящем столе.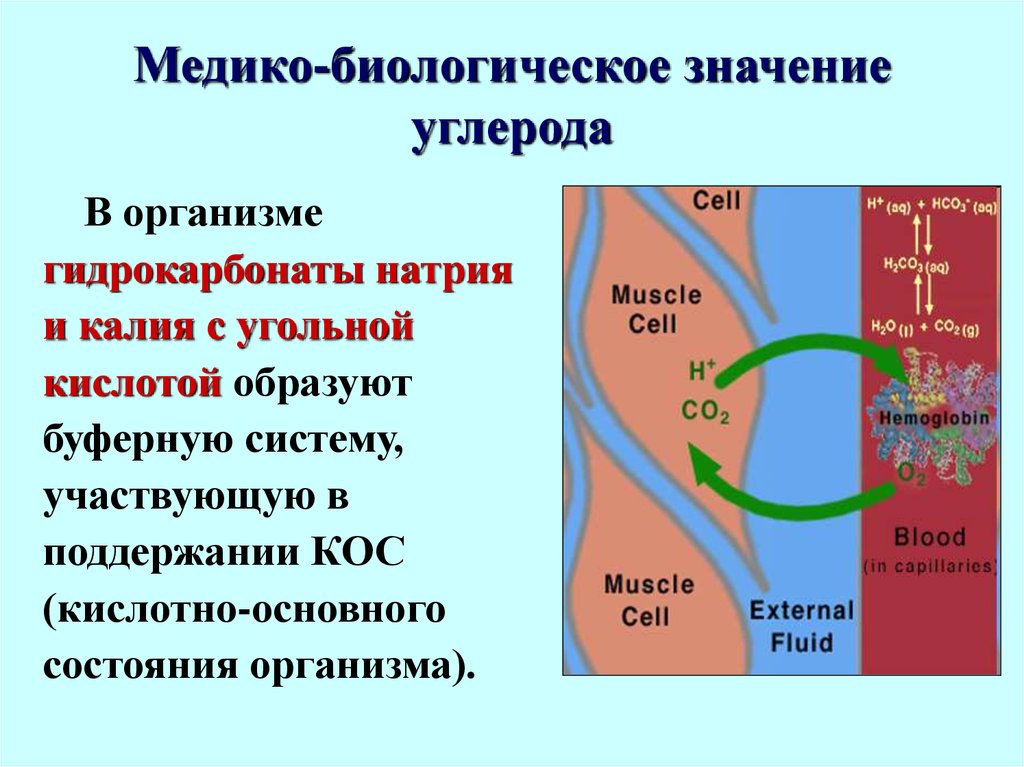 В результате получаются следующие продукты: (1) собственно алмаз — деформированные кубические кристаллические камни ювелирного качества, варьирующиеся от бесцветных до красных, розовых, голубых, зеленых или желтых; (2) борт — мельчайшие темные кристаллы абразивного, но не ювелирного качества; 3) баллас – беспорядочно ориентированные кристаллы абразивного качества; 4) маклеры — треугольные подушкообразные кристаллы, используемые в промышленности; 5) карбонадо – смешанные алмазно-графитовые кристаллиты, содержащие другие примеси.
В результате получаются следующие продукты: (1) собственно алмаз — деформированные кубические кристаллические камни ювелирного качества, варьирующиеся от бесцветных до красных, розовых, голубых, зеленых или желтых; (2) борт — мельчайшие темные кристаллы абразивного, но не ювелирного качества; 3) баллас – беспорядочно ориентированные кристаллы абразивного качества; 4) маклеры — треугольные подушкообразные кристаллы, используемые в промышленности; 5) карбонадо – смешанные алмазно-графитовые кристаллиты, содержащие другие примеси.
Успешное преобразование графита в алмаз в лаборатории было осуществлено в 1955 году. Процедура включала одновременное использование чрезвычайно высокого давления и температуры с железом в качестве растворителя или катализатора. Впоследствии железо заменили хромом, марганцем, кобальтом, никелем и танталом. Синтетические алмазы в настоящее время производятся в нескольких странах и все чаще используются вместо природных материалов в качестве промышленных абразивов.