Метионин — описание вещества, фармакология, применение, противопоказания, формула
Содержание
- Структурная формула
- Русское название
- Английское название
- Латинское название вещества Метионин
- Химическое название
- Брутто формула
- Фармакологическая группа вещества Метионин
- Нозологическая классификация
- Код CAS
- Фармакологическое действие
- Характеристика
- Фармакология
- Применение вещества Метионин
- Противопоказания
- Побочные действия вещества Метионин
- Передозировка
- Способ применения и дозы
- Торговые названия с действующим веществом Метионин
Структурная формула
Русское название
Метионин
Английское название
Methionine
Латинское название вещества Метионин
Methioninum (род. Methionini)
Methionini)
Химическое название
альфа-Амино-гамма-метилмеркаптомасляная кислота
Брутто формула
C5H11NO2S
Фармакологическая группа вещества Метионин
Белки и аминокислоты
Гепатопротекторы
Нозологическая классификация
Список кодов МКБ-10
- K76.0 Жировая дегенерация печени, не классифицированная в других рубриках
- K74 Фиброз и цирроз печени
- E46 Белково-энергетическая недостаточность неуточненная
- K70 Алкогольная болезнь печени
- K71 Токсическое поражение печени
Код CAS
63-68-3
Фармакологическое действие
Фармакологическое действие — восполняющее дефицит аминокислот, гепатопротективное, метаболическое.
Характеристика
Незаменимая аминокислота. Белый кристаллический порошок с характерным запахом серосодержащих соединений и слегка сладковатым вкусом. Мало растворим в воде.
Фармакология
Регулирует азотистый баланс. Содержит подвижную метильную группу и участвует в процессах метилирования, обеспечивающих синтез холина, адреналина, креатина и др. биологически важных соединений, обезвреживание токсичных продуктов, образование фосфолипидов. Тормозит отложение в печени нейтрального жира, оказывает липотропный эффект (удаление из печени избытка жира). Модулирует эффект гормонов и витаминов (B12, аскорбиновой и фолиевой кислот).
Применение вещества Метионин
Заболевания печени (цирроз, алкогольная гепатопатия, токсический гепатит), дистрофия, белковая недостаточность.
Противопоказания
Гиперчувствительность, вирусный гепатит.
Побочные действия вещества Метионин
Аллергические реакции, тошнота, рвота (вследствие неприятного запаха и вкуса).
Передозировка
Симптомы: снижение АД, тахикардия, дезориентация.
Лечение: симптоматическое.
Способ применения и дозы
Внутрь (за 0,5–1 ч до еды): взрослым — по 0,5–1,5 г, детям старше 6 лет — по 0,25–0,5 г 3–4 раза в день. Курс — 10–30 дней или по 10 дней с 10-дневными перерывами.
Торговые названия с действующим веществом Метионин
Сбросить фильтры
Лек. форма Все лек. формы субстанция-порошок таблетки, покрытые оболочкой таблетки, покрытые пленочной оболочкой
Дозировка Все дозировки 250 мг Без дозировки
Производитель Все производители АВВА РУС АО АВВА РУС ОАО Киевский витаминный завод ОАО Киевский витаминный завод ПАО Марбиофарм ОАО Озон ООО Полисинтез Фармстандарт-УфаВИТА Шицячжуан Шисин Амино Эсид Ко.
инструкция по применению, доставка на дом
Характеристики
| Зарегистрировано как | Лекарственное средство |
Описание
Состав Метионин 250 мг Вспомогательные вещества: метилцеллюлоза (метилцеллюлоза водорастворимая) — 2. 237 мг, целлюлоза микрокристаллическая — 47.559 мг, стеариновая кислота — 3.356 мг, магния стеарат — 3.356 мг, крахмал картофельный — 23.492 мг. Состав оболочки: гипромеллоза — 7.25 мг, полисорбат 80 — 2.207 мг, титана диоксид — 0.54 мг, краситель азорубин (E122) — 0.003 мг. Фармакологическое действие Незаменимая аминокислота, необходимая для поддержания роста и азотистого равновесия организма. Содержит метильную группу, которая участвует в процессе переметилирования и необходима для синтеза холина. За счет этого нормализует синтез фосфолипидов из жиров и уменьшает отложение в печени нейтрального жира. Участвует в обмене серосодержащих аминокислот, в синтезе эпинефрина, креатинина и других биологически активных веществ, активирует действие гормонов, витаминов (B12, аскорбиновой, фолиевой кислот), ферментов, белков, реакциях переметилирования, дезаминирования, декарбоксилирования. Необходим для дезинтоксикации ксенобиотиков. При атеросклерозе снижает концентрацию холестерина и повышает концентрацию фосфолипидов крови.
237 мг, целлюлоза микрокристаллическая — 47.559 мг, стеариновая кислота — 3.356 мг, магния стеарат — 3.356 мг, крахмал картофельный — 23.492 мг. Состав оболочки: гипромеллоза — 7.25 мг, полисорбат 80 — 2.207 мг, титана диоксид — 0.54 мг, краситель азорубин (E122) — 0.003 мг. Фармакологическое действие Незаменимая аминокислота, необходимая для поддержания роста и азотистого равновесия организма. Содержит метильную группу, которая участвует в процессе переметилирования и необходима для синтеза холина. За счет этого нормализует синтез фосфолипидов из жиров и уменьшает отложение в печени нейтрального жира. Участвует в обмене серосодержащих аминокислот, в синтезе эпинефрина, креатинина и других биологически активных веществ, активирует действие гормонов, витаминов (B12, аскорбиновой, фолиевой кислот), ферментов, белков, реакциях переметилирования, дезаминирования, декарбоксилирования. Необходим для дезинтоксикации ксенобиотиков. При атеросклерозе снижает концентрацию холестерина и повышает концентрацию фосфолипидов крови. Способ применения и дозы Взрослым — по 500 мг-1.5 г 3-4 раза/сут. Разовые дозы для детей в возрасте до 1 года — 100 мг, в возрасте 1-2 лет — 200 мг, в возрасте 3-4 лет — 250 мг, в возрасте 5-6 лет — 300 мг, в возрасте старше 7 лет — 500 мг . кратность приема — 3-4 раза/сут. Принимают за 1/2-1 ч до еды. Курс лечения — 10-30 дней или по 10 дней с 10-дневными перерывами. Меры предосторожности В период лечения возможно обострение псориаза. При феохромоцитоме пропранолол можно применять только после приема альфа-адреноблокатора. После продолжительного курса лечения пропранолол следует отменять постепенно, под наблюдением врача. На фоне лечения пропранололом следует избегать в/в введения верапамила , дилтиазема . За несколько дней перед проведением наркоза необходимо прекратить прием пропранолола или подобрать средство для наркоза с минимальным отрицательным инотропным действием. Влияние на способность к вождению автотранспорта и управлению механизмами У пациентов, деятельность которых требует повышенного внимания, вопрос о применении пропранолола амбулаторно следует решать только после оценки индивидуальной реакции пациента.
Способ применения и дозы Взрослым — по 500 мг-1.5 г 3-4 раза/сут. Разовые дозы для детей в возрасте до 1 года — 100 мг, в возрасте 1-2 лет — 200 мг, в возрасте 3-4 лет — 250 мг, в возрасте 5-6 лет — 300 мг, в возрасте старше 7 лет — 500 мг . кратность приема — 3-4 раза/сут. Принимают за 1/2-1 ч до еды. Курс лечения — 10-30 дней или по 10 дней с 10-дневными перерывами. Меры предосторожности В период лечения возможно обострение псориаза. При феохромоцитоме пропранолол можно применять только после приема альфа-адреноблокатора. После продолжительного курса лечения пропранолол следует отменять постепенно, под наблюдением врача. На фоне лечения пропранололом следует избегать в/в введения верапамила , дилтиазема . За несколько дней перед проведением наркоза необходимо прекратить прием пропранолола или подобрать средство для наркоза с минимальным отрицательным инотропным действием. Влияние на способность к вождению автотранспорта и управлению механизмами У пациентов, деятельность которых требует повышенного внимания, вопрос о применении пропранолола амбулаторно следует решать только после оценки индивидуальной реакции пациента. Побочное действие Возможно: аллергические реакции. В отдельных случаях: тошнота, рвота (вследствие неприятного запаха и вкуса). Особые указания С осторожностью применяют при почечной недостаточности (опасность нарастания гиперазотемии). При применении метионина у больных с атеросклерозом отмечено снижение содержания в крови холестерина и повышение уровня фосфолипидов. Следует назначать в балансе с другими аминокислотами. Несбалансированное применение метионина в больших дозах может оказать повреждающее действие на клетки печени и других органов. Применение при беременности и кормлении грудью Тип: Лекарственное средство Количество в упаковке, шт: 50 Срок годности: 60 мес Действующее вещество: Метионин (Methionine) Путь введения: Перорально Порядок отпуска: Без рецепта Форма выпуска: Без рецепта Условия хранения: В сухом месте, В защищенном от солнца помещении, Беречь от детей Максимальная допустимая температура хранения, °С: 25 Фармакологическая группа: A16AA Аминокислоты и их производные
Побочное действие Возможно: аллергические реакции. В отдельных случаях: тошнота, рвота (вследствие неприятного запаха и вкуса). Особые указания С осторожностью применяют при почечной недостаточности (опасность нарастания гиперазотемии). При применении метионина у больных с атеросклерозом отмечено снижение содержания в крови холестерина и повышение уровня фосфолипидов. Следует назначать в балансе с другими аминокислотами. Несбалансированное применение метионина в больших дозах может оказать повреждающее действие на клетки печени и других органов. Применение при беременности и кормлении грудью Тип: Лекарственное средство Количество в упаковке, шт: 50 Срок годности: 60 мес Действующее вещество: Метионин (Methionine) Путь введения: Перорально Порядок отпуска: Без рецепта Форма выпуска: Без рецепта Условия хранения: В сухом месте, В защищенном от солнца помещении, Беречь от детей Максимальная допустимая температура хранения, °С: 25 Фармакологическая группа: A16AA Аминокислоты и их производные
Действующие вещества
Метионин
Форма выпуска
Таблетки
Состав
Метионин 250 мг Вспомогательные вещества: метилцеллюлоза (метилцеллюлоза водорастворимая) — 2. 237 мг, целлюлоза микрокристаллическая — 47.559 мг, стеариновая кислота — 3.356 мг, магния стеарат — 3.356 мг, крахмал картофельный — 23.492 мг. Состав оболочки: гипромеллоза — 7.25 мг, полисорбат 80 — 2.207 мг, титана диоксид — 0.54 мг, краситель азорубин (E122) — 0.003 мг.
237 мг, целлюлоза микрокристаллическая — 47.559 мг, стеариновая кислота — 3.356 мг, магния стеарат — 3.356 мг, крахмал картофельный — 23.492 мг. Состав оболочки: гипромеллоза — 7.25 мг, полисорбат 80 — 2.207 мг, титана диоксид — 0.54 мг, краситель азорубин (E122) — 0.003 мг.
Фармакологический эффект
Незаменимая аминокислота, необходимая для поддержания роста и азотистого равновесия организма. Содержит метильную группу, которая участвует в процессе переметилирования и необходима для синтеза холина. За счет этого нормализует синтез фосфолипидов из жиров и уменьшает отложение в печени нейтрального жира. Участвует в обмене серосодержащих аминокислот, в синтезе эпинефрина, креатинина и других биологически активных веществ, активирует действие гормонов, витаминов (B12, аскорбиновой, фолиевой кислот), ферментов, белков, реакциях переметилирования, дезаминирования, декарбоксилирования. Необходим для дезинтоксикации ксенобиотиков. При атеросклерозе снижает концентрацию холестерина и повышает концентрацию фосфолипидов крови.
Показания
Заболевания печени, протекающие с жировой инфильтрацией гепатоцитов: токсический гепатит, гепатоз (в т.ч. алкогольный), цирроз, дистрофия печени . интоксикации. Профилактика токсических поражений печени мышьяком, хлороформом, бензолом, алкоголем. В составе комбинированной терапии: дефицит белка различного происхождения, атеросклероз, сахарный диабет.
Противопоказания
Повышенная чувствительность к метионину, тяжелая печеночная недостаточность, печеночная энцефалопатия, вирусный гепатит.
Способ применения и дозы
Взрослым — по 500 мг-1.5 г 3-4 раза/сут. Разовые дозы для детей в возрасте до 1 года — 100 мг, в возрасте 1-2 лет — 200 мг, в возрасте 3-4 лет — 250 мг, в возрасте 5-6 лет — 300 мг, в возрасте старше 7 лет — 500 мг . кратность приема — 3-4 раза/сут. Принимают за 1/2-1 ч до еды. Курс лечения — 10-30 дней или по 10 дней с 10-дневными перерывами.
Побочные действия
Возможно: аллергические реакции. В отдельных случаях: тошнота, рвота (вследствие неприятного запаха и вкуса).
В отдельных случаях: тошнота, рвота (вследствие неприятного запаха и вкуса).
Особые указания
Возможно: аллергические реакции. В отдельных случаях: тошнота, рвота (вследствие неприятного запаха и вкуса).
Добавка метионина влияет на метаболизм и снижает агрессивность опухоли в клетках рака печени
. 2020 16 ноября; 9 (11): 2491.
doi: 10.3390/cells9112491.
Фарида Триподи 1 , Беатрис Бадоне 1 , Марта Вескови 1 , Риккардо Миланези 1 , Симона Ноннис 2
3 , Элиза Маффиоли 2 , Марселла Бонаноми 1
4 , Даниэла Галио 4
5 , Габриэлла Тедески
Принадлежности
- 1 Факультет биотехнологии и биологических наук, Университет Милана-Бикокка, 20126 Милан, Италия.

- 2 DIMEVET-кафедра ветеринарной медицины Миланского университета, 20133 Милан, Италия.
- 3 CRC «Инновации для благополучия и окружающей среды (IWE)», Миланский университет, 20133 Милан, Италия.
- 4 SYSBIO.ISBE.IT, Центр системной биологии, 20126 Милан, Италия.
- 5 Институт молекулярной биовизуализации и физиологии (IBFM), Национальный исследовательский совет (CNR), Сеграте, 20090 Милан, Италия.
- PMID: 33207837
- PMCID: PMC7696226
- DOI:
10.
 3390/ячейки9112491
3390/ячейки9112491
Бесплатная статья ЧВК
Фарида Триподи и др. Клетки. .
Бесплатная статья ЧВК
. 2020 16 ноября; 9 (11): 2491.
дои: 10.3390/ячейки9112491.
Авторы
Фарида Триподи 1 , Беатрис Бадоне 1 , Марта Вескови 1 , Риккардо Миланези 1 , Симона Ноннис 2 3 , Элиза Маффиоли 2 , Марселла Бонаноми 1 4 , Даниэла Галио 4 5 , Габриэлла Тедески 2 3 , Паола Кокчетти 1
Принадлежности
- 1 Факультет биотехнологии и биологических наук, Университет Милана-Бикокка, 20126 Милан, Италия.

- 2 DIMEVET-кафедра ветеринарной медицины Миланского университета, 20133 Милан, Италия.
- 3 CRC «Инновации для благополучия и окружающей среды (IWE)», Миланский университет, 20133 Милан, Италия.
- 4 SYSBIO.ISBE.IT, Центр системной биологии, 20126 Милан, Италия.
- 5 Институт молекулярной биовизуализации и физиологии (IBFM), Национальный исследовательский совет (CNR), Сеграте, 2009 г.0 Милан, Италия.
- PMID: 33207837
- PMCID: PMC7696226
- DOI:
10.
 3390/ячейки9112491
3390/ячейки9112491
Абстрактный
Рак печени является одним из наиболее распространенных видов рака во всем мире с высокой смертностью. Метионин является незаменимой аминокислотой, необходимой для нормального развития и роста клеток, в основном метаболизируется в печени, и его роль в качестве противораковой добавки до сих пор остается спорной. Здесь мы оцениваем влияние добавок метионина на раковые клетки печени. Интегративный протеомный и метаболомный анализ указывает на перестройку центрального углеродного метаболизма с усилением цикла трикарбоновых кислот (TCA) и выработкой митохондриального аденозинтрифосфата (АТФ) в присутствии ингибирования высокого уровня метионина и AMP-активируемой протеинкиназы (AMPK). . Добавка метионина также снижает скорость роста клеток рака печени и вызывает активацию путей AMPK и mTOR. Интересно, что при высокой концентрации метионина ингибирование AMPK сильно ухудшает рост клеток, миграцию клеток и образование колоний, что указывает на основную роль AMPK в контроле фенотипов рака печени.
Ключевые слова: АМПК; ГЦК; цикл ТСА; рост; метаболомика; миграция; протеомика.
Заявление о конфликте интересов
Авторы заявляют об отсутствии конфликта интересов.
Цифры
Рисунок 1
Биоинформатический анализ протеомных…
Рисунок 1
Биоинформационный анализ протеомных данных клеток HepG2, выращенных в течение 48 ч…
фигура 1 Биоинформатический анализ протеомных данных клеток HepG2, выращенных в течение 48 часов (CTR), в присутствии соединения C (CTRCC), с высоким содержанием метионина (MET) и с высоким содержанием метионина и соединения C (METCC).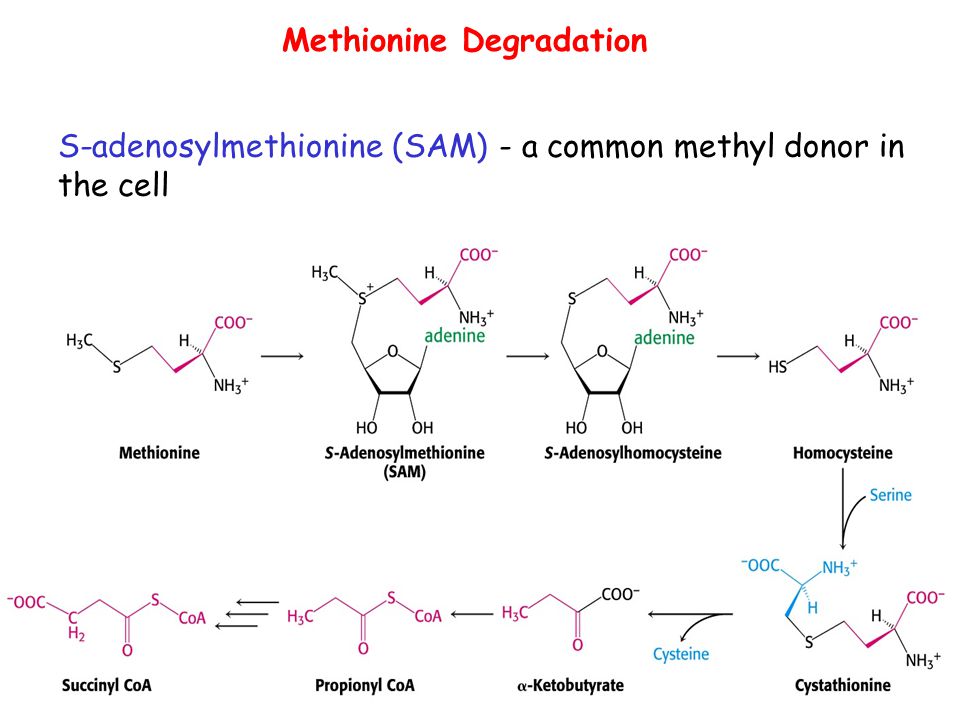 ( A ) Ingenuity ® Анализ путей (IPA), проведенный на 46 белках, общих для всех наборов данных, экспрессия которых статистически различается, показал, что 25 из 46 дифференциально экспрессируемых белков принадлежат к сети, классифицируемой как: рак , синтез белка, повреждение и восстановление РНК. Эти белки показаны пурпурным цветом среди всех белков, принадлежащих пути. О каждом белке сообщается с соответствующим символом IPA. ( B ) Анализ вышестоящего регулятора, основанный на предварительных знаниях об ожидаемых эффектах между регуляторами транскрипции и их генами-мишенями в IPA, показывает ядерный фактор 4 гепатоцитов (HNF4A) ( p — значение 0,001), который нацелен на 12/46 белков. дифференциально выражены. ( C ) Вулканические графики сравнения MET и CTR, METCC и MET, CTRCC и CTR. Зеленым цветом: активированы белки; красным цветом: белки подавлены; серым цветом: белки, которые статистически не отличаются (9 баллов по шкале Стьюдента).0173 t -тест p -значение = 0,05).
( A ) Ingenuity ® Анализ путей (IPA), проведенный на 46 белках, общих для всех наборов данных, экспрессия которых статистически различается, показал, что 25 из 46 дифференциально экспрессируемых белков принадлежат к сети, классифицируемой как: рак , синтез белка, повреждение и восстановление РНК. Эти белки показаны пурпурным цветом среди всех белков, принадлежащих пути. О каждом белке сообщается с соответствующим символом IPA. ( B ) Анализ вышестоящего регулятора, основанный на предварительных знаниях об ожидаемых эффектах между регуляторами транскрипции и их генами-мишенями в IPA, показывает ядерный фактор 4 гепатоцитов (HNF4A) ( p — значение 0,001), который нацелен на 12/46 белков. дифференциально выражены. ( C ) Вулканические графики сравнения MET и CTR, METCC и MET, CTRCC и CTR. Зеленым цветом: активированы белки; красным цветом: белки подавлены; серым цветом: белки, которые статистически не отличаются (9 баллов по шкале Стьюдента).0173 t -тест p -значение = 0,05).
Рисунок 2
Высокое содержание метионина и соединение C…
Рисунок 2
Высокое содержание метионина и соединение C вызывают протеомные изменения. (A–C) Функциональный анализ…
фигура 2 Высокое содержание метионина и соединение C вызывают протеомные изменения. (A-C) Функциональный анализ белков, дифференциально экспрессируемых при сравнении MET и CTR, METCC и MET, CTRCC и CTR. Белки считались дифференциально экспрессированными, если они присутствовали только в одном состоянии или демонстрировали значительные t — разность тестов (значение Стьюдента t -тест p = 0,05). ( A ) GO Биологические процессы увеличились в трех сравнениях ( B ) GO Биологические процессы уменьшились в трех сравнениях.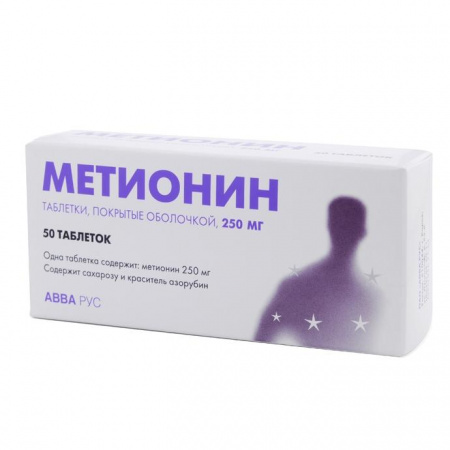 Функциональная группировка была основана на точном критерии Фишера p -значение ≤ 0,05 (т.е. -log10 ≥ 1,3) и не менее трех подсчетов. В каждом сравнении термины «увеличение» или «уменьшение» относятся к белкам, активность которых повышается или понижается при лечении.
Функциональная группировка была основана на точном критерии Фишера p -значение ≤ 0,05 (т.е. -log10 ≥ 1,3) и не менее трех подсчетов. В каждом сравнении термины «увеличение» или «уменьшение» относятся к белкам, активность которых повышается или понижается при лечении.
Рисунок 3
Биоинформатический анализ протеомных…
Рисунок 3
Биоинформатический анализ протеомных данных клеток HepG2, выращенных в течение 48 ч…
Рисунок 3 Биоинформатический анализ протеомных данных о клетках HepG2, выращенных в течение 48 часов (CTR), в присутствии соединения C (CTRCC), с высоким содержанием метионина (MET) и с высоким содержанием метионина и соединения C (METCC). Анализ проводили с помощью IPA белков, дифференциально экспрессируемых при сравнении MET с CTR, METCC с CTR и CTRCC с CTR.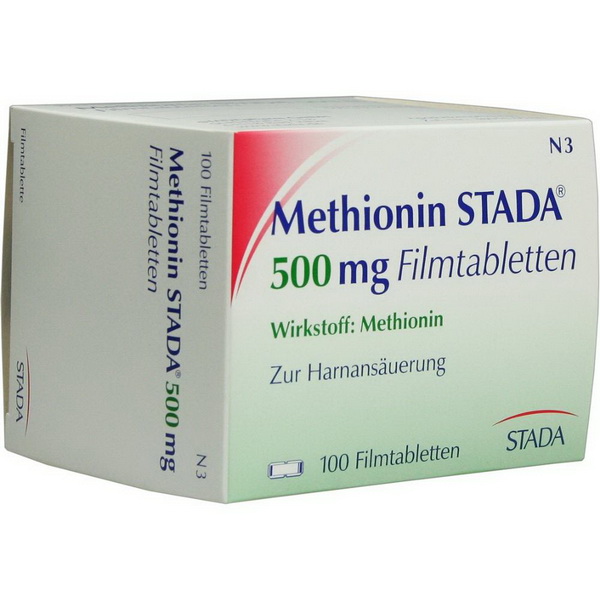 Белки считались дифференциально экспрессированными, если они присутствовали только в одном состоянии или демонстрировали значительные t -разность тестов ( t Стьюдента -тест p -значение 0,05). Функциональная группировка была основана на точном критерии Фишера p значение ≤ 0,05 и не менее трех подсчетов. Цветные столбцы являются визуальным представлением соответствующего значения –log p , сообщаемого в ряд.
Белки считались дифференциально экспрессированными, если они присутствовали только в одном состоянии или демонстрировали значительные t -разность тестов ( t Стьюдента -тест p -значение 0,05). Функциональная группировка была основана на точном критерии Фишера p значение ≤ 0,05 и не менее трех подсчетов. Цветные столбцы являются визуальным представлением соответствующего значения –log p , сообщаемого в ряд.
Рисунок 4
Высокое содержание метионина и соединение C…
Рисунок 4
Высокое содержание метионина и соединение C влияют на клеточный метаболизм. ( А , Б )…
Рисунок 4 Высокое содержание метионина и соединение C влияют на клеточный метаболизм. ( A , B ) HepG2 ( A ) и клетки Huh7 ( B ) выращивали в течение 48 часов в обычной среде или в присутствии высокого содержания метионина и/или соединения C. Среду из трех биологических повторов выращивали в течение 48 часов. собирают для измерения потребления глюкозы и глютамина, секреции лактата и глутамата. ( C – F ) Клетки HepG2 выращивали в течение 48 ч в обычной среде (CTR) или в присутствии высокого содержания метионина и/или соединения C. Метаболический анализ проводили с помощью ГХ/МС и ЖХ/МС на пяти биологических повторностях, каждая из которых проанализирована в техническом дубликате. ( C ) В этом анализе наиболее затронуты метаболические пути. Анализ метаболических путей проводили с помощью инструмента MetaboAnalyst 4.0. Метаболические пути представлены кружками. Интенсивность цвета (от белого к красному) и размер каждого круга отражают возрастающую статистическую значимость, основанную на p -значение [-log(P)] из анализа обогащения пути и значение воздействия пути, полученное из анализа топологии пути, соответственно.
( A , B ) HepG2 ( A ) и клетки Huh7 ( B ) выращивали в течение 48 часов в обычной среде или в присутствии высокого содержания метионина и/или соединения C. Среду из трех биологических повторов выращивали в течение 48 часов. собирают для измерения потребления глюкозы и глютамина, секреции лактата и глутамата. ( C – F ) Клетки HepG2 выращивали в течение 48 ч в обычной среде (CTR) или в присутствии высокого содержания метионина и/или соединения C. Метаболический анализ проводили с помощью ГХ/МС и ЖХ/МС на пяти биологических повторностях, каждая из которых проанализирована в техническом дубликате. ( C ) В этом анализе наиболее затронуты метаболические пути. Анализ метаболических путей проводили с помощью инструмента MetaboAnalyst 4.0. Метаболические пути представлены кружками. Интенсивность цвета (от белого к красному) и размер каждого круга отражают возрастающую статистическую значимость, основанную на p -значение [-log(P)] из анализа обогащения пути и значение воздействия пути, полученное из анализа топологии пути, соответственно..jpg) ( D – F ) Иерархические кластерные тепловые карты из одностороннего анализа ANOVA дифференциальных метаболитов, принадлежащих ( D ) метаболизму метионина и окислительно-восстановительного потенциала, ( E ) метаболизму аминокислот, ( F ) центральному углеродному метаболизму . Тепловые карты были получены с помощью инструмента MetaboAnalyst 4.0. Шкала цветового кода указывает нормализованное содержание метаболитов. ( G ) Гистограмма уровня метаболитов цикла ТСА в четырех состояниях в клетках HepG2, измеренная при метаболическом анализе. Уровень каждого метаболита в контроле был установлен равным 1. * p <0,05 по сравнению с контролем. ( H ) Анализ скорости аденозинтрифосфата (АТФ) морского конька в клетках HepG2 и Huh7, выращенных в течение 48 часов в обычной среде или в присутствии высокого содержания метионина и/или соединения C. * p < 0,05 для митоАТФ по сравнению с контроль, p <0,05 для гликоАТФ по сравнению с контролем.
( D – F ) Иерархические кластерные тепловые карты из одностороннего анализа ANOVA дифференциальных метаболитов, принадлежащих ( D ) метаболизму метионина и окислительно-восстановительного потенциала, ( E ) метаболизму аминокислот, ( F ) центральному углеродному метаболизму . Тепловые карты были получены с помощью инструмента MetaboAnalyst 4.0. Шкала цветового кода указывает нормализованное содержание метаболитов. ( G ) Гистограмма уровня метаболитов цикла ТСА в четырех состояниях в клетках HepG2, измеренная при метаболическом анализе. Уровень каждого метаболита в контроле был установлен равным 1. * p <0,05 по сравнению с контролем. ( H ) Анализ скорости аденозинтрифосфата (АТФ) морского конька в клетках HepG2 и Huh7, выращенных в течение 48 часов в обычной среде или в присутствии высокого содержания метионина и/или соединения C. * p < 0,05 для митоАТФ по сравнению с контроль, p <0,05 для гликоАТФ по сравнению с контролем.
Рисунок 4
Высокое содержание метионина и соединение C…
Рисунок 4
Высокое содержание метионина и соединение C влияют на клеточный метаболизм. ( А , Б )…
Рисунок 4 Высокое содержание метионина и соединение C влияют на клеточный метаболизм. ( 9Клетки 0167 A , B ) HepG2 ( A ) и Huh7 ( B ) выращивали в течение 48 ч в обычной среде или в присутствии высокого содержания метионина и/или соединения C. Среду собирали в трех биологических повторностях. для измерения потребления глюкозы и глютамина, секреции лактата и глутамата. ( C – F ) Клетки HepG2 выращивали в течение 48 часов в обычной среде (CTR) или в присутствии высокого содержания метионина и/или соединения C. Метаболический анализ проводили с помощью ГХ/МС и ЖХ/МС на пяти биологические повторы, каждый из которых проанализирован в техническом дубликате. ( C ) В этом анализе наиболее затронуты метаболические пути. Анализ метаболических путей проводили с помощью инструмента MetaboAnalyst 4.0. Метаболические пути представлены кружками. Интенсивность цвета (от белого к красному) и размер каждого круга отражают возрастающую статистическую значимость на основе p -значения [-log(P)] из анализа обогащения пути и значения воздействия пути, полученного из анализа топологии пути , соответственно. ( D – F ) Тепловые карты иерархической кластеризации из одностороннего анализа ANOVA дифференциальных метаболитов, принадлежащих ( D ) метиониновый и окислительно-восстановительный обмен, ( E ) метаболизм аминокислот, ( F ) центральный углеродный обмен. Тепловые карты были получены с помощью инструмента MetaboAnalyst 4.0. Шкала цветового кода указывает нормализованное содержание метаболитов.
Метаболический анализ проводили с помощью ГХ/МС и ЖХ/МС на пяти биологические повторы, каждый из которых проанализирован в техническом дубликате. ( C ) В этом анализе наиболее затронуты метаболические пути. Анализ метаболических путей проводили с помощью инструмента MetaboAnalyst 4.0. Метаболические пути представлены кружками. Интенсивность цвета (от белого к красному) и размер каждого круга отражают возрастающую статистическую значимость на основе p -значения [-log(P)] из анализа обогащения пути и значения воздействия пути, полученного из анализа топологии пути , соответственно. ( D – F ) Тепловые карты иерархической кластеризации из одностороннего анализа ANOVA дифференциальных метаболитов, принадлежащих ( D ) метиониновый и окислительно-восстановительный обмен, ( E ) метаболизм аминокислот, ( F ) центральный углеродный обмен. Тепловые карты были получены с помощью инструмента MetaboAnalyst 4.0. Шкала цветового кода указывает нормализованное содержание метаболитов. ( G ) Гистограмма уровня метаболитов цикла ТСА в четырех состояниях в клетках HepG2, измеренная при метаболическом анализе. Уровень каждого метаболита в контроле был установлен равным 1. * p <0,05 по сравнению с контролем. ( H ) Анализ скорости аденозинтрифосфата (АТФ) морского конька в клетках HepG2 и Huh7, выращенных в течение 48 ч в обычной среде или в присутствии высокого содержания метионина и/или соединения С. * p <0,05 для митоАТФ по сравнению с контролем , p <0,05 для гликоАТФ по сравнению с контролем.
( G ) Гистограмма уровня метаболитов цикла ТСА в четырех состояниях в клетках HepG2, измеренная при метаболическом анализе. Уровень каждого метаболита в контроле был установлен равным 1. * p <0,05 по сравнению с контролем. ( H ) Анализ скорости аденозинтрифосфата (АТФ) морского конька в клетках HepG2 и Huh7, выращенных в течение 48 ч в обычной среде или в присутствии высокого содержания метионина и/или соединения С. * p <0,05 для митоАТФ по сравнению с контролем , p <0,05 для гликоАТФ по сравнению с контролем.
Рисунок 5
Интеграция метаболомики и протеомики…
Рисунок 5
Интеграция метаболомного и протеомного анализа. ( A ) Метаболические и протеомные пути…
Рисунок 5 Интеграция анализа метаболомики и протеомики. ( A ) Метаболические и протеомные пути больше всего затрагиваются при MET по сравнению с CTR. ( B ) Метаболические и протеомные пути больше всего затронуты при CTRCC по сравнению с CTR. ( C ) Метаболические и протеомные пути больше всего затронуты при METCC по сравнению с CTR. Диаграммы рассеяния показывают сводку совместных доказательств из анализа обогащения ( p -значения) и анализ топологии (воздействие пути). Размер и цвет точек (от белого до красного) пропорциональны количеству генов и соединений, присутствующих в пути. ( E ) Список 10 наиболее значимых путей в каждом из трех сравнений. ( E ) Диаграмма рассеивания общих путей среди списка, показанного в ( D ).
( A ) Метаболические и протеомные пути больше всего затрагиваются при MET по сравнению с CTR. ( B ) Метаболические и протеомные пути больше всего затронуты при CTRCC по сравнению с CTR. ( C ) Метаболические и протеомные пути больше всего затронуты при METCC по сравнению с CTR. Диаграммы рассеяния показывают сводку совместных доказательств из анализа обогащения ( p -значения) и анализ топологии (воздействие пути). Размер и цвет точек (от белого до красного) пропорциональны количеству генов и соединений, присутствующих в пути. ( E ) Список 10 наиболее значимых путей в каждом из трех сравнений. ( E ) Диаграмма рассеивания общих путей среди списка, показанного в ( D ).
Рисунок 6
Высокое содержание метионина активирует АМК-активируемый белок…
Рисунок 6
Высокое содержание метионина активирует AMK-активируемую протеинкиназу (AMPK), пути mTOR и Akt. ( А…
( А…
Высокое содержание метионина активирует AMK-активируемую протеинкиназу (AMPK), пути mTOR и Akt. ( A ) HepG2 обрабатывали метионином в течение 24 часов, и состояние активации AMPK оценивали с помощью Вестерн-анализа с использованием антитела pT172-AMPK (против pT172 в петле активации) и с использованием анти-pS79-Антитело Acc1 (против сайта-мишени AMPK на Acc1). Общее антитело против AMPK и антитело против винкулина использовали в качестве контролей. ( B ) Клетки HepG2 и Huh7 помещали в контрольную среду и к культурам добавляли 1,5 г/л метионина в момент времени 0. Образцы собирали в указанные моменты времени для оценки активации AMPK с использованием антитела против pT172-AMPK и антитело против pS79-Acc1. Общее антитело к AMPK и антитело к тубулину использовали в качестве контролей. ( С ) Клетки HepG2 и Huh7 выдерживали в течение 48 ч в отсутствие или в присутствии соединения C. Затем к культурам добавляли 1,5 г/л метионина и в указанные моменты времени собирали образцы для оценки активации mTOR с использованием анти-pS6K. антитело и активация Akt с использованием антитела против pS473-Akt. Общее антитело к Akt и антитело к тубулину использовали в качестве контроля.
Затем к культурам добавляли 1,5 г/л метионина и в указанные моменты времени собирали образцы для оценки активации mTOR с использованием анти-pS6K. антитело и активация Akt с использованием антитела против pS473-Akt. Общее антитело к Akt и антитело к тубулину использовали в качестве контроля.
Рисунок 7
Высокое содержание метионина и соединение C…
Рисунок 7
Высокое содержание метионина и соединение C ингибируют фенотипы рака. ( А , Б )…
Рисунок 7 Высокое содержание метионина и соединение C ингибируют фенотипы рака. ( A , B ) Рост клеток ( A ) HepG2 и ( B ) Huh7 отслеживали до 72 часов в обычной среде (CTR) или в присутствии 1,5 г/л метионина (MET) и /или соединение C для получения частичной инактивации AMPK (2 мкМ соединения C для HepG2 и 1,5 мкМ для Huh7). Опыты проводили не менее чем в трехкратной повторности. ( C , D ) HepG2 или Huh7 выращивали в течение 24 ч в обычной среде (CTR) или в присутствии высокого содержания метионина и/или соединения C. Затем их голодали в течение 24 ч в той же среде без сыворотки и миграцию оценивали с помощью трансвелл-анализа в течение 24 часов. ( E , F ) Анализ образования колоний HepG2 или Huh7, выращенных в обычной среде или в присутствии высокого содержания метионина и/или соединения C. Эксперименты проводили в трех повторностях. * р < 0,05.
Опыты проводили не менее чем в трехкратной повторности. ( C , D ) HepG2 или Huh7 выращивали в течение 24 ч в обычной среде (CTR) или в присутствии высокого содержания метионина и/или соединения C. Затем их голодали в течение 24 ч в той же среде без сыворотки и миграцию оценивали с помощью трансвелл-анализа в течение 24 часов. ( E , F ) Анализ образования колоний HepG2 или Huh7, выращенных в обычной среде или в присутствии высокого содержания метионина и/или соединения C. Эксперименты проводили в трех повторностях. * р < 0,05.
Рисунок 8
Эффект высокого содержания метионина…
Рисунок 8
Эффект высокого содержания метионина и ингибирования AMPK специфичен для рака печени…
Рисунок 8 Эффект ингибирования высокого содержания метионина и AMPK специфичен для клеток рака печени. ( A , B ) Нокдаун гена AMPKα/α’ в клетках HepG2 и Huh7 был достигнут с помощью siRNA. ( A ) Уровень эндогенного белка AMPKα/α’ определяли с помощью иммуноблота с использованием суммарных антител против AMPK. антитубулиновое антитело использовали в качестве контроля загрузки. ( B ) Рост клеток HepG2 и Huh7, трансфицированных siCNT или siAMPKα/α’, отслеживали в течение 72 ч в обычной среде (CTR) или в присутствии 1,5 г/л метионина (MET). Рост клеток выражают как отношение к росту в контрольной среде. * p < 0,05 по сравнению с клетками siCNT. ( C ) Рост клеток колоректального рака SW480, A549клетки рака легкого и клетки рака молочной железы MCF7 отслеживали до 72 часов в обычной среде (CTR) или в присутствии 1,5 г/л метионина (MET) и/или 2 мкМ соединения C. Рост клеток выражали как отношение рост в контрольной среде. ( D ) Анализ образования колоний клеток SW480, A549 и MCF7, выращенных в обычной среде (CTR) или в присутствии высокого содержания метионина и/или 2 мкМ соединения C.
( A , B ) Нокдаун гена AMPKα/α’ в клетках HepG2 и Huh7 был достигнут с помощью siRNA. ( A ) Уровень эндогенного белка AMPKα/α’ определяли с помощью иммуноблота с использованием суммарных антител против AMPK. антитубулиновое антитело использовали в качестве контроля загрузки. ( B ) Рост клеток HepG2 и Huh7, трансфицированных siCNT или siAMPKα/α’, отслеживали в течение 72 ч в обычной среде (CTR) или в присутствии 1,5 г/л метионина (MET). Рост клеток выражают как отношение к росту в контрольной среде. * p < 0,05 по сравнению с клетками siCNT. ( C ) Рост клеток колоректального рака SW480, A549клетки рака легкого и клетки рака молочной железы MCF7 отслеживали до 72 часов в обычной среде (CTR) или в присутствии 1,5 г/л метионина (MET) и/или 2 мкМ соединения C. Рост клеток выражали как отношение рост в контрольной среде. ( D ) Анализ образования колоний клеток SW480, A549 и MCF7, выращенных в обычной среде (CTR) или в присутствии высокого содержания метионина и/или 2 мкМ соединения C.
См. это изображение и информацию об авторских правах в PMC
Похожие статьи
Амиды 2-арилтиазолидин-4-карбоновой кислоты (ATCAA) нацелены на двойные пути в раковых клетках: пути 5′-AMP-активируемой протеинкиназы (AMPK)/mTOR и пути PI3K/Akt/mTOR.
Li CM, Narayanan R, Lu Y, Hurh E, Coss CC, Barrett CM, Miller DD, Dalton JT. Ли К.М. и соавт. Int J Oncol. 2010 окт; 37 (4): 1023-30. Int J Oncol. 2010. PMID: 20811725
SR4 разобщает митохондриальное окислительное фосфорилирование, модулирует сигнализацию AMP-зависимой киназы (AMPK)-мишени рапамицина (mTOR) млекопитающих и ингибирует пролиферацию клеток гепатокарциномы HepG2.
Фигарола Дж.Л., Сингхал Дж., Томпкинс Дж.Д., Роджерс Г.В., Уорден С.
 , Хорн Д., Риггс А.Д., Авасти С., Сингхал С.С.
Фигарола Дж.Л. и соавт.
Дж. Биол. Хим. 2015 18 декабря; 290(51):30321-41. doi: 10.1074/jbc.M115.686352. Epub 2015 3 ноября.
Дж. Биол. Хим. 2015.
PMID: 26534958
Бесплатная статья ЧВК.
, Хорн Д., Риггс А.Д., Авасти С., Сингхал С.С.
Фигарола Дж.Л. и соавт.
Дж. Биол. Хим. 2015 18 декабря; 290(51):30321-41. doi: 10.1074/jbc.M115.686352. Epub 2015 3 ноября.
Дж. Биол. Хим. 2015.
PMID: 26534958
Бесплатная статья ЧВК.Сорафениб убивает раковые клетки печени, нарушая SCD1-опосредованный синтез мононенасыщенных жирных кислот через сигнальный путь ATP-AMPK-mTOR-SREBP1.
Лю Г., Куанг С., Цао Р., Ван Дж., Пэн К., Сунь К. Лю Г и др. FASEB J. 2019 Sep;33(9):10089-10103. doi: 10.1096/fj.201802619RR. Epub 2019 14 июня. ФАСЭБ Дж. 2019. PMID: 31199678
Изокверцитрин индуцирует апоптоз и аутофагию в клетках гепатоцеллюлярной карциномы через сигнальный путь AMPK/mTOR/p70S6K.
Шуй Л.
 , Ван В., Се М., Е Б., Ли Х., Лю Ю., Чжэн М.
Шуи Л. и др.
Старение (Олбани, штат Нью-Йорк). 2020 29 ноября; 12 (23): 24318-24332. doi: 10.18632/aging.202237. Epub 2020 29 ноября.
Старение (Олбани, штат Нью-Йорк). 2020.
PMID: 33260158
Бесплатная статья ЧВК.
, Ван В., Се М., Е Б., Ли Х., Лю Ю., Чжэн М.
Шуи Л. и др.
Старение (Олбани, штат Нью-Йорк). 2020 29 ноября; 12 (23): 24318-24332. doi: 10.18632/aging.202237. Epub 2020 29 ноября.
Старение (Олбани, штат Нью-Йорк). 2020.
PMID: 33260158
Бесплатная статья ЧВК.Ингибирование активности GSK-3β подавляет злокачественный фенотип ГЦК путем ингибирования гликолиза посредством активации передачи сигналов AMPK/mTOR.
Фанг Г., Чжан П., Лю Дж., Чжан С., Чжу С., Ли Р., Ван Х. Фанг Г. и др. Рак Летт. 2019 28 октября; 463: 11-26. doi: 10.1016/j.canlet.2019.08.003. Epub 2019 9 августа. Рак Летт. 2019. PMID: 31404613
Посмотреть все похожие статьи
Цитируется
Добавление питательных веществ-доноров метила к диете с высоким содержанием жиров и сахарозы во время беременности и лактации нормализует уровень циркулирующего 25-дигидроксихолекальциферола и облегчает воспаление у потомства.

Теох С.М., Купер А., Рентерия К.М., Лейн М., Чжу Дж., Кох Г.Ю. Тео С.М. и соавт. Метаболиты. 2022 12 декабря; 12 (12): 1252. дои: 10.3390/метабо12121252. Метаболиты. 2022. PMID: 36557290 Бесплатная статья ЧВК.
Аминокислотный профиль в ткани и сыворотке крови больных раком печени.
Лю Д.Х., Вэнь Г.М., Сонг С.Л., Цзи Л.Дж., Ся П. Лю Д.Х. и др. Open Med (Войны). 2022 18 ноября; 17 (1): 1797-1802. doi: 10.1515/med-2022-0589. Электронная коллекция 2022. Open Med (Войны). 2022. PMID: 36447523 Бесплатная статья ЧВК.
L-метионин может модулировать сборку SARS-CoV-2, вмешиваясь в механизм РНК-полимеразы.
Бенавидес М.А. Бенавидес М.А. Мед Гипотезы. 2022 Апр; 161:110798.
 doi: 10.1016/j.mehy.2022.110798. Epub 2022 14 февраля.
Мед Гипотезы. 2022.
PMID: 35185264
Бесплатная статья ЧВК.
doi: 10.1016/j.mehy.2022.110798. Epub 2022 14 февраля.
Мед Гипотезы. 2022.
PMID: 35185264
Бесплатная статья ЧВК.Выявление прогностических факторов риска синаптоянина 2 и его основных путей возмущений при гепатоцеллюлярной карциноме.
Чжан Р., Мо В.Дж., Хуан Л.С., Чен Д.Т., Ву В.З., Хе В.Ю., Фэн З.Б. Чжан Р. и др. Биоинженерия. 2021 Декабрь; 12 (1): 855-874. дои: 10.1080/21655979.2021.18
. Биоинженерия. 2021. PMID: 33641617 Бесплатная статья ЧВК.
использованная литература
- Кумари Р., Саху М.К., Трипати А., Утансингх К., Бехера М. Лечение гепатоцеллюлярной карциномы: препятствия, достижения и перспективы. Онкол. печени. 2018;5:HEP08. doi: 10.2217/hep-2018-0002. — DOI — ЧВК — пабмед
- Хе Л.
 , Тянь Д.-А., Ли П.-Ю., Хе Х.-Х. Мышиные модели рака печени: прогресс и рекомендации. Онкотаргет. 2015;6:23306–23322. doi: 10.18632/oncotarget.4202.
—
DOI
—
ЧВК
—
пабмед
, Тянь Д.-А., Ли П.-Ю., Хе Х.-Х. Мышиные модели рака печени: прогресс и рекомендации. Онкотаргет. 2015;6:23306–23322. doi: 10.18632/oncotarget.4202.
—
DOI
—
ЧВК
—
пабмед
- Хе Л.
- Рот Г.С., Декаенс Т. Иммунотолерантность печени и гепатоцеллюлярная карцинома: патофизиологические механизмы и терапевтические перспективы. Евро. Дж. Рак. 2017; 87: 101–112. doi: 10.1016/j.ejca.2017.10.010. — DOI — пабмед
- Rimassa L.

- Rimassa L.

 3390/ячейки9112491
3390/ячейки9112491
 3390/ячейки9112491
3390/ячейки9112491 , Хорн Д., Риггс А.Д., Авасти С., Сингхал С.С.
Фигарола Дж.Л. и соавт.
Дж. Биол. Хим. 2015 18 декабря; 290(51):30321-41. doi: 10.1074/jbc.M115.686352. Epub 2015 3 ноября.
Дж. Биол. Хим. 2015.
PMID: 26534958
Бесплатная статья ЧВК.
, Хорн Д., Риггс А.Д., Авасти С., Сингхал С.С.
Фигарола Дж.Л. и соавт.
Дж. Биол. Хим. 2015 18 декабря; 290(51):30321-41. doi: 10.1074/jbc.M115.686352. Epub 2015 3 ноября.
Дж. Биол. Хим. 2015.
PMID: 26534958
Бесплатная статья ЧВК. , Ван В., Се М., Е Б., Ли Х., Лю Ю., Чжэн М.
Шуи Л. и др.
Старение (Олбани, штат Нью-Йорк). 2020 29 ноября; 12 (23): 24318-24332. doi: 10.18632/aging.202237. Epub 2020 29 ноября.
Старение (Олбани, штат Нью-Йорк). 2020.
PMID: 33260158
Бесплатная статья ЧВК.
, Ван В., Се М., Е Б., Ли Х., Лю Ю., Чжэн М.
Шуи Л. и др.
Старение (Олбани, штат Нью-Йорк). 2020 29 ноября; 12 (23): 24318-24332. doi: 10.18632/aging.202237. Epub 2020 29 ноября.
Старение (Олбани, штат Нью-Йорк). 2020.
PMID: 33260158
Бесплатная статья ЧВК.
 doi: 10.1016/j.mehy.2022.110798. Epub 2022 14 февраля.
Мед Гипотезы. 2022.
PMID: 35185264
Бесплатная статья ЧВК.
doi: 10.1016/j.mehy.2022.110798. Epub 2022 14 февраля.
Мед Гипотезы. 2022.
PMID: 35185264
Бесплатная статья ЧВК. , Тянь Д.-А., Ли П.-Ю., Хе Х.-Х. Мышиные модели рака печени: прогресс и рекомендации. Онкотаргет. 2015;6:23306–23322. doi: 10.18632/oncotarget.4202.
—
DOI
—
ЧВК
—
пабмед
, Тянь Д.-А., Ли П.-Ю., Хе Х.-Х. Мышиные модели рака печени: прогресс и рекомендации. Онкотаргет. 2015;6:23306–23322. doi: 10.18632/oncotarget.4202.
—
DOI
—
ЧВК
—
пабмед