Соотношение между содержанием кортизола и уровнем свободнорадикального окисления у лиц с героиновой наркоманией с учетом гендерных различий
Соотношение между содержанием кортизола и уровнем свободнорадикального окисления у лиц с героиновой наркоманией с учетом гендерных различий
Сайт издательства «Медиа Сфера»
содержит материалы, предназначенные исключительно для работников здравоохранения. Закрывая это сообщение, Вы подтверждаете, что являетесь дипломированным медицинским работником или студентом медицинского образовательного учреждения.
Шатырко М.А.
ГБУЗ «Челябинская областная клиническая наркологическая больница», Челябинск
Изаровский Б.В.
ГБУЗ «Челябинская областная клиническая наркологическая больница», Челябинск
Голодный С.В.
ГБОУ ВПО «Южно-Уральский государственный медицинский университет» Минздрава РФ, Челябинск
Козочкин Д. А.
А.
ГБОУ ВПО «Южно-Уральский государственный медицинский университет» Минздрава РФ, Челябинск
Цейликман В.Э.
ГБОУ ВПО «Южно-Уральский государственный медицинский университет» Минздрава РФ, Челябинск
Соотношение между содержанием кортизола и уровнем свободнорадикального окисления у лиц с героиновой наркоманией с учетом гендерных различий
Авторы:
Шатырко М.А., Изаровский Б.В., Голодный С.В., Козочкин Д.А., Цейликман В.Э.
Подробнее об авторах
Журнал: Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. 2015;115(4‑2): 69‑72
DOI: 10.17116/jnevro20151154269-72
Как цитировать:
Шатырко М.А., Изаровский Б.В., Голодный С.В., Козочкин Д.А., Цейликман В.Э. Соотношение между содержанием кортизола и уровнем свободнорадикального окисления у лиц с героиновой наркоманией с учетом гендерных различий.
Shatyrko MA, Isarovskyi BV, Golodnii SV, Kozochkin DA, Tseilikman VE. The correlation between the levels of cortisol and free radical oxidation in patients with heroin addiction depending on gender differences. Zhurnal Nevrologii i Psikhiatrii imeni S.S. Korsakova. 2015;115(4‑2):69‑72. (In Russ.)
https://doi.org/10.17116/jnevro20151154269-72
Читать метаданные
Цель исследования — установление гендерных особенностей соотношения между содержанием кортизола молекулярных продуктов перекисного окисления липидов (ПОЛ) и карбонилирования белков при героиновой наркомании. Материал и методы. Обследовали 82 пациента, 49 мужчин и 33 женщины, с героиновой зависимостью. Для определения перечисленных показателей использовали соответствующие биохимические методы и статистическую обработку результатов. Результаты и заключение.
Ключевые слова:
героиновая наркомания
кортизол
перекисное окисление липидов
карбонилирование белков
Авторы:
Шатырко М.А.
ГБУЗ «Челябинская областная клиническая наркологическая больница», Челябинск
Изаровский Б.В.
ГБУЗ «Челябинская областная клиническая наркологическая больница», Челябинск
Голодный С.В.
ГБОУ ВПО «Южно-Уральский государственный медицинский университет» Минздрава РФ, Челябинск
Козочкин Д.А.
ГБОУ ВПО «Южно-Уральский государственный медицинский университет» Минздрава РФ, Челябинск
Цейликман В.Э.
ГБОУ ВПО «Южно-Уральский государственный медицинский университет» Минздрава РФ, Челябинск
Закрыть метаданные
В последнее десятилетие отмечено увеличение распространенности героиновой наркомании [1], а также наличие гендерных различий в ее клинических проявлениях [2]. Так, имеются данные о том, что у больных женского пола быстрее формируется систематический прием опиоидов, а ремиссии наступают значительно реже. В связи с этим уместно отметить, что потребление женщинами психоактивных веществ часто сопряжено с ранее пережитыми психотравмирующими событиями. У лиц, зависимых от психоактивных веществ, переживаемые стрессы сопряжены с активацией гипоталамо-гипофизарно-надпочечниковой системы (ГГНС), что сопровождается повышенным уровнем кортизола [3]. Глюкокортикоиды являются гормонами долговременного характера [4]. Поэтому они могут быть вовлечены в формирование характерных для наркотической зависимости стойких психосоматических нарушений. Однако низкий уровень глюкокортикоидов также может быть фоном, способствующим развитию характерных для наркомании поведенческих расстройств. В частности, среди пациентов с синдром посттравматического стрессорного расстройства встречаются зависимые от наркотиков лица с низким содержанием кортизола в крови [5]. На молекулярном уровне вызванные злоупотреблениями наркотиков нарушения ассоциируются с изменениями свободнорадикального окисления [6].
Так, имеются данные о том, что у больных женского пола быстрее формируется систематический прием опиоидов, а ремиссии наступают значительно реже. В связи с этим уместно отметить, что потребление женщинами психоактивных веществ часто сопряжено с ранее пережитыми психотравмирующими событиями. У лиц, зависимых от психоактивных веществ, переживаемые стрессы сопряжены с активацией гипоталамо-гипофизарно-надпочечниковой системы (ГГНС), что сопровождается повышенным уровнем кортизола [3]. Глюкокортикоиды являются гормонами долговременного характера [4]. Поэтому они могут быть вовлечены в формирование характерных для наркотической зависимости стойких психосоматических нарушений. Однако низкий уровень глюкокортикоидов также может быть фоном, способствующим развитию характерных для наркомании поведенческих расстройств. В частности, среди пациентов с синдром посттравматического стрессорного расстройства встречаются зависимые от наркотиков лица с низким содержанием кортизола в крови [5]. На молекулярном уровне вызванные злоупотреблениями наркотиков нарушения ассоциируются с изменениями свободнорадикального окисления [6].
Цель настоящего исследования — установление гендерных особенностей соотношения между содержанием кортизола, молекулярных продуктов ПОЛ и карбонилирования белков при героиновой наркомании.
Материал и методы
На базе Челябинской областной клинической наркологической больницы проведено проспективное рандомизированное двойное слепое обследование 82 пациентов обоего пола, страдающих наркотической зависимостью (героиновая наркомания).
Исследуемую выборку составили 49 мужчин и 33 женщины. Возраст обследуемых был от 18 до 45 лет.
В сыворотке крови содержание кортизола определяли флуориметрическим методом [6]. Содержание молекулярных продуктов ПОЛ определяли по методике И.А. Волчегорского и соавт. [8]. Данный методический подход основан на феномене перегруппировки двойных связей в диеновые коньюгаты при переокислении полиненасыщенных жирных кислот, сопровождающейся появлением максимума поглощения при 230—238 нм, что позволяет судить о содержании гидроперекисей в липидном экстракте по величине его оптической плотности при этих длинах волн. При этом содержание диеновых конъюгатов (первичные продукты ПОЛ) рассчитывалось как окислительный индекс в виде соотношения оптической плотности при длине волны 232 нм к оптической плотности при длине волны 220 нм (Е232/Е220). Содержание кетодиенов и сопряженных триенов (вторичные продукты ПОЛ) рассчитывалось по соотношению оптической плотности при длине волны 278 нм к оптической плотности при длине волны 220 нм (Е278/Е220). Содержание карбонилированных белков определяли по методике Е.
Для определения статистически значимых различий между двумя сравниваемыми группами использовали критерий Манна—Уитни (U). Различия считали значимыми при р≤0,05. Статистические взаимосвязи изучали при помощи непараметрического корреляционного анализа, выполняя расчет коэффициентов корреляции рангов по Спирмену (Rs) и Кенделлу (rk). Все математические расчеты выполнены с использованием персонального компьютера в среде Windows с помощью пакета прикладных программ Statistica for Windows, версия 6.
Результаты и обсуждение
Героиновая зависимость сопровождается активацией ГГНС. В нашей работе это проявлялось повышением уровня кортизола в крови как по выборке в целом, так и отдельно у мужчин и женщин. При этом у них отмечались одинаковые темпы прироста кортизола.
Развитие гиперкортикоидного состояния сопровождалось активацией окисления белков при неизменном уровне липопероксидации. Установлено увеличение содержания продуктов окислительной модификации белка, проявлявшееся в увеличении уровня кислых и нейтральных кетондинитрофенилгидразонов, а также альдегиддинитрофенилгидразонов. Синхронный прирост содержания уровня кортизола и карбонилированных белков наблюдался как у мужчин, так и у женщин, т. е. в этом отношении не было гендерных различий. В то же время прирост уровня карбонилированных белков был более выражен у мужчин.
При использовании кластерного анализа общую выборку пациентов удалось разделить на два кластера по уровню кортизола (табл. 1). Кластер 1 содержит пациентов с относительно высоким уровнем кортизола, а кластер 2 — с относительно низким. Сопоставляя изменения уровня кортизола в крови в исследуемых группах с уровнем окислительной модификации белка, следует обратить внимание на то, что наиболее высокому уровню кортизола соответствует наиболее высокое усиление окислительной модификации белка (карбонилированные белки), а наименее выраженному увеличению уровня кортизола соответствует наименее выраженная окислительная модификация белка. Эта закономерность подтверждается корреляционным анализом.
1). Кластер 1 содержит пациентов с относительно высоким уровнем кортизола, а кластер 2 — с относительно низким. Сопоставляя изменения уровня кортизола в крови в исследуемых группах с уровнем окислительной модификации белка, следует обратить внимание на то, что наиболее высокому уровню кортизола соответствует наиболее высокое усиление окислительной модификации белка (карбонилированные белки), а наименее выраженному увеличению уровня кортизола соответствует наименее выраженная окислительная модификация белка. Эта закономерность подтверждается корреляционным анализом.
Таблица 1. Изменения содержания карбонилированных белков в крови в зависимости от уровня кортизолемии при героиновой наркомании Примечание. Здесь и в табл. 2: ААдфг — алифатические альдегид-динитрофенилгидразоны; АКдфг (н) — алифатические кетондинитрофенилгидразоны нейтрального характера; АКдфг (о) — алифатические кетондинитрофенилгидразоны основного характера; * — статистически значимые отличия от соответствующих показателей контрольной группы; ** — статистически значимые различия между кластерами.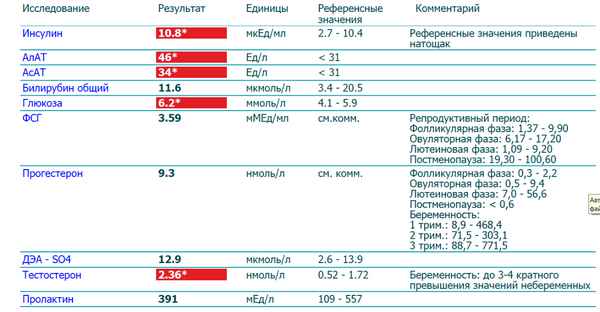
У пациентов с наркотической зависимостью обнаружена обратная корреляционная зависимость между уровнем кортизола и содержанием карбонилированных белков (rs= –0,62, p=0,014). Причем у пациентов кластера 1 с относительно высоким содержанием кортизола в крови коэффициент корреляции был выше (rs= –0,721, p=0,009), а у пациентов кластера 2 и в контрольной группе данная корреляционная зависимость не обнаруживалась. По данным кластерного анализа аналогичные изменения обнаружены для гептан-растворимых кетодиенов и сопряженных триенов. Это проявлялось в том, что наиболее высокому уровню кортизола соответствует наиболее высокое повышение содержания этой категории продуктов ПОЛ.
У мужчин кластер 1 с относительно высоким содержанием кортизола в крови (табл. 2) характеризовался более низким уровнем карбонилированных белков по сравнению с кластером 2 с относительно низким содержанием кортизола. При этом содержание алифатических кетондинитрофенилгидразонов нейтрального характера в кластере 2 было в 2,5 раза выше, чем в кластере 1. Аналогичная закономерность наблюдалась для кетондинитрофенилгидразонов основного характера, а также для альдегиднитрофенилгидразонов. При этом между кластером 1 и 2 отсутствовали статистически значимые различия по содержанию молекулярных продуктов ПОЛ. У женщин отсутствовали статистически значимые различия между кластерами с высоким и низким содержанием кортизола как по содержанию карбонилированных белков, так и по содержанию молекулярных продуктов ПОЛ. Соответственно содержание карбонилированных белков у мужчин кластера 2 было выше, чем у женщин кластера 2. Напротив, между мужчинами и женщинами кластера 1 отсутствовали гендерные различия по содержанию карбонилированных белков. Таким образом, полученные результаты свидетельствуют о том, что характерный для кластера 2 повышенный уровень карбонилированных белков на фоне относительного снижения содержания кортизола типичен только для мужчин. Данные кластерного анализа свидетельствуют о связи повышенного уровня кортизола и снижения свободнорадикального окисления при героиновой зависимости.
Аналогичная закономерность наблюдалась для кетондинитрофенилгидразонов основного характера, а также для альдегиднитрофенилгидразонов. При этом между кластером 1 и 2 отсутствовали статистически значимые различия по содержанию молекулярных продуктов ПОЛ. У женщин отсутствовали статистически значимые различия между кластерами с высоким и низким содержанием кортизола как по содержанию карбонилированных белков, так и по содержанию молекулярных продуктов ПОЛ. Соответственно содержание карбонилированных белков у мужчин кластера 2 было выше, чем у женщин кластера 2. Напротив, между мужчинами и женщинами кластера 1 отсутствовали гендерные различия по содержанию карбонилированных белков. Таким образом, полученные результаты свидетельствуют о том, что характерный для кластера 2 повышенный уровень карбонилированных белков на фоне относительного снижения содержания кортизола типичен только для мужчин. Данные кластерного анализа свидетельствуют о связи повышенного уровня кортизола и снижения свободнорадикального окисления при героиновой зависимости. Возможный механизм этого феномена связан со способностью глюкокортикоидов угнетать активность ферментов, генерирующих активные формы кислорода, и усиливать экспрессию антиоксидантных ферментов.
Возможный механизм этого феномена связан со способностью глюкокортикоидов угнетать активность ферментов, генерирующих активные формы кислорода, и усиливать экспрессию антиоксидантных ферментов.
Таблица 2. Уровень окислительной модификации белков плазмы крови у пациентов с героиновой зависимостью Примечание. * — статистически значимые отличия от соответствующих показателей контрольной группы; ** — статистически значимые различия между кластерами; # — гендерные различия.
Таким образом, в настоящей работе была установлена роль гендерных различий в системе изучавшихся явлений. У мужчин, употребляющих психоактивные вещества, по мере увеличения уровня кортизола снижалось содержание карбонилированных белков в крови. У женщин содержание карбонилированных белков не было чувствительным к изменениям уровня кортизола. Если рассматривать повышенный уровень глюкокортикоидов как адаптивную реакцию, направленную на ограничение окислительного стресса, то в таком случае стабильный уровень карбонилированных белков при повышенном и пониженном уровне кортизола может быть фоном, замедляющим наступление ремиссии./33/33.jpg) Но в то же время относительно сниженный уровень карбонилированных белков у женщин, вошедших в кластер 2, по сравнению с аналогичным кластером мужчин может способствовать более продолжительной ремиссии. Таким образом, полученные результаты свидетельствуют о том, что подъем уровня кортизола в условиях героиновой наркомании позволяет ограничить прирост содержания карбонилированных белков и предупредить возможную активацию ПОЛ. Это положение весьма красноречиво подтверждает факт нахождения на уровне контрольных значений содержания молекулярных продуктов ПОЛ в кластере с повышенным уровнем кортизола. Несмотря на то что в этом кластере прирост содержания карбонилированных белков повышен по сравнению с контролем, его амплитуда ниже, чем в кластере 2, в котором содержание кортизола близко к контрольному уровню.
Но в то же время относительно сниженный уровень карбонилированных белков у женщин, вошедших в кластер 2, по сравнению с аналогичным кластером мужчин может способствовать более продолжительной ремиссии. Таким образом, полученные результаты свидетельствуют о том, что подъем уровня кортизола в условиях героиновой наркомании позволяет ограничить прирост содержания карбонилированных белков и предупредить возможную активацию ПОЛ. Это положение весьма красноречиво подтверждает факт нахождения на уровне контрольных значений содержания молекулярных продуктов ПОЛ в кластере с повышенным уровнем кортизола. Несмотря на то что в этом кластере прирост содержания карбонилированных белков повышен по сравнению с контролем, его амплитуда ниже, чем в кластере 2, в котором содержание кортизола близко к контрольному уровню.
В соответствии с полученными данными могут быть сделаны следующие выводы: для мужчин с героиновой зависимостью содержание карбонилированых белков в крови очень чувствительно к изменению содержания кортизола. У лиц с высоким содержанием кортизола снижен уровень окисления белков, а у лиц со сниженным содержанием кортизола наблюдается повышенный уровень карбонилирования белков. У женщин с героиновой зависимостью уровень карбонилирования белков не столь чувствителен к изменениям уровня кортизола. Но при этом содержание карбонилированных белков у них ниже, чем у мужчин с героиновой зависимостью.
У лиц с высоким содержанием кортизола снижен уровень окисления белков, а у лиц со сниженным содержанием кортизола наблюдается повышенный уровень карбонилирования белков. У женщин с героиновой зависимостью уровень карбонилирования белков не столь чувствителен к изменениям уровня кортизола. Но при этом содержание карбонилированных белков у них ниже, чем у мужчин с героиновой зависимостью.
ЭНДОГЕННЫЙ ГИПЕРКОРТИЦИЗМ Сложности диагностики на пути к очевидному лечению — «ИнфоМедФармДиалог»
Skip to content ЭНДОГЕННЫЙ ГИПЕРКОРТИЦИЗМ Сложности диагностики на пути к очевидному лечениюЭНДОГЕННЫЙ ГИПЕРКОРТИЦИЗМ.
Сложности диагностики на пути к очевидному лечению
Плохо компенсированные сахарный диабет 2‑го типа и артериальная гипертензия, частые переломы могут быть вызваны гиперпродукцией кортизола. Тщательно собранный анамнез и несложные лабораторные тесты позволяют значительно ускорить диагностику эндогенного гиперкортицизма, которая запаздывает в среднем на 5–8 лет, и добиться в 80% случаев ремиссии заболевания.

Симптомы схожие – причины разные
А.В. АНДРЕЕВА – врач-эндокринолог, заместитель главного
врача по терапевтической помощи
ГБУЗ «ГКБ им. В.В. Вересаева ДЗМ»
В основе эндогенного гиперкортицизма лежит избыточная выработка корой надпочечников кортизола, который обусловливает развитие взаимосвязанных метаболических сдвигов. Клинические проявления заболевания могут включать округление лица, перераспределение жира с избыточным накоплением в области живота, верхнего плечевого пояса, в надключичных ямках и по задней поверхности шеи и, наоборот, похудение конечностей, а также появление акне, стрий, геморрагий. Несмотря на типичность клинических проявлений при эндогенном гиперкортицизме, необходимо понимать истинную причину его гиперпродукции в гипоталамо‑гипофизарно‑надпочечниковой системе. Поэтому при появлении в крови избыточного патологического уровня кортизола необходимо определить истинного «виновника» этого процесса. Если причина находится в самих надпочечниках, то чаще всего это доброкачественная опухоль – кортикостерома. Реже встречается злокачественная опухоль – адренокортикальный рак. Возможна также двусторонняя гиперплазия надпочечников на фоне экспрессии аберрантных рецепторов. Последняя патология редко встречается в эндокринологической практике, но тем не менее ее тоже следует принимать во внимание.
Реже встречается злокачественная опухоль – адренокортикальный рак. Возможна также двусторонняя гиперплазия надпочечников на фоне экспрессии аберрантных рецепторов. Последняя патология редко встречается в эндокринологической практике, но тем не менее ее тоже следует принимать во внимание.
Эндокринные опухоли имеют очень неприятную специфику – они могут возобновлять рост даже через несколько лет после операции. Доля рецидивов доходит до 30%
Второй вариант, о котором следует думать при гиперпродукции кортизола, обусловлен влиянием на надпочечники адренокортикотропного гормона, или АКТГ, который, в свою очередь, стимулируется кортикотропин‑рилизинг гормоном. Кортикотропинома – аденома гипофиза, автономно секретирующая АКТГ, что, соответственно, приводит к гиперпродукции кортизола в коре надпочечников. И это наиболее частая причина эндогенного гиперкортицизма.
Наконец, возможна выработка АКТГ опухолью, которая находится вне гипофиза. Такой вариант носит название синдрома эктопической продукции АКТГ. Чаще всего это следствие онкологических процессов. Нейроэндокринные опухоли гиперпродуцируют АКТГ либо подобные ему пептидные гормоны, которые опять же запускают всю патологическую цепочку, включая гиперсекрецию кортизола корой надпочечника.
Такой вариант носит название синдрома эктопической продукции АКТГ. Чаще всего это следствие онкологических процессов. Нейроэндокринные опухоли гиперпродуцируют АКТГ либо подобные ему пептидные гормоны, которые опять же запускают всю патологическую цепочку, включая гиперсекрецию кортизола корой надпочечника.
Жалобы, специфические и не очень
Кортизол влияет на весь спектр биохимических и метаболических процессов, что обусловливает множественные патологические процессы во всех органах при его гипо – и гиперпродукции. Основная нозологическая симптоматика может быть выражена достаточно ярко – худые ноги и руки в сочетании с абдоминальным ожирением, изменение формы лица (матронизм или лунообразное лицо). При этом кожа на лице приобретает гиперемированную окраску. Возможны специфические изменения на коже – стрии.
Все эти симптомы в совокупности встречаются довольно редко. Лишь в 30% случаев их можно увидеть у одного пациента. А в 55% случаев больные предъявляют жалобы, характерные для многих других более распространенных заболеваний. Это, например, артериальная гипертензия, ожирение, с которыми пациенту не удается справиться, участившиеся тромбозы, плохой сон, тревожное настроение, нарушение менструального цикла, снижение либидо. Терапевту следует обратить внимание на так называемые ассоциированные заболевания, в первую очередь сахарный диабет и артериальную гипертензию, которые при гиперкортицизме очень трудно поддаются лечению, несмотря на подбор многокомпонентной терапии. Нужно спросить у пациента о склонности к переломам, в особенности к так называемым низкоэнергетическим – при падении с высоты собственного роста, при выполнении повседневных функций. Сами больные очень редко связывают это со своим состоянием и не предъявляют жалоб при сборе анамнеза.
Это, например, артериальная гипертензия, ожирение, с которыми пациенту не удается справиться, участившиеся тромбозы, плохой сон, тревожное настроение, нарушение менструального цикла, снижение либидо. Терапевту следует обратить внимание на так называемые ассоциированные заболевания, в первую очередь сахарный диабет и артериальную гипертензию, которые при гиперкортицизме очень трудно поддаются лечению, несмотря на подбор многокомпонентной терапии. Нужно спросить у пациента о склонности к переломам, в особенности к так называемым низкоэнергетическим – при падении с высоты собственного роста, при выполнении повседневных функций. Сами больные очень редко связывают это со своим состоянием и не предъявляют жалоб при сборе анамнеза.
Если причина находится в самих надпочечниках, то чаще всего это доброкачественная опухоль – кортикостерома. Реже встречается злокачественная опухоль – адренокортикальный рак
То же касается и проблем гинекологической и сексуальной сферы, которые также могут быть связаны с гиперкортицизмом.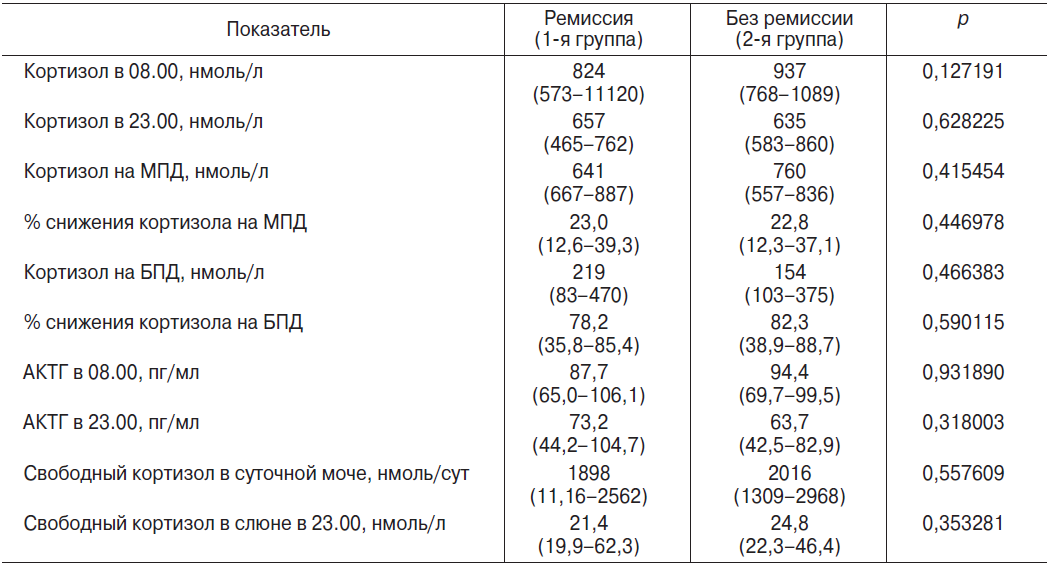 Очень важно понимать, что об этих проблемах женщины и мужчины не станут говорить терапевту без соответствующих наводящих вопросов.
Очень важно понимать, что об этих проблемах женщины и мужчины не станут говорить терапевту без соответствующих наводящих вопросов.
Повышенный уровень кортизола может приводить и к дерматологическим заболеваниям (акне, гнойничковые поражения кожи), и к снижению иммунитета (частые ОРВИ, бронхиты, пневмонии). В любом случае терапевту всегда необходимо подключать клиническое мышление, чтобы связать все жалобы воедино.
К сожалению, в России отмечаются серьезные проблемы с ранним выявлением гиперкортицизма. В среднем диагностика запаздывает на 6–8 лет. Конечно, многое зависит от того, в каком возрасте манифестирует заболевание. У пациентов младше 40 лет верификация диагноза происходит в течение в среднем 2 лет, у людей в возрасте 40–65 лет – 5 лет. Самая сложная в плане диагностики группа – больные старше 65 лет, это как раз те пациенты, которые приходят наблюдаться по поводу артериальной гипертензии, ожирения и сахарного диабета. Они требуют более пристального внимания со стороны врача и исключения гиперкортицизма как одной из причин этих заболеваний.
Скрининг и группы риска
Только на первый взгляд кажется, что эндогенный гиперкортицизм относится к числу редких заболеваний. Исследовательские работы, направленные на изучение эндогенного гиперкортицизма, свидетельствуют, что «редкость» связана с плохой выявляемостью. Это подтверждает скрининг пациентов с декомпенсированным сахарным диабетом 2‑го типа, где эндогенный гиперкортицизм можно выявить у 2–4% обследуемых. При патологических переломах эта доля возрастает до 6,5%.
По результатам ряда исследовательских работ было выделено несколько групп, подлежащих обязательному скринингу. В первую очередь это, конечно, пациенты с классическими признаками заболевания – большим животом, тонкими конечностями, расплывшимся лунообразным лицом, стриями.
Вторая группа – пожилые пациенты с сахарным диабетом 2‑го типа, артериальной гипертензией, не компенсирующимися на медикаментозной терапии, а также патологическими переломами.
Следующая скрининговая группа – это молодые люди с не характерными для их возраста заболеваниями, прежде всего сахарным диабетом 2‑го типа, злокачественной артериальной гипертензией, частыми переломами.
Очевидна необходимость скрининга и у детей при задержке роста и избыточной массе тела. Кстати, у детей признаки эндогенного гиперкортицизма прослеживаются наиболее четко, но при этом у них может и не быть классических проявлений заболевания в виде стрий или матронизма.
Наиболее частой причиной эндогенного гиперкортицизма является кортикотропинома – аденома гипофиза, автономно секретирующая АКТГ, что приводит к гиперпродукции кортизола в коре надпочечников
Наконец, обязательному скринингу подлежат пациенты со случайно выявленным образованием в надпочечниках во время УЗ – и КТ‑исследований. Случайная находка может быть результатом обследования брюшной полости по иному поводу, но она требует проведения лабораторных тестов на уровень кортизола. Раньше таких случаев было не так много, однако период пандемии эту статистику существенно изменил. При массовых КТ‑исследованиях легких надпочечники очень часто попадают в поле зрения, и выявление различных образований существенно увеличилось./16/16.jpg) В соответствии с клиническими рекомендациями врачи обязаны учитывать эти данные. Однако в 95% случаев визуализируемые инциденталомы надпочечников гормонально не активны и не мешают жить пациентам, поэтому массовый скрининг в этих случаях не оправдан. Кроме того, не следует забывать, что при коронавирусной инфекции часто применяют стероидные препараты, которые, влияя на гормональный фон, могут затруднять диагностику эндогенного гиперкортицизма. Таким образом, всегда необходим взвешенный подход к проведению скрининга с учетом сопутствующих заболеваний, недавно перенесенной новой коронавирусной инфекции и оценкой клинических показаний.
В соответствии с клиническими рекомендациями врачи обязаны учитывать эти данные. Однако в 95% случаев визуализируемые инциденталомы надпочечников гормонально не активны и не мешают жить пациентам, поэтому массовый скрининг в этих случаях не оправдан. Кроме того, не следует забывать, что при коронавирусной инфекции часто применяют стероидные препараты, которые, влияя на гормональный фон, могут затруднять диагностику эндогенного гиперкортицизма. Таким образом, всегда необходим взвешенный подход к проведению скрининга с учетом сопутствующих заболеваний, недавно перенесенной новой коронавирусной инфекции и оценкой клинических показаний.
В скрининговую группу следует обязательно включать женщин с гирсутизмом. Как правило, эти пациентки относятся к старшей возрастной категории, и очень важно, чтобы они не «потерялись» в общей массе. Именно у них чаще всего наблюдаются и артериальная гипертензия, и сахарный диабет, и ожирение. Поэтому женщин в случае сочетания этих заболеваний с избыточным оволосением по мужскому типу требуется в обязательном порядке обследовать на гиперкортицизм.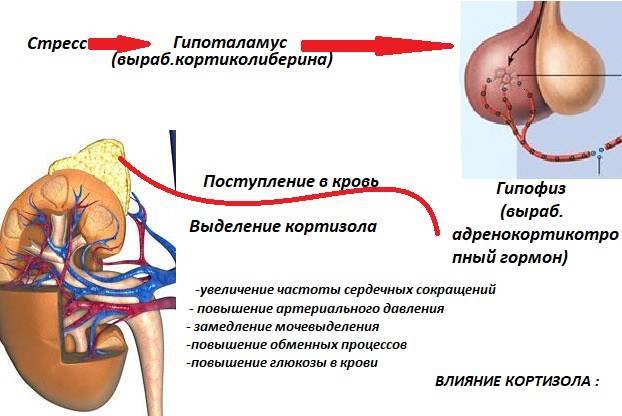
Нюансы дифференциальной диагностики
Избыточная продукция кортизола далеко не во всех случаях свидетельствует об эндогенном гиперкортицизме. Такие состояния, как беременность, хронический алкоголизм, пубертатное созревание, расстройства пищевого поведения, часто могут сопровождаться гиперпродукцией кортизола. Пациенты с хронической алкогольной интоксикацией могут даже приобретать стигмы и другие фенотипические черты пациента с эндогенным гиперкортицизмом. Нарушение метаболизма и синтетической белковой функции печени, которая отвечает за катаболизм кортизола, сопровождается избыточным накоплением гормона, не связанным с эндогенным гиперкортицизмом.
Повышенный уровень кортизола может наблюдаться и при хронической депрессии, и в случае приема препаратов, изменяющих метаболизм печеночных ферментов, особенно с цитохромом P450. Поэтому следует обязательно уточнять, наблюдается ли пациент у психотерапевта или психиатра – вряд ли он об этом скажет без наводящих вопросов.
Существует также группа больных с редким семейным анамнезом резистентности к кортизолу, которая сопровождается компенсаторным увеличением показателей активности гипоталамо‑гипофизарно‑надпочечниковой оси, в том числе чрезмерной секрецией андрогенов надпочечников. У этих пациентов нет типичных проявлений гиперкортицизма, однако клинические признаки в виде артериальной гипертензии, гирсутизма и гиперплазии надпочечников, а также лабораторный компонент диагноза могут привести к ложноположительному заключению и неправильной тактике ведения таких пациентов.
У этих пациентов нет типичных проявлений гиперкортицизма, однако клинические признаки в виде артериальной гипертензии, гирсутизма и гиперплазии надпочечников, а также лабораторный компонент диагноза могут привести к ложноположительному заключению и неправильной тактике ведения таких пациентов.
Кортизол в крови – недостаточный маркер
Несмотря на то, что увеличенная концентрация кортизола является ключевым маркером эндогенного гиперкортицизма, ориентироваться на степень его повышения как раз нельзя. Врач обязательно должен знать об этом. Уровень кортизола в крови, взятой утром натощак, – это абсолютно не информативный показатель. С одной стороны, он может свидетельствовать о заболевании, с другой – привести к гипердиагностике. Ведь кортизол – это гормон стресса, а некоторые пациенты воспринимают процедуру забора крови как стресс.
В то же время нормальный уровень кортизола (в т. ч. на верхней границе референсных значений) иногда встречается при прогрессирующем заболевании. И пациент в случае оценки только утреннего кортизола в крови может быть «потерян» в плане диагностики.
И пациент в случае оценки только утреннего кортизола в крови может быть «потерян» в плане диагностики.
Таким образом, опираясь только на данные уровня кортизола в крови, мы не можем ставить или опровергать диагноз «эндогенный гиперкортицизм». Если имеет место повышенная продукция гормона, то он будет обнаруживаться во всех биологических жидкостях – в крови, моче и слюне. Отсюда и рекомендуемые для дифференциальной диагностики лабораторные тесты.
Терапевту следует обратить внимание на так называемые ассоциированные заболевания, в первую очередь сахарный диабет и артериальную гипертензию, которые при гиперкортицизме очень трудно поддаются лечению, несмотря на подбор многокомпонентной терапии
В соответствии с клиническими рекомендациями для подтверждения диагноза эндогенного гиперкортицизма следует опираться на результаты двух анализов из пяти возможных. Хотя для максимальной чувствительности и специфичности необходимо проведение трех анализов.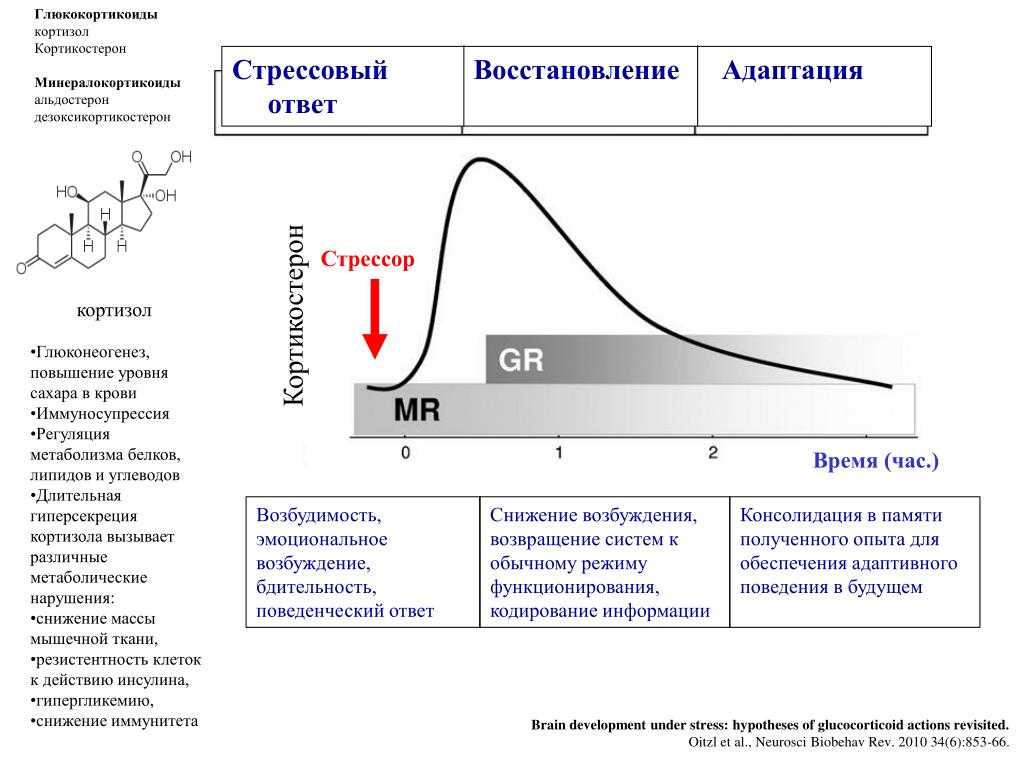 Первый (самый простой и удобный) – определение кортизола слюны в 23:00. Пациенту необходимо всего лишь обильно смочить шваб (тампон) из пробирки слюной, погрузить обратно в пробирку и утром отнести в лабораторию. Тест не вызывает ни трудностей, ни стресса, проводится в домашней, привычной для пациента обстановке. Второй обязательный тест – это малая проба с дексаметазоном. Он требует забора крови из вены, и его очень удобно делать в один день с первым тестом. Пациент после сбора слюны принимает 2 таблетки дексаметазона и ложится спать. Утром, относя пробирку с образцом слюны в лабораторию, он там же сдает кровь на кортизол. Третий тест – это уровень свободного кортизола в суточном анализе мочи. Он тоже проводится в домашних условиях, что исключает волнение пациента. Трех тестов абсолютно достаточно для верификации диагноза эндогенного гиперкортицизма. При этом вовсе не нужно при обнаружении кортизола в крови проходить дорогие обследования (УЗИ, КТ, МРТ) в тех случаях, когда они не предусмотрены клиническими рекомендациями.
Первый (самый простой и удобный) – определение кортизола слюны в 23:00. Пациенту необходимо всего лишь обильно смочить шваб (тампон) из пробирки слюной, погрузить обратно в пробирку и утром отнести в лабораторию. Тест не вызывает ни трудностей, ни стресса, проводится в домашней, привычной для пациента обстановке. Второй обязательный тест – это малая проба с дексаметазоном. Он требует забора крови из вены, и его очень удобно делать в один день с первым тестом. Пациент после сбора слюны принимает 2 таблетки дексаметазона и ложится спать. Утром, относя пробирку с образцом слюны в лабораторию, он там же сдает кровь на кортизол. Третий тест – это уровень свободного кортизола в суточном анализе мочи. Он тоже проводится в домашних условиях, что исключает волнение пациента. Трех тестов абсолютно достаточно для верификации диагноза эндогенного гиперкортицизма. При этом вовсе не нужно при обнаружении кортизола в крови проходить дорогие обследования (УЗИ, КТ, МРТ) в тех случаях, когда они не предусмотрены клиническими рекомендациями.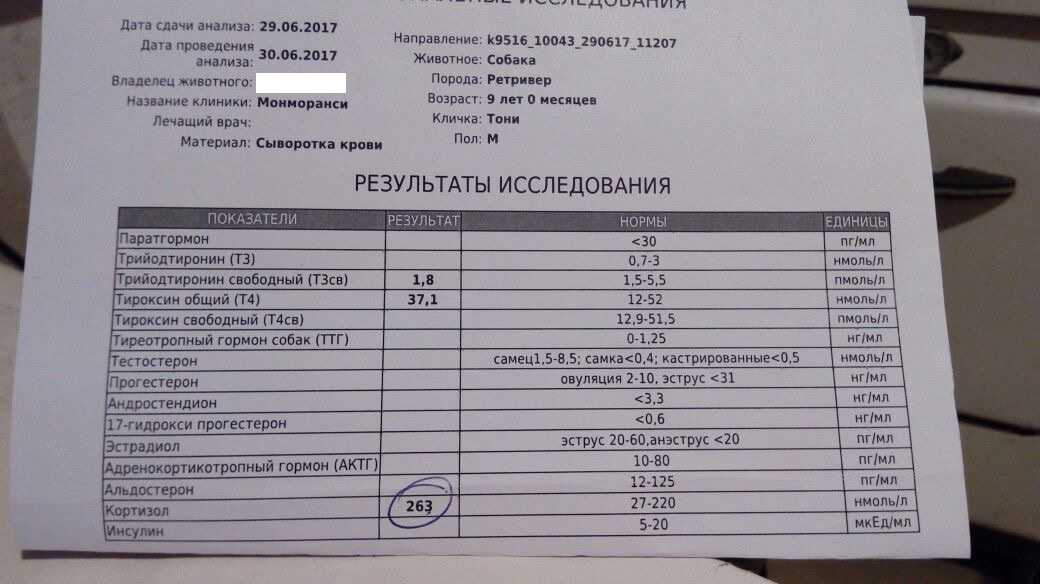
Диагноз подтвердился. Что дальше?
Если по результатам трех тестов и клиническим симптомам эндогенный гиперкортицизм подтвердился, следует выявить источник его гиперпродукции. И для этого необходимо определить уровень адренокортикотропного гормона (АКТГ).
Уровень АКТГ менее 5–10 пг/мл полностью возлагает «вину» на надпочечники. Любой показатель АКТГ выше указанной отрезной точки и тем более выше референсных значений может говорить либо об аденоме гипофиза, т. е. болезни Иценко–Кушинга, либо о наличии синдрома эктопической продукции АКТГ. В последнем случае кортизол может вырабатывать образование, не ассоциированное с гипофизом. Чаще всего это карциноид бронха, тимома, опухоли яичника, поджелудочной железы и толстой кишки.
Для дальнейшего уточнения диагноза нам необходимо использовать методы визуализации – провести КТ надпочечников с контрастированием (если она еще не проведена), МРТ гипофиза с контрастированием, КТ других связанных областей. В этом случае применение методов КТ и МРТ совершенно обосновано и позволяет локализовать источник патологического процесса.
Опираясь только на данные уровня кортизола в крови, мы не можем ставить или опровергать диагноз «эндогенный гиперкортицизм». Если имеет место повышенная продукция гормона, то он будет обнаруживаться во всех биологических жидкостях – в крови, моче и слюне
Хирургия в приоритете
После верификации диагноза и визуализации патологического образования врач должен принять решение о дальнейшей тактике ведения пациента. Хирургическое вмешательство в большинстве случаев рассматривается как первая линия лечения. При болезни Иценко–Кушинга трансназальная транссфеноидальная аденомэктомия показана практически всем пациентам. При кортикостероме – адреналэктомия. При опухоли эктопического очага –резекция образования и совместная работа с онкологом по этапности лечебного процесса.
Медикаментозную терапию при гормонально‑активных опухолях назначают в качестве терапии второй‑третьей линии. Порой на короткое время, необходимое для подготовки к операции. Она направлена на подавление избыточной продукции кортизола, нормализацию гемодинамики, показателей глюкозы. Такая терапия не может быть вариантом пожизненного лечения из‑за серьезных побочных эффектов лекарственных средств.
Она направлена на подавление избыточной продукции кортизола, нормализацию гемодинамики, показателей глюкозы. Такая терапия не может быть вариантом пожизненного лечения из‑за серьезных побочных эффектов лекарственных средств.
Вторая линия терапии – это стереотаксическая радиохирургия. К ней прибегают либо в случаях, когда полностью опухоль удалить не удается, либо если заболевание имеет торпидное течение и у пациента есть шанс на постепенную ремиссию. В этом случае регресс опухоли будет выражаться в снижении уровня кортизола. Это может быть долгим процессом, иногда до 3–5 лет, но такой подход совершенно оправдан.
Консервативное лечение используется также при невозможности радикального удаления аденомы гипофиза. По статистике доля таких случаев составляет 10–15%. Как правило, это макроаденомы размером более 10 мм, которые могут выходить за пределы турецкого седла и/или прорастать в кавернозный синус. И в этом случае шанс на радикальное удаление опухоли существенно снижается.
Не выпускать из виду
Эндокринные опухоли имеют очень неприятную специфику – они могут возобновлять рост даже через несколько лет после операции. Доля рецидивов доходит до 30%. Кроме того, пожилым пациентам с ассоциированными заболеваниями необходима дальнейшая консервативная терапия. Ведь даже после удаления опухоли у них остается и сахарный диабет, и остеопороз, и метаболические нарушения, хотя их и удается взять под контроль. В течение начального периода наблюдения (около 12 недель) дозы сахароснижающих, гипотензивных препаратов, безусловно, снижаются. Однако уйти от медикаментозной терапии не удается. Поэтому очень важно объяснить и убедить пациента в том, что даже после радикальной операции ему будет необходимо посещать эндокринолога ежегодно в течение всей жизни.
Доля рецидивов доходит до 30%. Кроме того, пожилым пациентам с ассоциированными заболеваниями необходима дальнейшая консервативная терапия. Ведь даже после удаления опухоли у них остается и сахарный диабет, и остеопороз, и метаболические нарушения, хотя их и удается взять под контроль. В течение начального периода наблюдения (около 12 недель) дозы сахароснижающих, гипотензивных препаратов, безусловно, снижаются. Однако уйти от медикаментозной терапии не удается. Поэтому очень важно объяснить и убедить пациента в том, что даже после радикальной операции ему будет необходимо посещать эндокринолога ежегодно в течение всей жизни.
Высокий уровень кортизола: симптомы, причины и многое другое
Кортизол известен как гормон стресса из-за его роли в реакции организма на стресс. Но кортизол играет гораздо большую роль в организме, чем реакция «бей или беги».
Время от времени у каждого человека бывает высокий уровень кортизола, и его уровень меняется в течение дня. Это часть естественной реакции вашего тела на угрозу причинения вреда или опасности.
Но если ваше тело постоянно вырабатывает слишком много кортизола, это обычно указывает на основную проблему со здоровьем. Врачи могут называть высокий уровень кортизола синдромом Кушинга или гиперкортицизмом.
Читайте дальше, чтобы узнать, как распознать симптомы и возможные причины.
Надпочечники вырабатывают этот стероидный гормон, но ось гипоталамус-гипофиз-надпочечники контролирует, сколько высвобождает ваш организм.
Большинство клеток вашего тела имеют рецепторы кортизола. Они используют его для различных функций, таких как:
- регулирование уровня сахара в крови
- уменьшение воспаления
- регулирование обмена веществ
- формирование памяти
Кортизол важен для вашего здоровья, но слишком много его может нанести вред вашему телу и вызвать несколько нежелательных симптомов.
Высокий уровень кортизола может вызывать ряд симптомов в организме. Симптомы могут варьироваться в зависимости от того, что вызывает повышение уровня кортизола.
Общие признаки и симптомы избытка кортизола включают:
- увеличение массы тела, в основном в средней части и верхней части спины
- увеличение массы тела и округление лица
- акне
- thinning skin
- easy bruising
- flushed face
- slowed healing
- muscle weakness
- severe fatigue
- irritability
- difficulty concentrating
- high blood pressure
- headache
The brain’s hypothalamus interacts with various glands in our организм регулирует уровень гормонов. Когда дело доходит до кортизола, это известно как гипоталамо-гипофизарно-надпочечниковая ось.
Когда уровень кортизола низкий, гипоталамус высвобождает кортикотропин-рилизинг-гормон (CRH), который запускает переднюю долю гипофиза для высвобождения адренокортикотропного гормона (АКТГ). Затем АКТГ заставляет надпочечники создавать и выделять больше кортизола.
Затем АКТГ заставляет надпочечники создавать и выделять больше кортизола.
Существуют разные причины, по которым надпочечники могут выделять слишком много кортизола.
Стресс
Стресс вызывает в организме комбинацию сигналов от гормонов и нервов. Эти сигналы заставляют ваши надпочечники выделять гормоны, в том числе адреналин и кортизол.
В результате учащается сердцебиение и увеличивается энергия, что является частью реакции «бей или беги». Это способ вашего тела подготовиться к потенциально опасным или вредным ситуациям.
Кортизол также помогает ограничить любые функции, которые не являются необходимыми в ситуации борьбы или бегства. Как только угроза минует, ваши гормоны вернутся к своему обычному уровню, а функции организма вернутся к обычному уровню.
Но когда вы находитесь в постоянном стрессе, эта реакция не всегда отключается.
Длительное воздействие кортизола и других гормонов стресса может негативно повлиять практически на все процессы в организме. Это может увеличить риск возникновения проблем со здоровьем, таких как болезни сердца, проблемы с легкими, ожирение, беспокойство, депрессия и многое другое.
Это может увеличить риск возникновения проблем со здоровьем, таких как болезни сердца, проблемы с легкими, ожирение, беспокойство, депрессия и многое другое.
Проблемы с гипофизом
Гипофиз расположен в основании головного мозга. Люди иногда называют ее «главной железой», потому что она контролирует и помогает контролировать многие функции организма, выделяя гормоны.
Проблемы с гипофизом могут привести к недостаточной или чрезмерной выработке гормонов, в том числе АКТГ, что затем заставляет надпочечники вырабатывать больше кортизола.
Заболевания гипофиза, которые могут вызывать высокие уровни кортизола, включают:
- гиперпитуитаризм (сверхактивный гипофиз)
- доброкачественные опухоли гипофиза, включая аденомы
- раковые опухоли гипофиза
опухоли надпочечников
Ваши надпочечники расположены над каждой почкой. Опухоли надпочечников могут быть доброкачественными (нераковыми) или злокачественными (раковыми) и различаться по размеру. Оба типа могут выделять высокие уровни гормонов, включая кортизол.
Оба типа могут выделять высокие уровни гормонов, включая кортизол.
Кроме того, если опухоль достаточно велика, чтобы сдавливать близлежащие органы, вы можете почувствовать боль или чувство переполнения в животе.
Опухоли надпочечников обычно являются доброкачественными и обнаруживаются примерно у 1 из 10 человек, которым проводится визуализирующее исследование надпочечников. Рак надпочечников встречается гораздо реже.
Побочные эффекты лекарств
Некоторые лекарства могут вызывать повышение уровня кортизола. Например, в некоторых исследованиях отмечается связь между оральными контрацептивами и уровнем кортизола в крови.
Кортикостероидные препараты, используемые для лечения астмы, артрита, некоторых видов рака и других состояний, также могут вызывать повышение уровня кортизола при приеме в высоких дозах или в течение длительного периода времени.
Commonly prescribed corticosteroids include:
- prednisone (Deltasone, Prednicot, Rayos)
- cortisone (Cortone Acetate)
- methylprednisolone (Medrol, Methylprednisolone dose pack)
- dexamethasone (Dexamethasone Intensol, DexPak, Baycadron)
Finding правильная доза и прием кортикостероидов в соответствии с предписаниями могут помочь снизить риск развития высокого уровня кортизола.
Вы никогда не должны прекращать прием стероидных препаратов без постепенного снижения или предварительной консультации с врачом. Резкая остановка может привести к снижению уровня кортизола. Это может вызвать низкое кровяное давление или уровень сахара в крови, кому и смерть.
Если вы подозреваете, что у вас может быть высокий уровень кортизола, обратитесь к врачу, чтобы сдать анализ крови. Высокий уровень кортизола вызывает несколько неспецифических симптомов, а это означает, что за них могут быть ответственны несколько заболеваний и заболеваний.
При появлении симптомов врач может порекомендовать следующие анализы:
- Анализ мочи и крови на кортизол . Эти тесты измеряют уровень кортизола в крови и моче. В анализе крови используется образец крови, взятый из вашей вены. Анализ мочи на кортизол представляет собой 24-часовой тест экскреции кортизола без мочи, который влечет за собой сбор мочи в течение 24-часового периода. Образцы крови и мочи затем анализируются в лаборатории на уровень кортизола.

- Анализ слюны на кортизол. Этот тест проверяет наличие синдрома Кушинга. Образец слюны, собранный ночью, анализируется, чтобы определить, высок ли у вас уровень кортизола. Уровни кортизола повышаются и падают в течение дня и значительно снижаются ночью у людей без синдрома Кушинга. Высокий уровень кортизола ночью указывает на то, что у вас может быть синдром Кушинга.
- Визуальные тесты. Компьютерная томография или магнитно-резонансная томография могут быть использованы для получения изображений гипофиза и надпочечников для проверки на наличие опухолей или других аномалий.
Плохо контролируемый высокий уровень кортизола может иметь серьезные последствия для вашего здоровья. Без лечения высокий уровень кортизола может увеличить риск серьезных заболеваний, включая:
- сердечно-сосудистые заболевания
- остеопороз
- резистентность к инсулину и диабет
- психические расстройства
В следующих разделах приведены ответы на некоторые часто задаваемые вопросы о высоком уровне кортизола.
Что вызывает повышение уровня кортизола?
Если у вас повышается уровень кортизола, прямой причиной является высокий уровень АКТГ в надпочечниках. Это может быть связано с основным состоянием здоровья, приемом лекарств или другими причинами.
Как узнать, повышен ли у меня уровень кортизола?
Высокий уровень кортизола может вызывать ряд симптомов, таких как увеличение веса, головные боли, раздражительность и другие. В большинстве случаев симптомы не являются специфическими для повышенного уровня кортизола. Вам нужно будет обратиться к врачу для формального диагноза, который часто требует анализа крови, слюны или мочи.
Снижает ли витамин D уровень кортизола?
Некоторые данные свидетельствуют о том, что добавки с витамином D могут помочь снизить уровень кортизола в крови и моче. Это может помочь снизить риск сердечно-сосудистых заболеваний.
Высокий уровень кортизола в течение длительного периода времени может иметь долгосрочные негативные последствия для вашего здоровья. Это известно как синдром Кушинга.
Это известно как синдром Кушинга.
Если у вас есть симптомы высокого уровня кортизола, вам следует обратиться к врачу. Врач может помочь определить основную причину ваших симптомов и помочь вам лечить или управлять состоянием.
Высокий уровень кортизола: симптомы, причины и многое другое
Кортизол известен как гормон стресса из-за его роли в реакции организма на стресс. Но кортизол играет гораздо большую роль в организме, чем реакция «бей или беги».
Время от времени у каждого человека бывает высокий уровень кортизола, и его уровень меняется в течение дня. Это часть естественной реакции вашего тела на угрозу причинения вреда или опасности.
Но если ваше тело постоянно вырабатывает слишком много кортизола, это обычно указывает на основную проблему со здоровьем. Врачи могут называть высокий уровень кортизола синдромом Кушинга или гиперкортицизмом.
Читайте дальше, чтобы узнать, как распознать симптомы и возможные причины.
Надпочечники вырабатывают этот стероидный гормон, но ось гипоталамус-гипофиз-надпочечники контролирует, сколько высвобождает ваш организм.
Большинство клеток вашего тела имеют рецепторы кортизола. Они используют его для различных функций, таких как:
- регулирование уровня сахара в крови
- уменьшение воспаления
- регулирование обмена веществ
- формирование памяти
Кортизол важен для вашего здоровья, но слишком много его может нанести вред вашему телу и вызвать несколько нежелательных симптомов.
Высокий уровень кортизола может вызывать ряд симптомов в организме. Симптомы могут варьироваться в зависимости от того, что вызывает повышение уровня кортизола.
Общие признаки и симптомы избытка кортизола включают:
- увеличение массы тела, в основном в средней части и верхней части спины
- увеличение массы тела и округление лица
- акне
- thinning skin
- easy bruising
- flushed face
- slowed healing
- muscle weakness
- severe fatigue
- irritability
- difficulty concentrating
- high blood pressure
- headache
The brain’s hypothalamus interacts with various glands in our организм регулирует уровень гормонов.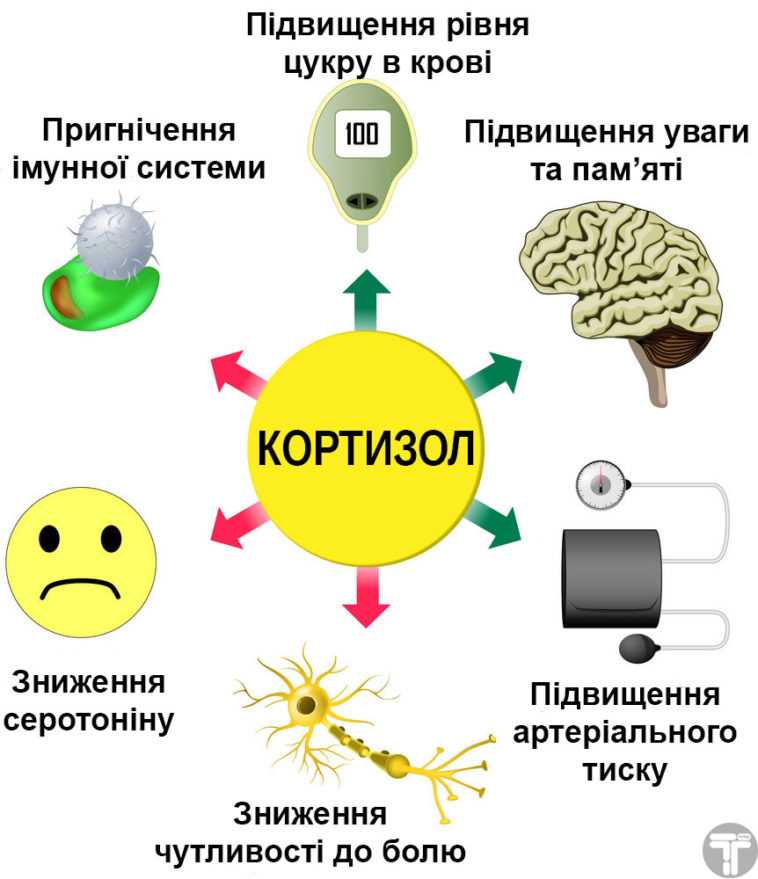 Когда дело доходит до кортизола, это известно как гипоталамо-гипофизарно-надпочечниковая ось.
Когда дело доходит до кортизола, это известно как гипоталамо-гипофизарно-надпочечниковая ось.
Когда уровень кортизола низкий, гипоталамус высвобождает кортикотропин-рилизинг-гормон (CRH), который запускает переднюю долю гипофиза для высвобождения адренокортикотропного гормона (АКТГ). Затем АКТГ заставляет надпочечники создавать и выделять больше кортизола.
Существуют разные причины, по которым надпочечники могут выделять слишком много кортизола.
Стресс
Стресс вызывает в организме комбинацию сигналов от гормонов и нервов. Эти сигналы заставляют ваши надпочечники выделять гормоны, в том числе адреналин и кортизол.
В результате учащается сердцебиение и увеличивается энергия, что является частью реакции «бей или беги». Это способ вашего тела подготовиться к потенциально опасным или вредным ситуациям.
Кортизол также помогает ограничить любые функции, которые не являются необходимыми в ситуации борьбы или бегства. Как только угроза минует, ваши гормоны вернутся к своему обычному уровню, а функции организма вернутся к обычному уровню.
Но когда вы находитесь в постоянном стрессе, эта реакция не всегда отключается.
Длительное воздействие кортизола и других гормонов стресса может негативно повлиять практически на все процессы в организме. Это может увеличить риск возникновения проблем со здоровьем, таких как болезни сердца, проблемы с легкими, ожирение, беспокойство, депрессия и многое другое.
Проблемы с гипофизом
Гипофиз расположен в основании головного мозга. Люди иногда называют ее «главной железой», потому что она контролирует и помогает контролировать многие функции организма, выделяя гормоны.
Проблемы с гипофизом могут привести к недостаточной или чрезмерной выработке гормонов, в том числе АКТГ, что затем заставляет надпочечники вырабатывать больше кортизола.
Заболевания гипофиза, которые могут вызывать высокие уровни кортизола, включают:
- гиперпитуитаризм (сверхактивный гипофиз)
- доброкачественные опухоли гипофиза, включая аденомы
- раковые опухоли гипофиза
опухоли надпочечников
Ваши надпочечники расположены над каждой почкой. Опухоли надпочечников могут быть доброкачественными (нераковыми) или злокачественными (раковыми) и различаться по размеру. Оба типа могут выделять высокие уровни гормонов, включая кортизол.
Опухоли надпочечников могут быть доброкачественными (нераковыми) или злокачественными (раковыми) и различаться по размеру. Оба типа могут выделять высокие уровни гормонов, включая кортизол.
Кроме того, если опухоль достаточно велика, чтобы сдавливать близлежащие органы, вы можете почувствовать боль или чувство переполнения в животе.
Опухоли надпочечников обычно являются доброкачественными и обнаруживаются примерно у 1 из 10 человек, которым проводится визуализирующее исследование надпочечников. Рак надпочечников встречается гораздо реже.
Побочные эффекты лекарств
Некоторые лекарства могут вызывать повышение уровня кортизола. Например, в некоторых исследованиях отмечается связь между оральными контрацептивами и уровнем кортизола в крови.
Кортикостероидные препараты, используемые для лечения астмы, артрита, некоторых видов рака и других состояний, также могут вызывать повышение уровня кортизола при приеме в высоких дозах или в течение длительного периода времени.
Commonly prescribed corticosteroids include:
- prednisone (Deltasone, Prednicot, Rayos)
- cortisone (Cortone Acetate)
- methylprednisolone (Medrol, Methylprednisolone dose pack)
- dexamethasone (Dexamethasone Intensol, DexPak, Baycadron)
Finding правильная доза и прием кортикостероидов в соответствии с предписаниями могут помочь снизить риск развития высокого уровня кортизола.
Вы никогда не должны прекращать прием стероидных препаратов без постепенного снижения или предварительной консультации с врачом. Резкая остановка может привести к снижению уровня кортизола. Это может вызвать низкое кровяное давление или уровень сахара в крови, кому и смерть.
Если вы подозреваете, что у вас может быть высокий уровень кортизола, обратитесь к врачу, чтобы сдать анализ крови. Высокий уровень кортизола вызывает несколько неспецифических симптомов, а это означает, что за них могут быть ответственны несколько заболеваний и заболеваний.
При появлении симптомов врач может порекомендовать следующие анализы:
- Анализ мочи и крови на кортизол . Эти тесты измеряют уровень кортизола в крови и моче. В анализе крови используется образец крови, взятый из вашей вены. Анализ мочи на кортизол представляет собой 24-часовой тест экскреции кортизола без мочи, который влечет за собой сбор мочи в течение 24-часового периода. Образцы крови и мочи затем анализируются в лаборатории на уровень кортизола.
- Анализ слюны на кортизол. Этот тест проверяет наличие синдрома Кушинга. Образец слюны, собранный ночью, анализируется, чтобы определить, высок ли у вас уровень кортизола. Уровни кортизола повышаются и падают в течение дня и значительно снижаются ночью у людей без синдрома Кушинга. Высокий уровень кортизола ночью указывает на то, что у вас может быть синдром Кушинга.
- Визуальные тесты. Компьютерная томография или магнитно-резонансная томография могут быть использованы для получения изображений гипофиза и надпочечников для проверки на наличие опухолей или других аномалий.

Плохо контролируемый высокий уровень кортизола может иметь серьезные последствия для вашего здоровья. Без лечения высокий уровень кортизола может увеличить риск серьезных заболеваний, включая:
- сердечно-сосудистые заболевания
- остеопороз
- резистентность к инсулину и диабет
- психические расстройства
В следующих разделах приведены ответы на некоторые часто задаваемые вопросы о высоком уровне кортизола.
Что вызывает повышение уровня кортизола?
Если у вас повышается уровень кортизола, прямой причиной является высокий уровень АКТГ в надпочечниках. Это может быть связано с основным состоянием здоровья, приемом лекарств или другими причинами.
Как узнать, повышен ли у меня уровень кортизола?
Высокий уровень кортизола может вызывать ряд симптомов, таких как увеличение веса, головные боли, раздражительность и другие. В большинстве случаев симптомы не являются специфическими для повышенного уровня кортизола.