Остеохондроз стопы и нижней конечности » Медвестник
Остеохондроз нижней конечности – это заболевание, характерное для детского возраста. Нагрузки, которые испытывают кости ребенка, влияют на ростовую пластину и могут привести к нарушениям ее развития. Педиатру важно знать основные признаки этого заболевания, чтобы не пропустить его у маленьких пациентов.
Чем быстрее ребенок развивается, тем более уязвимыми становятся точки роста. Это особенно заметно у мальчиков в 4, 7-8 и 12 лет. То есть в том возрасте, когда происходит очередной скачок роста, и дети начинают активно заниматься спортом. А родители – переживать за их спортивные успехи.
На что обратить внимание, как не пропустить начало заболевания или его осложнения обсудили с Ольгой Чижевской, исполнительным директором Лиги содействия развитию подиатрии.
Признаки подверженности остеохондрозамКость развивается из гиалинового хряща, в котором постепенно происходят процессы оссификации и кальцификации. И к моменту рождения единственными зонами, где остается гиалиновый хрящ, являются суставная поверхность и зона пластины роста. Причем в последней мы наблюдаем наличие хряща даже к периоду скелетного созревания. То есть эта область остается уязвимой даже во взрослом состоянии.
И к моменту рождения единственными зонами, где остается гиалиновый хрящ, являются суставная поверхность и зона пластины роста. Причем в последней мы наблюдаем наличие хряща даже к периоду скелетного созревания. То есть эта область остается уязвимой даже во взрослом состоянии.
Можно выделить три основных фактора, которые влияют на развитие остеохондроза: интенсивность роста, вес ребенка и его активность.
Вес ребенка связан с вертикальной нагрузкой на стопу и нижнюю конечность. При превышении оптимальной массы тела стопа испытывает дополнительную нагрузку, что может привести как к развитию плоскостопия, так и к более серьезным проблемам, включая остеохондроз.
«Скачки роста часто совпадают с началом занятия определенным видом спорта. Если плавание или велосипедный спорт разгружают стопу, то бег или футбол с повышенными вертикальными нагрузками наоборот способствуют развитию дегенеративных изменений.
В этом случае полезно чередовать разные виды спорта. Это поможет не только снизить риск развития остеохондроза, но и гармонично развивать скелетно-мышечный комплекс и даже позволит ребенку добиться более значимых спортивных результатов», – считает Владимир Нечаев, врач травматолог-ортопед, мануальный терапевт, спортивный врач, остеопат.
Первое, на что должен обратить внимание врач при диагностике остеохондроза нижних конечностей, это возраст пациента. Из-за физиологии развития костной системы, в разные периоды жизни наиболее уязвимыми оказываются разные отделы и кости.
Второе – клинические признаки. Чаще всего это болезненность без признаков воспаления. Если в области поражения наблюдается местное повышение температуры, покраснение кожи и отек, возможно развитие более серьезных воспалительных заболеваний.
Третий критерий диагностики – результаты рентгенологического исследования. Но они могут быть валидными только при наличии клинической картины.
Болезнь Кохлера (Kohler) – остеохондроз ладьевидной костиЭтот нечастый вариант остеохондроза, встречающийся у мальчиков в возрасте от 2 лет. В этом возрасте ребенок начинает ходить, стопа начинает испытывать весовую нагрузку и в ладьевидной кости появляются вторичные очаги оссификации.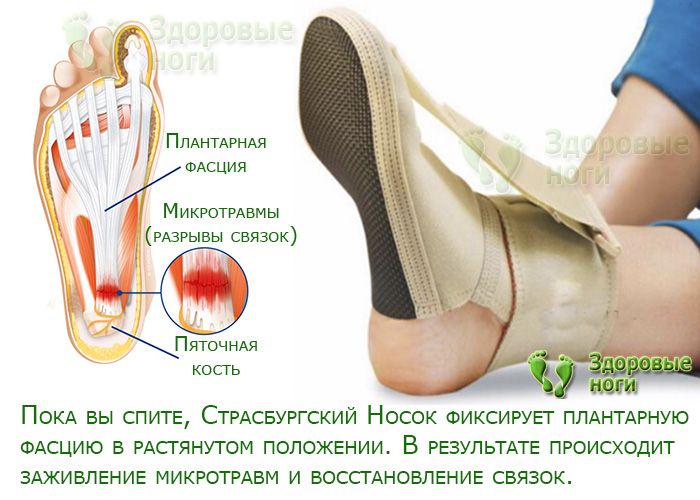
При этом заболевании ребенок просто отказывается нагружать больную ногу, отказывается ходить. Попытки осмотра и пальпации также вызывают острую боль и плач. В этой ситуации возможна только осторожная поверхностная пальпация, при которой можно обнаружить болезненность именно в области ладьевидной кости.
Главная опасность этого состояния в том, что может развитьсяа асептический некроз. Также всегда стоит помнить о риске осложнений, в том числе инфекционных. Поэтому если при обследовании выявляется не только болезненность, но и признаки воспаления – стоит особенно тщательно подойти к диагностике.
Самый простой метод лечения – наложение гипсовой иммобилизирующей повязки на 4-6 недель. Также в зависимости от индивидуального состояния стопы можно использовать ортезы, чтобы разгрузить пораженную конечность. При подборе лечения всегда нужно обращать внимание на выраженность болевого синдрома, скорость восстановления функции нижней конечности при уменьшении весовой нагрузки.
Болезнь Севера (Sever) – апофизит пяточной костиНаиболее распространенный вариант остеохондроза стопы. Заболевание развивается у детей в возрасте 7-14 лет. Именно в этом возрасте в пяточной кости появляется вторичный центр оссификации. Такие дети будут жаловаться на боль в пятке после занятий спортом и периодически появляющуюся хромоту. Если пятку сжать при осмотре, то ребенок почувствует болезненность.
Заболевание развивается у детей в возрасте 7-14 лет. Именно в этом возрасте в пяточной кости появляется вторичный центр оссификации. Такие дети будут жаловаться на боль в пятке после занятий спортом и периодически появляющуюся хромоту. Если пятку сжать при осмотре, то ребенок почувствует болезненность.
Клинически врач должен подтвердить поражение именно апофиза, а не самой пяточной кости или голеностопного сустава. Если есть признаки воспаления или ребенок жалуется на боль не только после занятий спортом, а и в другие периоды, то стоит более внимательно подойти к диагностике чтобы исключить осложнения, в том числе идиопатический ювенильный артрит.
При лечении можно рекомендовать растягивать икроножную группу мышц, использовать обувь с высоким подпяточником, чтобы разгрузить нужные отделы стопы и ростовой пластинки. При правильном подборе обуви ребенок может вернуться в спорт и продолжать тренировки.
Болезнь Перте (Perthe) – остеохондроз тазобедренного суставаЭто заболевание развивается с 4 лет и поражает детей в возрасте до 10 лет. Мальчики болеют в 4 раза чаще, чем девочки. Как правила, сустав поражается только на одной стороне, хотя возможно и двустороннее заболевание.
Мальчики болеют в 4 раза чаще, чем девочки. Как правила, сустав поражается только на одной стороне, хотя возможно и двустороннее заболевание.
Клинически проявляется хромотой. При осмотре у ребенка сокращен объем движений в пораженном тазобедренном суставе по сравнению со здоровым. На рентгенограмме видна фрагментация суставной поверхности.
Также этот вид остеохондроза может проявляться болью в колене. Поэтому если при характерных жалобах при обследовании нет никаких структурных изменений именно в области колена, стоит обратить внимание на тазобедренный сустав.
Ведение такого пациента предполагает в основном покой и разгрузку пораженной конечности. Но ребенку в таком возрасте тяжело отказаться от активности. В этом случае можно заменить бег на плавание, чтобы разгрузить тазобедренный сустав.
Болезнь Осгуда-Шляттера (Osgood Schlatter) – остеохондроз бугристости большеберцовой костиТак же как пятка – самая страдающая кость стопы, поражение колена – самый часто встречающийся остеохондроз нижней конечности.
Это состояние развивается у детей 8 лет, средний возрастной диапазон – 8-15 лет. Это заболевание называют самолимитирующим состоянием, то есть считается, что к 15-18 годам оно проходит самостоятельно. Но последние исследования говорят о том, что не все так просто.
Примерно у 40% детей спустя 2 года после начала заболевания все еще сохраняются признаки поражения. То есть ребенок все еще ограничен в своей физической активности. У 25% детей они сохраняются даже спустя 8-10 лет после манифестации.
Клинически ребенок испытывает боль при беге, занятиях спортом и любой физической активности, где требуются резкие разгибательные движения колена. При осмотре зона бугристости большеберцовой кости резко болезненна при пальпации. Надколенник может стоять достаточно высоко.
В течение первого месяца рекомендовано обеспечить покой. Также стоит сменить вид активности с бега или других видов спорта с высокой нагрузкой на колено на плавание. Хороший результат дают тренировки, направленные на укрепление четырехглавой мышцы бедра.
При дифференциальной диагностике следует помнить, что подобные признаки могут давать и более серьезные заболевания. Самое опасное из них – остеогенная саркома. В этом случае характерным симптомом будет боль по ночам.
При диагностике остеохондрозов нижних конечностей стоит обращать внимание не только на клиническую картину, но и на возраст манифестации, который характерен для определенных заболеваний. Также важно не пропустить развивающиеся осложнения, такие как идиопатический ювенильный артрит, инфекционные осложнения, травмы, остеогенную саркому или асептический некроз.
Как подчеркивает , исполнительный директор Лиги содействия развитию подиатрии, при лечении остеохондроза у детей нужно обеспечить пораженному суставу покой через ограничение физических нагрузок или наложение шины. Также можно разгрузить сустав с помощью ортопедической обуви или ортезов, сменить вид физической активности и чередовать различные виды спорта.
Боли в ногах при остеохондрозе
Боли в ногах при остеохондрозе проявляются при обострении заболевания. Иногда они бывают весьма интенсивными, но обычно имеют тянущий характер. Из-за болей ухудшается качество жизни больного, нарушается режим сна, появляется хроническая усталость. При появлении болей необходимо проводить своевременное лечение остеохондроза. При отсутствии должного лечения возможны различные осложнения — нарушение подвижности стоп, отёчность ног, многочисленные трофические язвы.
Иногда они бывают весьма интенсивными, но обычно имеют тянущий характер. Из-за болей ухудшается качество жизни больного, нарушается режим сна, появляется хроническая усталость. При появлении болей необходимо проводить своевременное лечение остеохондроза. При отсутствии должного лечения возможны различные осложнения — нарушение подвижности стоп, отёчность ног, многочисленные трофические язвы.
Причины
Боли в ногах при остеохондрозе возникают в результате повреждения спинномозговых нервов. Выделяют несколько факторов, которые могут способствовать развитию заболевания: нарушение осанки, вредные привычки, нарушение обмена веществ, стрессы, плохое питание, ожирение, малоподвижный образ жизни.
Симптомы
Боли в нижних конечностях при остеохондрозе обычно выражены слабо и являются непостоянными. Боли в ногах могут сопровождаться хрустом при движениях, онемением пальцев, побледнением ступней, неприятными ощущениями при ходьбе, увеличением суставов. Симптомы обостряются на поздних стадиях.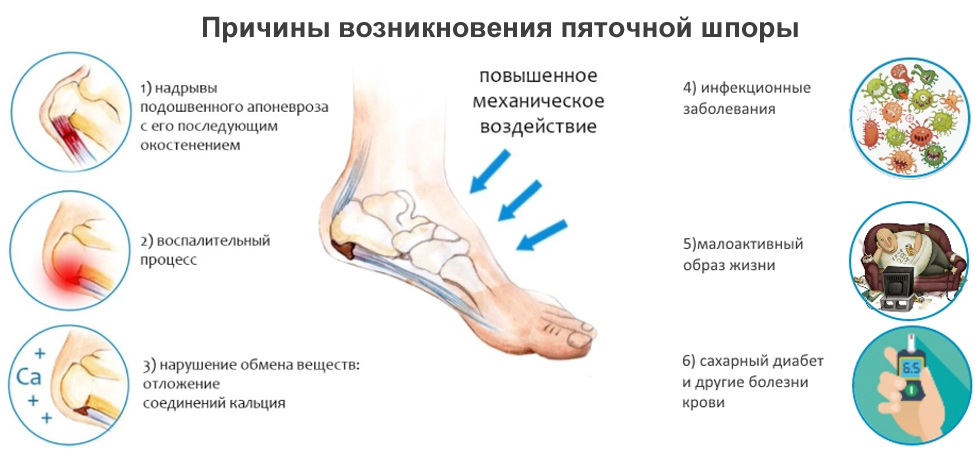 Наблюдается деформация суставов, появляются серьёзные ограничения движений.
Наблюдается деформация суставов, появляются серьёзные ограничения движений.
Диагностика
В нашей клинике успешно лечат гипертонию, остеохондроз, атеросклероз, протрузии и грыжи позвоночника, а также другие заболевания не прибегая к помощи лекарств или операций.
Для диагностики болей в ногах при остеохондрозе используются различные методики. К наиболее распространённым методам относятся врачебный осмотр пациента, рентгенография (на снимках заметны разрушительные процессы в позвоночнике, например, уменьшение высоты межпозвоночных дисков), допплерография (позволяет определить состояние сердца и сосудов), МРТ (высокоточное исследование для выявления структурных нарушений позвоночника)
Лечение
Лечение болей в ногах подбирается в зависимости от степени заболевания. Наиболее распространёнными методиками являются физиопроцедуры, лечебная физкультура (ЛФК), массаж. Все занятия должны проводиться в период ремиссии.
- Физиотерапевтические процедуры позволяют снять отёки и боли, а также замедлить разрушение хрящей в суставах.
 Основными методиками являются электрофорез, УВЧ, магнитотерапия, лазерная терапия. При назначении процедур учитываются противопоказания, такие как сердечные заболевания и онкообразования.
Основными методиками являются электрофорез, УВЧ, магнитотерапия, лазерная терапия. При назначении процедур учитываются противопоказания, такие как сердечные заболевания и онкообразования. - Упражнения ЛФК способствуют возвращению подвижности суставов и укрепляют мышцы. Занятия должны проходить без резких поворотов. Интенсивность занятий можно увеличить со временем.
- Массаж должен выполняться только квалифицированным специалистом. Он улучшает кровоток, устраняет застой в нижних конечностях, выводит токсины из организма. При массажных процедурах можно использовать разогревающие мази.
Профилактика
Для профилактики остеохондроза необходимо полноценное питание, которое включает большое количество белка, фосфора и кальция, а острые блюда, жиры и копчёности нужно свести к минимуму. Также следует избегать поднятия тяжестей, вести активный образ жизни, регулярно заниматься зарядкой, отказаться от курения и алкоголя.
Боли в ногах при остеохондрозе могут доставить человеку множество неприятностей.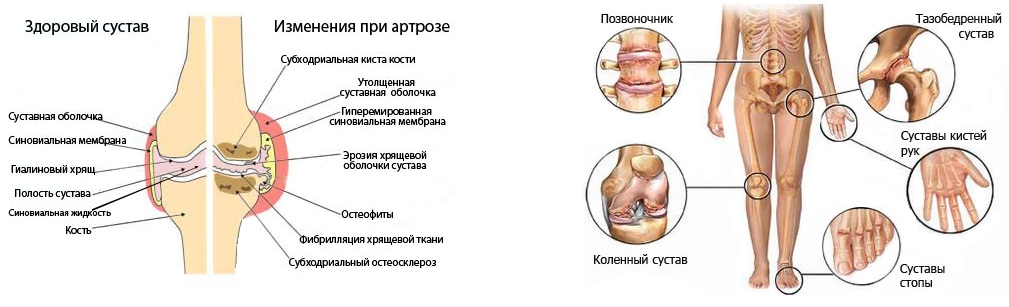 Своевременное лечение остеохондроза помогает устранить болевые ощущения.
Своевременное лечение остеохондроза помогает устранить болевые ощущения.
Остеохондроз стопы и голеностопного сустава
ОСТЕОХОНДРАЛЬНЫЕ ПОРАЖЕНИЯ ТАРАННОЙ КАРАННЫ
Трансхондральные поражения представляют собой локализованное повреждение суставной поверхности сустава, а также соответствующей части субхондральной кости. В голеностопном суставе повреждение обычно представлено сдавлением или отрывом отломка от купола таранной кости. Если после травмы не происходит заживления, фрагмент может подвергнуться аваскулярному некрозу. Эти поражения могут быть источником сильной боли и инвалидности. Когда-то считавшиеся необычными, трансхондральные поражения таранной кости диагностируются с большей частотой в результате повышения осведомленности врачей и более точных методов диагностической визуализации.
Ранние исследователи, наблюдавшие свободные тела в суставах, предположили возможные факторы, вызывающие отделение небольшого фрагмента кости и хряща от суставной поверхности. О первом случае свободного фрагмента кости в голеностопном суставе сообщил Александр Мунро в 1856 г. Хотя не было предпринято никаких попыток классифицировать процесс, он все же полагал, что поражение было результатом травмы (1). Konig в 1888 г., по-видимому, положил начало полемике относительно этиологии этих поражений, когда он сообщил о нескольких неприкрепленных телах в коленном суставе (2). В ту эпоху эти фрагменты называли артрофитами или подвижными телами (3). Кениг считал, что эти поражения не могли быть вызваны каким-либо известным заболеванием, опухолью или травмой, и решил, что этиология связана с воспалительным процессом поверхностей суставов, который привел к спонтанному некрозу части кости. Он назвал эти поражения «рассекающим остеохондритом» (2). Слово «остеохондрит» относится к воспалительному процессу в суставе, а «диссеканс» происходит от латинского слова dessec, что означает «отделять» (3). Более поздние исследователи не обнаружили во фрагментах воспалительных клеток; однако термин остеохондрит сохраняется и по сей день (3).
О первом случае свободного фрагмента кости в голеностопном суставе сообщил Александр Мунро в 1856 г. Хотя не было предпринято никаких попыток классифицировать процесс, он все же полагал, что поражение было результатом травмы (1). Konig в 1888 г., по-видимому, положил начало полемике относительно этиологии этих поражений, когда он сообщил о нескольких неприкрепленных телах в коленном суставе (2). В ту эпоху эти фрагменты называли артрофитами или подвижными телами (3). Кениг считал, что эти поражения не могли быть вызваны каким-либо известным заболеванием, опухолью или травмой, и решил, что этиология связана с воспалительным процессом поверхностей суставов, который привел к спонтанному некрозу части кости. Он назвал эти поражения «рассекающим остеохондритом» (2). Слово «остеохондрит» относится к воспалительному процессу в суставе, а «диссеканс» происходит от латинского слова dessec, что означает «отделять» (3). Более поздние исследователи не обнаружили во фрагментах воспалительных клеток; однако термин остеохондрит сохраняется и по сей день (3).
Kappis (4) в 1922 году первым применил термин «рассекающий остеохондрит» к голеностопному суставу. Ренду (5) в 1932 г. сообщил о случае свободного тела в голеностопном суставе, который он назвал внутрисуставным фрагментарным переломом таранной кости, указывая на его убежденность в том, что причиной повреждения была травма. Поражение, описанное Рендю, было основано на рентгенограммах и похоже на то, что описано Мунро (1) и Капписом (4). Fairbanks (6) в 1933 г. писал, что травма без каких-либо основных сосудистых нарушений была единственной причиной рыхлых внутрисуставных тел. В 1953, Roden et al (7) представили первое тщательное исследование, в котором рассмотрели 55 случаев костно-хрящевых поражений таранной кости. В результате их исследования было получено значительное количество информации, которая окажется полезной для понимания этого состояния. Они определили, что латеральные поражения чаще возникают из-за травмы, редко заживают спонтанно и вызывают больше симптомов, чем медиальные.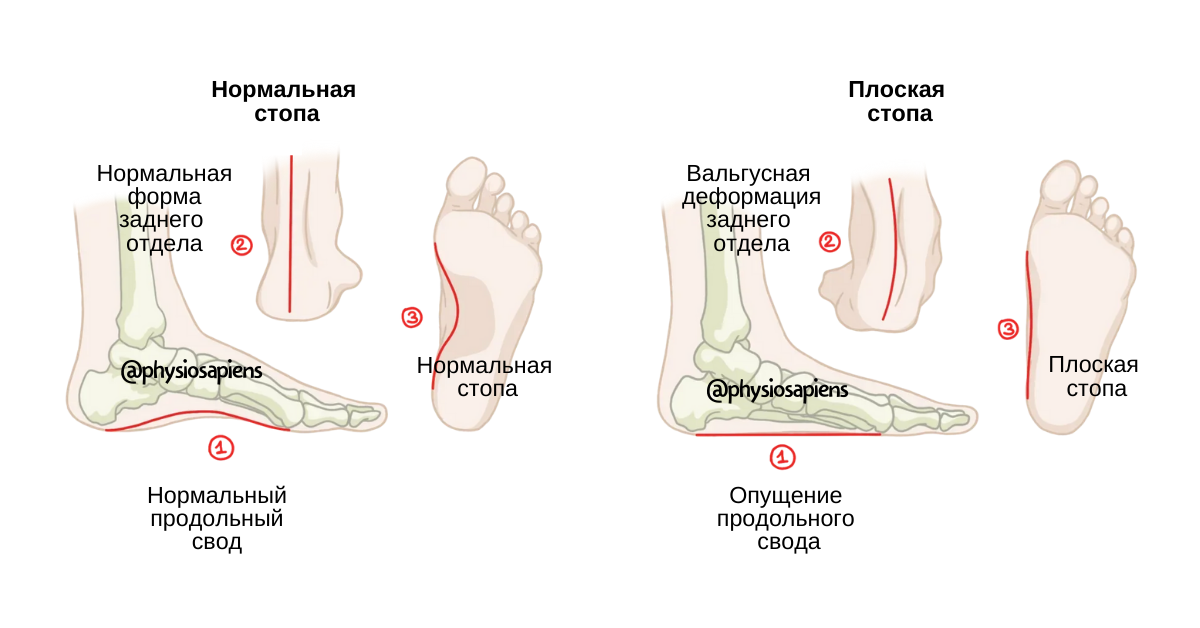 Хирургическое лечение было рекомендовано при боковых поражениях, поскольку они часто приводили к артритическим изменениям в суставе (7).
Хирургическое лечение было рекомендовано при боковых поражениях, поскольку они часто приводили к артритическим изменениям в суставе (7).
Более глубокое понимание остеохондральных поражений было получено в 1959 г. в исследовании Berndt и Harty (8). Исследователи экспериментально установили на трупных конечностях, что травма привела к локальным переломам купола таранной кости. Они также смогли определить механизм повреждения как медиальных, так и латеральных поражений. Пытаясь отразить этиологию травмы и локализацию повреждения на куполе таранной кости, они ввели термин «трансхондральный перелом» для описания костно-хрящевых поражений в этой области. О’Донохью (9, 10 и 11) опубликовал несколько статей, в которых обсуждались костно-хрящевые фрагменты в колене, и поддержал концепцию травматической этиологии. Считалось, что многое из того, что он написал, применимо и к поражениям, обнаруженным на лодыжке (12).
Несмотря на то, что предшествовавшая травма, по-видимому, является этиологией большинства поражений, другие продолжали полагать, что возможна альтернативная этиология из-за множества сообщений о трансхондральных поражениях без травм в анамнезе (13). Некоторые авторы полагали, что латеральные поражения, вероятно, были вызваны травматическими событиями, но подвергали сомнению этиологию медиальных поражений купола таранной кости (7,14). Flick и Gould (15) изучили медицинскую литературу и определили, что 9Сообщалось, что 8% латеральных поражений и только 70% медиальных поражений были вызваны травмой. Campbell и Ranawat считали, что ишемические изменения могут играть роль в развитии остеохондральных поражений. Они смогли продемонстрировать на своих образцах, что костный инфаркт предшествует патологическому перелому через субхондральную кость, и предположили, что повторяющиеся незначительные эпизоды травмы могут привести к перелому и возможному отделению костно-хрящевого фрагмента (16).
Некоторые авторы полагали, что латеральные поражения, вероятно, были вызваны травматическими событиями, но подвергали сомнению этиологию медиальных поражений купола таранной кости (7,14). Flick и Gould (15) изучили медицинскую литературу и определили, что 9Сообщалось, что 8% латеральных поражений и только 70% медиальных поражений были вызваны травмой. Campbell и Ranawat считали, что ишемические изменения могут играть роль в развитии остеохондральных поражений. Они смогли продемонстрировать на своих образцах, что костный инфаркт предшествует патологическому перелому через субхондральную кость, и предположили, что повторяющиеся незначительные эпизоды травмы могут привести к перелому и возможному отделению костно-хрящевого фрагмента (16).
Другие предполагают, что существуют две формы остеохондрита. Один тип развивается у детей старшего возраста и взрослых и связан с травматическим событием. Другая форма, встречающаяся у детей, обусловлена локализованным аваскулярным некрозом. Smith (17) отметил, что эти поражения часто были множественными, а иногда и семейными. Смайли также считал, что существует как взрослая, так и ювенильная форма остеохондрита. Высказано предположение, что в основе ювенильной формы лежит аномалия окостенения, чаще всего энхондральный дизостоз, приводящий к развитию добавочного центра окостенения. Если последующая травма нарушала кровоснабжение этой области, результирующая ишемия приводила к остеохондриту (18).
Смайли также считал, что существует как взрослая, так и ювенильная форма остеохондрита. Высказано предположение, что в основе ювенильной формы лежит аномалия окостенения, чаще всего энхондральный дизостоз, приводящий к развитию добавочного центра окостенения. Если последующая травма нарушала кровоснабжение этой области, результирующая ишемия приводила к остеохондриту (18).
Другие возможные этиологии остеохондрита, которые были предложены, включали врожденную предрасположенность к
асептическому отделению суставного костно-хрящевого фрагмента (19), другие врожденные или наследственные факторы (20), эмболию эпифизарных артерий (21), эндокринный дисбаланс в время полового созревания (22) и аномалии развития (23). Axhausen (24) полагал, что удар с противоположных суставных поверхностей повреждает кровеносные сосуды, что приводит к некрозу области, снабжаемой этими сосудами. Это привело к абсорбции, отделению и, в конечном итоге, выдавливанию мертвой части кости в сустав. В одном исследовании, в котором оценивались члены семей 34 пациентов с расслаивающим остеохондритом и 86 их родственников первой степени родства, только у 1 дополнительного человека был обнаружен рассекающий остеохондрит. Ассоциация с другими формами рассекающего остеохондрита, эндокринными нарушениями и карликовостью не может быть продемонстрирована (25).
Ассоциация с другими формами рассекающего остеохондрита, эндокринными нарушениями и карликовостью не может быть продемонстрирована (25).
ЗАБОЛЕВАЕМОСТЬ
Сообщалось, что трансхондральные поражения составляют 0,09% всех переломов (26) и 1% всех переломов таранной кости (27). По оценкам, распространенность составляет 0,002 случая на 1000 человек (28). Рассекающий остеохондрит таранной кости составляет 4% всех зарегистрированных случаев остеохондрита (29), а остеохондральные поражения таранной кости являются вторым наиболее частым местом для этого процесса после латеральной поверхности медиального надмыщелка колена (30).
Число зарегистрированных случаев трансхондральных поражений, вероятно, намного ниже фактической заболеваемости. В одном исследовании врачи отделения неотложной помощи неправильно диагностировали у семи из 16 пациентов растяжение связок голеностопного сустава, однако ретроспективный анализ рентгенограмм показал трансхондральный перелом (15). В некоторых случаях средняя продолжительность времени от появления симптомов до постановки диагноза составляет 36 месяцев (31). Трансхондральные поражения были обнаружены у 6,5% из 133 пациентов, получавших лечение по поводу растяжения связок голеностопного сустава. Большинство этих травм произошло, когда пациенты занимались спортом (32). Таким образом, кажется логичным, что в некоторых случаях сопутствующий костно-хрящевой перелом остается недиагностированным без высокого индекса подозрения.
Трансхондральные поражения были обнаружены у 6,5% из 133 пациентов, получавших лечение по поводу растяжения связок голеностопного сустава. Большинство этих травм произошло, когда пациенты занимались спортом (32). Таким образом, кажется логичным, что в некоторых случаях сопутствующий костно-хрящевой перелом остается недиагностированным без высокого индекса подозрения.
Сообщалось о трансхондральных поражениях у обоих полов, но незначительное большинство наблюдается у мужчин в возрасте от второго до четвертого десятилетия жизни. Средний возраст составляет около 25 лет, хотя случаи также были зарегистрированы у пациентов на пятом и шестом десятилетиях жизни (15, 29, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42 и 43). ). Хотя они встречаются не так часто, у детей также могут быть трансхондральные травмы. Wester и коллеги (44) сообщили, что среди 18 детей, участвовавших в его исследовании, возраст варьировал от 2 до 14 лет, при этом средний возраст на момент получения травмы составлял 9 лет. годы. В аналогичном отчете с участием 18 подростков с трансхондральными поражениями возраст пациентов варьировал от 9,9 до 16 лет, при этом средний возраст составлял 14,2 года (45). Существуют некоторые разногласия относительно заживления трансхондральных поражений у детей. Было высказано предположение, что поражения зажили спонтанно (28), но в одном отчете было описано три случая трансхондральных поражений у детей, которые не зажили при консервативном лечении (15).
годы. В аналогичном отчете с участием 18 подростков с трансхондральными поражениями возраст пациентов варьировал от 9,9 до 16 лет, при этом средний возраст составлял 14,2 года (45). Существуют некоторые разногласия относительно заживления трансхондральных поражений у детей. Было высказано предположение, что поражения зажили спонтанно (28), но в одном отчете было описано три случая трансхондральных поражений у детей, которые не зажили при консервативном лечении (15).
КЛИНИЧЕСКАЯ КАРТИНА
Из-за хронического характера многих трансхондральных поражений таранной кости и различной степени тяжести повреждения купола таранной кости специфических патогномоничных клинических признаков этого состояния нет. Поскольку механизм повреждения, связанный с повреждениями, заключается в инверсии голеностопного сустава, у пациентов с растяжением связок голеностопного сустава в анамнезе можно заподозрить трансхондральные переломы. Большое количество пациентов с поражением купола таранной кости вспоминают о предыдущей травме лодыжки (31, 37), а в некоторых случаях это был перелом лодыжки (37).
При недавних острых травмах у пациента могут проявляться обычные признаки и симптомы растяжения связок голеностопного сустава, включающие боль, отек, экхимоз, эритему и снижение подвижности в результате ограждения. Постепенно симптомы, связанные с острым растяжением связок голеностопного сустава, будут улучшаться, но если присутствует трансхондральное поражение, голеностопный сустав может никогда не стать полностью бессимптомным или пациент может чувствовать себя хорошо в течение определенного периода времени только для того, чтобы развить более поздние симптомы (45,46).
Симптомы хронического трансхондрального поражения могут включать боль, отек, блокировку сустава, тугоподвижность, нестабильность голеностопного сустава (45,46), хронические растяжения связок без блокировки голеностопного сустава, функциональную нестабильность голеностопного сустава и снижение объема движений с синовиальным выпотом (45). В одном крупном исследовании наиболее распространенными симптомами оказались боль при физической активности, ежедневная боль, еженедельная боль, ночная боль и отек.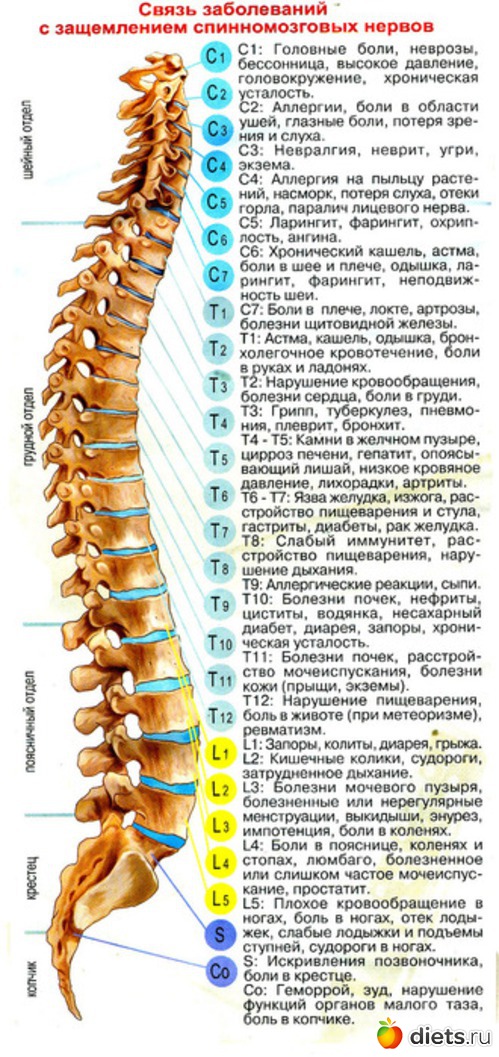 Физикальное обследование оказалось не очень полезным в диагностике трансхондральных поражений. У 50% пациентов отмечалось незначительное уменьшение объема движений в голеностопном суставе, подошвенное сгибание обычно было снижено. Двадцать процентов пациентов также имели некоторую потерю подвижности подтаранного сустава (31).
Физикальное обследование оказалось не очень полезным в диагностике трансхондральных поражений. У 50% пациентов отмечалось незначительное уменьшение объема движений в голеностопном суставе, подошвенное сгибание обычно было снижено. Двадцать процентов пациентов также имели некоторую потерю подвижности подтаранного сустава (31).
КЛАССИФИКАЦИЯ
Наиболее общепринятой классификацией трансхондральных поражений является система, разработанная Berndt и Harty (рис. 54.1). Трансхондральные поражения были разделены на четыре стадии: I стадия представляет собой небольшой участок субхондральной компрессии кости, II стадия — частично отслоившийся костно-хрящевой фрагмент, III стадия — полностью отслоившийся фрагмент без смещения и остающийся в кратере, IV стадия — костно-хрящевой фрагмент полностью оторвавшийся и смещенный от кратера (8). Трудно точно диагностировать поражения I степени и дифференцировать степени I, II и III на стандартных рентгенограммах. В
, Лумер и др., используя сканирование костей и компьютерную томографию (КТ), отметили, что у 77% пациентов система Берндта и Харти оказалась неадекватной для описания поражений.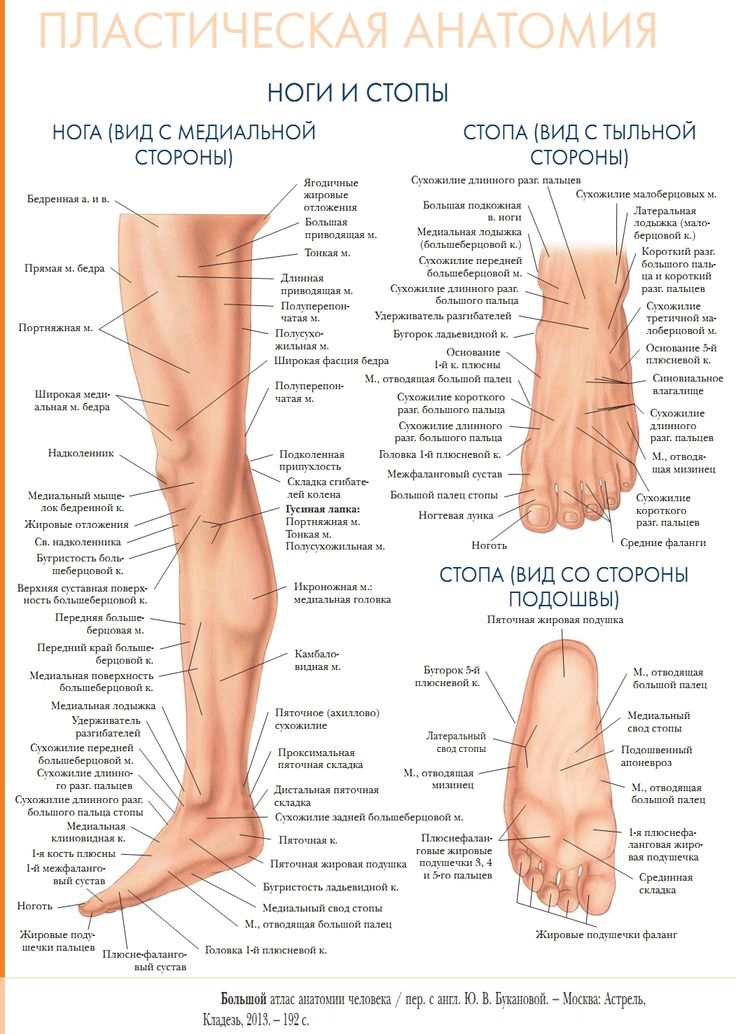 Основываясь на своих выводах, они добавили к классификации пятую категорию, которую назвали рентгенопрозрачным дефектом. Это было наиболее распространенным поражением, наблюдаемым в их исследовании (31).
Основываясь на своих выводах, они добавили к классификации пятую категорию, которую назвали рентгенопрозрачным дефектом. Это было наиболее распространенным поражением, наблюдаемым в их исследовании (31).
Рисунок 54.1. Четыре стадии костно-хрящевого поражения таранной кости по классификации Берндта и Харти. |
Дополнительные системы классификации были разработаны на основе результатов магнитно-резонансной томографии (МРТ) и артроскопии голеностопного сустава (37,47,48). Pritsch и коллеги разработали артроскопическую систему классификации, которая, по их мнению, была более значимой, чем рентгенологические проявления поражений. Эта система основывалась на состоянии суставного хряща таранной кости. I степень — неповрежденный, твердый, блестящий хрящ; степень II не повреждена, но мягкий хрящ; и степень III — изношенный хрящ. Авторы определили, что увеличение рентгенологической стадии поражения не обязательно является предиктором увеличения фрагментации или ослабления поражения (48). Феркель и др. (49) разработал классификацию стадий КТ: I стадия, кистозное поражение в пределах купола таранной кости; стадия IIA, кистозное поражение, сообщающееся с поверхностью купола таранной кости; стадия IIB, открытое поражение суставной поверхности с вышележащим несмещенным отломком; стадия III, поражение без смещения с просветлением; и стадия IV смещенный фрагмент.
Феркель и др. (49) разработал классификацию стадий КТ: I стадия, кистозное поражение в пределах купола таранной кости; стадия IIA, кистозное поражение, сообщающееся с поверхностью купола таранной кости; стадия IIB, открытое поражение суставной поверхности с вышележащим несмещенным отломком; стадия III, поражение без смещения с просветлением; и стадия IV смещенный фрагмент.
Ly и Fallat (37) разработали упрощенную систему оценивания с хорошим практическим применением. Поражение I стадии представляет собой недавний перелом купола таранной кости. Фрагмент может оставаться в удовлетворительном положении или может быть смещен. Стадия II представляет собой более старое хроническое поражение, которое еще не зажило. Произошел аваскулярный некроз субхондральной кости, и это поражение видно как светлое на стандартных рентгенограммах.
РАСПОЛОЖЕНИЕ ПОРАЖЕНИЙ
Berndt и Harty первыми определили характерные места трансхондральных поражений купола таранной кости. В своем трупном исследовании они продемонстрировали, что 43,7% поражений возникали латерально, большинство из которых находились в средней трети купола таранной кости.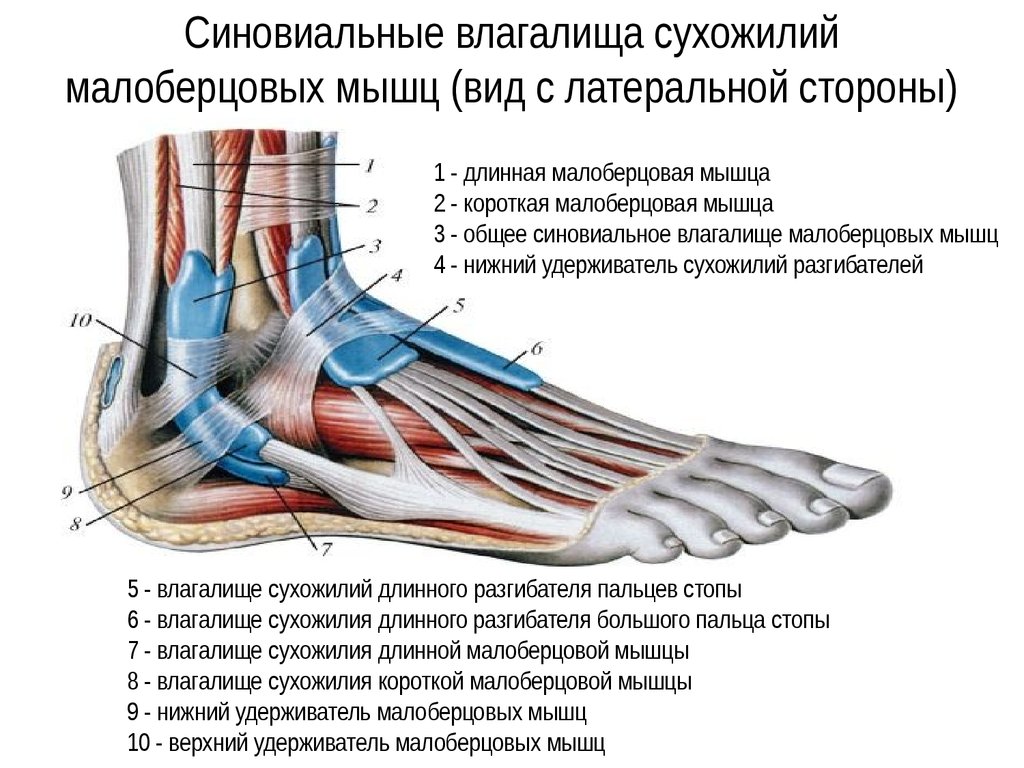 Медиальные поражения встречались в 56,3% случаев, которые обычно локализовались в задней трети медиального края купола таранной кости (рис. 54.2) (8). Большинство исследователей сообщают об аналогичной частоте и характере расположения, хотя некоторые авторы считают, что латеральное расположение является наиболее распространенным, и было отмечено, что поражения развиваются в разных местах на каждой границе купола таранной кости (12, 14, 15, 15). 37,50,51). Сообщалось также о центральных трансхондральных поражениях, хотя и с очень низкой частотой (14, 52, 53), и сообщалось о случаях как медиальных, так и латеральных поражений в одной и той же лодыжке (34, 37). Loomer и коллеги (31) обнаружили, что локализация трансхондральных поражений более разнообразна, чем сообщалось ранее, причем локализация варьирует по периферии купола таранной кости. Наиболее частыми локализациями были переднебоковой квадрант, за которым следовал задний медиальный квадрант (рис. 54.3) (46). Raikin et al ретроспективно проанализировали МРТ-исследования 424 пациентов и обнаружили, что медиальный центральный купол таранной кости был наиболее часто вовлечен в 53,0% поражений, расположенных там.
Медиальные поражения встречались в 56,3% случаев, которые обычно локализовались в задней трети медиального края купола таранной кости (рис. 54.2) (8). Большинство исследователей сообщают об аналогичной частоте и характере расположения, хотя некоторые авторы считают, что латеральное расположение является наиболее распространенным, и было отмечено, что поражения развиваются в разных местах на каждой границе купола таранной кости (12, 14, 15, 15). 37,50,51). Сообщалось также о центральных трансхондральных поражениях, хотя и с очень низкой частотой (14, 52, 53), и сообщалось о случаях как медиальных, так и латеральных поражений в одной и той же лодыжке (34, 37). Loomer и коллеги (31) обнаружили, что локализация трансхондральных поражений более разнообразна, чем сообщалось ранее, причем локализация варьирует по периферии купола таранной кости. Наиболее частыми локализациями были переднебоковой квадрант, за которым следовал задний медиальный квадрант (рис. 54.3) (46). Raikin et al ретроспективно проанализировали МРТ-исследования 424 пациентов и обнаружили, что медиальный центральный купол таранной кости был наиболее часто вовлечен в 53,0% поражений, расположенных там.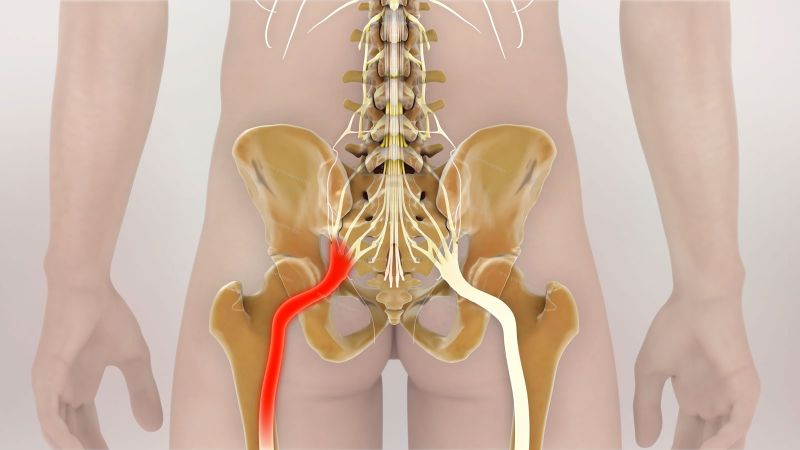 Боковая центральная часть купола таранной кости была второй, представляя 25,7% поражений (54) (рис. 54.4).
Боковая центральная часть купола таранной кости была второй, представляя 25,7% поражений (54) (рис. 54.4).
Постеромедиальные поражения обычно более стабильны и менее симптоматичны, чем латеральные поражения. |
Частота возникновения каждой стадии трансхондрального поражения обычно не сообщалась до недавнего времени. Loomer и коллеги (31) сообщили, что 2% случаев в их серии были компрессионными травмами, 1% — частичными переломами, 13% — полными, но без смещения, и 7% — переломами со смещением. Ly и Fallat (37) сообщили, что поражения стадии II были наиболее распространенными среди латеральных поражений, а стадия III была наиболее частым срединным поражением.
МЕХАНИЗМ ТРАВМЫ
Латеральные трансхондральные поражения возникают при воздействии инверсионной силы на стопу, согнутую в тыльном направлении. Более широкая передняя часть таранной кости вклинивается в впадину лодыжки, в результате чего передняя и средняя части латеральной границы купола таранной кости упираются в латеральную лодыжку. Это приводит к локализованной области субхондральной компрессии кости, характерной для I стадии поражения. Для развития этого поражения нет необходимости разрывать боковые связки. При приложении большей силы связки разрываются, что приводит к продолжению инверсии и ротации таранной кости, создавая эффект сдвига, поскольку таранная кость
Это приводит к локализованной области субхондральной компрессии кости, характерной для I стадии поражения. Для развития этого поражения нет необходимости разрывать боковые связки. При приложении большей силы связки разрываются, что приводит к продолжению инверсии и ротации таранной кости, создавая эффект сдвига, поскольку таранная кость
истирает малоберцовую кость. Это может привести к характерному неглубокому поражению пластинчатой формы, которое часто наблюдается на латеральной стороне таранной кости (8). Фрагмент поднимается с латеральной поверхности таранной кости, и перелом распространяется на небольшое расстояние поперек свода до тех пор, пока сила не рассеется или пока фрагмент не сместится. По-видимому, чаще встречаются латеральные поражения стадии IV, и свободные фрагменты могут быть причиной усиления симптомов, связанных с латеральными поражениями.
(Перерисовано по материалам Loomer R, Fisher C, Lloyd-Smith R, et al. Рис. 54.4 Анатомическая девятизонная сетка на куполе таранной кости. Зоны 1, 4 и 7 представляют собой медиальную таранную кость, а зоны 1, 2 и 3 представляют собой переднюю таранную кость. (Перерисовано после Elias I, Zoga AC, Morrison WB, et al. Остеохондральные поражения таранной кости: локализация и морфологические данные 424 пациентов с использованием новой схемы анатомической сетки. Foot Ankle Int 2007; 28:154-161.) |
Медиальные трансхондральные поражения, охватывающие заднюю треть купола таранной кости, могут быть вызваны инверсией и подошвенными сгибающими силами голеностопного сустава с сопутствующим латеральным вращением большеберцовой кости на таранной кости. Когда стопа находится в этом положении, инверсия и ротация таранной кости приводят к тому, что медиальная граница купола таранной кости упирается либо в медиальную лодыжку, либо в заднюю губу большеберцовой кости. По мере того, как сила продолжается, латеральные связки голеностопного сустава натягиваются, и движение в поперечной плоскости преобразуется в движение в сагиттальной плоскости, что приводит к большему столкновению большеберцовой кости с таранной костью (8). Повреждения медиального купола обычно глубокие и чашеобразные по внешнему виду (рис. 54.5). Как и при боковых поражениях, дефект I стадии может возникать без разрыва коллатеральных связок голеностопного сустава. При дальнейшем усилии задние волокна дельтовидной связки могут порваться, создавая большую нестабильность. Кроме того, компрессия таранной кости по отношению к большеберцовой кости может привести к отрыву костно-хрящевого фрагмента от таранной кости, что приведет к другим стадиям трансхондрального поражения (8, 34, 46).
По мере того, как сила продолжается, латеральные связки голеностопного сустава натягиваются, и движение в поперечной плоскости преобразуется в движение в сагиттальной плоскости, что приводит к большему столкновению большеберцовой кости с таранной костью (8). Повреждения медиального купола обычно глубокие и чашеобразные по внешнему виду (рис. 54.5). Как и при боковых поражениях, дефект I стадии может возникать без разрыва коллатеральных связок голеностопного сустава. При дальнейшем усилии задние волокна дельтовидной связки могут порваться, создавая большую нестабильность. Кроме того, компрессия таранной кости по отношению к большеберцовой кости может привести к отрыву костно-хрящевого фрагмента от таранной кости, что приведет к другим стадиям трансхондрального поражения (8, 34, 46).
Центрально расположенные трансхондральные поражения таранной кости встречаются редко, и механизм повреждения до конца не изучен. Теоретически центральное поражение возникает при приложении нагрузки со смещением таранной кости вперед или смещением большеберцовой кости кзади с последующим тыльным сгибанием стопы (52,53). Внезапный удар таранной костью в положении подошвенного сгибания и со смещением кпереди может привести к центральному трансхондральному дефекту (53).
Внезапный удар таранной костью в положении подошвенного сгибания и со смещением кпереди может привести к центральному трансхондральному дефекту (53).
ТЕЧЕНИЕ ПОРАЖЕНИЯ
Инверсионные растяжения связок голеностопного сустава, по-видимому, являются инициирующим событием, которое приводит к костно-хрящевым переломам купола таранной кости. При этом типе травмы перелом распространяется через хрящ в субхондральную кость, что приводит к разрушению фрагмента перелома. Если фрагмент стабилен и подвижность устранена, заживление может произойти, когда капиллярные зачатки пересекают линию перелома и проникают в костный фрагмент. Если во время заживления происходит движение, то на линии перелома образуется фиброзная ткань, которая действует как барьер, предотвращающий врастание капилляров (8). Таким образом, фрагмент становится секвестрированным, что по существу приводит к несращению. Вскоре развивается аваскулярный некроз, который можно увидеть на рентгенограммах в виде локализованной области просветления в куполе таранной кости (рис. 54.6).
54.6).
Медиальные поражения глубокие и чашеобразные, тогда как латеральные поражения неглубокие и вафельные. |
Суставной хрящ, покрывающий таранную кость, по-разному реагирует на травму и процесс заживления. Из-за эластичности хряща он может оставаться прикрепленным к соседнему хрящу, что чаще наблюдается при компрессионных травмах, или может быть сильно поврежден и смещен, как при травмах сдвига. В любом случае хрящ, покрывающий костный фрагмент, может сохранять жизнеспособность еще долгое время после того, как костный сегмент подвергся аваскулярному некрозу. Воспалительная фаза заживления не происходит в хряще из-за аваскуляризации этой ткани. Однако хондроциты способны получать питание из синовиальной жидкости и могут оставаться жизнеспособными в течение значительного периода времени (55).
Повреждение хряща во время травмы или повторная нагрузка по мере того, как субхондральная кость некротизируется и резорбируется, приводит к неравномерной нагрузке на таранную кость, вызывая еще большую травму (56). Эта проблема может привести к тому, что хрящ станет мягким, рыхлым, потрескавшимся и обесцвеченным, с последующими дегенеративными артритическими изменениями (12,57).
Эта проблема может привести к тому, что хрящ станет мягким, рыхлым, потрескавшимся и обесцвеченным, с последующими дегенеративными артритическими изменениями (12,57).
ИЗОБРАЖЕНИЕ
В некоторых случаях рентгенограммы могут выявить трансхондральный перелом у пациентов с острой травмой или с более хроническими симптомами голеностопного сустава (31,34,41,46,51,58). Тем не менее, небольшие незаметные поражения могут не визуализироваться на рентгенограммах или могут быть пропущены. Повреждения стадии I могут не демонстрировать каких-либо специфических изменений на стандартных рентгенограммах (59). Единственной аберрацией может быть изменение плотности кости на краю купола таранной кости (60). У многих пациентов поражения не видны на стандартных рентгенограммах до тех пор, пока они не перейдут в более тяжелую стадию (58). Кроме того, стандартные рентгенограммы могут иметь мало значения не только для выявления поражений, но и для определения их размера и формы (61) (рис. 54. 7)
7)
Для тщательной оценки купола таранной кости рекомендуется переднезадняя, боковая и врезная проекции. Трансхондральное поражение лучше визуализируется в прорези и иногда в переднезадней проекции (60). Боковая проекция редко полезна для диагностики трансхондрального поражения, но может выявить синовиальный выпот, что может указывать на этот тип процесса (60). Лучшей визуализации поражений медиального купола таранной кости можно добиться, взяв переднезаднюю проекцию с подошвенно согнутой стопой. Боковые поражения легче визуализировать, когда стопа находится в тыльном согнутом положении (62). Виды с инверсией напряжения также могут помочь в выявлении повреждений купола таранной кости (14, 63, 64 и 65). В одном исследовании, когда наклон таранной кости превышал 18 градусов, трансхондральные поражения были отмечены в 77% случаев.
Рис. 54.7 Стандартные рентгенограммы, указывающие на медиальный костно-хрящевой дефект. |
Когда остеонекроз развился на стадиях поражения I, II или III, рентгенограммы могут демонстрировать просветление, которое можно увидеть на вершине купола таранной кости, иногда со склеротическим слоем вследствие ремоделирования субхондральной кости (65 ). Иногда в центре кратера также имеется небольшая склеротическая область, которую называют очагом или деформацией «бычий глаз». Это представляет собой секвестрированную часть костно-хрящевого фрагмента, которая еще не рассосалась (65) (рис. 54.8).
КТ высокого разрешения оказалась очень надежной при выявлении и оценке трансхондральных поражений (рис. 54.9). Качество изображения превосходит томографию (61), а КТ также обеспечивает лучший контраст между костями и мягкими тканями (61, 66). Разрезы изображений делаются с интервалом 2 мм, чтобы получить изображение, отражающее истинные размеры поражения (40). Это позволяет врачу определить точный размер, форму и расположение поражения. Простые рентгенограммы показывают меньший размер дефекта (43). КТ также можно получить, когда пациент носит гипсовую повязку (37).
КТ также можно получить, когда пациент носит гипсовую повязку (37).
МРТ также дает изображения поперечного сечения таранной кости и предлагает точную, неинвазивную, безрадиационную оценку местоположения и размера трансхондрального поражения (рис. 54.10) (61, 67). Уникальной особенностью МРТ является то, что она предоставляет информацию относительно стабильности поражения и позволяет оценить состояние суставного хряща (15,48). Частично прикрепленные трансхондральные поражения II степени демонстрируют неравномерную зону высокого сигнала на Т2-взвешенных изображениях в месте соединения фрагмента и тела таранной кости. Полностью отделенный фрагмент, связанный с травмами III стадии, демонстрирует кольцо жидкости, окружающее поражение (35). Артроскопия голеностопного сустава и артротомия подтвердили точность и эффективность МРТ в дифференциации поражений стадии II от стадии III (47,66,67).
Хотя МРТ используется для определения стадии костно-хрящевого поражения и оценки суставного хряща, она не позволяет определить кору так же хорошо, как КТ. В современной литературе было проведено много сравнений КТ, МРТ и диагностической артроскопии с КТ и МРТ, что дало сходные
В современной литературе было проведено много сравнений КТ, МРТ и диагностической артроскопии с КТ и МРТ, что дало сходные
результаты (59, 68, 69). Было показано, что МРТ имеет небольшое диагностическое преимущество, когда рентгенограммы и клинические данные не являются диагностическими, и КТ предпочтительнее, если было диагностировано костно-хрящевое поражение (58, 68).
Рисунок 54.8 Типичный очаг (стрелка). Это представляет собой часть кортикальной кости, которая не полностью резорбирована. |
они четко определяют локализацию и размер поражения. |
Трехфазное сканирование костей также может быть эффективным методом, когда рентгенограммы отрицательные, но есть подозрение на трансхондральное поражение (47,64). Сканирование костей высокочувствительно, однако оно не является специфичным для типа костной патологии, которая может присутствовать (рис. 54.11). Новообразования, аваскулярный некроз таранной кости и инфекция приводят к повышенному поглощению радиофармпрепарата (60). Считалось, что наличие гиперемии в фазе пула крови на 100 % чувствительно и на 83 % специфично для остеохондральных переломов таранной кости (70). Сканирование костей очень точное, если оно выполнено по крайней мере через 48 часов после травмы, но когда оно выполняется в течение 48 часов после травмы, оно может давать ложноотрицательные результаты (61). Положительный результат сканирования кости может подтвердить наличие костной патологии таранной кости, и для дальнейшей оценки поражения купола таранной кости может потребоваться дополнительное обследование с помощью КТ или МРТ (64).
Сканирование костей высокочувствительно, однако оно не является специфичным для типа костной патологии, которая может присутствовать (рис. 54.11). Новообразования, аваскулярный некроз таранной кости и инфекция приводят к повышенному поглощению радиофармпрепарата (60). Считалось, что наличие гиперемии в фазе пула крови на 100 % чувствительно и на 83 % специфично для остеохондральных переломов таранной кости (70). Сканирование костей очень точное, если оно выполнено по крайней мере через 48 часов после травмы, но когда оно выполняется в течение 48 часов после травмы, оно может давать ложноотрицательные результаты (61). Положительный результат сканирования кости может подтвердить наличие костной патологии таранной кости, и для дальнейшей оценки поражения купола таранной кости может потребоваться дополнительное обследование с помощью КТ или МРТ (64).
Суставной остеохондроз нижних конечностей
История болезни: 9-летний мальчик поступил на визуализацию с 4-недельной историей болей в медиальной и латеральной лодыжках и прогрессирующего отека.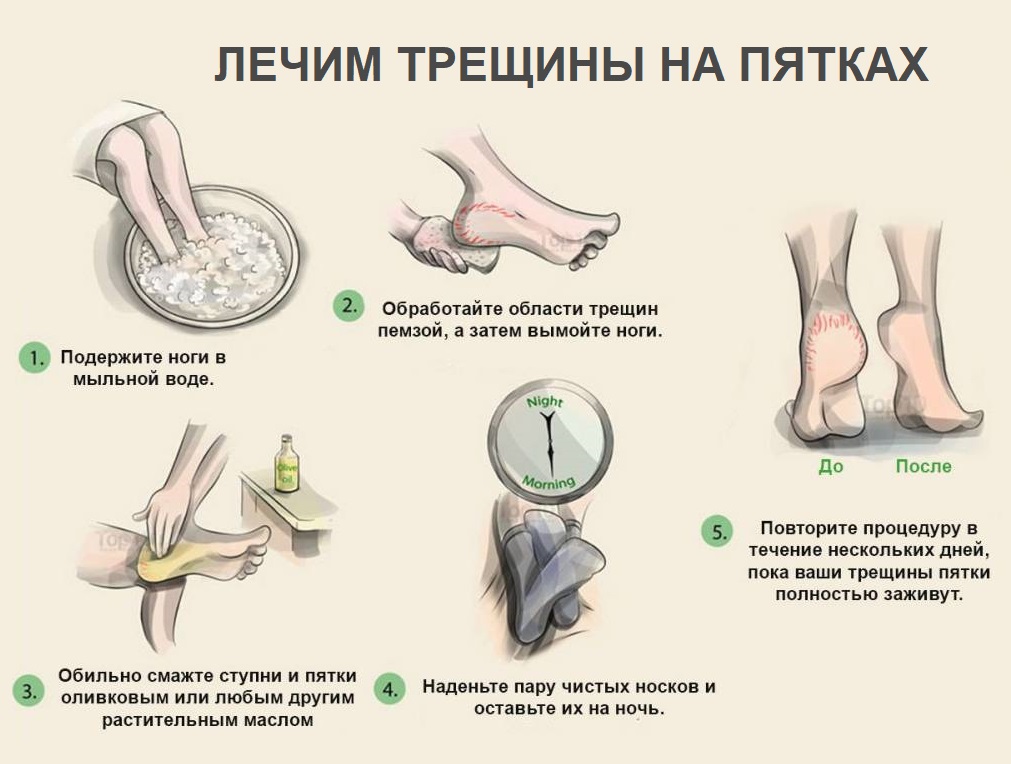 (1a) Представлено одиночное сагиттальное Т1-взвешенное изображение через правую стопу. Каковы выводы? Какой диагноз?
(1a) Представлено одиночное сагиттальное Т1-взвешенное изображение через правую стопу. Каковы выводы? Какой диагноз?
1
Рис. 1:(1a) Одиночное сагиттальное Т1-взвешенное изображение через правую стопу.
Выводы
2
Рис. 2:Сагиттальное Т1-взвешенное изображение через лодыжку демонстрирует область низкой интенсивности сигнала (стрелка) по всей ладьевидной кости с небольшим уменьшением ее переднезаднего размера.
Диагноз
Суставной ладьевидный остеохондроз (болезнь Келера).
Ниже приведены дополнительные изображения из кейса.
3
Рис. 3: Сагиттальное Т2-взвешенное изображение с подавлением жира с центром в средней части стопы демонстрирует уменьшение переднезаднего размера и диффузно и неоднородно повышенную интенсивность сигнала (стрелка) по всей ладьевидной кости. Пятнистые области гиперинтенсивности костного мозга в заднем отделе стопы, вероятно, связаны с измененной биомеханикой или неиспользованием.
Пятнистые области гиперинтенсивности костного мозга в заднем отделе стопы, вероятно, связаны с измененной биомеханикой или неиспользованием.
4
Рис. 4:Длинноосевое протонно-взвешенное по плотности изображение с подавлением жира через стопу демонстрирует уплощение коры (стрелки), более выраженное латерально, с аномальным сигналом, затрагивающим латеральные 2/3 ладьевидной кости.
Обсуждение
Остеохондроз – это любое заболевание, которое влияет на ход роста костей с вовлечением центров окостенения. Категория остеохондроза зависит от того, поражает ли он эпифиз (суставная форма), апофиз (несуставная форма) или физ. 1 В этой веб-клинике подробно описаны формы заболеваний суставов нижних конечностей, включая болезнь Келера, болезнь Фрайберга и болезнь Легга-Кальве-Пертеса.
БОЛЕЗНЬ КЕЛЕРА (Суставной остеохондроз ладьевидной кости) Болезнь Келера, самокупирующееся заболевание ладьевидной кости стопы у детей, возникающее в результате временного нарушения костного кровоснабжения. Заболевание чаще встречается у мальчиков, обычно в возрасте от 3 до 10 лет. Хотя чаще одностороннее, заболевание может возникать двусторонне в 25 процентах случаев. Пациенты обычно обращаются с отечностью и болью, которые чаще встречаются вдоль медиальной части стопы, вызывая хромоту с переносом веса на более латеральную сторону. Часто отмечается покраснение и повышение температуры над точечной нежной ладьевидной костью. Причина идиопатическая; однако травма также описывается как катализатор. Одна из теорий состоит в том, что замедленная оссификация ладьевидной кости по сравнению с окружающими окостеневшими костями приводит к аномальному сдавлению ладьевидной кости и ее кровеносных сосудов. 2 Кровеносные сосуды проникают в хрящевую часть кости, но в неоссифицированной ладьевидной кости нет зрелой артериальной сети анастомозов.
Заболевание чаще встречается у мальчиков, обычно в возрасте от 3 до 10 лет. Хотя чаще одностороннее, заболевание может возникать двусторонне в 25 процентах случаев. Пациенты обычно обращаются с отечностью и болью, которые чаще встречаются вдоль медиальной части стопы, вызывая хромоту с переносом веса на более латеральную сторону. Часто отмечается покраснение и повышение температуры над точечной нежной ладьевидной костью. Причина идиопатическая; однако травма также описывается как катализатор. Одна из теорий состоит в том, что замедленная оссификация ладьевидной кости по сравнению с окружающими окостеневшими костями приводит к аномальному сдавлению ладьевидной кости и ее кровеносных сосудов. 2 Кровеносные сосуды проникают в хрящевую часть кости, но в неоссифицированной ладьевидной кости нет зрелой артериальной сети анастомозов.
Типичные рентгенологические признаки представляют собой сочетание уплощения, фрагментации и склероза ладьевидной кости. Обычно для постановки диагноза необходимо наличие двух или более из них. Многие считают, что это на самом деле не «болезнь», а скорее изменение в последовательности окостенения предплюсны, и некоторые выступают за требование увидеть изменение по сравнению с ранее нормальной костью, чтобы поставить этот диагноз. 3
Многие считают, что это на самом деле не «болезнь», а скорее изменение в последовательности окостенения предплюсны, и некоторые выступают за требование увидеть изменение по сравнению с ранее нормальной костью, чтобы поставить этот диагноз. 3
Анатомия
Ладьевидная кость является последней костью предплюсны, которая окостеневает в стопе. Считается, что это замедленное развитие делает кость более восприимчивой к компрессии и последующему повреждению сосудов. Если повреждение серьезное, кровоснабжение ладьевидной кости может быть нарушено, что приведет к аваскулярному некрозу. Как правило, края ладьевидной кости получают наибольшее количество крови, кровоснабжаемой тыльной артерией стопы латерально и ветвями задней большеберцовой артерии медиально. Центральная ладьевидная кость наименее хорошо снабжается кровью, происходящей из концевых ветвей.
5
Рис. 5: Трехмерное изображение кровоснабжения ладьевидной кости демонстрирует области сосудов, снабжаемых латерально тыльной мышцей стопы и медиально задней большеберцовой артерией. Центральная область (синяя) относительно бессосудистая.
Центральная область (синяя) относительно бессосудистая.
Рентгенологическое исследование и МРТ-обследование
Хотя болезнь Келера в основном является клиническим диагнозом, переднезадняя и боковая рентгенограммы в положении стоя могут показать характерные признаки аваскулярного некроза, включая фрагментацию, склероз и уплощение кости. Ранние рентгенологические изменения включают коллапс и повышенную плотность/склероз ладьевидной кости с последующей очаговой деоссификации и фрагментации. Наконец происходит заживление, и ладьевидная кость восстанавливается. 4 МРТ обычно показывает снижение сигнала при Т1-взвешивании и усиление сигнала при Т2-взвешивании на ранней и средней стадиях заболевания. Костное уплощение может присутствовать. Может произойти фрагментация центра окостенения ладьевидной кости, но вышележащий хрящ, как правило, не поврежден. Инфекция может имитировать клинические симптомы болезни Келера, и МРТ может быть полезна для дифференциации этих образований с признаками, характерными для остеомиелита, такими как эрозия коры, абсцесс прилегающих мягких тканей и покрывающий целлюлит (6a). Также может быть проведена ядерно-медицинская сцинтиграфия, которая обычно показывает снижение поглощения радиофармпрепарата в условиях болезни Келера.
Также может быть проведена ядерно-медицинская сцинтиграфия, которая обычно показывает снижение поглощения радиофармпрепарата в условиях болезни Келера.
6
Рис. 6:Сагиттальное Т2-взвешенное изображение с подавлением жира через среднюю часть стопы у 5-летней девочки с жалобами на боль вдоль медиальной стороны стопы с хромотой, отечностью и кровоподтеками. Изображение демонстрирует признаки остеомиелита с выраженной гиперинтенсивностью костного мозга (стрелка) в пределах окостеневшей части ладьевидной кости и дорсальной эрозии коры. Видно расширение мягких тканей, совместимое с флегмоной и целлюлитом (стрелка).
Лечение
Лечение обычно консервативное и направлено на облегчение симптомов. Это включает в себя использование обезболивающих и поддержки свода стопы. Если симптомы не исчезают, накладывают короткую гипсовую повязку на 4-6 недель с модификацией обуви по мере необходимости. Длительные исследования показали восстановление функции почти у всех пациентов с болезнью Келера с восстановлением ладьевидной кости. 5
5
Болезнь Фрайберга — болезненный остеохондроз, поражающий головки плюсневых костей. Термин «нарушение» первоначально был придуман из-за связи этого состояния с травмой. Точная этиология остается неизвестной, основные факторы включают повторяющийся стресс и неправильное ношение обуви, включая высокие каблуки. 6 Это состояние возникает двусторонне менее чем в 10 процентах случаев. Болезнь Фрайберга обычно затрагивает 2-ю плюсневую кость чаще, чем 3-ю, но в редких случаях также описано поражение 4-й или 5-й плюсневой кости. Это состояние чаще всего возникает у девочек-подростков, занимающихся балетом и танцами. 7
Анатомия
В плюсневых костях имеется два центра окостенения. Первичный центр окостенения виден для каждой из диафизов плюсневых костей, в то время как каждая малая плюсневая головка содержит эпифизарный центр окостенения.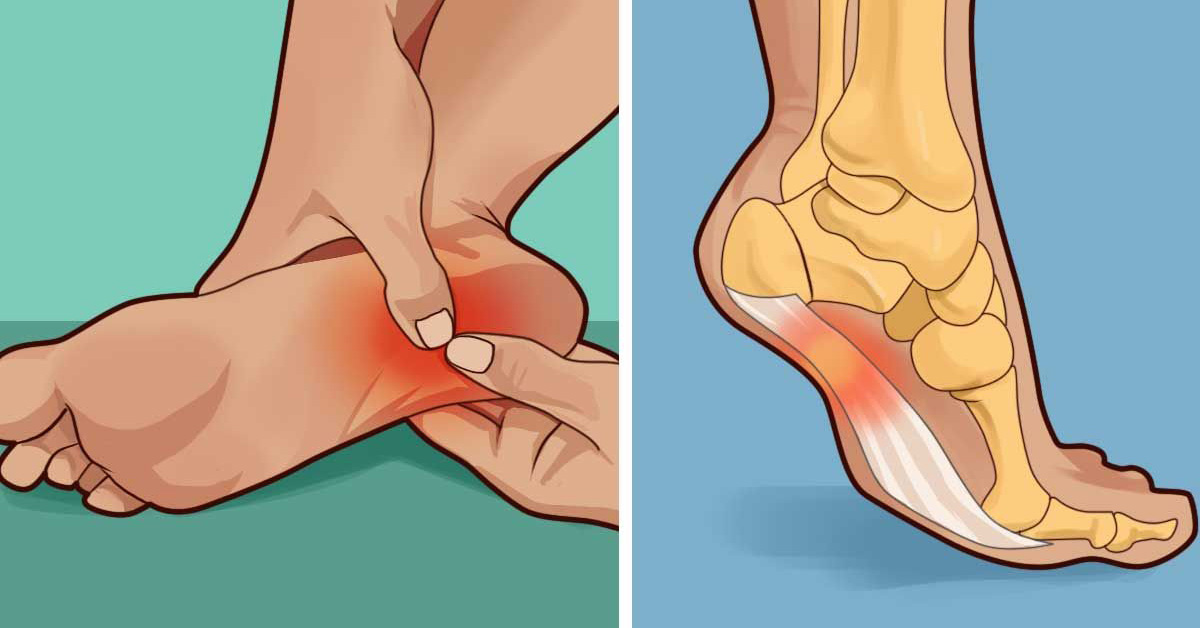 Эти дистальные центры окостенения начинают развиваться к третьему-четвертому годам жизни и полностью срастаются с диафизами к 17-20 годам. Кровоснабжение головок плюсневых костей осуществляется из двух артериальных источников, образующих богатую сеть внекостных анастомозов. К ним относятся тыльные плюсневые артерии (отходящие от тыльной артерии стопы) и подошвенные плюсневые артерии (ветви задней большеберцовой артерии). 8 Ишемический некроз вследствие повторяющихся травм, вероятно, приводит к нарушению конечного артериального кровоснабжения этой области.
Эти дистальные центры окостенения начинают развиваться к третьему-четвертому годам жизни и полностью срастаются с диафизами к 17-20 годам. Кровоснабжение головок плюсневых костей осуществляется из двух артериальных источников, образующих богатую сеть внекостных анастомозов. К ним относятся тыльные плюсневые артерии (отходящие от тыльной артерии стопы) и подошвенные плюсневые артерии (ветви задней большеберцовой артерии). 8 Ишемический некроз вследствие повторяющихся травм, вероятно, приводит к нарушению конечного артериального кровоснабжения этой области.
7
Рисунок 7:Подобно ладьевидной кости, дистальная плюсневая кость кровоснабжается относительно богато по периферии, но центральная плюсневая головка снабжается небольшими концевыми артериальными ветвями.
Рентгенологическое и МРТ-обследование
Ранние рентгенологические признаки болезни Фрайберга включают выпот в сустав с расширением суставной щели ПФС, прогрессирующий до аваскулярного некроза, включая склероз, развитие кисты и, наконец, уплощение головки плюсневой кости. 9 Система классификации была разработана Смилли в 1957 году для постановки. 10
9 Система классификации была разработана Смилли в 1957 году для постановки. 10
Стадия 1: тонкая линия перелома через эпифиз.
Стадия 2: ранний коллапс и центральная депрессия.
3 стадия: центральная депрессия (рассасывание).
Стадия 4: образование рыхлого тела за счет высвобождения центрального фрагмента.
5 стадия: уплощение головки плюсневой кости с вторичным артрозом.
МРТ наиболее полезна на ранних стадиях заболевания, когда тонкая линия перелома может быть незаметна. На ранних стадиях заболевания могут присутствовать только выпот в суставах и отек костного мозга. Более поздние стадии аналогичны ассоциированному уплощению коры и склерозу (8a, 8b).
8a
8b
Рис. 8: (8a) Длинноосное коронарное Т1-взвешенное изображение через правую стопу демонстрирует потерю нормального костно-мозгового сигнала на всем протяжении эпифиза и диафиза 2-й плюсневой кости с уплощением эпифизарная головка (стрелка). (8b) Соответствующее сагиттальное Т2-взвешенное изображение с подавлением жира показывает выраженный отек костного мозга на всем протяжении 2-й плюсневой кости с дистальным уплощением суставной поверхности (стрелка). Также присутствует реактивный суставной выпот в плюснефаланговом суставе.
(8b) Соответствующее сагиттальное Т2-взвешенное изображение с подавлением жира показывает выраженный отек костного мозга на всем протяжении 2-й плюсневой кости с дистальным уплощением суставной поверхности (стрелка). Также присутствует реактивный суставной выпот в плюснефаланговом суставе.
Лечение
В большинстве случаев болезнь Фрайберга на ранних стадиях разрешается с регрессом симптомов после консервативной терапии. Это включает противовоспалительные препараты и модификацию активности, обычно путем иммобилизации стопы на 4-6 недель с последующим постепенным возвращением к активности с модификацией ношения обуви, включая индивидуальные ортопедические стельки и прокладки. 11 Хирургическое вмешательство необходимо в случае неэффективности консервативных мер по купированию симптомов. Более поздние стадии заболевания также могут потребовать хирургического вмешательства из-за стойких симптомов артроза и свободных тел в суставе.
БОЛЕЗНЬ НОГА-Кальве-Пертеса (СУСТАВНОЙ ОСТЕОХОНДРОЗ ГОЛОВКИ БЕДРА) Болезнь Легга-Кальве-Пертеса (БКП) представляет собой болезненный остеохондроз тазобедренного сустава, вызывающий хромоту у больного ребенка.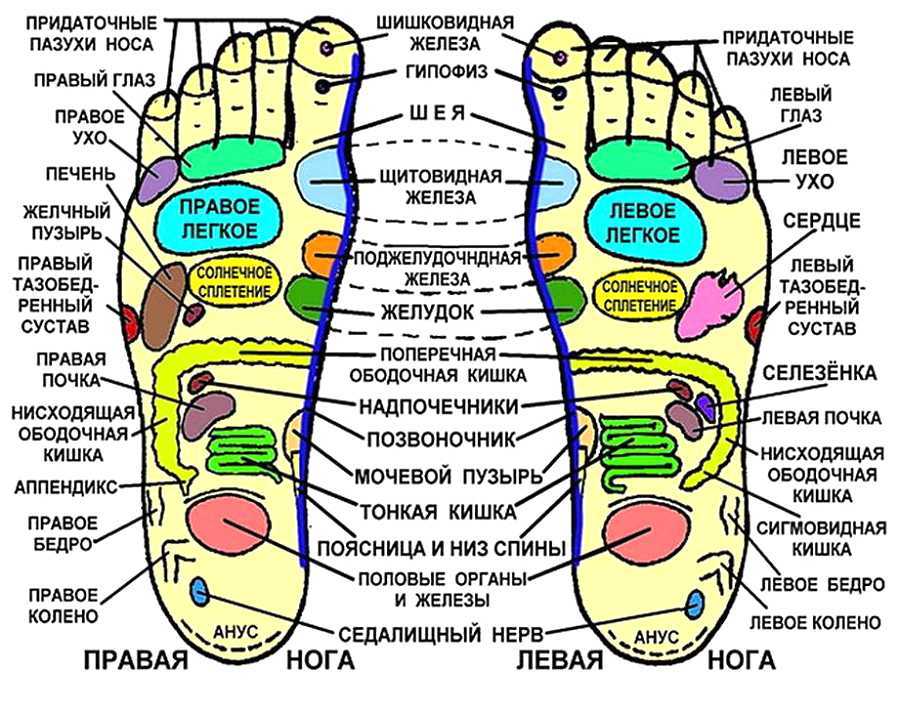 Обычно это замечают в ранней аваскулярной фазе болезненного процесса. Вероятность развития этого заболевания у мальчиков в пять раз выше, чем у девочек, с пиком заболеваемости в возрасте 5-6 лет. Пациенты, как правило, представители европеоидной расы, и дети с более низким социально-экономическим статусом и отсроченным возрастом скелета подвергаются большему риску. 12 Причина идиопатическая, так как точная этиология прерывания сосудистого русла неизвестна, с диагнозом исключения после устранения других причин асептического некроза головки бедренной кости, таких как серповидно-клеточная анемия, лейкемия, длительный прием стероидов и болезнь Гоше. 13 LCP является двусторонним только в 15 процентах случаев, поэтому двустороннее обнаружение может указывать на одно из этих других системных заболеваний. Травма в анамнезе встречается примерно в 25% случаев LCP.
Обычно это замечают в ранней аваскулярной фазе болезненного процесса. Вероятность развития этого заболевания у мальчиков в пять раз выше, чем у девочек, с пиком заболеваемости в возрасте 5-6 лет. Пациенты, как правило, представители европеоидной расы, и дети с более низким социально-экономическим статусом и отсроченным возрастом скелета подвергаются большему риску. 12 Причина идиопатическая, так как точная этиология прерывания сосудистого русла неизвестна, с диагнозом исключения после устранения других причин асептического некроза головки бедренной кости, таких как серповидно-клеточная анемия, лейкемия, длительный прием стероидов и болезнь Гоше. 13 LCP является двусторонним только в 15 процентах случаев, поэтому двустороннее обнаружение может указывать на одно из этих других системных заболеваний. Травма в анамнезе встречается примерно в 25% случаев LCP.
Анатомия
Сосудистый рисунок головки бедренной кости изменяется с течением времени по мере развития вторичного центра окостенения.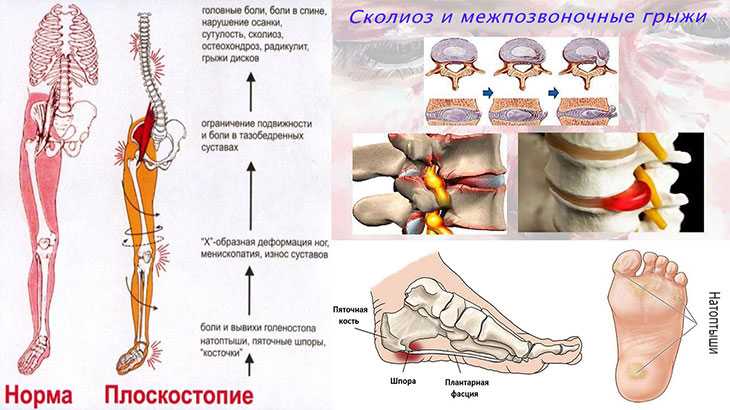 Центр окостенения головки бедренной кости обычно одиночный, но иногда может начинаться с нескольких ядер примерно в возрасте 4 месяцев, кровоснабжаемых метафизарными и латеральными эпифизарными артериями, последняя из которых отходит от медиальной огибающей артерии. К 8-месячному возрасту восходящие метафизарные артерии плода начинают регрессировать с увеличением центра окостенения, а к 4-7 годам основное кровоснабжение происходит из латеральных эпифизарных артерий, плотно сгруппированных на латеральной стороне головы. . 14 Повреждение этих боковых сосудов предположительно является причиной LCP. Только к 9-10 годам сосудистые связки обеспечивают дополнительное кровоснабжение через медиальные эпифизарные артерии, образуя сеть эпифизарных анастомозов. В подростковом возрасте эпифизарная пластинка пересекается взрослыми метафизарными артериями по мере слияния.
Центр окостенения головки бедренной кости обычно одиночный, но иногда может начинаться с нескольких ядер примерно в возрасте 4 месяцев, кровоснабжаемых метафизарными и латеральными эпифизарными артериями, последняя из которых отходит от медиальной огибающей артерии. К 8-месячному возрасту восходящие метафизарные артерии плода начинают регрессировать с увеличением центра окостенения, а к 4-7 годам основное кровоснабжение происходит из латеральных эпифизарных артерий, плотно сгруппированных на латеральной стороне головы. . 14 Повреждение этих боковых сосудов предположительно является причиной LCP. Только к 9-10 годам сосудистые связки обеспечивают дополнительное кровоснабжение через медиальные эпифизарные артерии, образуя сеть эпифизарных анастомозов. В подростковом возрасте эпифизарная пластинка пересекается взрослыми метафизарными артериями по мере слияния.
9
Рис. 9: Трехмерное изображение кровоснабжения головки бедренной кости у ребенка 4–7 лет показывает первичное кровоснабжение, происходящее из латеральных эпифизарных артерий, которое, как считается, подвержено травмам у пациентов с разработать ЛКП.
Рентгенологическое и МРТ-обследование
Рентгенограмма переднезадней и лягушачьей лапки на ранней аваскулярной стадии заболевания может быть нормальной, в то время как МРТ более чувствительна при визуализации аномалий сигнала в центре бедренной кости. Может присутствовать отек костного мозга, демонстрируемый усилением сигнала на Т2-взвешенных или STIR-изображениях. Также обычно присутствует выпот, который на рентгенограмме можно увидеть, распознав расширенное слезоточивое расстояние, указывающее на латеральное смещение центра окостенения (симптом Вальденстрема). Признак «полумесяца», который можно увидеть как на рентгенограмме, так и на МРТ, обычно указывает на наличие субхондрального перелома, обычно поражающего передне-верхнюю часть головки бедренной кости (10a, 11a). Это может прогрессировать до некроза головки бедренной кости, характеризующегося слабым сигналом на всех последовательностях изображений (12a, 13a). Рентгенография и МРТ на поздней аваскулярной стадии могут выявить малые размеры ядра бедренной окостенения, трещины/трещины бедренного центра окостенения, уплощение и склероз бедренного центра окостенения или внутриэпифизарный газ. 13
13
Репаративно-реваскулярная стадия БКП обычно развивается в течение нескольких лет и включает резорбцию некротизированной кости. Возможно развитие метафизарных кист/люцентов (14a). Боковое смещение головки бедренной кости может сохраняться из-за продолжающегося синовита и утолщения хряща. Уплощение суставной поверхности (coxa plana) является частым признаком на более поздних стадиях (15a). Также можно увидеть расширение шейки и головки бедренной кости (coxa magna) (16а). Физиология также может быть вовлечена и может иметь волнообразную форму, углубление или перемычки костей, вызывающие раннюю остановку кости или несоответствие длины конечностей. Несоответствие головки бедренной кости может привести к вторичному остеоартрозу.
10
Рис. 10: На сагиттальном изображении, протонно-взвешенном изображении с подавлением жира, у этого 10-летнего мальчика, жалующегося на боль в бедре, выявляется субхондральный «симптом полумесяца» из-за линии перелома вдоль передне-верхней поверхности бедренной кости.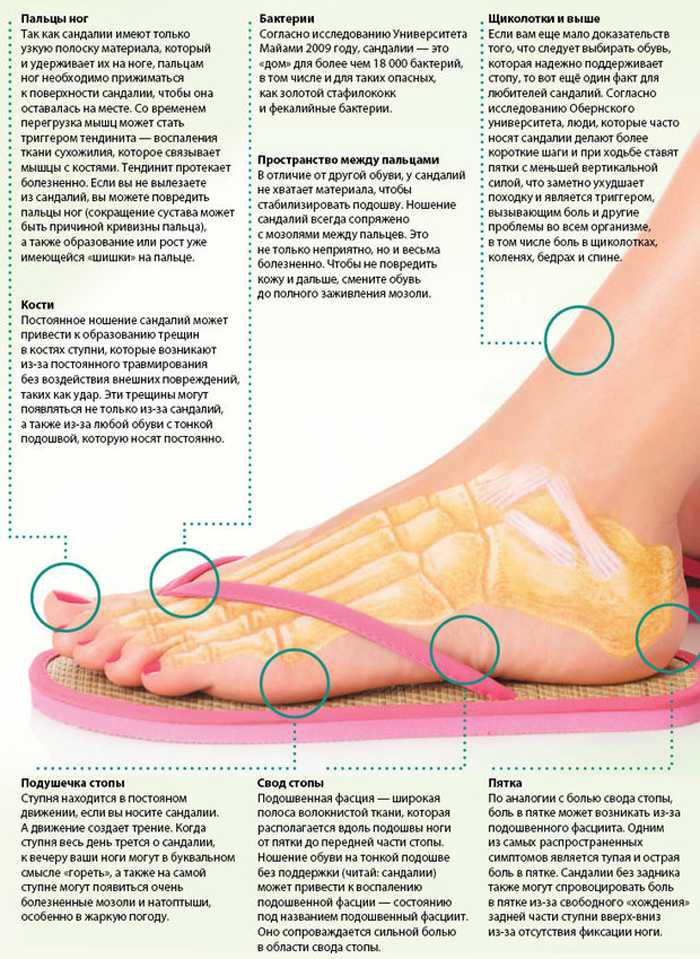 центр окостенения (стрелка). Имеется локальный отек вокруг костного мозга и выпот в суставах.
центр окостенения (стрелка). Имеется локальный отек вокруг костного мозга и выпот в суставах.
11
Рис. 11:Соответствующая аксиальная протонная плотность с подавлением жира подтверждает субхондральную линию перелома «знак полумесяца» (стрелка). Присутствуют локальный отек костного мозга и суставной выпот. Обратите внимание на легкое разрушение поверхности вышележащего суставного хряща, что приводит к неконгруэнтности.
12
Рис. 12:Сагиттальное протонно-взвешенное изображение с подавлением жира у 6-летнего мальчика с болью в бедре. Аномально низкая интенсивность сигнала видна в центре бедренной кости (стрелка). Окружающий отек костного мозга отсутствует.
13
Рис. 13: Область, занимающая центр окостенения бедренной кости, также имеет низкую интенсивность сигнала на Т1-взвешенном коронарном изображении, что свидетельствует о склерозе (стрелка).
14
Рис. 14:Представлено аксиальное Т2-взвешенное изображение 4-летнего мальчика с болью в бедре. Присутствует метафизарная киста (стрелка).
15
Рис. 15:Коронарное Т1-взвешенное изображение через таз у 43-летнего мужчины с болью в левом бедре и отдаленным анамнезом ЛКП. Присутствует уплощение суставной поверхности головки бедренной кости, совместимое с тазиком.
16
Рис. 16:Коронарное Т2-взвешенное изображение с подавлением жира у 50-летнего мужчины с болью в левом бедре и отдаленным анамнезом ЛКП. Демонстрируются головка бедренной кости, уплощение суставной поверхности (coxa plana) и расширение шейки бедра (coxa magna). Присутствуют суставной выпот и вторичные изменения остеоартроза.
Лечение
Подсчитано, что 60-70% тазобедренных суставов, пораженных болезнью LCP, заживают спонтанно без функциональных нарушений в зрелом возрасте; однако значительное количество тазобедренных суставов прогрессирует с болью и вторичной дегенерацией. 16 Лечение варьируется и основано на разных критериях. Консервативные меры включают увеличение диапазона движений с использованием физиотерапии и инъекций ботокса в приводящие мышцы. Также используются меры по облегчению боли и веса, включая использование различных шин и гипсовых повязок и постельный режим. Хирургия обычно предназначена для пожилых пациентов с ограниченным диапазоном движений для увеличения конгруэнтности тазобедренного сустава, но в настоящее время нет единого мнения о правильном подходе к лечению этих пациентов. 17
16 Лечение варьируется и основано на разных критериях. Консервативные меры включают увеличение диапазона движений с использованием физиотерапии и инъекций ботокса в приводящие мышцы. Также используются меры по облегчению боли и веса, включая использование различных шин и гипсовых повязок и постельный режим. Хирургия обычно предназначена для пожилых пациентов с ограниченным диапазоном движений для увеличения конгруэнтности тазобедренного сустава, но в настоящее время нет единого мнения о правильном подходе к лечению этих пациентов. 17
Заключение
Суставные остеохондрозы нижних конечностей могут быть болезненными и изнуряющими расстройствами, поражающими растущий скелет у детей и подростков. Раннее распознавание с помощью изображений и, в частности, МРТ, имеет решающее значение для принятия правильных управленческих решений и предотвращения долгосрочных осложнений.
Ссылки
1 Зифферт Р.С., Аркин А.М. Посттравматический асептический некроз дистального эпифиза большеберцовой кости. J Bone Joint Surg. 1950; 32А:691-695.
J Bone Joint Surg. 1950; 32А:691-695.
2 Сактхивел-Уэйнфорд, К. (2011). Самооценка при патологии опорно-двигательного аппарата. Рентген. (стр. 44) Издательство М&К.
3 Резник Д. (1996). Остеохондроз. Визуализация костей и суставов (2-е изд., стр. 960-977) Philadelphia, W.B. Компания Сондерс.
4 Staheli, LT (2003). Основы детской ортопедии. (стр.58) Филадельфия, Липпинкотт Уильямс и Уилкинс.
5 Williams GA, Cowell HR. Болезнь Келера ладьевидной кости предплюсны. Clin Orthop Relat Relat Res. 1981; 158:53-58
6 Кармонт М.Р., Риз Р.Дж., Бланделл К.М. Обзор современных концепций: болезнь Фрейберга. Стопа лодыжки Int. 2009;30(2):167-176.
7 Air ME, Rietveld, AB. Болезнь Фрайберга как редкая причина ограниченного и болезненного веселья у танцоров. J Dance Med Sci. 2010 г.; 14(1)32-36.
8 Peterson WJ, Lankes JM, Paulsen F, Hassenpflug J. Артериальное снабжение головок малых плюсневых костей: исследование сосудистых инъекций на человеческих трупах.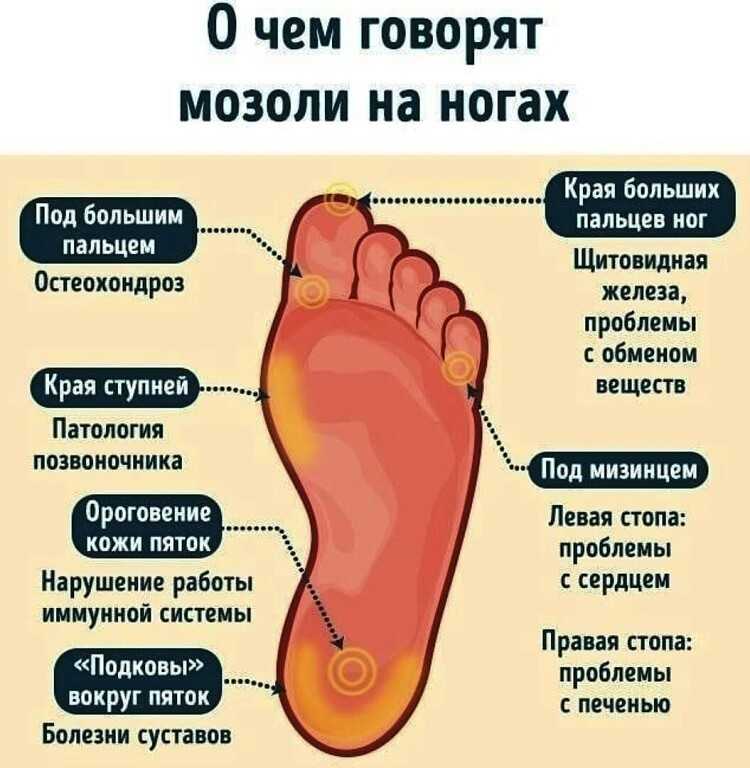 Междунар. лодыжка стопы. 2002 июнь; 23(6) 491-5.
Междунар. лодыжка стопы. 2002 июнь; 23(6) 491-5.
9 Озонофф М.Б.: Стопа. В Ozonoff MB (ed): Детская ортопедическая радиология. Филадельфия, WB Saunders, 1992, стр. 304-396
10 Simillie. Лечение инфаркта Фрейберга. Proc R Soc Med. 1967; 60:29-31.
11 Mah, CD: Болезнь Фрайберга. См. www.podiatryinstitute.com/pdfs/Update_2008/2008_04.pdf Глава 4, стр. 13–15.
13 Диллман Дж. Р., Эрнандес Р. МРТ болезни Легга-Кальве-Пертеса. АЖР. 2009 ноябрь; 193: 1394-1407.
14 Trueta J. Нормальная сосудистая анатомия головки бедренной кости человека в процессе роста. Журнал костной и совместной хирургии. 1957 май; 39B (2): 358-394
15 Резник Д. (1996). Остеохондроз. Визуализация костей и суставов (2-е изд., стр. 960-977) Philadelphia, W.B. Компания Сондерс.
16 Диллман Дж.
 Основными методиками являются электрофорез, УВЧ, магнитотерапия, лазерная терапия. При назначении процедур учитываются противопоказания, такие как сердечные заболевания и онкообразования.
Основными методиками являются электрофорез, УВЧ, магнитотерапия, лазерная терапия. При назначении процедур учитываются противопоказания, такие как сердечные заболевания и онкообразования. Остеохондральные поражения таранной кости. Am J Sports Med 1993; 21:13-19.)
Остеохондральные поражения таранной кости. Am J Sports Med 1993; 21:13-19.)