Нестероидные противовоспалительные препараты в лечении при остеоартрозе: оптимизация применения с учетом факторов риска сердечно-сосудистых и гастроинтестинальных осложнений
Введение
Остеоартроз является одним из наиболее частых заболеваний опорно-двигательного аппарата. При этом распространенность данной патологии значительно варьирует в географическом разрезе. Данный показатель в Украине составляет 2,2% (2200 на 100 тыс. населения), заболеваемость — 497 человек на 100 тыс. населения, что значительно меньше, чем в США, что, возможно, обусловлено гиподиагностикой остеоартроза в нашей стране (Поворознюк В.В., Быстрицкая М.А., 2011). При этом поражение компонентов опорно-двигательного аппарата чаще отмечают у женщин, чем у мужчин, и у лиц старшего возраста (Чичасова Н.В., 2011).
Как известно, остеоартроз относится к дегенеративным поражениям суставов, тем не менее для его течения также характерно развитие синовита, что является показанием для назначения препаратов, купирующих воспалительный процесс. Кроме того, воспалительным процессам, протекающим в суставе, часто сопутствует болевой синдром, который, однако, не всегда коррелирует по своей интенсивности с выраженностью воспаления (Чичасова Н.В., 2011).
Кроме того, воспалительным процессам, протекающим в суставе, часто сопутствует болевой синдром, который, однако, не всегда коррелирует по своей интенсивности с выраженностью воспаления (Чичасова Н.В., 2011).
В патогенезе остеоартроза важную роль играет воспаление и дисрегуляция цитокинового каскада, которая способствует нарушению баланса между анаболическими и катаболическими процессами. В исследованиях in vitro и in vivo показана роль провоспалительных цитокинов — интерлейкина-1 и фактора некроза опухоли-α в развитии патологических изменений хряща, а также оксида азота и различных металлопротеиназ, которые деградируют межклеточный матрикс (Goldring M.B., Berenbaum F., 2004; Kobayashi M. et al., 2005; Bondeson J. et al., 2006; Goldring M.B. et al., 2008). Не менее важное значение в развитии остеоартроза имеют возрастные изменения и биомеханическое воздействие.
В терапии при остеоартрозе широко применяют нестероидные противовоспалительные препараты (НПВП), которые, согласно рекомендациям OARSI (2008) по лечению остеоартроза коленного и тазобедренного суставов, характеризуются наибольшей доказательностью (степень доказательности 93% из 100% возможных) (Zhang W. et al., 2008; Поворознюк В.В., Быстрицкая М.А., 2011).
et al., 2008; Поворознюк В.В., Быстрицкая М.А., 2011).
Таким образом, НПВП являются препаратами первого ряда симптоматического лечения при остеоартрозе. Анальгезирующий и противовоспалительный эффект НПВП обусловлен неселективным ингибированием циклооксигеназы (ЦОГ) — фермента, катализирующего синтез простаноидов, в том числе простагландинов, простациклинов и тромбоксанов. Простаноиды — медиаторы воспаления, боли, терморегуляции; они имеют большое значение для регулирования функций сосудов, почек, костной ткани, желудочно-кишечного тракта и других органов и тканей. Известны три изоформы ЦОГ, наибольшее значение имеют ЦОГ-1 и -2. ЦОГ-1 выявляют во всех тканях, и ее продукция не зависит от воспаления. Экспрессия ЦОГ-2 связана с воспалением и индуцируется медиаторами воспаления — липополисахаридами, интерлейкином-1, фактором некроза опухоли-α в клетках и тканях (Rainsford K.D., 2007; Лапина Т.Л., 2013).
Необходимо учитывать, что терапия пациентов с остеоартрозом осложняется тем, что большинство из них — люди пожилого возраста, для которых характерно наличие широкого спектра сопутствующих заболеваний и, соответственно, применение препаратов для их лечения. Указанные аспекты являются факторами риска развития побочных эффектов при применении НПВП. Сегодня проблема коморбидности в различных терапевтических направлениях чрезвычайно актуальна, что во многом обусловлено постарением населения во всем мире.
Указанные аспекты являются факторами риска развития побочных эффектов при применении НПВП. Сегодня проблема коморбидности в различных терапевтических направлениях чрезвычайно актуальна, что во многом обусловлено постарением населения во всем мире.
В последнее время проблема коморбидности в контексте терапии при остеоартрозе нашла широкое развитие. В частности проведено несколько исследований, позволяющих всесторонне оценить распространенность сопутствующих заболеваний и их структуру в группе пациентов с заболеваниями опорно-двигательного аппарата, в том числе больных остеоартрозом.
Результаты анализа данных о более 9 тыс. пациентов, у 60% из которых была сопутствующая патология, выявили среди наиболее частых сопутствующих заболеваний артериальную гипертензию, сердечную недостаточность, сахарный диабет, ишемическую болезнь сердца, заболевания почек, инсульт, инфаркт миокарда (ИМ) и заболевания печени (Чичасова Н.В., 2011).
В другом исследовании при сравнении частоты развития сопутствующих заболеваний у 11 375 пациентов с остеоартрозом по сравнению с 11 780 пациентами без данной патологии показано повышение частоты развития на фоне остеоартроза ожирения (в 2,25 раза), гастрита (в 1,98 раза), флебита (в 1,8 раза), грыжи диафрагмы (в 1,8 раза), ишемической болезни сердца (в 1,73 раза), дивертикулеза кишечника (в 1,63 раза ) (Kadam U. T. et al., 2004).
T. et al., 2004).
Известно, что применение некоторых НПВП связано с развитием побочных эффектов, которые могут усугублять течение артериальной гипертензии, снижать эффективность антигипертензивной терапии, негативно влиять на состояние пациентов с застойной сердечной недостаточностью (Heerdink E.R. et al., 1998; Page J., Henry D., 2000; Warksman J.C., 2007; Чичасова Н.В., 2011).
Таким образом, необходимо принимать во внимание как достаточно частое развитие побочных эффектов при применении НПВП при остеоартрозе, так и их возможное влияние на характер течения сопутствующей патологии, особенно у пациентов пожилого возраста. Особенного внимания заслуживает этот вопрос в свете того, что такие пациенты принимают НПВП в 4 раза чаще, чем лица молодого возраста (Балабанова Р.М., Егорова О.Н., 2011).
В этом контексте для лечения при хроническом болевом синдроме, в том числе при остеоартрозе, особенно у пациентов пожилого возраста, препаратами выбора являются частично селективные ингибиторы ЦОГ-2, поскольку они обладают более низким риском развития гастроинтестинальных осложнений по сравнению с неселективными НПВП (например диклофенак) и более низким риском кардиоваскулярных осложнений по сравнению с селективными НПВП (различные коксибы).
Одним из наиболее изученных препаратов этой группы является мелоксикам, применяемый с 1995 г. (Поворознюк В.В., Быстрицкая М.А., 2011). Мелоксикам обладает противовоспалительным, обезболивающим и жаропонижающим свойствами, связанными с селективным ингибированием ЦОГ-2. При этом он структурно отличается от других ингибиторов ЦОГ-2, например коксибов, в связи с чем связывается с верхней частью канала ЦОГ-2, а не с боковой, как целекоксиб (Чичасова Н.В., 2011). Мелоксикам легко проникает в синовиальную жидкость, где его концентрация составляет 45–57% таковой в плазме крови (Warksman J.C., 2007).
Эффективность мелоксикама
Эффективность мелоксикама при лечении пациентов с остеоартрозом доказана в ходе многих клинических исследований. Так, согласно результатам 11 рандомизированных двойных слепых клинических исследований, проанализированных в рамках систематического обзора, в котором оценивали эффективность частично селективных НПВП по сравнению с неселективными НПВП, достоверных различий в эффективности мелоксикама (7,5; 15 или 22,5 мг) у пациентов с остеоартритом коленных суставов в сравнении с другими НПВП (диклофенак 100–150 мг/сут, пироксикам 20 мг/сут, напроксен 750 мг/сут) не отмечено (Chou R. et al., 2011). Аналогичные результаты получены в 12-недельном двойном слепом плацебо-контролируемом клиническом исследовании эффективности и безопасности применения мелоксикама при остеоартрозе. Показано, что мелоксикам также эффективен в лечении при остеоартрозе, как и неселективные НПВП (диклофенак, пироксикам) (Dekueker J. et al., 1998; Yocum D. et al., 2000).
et al., 2011). Аналогичные результаты получены в 12-недельном двойном слепом плацебо-контролируемом клиническом исследовании эффективности и безопасности применения мелоксикама при остеоартрозе. Показано, что мелоксикам также эффективен в лечении при остеоартрозе, как и неселективные НПВП (диклофенак, пироксикам) (Dekueker J. et al., 1998; Yocum D. et al., 2000).
Что касается сравнения эффективности мелоксикама и селективных НПВП, то имеется достаточно ограниченное количество крупных клинических исследований, проведенных с целью прямого сравнения терапевтического потенциала этих препаратов. Тем не менее, например в исследовании с участием пациентов с ревматоидным артритом, эффективность мелоксикама (15 мг) и целекоксиба (200 мг) была сопоставима (Shi W. et al., 2004).
Таким образом, мелоксикам не уступает в эффективности как неселективным, так и селективным НПВП. В этих условиях на первый план выходит профиль безопасности — вероятность развития побочных эффектов, переносимость и взаимодействие с другими лекарственными средствами.
Особенности профиля безопасности мелоксикама в сравнении с неселективными и селективными НПВП
При длительном применении мелоксикама, особенно у пациентов старшего возраста, особое внимание необходимо уделить профилю его безопасности.
Среди наиболее распространенных побочных эффектов, характерных для НПВП, выделяют гастроинтестинальные и сердечно-сосудистые осложнения.
Риск развития гастроинтестинальных побочных эффектов (как основных для группы НПВП) зависит от влияния препарата на ЦОГ-1, то есть его ЦОГ-2- селективности. Мелоксикам обладает высокой ЦОГ-2-селективностью (индекс ЦОГ-2- селективности составляет 0,09), которая обусловливает более низкий риск развития побочных эффектов со стороны желудочно-кишечного тракта) (Поворознюк В.В., Быстрицкая М.А., 2011).
Так, наряду с сопоставимой эффективностью, по сравнению с диклофенаком и пироксикамом, мелоксикам характеризуется лучшей переносимостью, что доказано в ряде клинических исследований, в том числе с наивысшим уровнем доказательности (Dekueker J. et al., 1998; Yocum D. et al., 2000). Согласно результатам двух крупных 4-недельных рандомизированных клинических исследований MELISSA и SELECT, в которых суммарно приняли участие почти 18 тыс. пациентов, мелоксикам (7,5 мг/сут) обладал более благоприятным профилем безопасности в отношении развития гастроинтестинальных побочных эффектов по сравнению с неселективными НПВП (Dekueker J. et al., 1998; Hawkey C. et al., 1998). Результаты исследования MELISSA продемонстрировали, что применение мелоксикама достоверно реже, чем диклофенака, приводило к развитию побочных эффектов со стороны желудочно-кишечного тракта — 13,3 и 18,7% соответственно. В клиническом исследовании SELECT мелоксикам показал достоверное преимущество, по сравнению с пироксикамом, относительно риска развития серьезных побочных реакций со стороны желудочно-кишечного тракта. Также при применении мелоксикама реже по сравнению с пироксикамом отмечены такие побочные эффекты, как диспепсия: 10,3 и 15,4 соответственно.
et al., 1998; Yocum D. et al., 2000). Согласно результатам двух крупных 4-недельных рандомизированных клинических исследований MELISSA и SELECT, в которых суммарно приняли участие почти 18 тыс. пациентов, мелоксикам (7,5 мг/сут) обладал более благоприятным профилем безопасности в отношении развития гастроинтестинальных побочных эффектов по сравнению с неселективными НПВП (Dekueker J. et al., 1998; Hawkey C. et al., 1998). Результаты исследования MELISSA продемонстрировали, что применение мелоксикама достоверно реже, чем диклофенака, приводило к развитию побочных эффектов со стороны желудочно-кишечного тракта — 13,3 и 18,7% соответственно. В клиническом исследовании SELECT мелоксикам показал достоверное преимущество, по сравнению с пироксикамом, относительно риска развития серьезных побочных реакций со стороны желудочно-кишечного тракта. Также при применении мелоксикама реже по сравнению с пироксикамом отмечены такие побочные эффекты, как диспепсия: 10,3 и 15,4 соответственно.
Таким образом, в отношении частоты гастроинтестинальных побочных эффектов мелоксикам обладает выраженным преимуществом по сравнению с неселективными НПВП, в том числе диклофенаком, обладая при этом сопоставимой эффективностью.
Оценка кардиоваскулярных рисков при выборе НПВП приобретает чрезвычайно важное значение в терапии пациентов старшего возраста, у которых часто ревматическая патология сопровождается развитием атеросклероза и высоким риском смертности от кардиоваскулярных осложнений (Елисеев М.С., Барскова В.Г., 2010). Особый интерес к этой группе побочных реакций НПВП возник после исследований VIGOR, CLASS (Bombardier C. et al., 2000; Silverstein F.E. et al., 2000), в которых высокий относительный риск кардиоваскулярных осложнений получен у препаратов с низким гастроинтестинальным риском, к которым, как известно, относятся селективные НПВП. Так, результаты исследования VIGOR продемонстрировали значительно большую частоту развития ИМ у пациентов с ревматоидным артритом, применявших селективный НПВП рофекоксиб, по сравнению с неселективным НПВП напроксеном. Такой высокий уровень кардиоваскулярных осложнений при применении селективных НПВП может быть связан с тем, что некоторые из них подавляют синтез простациклина и недостаточно влияют на продукцию тромбоксанов, регулирующих агрегацию тромбоцитов и время кровотечения. При этом может нарушаться равновесие между синтезом тромбоксанов, оказывающего протромбогенное действие, и «антитромбогенных» эйкозаноидов (простациклин), что ведет к повышению риска развития тромбоза (Елисеев М.С., Барскова В.Г., 2010).
При этом может нарушаться равновесие между синтезом тромбоксанов, оказывающего протромбогенное действие, и «антитромбогенных» эйкозаноидов (простациклин), что ведет к повышению риска развития тромбоза (Елисеев М.С., Барскова В.Г., 2010).
Отметим, что в этом аспекте свойства мелоксикама в значительной степени отличаются от селективных НПВП. В частности, согласно результатам клинического исследования, у пациентов с ревматоидным артритом применение мелоксикама в дозе 7,5 мг/сут в течение 14 дней не оказывало существенного влияния на агрегацию тромбоцитов, длительность кровотечения и уровень тромбоксанов. При этом применение напроксена в дозе 500 мг/сут приводило к более чем 2-кратному снижению уровня тромбоксанов — с 228 до 117 пг/мл по сравнению с 246 пг/мл при применении мелоксикама (Knijff-Dutmer E.A. et al., 2002). Также прием напроксена способствовал подавлению агрегации тромбоцитов, что значительно увеличивало время кровотечения.
В другом исследовании показано, что мелоксикам, в отличие от неселективного НПВП индометацина, не оказывает влияния на индуцированную коллагеном или арахидоновой кислотой агрегацию тромбоцитов (De Meijer A. et al., 1999). Приведенные данные свидетельствуют в пользу частичной селективности мелоксикама в отношении ЦОГ-2 по сравнению селективными НПВП.
et al., 1999). Приведенные данные свидетельствуют в пользу частичной селективности мелоксикама в отношении ЦОГ-2 по сравнению селективными НПВП.
Согласно результатам метаанализа, включившего данные о более чем 20 тыс. пациентов из почти 30 исследований, риск сердечно-сосудистых осложнений при применении мелоксикама (в дозе 7,5 и 15 мг/сут) значительно ниже такового для неселективных НПВП (Singh G. et al., 2004).
Это подтверждают данные еще одного исследования, в котором сравнивали профиль цереброваскулярной безопасности мелоксикама и селективного НПВП целекоксиба. Согласно полученным результатам, уже спустя 3 мес лечения частота развития цереброваскулярных тромбоэмболических побочных эффектов при применении целекоксиба была достоверно выше, чем при лечении мелоксикамом, и тенденция к увеличению этих различий сохранялась на протяжении 9 мес наблюдения (Layton D. et al., 2003). Согласно данным другого исследования, риск развития ИМ при применении мелоксикама сопоставим с таковым для целекоксиба и ибупрофена (Каратеев А. Е., 2013).
Е., 2013).
Еще в одном исследовании изучена вероятность развития инсульта у пациентов с артритом при применении различных НПВП. Согласно полученным данным, относительный риск развития инсульта при применении мелоксикама был наиболее низким — 0,88 — по сравнению с таковым при применении других препаратов: для рофекоксиба он составил 1,26, метиндола —1,26, пироксикама — 1,25, напроксена — 1,24, вальдекоксиба — 1,22, ибупрофена — 1,19, набуметона — 1,01, диклофенака — 0,98 и целекоксиба — 0,97 (Елисеев М.С., Барскова В.Г., 2010).
Еще более интересными представляются результаты рандомизированного проспективного клинического исследования, проведенного R. Altman и соавторами (2002), которые позволяют предположить, что применение мелоксикама может оказывать благоприятное действие при остром коронарном синдроме. Так, при применении мелоксикама в сочетании со стандартной антитромботической терапией (ацетилсалициловая кислота и гепарин) у пациентов с острым коронарным синдромом (без подъема сегмента ST) отмечено снижение частоты кардиоваскулярных катастроф по сравнению с пациентами, не получавшими мелоксикам. Кроме того, по сравнению с группой получавших только ацетилсалициловую кислоту и гепарин, в группе дополнительно принимавших мелоксикам зарегистрирована более низкая частота приступов стенокардии (15% против 35%), потребности в реваскуляризации миокарда, ИМ и смерти (10% против 26,7%).
Кроме того, по сравнению с группой получавших только ацетилсалициловую кислоту и гепарин, в группе дополнительно принимавших мелоксикам зарегистрирована более низкая частота приступов стенокардии (15% против 35%), потребности в реваскуляризации миокарда, ИМ и смерти (10% против 26,7%).
Другим важным вопросом, которому часто не уделяют достаточно внимания, являются побочные эффекты НПВП, приводящие к нарушениям функции почек. Профиль безопасности мелоксикама изучен в 4-недельном клиническом исследовании с участием пациентов старшего возраста с ревматическими заболеваниями и сопутствующим поражением почек. Показано, что применение мелоксикама в дозе 15 мг/сут не сопровождается значительными изменениями клиренса креатинина и повышением уровня креатинина, мочевины и калия в плазме крови. При этом гастроинтестинальные побочные эффекты отмечены лишь у 5% пациентов (Bevis P.J. et al., 1996).
Взаимодействие мелоксикама с другими лекарственными средствами
Как правило, пациенты старшего возраста наряду с НПВП нередко применяют и другие лекарственные средства для коррекции в том числе сопутствующей патологии.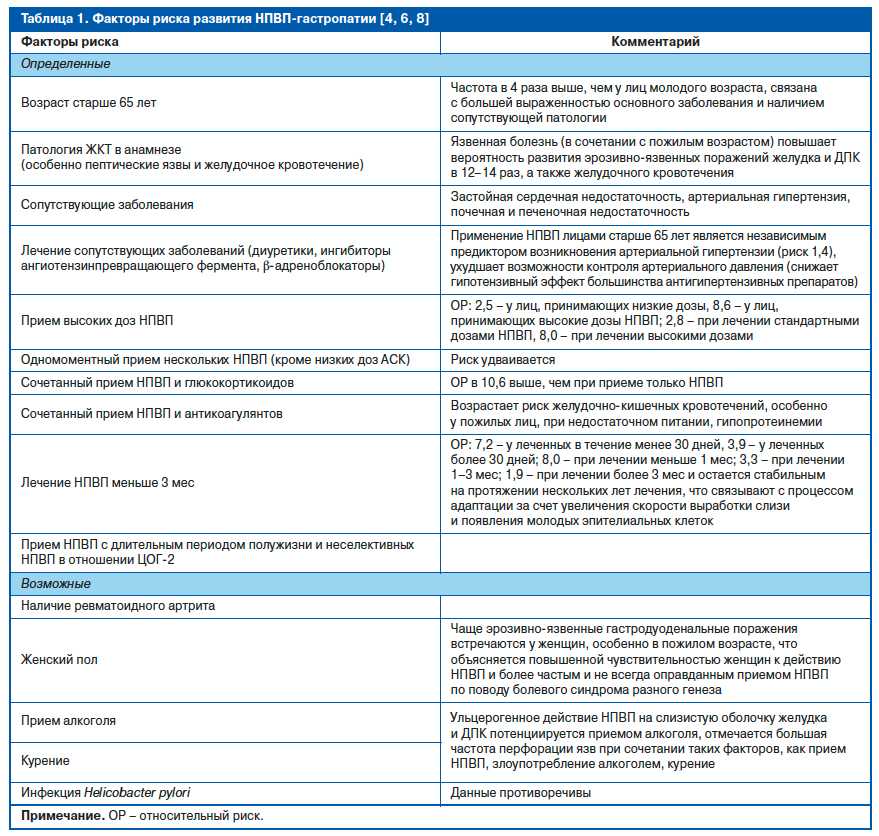 Важно учитывать совместимость применения данных препаратов с НПВП.
Важно учитывать совместимость применения данных препаратов с НПВП.
Отметим, что мелоксикам в организме человека не вступает во взаимодействие с другими лекарственными средствами, включая цитостатики, сердечные гликозиды, диуретики и др. Такие свойства препарата имеют решающее значение наряду с профилем безопасности при выборе рациональной терапии пациентов с сопутствующими заболеваниями, особенно если это лица пожилого возраста (Балабанова Р.М., Егорова О.Н., 2011).
Выводы
1. Представленные результаты многочисленных клинических исследований, в том числе с наивысшим уровнем доказательности, свидетельствуют о том, что мелоксикам является препаратом выбора у пациентов с остеоартрозом, особенно лиц пожилого возраста, благодаря особенностям его фармакокинетики, приемлемому профилю безопасности и совместимости с другими лекарственными средствами.
2. Применение мелоксикама целесообразно у пациентов, особенно старшего возраста, с высоким риском развития нарушений со стороны желудочно-кишечного тракта и сердечно-сосудистой системы в связи с наличием коморбидной патологии.
Список использованной литературы
Нестероидные противовоспалительные препараты при лечении заболеваний суставов
В статье представлен обзор данных о терапии нестероидными противовоспалительными препаратами при лечении заболеваний суставов
Для цитирования. Имаметдинова Г.Р., Чичасова Н.В. Нестероидные противовоспалительные препараты при лечении заболеваний суставов // РМЖ. 2015. No 25. С. 1491–1495.
Заболевания опорно-двигательного аппарата являются одной из самых частых причин обращения пациентов к врачу. Широкая распространенность в популяции, многолетнее персистирование боли и воспаления, неуклонное прогрессирование, быстрое развитие инвалидизации, ухудшение качества жизни, уменьшение ее продолжительности, а также значительный экономический ущерб для больных и общества определяют не только клиническую, но и социальную значимость хронических заболеваний опорно-двигательного аппарата [1–3].
Основными симптомами заболеваний опорно-двигательного аппарата являются боль и воспаление.
НПВП относятся к числу наиболее широко применяемых в клинической практике лекарственных препаратов [4]. Их использует примерно каждый 4-й человек на планете, каждый 3-й – в возрасте старше 60 лет [5]. Хорошо известно, что основным механизмом действия НПВП является подавление активности циклооксигеназы (ЦОГ) [6]. При этом большинство положительных эффектов НПВП (подавление воспаления, боли, лихорадки) связаны с подавлением активности ЦОГ-2, а побочных реакций – с подавлением активности ЦОГ-1 [7–9].
 По механизму действия НПВП разделяют на неселективно подавляющие активность ЦОГ-1 и ЦОГ-2 (н–НПВП) и селективно подавляющие активность ЦОГ-2 (с–НПВП). С-НПВП эффективны в лечении боли и воспаления при более низкой частоте развития побочных реакций по сравнению с н-НПВП.
По механизму действия НПВП разделяют на неселективно подавляющие активность ЦОГ-1 и ЦОГ-2 (н–НПВП) и селективно подавляющие активность ЦОГ-2 (с–НПВП). С-НПВП эффективны в лечении боли и воспаления при более низкой частоте развития побочных реакций по сравнению с н-НПВП. Подавление ЦОГ-1 обусловливает широкий спектр побочных реакций н-НПВП. Наиболее частым является поражение желудочно-кишечного тракта (ЖКТ) (НПВП-гастропатия) [10, 11], что нередко становится основанием для прерывания лечения. Следует подчеркнуть отсутствие связи между субъективными побочными эффектами и эндоскопически выявляемыми язвами и тяжелыми ЖКТ-осложнениями. Так, в 58–80% случаев язвы на фоне анальгетического эффекта НПВП бессимптомны [12]. Однако клиницисты должны четко выделять факторы риска развития тяжелых осложнений со стороны ЖКТ – язвенного кровотечения и сердечно-сосудистой системы (ССС): инфаркта миокарда, инсульта.
 Совместное обсуждение на экспертном совете выработало единый подход к выделению факторов риска нежелательных явлений со стороны ЖКТ и ССС. Основные положения, представленные в рекомендациях, включают: структурированный подход к назначению НПВП, стратификацию сердечно-сосудистых факторов риска, алгоритм назначения НПВП.
Совместное обсуждение на экспертном совете выработало единый подход к выделению факторов риска нежелательных явлений со стороны ЖКТ и ССС. Основные положения, представленные в рекомендациях, включают: структурированный подход к назначению НПВП, стратификацию сердечно-сосудистых факторов риска, алгоритм назначения НПВП. Алгоритм назначения НПВП в соответствии с рекомендациями представлен в таблице 1. Согласно этим рекомендациям, с-НПВП показаны при умеренном риске кардиоваскулярных осложнений и умеренном и высоком риске ЖКТ-осложнений.
Известно, что н-НПВП отрицательно влияют на хрящ и утяжеляют течение артроза, оказывают негативное влияние на функцию печени и почек, а у больных, имеющих сопутствующие заболевания бронхов, могут вызывать бронхоспазм, усугублять течение бронхиальной астмы.
В последние годы появляются все новые данные о частоте сопутствующей патологии у пациентов с заболеваниями опорно-двигательного аппарата. Необходимость в противовоспалительной терапии, подчас длительной, чаще возникает у лиц пожилого возраста, как правило, имеющих коморбидные состояния и сопутствующую им терапию. По мнению многих авторов [14–17], наиболее частыми коморбидными состояниями являются артериальная гипертензия (АГ), ишемическая болезнь сердца (ИБС), сахарный диабет, патология ЖКТ. С одной стороны, это факторы риска непереносимости НПВП, а с другой стороны, прием НПВП усугубляет течение АГ, застойной сердечной недостаточности, уменьшает эффективность антигипертензивной терапии [18–22].
По мнению многих авторов [14–17], наиболее частыми коморбидными состояниями являются артериальная гипертензия (АГ), ишемическая болезнь сердца (ИБС), сахарный диабет, патология ЖКТ. С одной стороны, это факторы риска непереносимости НПВП, а с другой стороны, прием НПВП усугубляет течение АГ, застойной сердечной недостаточности, уменьшает эффективность антигипертензивной терапии [18–22].
Результаты целого ряда исследований in vitro и ex vivo свидетельствуют, что нимесулид более селективно ингибирует ЦОГ-2, чем ЦОГ-1 [24–28] (рис.
 1).
1).
В терапевтических концентрациях нимесулид ингибирует 88% активности ЦОГ-2 и 45% активности ЦОГ-1 [29]. При этом если воздействие на ЦОГ-1 прекращается по истечении 24 ч, то воздействие на ЦОГ-2 продолжается намного дольше [30], и это различие сохраняется при длительном применении [31]. Этот своеобразный механизм действия объясняет низкое число осложнений со стороны ЖКТ. Весьма интересным является тот факт, что низкую частоту поражения ЖКТ на фоне лечения нимесулидом связывают не только с ЦОГ-2 селективностью препарата, но и с антигистаминным действием, приводящим к снижению секреции соляной кислоты в желудке [32]. Также установлено, что нимесулид обладает способностью ингибировать интерлейкин-1β (IL–1β) в культуре синовиальных фибробластов [33]. Имеются данные о том, что наряду с ингибицией ЦОГ нимесулид обладает целым рядом ЦОГ-независимых механизмов, среди которых особенно важное значение имеет его способность ингибировать апоптоз хондроцитов [34]. Кроме того, препарат и его метаболиты проявляют непосредственно антиоксидантную активность в отношении различных свободных радикалов [35].
Короткий период полувыведения (1,8–4,7 ч), быстрое достижение максимальной концентрации в плазме крови и синовиальной жидкости обусловливает высокую скорость наступления анальгетического эффекта и уменьшение частоты побочных эффектов нимесулида. При пероральном приеме препарат быстро и практически полностью абсорбируется независимо от приема пищи. Благодаря своим биохимическим свойствам нимесулид легко попадает в очаг воспаления. Концентрация свободного нимесулида непосредственно в очаге воспаления (особенно в ткани сустава), где рН среды более низкий, может быть намного выше его плазменной концентрации [39, 40].

Результаты исследований, проведенных отечественными и зарубежными авторами, подтверждают высокую эффективность нимесулида при лечении острой [41, 42] и хронической боли. Так, показано, что эффективность нимесулида была сопоставима с эффективностью диклофенака [43] и напроксена [44] у больных остеоартрозом (ОА) и ревматоидным артритом (РА) [44, 45].
Оценке безопасности нимесулида посвящен целый ряд краткосрочных и пролонгированных исследований. По данным мировой литературы, частота побочных явлений при лечении нимесулидом колеблется в пределах 6,8–36% с четкой зависимостью от дозы и длительности приема препарата. В частности, при анализе результатов нескольких клинических исследований, включавших 22 938 больных ОА, пролеченных нимесулидом в дозе 100–400 мг в течение 5–21 сут (в среднем 12 сут), общая частота побочных реакций составила 8,2% [47]. По данным другого многоцентрового исследования, в котором участвовали 12 607 пациентов с различными ревматическими и ортопедическими заболеваниями, на фоне лечения нимесулидом 400–200 мг/сут в течение 21 сут частота развития побочных эффектов составила 6,8% [48].

Особого внимания заслуживают исследования, проводящиеся в условиях реальной клинической практики. Bradbury F. представил данные о частоте ЖКТ-осложнений при использовании диклофенака, нимесулида и ибупрофена. Суммарная частота поражения ЖКТ при использовании нимесулида была достоверно ниже по сравнению с таковой диклофенака (12,1%) и не отличалась от таковой ибупрофена – 8,1% и 8,6% соответственно [49]. Отечественными авторами была проведена оценка безопасности применения нимесулида в реальной клинической практике у 322 больных ревматическими заболеваниями, получавших нимесулид в суточной дозе 200 мг длительные сроки (12 мес.

 При анализе 10 608 спонтанных сообщений о серьезных побочных эффектах НПВП за период 1988–2000 гг., проведенном итальянскими учеными [54], оказалось, что частота побочных реакций со стороны ЖКТ на фоне приема нимесулида была в 2 раза ниже, чем на фоне препаратов сравнения (рис. 3).
При анализе 10 608 спонтанных сообщений о серьезных побочных эффектах НПВП за период 1988–2000 гг., проведенном итальянскими учеными [54], оказалось, что частота побочных реакций со стороны ЖКТ на фоне приема нимесулида была в 2 раза ниже, чем на фоне препаратов сравнения (рис. 3). Большой интерес представляют исследования безопасности применения нимесулида в высокой суточной дозе. Так, применение нимесулида в суточной дозе 400 мг у больных РА продемонстрировало не только высокую эффективность, но и хорошую переносимость препарата [55]. Позднее отечественными авторами было проведено многоцентровое исследование эффективности и безопасности нимесулида в суточных дозах 200 и 400 мг в сравнении с диклофенаком 100 и 200 мг/сут в течение 4-х нед. с ЭГДС-контролем при раннем РА. Результаты исследования продемонстрировали, что эффективность нимесулида была несколько выше, чем диклофенака, а развитие язв и множественных эрозий желудка или ДПК на фоне приема нимесулида было достоверно ниже, чем у больных, принимавших диклофенак, – 1,3% и 5,9% соответственно [45]. Совсем недавно были опубликованы результаты популяционного исследования, проведенного итальянскими учеными. Оценивался риск развития НПВП-ассоциированных осложнений со стороны ЖКТ у 588 827 пациентов при 3 623 341 назначений различных НПВП за период с 2001 по 2008 г. Следует особо подчеркнуть, что низкий риск развития серьезных ЖКТ-осложнений на фоне приема нимесулида был сопоставим с таковым у целекоксиба [56].
Совсем недавно были опубликованы результаты популяционного исследования, проведенного итальянскими учеными. Оценивался риск развития НПВП-ассоциированных осложнений со стороны ЖКТ у 588 827 пациентов при 3 623 341 назначений различных НПВП за период с 2001 по 2008 г. Следует особо подчеркнуть, что низкий риск развития серьезных ЖКТ-осложнений на фоне приема нимесулида был сопоставим с таковым у целекоксиба [56].
Аспекты кардиоваскулярной безопасности с-НПВП широко обсуждаются в мировой литературе. По результатам анализа, проведенного А. Helin-Salmivaara еt al., значение относительного риска инфаркта миокарда для нимесулида составило 1,69, что не превышало суммарного риска для всего класса [57]. По данным отечественных авторов, из 322 больных РА инфаркт миокарда был зафиксирован у 1 мужчины 68 лет с длительным анамнезом ИБС и АГ. Стойкое повышение АД отмечено у 11,5% больных, у 2 больных с наличием высокой степени риска АГ в анамнезе была выявлена отрицательная динамика на ЭКГ [50]. Следует отметить, что в исследованиях, проведенных зарубежными авторами (результаты которых упоминались выше), значимого повышения частоты кардиоваскулярных осложнений на фоне приема нимесулида не отмечалось [43, 44].
Следует отметить, что в исследованиях, проведенных зарубежными авторами (результаты которых упоминались выше), значимого повышения частоты кардиоваскулярных осложнений на фоне приема нимесулида не отмечалось [43, 44].
Вопросы гепатотоксичности нимесулида многократно обсуждались медицинской общественностью на протяжении нескольких последних лет. Анализ литературных данных свидетельствует о том, что гепатотоксичность нимесулида не выше, чем у других НПВП [58]. При кратковременном использовании нимесулида (не более 30 дней) повышение АЛТ и АСТ в 2 и более раз отмечается лишь у 0,4% больных, а при длительном (более 6 мес.) – частота подобных изменений не превышает 1,5% [59, 60]. У 322 больных, получавших нимесулид в течение 12 мес., не было выявлено ни одного случая развития клинических симптомов поражения печени (желтухи, гепатомегалии, симптомов печеночной недостаточности). Повышение уровня печеночных трансаминаз (АСТ, АЛТ) более чем в 2 раза было зарегистрировано в 7 случаях (2,2%) у больных РА, получавших еще и метотрексат и лефлуномид [50].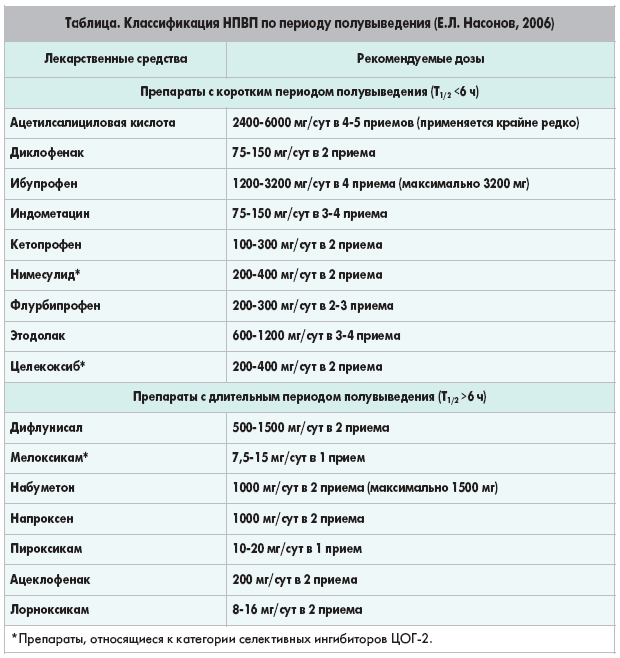 В самом крупном популяционном исследовании гепатотоксичности нимесулида [61] представлен анализ частоты лекарственного поражения печени у 397 537 пациентов, получавших различные НПВП за период 1997–2001 гг. Было показано, что нимесулид вызывал гепатопатии в 35,5 случая на 100 тыс. пациентов, что значительно реже, чем диклофенак – 39,2 и ибупрофен – 44,6. По данным испанских исследователей [62], за 10-летний период применения нимесулида серьезные гепатотоксические осложнения развивались крайне редко (рис. 4). Интересны результаты, полученные отечественными авторами в ходе изучения влияния нимесулида на функцию печени при лечении подагрического артрита. Как известно, пациенты с подагрой зачастую имеют метаболические нарушения и высокую частоту злоупотребления алкоголем, что повышает риск развития побочных реакций со стороны печени. Однако на фоне использования нимесулида в дозах до 400 мг/сут отсутствовала отрицательная динамика биохимических показателей крови, свидетельствующих о поражении печеночных клеток или холестазе [63].
В самом крупном популяционном исследовании гепатотоксичности нимесулида [61] представлен анализ частоты лекарственного поражения печени у 397 537 пациентов, получавших различные НПВП за период 1997–2001 гг. Было показано, что нимесулид вызывал гепатопатии в 35,5 случая на 100 тыс. пациентов, что значительно реже, чем диклофенак – 39,2 и ибупрофен – 44,6. По данным испанских исследователей [62], за 10-летний период применения нимесулида серьезные гепатотоксические осложнения развивались крайне редко (рис. 4). Интересны результаты, полученные отечественными авторами в ходе изучения влияния нимесулида на функцию печени при лечении подагрического артрита. Как известно, пациенты с подагрой зачастую имеют метаболические нарушения и высокую частоту злоупотребления алкоголем, что повышает риск развития побочных реакций со стороны печени. Однако на фоне использования нимесулида в дозах до 400 мг/сут отсутствовала отрицательная динамика биохимических показателей крови, свидетельствующих о поражении печеночных клеток или холестазе [63].
Результаты метаанализа за 10-летний период (с 1988 по 1997 г.) продемонстрировали, что на 100 тыс. пациентов, принимавших нимесулид, отмечено только 11 случаев возможной связи почечных осложнений с приемом препарата, из которых только в 4-х проводилась монотерапия нимесулидом [64].
Установлено, что нимесулид крайне редко вызывает усиление бронхоспазма у больных, страдающих бронхиальной астмой и гиперчувствительностью к ацетилсалициловой кислоте или другим НПВП, поскольку не обладает перекрестной реактивностью с ацетилсалициловой кислотой и н-НПВП в отношении индукции обострения астмы и является одним из препаратов выбора (среди с-НПВП) у этих больных [25, 65].
Как уже упоминалось, экспериментальные данные продемонстрировали отсутствие у нимесулида отрицательного действия на хрящ [33, 34]. Несколько позже W. Kullch et al. в пилотном клиническом исследовании отметили положительное влияние нимесулида на течение ОА тазобедренных и коленных суставов [66].
Результаты научных исследований и большой клинический опыт применения нимесулида свидетельствуют о его высокой анальгетической и противовоспалительной активности и хорошей переносимости. Все вышесказанное послужило основанием для появления целого ряда дженериков этого препарата. Недавно в России появился новый дженерик нимесулида – Немулекс® в виде гранул для приготовления суспензии. Такая лекарственная форма препарата обеспечивает более быстрое наступление клинического эффекта по сравнению с таблетированной формой. Отличительной особенностью Немулекса является отсутствие в его составе высококалорийного полисахарида мальтодекстрина, что позволяет назначать препарат пациентам с СД, избыточной массой тела, нарушением обмена веществ.
К настоящему времени уже имеются данные о результатах открытых проспективных краткосрочных (10–15 дней) клинических исследований препарата в суточной дозе 200 мг в ревматологической и неврологической практике [67–69].
Так, положительный эффект препарата Немулекс® в отношении основных клинических проявлений анкилозирующего спондилита у 30 больных продемонстрирован в исследовании НАУТИЛУС. По данным авторов, клинически значимого улучшения достигли 60% пациентов, при этом выраженность боли в спине уменьшилась в 2 раза. Побочные реакции включали повышение АСТ, АЛТ у 10% пациентов (купировались в течение 1 нед. на фоне диеты и назначения гепатопротекторов) и диспетические проявления у 10% пациентов (без наличия эрозивных изменений ЖКТ при проведении ЭГДС-контроля) [67].
По данным авторов, клинически значимого улучшения достигли 60% пациентов, при этом выраженность боли в спине уменьшилась в 2 раза. Побочные реакции включали повышение АСТ, АЛТ у 10% пациентов (купировались в течение 1 нед. на фоне диеты и назначения гепатопротекторов) и диспетические проявления у 10% пациентов (без наличия эрозивных изменений ЖКТ при проведении ЭГДС-контроля) [67].
Еще одно исследование было посвящено оценке эффективности и безопасности препарата Немулекс® в сравнении с диклофенаком, индометацином у 30 больных ОА. По данным авторов, эффективность всех препаратов была сопоставимой и не различалась статистически. Однако при использовании Немулекса анальгетический эффект развивался примерно на 2 дня раньше, чем у препаратов сравнения. Побочные эффекты на фоне приема Немулекса отмечались у 4 пациентов (13% случаев). У 3 больных имели место диспептические расстройства, у 1 – подъем АД. Побочные реакции были слабо выражены и не требовали отмены препарата [68].
По данным Д.И. Лахина, у 30 больных ОА через 15 дней лечения отмечены исчезновение признаков синовита, достоверное уменьшение боли (с 69,3±0,74 до 21±0,29), а также улучшение функции суставов у всех пациентов. Среди побочных реакций фигурировали только признаки гастропатии у 2 (6,7%) пациентов (при наличии в анамнезе язвенной болезни желудка). По мнению подавляющего большинства пациентов (23 человека – 76,6%), переносимость лечения была хорошей, у 7 (23,3%) – удовлетворительной [69].
В амбулаторных условиях проведено исследование, включавшее 49 пациентов с дорсопатией. Все пациенты получали комплексное лечение, включающее Немулекс® и Хондрогард. Через 15 дней большинство пациентов (29 человек – 59,5%) отметили исчезновение болей в спине. 2 пациента (4%) отметили появление дискомфорта в эпигастрии, что привело к самостоятельной отмене препарата. При этом, по данным автора, контрольная ЭГДС патологических изменений не выявила [72].
Таким образом, результаты исследований показали, что Немулекс® обладает отчетливым анальгетическим и противовоспалительным свойствами в сочетании с хорошей переносимостью. Тем не менее, учитывая короткие сроки и небольшое количество исследований, целесообразно изучить эффективность и безопасность препарата в более длительные сроки на различных когортах пациентов.
Тем не менее, учитывая короткие сроки и небольшое количество исследований, целесообразно изучить эффективность и безопасность препарата в более длительные сроки на различных когортах пациентов.
Выбор нестероидных противовоспалительных препаратов у больных ревматологического профиля с сопутствующими сердечно-сосудистыми заболеваниями | #07/16
Современную клиническую практику трудно представить без нестероидных противовоспалительных лекарственных препаратов (НПВП), сочетающих в себе противовоспалительный, анальгезирующий и жаропонижающий эффекты. Этот класс препаратов широко используется при различных ревматологических заболеваниях (РЗ), которые имеют высокую распространенность в Российской Федерации, — ими страдают более 16 млн человек. В структуре РЗ лидирующую позицию занимает остеоартрит (ОА) (более 4 млн человек), далее следуют ревматоидный артрит (РА) (около 280 тысяч больных), остеопороз (более 150 тысяч больных) и спондилопатии (около 90 тысяч больных) [1, 2].
Большая распространенность различных РЗ во всех возрастных группах, в том числе у лиц пожилого и старческого возраста, тенденция к прогрессированию и хронизации течения, ранняя инвалидизация больных, негативное влияние заболеваний на качество жизни пациентов делают РЗ серьезной медико-социальной проблемой, требующей особого внимания со стороны практикующих врачей [3].
Коморбидность в ревматологии
Особенностью течения РЗ в старших возрастных группах является частое наличие различных коморбидных заболеваний и состояний, которые оказывают дополнительное негативное влияние на течение заболевания, на качество жизни, на прогноз и, что не менее важно, зачастую затрудняют проведение эффективной и безопасной фармакотерапии. Последнее напрямую связано с часто встречающейся у этих больных необоснованной полипрагмазией, потенциально опасными межлекарственными взаимодействиями и, как следствие, высоким риском развития нежелательных лекарственных реакций (НЛР).
У больных старшего возраста наиболее частым коморбидным фоном при РЗ, прежде всего при остеоартрите, являются сердечно-сосудистые заболевания (ССЗ), такие как артериальная гипертензия (АГ) и ишемическая болезнь сердца (ИБС), а также ожирение и сахарный диабет 2-го типа (СД 2-го типа) [4]. Так, при ОА ожирение встречается в 2,25 раза чаще, а ИБС в 1,73 раза чаще, чем у больных без ОА [5]. У больных с РА часто встречаются АГ, дислипидемия, переломы костей различной локализации, ИБС и СД 2-го типа [6].
Так, при ОА ожирение встречается в 2,25 раза чаще, а ИБС в 1,73 раза чаще, чем у больных без ОА [5]. У больных с РА часто встречаются АГ, дислипидемия, переломы костей различной локализации, ИБС и СД 2-го типа [6].
Следует отметить, что и АГ, и дислипидемия, и ожирение, часто встречающиеся у больных с различными РЗ, по сути являются компонентами метаболического синдрома (МС) — совокупности факторов риска ССЗ и СД 2-го типа, имеющих общие патогененетические механизмы, в основе которых лежат инсулинорезистентность и гиперинсулинемия [7]. Клинические проявления МС чрезвычайно многообразны, и к ним относятся, помимо вышеперечисленных, также жировая дистрофия печени, нарушения пуринового обмена, синдром поликистозных яичников, заболевания периферических сосудов, цереброваскулярные заболевания, эректильная дисфункция и хронические заболевания почек [8].
Высокая распространенность МС среди пациентов с РЗ по сравнению с общей популяцией объясняется общностью патогенеза отдельных компонентов МС и РЗ. Так, доказано, что жировая ткань способна вырабатывать огромное количество биологически активных веществ — адипокинов, оказывающих влияние напрямую или через различные нейроэндокринные механизмы на различные процессы в организме человека. В частности, изучение таких адипокинов, как лептин, адипонектин, висфатин и резистин, показало их роль в патогенезе как сердечно-сосудистых (СС), так и ревматологических заболеваний [9].
Так, доказано, что жировая ткань способна вырабатывать огромное количество биологически активных веществ — адипокинов, оказывающих влияние напрямую или через различные нейроэндокринные механизмы на различные процессы в организме человека. В частности, изучение таких адипокинов, как лептин, адипонектин, висфатин и резистин, показало их роль в патогенезе как сердечно-сосудистых (СС), так и ревматологических заболеваний [9].
Общая характеристика НПВП
НПВП — большая гетерогенная группа лекарственных средств (ЛС), обладающих обезболивающими, противовоспалительными и жаропонижающими свойствами.
В настоящее время в клинической практике известно более 20 различных представителей этой группы, имеющих различия по химической структуре, особенностям механизма действия, показаниям к применению и переносимости.
Механизм действия всех НПВП основывается на ингибировании фермента циклооксигеназы (ЦОГ), и тем самым нарушается образование синтеза простагландинов, которые являются важными физиологическими и патологическими медиаторами. Простагландины принимают участие в таких процессах, как боль, воспаление, гипертермия, онкогенез, остеопороз, регуляция работы почек и т. д. Из арахидоновой кислоты с участием ЦОГ образуется простагландин H2, который является предшественником таких простагландинов, как тромбоксан (TxA2), простациклин (PGI2), D2, E2 и F2 (рис. 1).
Простагландины принимают участие в таких процессах, как боль, воспаление, гипертермия, онкогенез, остеопороз, регуляция работы почек и т. д. Из арахидоновой кислоты с участием ЦОГ образуется простагландин H2, который является предшественником таких простагландинов, как тромбоксан (TxA2), простациклин (PGI2), D2, E2 и F2 (рис. 1).
Известно две основные изоформы ЦОГ — ЦОГ-1 и ЦОГ-2. Выделение в экспериментальных условиях третьей изоформы ЦОГ-3 как варианта ЦОГ-1 остается дискутабельным [12, 13]. Первая изоформа ЦОГ-1 синтезируется постоянно и работает по универсальному механизму, т. е. независимо от того, в каком органе или ткани идет синтез. Синтез второй изоформы ЦОГ-2 стимулируется различными факторами воспаления (липополисахариды, интерлейкины, ФНО-α) в различных клетках организма человека, таких как эндотелий, остеокласты, синовиоциты, моноциты и макрофаги [10].
Основные фармакодинамические свойства НПВП — это противовоспалительный, жаропонижающий и обезболивающие эффекты, обеспечиваются посредством ингибирования ЦОГ-1 и ЦОГ-2 [14, 15]. И именно ингибированием ЦОГ-1 и ЦОГ-2 обусловлены основные нежелательные реакции на фоне применения НПВП. Простагландины PGE2 и PGI2, которые синтезируются с участием ЦОГ-1 в желудочно-кишечном тракте (ЖКТ), являются цитопротекторами слизистой оболочки за счет снижения секреции париетальными клетками желудка соляной кислоты, улучшения кровотока и стимуляции выработки слизи. Кроме того, с участием ЦОГ-1 происходит синтез тромбоксана TxA2 в тромбоцитах, обладающего вазоконстриктивными и проагрегантными свойствами. НПВП, блокируя синтез ЦОГ-1, могут приводить к повреждению слизистой оболочки желудка и кишечника и нарушению агрегации тромбоцитов. Таким образом, НПВП увеличивают риск развития таких серьезных желудочно-кишечных заболеваний, как воспаление, кровотечение и пенетрация желудка или кишечника. Риск развития таких осложнений выше у людей пожилого возраста и не зависит от длительности применения ЛС [16].
И именно ингибированием ЦОГ-1 и ЦОГ-2 обусловлены основные нежелательные реакции на фоне применения НПВП. Простагландины PGE2 и PGI2, которые синтезируются с участием ЦОГ-1 в желудочно-кишечном тракте (ЖКТ), являются цитопротекторами слизистой оболочки за счет снижения секреции париетальными клетками желудка соляной кислоты, улучшения кровотока и стимуляции выработки слизи. Кроме того, с участием ЦОГ-1 происходит синтез тромбоксана TxA2 в тромбоцитах, обладающего вазоконстриктивными и проагрегантными свойствами. НПВП, блокируя синтез ЦОГ-1, могут приводить к повреждению слизистой оболочки желудка и кишечника и нарушению агрегации тромбоцитов. Таким образом, НПВП увеличивают риск развития таких серьезных желудочно-кишечных заболеваний, как воспаление, кровотечение и пенетрация желудка или кишечника. Риск развития таких осложнений выше у людей пожилого возраста и не зависит от длительности применения ЛС [16].
НПВП принято разделять на три группы (табл. 1):
1):
- традиционные — неселективные ингибиторы ЦОГ-1 и ЦОГ-2;
- селективные ингибиторы ЦОГ-2, которые в меньшей степени оказывают влияние на ЦОГ-1;
- высокоселективные ингибиторы ЦОГ-2, практически не действующие на ЦОГ-1.
Селективность НПВП в отношении изоформ ЦОГ принято оценивать по отношению степени ингибирования ЦОГ-1 к ЦОГ-2 (коэффициент селективности). Селективными ингибиторами ЦОГ-2 являются те НПВП, у которых данный коэффициент более 5, высокоселективными ингибиторами — если данный коэффициент более 50. НПВП, которые имеют высокую селективность в отношении ЦОГ-2, получили название коксибов (от англ. сyclo-oxygenase, сокращенный вариант COX).
В настоящее время на рынке лекарственных средств по статистике продаж самыми популярными из НПВП являются препараты первых двух групп — ибупрофен, кеторолак, диклофенак, нимесулид, мелоксикам, кетопрофен, индометацин [17].
Несмотря на значимость фармакологических эффектов НПВП и их широкое применение в клинической практике, следует помнить о потенциальном риске развития НЛР, в том числе и серьезных, таких как желудочно-кишечные кровотечения, острый инфаркт миокарда, острая почечная недостаточность и др. Чаще всего встречающиеся НЛР при приеме НПВП развиваются со стороны ЖКТ — 10–50%, со стороны сердечно-сосудистой системы (ССС) — до 5%, мочевыделительной системы — до 5% и др. [18].
Чаще всего встречающиеся НЛР при приеме НПВП развиваются со стороны ЖКТ — 10–50%, со стороны сердечно-сосудистой системы (ССС) — до 5%, мочевыделительной системы — до 5% и др. [18].
Кардиоваскулярные осложнения при приеме НПВП
Учитывая высокую распространенность коморбидности сердечно-сосудистых и ревматических заболеваний, особую актуальность имеют вопросы кардиоваскулярной токсичности НПВП, а также безопасности сопутствующей фармакотерапии. Следует вспомнить, что первоначально разработка селективных ингибиторов ЦОГ-2 была направлена на преодоление ограничений применения НПВП из-за риска развития нежелательных реакций со стороны ЖКТ, однако внедрение в клиническую практику коксибов столкнулось с другой проблемой безопасности при длительном применении — увеличением риска сердечно-сосудистых тромботических осложнений, инфаркта миокарда и инсульта [19].
В основе повышения риска тромботических осложнений на фоне селективных ингибиторов ЦОГ-2 лежит нарушение баланса между тромбоксаном и простациклином, регулирующими эндотелиальную функцию и агрегацию тромбоцитов. Селективные коксибы за счет избирательной блокады ЦОГ-2 нарушают баланс между уровнем тромбоксана и простациклина, что является основой для развития тромботических осложнений, однако результаты последующих клинических наблюдений показали, что и на фоне применения неселективных НПВП также повышается риск сердечно-сосудистых осложнений [20, 21].
Селективные коксибы за счет избирательной блокады ЦОГ-2 нарушают баланс между уровнем тромбоксана и простациклина, что является основой для развития тромботических осложнений, однако результаты последующих клинических наблюдений показали, что и на фоне применения неселективных НПВП также повышается риск сердечно-сосудистых осложнений [20, 21].
Возрос интерес к влиянию НПВП на ССС после изъятия с рынка высокоселективного ингибитора ЦОГ-2 рофекоксиба в связи с увеличением риска фатальных СС-событий. Встал вопрос о безопасности других НПВП, как традиционных, так и селективных ингибиторов ЦОГ-2.
Многолетний опыт применения различных НПВП во всем мире показал, что они оказывают неблагоприятное влияние на артериальное давление (АД), повышают риск развития тромботических осложнений и фибрилляции предсердий (ФП).
Современные международные рекомендации, основанные на результатах долгосрочных клинических исследований, ограничивают применение и коксибов, и неселективных НПВП у больных ИБС, инсультом или наличием высокого риска развития ИБС [22, 23].
Адекватный контроль АД один из важнейших факторов, влияющих на прогноз ССЗ. Было доказано, что НПВП способствуют повышению АД и снижают эффективность антигипертензивной терапии [24].
Другой нежелательной реакцией на фоне длительного применения НПВП является нарушение почечной функции, поскольку обе изоформы ЦОГ играют значимую роль в регуляции работы почек. Простагландины регулируют тонус сосудов, поддерживают нормальный кровоток, что является необходимым для поддержания нормальной функции почек. В настоящее время известно, что ингибирование ЦОГ-1 приводит к снижению клубочковой фильтрации, а ингибирование ЦОГ-2 замедляет реабсорбцию натрия у здоровых добровольцев и у людей пожилого возраста. Все это приводит к НПВП-индуцированному электролитному дисбалансу, который встречается почти у четверти больных, в сочетании со снижением уровня сосудорасширяющего простациклина приводит к увеличению АД и, следовательно, увеличивает риск осложнений со стороны ССС. Снижением уровня простациклина, участвующего в регуляции ренин-ангионтензин-альдестероновой системы, объясняется и развитие гиперкалиемии [25, 45].
По данным метаанализа селективные ингибиторы ЦОГ-2 увеличивают риск развития почечной недостаточности и аритмии [26].
Еще один механизм действия НПВП на ССС был продемонстрирован в экспериментальных исследованиях: ингибирование сосудистой ЦОГ-2 НПВП приводило к более низкому содержанию PG М-I (основного метаболита простациклина) в моче и ассоциировалось с повышением риска гипертонии и тромбозов. Именно дисбаланс между TxA2 и простагландинами с антитромботической активностью приводит к увеличению риска тромботических осложнений. К тому же снижение уровня простагландинов, участвующих в активации NO-синтетазы, и как следствие снижение биосинтеза оксида азота также способствуют дестабилизации АД.
Также одним из механизмов повышения АД может быть повышение периферического сопротивления, вследствие НПВП-ассоциированного склерозирования артерий [27].
Влияние НПВП на кальций-активируемые калиевые каналы также может способствовать развитию кардиоваскулярных осложнений [28].
Многочисленные исследования указывают на повышенный риск развития ФП, связанный с применением НПВП [29]. Механизм развития данного феномена до конца не изучен. Отмечено, что риск развития ФП выше у пациентов, принимающих НПВП более одного года [30].
И хотя все вышеописанные механизмы воздействия на ССС характерны для всех НПВП, независимо от ЦОГ-селективности, есть некоторые препараты, которые проявляют большую токсичность, чем другие. По наблюдениям, среди популярных НПВП диклофенак демонстрирует самый высокий риск развития осложнений со стороны ССС [31]. Однако считается, что низкие терапевтические дозы НПВП безопасны для назначения больным, не имеющим в анамнезе серьезных заболеваний почек и ССС. Более того, низкие дозы некоторых НПВП, таких как ибупрофен и напроксен, обладают антитромботической активностью. В свою очередь, высокие дозы НПВП, за исключением напроксена, ассоциируются с риском развития острого инфаркта миокарда.
По имеющимся на сегодняшний день данным наиболее безопасными НПВП являются амтолметин гуацил, напроксен и целекоксиб [32, 33, 46].
Особый интерес среди них представляет неселективный ингибитор ЦОГ — амтолметин гуацил, имеющий сопоставимую с другими НПВП эффективность, при этом не имеющий серьезных побочных эффектов со стороны ССС и ЖКТ [33–36]. На нашем фармацевтическом рынке он представлен препаратом Найзилат. Найзилат обладает всеми характерными для НПВП свойствами: противовоспалительное, жаропонижающее, обезболивающее, а также хорошим профилем безопасности, принципиально отличающим его от других НПВП. Главное отличие состоит в том, что препарат обладает защитным действием на слизистую ЖКТ, и реализуется оно за счет стимуляции рецепторов капсакаина и последующего высвобождения оксида азота.
По данным ряда клинических исследований и проведенного на их основе метаанализа амтолметин гуацила не уступает другим НПВП (диклофенак, пироксикам, напроксен, индометацин, ибупрофен и др.), однако по эффективности превосходит их по параметрам безопасности и профилю переносимости. Так, при приеме амтолметин гуацила ниже частота развития НЛР, особенно со стороны ЖКТ (подтверждено при эндоскопических исследованиях) [37], нет значимого влияния на уровень АД [38]. Чрезвычайно важным представляется и тот факт, что, в отличие от селективных ЦОГ-2 НПВП, которые не влияют на агрегацию тромбоцитов [39], амтолметин гуацила обладает сравнимой с действием АСК антитромбоцитарной активностью [40]. Благодаря наличию этого фармакологического эффекта препарат может являться препаратом выбора для пациентов.
Чрезвычайно важным представляется и тот факт, что, в отличие от селективных ЦОГ-2 НПВП, которые не влияют на агрегацию тромбоцитов [39], амтолметин гуацила обладает сравнимой с действием АСК антитромбоцитарной активностью [40]. Благодаря наличию этого фармакологического эффекта препарат может являться препаратом выбора для пациентов.
Наличие антитромбоцитарной активности и уникальный механизм защиты желудка, а также хорошая переносимость при длительных курсах терапии позволяют рассматривать амтолметин гуацила в качестве препарата выбора из группы НПВП у больных ревматологического профиля с сопутствующими сердечно-сосудистыми заболеваниями, с наличием факторов сердечно-сосудистого риска и другой соматической патологией (в частности, желудочно-кишечного тракта).
Фармакогенетические аспекты выбора НПВП
Главным принципом рациональной фармакотерапии является максимальная ее эффективность в сочетании с безопасностью. Эти параметры зависят от множества факторов, среди которых большое значение имеет функциональное состояние печени. Особенно важно это в отношении тех ЛС, которые метаболизируются в печени с участием целого ряда различных ферментов биотрансформации. Большое количество ЛС метаболизируются через систему цитохрома Р450, в том числе и НПВП. Генетические особенности пациентов также имеют важное значение в первую очередь для лекарственных препаратов, метаболизм которых происходит с участием изоферментов цитохрома Р450, различными аллельными вариантами которых и объясняется разнообразие фармакологических ответов у разных пациентов [41]. Знание генетических особенностей организма позволит практикующему врачу индивидуализировать фармакотерапию и персонализированно подходить к выбору ЛС и режима дозирования у каждого конкретного пациента, обеспечивая максимально эффективную и безопасную фармакотерапию. Такой подход позволит снизить частоту развития НЛР на лекарства, что напрямую связано с показателями приверженности пациентов к лечению. Для разных групп ЛС существуют свои гены-кандидаты, полиморфизмы в которых определяют фармакологический ответ и, следовательно, эффективность и безопасность фармакотерапии.
Особенно важно это в отношении тех ЛС, которые метаболизируются в печени с участием целого ряда различных ферментов биотрансформации. Большое количество ЛС метаболизируются через систему цитохрома Р450, в том числе и НПВП. Генетические особенности пациентов также имеют важное значение в первую очередь для лекарственных препаратов, метаболизм которых происходит с участием изоферментов цитохрома Р450, различными аллельными вариантами которых и объясняется разнообразие фармакологических ответов у разных пациентов [41]. Знание генетических особенностей организма позволит практикующему врачу индивидуализировать фармакотерапию и персонализированно подходить к выбору ЛС и режима дозирования у каждого конкретного пациента, обеспечивая максимально эффективную и безопасную фармакотерапию. Такой подход позволит снизить частоту развития НЛР на лекарства, что напрямую связано с показателями приверженности пациентов к лечению. Для разных групп ЛС существуют свои гены-кандидаты, полиморфизмы в которых определяют фармакологический ответ и, следовательно, эффективность и безопасность фармакотерапии. Гены-кандидаты могут определять фармакокинетику (ферменты биотрансформации, транспортеры) и фармакодинамику (рецепторы, ферменты, ионные каналы, липопротеины, белки клеточного цикла, сигнальные белки, факторы свертывания) ЛС [41].
Гены-кандидаты могут определять фармакокинетику (ферменты биотрансформации, транспортеры) и фармакодинамику (рецепторы, ферменты, ионные каналы, липопротеины, белки клеточного цикла, сигнальные белки, факторы свертывания) ЛС [41].
Для оценки эффективности и безопасности НПВП наиболее клинически значимо изучение гена-кандидата CYP2C9 [42].
Большинство НПВП являются субстратами CYP2C9, т. е. они метаболизируются с участием данного изофермента, и многие препараты, влияющие на активность CYP2C9 (индукторы или ингибиторы), могут менять фармакологический ответ на НПВП (рис. 2).
Имеет значение также полиморфизм гена CYP2C9. Так, у пациентов с аллельными вариантами CYP2C9*2 и CYP2C9*3 отмечаются более высокие значения максимальной концентрации НПВП в крови и увеличение периода полувыведения по сравнению с носителями CYP2C9*1/1 и, как следствие, выше риск развития НЛР [43] (рис. 3).
Наличие поражений печени различной этиологии, в том числе имеющих место у больных с МС, также может нарушать процессы трансформации лекарственных препаратов, метаболизм которых происходит в печени, изменять активность изоферментов цитохрома Р450 и, как следствие, изменять фармакологический ответ на НПВП [44], т. е. у больных с МС выше риск развития НЛР или низкой эффективности терапии.
е. у больных с МС выше риск развития НЛР или низкой эффективности терапии.
Межлекарственные взаимодействия НПВП
Еще один важный аспект фармакотерапии — это анализ межлекарственных взаимодействий НПВП с другими классами ЛС, также широко используемых у больных с сердечно-сосудистыми заболеваниями. Из антигипертензивных препаратов НПВП взаимодействуют практически со всеми, кроме антагонистов кальция (табл. 2).
Гиполипидемические препараты (ингибиторы ГМГ-КоА редуктазы или статины, секвестранты желчных кислот, эзетимиб, фибраты, никотиновая кислота, омега-3 полиненасыщенные жирные кислоты) не взаимодействуют с НПВП.
Из препаратов, используемых для лечения ишемической болезни сердца, клиническую значимость могут иметь межлекарственные взаимодействия с антитромботическими препаратами (клопидогрелом, АСК) (табл. 3).
При ФП и других видах аритмий могут быть назначены антиаритмики различных классов, а также антикоагулянты, такие как варфарин и новые оральные антикоагулянты (НОАК). Потенциально возможные результаты взаимодействия НПВП с данными ЛС представлены в табл. 4.
Потенциально возможные результаты взаимодействия НПВП с данными ЛС представлены в табл. 4.
Сахарный диабет 2-го типа — одно из самых серьезных проявлений метаболического синдрома, требующих обязательной и постоянной фармакотерапии. Из всех сахароснижающих препаратов неблагоприятные лекарственные взаимодействия возможны только с производными сульфонилмочевины (усиление гипогликемического эффекта) (табл. 5).
Заключение
Таким образом, широкое распространение в клинической практике коморбидных состояний и заболеваний, среди которых большую распространенность имеют ревматические заболевания и метаболический синдром, определяют необходимость выбора оптимальной фармакотерапии. В вопросах рационального выбора НПВП у ревматологических больных с коморбидными заболеваниями остается еще много нерешенных вопросов.
Наличие антитромбоцитарной активности и уникальный механизм защиты желудка, а также хорошая переносимость при длительных курсах терапии позволяют рассматривать амтолметин гуацила в качестве препарата выбора из группы НПВП у больных ревматологического профиля с сопутствующими сердечно-сосудистыми заболеваниями, с наличием факторов сердечно-сосудистого риска и другой соматической патологией (в частности, желудочно-кишечного тракта).
Перспективным также представляется поиск новых подходов к прогнозированию и профилактике возможных НЛР при применении различных НПВП в зависимости от функциональных показателей печеночного метаболизма.
Литература
- Балабанова Р. М., Эрдес Ш. Ф. Распространенность ревматических заболеваний в России в 2012–2013 гг. // Научно-практическая ревматология. 2015; 53 (2): 120–124.
- Каратеев А. Е., Насонов Е. Л., Яхно Н. Н. и др. Клинические рекомендации «Рациональное применение нестероидных противовоспалительных препаратов (НПВП) в клинической практике» // Современная ревматология. 2015.
- Насонова В. А., Фоломеева О. М., Эрдес Ш. Ф. Ревматические заболевания в Российской Федерации в начале XXI века глазами статистики // Терапевтический архив. 2009; (6): 5–10.
- Rosemann T., Laux G., Szecsenyi J. Osteoarthritis: quality of life, comorbidities, medication and health service utilization assessed in a large sample of primary care patients // J Orthop Surg Res.
 2007, Jun 30; 2: 12.
2007, Jun 30; 2: 12. - Kadam U. T., Jordan K., Croft P. R. Clinical comorbidity in patients with osteoarthritis: a case-control study of general practice consulters in England and Wales // Ann Rheum Dis. 2004 Apr; 63 (4): 408–414.
- Панафидина Т. А., Кондратьева Л. В., Герасимова Е. В. и др. Коморбидность при ревматоидном артрите // Научно-практическая ревматология. 2014; 52 (3): 283–289.
- Reaven G. M. Banting lecture 1988. Role of insulin resistance inhuman disease // Diabetes. 1988; 37: 1595–1607.
- Lam D. W., LeRoith D. Metabolic Syndrome. [Updated 2015 May 19]. In: De Groot L. J., Beck-Peccoz P., Chrousos G. et al., editors. Endotext.
- Abella V., Scotece M., Conde J. et al. Adipokines, metabolic syndrome and rheumatic diseases // Journal of Immunology Research. 2014; 2014: 14.
- Rao P., Knaus E. E. Evolution of nonsteroidal anti-inflammatory drugs (NSAIDs): Cyclooxygenase (COX) inhibition and beyond // J.
 Pharm. & Pharm. Sci. 2008, 11, 81s–110s.
Pharm. & Pharm. Sci. 2008, 11, 81s–110s. - Herndon C. M., Hutchison R. W., Berdine H. J. et al. Management of Chronic Nonmalignant Pain with Nonsteroidal Antiinflammatory Drugs Joint Opinion Statement of the Ambulatory Care, Cardiology, and Pain and Palliative Care Practice and Research Networks of the American College of Clinical Pharmacy // Pharmacotherapy. 2008; 28 (6): 788–805.
- Simmons D. L. Variants of cyclooxygenase-1 and their roles in medicine // Thromb Res. 2003, Jun 15; 110 (5–6): 265–268.
- Chandrasekharan N. V., Hu Dai, Lamar Turepu Roos K., Nathan K. Evanson, Joshua Tomsik, Terry S. Elton, Daniel L. Simmons. COX-3, a cyclooxygenase-1 variant inhibited by acetaminophen and other analgesic/antipyretic drugs: Cloning, structure, and expression PNAS published September 19, 2002, 10.1073/pnas.162468699.
- Zidar N., Odar K., Glavac D., Jerse M., Zupanc T., Stajer D. Cyclooxygenase in normal human tissues — is COX-1 really a constitutive isoform, and COX-2 an inducible isoform? // J Cell Mol Med.
 2009 Sep; 13 (9 B): 3753–3763.
2009 Sep; 13 (9 B): 3753–3763. - Khan K. N., Stanfield K. M., Dannenberg A., Seshan S. V., Baergen R. N., Baron D. A. et al. Cyclooxygenase-2 expression in the developing human kidney // Pediatr Develop Pathol. 2001, Sep-Oct; 4 (5): 461–466.
- Henry D., Lim L. L.-Y., Rodriguez L. G. et al. Variability in risk of gastrointestinal complications with individual NSAIDs: results of a collaborative meta-analysis // BrMed J. 1996: 312: 1563–1566.
- Барскова В. Г. Что нам дает изучение статистики продаж нестероидных противовоспалительных препаратов в Российской Федерации? // Современная ревматология. 2011, № 3, с. 68–72.
- Harirforoosh S., Asghar W., Jamali F. Adverse Effects of Nonsteroidal Antiinflammatory Drugs: An Update of Gastrointestinal, Cardiovascular and Renal Complications // J Pharm Pharm Sci. 2013; 16 (5): 821–847.
- Solomon S. D., Wittes J., Finn P. V. et al.
 For the Cross Trial Safety Assessment Group. Cardiovascular risk of celecoxib in 6 randomized placebo-controlled trials: the cross trial safety analysis // Circulation. 2008; 117 (16): 2104–2113.
For the Cross Trial Safety Assessment Group. Cardiovascular risk of celecoxib in 6 randomized placebo-controlled trials: the cross trial safety analysis // Circulation. 2008; 117 (16): 2104–2113. - Gislason G. H., Jacobsen S., Rasmussenet J. N. et al. Risk of death or reinfarction associated with the use of selective cyclooxygenase-2 inhibitors and nonselective nonsteroidal antiinflammatory drugs after acute myocardial infarction // Circulation. 2006; 113: 2906–2913.
- McGettigan P., Henry D. Cardiovascular risk and inhibition of cyclooxygenase. A systematic review of the observational studies of selective and nonselective inhibitors of cyclooxygenase // JAMA. 2006; 296: 1633–1644.
- Herndon C. M., Hutchison R. W., Berdine H. J. et al. Management of Chronic Nonmalignant Pain with Nonsteroidal Antiinflammatory Drugs Joint Opinion Statement of the Ambulatory Care, Cardiology, and Pain and Palliative Care Practice and Research Networks of the American College of Clinical Pharmacy // Pharmacotherapy.
 2008; 28 (6): 788–805.
2008; 28 (6): 788–805. - Antman E. M., Bennett J. S., Daughertyet А. et al. Use of nonsteroidal antiinflammatory drugs: an update for clinicians: a scientific statement from the American Heart Association // Circulation. 2007, 115, 1634–1642.
- Forman J. P., Rimm E. B., Curhan G. C. Frequency of analgesic use and risk of hypertension among men // Arch Intern Med. 2007, Feb 26; 167 (4): 394–399.
- Stichtenoth D. O., Frolich J. C. COX-2 and the kidneys // Curr Pharm Des. 2000; 6 (17): 1737–53.
- Zhang J., Ding E. L., Song Y. Adverse Effects of Cyclooxygenase 2 Inhibitors on Renal and Arrhythmia Events Meta-analysis of Randomized Trials // JAMA. 2006; 296 (13): 1619–1632.
- Yu Z., Crichton I., Tang S. Y., Hui Y., Ricciotti E., Levin M. D. et al. Disruption of the 5-lipoxygenase pathway attenuates atherogenesis consequent to COX-2 deletion in mice // Proc Natl Acad Sci USA. 2012, Apr 24; 109 (17): 6727–6732.

- Brueggemann L. I., Mackie A. R., Cribbs L. L., Byron K. L. Novel Actions of Nonsteroidal Anti-Inflammatory Drugs on Vascular Ion Channels: Accounting for Cardiovascular Side Effects and Identifying New Therapeutic Applications Mol Cell Pharmacol. 2010; 2 (1): 15–19.
- Schmidt M., Christiansen C. F., Mehnert F., Rothman K. J., Sorensen H. T. Non-steroidal anti-inflammatory drug use and risk of atrial fibrillation or flutter: population based case-control study // Brit Med J. 2011; 343: d3450.
- De Caterina R., Ruigomez A., Rodriguez L. A. Long-term use of anti-inflammatory drugs and risk of atrial fibrillation // Arch Intern Med. 2010 Sep 13; 170 (16): 1450–1455.
- Fosbol E. L., Gislason G. H., Jacobsen S., Folke F., Hansen M. L., Schramm T. K. et al. Risk of myocardial infarction and death associated with the use of nonsteroidal anti-inflammatory drugs (NSAIDs) among healthy individuals: a nationwide cohort study // Clin Pharmacol Ther.
 2009 Feb; 85 (2): 190–197.
2009 Feb; 85 (2): 190–197. - Fosbol E. L., Folke F., Jacobsen S., Rasmussen J. N., Sorensen R., Schramm T. K. et al. Cause-specific cardiovascular risk associated with nonsteroidal anti-inflammatory drugs among healthy individuals. Circulation Cardiovascular quality and outcomes. 2010 Jul; 3 (4): 395–405.
- Пахомова И. Г. Новые возможности в минимизации риска НПВП-индуцированных гастропатий // Рус. мед. журн. 2014; 10: 772–776.
- Пасечников В. Д. Механизмы защиты слизистой оболочки желудка и NO-высвобождающие нестероидные противовоспалительные препараты // Consilium Medicum. 2013; 9: 76–80.
- Якоб О. В. Есть ли возможность снизить риск развития НПВП-гастропатии // Фарматека. 2013; 6: 16–21.
- Тавелла А., Урсини Дж. Клиническое исследование противовоспалительной ак-тивности и переносимости со стороны желудочно-кишечного тракта Амтолметина гуацила (нового НПВП) по сравнению с диклофенаком у пациентов пожилого возраста с патологиями костно-суставной системы // Рус.
 мед. журн. 2013; 32.
мед. журн. 2013; 32. - Marcolongo R., Frediani B., Biasi G. et al. Metanalysis of the tolerability of amtolmetin-guacyl, a new, efficacious, non-steroidal anti-inflammatory drug, compared with traditional NSAIDs // Clin Drug Invest. 1999; 17: 89–96.
- Гайдукова И. З., Ребров А. П., Хондкарян Э. В., Апаркина А. В. Эффективность и кардиоваскулярная безопасность амтолметин гуацила в лечении больных анкилозирующим спондилитом (болезнь Бехтерева): окончательные результаты исследования КОРОНА // Фарматека. 2016, № 7, с. 53–58.
- Wilner K. D., Rushing M., Walden C. et al. Celecoxib does not affect the antiplatelet activity of aspirin in healthy volunteers // J Clin Pharmacol. 2002; 42: 1027–1030.
- Tubaro E., Belogi L., Mezzadri C. M. Anti-inflammatory and antiplatelet effect of Amtolmetin Guacyl, a new gastroprotective non-steroidal anti-inflammatory drug // Arzneim Forsch Drug Res. 2001; 51: 737–742.

- Сычев Д. А., Кукес В. Г. и соавт. Клиническая фармакогенетика. М.: ГЭОТАР-Медиа, 2004.
- Сычев Д. А. и др. Фармакогенетика в ревматологии: перспективы индивидуализации фармакотерапии // Научно-практ. ревматология. 2005. № 5. С. 59–63.
- Carmen Marti´nez, Gerardo Blanco, Jose´ M. Ladero and etc. Genetic predisposition to acute gastrointestinal bleeding after NSAIDs use // Br J Pharmacol. 2004, Jan; 141 (2): 205–208.
- Merrell M. D., Cherrington N. J. Drug metabolism alterations in nonalcoholic fatty liver disease // Drug Metab Rev. 2011, August; 43 (3): 317–334.
- Brater D. C. Effects of nonsteroidal anti-inflammatory drugs on renal function: focus on cyclooxygenase-2-selective inhibition // Am J Med. 1999; 107 (6 A): 65 S-70 S.
- Khan M., Fraser A. Cox-2 inhibitors and the risk of cardiovascular thrombotic events // Ir Med J. 2012, Apr; 105 (4): 119–121.

Т. Е. Морозова1, доктор медицинских наук, профессор
Д. Г. Шмарова
С. М. Рыкова, кандидат медицинских наук
ГБОУ ВПО Первый МГМУ им. И. М. Сеченова МЗ РФ, Москва
Контактная информация: [email protected]
НПВП (нестероидные противовоспалительные препараты) от боли при артрите Лекарства
НПВП — нестероидные противовоспалительные препараты — относятся к типу болеутоляющих средств. В дозах, отпускаемых по рецепту, эти препараты также сдерживают воспаление.
Врачи используют НПВП для лечения многих заболеваний, вызывающих боль или воспаление, включая артрит.
Безрецептурные противовоспалительные препараты
НПВП, которые можно купить без рецепта, включают:
Никогда не используйте безрецептурные НПВП более 10 дней без консультации с врачом. НПВП, отпускаемые без рецепта, являются эффективными болеутоляющими средствами, но они предназначены для кратковременного применения. При приеме НПВП в течение длительного периода времени ваш врач должен внимательно следить за вашим самочувствием, чтобы он мог наблюдать за побочными эффектами и при необходимости изменить ваше лечение.
Рецептурные противовоспалительные препараты
The following NSAIDs are available only with a doctor’s prescription:
BRAND NAME | GENERIC NAME | |
Anaprox | naproxen sodium | |
Cambia, Cataflam | диклофенак калия | |
Целебрекс | целекоксиб | |
Clinoril | sulindac | |
Daypro | oxaprozin | |
Feldene | piroxicam | |
Indocin, Tivorbex | indomethacin | |
Мобик, Вивлодекс | Мелоксикам | |
Нальфон | fenoprofen | |
Naprelan, Naprosyn | naproxen | |
Vimovo | naproxen/esomeprazole | |
Voltaren, Zorvolex | diclofenac | |
дифлюнизал | ||
| этодолак |
|
| ketorolac tromethamine | |
| meclofenamate | |
| nabumetone | |
| salsalate |
Все отпускаемые по рецепту НПВП имеют предупреждение о том, что лекарства могут увеличить вероятность сердечного приступа, инсульта и желудочного кровотечения.
Все ли они работают одинаково?
Все они уменьшают боль и воспаление, но вы можете обнаружить, что один НПВП приносит больше облегчения, чем другой, а некоторые НПВП могут иметь меньше побочных эффектов, чем другие. Эффект отличается от человека к человеку.
Некоторые НПВП также могут быть более удобными, так как их нужно принимать только один или два раза в день.
Каковы общие побочные эффекты?
НПВП повышают риск сердечного приступа или инсульта, особенно в более высоких дозах. Они также могут вызвать желудочное кровотечение.
НПВП наиболее безопасны, если принимать их в малых дозах в течение коротких периодов времени. Побочные эффекты чаще всего возникают, если вы принимаете большие дозы в течение длительного времени (месяцы или годы).
Некоторые побочные эффекты незначительны и проходят сами по себе или после снижения дозы. Другие могут быть более серьезными и нуждаться в медицинской помощи.
Общие побочные эффекты НПВП включают:
- Боль в животе и изжогу
- Язвы желудка
- Склонность к усилению кровотечения, особенно при приеме аспирина.
 Ваш врач может посоветовать вам прекратить прием НПВП перед операцией. Спросите своего врача, прежде чем принимать НПВП, если вы принимаете разжижающие кровь препараты (например, кумадин).
Ваш врач может посоветовать вам прекратить прием НПВП перед операцией. Спросите своего врача, прежде чем принимать НПВП, если вы принимаете разжижающие кровь препараты (например, кумадин). - Головные боли и головокружение
- Звон в ушах
- Аллергические реакции, такие как сыпь, свистящее дыхание и отек горла
- Проблемы с печенью или почками. Если у вас есть какие-либо проблемы с почками, вам не следует принимать НПВП без консультации с врачом.
- Высокое кровяное давление
- Отек ног
Другие побочные эффекты встречаются реже.
У кого чаще возникают язвы желудка и кровотечения?
Любой человек может заболеть язвой желудка при приеме НПВП. Но это может быть более вероятно, если вы:
- Люди старше 60 лет
- Курят
- Имеют язву желудка в анамнезе
- Имеют более одной проблемы со здоровьем
- Употребляют три или более порций алкоголя в день
- Принимают противовоспалительные стероиды, такие как преднизолон111 почечная недостаточность
Как уменьшить побочные эффекты
Невозможно избежать побочных эффектов любого лекарства. Но вы и ваш врач можете снизить риск возникновения побочных эффектов от НПВП. Например:
Но вы и ваш врач можете снизить риск возникновения побочных эффектов от НПВП. Например:
- Используйте ацетаминофен вместо НПВП для облегчения боли, которая, по мнению вашего врача, не требует противовоспалительных препаратов.
- Примите наименьшую дозу НПВП, которая вам необходима.
- Принимайте НПВП вместе с пищей.
Если вам не требуется круглосуточное облегчение, избегайте приема одной дозы НПВП в день, особенно если вы старше 60 лет. Эти лекарства дольше остаются в организме и могут вызывать больше побочных эффектов.
Спросите своего врача о приеме второго препарата, такого как блокатор кислоты, который может снизить риск язвы желудка и кровотечения. Некоторые лекарства сочетают в себе НПВП и блокаторы кислоты в одной таблетке.
Если после начала приема НПВП вы испытываете длительную или необычную боль в животе, немедленно сообщите об этом своему врачу.
Как назначают НПВП?
Врачи назначают НПВП в разных дозах в зависимости от вашего состояния.
Дозировки могут варьироваться от одного до четырех раз в день, в зависимости от того, как долго каждый препарат остается в организме. Ваш врач может назначить более высокие дозы НПВП, если у вас, например, ревматоидный артрит (РА), потому что при РА часто наблюдается сильный жар, отек, покраснение и скованность в суставах.
Меньшие дозы могут быть достаточными при остеоартрите и мышечных травмах, так как обычно наблюдается меньший отек и часто нет тепла или покраснения в суставах.
Ни один НПВП не гарантирует эффективность. Ваш врач может назначить несколько типов НПВП, прежде чем найти тот, который лучше всего подходит для вас.
Могу ли я принимать НПВП, если меня лечат от высокого кровяного давления?
НПВП могут повышать артериальное давление у некоторых людей. Некоторым людям с высоким кровяным давлением, возможно, придется прекратить прием НПВП, если их кровяное давление повышается, даже если они регулярно принимают лекарства от кровяного давления.
Кому не следует принимать НПВП?
Попросите вашего врача, прежде чем принимать НПВП, если:
- У вас были серьезные побочные эффекты от приема болеутоляющего или жаропонижающего средства.
- У вас повышен риск желудочного кровотечения.
- У вас проблемы с желудком, в том числе изжога.
- У вас высокое кровяное давление, заболевание сердца, цирроз печени или заболевание почек.
- У вас астма.
- Вы принимаете мочегонное лекарство.
НПВП (нестероидные противовоспалительные препараты) при боли при артрите
Написано редакционными авторами WebMD
Медицинский обзор Дэвида Зельмана, доктора медицинских наук, 4 декабря 2020 г.
В этой статье Все работают одинаково?
НПВП — нестероидные противовоспалительные препараты — относятся к типу болеутоляющих средств. В дозах, отпускаемых по рецепту, эти препараты также сдерживают воспаление.
В дозах, отпускаемых по рецепту, эти препараты также сдерживают воспаление.
Врачи используют НПВП для лечения многих заболеваний, вызывающих боль или воспаление, включая артрит.
Противовоспалительные препараты, отпускаемые без рецепта
НПВП, которые можно купить без рецепта, включают:
Никогда не принимайте безрецептурные НПВП более 10 дней без консультации с врачом. НПВП, отпускаемые без рецепта, являются эффективными болеутоляющими средствами, но они предназначены для кратковременного применения. При приеме НПВП в течение длительного периода времени ваш врач должен внимательно следить за вашим самочувствием, чтобы он мог наблюдать за побочными эффектами и при необходимости изменить ваше лечение.
Противовоспалительные препараты, отпускаемые по рецепту
Следующие НПВП отпускаются только по рецепту врача:
BRAND NAME | GENERIC NAME | |
Anaprox | naproxen sodium | |
Cambia, Cataflam | diclofenac potassium | |
Целебрекс | Целекоксиб | |
Клинорил | Сулиндак | |
Daypro | oxaprozin | |
Feldene | piroxicam | |
Indocin, Tivorbex | indomethacin | |
Mobic, Vivlodex | meloxicam | |
Нальфон | фенопрофен | |
Напрелан, Напросин | naproxen | |
Vimovo | naproxen/esomeprazole | |
Voltaren, Zorvolex | diclofenac | |
| diflunisal | |
| этодолак | |
кеторолака трометамин | ||
| meclofenamate | |
| nabumetone | |
| salsalate |
All prescription NSAIDs have a warning that the medications может увеличить вероятность сердечного приступа, инсульта и желудочного кровотечения.
Все ли они работают одинаково?
Все они уменьшают боль и воспаление, но вы можете обнаружить, что один НПВП приносит больше облегчения, чем другой, а некоторые НПВП могут иметь меньше побочных эффектов, чем другие. Эффект отличается от человека к человеку.
Некоторые НПВП также могут быть более удобными, так как их нужно принимать только один или два раза в день.
Каковы общие побочные эффекты?
НПВП повышают риск сердечного приступа или инсульта, особенно в более высоких дозах. Они также могут вызвать желудочное кровотечение.
НПВП наиболее безопасны, если принимать их в малых дозах в течение коротких периодов времени. Побочные эффекты чаще всего возникают, если вы принимаете большие дозы в течение длительного времени (месяцы или годы).
Некоторые побочные эффекты незначительны и проходят сами по себе или после снижения дозы. Другие могут быть более серьезными и нуждаться в медицинской помощи.
Общие побочные эффекты НПВП включают:
- Боль в животе и изжогу
- Язвы желудка
- Склонность к усилению кровотечения, особенно при приеме аспирина.
 Ваш врач может посоветовать вам прекратить прием НПВП перед операцией. Спросите своего врача, прежде чем принимать НПВП, если вы принимаете разжижающие кровь препараты (например, кумадин).
Ваш врач может посоветовать вам прекратить прием НПВП перед операцией. Спросите своего врача, прежде чем принимать НПВП, если вы принимаете разжижающие кровь препараты (например, кумадин). - Головные боли и головокружение
- Звон в ушах
- Аллергические реакции, такие как сыпь, свистящее дыхание и отек горла
- Проблемы с печенью или почками. Если у вас есть какие-либо проблемы с почками, вам не следует принимать НПВП без консультации с врачом.
- Высокое кровяное давление
- Отек ног
Другие побочные эффекты встречаются реже.
У кого чаще возникают язвы желудка и кровотечения?
Любой человек может заболеть язвой желудка при приеме НПВП. Но это может быть более вероятно, если вы:
- старше 60 лет
- курите
- имеете язву желудка в анамнезе
- Имеют более одной медицинской проблемы
- Употребляют три или более порций алкоголя в день
- Принимают противовоспалительные стероиды, такие как преднизолон
- Имеют почечную недостаточность
Как уменьшить побочные эффекты
Нет способа избежать побочные эффекты любого препарата. Но вы и ваш врач можете снизить риск возникновения побочных эффектов от НПВП. Например:
Но вы и ваш врач можете снизить риск возникновения побочных эффектов от НПВП. Например:
- Используйте ацетаминофен вместо НПВП для облегчения боли, которая, по мнению вашего врача, не требует противовоспалительных препаратов.
- Примите наименьшую дозу НПВП, которая вам необходима.
- Принимайте НПВП вместе с пищей.
Если вам не требуется круглосуточное облегчение, избегайте приема одной дозы НПВП в день, особенно если вы старше 60 лет. Эти лекарства дольше остаются в организме и могут вызывать больше побочных эффектов.
Спросите своего врача о приеме второго препарата, такого как блокатор кислоты, который может снизить риск язвы желудка и кровотечения. Некоторые лекарства сочетают в себе НПВП и блокаторы кислоты в одной таблетке.
Если после начала приема НПВП вы испытываете длительную или необычную боль в животе, немедленно сообщите об этом своему врачу.
Как назначают НПВП?
Врачи назначают НПВП в разных дозах в зависимости от вашего состояния.
Дозировки могут варьироваться от одного до четырех раз в день, в зависимости от того, как долго каждый препарат остается в организме. Ваш врач может назначить более высокие дозы НПВП, если у вас, например, ревматоидный артрит (РА), потому что при РА часто наблюдается сильный жар, отек, покраснение и скованность в суставах.
Меньшие дозы могут быть достаточными при остеоартрите и мышечных травмах, так как обычно наблюдается меньший отек и часто нет тепла или покраснения в суставах.
Ни один НПВП не гарантирует эффективность. Ваш врач может назначить несколько типов НПВП, прежде чем найти тот, который лучше всего подходит для вас.
Могу ли я принимать НПВП, если меня лечат от высокого кровяного давления?
НПВП могут повышать артериальное давление у некоторых людей. Некоторым людям с высоким кровяным давлением, возможно, придется прекратить прием НПВП, если их кровяное давление повышается, даже если они регулярно принимают лекарства от кровяного давления.
Кому не следует принимать НПВП?
Попросите вашего врача, прежде чем принимать НПВП, если:
- У вас были серьезные побочные эффекты от приема болеутоляющего или жаропонижающего средства.
- У вас повышен риск желудочного кровотечения.
- У вас проблемы с желудком, в том числе изжога.
- У вас высокое кровяное давление, заболевание сердца, цирроз печени или заболевание почек.
- У вас астма.
- Вы принимаете мочегонное лекарство.
Лекарства от ревматоидного артрита: DMARD, НПВП и др.
Ревматоидный артрит (РА) является одной из наиболее распространенных форм артрита.
РА является воспалительным и аутоиммунным заболеванием. Это происходит, когда ваше тело атакует собственные здоровые ткани суставов. Это приводит к покраснению, воспалению и боли.
Основной целью препаратов против ревматоидного артрита является блокирование воспаления для предотвращения повреждения суставов.
Читайте дальше, чтобы узнать о многих вариантах лечения ревматоидного артрита.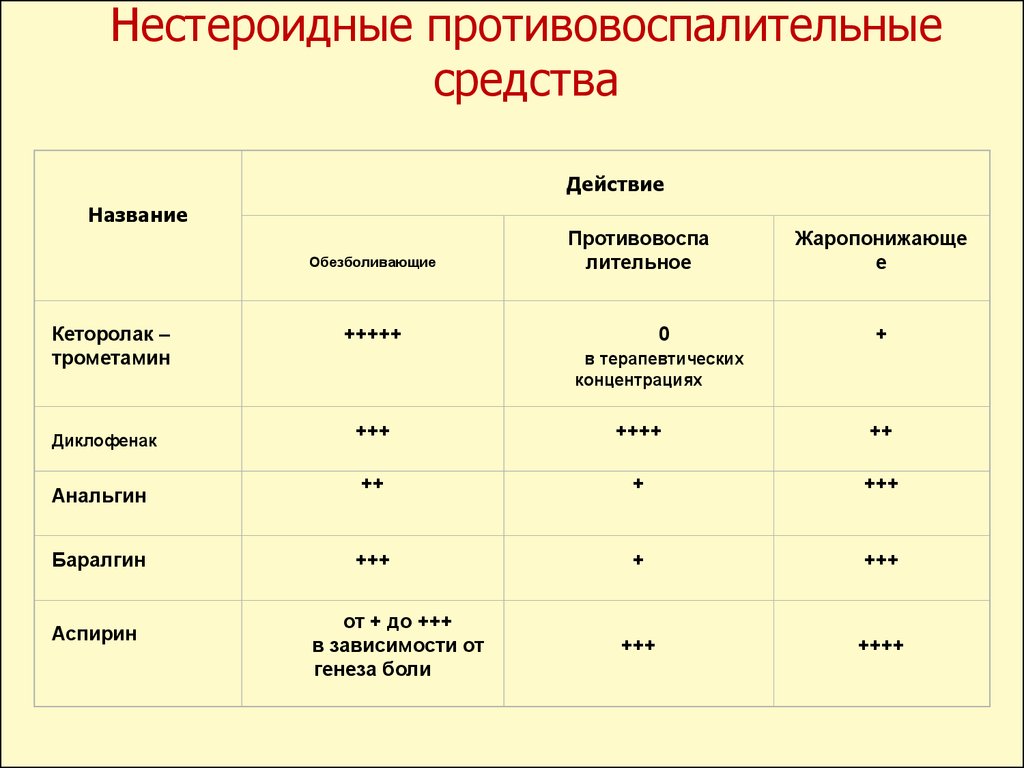
БПВП
Болезнь-модифицирующие противоревматические препараты (БПВП) используются для уменьшения воспаления. В отличие от других лекарств, которые временно облегчают боль и воспаление, DMARD могут замедлить прогрессирование РА. Это означает, что со временем у вас может быть меньше симптомов и меньше повреждений.
Наиболее распространенные DMARDS, используемые для лечения RA, включают в себя:
- Гидроксихлорохин (Plaquenil)
- Лефлуномид (ARAVA)
- Метотрексат (TREXALL)
- SULFASALAZIN Они работают, блокируя специфические воспалительные пути, создаваемые иммунными клетками. Это уменьшает воспаление, вызванное РА. Врачи назначают биологические препараты, когда одних БПВП недостаточно для лечения симптомов РА.
Биопрепараты не рекомендуются людям с ослабленной иммунной системой или инфекцией. Это потому, что они могут повысить риск серьезных инфекций.
The most common biologics include:
- abatacept (Orencia)
- adalimumab (Humira)
- certolizumab pegol (Cimzia)
- etanercept (Enbrel)
- golimumab (Simponi)
- infliximab (Remicade)
- rituximab ( Ритуксан)
- тоцилизумаб (Актемра)
Ваш врач может назначить ингибиторы JAK, если DMARD или биологические препараты также не лечат ревматоидный артрит.
 Эти лекарства влияют на гены и активность иммунных клеток в организме. Они помогают предотвратить воспаление и остановить повреждение суставов и тканей.
Эти лекарства влияют на гены и активность иммунных клеток в организме. Они помогают предотвратить воспаление и остановить повреждение суставов и тканей.Американский колледж ревматологов (ACR) классифицирует ингибиторы JAK как целевые синтетические DMARD.
Ингибиторы JAK включают:
- барицитиниб (Olumiant)
- тофацитиниб (Xeljanz, Xeljanz XR)
- упадацитиниб (Rinvoq)
Перед началом приема ингибитора JAK попросите своего врача убедиться, что вы в курсе всех прививок, включая профилактические прививки от опоясывающего лишая (вакцина против опоясывающего лишая).
Наиболее распространенные побочные эффекты этих препаратов включают:
- инфекции верхних дыхательных путей, такие как синусит или простуда
- заложенность носа
- насморк
- боль в горле
- грипп
- цистит
- инфекция)
Ацетаминофен доступен без рецепта. Он выпускается в виде перорального препарата и ректального суппозитория.

Другие препараты намного эффективнее уменьшают воспаление и лечат боль при РА. Это связано с тем, что ацетаминофен может снимать боль от легкой до умеренной, но не обладает противовоспалительной активностью. Таким образом, это не очень хорошо работает для лечения РА.
Этот препарат может вызвать серьезные проблемы с печенью, включая печеночную недостаточность. Принимайте одновременно только один препарат, содержащий ацетаминофен.
НПВП являются одними из наиболее часто используемых препаратов для лечения ревматоидного артрита. В отличие от других обезболивающих, НПВП более эффективны при лечении симптомов РА. Это потому, что они предотвращают воспаление.
Некоторые люди используют безрецептурные НПВП. Однако более сильные НПВП доступны по рецепту.
Побочные эффекты НПВП включают:
- раздражение желудка
- язвы
- эрозии или жжение в желудке или кишечнике
- желудочное кровотечение
- повреждение почек
В редких случаях эти побочные эффекты могут привести к смерти.
 Если вы принимаете НПВП в течение длительного времени, ваш врач будет контролировать функцию ваших почек. Это особенно вероятно, если у вас уже есть заболевание почек.
Если вы принимаете НПВП в течение длительного времени, ваш врач будет контролировать функцию ваших почек. Это особенно вероятно, если у вас уже есть заболевание почек.Ибупрофен (Адвил, Мотрин IB, Нуприн)
Безрецептурный ибупрофен является наиболее распространенным НПВП. Если это не предписано врачом, не принимайте ибупрофен более нескольких дней подряд. Прием этого препарата слишком долго может вызвать желудочное кровотечение. Этот риск выше у пожилых людей.
Ибупрофен также доступен по рецепту. В рецептурных вариантах дозировка выше. Ибупрофен также можно комбинировать с опиоидами, другим типом обезболивающего. Примеры этих комбинированных препаратов, отпускаемых по рецепту, включают:
- ибупрофен/гидрокодон (викопрофен)
- ибупрофен/оксикодон (комбунокс)
напроксен натрия (алив)
напроксен натрия является безрецептурным НПВП. Его часто используют в качестве альтернативы ибупрофену. Это потому, что он вызывает немного меньше побочных эффектов.
 Варианты рецепта этого препарата предлагают более сильные дозировки.
Варианты рецепта этого препарата предлагают более сильные дозировки.Аспирин (Bayer, Bufferin, St. Joseph)
Аспирин — пероральное обезболивающее. Он используется для лечения легкой боли, лихорадки и воспаления. Его также можно использовать для профилактики сердечного приступа и инсульта.
НПВП, отпускаемые по рецепту
Если безрецептурные НПВП не облегчают симптомы РА, врач может выписать рецептурный НПВП. Это пероральные препараты. Наиболее распространенные варианты включают:
- целекоксиб (целебрекс)
- ибупрофен (рецептурная сила)
- Набуметон (Relafen)
- напроксен (напросин)
- напроксен натрия (Anaprox)
- Piroxicam (Feldene)
Другие NSAID включают:
- Diclofenac (Voltaren, Diclifen, 9009
- , Diclofenac (Voltaren, diclifen.
- индометацин (Indocin)
- кетопрофен (Orudis, Ketoprofen ER, Oruvail, Actron)
- этодолак (Lodine)
- фенопрофен (Nalfon)
- флурбипрофен
- кеторолак0011
- Meclofenamate
- Мефенамовая кислота (Ponstel)
- Meloxicam (Mobic)
- Oxaprozin (DayPro)
- Sulindac (Clinoril)
- Салсалат (Divalcid, Amigesic, Marthritic, Salflex.
 толметин (Tolectin)
толметин (Tolectin)
Диклофенак/мизопростол (Arthrotec)
Это пероральный препарат, сочетающий НПВП диклофенак с мизопростолом. НПВП могут вызывать язву желудка. Этот препарат помогает предотвратить их.
Капсаицин для местного применения (капсин, зострикс, долорак)
Безрецептурный крем с капсаицином для местного применения может облегчить легкую боль, вызванную ревматоидным артритом. Вы втираете этот крем в болезненные участки тела.
Диклофенак натрия гель для местного применения (Вольтарен 1%)
Вольтарен гель 1% является НПВП для местного применения. Это означает, что вы втираете его в кожу. Он одобрен для лечения боли в суставах, в том числе в руках и коленях.
Этот препарат вызывает те же побочные эффекты, что и пероральные НПВП. Однако только около 4 процентов этого препарата всасывается в ваш организм. Это означает, что у вас может быть меньше побочных эффектов.
Диклофенак натрия раствор для местного применения (Pennsaid 2%)
Диклофенак натрия (Pennsaid 2%) и 1,5% растворы для местного применения, используемые при болях в коленях.
 Вы втираете его в колено, чтобы облегчить боль.
Вы втираете его в колено, чтобы облегчить боль.Опиоиды — самые сильные обезболивающие на рынке. Они доступны только по рецепту.
Опиоиды бывают пероральными и инъекционными. Они используются только при тяжелом ревматоидном артрите, вызывающем сильную боль, поскольку опиоиды могут привести к зависимости. Если ваш врач пропишет опиоид, он будет внимательно следить за вами.
Людям с ревматоидным артритом, принимающим опиоиды, также следует использовать другие виды лечения. Это потому, что опиоиды меняют только то, как вы испытываете боль. Они не замедляют течение болезни и не предотвращают воспаление.
Opioids include:
- acetaminophen/codeine
- codeine
- fentanyl
- hydrocodone (Vicodin)
- hydromorphone
- meperidine (Demerol)
- methadone
- morphine
- oxycodone (OxyContin)
- oxymorphone (Opana, Опана ER)
- трамадол (ультрам)
Кортикостероиды также называют стероидами.
 Они бывают пероральными и инъекционными препаратами. Эти препараты могут помочь уменьшить воспаление при РА. Они также могут помочь уменьшить боль и ущерб, вызванный воспалением. Эти препараты не рекомендуются для длительного применения.
Они бывают пероральными и инъекционными препаратами. Эти препараты могут помочь уменьшить воспаление при РА. Они также могут помочь уменьшить боль и ущерб, вызванный воспалением. Эти препараты не рекомендуются для длительного применения.Побочные эффекты могут включать:
- высокий уровень сахара в крови
- язва желудка
- высокое кровяное давление
- эмоциональные побочные эффекты, такие как раздражительность и возбудимость
- Катаракта, или омрачение линзы в вашем глаз
- Остеопороз
Стероиды, используемые для RA, включают:
- Бетаметазон
- Cortisone
- Dexamethasone (Dexpak Taperpak, Decadron, Hexafolis (Hexafrol). Гидрокорт)
- метилпреднизолон (медрол, метакорт, депопред, предакортен)
- преднизолон
- преднизолон (дельтазон, стерапред, жидкий пред)
Эти препараты борются с повреждениями, вызванными аутоиммунными заболеваниями, такими как РА.

 2007, Jun 30; 2: 12.
2007, Jun 30; 2: 12. Pharm. & Pharm. Sci. 2008, 11, 81s–110s.
Pharm. & Pharm. Sci. 2008, 11, 81s–110s. 2009 Sep; 13 (9 B): 3753–3763.
2009 Sep; 13 (9 B): 3753–3763. For the Cross Trial Safety Assessment Group. Cardiovascular risk of celecoxib in 6 randomized placebo-controlled trials: the cross trial safety analysis // Circulation. 2008; 117 (16): 2104–2113.
For the Cross Trial Safety Assessment Group. Cardiovascular risk of celecoxib in 6 randomized placebo-controlled trials: the cross trial safety analysis // Circulation. 2008; 117 (16): 2104–2113. 2008; 28 (6): 788–805.
2008; 28 (6): 788–805.
 2009 Feb; 85 (2): 190–197.
2009 Feb; 85 (2): 190–197. мед. журн. 2013; 32.
мед. журн. 2013; 32.

 Ваш врач может посоветовать вам прекратить прием НПВП перед операцией. Спросите своего врача, прежде чем принимать НПВП, если вы принимаете разжижающие кровь препараты (например, кумадин).
Ваш врач может посоветовать вам прекратить прием НПВП перед операцией. Спросите своего врача, прежде чем принимать НПВП, если вы принимаете разжижающие кровь препараты (например, кумадин). Ваш врач может посоветовать вам прекратить прием НПВП перед операцией. Спросите своего врача, прежде чем принимать НПВП, если вы принимаете разжижающие кровь препараты (например, кумадин).
Ваш врач может посоветовать вам прекратить прием НПВП перед операцией. Спросите своего врача, прежде чем принимать НПВП, если вы принимаете разжижающие кровь препараты (например, кумадин). Эти лекарства влияют на гены и активность иммунных клеток в организме. Они помогают предотвратить воспаление и остановить повреждение суставов и тканей.
Эти лекарства влияют на гены и активность иммунных клеток в организме. Они помогают предотвратить воспаление и остановить повреждение суставов и тканей.
 Если вы принимаете НПВП в течение длительного времени, ваш врач будет контролировать функцию ваших почек. Это особенно вероятно, если у вас уже есть заболевание почек.
Если вы принимаете НПВП в течение длительного времени, ваш врач будет контролировать функцию ваших почек. Это особенно вероятно, если у вас уже есть заболевание почек. Варианты рецепта этого препарата предлагают более сильные дозировки.
Варианты рецепта этого препарата предлагают более сильные дозировки. толметин (Tolectin)
толметин (Tolectin) Вы втираете его в колено, чтобы облегчить боль.
Вы втираете его в колено, чтобы облегчить боль. Они бывают пероральными и инъекционными препаратами. Эти препараты могут помочь уменьшить воспаление при РА. Они также могут помочь уменьшить боль и ущерб, вызванный воспалением. Эти препараты не рекомендуются для длительного применения.
Они бывают пероральными и инъекционными препаратами. Эти препараты могут помочь уменьшить воспаление при РА. Они также могут помочь уменьшить боль и ущерб, вызванный воспалением. Эти препараты не рекомендуются для длительного применения.