Витамин В3 – никотинамид, плазма (Витамин PP, ниацин, Vitamin B3 – Nicotinamide, Niacinamide, plasma)
Метод определения ВЭЖХ-МС (высокоэффективная жидкостная хроматография с масс-селективным детектированием).
Исследуемый материал Плазма крови (ЭДТА)
Синонимы: Никотиновая кислота; Витамин РР; Противопеллагрический фактор; 3-пиридинкарбоновая кислота.
Niacin; Vitamin B3; Nicotinicacid; Vitamin PP; Pyridine-3-carboxylicacid; 3-pyridinecarboxylicacid; Apelagrin; Pellagrin.
Краткая характеристика определяемого вещества Витамин В3 – никотинамид
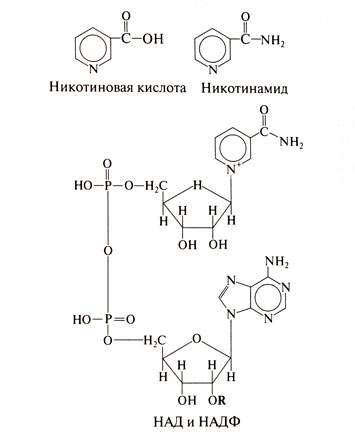
Витамин В3 включает две основные формы – никотинамид и никотиновую кислоту. В ходе метаболических процессов в организме они преобразуются в никотинамидадениндинуклеотид (НАД, nicotinamide adenine dinucleotide – NAD) и никотинамидадениндинуклеотидфосфат (НАДФ, nicotinamide adenine dinucleotide phosphate – NADP) – коферменты множества окислительно-восстановительных реакций, жизненно важных для клеточного метаболизма.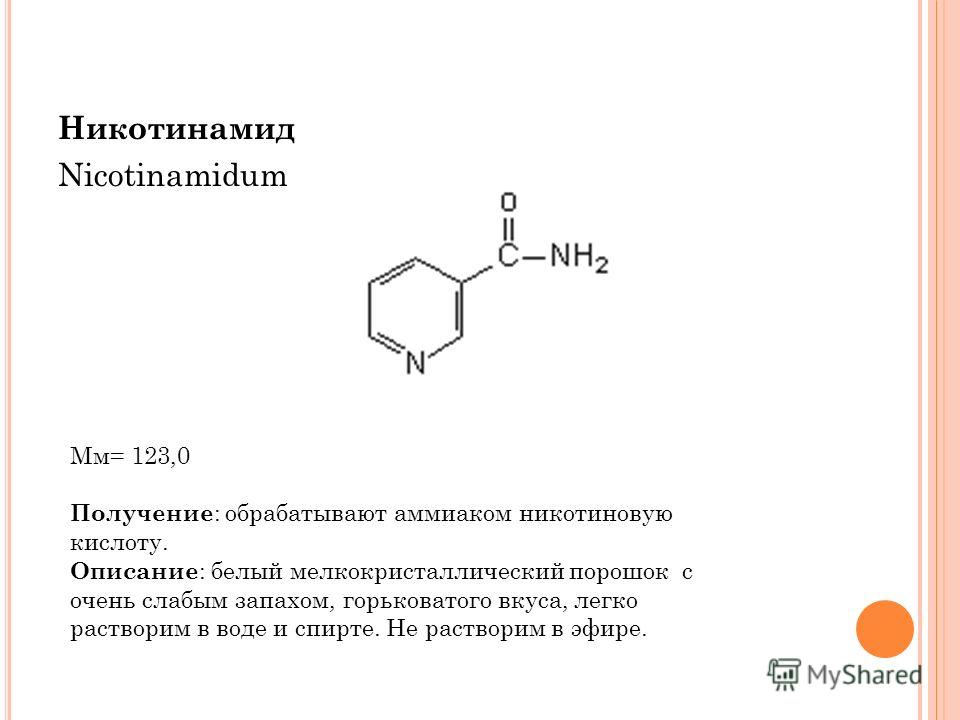
Никотинамид важен для развития и функционирования центральной нервной системы (ЦНС). Считается, что никотинамид играет важную роль в защите нейронов при травматических повреждениях, ишемии и инсульте и может быть вовлечен в патогенез трех наиболее распространенных нейродегенеративных состояний: болезней Альцгеймера, Паркинсона и Гентингтона. Ключевым фактором при этом является биодоступность никотинамида, низкая концентрация которого может привести к неврологическому дефициту и деменции, а высокая – к потенциальной нейротоксичности. Дефицит В3 в его классической форме проявляется пеллагрой, и одно из распространенных названий этого витамина «PP» происходит от pellagra prevention – предотвращающий пеллагру. Клинические проявления этой болезни включают дерматит билатеральный симметричный на участках кожи, доступных воздействию солнечного света; обширное воспаление слизистых оболочек, проявляющееся диареей, ахлоргидрией, глосситом, стоматитом, вагинитом; психические проявления, включающие усталость, бессонницу, апатию, в тяжелых случаях – энцефалопатию с дезориентацией, галлюцинациями, потерей памяти, психозами и деменцией.
Основные пищевые источники витамина В3 – продукты, содержащие дрожжи, нежирное мясо, печень, мясо птицы. Меньшее количество этого витамина (однако достаточное, чтобы избежать дефицита) содержится в молоке, различных зеленых листовых овощах, консервированном лососе. В некоторых растительных продуктах, особенно в злаковых (кукуруза, пшеница), ниацин связан с пептидами и сахарами и менее доступен для усвоения. До двух третей необходимого количества витамина В3 у взрослых может образовываться в самом организме путем метаболизма триптофана.
Пищевой дефицит В3 связан с нехваткой белковой пищи и в развитых странах наблюдается редко, он чаще может возникнуть при преобладании в рационе кукурузы (маиса), бедной по содержанию как ниацина, так и триптофана. Пеллагра иногда может быть вторичным проявлением карциноидного синдрома, при котором до 60% триптофана катаболизируется в 5-ОН-триптофан и серотонин; и болезни Хартнупа – генетического нарушения, сопровождаемого нарушением всасывания аминокислот, включая триптофан.
К недостатку витамина может приводить алкоголизм, действие некоторых лекарственных препаратов. Осложняющим фактором может служить дефицит витаминов В2, В6 и железа, которые участвуют в процессах конверсии триптофана в ниацин.
С какой целью определяют уровень витамина В3 в крови
Тест используют для оценки статуса витамина В3 в организме.
Препараты витамина В3 используют в медицинской практике, в том числе никотинамид, в лечении пеллагры, карциноидного синдрома, болезни Хартнупа, никотиновую кислоту – в гиполипидемической терапии, используя спектр ее воздействий на липидный обмен. Хотя прием витамина В3 в его естественном виде с пищевыми продуктами не ассоциирован с какими-либо токсическими эффектами, однако фармакологические дозы никотиновой кислоты могут иметь побочное действие. Чаще оно проявляется покраснением и чувством покалывания лица, рук, груди. Другие возможные побочные эффекты применения высоких доз никотиновой кислоты – зуд, гастрит, иногда гепатотоксичность, ухудшение углеводного обмена, повышение уровня мочевой кислоты, что ограничивает применение этого препарата.
Литература
Основная литература:
- Литвицкий П.Ф. Нарушения обмена витаминов. Вопросы современной педиатрии. 2014;13(4):40-47.
- Клиническое руководство Тица по лабораторным тестам. 4-е изд. (ред. Алан Г.Б. Ву). — М.: Изд. «Лабора». 2013:1279.
- Fricker R.A., Green E.L., Jenkins S.I., Griffin S.M. The Influence of Nicotinamide on Health and Disease in the Central Nervous System. International Journal of Tryptophan Research. 2018;11:1178646918776658. doi: 10.1177/1178646918776658. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5966847/
- Johnson L.E. Niacin (Nicotinic Acid). In: MSD Manual Professional Version. www.msdmanuals.com
- Tietz Textbook of Clinical Chemictry and Molecular Diagnostics (Ed. Burtis C.A., Ashwood E.R., Bruns D.E.), 5th ed., Elseivier. 2012:2238.
Публикации в СМИ
Витамин PP (витамин B3, ниацин, никотиновая кислота, никотинамид) — водорастворимый витамин, содержащийся в мясных и рыбных продуктах. Найден в большинстве продуктов, содержащих витамин В1. При выраженной недостаточности в пище развивается пеллагра. Эндемична для некоторых районов Африки и Азии, спорадически встречают повсеместно.
Найден в большинстве продуктов, содержащих витамин В1. При выраженной недостаточности в пище развивается пеллагра. Эндемична для некоторых районов Африки и Азии, спорадически встречают повсеместно.
Источники витамина — мясо, печень, почки, молоко, рыба, дрожжи, овощи, фрукты, гречневая крупа.
Физиологическая роль. Амид никотиновой кислоты — простетическая группа, входящая в состав НАД и НАДФ. НАД и НАДФ — акцепторы водорода и электронов, участвуют в окислительно-восстановительных процессах, т.е. принимают участие в клеточном дыхании.
Суточная потребность • Для взрослых — 18–24 мг • Для детей •• 6 мес–1 год — 6 мг •• 1–1,5 года — 9 мг •• 1,5–2 года — 10 мг •• 3–4 года — 12 мг •• 5–6 лет — 13 мг •• 7–10 лет — 15 мг •• 11–13 лет — 19 мг.
НЕДОСТАТОЧНОСТЬ ВИТАМИНА РР
Причины • Первичная — недостаток в поступающей пище, например, при преобладании в рационе кукурузы, поскольку витамин РР, хотя и содержится в ней, находится в связанном состоянии и не ассимилируется в ЖКТ.
Клиническая картина. При недостаточности витамина РР возникают нарушения функций кожи, слизистых оболочек, ЖКТ и ЦНС. Характерно наличие трёх Д (дерматит, диарея, деменция) и поражение слизистых оболочек.
• Стадия прегиповитаминоза — неспецифические нарушения (слабость, утомляемость, снижение аппетита и т.д.).
• Стадии гипо- и авитаминоза •• Дерматит. Поражение кожи может быть четырёх типов. Чаще всего оно симметрично и возникает на участках кожи, подвергающихся солнечному облучению или травматизации (давлению) ••• Остро возникают кожные проявления в виде пеллагрической эритемы с последующим образованием пузырьков, пузырей, корочек.


Диагноз • Выделение N’-метилникотинамида с мочой менее 4 мг/сут • Снижение содержания никотиновой кислоты • Снижается содержание в крови и моче других витаминов группы В.
Дифференциальная диагностика — другие причины стоматитов, глосситов, диареи, деменции. При появлении признаков нарушений ЦНС необходимо дифференцировать от такового при недостаточности витамина В1.
Лечение • В среднетяжёлых и тяжёлых случаях необходима госпитализация • Диета. Включение в рацион продуктов, богатых витамином РР (мясо, яйца) и триптофаном (молоко) • Назначение никотиновой кислоты (или никотинамида) от 300 до 1000 мг/сут внутрь в начале лечения при выраженном снижении содержания витамина РР в плазме крови, затем по 300–500 мг • При заболеваниях ЖКТ никотиновую кислоту (или никотинамид) вводят парентерально (50–100 мг в/м 2–5 раз/сут или 25–100 мг в/в) • Одновременно назначают по 5 мг тиамина, рибофлавина и пиридоксина • Следует соблюдать осторожность при применении никотиновой кислоты при сопутствующей глаукоме (возможно обострение), подагре (большие дозы вызывают гиперурикемию), патологии печени (большие дозы могут оказать гепатотоксическое действие), артериальной гипотензии (в связи с сосудорасширяющим действием препарата), пептической язве (возможно обострение) • Для уменьшения побочных эффектов никотиновой кислоты (покраснение лица и верхней половины туловища, головокружение, сыпь) рекомендовано начать лечение с низких доз препарата с постепенным их повышением, и/или принимать никотиновую кислоту внутрь после еды или запивать молоком. Толерантность к сосудорасширяющему действию никотиновой кислоты обычно развивается в течение первых 2 недель • Никотинамид в отличие от никотиновой кислоты не оказывает сосудорасширяющего действия.
Толерантность к сосудорасширяющему действию никотиновой кислоты обычно развивается в течение первых 2 недель • Никотинамид в отличие от никотиновой кислоты не оказывает сосудорасширяющего действия.
Течение обычно прогрессирующее.
Профилактика • Питание с достаточным содержанием в пищевом рационе продуктов, богатых никотиновой кислотой • При эндогенной форме — своевременная диагностика и лечение заболеваний, нарушающих всасывание и усвоение витамина РР, профилактическое введение препаратов никотиновой кислоты; дополнительное введение витамина РР лицам с увеличенной в нём потребностью.
Синонимы • Болезнь астурийская розовая • Болезнь розовая • Пеллагра • Пеллагра ломбардская • Cкорбут альпийский
МКБ-10 • E52 Недостаточность никотиновой кислоты [пеллагра]
НИКОТИНАМИД, ВИТАМИНЫ В3, РР, К3
Название по ИЮПАК: pyridine-3-carboxamide
Другие названия:
nicotinamide,
3-pyridinecarboxamidem,
niacinamide,
nicotinic acid amide,
vitamin PP;
Pyridine-3-carboxamide;
niacinamide cell culture tested;
3-Pyridinecarboxyamide;
Vitamin B3
Регистрационный номер CAS: 98-92-0
Химическая формула: C6H6N2O
Молярная масса: 122. 12 г/моль
12 г/моль
Температура плавления: 128-131 ℃
Белый кристаллический витамин PP – есть амид никотиновой кислоты. Витамин группы В – никотинамид. Ниоатиномид — водорастворимый витаминный комплекс.
Ниоатинамид — это никотиновая кислота, её также называют ниацин, преобразованная в живом организме. Ниацин и никотинамид имеют как общие характеристики, так и различные.
- Оба заключают в себе равные функции витамина.
- Никотинамид не включает в себя фармакологические и токсические следствия ниацина.
При использовании ниоатиномида можете н переживать за покраснения и за свой степень холестерина.
- Снижает уровень холестерина
- Не вызывает покраснения
Хоть и ниоатиновая кислота и никотинамид очень похожи, ниацин, в клетках, преобразуется в:
- никотинамидадениндинуклеотид
- никотинамидадениндинуклеотид
- никотинамидадениндинуклеотидфосфат
NAD+ и NADP+ действуют соединениями для большого количества энзимных окислительно-восстановительных реакций.
Никотинамид – атрибуты:
- Противовоспалительное свойство
- Блокирования воспаления иодидов. Иоиды — участвуют в проявлении угрей.
- Успокаивает
-
Имеет действие химио- и радио-сенсибилизирующего средства, а значит:
- Улучшает качество потока крови опухоли
- Сбавляет гипоксию опухоли
- Совместно с витамином С применяется для исцеления от рака
Витамин В3, РР, К3 почти не имеет побочных действий, а если всё же они проявляются, то в редких случаях. Никотинамид является одним из наиболее щадящий компонентов в косметологии и лекарствах, так же является пищевой добавкой.
Никотинамид имеет свойство результативно отбеливать кожу, при местном применении.
Наша компания обеспечивает доставку:
- Витамин PP
- Никотинамид — стандарта USP32
- Никотинамид – стандарта USP34
- Технический никотинамид
- Кормовой никотинамид
- Пищевой никотиномид
- Фармацевтический никотиномид
Использование никотинамида при лечении инсулинзависимого сахарного диабета в дебюте заболевания | Горелышева
В последние годы стало очевидным, что ведущую роль в развитии инсулинзависимого сахарного диабета (ИЗСД) играют аутоиммунные механизмы. По современным представлениям ИЗСД является классическим органоспецифическим аутоиммунным заболеванием, при котором р-клет- ки разрушаются с участием механизмов, опосредованных Т-лимфоцитами и циркулирующими аутоантителами. Однако имеются экспериментальные доказательства, что первичным механизмом повреждения р-клетки является действие цитокинов. Таким образом, разрушение р-клеток происходит в две фазы: первая — независимая от лимфоцитов, начальная, вторая — опосредованная действием Т-лимфоцитов.
По современным представлениям ИЗСД является классическим органоспецифическим аутоиммунным заболеванием, при котором р-клет- ки разрушаются с участием механизмов, опосредованных Т-лимфоцитами и циркулирующими аутоантителами. Однако имеются экспериментальные доказательства, что первичным механизмом повреждения р-клетки является действие цитокинов. Таким образом, разрушение р-клеток происходит в две фазы: первая — независимая от лимфоцитов, начальная, вторая — опосредованная действием Т-лимфоцитов.
Согласно Копенгагенской модели патогенеза ИЗСД {38], факторы внешней и внутренней среды (вирусы, химические вещества, пищевые факторы, интерлейкин-1) вызывают активацию процесса свободнорадикального окисления в р-клетках. Под воздействием свободных радикалов (О2 , NO) белки р-клетки меняют свои природные свойства («денатурируют») и становятся антигенами для собственной иммунной системы. Повышенная чувствительность р-клетки к действию свободных радикалов обусловлена тем, что в ней снижена активность антиоксидантных защитных систем- (супероксиддисмутазы, глутатионпероксидазы, каталазы). —) и окись азота (NO) вызывают нарушения в структуре ДНК инсулинпродуцирующих клеток, стимулируют патологическую активацию по- ли(АДф-рибоз)синтетазы, ответственной за репликацию ДНК, что приводит к повышению утилизации НАД+ с последующим истощением его запасов в клетке: это является причиной снижения синтеза протеинов, включая проинсулин, и последующей гибели р-клетки.
—) и окись азота (NO) вызывают нарушения в структуре ДНК инсулинпродуцирующих клеток, стимулируют патологическую активацию по- ли(АДф-рибоз)синтетазы, ответственной за репликацию ДНК, что приводит к повышению утилизации НАД+ с последующим истощением его запасов в клетке: это является причиной снижения синтеза протеинов, включая проинсулин, и последующей гибели р-клетки.
Среди возможных средств фармакологической регуляции свободнорадикальных процессов в организме могут быть использованы различные вещества, в частности витамины (сс-токоферола ацетат, никотинамид, аскорбиновая кислота) и др.
Одним из наиболее интересных и перспективных препаратов, которые могут быть применены не только для лечения ИЗСД, но и для его профилактики, является никотинамид. В 1947 г. A. Lazarow [32] первым сообщил о том, что введение крысам никотинамида предотвращает развитие аллоксанового диабета. Дальнейшее изучение препарата стало возможным после разработки экспериментальных моделей ИЗСД [43].
Никотинамид (амид никотиновой кислоты) по строению и действию близок к никотиновой кислоте и рассматривается как витамин РР. Суточная потребность в никотинамиде составляет около 20 мг. Фармакокинетика препарата в настоящее время изучается. Известно, что период полувыведения составляет 9 ч. Никотинамид накапливается преимущественно в печени и эритроцитах [45].
Имеется много экспериментальных данных, подтверждающих, что никотинамид в отличие от никотиновой кислоты замедляет или приостанавливает развитие диабета у NOD-мышей [20, 37], а также развитие инсулита под действием малых доз стрептозотоцина [51].
Установлено также, что никотинамид подавляет отторжение пересаженных р-клеток у NOD- мышей [39] и благоприятствует регенерации островковых клеток у крыс с частичной панкреатэк- томией [27, 61].
Одним из механизмов действия никотинамида является ингибирование патологической активности полиаденозиндифосфатрибозсинтетазы, следующей за поражением ДНК р-клеток свободными радикалами кислорода [40, 51].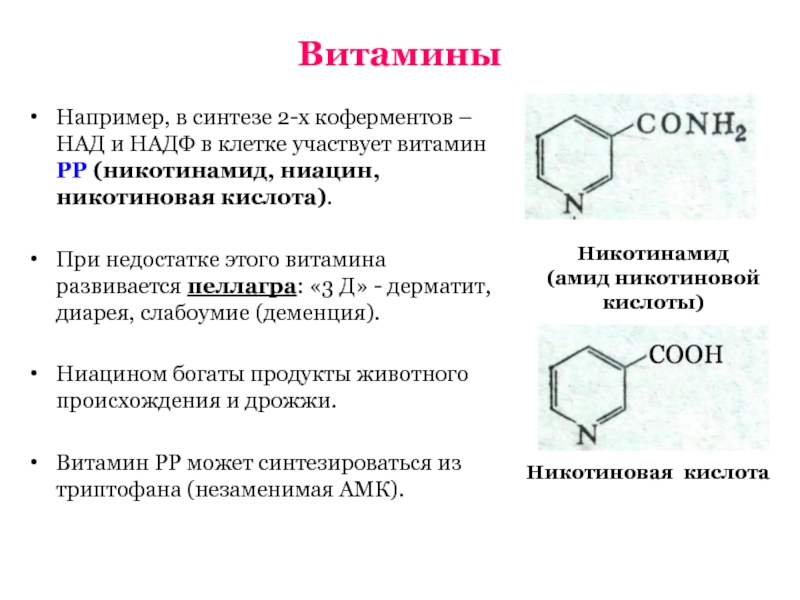 Такое подавление позволяет избежать уменьшение содержания НАД+ в р-клетке, что благоприятно влияет на синтез проинсулина. Доказано, что никотинамид также ингибирует (in vitro) активированные макрофаги, выделяющие огромное количество свободных радикалов, повреждающих р-клетки [29, 31, 36]. Экспериментально установлено, что преинкубация с никотинамидом защищает ДНК и митохондрии р-клеток от повреждения свободными радикалами [15, 30].
Такое подавление позволяет избежать уменьшение содержания НАД+ в р-клетке, что благоприятно влияет на синтез проинсулина. Доказано, что никотинамид также ингибирует (in vitro) активированные макрофаги, выделяющие огромное количество свободных радикалов, повреждающих р-клетки [29, 31, 36]. Экспериментально установлено, что преинкубация с никотинамидом защищает ДНК и митохондрии р-клеток от повреждения свободными радикалами [15, 30].
Высокие дозы никотинамида не оказывают токсического действия на островковые клетки. Напротив, никотинамид способствует сохранению структуры клетки, стимулирует синтез инсулина и является сильным ингибитором роста соединительной ткани [55].
Недавно были получены данные о том, что никотинамид способен блокировать nitric oxide (NO)-синтетазу, препятствуя таким образом накоплению токсичных NO-радикалов — важного элемента аутоиммунного поражения р-клеток [13, 17, 28].
Исследования ряда авторов [1, 2, 4] подтверждают, что способность никотинамида тормозить окисление липидов в микросомах обусловлена взаимодействием его с цитохромом Р-450. Однако связывание цитохрома Р-450 с никотинамидом, по-видимому, не является единственным механизмом его антиокислительного действия. Никотинамид в концентрациях 50 и 100 мМ способен значительно подавлять хемилюминесценцию не только в микросомальной фракции, но и в плазме крови. На основании этих данных можно предположить, что одним из механизмов антиоксидантного действия никотинамида является его способность непосредственно взаимодействовать с гидроперекисями липидов с образованием в этих реакциях N-оксида никотинамида [1]. Имеются сообщения о том, что никотинамид служит блокатором гидроксильных радикалов (ОН—) [24, 33, 59].
Однако связывание цитохрома Р-450 с никотинамидом, по-видимому, не является единственным механизмом его антиокислительного действия. Никотинамид в концентрациях 50 и 100 мМ способен значительно подавлять хемилюминесценцию не только в микросомальной фракции, но и в плазме крови. На основании этих данных можно предположить, что одним из механизмов антиоксидантного действия никотинамида является его способность непосредственно взаимодействовать с гидроперекисями липидов с образованием в этих реакциях N-оксида никотинамида [1]. Имеются сообщения о том, что никотинамид служит блокатором гидроксильных радикалов (ОН—) [24, 33, 59].
Таким образом, никотинамид, тормозя аутоиммунные процессы и снижая активность перекисного окисления липидов, оказывает защитное действие на р-клетки, воздействуя тем самым на два направления патогенетической цепи в развитии заболевания.
Помимо указанных свойств, никотинамид является одним из активных ингибиторов липаз и фосфолипаз [8]. Он предотвращает рост концентрации свободных жирных кислот и тем самым их повреждающее действие на клеточные мембраны.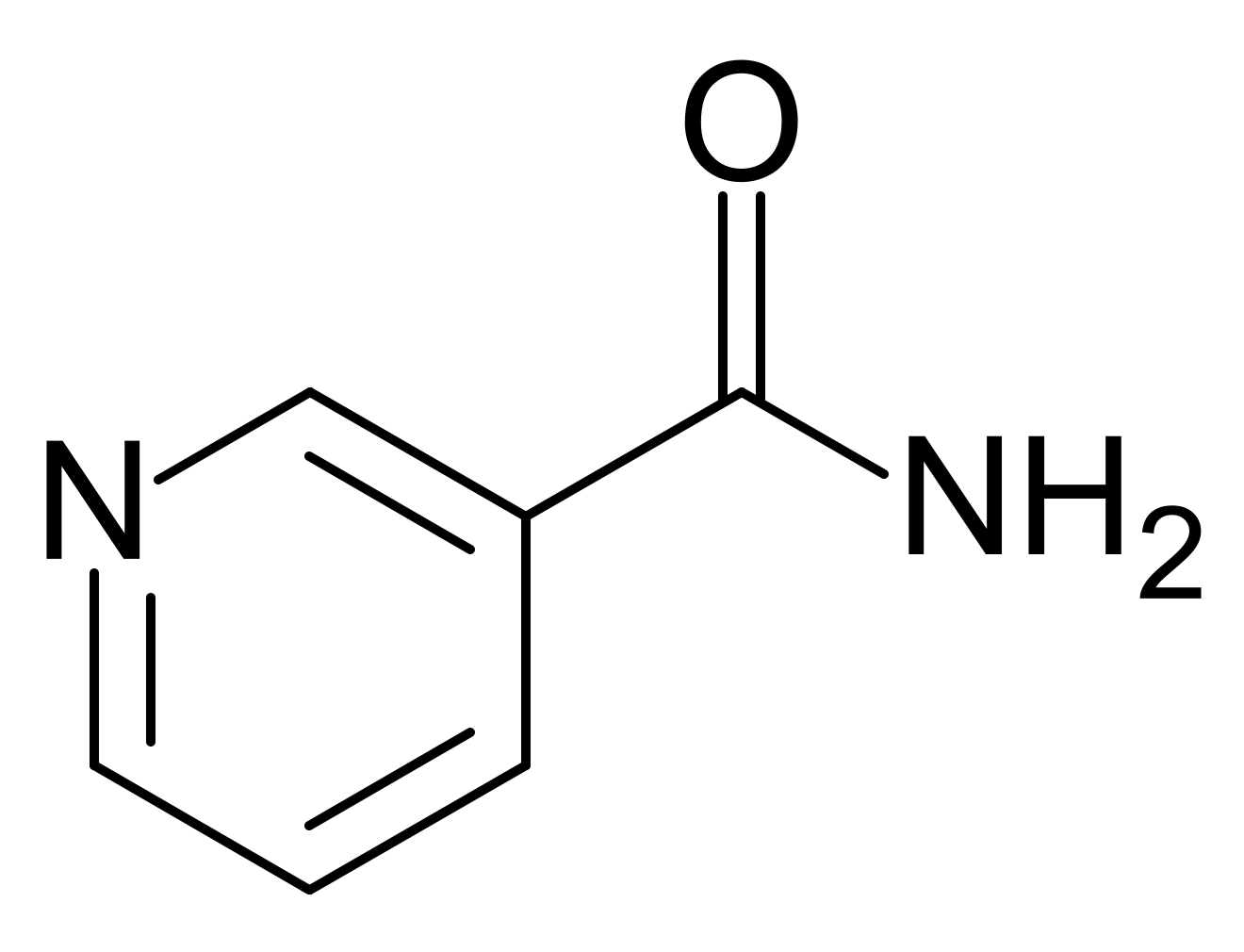 Препарат способствует нормализации внутриклеточной регуляции углеводного обмена [9]. Составными частями гипогликемизирующего действия никотинамида являются ингибирование ключевых ферментов глюконеогенеза в печени крыс, что определяется повышением окислительных свойств NAD-nap цитоплазмы гепатоцитов; повышение чувствительности инсулиновых рецепторов; интенсификация процессов окисления глюкозы в инсулиннечувствительных тканях; усиление биосинтеза и секреции инсулина в неповрежденных р-клетках; участие в гормонально-постре- цепторных взаимодействиях. Никотинамид относят также к группе «антисорбитоловых» препаратов. Никотинамид повышает содержание окисленных форм (НАД и НАДФ) при практически неизмененном уровне восстановленных форм. Он вызывает сдвиг окислительно-восстановительного состояния никотинамидных коферментов в сторону возрастания окислительных свойств, что обусловливает угнетение образования сорбитола в альдозо-редуктазной реакции и активации его окисления в сорбитол-дегидрогеназной реакции.
Препарат способствует нормализации внутриклеточной регуляции углеводного обмена [9]. Составными частями гипогликемизирующего действия никотинамида являются ингибирование ключевых ферментов глюконеогенеза в печени крыс, что определяется повышением окислительных свойств NAD-nap цитоплазмы гепатоцитов; повышение чувствительности инсулиновых рецепторов; интенсификация процессов окисления глюкозы в инсулиннечувствительных тканях; усиление биосинтеза и секреции инсулина в неповрежденных р-клетках; участие в гормонально-постре- цепторных взаимодействиях. Никотинамид относят также к группе «антисорбитоловых» препаратов. Никотинамид повышает содержание окисленных форм (НАД и НАДФ) при практически неизмененном уровне восстановленных форм. Он вызывает сдвиг окислительно-восстановительного состояния никотинамидных коферментов в сторону возрастания окислительных свойств, что обусловливает угнетение образования сорбитола в альдозо-редуктазной реакции и активации его окисления в сорбитол-дегидрогеназной реакции.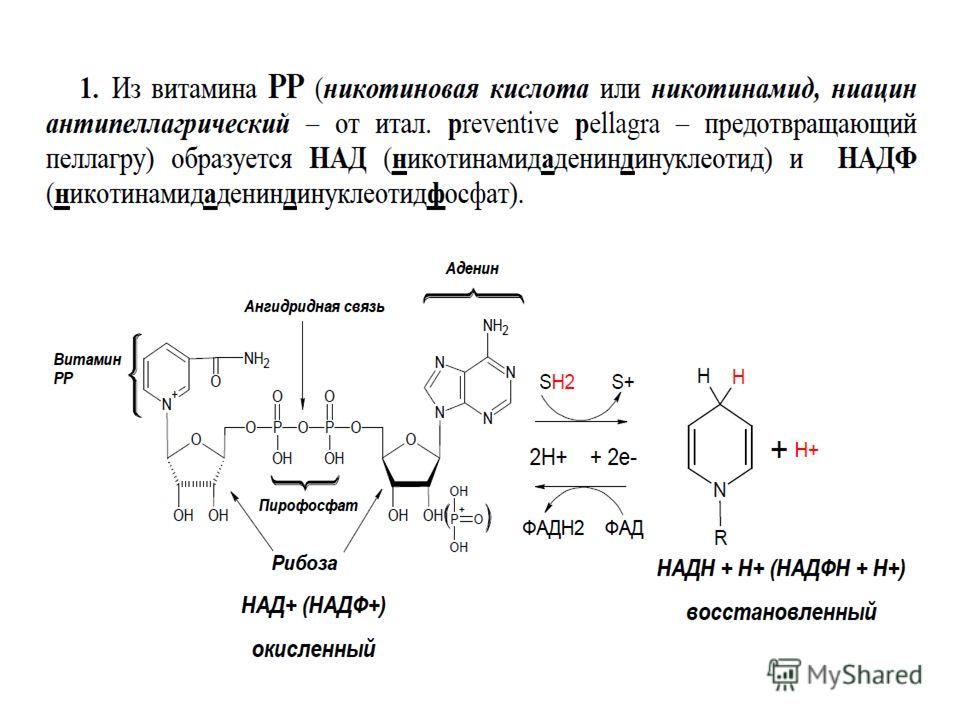 Это в конечном счете приводит к снижению содержания сорбитола [3, 10].
Это в конечном счете приводит к снижению содержания сорбитола [3, 10].
Таким образом, в настоящее время описано несколько механизмов действия никотинамида: уменьшение токсичного действия свободных радикалов кислорода [33, 59], улучшение секреции инсулина путем повышения содержания NAD+ в клетке. Никотинамид также способствует регенерации [3-клетки [42], предотвращает токсическое влияние NO на островковые клетки [28], а также снижает тормозящее влияние интерлейкина-lb на выделение инсулина р-клетками [16, 45]. Никотиновая кислота подобного действия не оказывает.
Никотинамид дает выраженный лечебный эффект при сахарном диабете. Опыт его использования у больных диабетом с ангиопатиями показал хорошие результаты [7].
Вместе с тем нам практически не встретилось отечественных работ, посвященных изучению действия никотинамида у больных с впервые выявленным ИЗСД, тогда как в современной зарубежной литературе этому вопросу уделяется большое внимание. Работы проводятся для изучения защитного действия никотинамида с целью сохранения секреторной способности р-клеток [18, 23, 35, 43, 45, 52, 53].
Хотя в экспериментальных работах давно была установлена способность никотинамида предотвращать разрушение р-клеток [32], клиническое его применение при сахарном диабете начато в середине 80-х годов. Одними из первых были опубликованы данные [52, 54] о том, что высокие дозы никотинамида (3 г в сутки) способствуют повышению частоты клинической ремиссии у больных с впервые выявленым ИЗСД, при этом отмечается значительное снижение суточной потребности в инсулине и достоверное увеличение секреции инсулина.
Спонтанное увеличение инсулиновой секреции, оцененное по уровню С-пептида, наблюдается у больных с впервые выявленным ИЗСД в начале лечения экзогенным инсулином [54], и это затрудняет оценку терапевтического эффекта никотинамида. Однако через 6 мес после клинического начала заболевания обычно отмечается неуклонное снижение секреции инсулина [50].
Р. Vague и соавт. применяли высокие дозы никотинамида у больных ИЗСД по истечении 2-лет- него периода болезни тогда, когда период ремиссии закончился [59].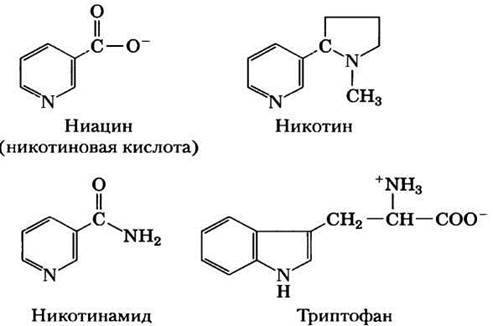 Было отмечено, что и в этом случае уровень HbAlc был значительно ниже, а уровень базального и стимулированного С- пептида — существенно выше в группе больных, получавших 3 г никотинамида в сутки, по сравнению с группой контроля.
Было отмечено, что и в этом случае уровень HbAlc был значительно ниже, а уровень базального и стимулированного С- пептида — существенно выше в группе больных, получавших 3 г никотинамида в сутки, по сравнению с группой контроля.
Диапазон доз никотинамида, применяемых в лечебных целях при ИЗСД, довольно широк и колеблется от 200 мг/сут [46] до 3 г/сут [53]. Сообщается об эффективности других доз никотинамида: 1 г/сут [18], 1,5 г/сут [35]. Результаты, полученные исследователями, неоднозначны.
Большинство авторов отмечают значительное улучшение метаболического контроля, снижение потребности в инсулине, повышение уровней базального и стимулированного С-пептида, увеличение частоты ремиссии. Однако после отмены никотинамида все эти показатели значительно ухудшаются [5, 35, 46, 52, 53].
В то же время Н. Chase и соавт. [18] не обнаружили существенных различий в уровнях базального и стимулированного С-пептида, суточной потребности в инсулине, уровне HbAlc между пациентами, получавшими никотинамид, и контрольной группой. Аналогичные данные приводят Н. Ilkova и соавт. [26].
Аналогичные данные приводят Н. Ilkova и соавт. [26].
Отсутствие эффекта от применения никотинамида могло зависеть от нескольких факторов: возраста больных, остроты начала заболевания, поскольку известно, что в более молодом возрасте уменьшение массы функционирующих р-клеток происходит более быстро, достигая к концу первого года заболевания критических значений [41]. В этих случаях не приходится рассчитывать на успех [50, 58].
Эти данные были подтверждены в одной из последних работ группы исследователей под руководством Р. Pozzilli [45]. Авторами показано, что никотинамид может сохранить и улучшить функцию р-клеток у больных с началом заболевания в постпубертатном периоде (старше 15 лет). Несмотря на то что дозы никотинамида, применяемые для лечения больных с впервые выявленным ИЗСД, в 100—150 раз превышают суточную потребность в нем здорового человека, существенных побочных эффектов при его использовании не отмечено [42, 53].
С тех пор как никотинамид и никотиновая кислота были использованы для лечения шизофрении, литература по психиатрии является хорошим источником информации, касающейся побочного действия этих препаратов. Диапазон применяемых при этом доз был весьма широк и колебался от 3 до 12 г в сутки. Токсическое поражение печени встречалось крайне редко — описан только один случай из 6000 наблюдений [25]. Таким образом, по данным литературы, прием никотинамида в дозе 3 г в сутки относительно безопасен, хотя целесообразен регулярный контроль функции печени.
Диапазон применяемых при этом доз был весьма широк и колебался от 3 до 12 г в сутки. Токсическое поражение печени встречалось крайне редко — описан только один случай из 6000 наблюдений [25]. Таким образом, по данным литературы, прием никотинамида в дозе 3 г в сутки относительно безопасен, хотя целесообразен регулярный контроль функции печени.
Обсуждается вопрос о возможном канцерогенном действии никотинамида. Т. Yamagami и соавт. [60] показали, что никотинамид вместе с аллоксаном и стрептозотоцином оказывает канцерогенное действие у крыс. Однако впоследствии не сообщалось данных в отношении онкогенного действия никотинамида у животных [40]. Более того, исследования S. Le Doux [33], проведенные в культуре клеток инсулиномы крыс, показали, что прямые повреждения цепи ДНК в аллоксановой модели диабета уменьшались в присутствии никотинамида. Поэтому нет никаких веских аргументов, запрещающих применение никотинамида у больных ИЗСД [42, 53].
В настоящее время имеется два основных направления в исследовании свойств никотинамида. Первое — изучение эффективности никотинамида в доклинической стадии развития сахарного диабета у взрослых и детей [21, 22]. В стадии иммунологических нарушений, когда р-клетки еще не истощились и способны производить большое количество инсулина, никотинамид может быть особо эффективен [31, 34, 42]. Рекомендуется назначать никотинамид родственникам больных сахарным диабетом первой степени родства при выявлении у них высоких титров антител к р-клетке (ICA) — более 20 JDF units. Вместе с тем при уровне ICA 80 и более JDF препарат менее эффективен.
Первое — изучение эффективности никотинамида в доклинической стадии развития сахарного диабета у взрослых и детей [21, 22]. В стадии иммунологических нарушений, когда р-клетки еще не истощились и способны производить большое количество инсулина, никотинамид может быть особо эффективен [31, 34, 42]. Рекомендуется назначать никотинамид родственникам больных сахарным диабетом первой степени родства при выявлении у них высоких титров антител к р-клетке (ICA) — более 20 JDF units. Вместе с тем при уровне ICA 80 и более JDF препарат менее эффективен.
Второе направление — исследование эффективности никотинамида у больных с впервые выявленным ИЗСД в стадии клинической манифестации.
а) Необходимо определить достаточные и эффективные дозы, обеспечивающие наступление клинической ремиссии, сохранение остаточной инсулиновой секреции и улучшение метаболического контроля.
б) Следует изучить возможность сочетания с другими препаратами, в частности с иммуномодуляторами. В схемы лечения могут быть включены интенсифицированная инсулинотерапия [14, 48], низкие дозы циклоспорина А [56], глюкокортикоиды [57], ингибиторы свободных радикалов [44, 47], поскольку все эти препараты влияют на различные стадии инсулита.
Никотинамид и его сочетание с ос-токоферола ацетатом были нами применены в комплексной терапии больных с впервые выявленным ИЗСД [5, 6, 11, 12, 19, 49]. В группу обследованных был включен 61 пациент (33 женщины и 28 мужчин) в возрасте от 17 до 30 лет (21,4 ± 6,3 года). Длительность заболевания колебалась от 1 до 10 мес. Все больные исходно были в состоянии декомпенсации (HbAlc 10,9 ± 1,72%). Интеркуррент- ные заболевания и сосудистые осложнения отсутствовали. Все пациенты получали лечение диетой и инсулином (инсулин средней продолжительности действия дважды в день и короткого действия перед каждым приемом пищи).
Все больные были разделены на 4 группы методом случайной выборки.
В 1-й группе (п = 12), помимо традиционной инсулинотерапии, больным назначали ос-токоферола ацетат в дозе 10 мг на 1 кг массы тела в сутки (600—800 мг/сут) в течение 6 мес.
Во 2-й группе (и = И) больные получали никотинамид в дозе 20 мг на 1 кг массы тела в сутки (1600—1800 мг/сут) в течение того же периода.
В 3-й группе (п = 12) проведено лечение сочетанием вышеуказанных препаратов в тех же дозах.
В четвертой группе (п ■= 26) больные получали только инсулинотерапию. (В дальнейшем 8 человек были исключены в связи с отказом от обследования).
Об эффективности проводимого лечения судили по степени компенсации углеводного обмена (HbAlc), уровням базального и стимулированного пищевой нагрузкой С-пептида, суточной потребности в инсулине (доза инсулина на 1 кг массы тела), частоте развития клинической ремиссии.
Проведена оценка функциональной активности мононуклеарных клеток по способности секретировать интерлейкин-1 и содержанию этого цитокина в сыворотке крови.
При применении различных схем лечения нами были получены следующие результаты: отмечено достоверное повышение уровня стимулированного С-пептида в группах больных, получавших никотинамид и его сочетания с ос-токоферола ацетатом. После отмены антиоксидантов к концу первого года наблюдения достаточные уровни стимулированного С-пептида сохранялись в этих же группах. В группе больных, получавших монотерапию инсулином, отмечено неуклонное снижение уровня С-пептида.
В группе больных, получавших монотерапию инсулином, отмечено неуклонное снижение уровня С-пептида.
Лучшие показатели компенсации по уровню гликированного гемоглобина наблюдались в группах больных, получавших никотинамид и его сочетание с ос-токоферола ацетатом, но только в группе пациентов, получавших сочетание антиоксидантов, этот показатель приблизился к норме. После отмены антиоксидантов во всех группах отмечено ухудшение показателей компенсации.
Содержание интерлейкина-1 в сыворотке крови снизилось во всех группах обследованных, но максимально приблизилось к норме только в группе пациентов, которым был назначен никотинамид. Функциональная активность мононук- леарных клеток по способности секретировать интерлейкин-1 неуклонно нарастала у больных, получавших лечение только инсулином. Значительно меньшее нарастание этого показателя отмечено в группах пациентов, получавших антиоксиданты. Это увеличение было минимальным у больных, получавших, помимо инсулинотерапии, сочетание никотинамида и ос-токоферола ацетата. Полученные результаты позволили предположить, что применение никотинамида и его сочетание с ос-токоферола ацетатом может препятствовать развитию новой аутоиммунной атаки против оставшихся р-клеток.
Полученные результаты позволили предположить, что применение никотинамида и его сочетание с ос-токоферола ацетатом может препятствовать развитию новой аутоиммунной атаки против оставшихся р-клеток.
При применении антиоксидантов нами отмечено достоверное повышение активности защитных ферментов клетки (СОД и ГЛП), оно было наибольшим в группе пациентов, получавших сочетание антиоксидантов.
Критерием клинической ремиссии считали потребность в инсулине не более 0,4 ЕД на 1 кг массы тела при условии поддержания нормогликемии и агглюкозурии и уровня HbAlc < 6%. В группе пациентов, получавших монотерапию инсулином, ремиссия наступила в 17% наблюдений, при использовании ос-токоферола ацетата — в 33%, никотинамида — в 45%, и сочетания ос-токоферола ацетата и никотинамида — в 89% наблюдений.
В ходе нашего обследования мы не выявили побочных эффектов при применении достаточно больших доз указанных препаратов.
На основании полученных нами данных был сделан вывод о том, что применение в комплексной терапии впервые выявленного ИЗСД достаточных доз никотинамида и ос-токоферола ацетата вызывает увеличение секреции С-пептида, улучшение компенсации углеводного обмена, снижение потребности в инсулине, способствует развитию клинической ремиссии заболевания. Сдерживающий эффект сочетания никотинамида и ос-токоферола ацетата на функциональную активность мононуклеарных клеток может предотвратить развитие новой аутоиммунной атаки и защитить оставшиеся р-клетки от токсичных продуктов свободнорадикального окисления. Это позволяет предположить, что применение указанных препаратов необходимо на самых ранних этапах заболевания.
Сдерживающий эффект сочетания никотинамида и ос-токоферола ацетата на функциональную активность мононуклеарных клеток может предотвратить развитие новой аутоиммунной атаки и защитить оставшиеся р-клетки от токсичных продуктов свободнорадикального окисления. Это позволяет предположить, что применение указанных препаратов необходимо на самых ранних этапах заболевания.
Тем не менее на сегодняшний день остаются нерешенными многие вопросы как теоретического, так и практического плана. Необходимо разработать алгоритм применения никотинамида и ос- токоферола ацетата, уточнить длительность курсов и целесообразность их повторения, вопросы ежедневной и курсовой доз, необходимого и достаточного набора иммунологических, метаболических и функциональных маркеров для формирования групп высокого риска и дальнейшего слежения за эффективностью терапии.
Другой стороной проблемы является необходимость ранней профилактики сосудистых осложнений диабета. В этом смысле, учитывая их патогенез, антиоксидантные препараты незаменимы.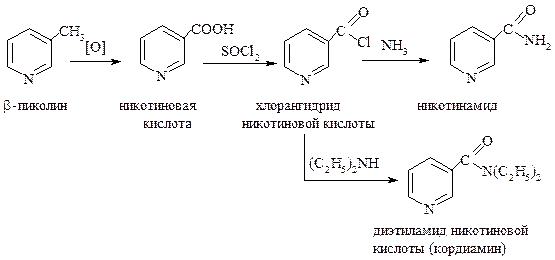 Согласно нашим данным [11], уже в дебюте ИЗСД у ряда больных с поликлональной активацией иммунной системы, усилением процессов пероксидации липидов и ослаблением антиоксидантной защиты появляются условия для развития первых признаков сосудистых осложнений заболевания. Это делает необходимым назначение комплексной терапии никотинамидом и антиоксидантными препаратами уже в дебюте заболевания, что позволит улучшить течение заболевания и отсрочить развитие поздних сосудистых осложнений [45].
Согласно нашим данным [11], уже в дебюте ИЗСД у ряда больных с поликлональной активацией иммунной системы, усилением процессов пероксидации липидов и ослаблением антиоксидантной защиты появляются условия для развития первых признаков сосудистых осложнений заболевания. Это делает необходимым назначение комплексной терапии никотинамидом и антиоксидантными препаратами уже в дебюте заболевания, что позволит улучшить течение заболевания и отсрочить развитие поздних сосудистых осложнений [45].
1. Абакумов Г. 3., Бушма М. И., Лукиенко П. И. // Вопр. мед. химии. — 1988. — № 1. — С. 39—41.
2. Арчаков А. И. Микросомальное окисление. — М., 1975.
3. Великий Н. Н., Обросова И. Г., Ефимов А. С. // Вопр. мед. химии. — 1992. — № 4. — С. 45—52.
мед. химии. — 1992. — № 4. — С. 45—52.
4. Владимиров Ю. А. Перекисное окисление липидов в биологических мембранах. — М., 1972.
5. Горелышева В. А. Перекисное окисление липидов и состояние антиокислительных ферментов у больных с впервые выявленным инсулинзависимым сахарным диабетом: Дис. … канд. мед. наук. — М., 1994. — С. 39—42.
6. Горелышева В. А., Смирнова О. М., Романовская Г. А., Филиппов И. К. // Клин, фармакол. и тер. — 1993. — №3. — С. 51-53.
7. Ефимов А. С. Диабетические ангиопатии. — М., 1989.
8. Меерсон Ф. З. Патогенез и предупреждение стрессорных и ишемических повреждений сердца.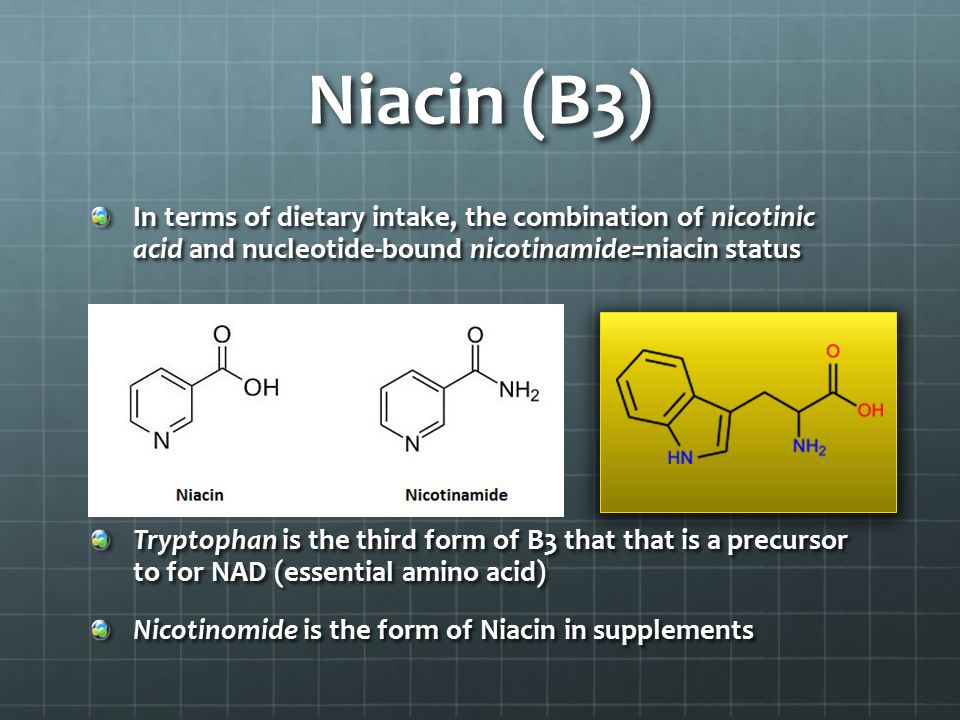 — М., 1984.
— М., 1984.
9. Обросова И. Г. Изучение действия никотинамида на сорбитоловый путь обмена глюкозы при экспериментальном диабете: Автореф. дис. … канд. мед. наук. — Киев, 1985.
10. Обросова И. Г., Великий Н. Н., Ефимов А. С. // Пробл. эндокринол. — 1988. — № 1. — С. 74—80.
11. Смирнова О. М. Клинические, иммуногенетические гормонально-метаболические аспекты впервые выявленного инсулинзависимого сахарного диабета (клиника, диагностика, лечение, профилактика): Дис. … д-ра мед. наук. — М., 1995.
12. Смирнова О. М., Горелышева В. А., Арбузова М. И. и др. // Симпозиум. Сахарный диабет сегодня: Материалы. — М., 1995. — С. 33.
13. Andersen Н. U., Jorgensen К. H., Egeberg J. // European Association for the Study of Diabetes. 29-th Annual Meeting Abstracts-Istanbul, 1993. — N 231. — P. A62.
Andersen Н. U., Jorgensen К. H., Egeberg J. // European Association for the Study of Diabetes. 29-th Annual Meeting Abstracts-Istanbul, 1993. — N 231. — P. A62.
14. Brunetti P., Bolli G. B. // Immunotherapy of Type I Diabetes / Eds D. Andreani, H. Kolb, P. Pozzilli. — Chichester, 1989.
15. Burkard V., Fengler E. M., Kolb H. // Diabetologia. — 1992. — Vol. 35, Suppl. 1. — P. A215.
16. Buscema M., Vinci C, Gatta C. et al. // Metabolism. — 1992. — Vol. 41. — P. 296-300.
17. Cetkovic-Cvrlje M., Sandler S., Eizirik D. L. // European Association for the Study of Diabetes. 29-th Annual Meeting. Abstracts — Istanbul, 1993. — N 229. — P. A61.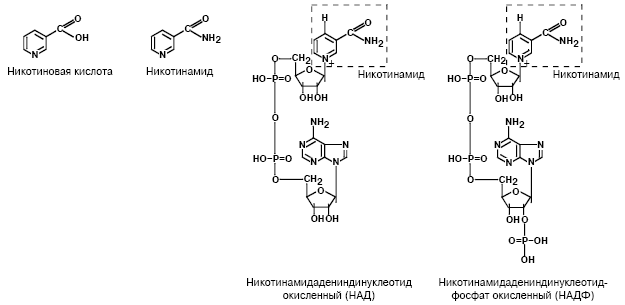
18. Chase H. P., Batter-Simon N., Garg S. // Diabetologia. — 1990. — Vol. 33. — P. 444-446.
19. Dedov I. I., Gorelysheva V. A., Smirnova О. M. et al. // International Diabetes Congress: 15-th Abstracts. Kobe. — 1994. — P. 314.
20. Elliott R. B., Bibby N. J., Reddy S. // Immunology of Diabetes. (Proceedings. 19-th International Workshop) / Eds E. Shafir, P. Vardy. — Jerusalem, 1990. — P. 34.
21. Elliott R. B., Chase H. P., Pilcher С. C. // The Immunology of Diabetes (9-th International Workshop) — Melbourne, 1988. — P. 18.
22. Elliott R. B., Chase H. P. // Diabetologia. — 1991. — Vol. 34. — P. 362-365.
23. Gorelysheva V. A., Smirnova О. M., Dedov I. I. // Horm. Metab. Res. — 1995. — Suppl. 1. — P. 14.
24. Grankvist K, Marklund S. L., Taljedal J.-B. // Biochem. J. — 1981. — Vol. 182. — P. 17-23.
25. Hoffer A. // Schizophrenia. — 1969. — Vol. 1. — P. 78—87.
26. Ilkova H, Gorpe U., Kadioglu P. et al. // International Congress of Endocrinology, 9-th: Abstracts. — Nice, 1992. — P. 376.
27. Jnone Y., Tanigawa K, Tamura K. et al. // Diabetologia. — 1992. — Vol. 35, Suppl. 1. — P. A115.
28. Kaliman B., Burkard U., Krancke K. D. et al. // Life Sci. — 1992. — Vol. 51. — P. 671-678.
29. Kolb H., Burkard V., Appels M. // J. Autoimmun. — 1990. — Vol. 3. — P. 1-4.
30. Kroncke K.-D., Funda J., Berschick B. // Diabetologia. — 1991. — Vol. 34. — P. 232-238.
31. Lampeter E. F. // Diabet. Metab. — 1993. — Vol. 19, N 1—2. — P. 105-109.
32. Lazarow A. // Anat. Rec. — 1947. — Vol. 97. — P. 353-358.
33. Le Doux S. P., Hall C. R., Forbes P. M. // Diabetes. — 1988. — Vol. 37. — P. 1015-1019.
34. Manna R., Migliore A., Martin L. S. // Brit. J. clin. Pract. — 1992. — Vol. 46, N 3. — P. 177-179.
35. Mendpla G., Casamitjana R., Gomis R. // Diabetologia. — 1989. — Vol. 32. — P. 160-162.
36. Mendola J., Wright J. R., Lacy P. E. // Diabetes. — 1989. — Vol. 3.5. — P. 379-385.
37. Nakajama H, Fujino-Kurihara H, Hanafusa T. et al. // Biomed. Res. — 1985. — Vol. 6. — P. 185-189.
38. Nerup J. // Diabetologia. — 1994. — Vol. 37, Suppl. 2. — P. S82-S89.
39. Nomicos I. N., Prowse S. J., Carotenuto P. // Diabetes. — 1986. — Vol. 35. — P. 1302-1304.
40. Okamoto H. // Bio Essays. — 1985. — Vol. 2. — P. 15-21.
41. Pipeleers D., Ling Zh. et al. // Diabet. Metab. Rev. — 1992. — Vol. 8, N 3. — P. 209-227.
42. Pociot E, Reimers J. I., Andersen H. U. // Diabetologia. — 1993. — Vol. 36, N 6. — P. 574-576.
43. Pozzilli P., Lampeter E., Di Mario U., Andreani D. // Immunotherapy of Type I Diabetes. — London, 1989. — P. 35—54.
44. Pozzilli P. The IMDIAB Study Group // Diabetologia. — 1994. — Vol. 37. — P. 314.
45. Pozzilli P., Visalli N., Signore A. et al. // Diabetologia. — 1995. — Vol. 38. — P. 848-852.
46. Pozzilli P., Visalli N., Ghirlanda G. // Diabet. Med. — 1989. — Vol. 6. — P. 568-572.
47. Pozzilli P., Andreani D. // Diabet. Metab. Rev. — 1993. — Vol. 9. — P. 219-239.
48. Shah S. C., Malone J. I., Simpson M. E. // N. Engl. J. Med. — 1989. — Vol. 320. — P. 550-554.
49. Smirnova O., Tchugunova L., Gorelysheva V et al. // Horm. Metab. Res. — 1995. — Suppl. 1. — P. 14.
50. The DCCT Research Group. Effects of age, duration and treatment of insulin-dependent diabetes mellitus on residual beta-cell function: Observation during eligibility teasting for the diabetes control and complications trial (DCCT) // J. clin. Endocrin. Metab. — 1987. — Vol. 65. — P. 30—36.
51. Uchigata Y., Yamamoto H., Nagai H. et al. // Diabetes. — 1983. — Vol. 32. — P. 316-318.
52. Vague P., Vialettes B., Lassmann-Vague V. // Lancet. — 1987. — Vol. 1. — P. 619-620.
53. Vague P., Picq R., Bernal M. // Diabetologia. — 1989. — Vol. 32. — P. 316-321.
54. Vague P., Vialettes B., Lassman V. // Acta diabetol. lat. — 1985. — Vol. 21. — P. 293-304.
55. Varsanyi-Nagy M., Datufalsa V., Buckingham B. // Diabetologia. — 1992. — Vol. 35, Suppl. 1. — P. 496.
56. Vialettes B., Picq R., du Rostu M. // Diabet. Med. — 1990. — Vol. 7, N 8. — P. 731-735.
57. Visalli N., Lucentini L., Crino A. // Diabetologia. — 1992. — Vol. 35, Suppl. 1. — P. A218.
58. Wallensteen M., Dahlquist G., Persson B. // Ibid. — 1988. — Vol. 31. — P. 664-669.
59. Wilson G. L., Patton N J., McCord J. M. // Ibid. — 1984. — Vol. 27. — P. 587-591.
60. Yamagami T, Miwa A., Takas aw a S. et al. // Cancer Res. — 1985. — Vol. 45. — P. 1845-1849.
61. Yonemura Y., Takashima T, Miwa K. et al. // Diabetes. — 1984. — Vol. 33. — P. 401-404.
Витамин В5 (никотиновая кислота, никотинамид, ниацин)
Витамин В5 (витамин PP, никотиновая кислота, ниацин, никотинамид) – относится к группе водорастворимых витаминов. Никотиновая кислота является образующей коферментов NAD+ и NADP+ и играет ключевую роль в переносе водорода при окислении углеводов, жиров и белков. Обладает ключевыми функциями в энергетическом обмене. Никотиновая кислота всасывается в желудке и в двенадцатиперстной кишке, а затем подвергается аминированию, в результате чего получается никотинамид, который в организме в комплексе с белками образует более 80 ферментов. Это основная физиологическая роль витамина В5.
Никотиновая кислота регулирует уровень сахара в крови уменьшает холестерин, расширяет периферические сосуды, т.е. обладает холинергическим действием. Биологический эффект никотиновой кислоты проявляется в виде стимуляции секреторной функции желудка и пищеварительных желез (в ее присутствии в желудке повышается концентрация свободной соляной кислоты).
Недостаток никотиновой кислоты ведет к расстройству нервной системы, патологии кожи, воспалению и язвам слизистьrх оболочек. Эта кислота необходима для обеспечения нормальной функции нервной системы, кожи (пера) и пищеварительной системы.
Витамин В5 кормовой содержит в качестве действующего вещества полученную химическим синтезом никотиновую кислоту- не менее 99,5 %. Представляет собой мелкий порошок от белого до слегка желтоватого цвета, неэлектростатичен, обладает хорошей сыпучестью, имеет пониженное пылеобразование. Слаборастворим в воде.
Витамин В5 кормовой применяют для обогащения и балансирования рационов животных по никотиновой кислоте, а также производства премиксов и кормовых добавок. Вносят в корма на комбикормовых предприятиях, имеющих оборудование для ступенчатого смешивания, или используют в производстве премиксов.
Витамин В5 кормовой стабилен и совместим со всеми ингредиентами корма, лекарственными средствами и другими кормовыми добавками. Побочных явлений и осложнений при применении витамина в соответствии с существующими нормами не выявлено. Противопоказания не установлены.
Фасовка: многослойные бумажные мешки или картонные коробки с полиэтиленовым вкладышем массой от 20 до 25 кг.
Условия хранения: хранят в упаковке производителя, в сухом хорошо проветриваемом помещении, в защищенном от прямых солнечных лучей месте. Температура хранения от 0 ˚С до 25 ˚С.
застосування, побічні ефекти, застереження по використанню, користь та шкода здоров’ю
Никотиновая кислота (ниацин) — это водорастворимый витамин, принадлежит к семейству витаминов группы В, который встречается во многих тканях животных и растений, имеет антигиперлипидемичну активность. Ниацин превращается в его активную форму ниацинамид, который является компонентом коферментов никотинамида-аденинудинуклеотида (НАД) и его фосфатной формы НАДФ. Эти коферменты играют важную роль в тканевом дыхании и метаболизме гликогена, липидов, аминокислот, белков и пурина. Хотя точный механизм действия, с помощью которого никотиновая кислота снижает уровень холестерина, не вполне понятен, эта субстанция может действовать, ингибируя синтез липопротеидов очень низкой плотности (VLDL), ингибируя высвобождение свободных жирных кислот из жировой ткани, увеличивая активность липопротеиновой липазы и снижая печеночный синтез VLDL-C и LDL-C.
Ниацин, также известный как никотиновая кислота и витамин В3, является водорастворимым, необходимым витамином группы В, который при введении в высоких дозах эффективен для снижения холестерина липопротеидов низкой плотности (ЛПНП) и повышение уровня холестерина липопротеидов высокой плотности (ЛПВП), благодаря чему это средство приобретает уникальные ценности в терапии дислипидемии. Ниацин может вызвать легкое к умеренному повышению уровня сывороточной аминотрансферазы, а высокие дозы, определенных форм ниацина связанные с клинически очевидными, острыми травмами печени, которые могут быть как тяжелыми, так и смертельными.
Ниацин (никотиновая кислота) используется для профилактики и лечения дефицита ниацина (пеллагра). Дефицит ниацина может быть следствием определенных заболеваний (например, злоупотребление алкоголем, синдрома мальабсорбции, болезни Хартнупа), неправильной диеты или длительного использования определенных лекарств (например, изониазида).
Продукты содержащие витамин В3
- авокадо
- брокколи
- помидоры
- грибы
- спаржа
- морковь
- рис
- бобовые
- шпинат
- сладкий картофель
Дефицит ниацина может вызвать диарею, спутанность сознания (слабоумие), покраснение / отек языка и шелушение затвердевшой красной кожи. Никотиновая кислота помогает поддерживать способность организма производить и расщеплять природные соединения (обмен веществ), необходимые для крепкого здоровья. Ниацинамид (никотинамид) — это другая форма витамина В3, но сама она не работает так же, как ниацин.
Побочные эффекты употребления ниацина
Раздражение в области лица и шеи, головная боль, зуд, жжение, потливость, озноб или покалывание могут возникнуть в течение 20 минут до 4 часов после приема этого препарата. Раздражение могут продолжаться в течение нескольких часов. Эти эффекты должны сглаживаться или угасать, когда ваш организм адаптируется к лекарствам. Также может наблюдаться расстройство желудка, изжога, тошнота, рвота и диарея. Если любой из этих эффектов сохраняется или ухудшается, немедленно сообщите об этом врача или фармацевта.
Ниацин в ветеринарии
Как и большинство животных, собаки могут синтезировать определенное количество ниацина из незаменимой аминокислоты триптофана. Метаболит триптофана может образовываться одним из двух путей: может быть образован пиколиновой карбоксилазой, или может быть использован для получения никотинамида. Кошки, в отличие от собак, не способны синтезировать значительные количества ниацина из триптофана, поскольку они имеют очень высокую активность фермента пиколиновой карбоксилазы, что приводит к быстрому катаболизму трипофана. Таким образом, кошки нуждаются в рационе предварительно готового ниацина.
Диетические источники никотиновой кислоты
Ниацин естественным образом встречается в мясе и в бобовых. Диетический ниацин обычно содержится в форме никотиновой кислоты в растительных материалах, а также как NAD или NADP в животных материалах. Некоторые цельнозерновые злаки, такие как кукуруза и сорго, имеют относительно высокое содержание ниацина, но в этих продуктах ниацин сконцентрирован в высевающих и зародышевых слоях и имеет плохую биодоступность (то есть связан внутри клетки), что делает корм плохим источником диетического ниацина. Ниацин также чувствителен к распаду при нагревании и нужны специальные добавки для коммерческих кормов чтобы его состояние оставалось стабильным.
Диагностирования дефицита ниацина
Диагностика дефицита ниацина может быть поставлена с помощью теста на никотинамид, измеряющий выведение с мочой метаболитов ниацина, сам тест происходит в ветеринарных контрольных лабораториях. Диагностика также проводится по клиническим признакам, соответствующие дефицита и оценке диеты.
Роль никотиновой кислоты в теле животного
Синтез, строение и термическое поведение комплексного соединения никотината кальция с никотинамидом
АННОТАЦИЯ
В статье приведены результаты физико-химического исследования комплексного соединения никотината кальция с никотинамидом. Определены состав, индивидуальность, термическое поведение, способы координации молекул никотинамида и никотиновой кислоты в составе координационного соединения никотината кальция с никотинамидом.
ABSTRACT
The article presents the results of a physicochemical study of the complex compound of calcium nicotinate with nicotinamide. The composition, personality, thermal behavior, methods of coordination of nicotinamide and nicotinic acid molecules in the coordination compound of calcium nicotinate with nicotinamide are determined.
Ключевые слова: никотинат кальция, никотинамид, никотиновая кислота, комплексное соединение, синтез, ИК-спектроскопия, рентгенофазовый анализ, термический анализ.
Keywords: calcium nicotinate, nicotinamide, nicotinic acid, complex compound, synthesis, IR spectroscopy, X-ray phase analysis, thermal analysis.
Комплексные соединения находят широкое применение в самых различных областях науки и технологий. Применение координационных соединений в фармацевтической отрасли в течение многих лет является основным научным направлением при создании новых лекарственных препаратов. При этом одной из актуальных проблем современной медицины является лечение болезней сердца, в частности аритмии сердца человека [5; 21-24; 26]. В данной статье приводятся результаты синтеза и анализа нового комплексного соединения никотината кальция с никотинамидом, которое проявило специфическую активность при аритмии сердца [2; 17].
В процессе выполнения настоящего исследования для синтеза комплексного соединения Ca(НК-Н)2.2АНК использовали безводный хлорид кальция, никотинамид и никотиновую кислоту марки «чда» или «хч». Количество металла в синтезированном соединении определяли на атомно-абсорбционном спектрофотометре марки novAA 300 фирмы Analitik Jena AG (Германия) [15; 20]. Азот определяли по методу Кьельдаля [8], углерод и водород – сжиганием в токе кислорода [11]. Для установления индивидуальности синтезированных комплексных соединений снимались рентгенограммы на рентгеновском дифрактометре «Дрон-2,0» [12]. Для расчета межплоскостных расстояний использовались таблицы [7], а относительная интенсивность линии I/I1 определялась в процентах от наиболее сильно выраженного рефлекса в максимуме.
Ик-спектры поглощения записывали в области 400-4000 см—1 на ИК-спектрометре Cary 630 FTIR фирмы Agilent Technologies (США).
Термический анализ проводили на дериватографе системы Паулик-Паулик-Эрдей [25] со скоростью 10 град/мин и навеской 0,1 г при чувствительности гальванометров Т-900, ТГ-100, ДТА-1/10, ДТГ-1/10. Запись проводили при атмосферных условиях с постоянным удалением газовой среды с помощью водоструйного насоса. Держателем служил платиновый тигель диаметром 7 мм без крышки. В качестве эталона использовали Al2O3.
Для проведения синтеза комплексного соединения 0,01 моль никотиновую кислоту растворяли в 100 мл 96% этилового спирта, добавляли 30 мл 0,01 М раствора гидроксида натрия, перемешивали 30 мин в магнитной мешалке, после чего добавляли 30 мл 0,05 М раствора хлорида кальция и перемешивали в течение 25-30 мин на водяной бане при температуре 55-60°С. Раствор охлаждали до комнатной температуры, при этом выпадал белый творожистый осадок, который фильтровали через бумажный фильтр «Watman», промывали 3-4 раза по 25 мл этиловым спиртом, высушивали на воздухе. В результате был получен кристаллический порошок белого цвета, без запаха. Выход составил 95,56%.
Отсутствие ионов хлора в соединении тестировали посредством 0,1 М раствора Ag(NO3)2. При этом не наблюдалось появление белого осадка и изменение цвета раствора.
Дериватографический анализ показал, что соединение никотината кальция содержит одну молекулу воды.
Комплекс состава Ca(C5H4NCOO)2·2NС5Н4CОNH2 (условное обозначение Ca(НК-Н)2.2АНК) синтезирован путем интенсивного перемешивания 0,05 мольмоногидрата никотината кальция с 0,1 моль никотинамида в шаровой мельнице фирмы «Retsch» при комнатной температуре в течение 0,3 часа [1; 4; 9; 10; 13; 16; 18].
Результаты элементного анализа синтезированного координационного соединения Ca(НК-Н)2.2АНК имеют следующие значения. Вычислено: Са –8,01%; N – 11,19%, С – 57,59%, H – 4,03%. Найдено: Са – 7,98%; N – 10,89%, С – 57,67%; H – 3,93%.
Индивидуальность синтезированного вещества определяли посредством сравнения межплоскостных расстояний и относительной интенсивности линий никотинамида, молекулы никотиновой кислоты и полученного комплекса на их основе. По результатам исследования показатели нового координационного соединения отличаются от исходных компонентов, следовательно, соединение Ca(НК-Н)2.2АНК имеет индивидуальную кристаллическую решетку (рис. 1).
Рисунок 1. 1 – никотинамид; 2 – никотиновая кислота; 3 – никотинат кальция; 4 – комплексное соединение Ca(НК-Н)2.2АНК
ИК-спектры поглощения свободной молекулы никотинамида, никотината кальция и их комплексного соединения приведены на рис. 2. Некоторые колебательные частоты в ИК-спектрах поглощения свободной молекулы никотинамда, никотината кальция и их комплексного соединения приведены в таблице 1.
Рисунок 2. ИК-спектры: 1 – никотиновая кислота; 2 – никотинамид; 3 –моногидрат никотината кальция; 4 – комплексное соединение Ca(НК-Н)2.2АНК
Таблица 1.
Некоторые основные колебательные частоты в см-1
|
№ № |
Название веществ |
Полосы |
|||||||
|
-NH2 |
C=O |
CH |
C=N |
CONH2 |
C-O |
COOCa O-Ca |
-NHкоорд.бидент. |
||
|
11. |
Никотиновая кислота |
— |
1700 |
1415 |
1593 |
— |
1291 |
— |
— |
|
22. |
Никотинамид |
3356 |
1613 |
1390 |
1613 |
1674 |
1200 |
— |
— |
|
33. |
Кальций никотинат |
— |
1602 |
703 757 |
1557 |
— |
1190 |
1407 |
— |
|
44. |
Комплексное соединение Ca(НК-Н)2.2АНК |
3364 |
1679 |
757 767 |
1606 |
1630 |
1199 |
1402 |
1583 1562 1340 1326 |
В ИК-спектре поглощения комплексного соединения «Ca(НК-Н)2.2АНК» обнаружены следующие частоты: 1679 см-1(C=O), 1630 см-1(H2NC=O), 3364 см-1(-NH2) и внутриводородные частоты при 3154 см-1(С=N), 1606 см-1, 1583 см-1и 1562 см-1,соответствующие интенсивным валентным и деформационным колебаниям, частоты 1402 см-1 (О-Са), 1340 см-1, 1326 см-1 на 1029 см-1соответствуют бидентатной координационной связи HN [3; 6; 19].
На основании спектроскопических данных предложено следующее строение комплекса:
На дериватограмме комплексного соединения Ca(НК-Н)2.2АНК (рис. 3) наблюдаются шесть эндотермических эффектов при 63°С, 118°С, 150°С, 255°С, 275°С, 745°С и два экзотермических эффекта при 375°С и 570°С. При первом эндотермическом эффекте изменение массы не наблюдалось. Второй и третий эндотермические эффекты в интервале температур 65°-190°С сопровождаются уменьшением массы на 1,72%. Четвертый эндотермический эффект протекает интенсивным разложением образца. Потеря массы в диапазоне температур 190°-262°С по кривой термогравиметрии составляет 27,59%. Последний эндотермический эффект протекает в области температур 262°-310°С, и убыль массы составляет 19,97%. Первый экзотермический эффект при 375°С протекает в интервале 310-405°С, и уменьшение массы составляет 0,60%. При экзотермическом эффекте при 570°С потеря массы составляет 32,33%. Характер эндотермического эффекта при 745°С соответствует разложению продуктов термолиза, и в области 600-830°С уменьшение массы составляет 7,58%. Общая потеря массы в диапазоне температур 65-830°С составляет 88,79%.
Рисунок 3. Дериватограмма комплексного соединения Ca(НК-Н)2.2АНК
Впервые синтезировано смешаннолигандное комплексное соединение никотината кальция с никотинамидом состава Ca(C5H4NCOO)2·2NС5Н4CОNH2. Методами рентгенофазового, дериватографического анализов, колебательной спектроскопии доказаны индивидуальность, способы координации молекул никотинамида и никотинатного фрагмента, изучено термическое поведение соединения.
Заключение. На основании анализа спектроскопических данных установлено, что молекула никотинамида выступает в роли монодентатного лиганда, координируясь через гетероатом азота пиридинового кольца. Анионы никотиновой кислоты координируются бидентатным способом. Исследовано термическое поведение синтезированного комплекса.
Список литературы:
1. Аввакумов Е.Г. Механические методы активации химических процессов. – Новосибирск: Наука, 1986. – 305 с.
2. Беликов В.Г. Специальная фармацевтическая химия. – Пятигорск: «Высшая школа», 1996. – Т. 2. – С. 383.
3. Беллами Л. Инфракрасные спектры сложных молекул. – М.: Изд-во иностр. лит-ы, 1963. – С. 237.
4. Болдырев В.В. О кинетических факторах, определяющих специфику механохимических процессов в неорганических системах // Кинетика и катализ. – 1972. – № 13. – C. 1411-1421.
5. Болезни сердца и сосудов: В 4-х т. / Е.И. Чазов, Г.Г. Арабидзе, Ю.И. Бредикис и др. – М.: Медицина, 1992. – Т. 3. – С. 5-11.
6. Варшавский Ю.С., Комаров Е.В., Суглобов Д.Н. Исследование комплексных соединений методом инфракрасной спектроскпии // Спектроскопические методы в химии комплексных соединений. – М.-Л., 1964. – С. 124.
7. Гиллер Я.Л. Таблицы межплоскостных расстояний. – М.: Недра, 1966. – Т. 1. – 362 с.
8. Государственная фармакопея СССР. – Изд. 11. Определение азота в органических соединениях. – М.: Медицина, 1987. – Вып. I. – 180 c.
9. Ениколопов Н.С. Твердофазные химические реакции и новые технологии // Успехи химии. – 1991. – Т. 60. – № 3. – С. 586-594.
10. Ибодуллоева М.И. Смешанноамидоникотинатные координационные соединения ряда металлов: Автореф. канд. хим. наук. – Ташкент, 2011. – 12 с.
11. Климова В.А. Основы микрометоды анализа органических соединений. –М.: Химия, 1967. – С. 19.
12. Ковба П.М., Трунов В.К. Рентгенофазовый анализ. – М.: МГУ, 1976. – 232 с.
13. Коновалов Л.В., Масленников И.С., Шемякин В.Н. Координационные центры амида никотиновой кислоты (АНК) в комплексах с солями переходных металлов // Журнал неорганической химии. – 1970. – Т. 15. – № 7. – C. 1993-1995.
14. Коротченкова Н.В., Самаренко В.Я. Витамины гетероциклического ряда: строение, свойства, синтез, химическая технология. – СПб.: СПХФА, 2006. – С. 4-13.
15. Кукушкин Ю.Н. Химия координационных соединений. – М.: Высшая школа, 1985. – 413 с.
16. Массалимов И.А. Образование неравновесных состояний вещества при ударных воздействиях // Башкирский химический журнал. – 1998. – Т. 5. – № 1. – С. 55-58.
17. Машковский М.Д. Лекарственные средства: Пособие для врачей: В 2-х т. – М.: ООО «Новая волна», издатель С.Б. Дивов, 2002. – Т. 1. – 452 с.
18. Механохимический синтез пигментов на основе гексацианоферратов (II, III) 3d-элементов / В.К. Половняк, Д.В. Саниева, С.В. Половняк, Р.Я. Дебердеев // Вестник Удмуртского университета. – 2005. – № 8. – С. 111-116.
19. Накамото К. Инфракрасные спектры неорганических и координационных соединений. – М.: Мир, 1966. – С. 268.
20. Agilent in Pharmaceutical Issue 1, Winter 2002 Analysis. P. 102.
21. Class IV agents affect calcium channels and the AV node. K channel blocker;Kulmatycki K.M, Abouchehade K., Sattari S, Jamali F (May 2001). «Drug-disease interactions: reduced beta-adrenergic and potassium channel antagonist activities of sotalol in the presence of acute and chronic inflammatory conditions in the rat». Br. J. Pharmacol.133 (2): 286–94.
22. Conti J.B., Belardinelli L., Utterback D.B., Curtis A.B. Endogenous adenosine is an antiarrhythmic agent. Circulation. 1995. Vol. 91 (6). Р. 1761
23. Lenz T.L., Hilleman D.E. Dofetilide, a New Class III Antiarrhythmic Agent. Department of Cardiology, Creighton University, Omaha, Nebraska. Pharmacotherapy. 2000. Vol. 20 (7). Р. 776-786.
24. Milne J.R., Hellestrand K.J., Bexton R.S., Burnett P.J., Debbas N.M., Camm A.J. Class 1 antiarrhythmic drugs—characteristic electrocardiographic differences when assessed by atrial and ventricular pacing. Eur. Heart J. 1984. Vol. 5 (2). Р. 99-107.
25. Paulix F., Paulix I., Erdey L. Derivatograph. I. Mittelung Ein automatish registriender Apparat zur gleichzeitigen Ausguchrund der Differential-ther mogravimetrishen Untersuchengen. UZ. Anal. Chem. 1958. Vol. 160. No. 4. P. 241-250.
26. Trevor A.J., Katzung B.G. Pharmacology. New York: Lange Medical Books/McGraw-Hill, Medical Publishing Division, 2003. P. 43.
Ниацин — Энциклопедия Нового Света
Ниацин , также известный как никотиновая кислота или витамин B 3 , представляет собой витамин, производные которого НАД, НАДН, НАД + и НАДФ играют важную роль в энергетическом обмене. в живой клетке и репарации ДНК. Обозначение витамин B 3 , химическая формула которого C 5 H 4 NCOOH (или, альтернативно, C 6 H 6 NO 2 ), также включает соответствующий амид никотинамид, или ниацинамид , химическая формула которого C 6 H 6 N 2 O.
Ниацин — один из витаминов группы B (комплекс витаминов B), группа химически различных водорастворимых витаминов, в которую также входят тиамин, рибофлавин, пантотеновая кислота, биотин, пиридоксин, фолиевая кислота и другие. Когда-то витамин B считался одним витамином, а теперь он рассматривается как комплекс различных витаминов, которые обычно содержатся в одних и тех же продуктах. Витамины — это органические (содержащие углерод) питательные вещества, получаемые с пищей и необходимые в небольших количествах для нормальных метаболических реакций.
Превращение ниацина в НАД и НАДФ и использование этих коферментов в сложных биологических процессах, таких как цикл лимонной кислоты, выявляют сложную координацию в живых организмах.
Ниацин, помимо других источников, содержится в мясе, рыбе, орехах, зеленых овощах и дрожжах. Дефицит ниацина приводит к пеллагре, что свидетельствует о необходимости полноценного и разнообразного питания.
Функция: НАД и НАДФ
Никотинамидадениндинуклеотид (НАД + )Никотиновая кислота и никотинамид используются для образования коферментов НАД и НАДФ, которые являются важными кофакторами, обнаруженными в клетках.
Никотинамидадениндинуклеотид (NAD + ) и никотинамидадениндинуклеотидфосфат (NADP + ) играют ключевую роль в качестве переносчиков электронов в передаче восстановительного потенциала. НАДН — это восстановленная форма НАД + , а НАД + — окисленная форма НАДН. Точно так же НАДФН — это восстановленная форма НАДФ + , а НАДФ + — окисленная форма НАДФН.
Для многих ферментов необходимы коферменты ниацина НАД и НАДФ.Хотя НАД и НАДФ отличаются только одной фосфатной группой, они имеют разные функции в биохимии. НАД (НАДН) широко используется в катаболизме углеводов, жиров, белков и алкоголя для производства энергии. Таким образом, он играет важную роль в гликолизе и цикле лимонной кислоты клеточного дыхания. Напротив, НАДФ (НАДФН) используется в анаболических реакциях (биосинтез), таких как синтез нуклеиновых кислот, жирных кислот и холестерина (Higdon 2002).
При синтезе NAD + никотиниамид соединяется с рибозой и ADP с образованием NAD + .Из NAD + добавление фосфатной группы в положение 2 ‘аденильного нуклеотида через сложноэфирную связь образует NADP + .
НАД (и ниацин) также может синтезироваться в печени из аминокислоты триптофана (Hidgon 2002).
Дефицит и передозировка
Химическая структура никотинамидаСильный недостаток ниацина вызывает болезнь дефицита пеллагры, тогда как легкий дефицит замедляет метаболизм, снижая толерантность к холоду. Симптомы пеллагры включают высокую чувствительность к солнечному свету, агрессию, дерматит, покраснение кожи, бессонницу, слабость, спутанность сознания, диарею и деменцию (в конечном итоге).В целом, основные результаты пеллагры легко запомнить как «четыре D»: диарея, дерматит, слабоумие и смерть. Без лечения болезнь может убить в течение четырех или пяти лет.
Чрезвычайно высокие дозы ниацина могут вызвать макулопатию ниацина, утолщение макулы и сетчатки, что приводит к нечеткости зрения и слепоте (Gass 1973).
Ниацин сам по себе не токсичен, но химические вещества, превращаемые ниацином, токсичны для кожи и печени при передозировке, и высокие дозы ниацина должны быть достигнуты только при постепенном увеличении.Исследования на лабораторных животных продемонстрировали изменения в поведении при приеме больших доз ниацина (Sullivan 1958).
Рекомендуемая суточная доза ниацина составляет 2-12 миллиграммов в день для детей, 14 миллиграммов в день для женщин, 16 миллиграммов в день для мужчин и 18 миллиграммов в день для беременных или кормящих женщин (Higdon 2002). Более 20 миллиграммов в день могут вызвать приливы продолжительностью 15-30 минут.
Дефицит ниацина может быть вызван недостаточным потреблением ниацина с пищей или недостаточным потреблением аминокислоты триптофана, который может быть преобразован в ниацин, хотя коэффициент конверсии низок (Hidgon 2002).
Discovery
Никотиновая кислота была впервые обнаружена в результате окисления никотина. Когда были обнаружены свойства никотиновой кислоты, было сочтено благоразумным выбрать название, чтобы отделить ее от никотина и избежать мысли о том, что либо курение дает витамины, либо эта полезная пища содержит яд. Полученное в результате название «ниацин» произошло от ni cotinic ac id + vitam in . Ниацин относится как к никотиновой кислоте, так и к никотинамиду.
Витамин B 3 также упоминается как «витамин PP», название, производное от устаревшего термина «фактор предотвращения пеллагры».
Биодоступность и биосинтез
Печень может синтезировать ниацин из незаменимой аминокислоты триптофана, но синтез происходит очень медленно; Для производства одного миллиграмма ниацина требуется 60 миллиграммов триптофана (Higdon 2002). Биосинтез ниацина из триптофана требует как витамина B6, так и рибофлавина.
Диетический дефицит ниацина исторически был заметен в регионах, где люди едят кукурузу, зерно с низким содержанием ниацина, в качестве основного продукта питания, и , которые не используют известь при производстве кукурузной муки / муки.Хотя кукуруза содержит значительное количество ниацина, она химически связана в форме, недоступной для человека (Higdon 2002). Щелочная известь высвобождает триптофан из кукурузы, чтобы он мог абсорбироваться в кишечнике и превращаться в ниацин (UMMC 2004).
5-членный ароматический гетероцикл незаменимой аминокислоты, триптофана, расщепляется и перестраивается с альфа-аминогруппой триптофана в 6-членный ароматический гетероцикл ниацина по следующей реакции:
- Биосинтез: триптофан → кинуренин → ниацин
Источники пищи
Другое применение
Ниацин играет важную роль в выработке нескольких гормонов, связанных с сексом и стрессом, особенно тех, которые вырабатываются надпочечниками.Он также играет важную роль в удалении токсичных и вредных химических веществ из организма (UMMC 2004).
При приеме в больших дозах ниацин повышает уровень липопротеинов высокой плотности (ЛПВП) или «хорошего» холестерина в крови, и иногда его назначают пациентам с низким уровнем ЛПВП и с высоким риском сердечного приступа (McGovern 2005). Ниацин (хотя и не ниацинамид) также используется при лечении гиперлипидемии, поскольку он снижает уровень липопротеинов очень низкой плотности (ЛПОНП), предшественника липопротеинов низкой плотности (ЛПНП) или «плохого» холестерина, секрецию печени и подавляет синтез холестерина ( Trevor et al.2005). Основная проблема клинического использования ниацина при дислипидемии — это покраснение кожи даже при приеме умеренных доз (NLM and NIH 2005).
В настоящее время предпринимаются попытки создать состав вещества с пролонгированным высвобождением, чтобы его можно было использовать более часто и более комфортно (Barter 2006).
Промышленное использование
Никотиновая кислота реагирует с гемоглобином и миоглобином в мясе с образованием ярко окрашенного комплекса и, таким образом, используется в качестве пищевой добавки, обычно для улучшения цвета фарша (фарша).Ниацин лицензирован в качестве пищевого красителя в некоторых странах.
Примечания
- ↑ Merck Index , 11-е издание, 6435 .
Ссылки
- Бартер П. «Варианты терапевтического вмешательства: насколько эффективны различные агенты?» Дополнения к Европейскому кардиологическому журналу 8 (Приложение F): F47-F53. Проверено 28 января 2007 года.
- Школа Файнберга, Северо-Западный университет. 2006. Информационный бюллетень о питании: ниацин (витамин B3). Северо-Западное питание . Проверено 28 января 2007 года.
- Гасс, Дж. Д. 1973. Макулопатия никтоновой кислоты. Am. J. Opthamology 76: 500-10.
- Хигдон, Дж. 2002. Ниацин. Институт Линуса Полинга (Университет штата Орегон). Проверено 28 января 2007 года.
- Макговерн, М. Э. 2005. «Стремление к Х-ЛПВП: повышение уровней для снижения риска сердечно-сосудистых заболеваний». Аспирантура 117 (4).
- Sullivan, W. T. 1958. «Поведенческие изменения у крыс и морских свинок, вызванные введением индол-3-уксусной кислоты и 6-аминоникотинамида.» Журнал питания (10 июня 1958 г.): 199-209.
- Тревор, А. Дж., Б. Г. Кацунг и С. Б. Мастерс. 2005. Фармакологический экзамен Кацунг и Треворс и обзор совета директоров , 7-е издание. Lange Medical Books / McGraw-Hill.
- Медицинский центр Университета Мэриленда (УГМК). 2004. Витамин B3 (ниацин). Веб-сайт Медицинского центра Университета Мэриленда. Проверено 28 января 2007 г.
- Национальная медицинская библиотека США и Национальные институты здравоохранения (NLM и NIH).2005. Ниацин. Медлайн Плюс. Проверено 28 января 2007 г.
Источники
Энциклопедия Нового Света Писатели и редакторы переписали и завершили статью Википедии в соответствии со стандартами New World Encyclopedia . Эта статья соответствует условиям лицензии Creative Commons CC-by-sa 3.0 (CC-by-sa), которая может использоваться и распространяться с указанием авторства. Кредит предоставляется в соответствии с условиями этой лицензии, которая может ссылаться как на участников Энциклопедии Нового Света, и на самоотверженных добровольцев Фонда Викимедиа.Чтобы процитировать эту статью, щелкните здесь, чтобы просмотреть список допустимых форматов цитирования. История более ранних вкладов википедистов доступна исследователям здесь:
История этой статьи с момента ее импорта в Энциклопедия Нового Света :
Примечание. могут применяться ограничения на использование отдельных изображений, на которые распространяется отдельная лицензия.
Ниацин против никотинамида против никотинамида Рибозид
Витамин B3 является таким же стандартным, как и ваш ежедневный поливитамин, но этот важный микронутриент не так уж и прост, как кажется.
Первоначально названный ниацином еще на рубеже двадцатого века, витамин B3 не всегда является чистым и подходящим с молекулярной точки зрения или точки зрения безопасности. Сегодня витамин B3 принимает три различных формы. Мы обсудим различия между ними: ниацин, никотинамид и никотинамид рибозид.
Ниацин, оригинальный витамин B3.
Витамин B3 чаще всего ассоциируется с ниацином, почти синонимом поливитаминов. Корни ниацина старые, уходят корнями в прошлое, когда он использовался для лечения болезни под названием пеллагра, что по-итальянски означает «грубая кожа».«Распространение пеллагры по всему Югу Америки, пациенты с пеллагрой страдали тяжелыми симптомами, известными как« 4 D »: дерматит, диарея, деменция и смерть.
Пеллагра продолжала оставаться неуправляемой проблемой, пока доктор Джозеф Голдбергер не связал пеллагру с диетой дефицит витамина B3 в 1926 году. Впоследствии открытие Голдбергера привело к широкому распространению добавок ниацина в качестве эффективного лечения. Постановления правительства требовали, чтобы такие группы продуктов питания, как мука, были обогащены ниацином в целях решения проблем более широких слоев населения.
Ниацин как средство от повышенного холестерина.Пеллагра ушла в прошлое, но мы узнали, что ниацин делает гораздо больше, и в последующие десятилетия его идентифицировали как средство от высокого холестерина.
Как отмечают в клинике Майо, врачи иногда назначают ниацин, чтобы повысить уровень холестерина липопротеинов высокой плотности (ЛПВП) , более широко известного как «хороший холестерин». «Хороший холестерин» снижает уровень холестерина липопротеинов низкой плотности (ЛПНП) в крови, также известного как «плохой холестерин», и его уровни связаны с более низким риском сердечно-сосудистых заболеваний.
CDC отмечает повышение уровня «плохого холестерина» , что увеличивает риск образования бляшек в кровеносных сосудах. Наращивание зубного налета и воспаление могут сделать сосуды жесткими, что приведет к повышению артериального давления. Ниацин помогает предотвратить этот процесс, регулируя выработку холестерина печенью.
Ниацин может улучшить функцию почек.Ниацин также исследовался на предмет его роли в поддержке функции почек. Когда почки теряют функцию, они не избавляются от достаточного количества фосфата, который затем связывает кальций и нарушает жизненно важные функции сердца и мышц.
Ниацин помогает поддерживать клетки под принуждением, например клетки почек при хронических заболеваниях. Исследование, опубликованное в Clinical Journal of the American Society of Nephrology , показывает, что ниацин способствует контролю фосфатов в почках.
Побочные эффекты ниацина.Как отмечает Healthline, у ниацина есть ахиллесова пята: интенсивное покраснение . Несмотря на то, что никотиновая кислота считается безвредной, она может вызывать дискомфорт, вызывая покраснение, зуд и тепло кожи.
Обычно покраснение проходит по мере того, как ваше тело акклиматизируется, но большая часть энтузиазма вокруг ниацина ослабевает после того, как вы узнали об этом неприятном побочном эффекте.
Никотинамид, младший брат ниацина.
Никотинамид, иногда известный как ниацинамид, действует аналогично ниацину, но имеет другую молекулярную структуру. Это тонкое различие позволяет никотинамиду обойти этап, вызывающий раздражающую приливу ниацина, обеспечивая преимущества витамина B3, не заставляя вас стесняться.
Никотинамид может помочь при угревой сыпи.Никотинамид частично исследуется на предмет его способности поддерживать здоровье кожи, контролируя воспаление, сверхактивную реакцию иммунной системы организма.
Угри часто вызываются сверхактивной реакцией иммунной системы на естественные бактерии кожи. Это часто проявляется в виде покраснения, тепла, отека, корок и других симптомов прыщей.
Обзорная статья, опубликованная в Dermatologic Therapy , описывает, как многочисленные исследования показали, что никотинамид является эффективным средством лечения неконтролируемых прыщей .Хотя многие дерматологи в настоящее время рекомендуют никотинамид, данные остаются неубедительными, и для оценки эффективности требуются крупные испытания.
Побочные эффекты никотинамида.Обзор, опубликованный в Diabetologia , сообщает о некоторых людях, у которых при приеме никотинамида наблюдается желудочно-кишечных симптомов . В той же публикации сообщается, что может увеличить риск диабета типа в высоких дозах.
Никотинамид также может ингибировать уникальный класс защитных ферментов, называемых сиртуинами.Как сообщается в Journal of Cell Science , сиртуины необходимы для репарации ДНК и выживания клеток . Сиртуины, как и многие регуляторные ферменты, помогают клеткам отслеживать и исправлять свою ДНК до того, как они начнут реплицироваться. Этот процесс предотвращает передачу клетками мутировавших генов, что сродни ошибочной инструкции, что может привести к нарушению многих клеточных процессов.
Сиртуины регулируют скорость, с которой наши клетки расщепляют энергию, поддерживают свои механизмы и размножаются, что делает их популярной целью для исследований долголетия.Обзор, опубликованный в Biogerontology , предполагает, что сиртуины могут даже продлить продолжительность жизни у некоторых животных. К сожалению, никотинамид, кажется, отключает сиртуины, что может отрицательно сказаться на здоровье и выживании клеток.
Новый взгляд на витамин B3: никотинамид рибозид.
Никотинамид рибозид был впервые идентифицирован в 1940-х годах, но в 2000-х годах ученые обнаружили, что он может вырабатывать кофермент под названием NAD + гораздо более эффективно, чем ниацин или никотинамид.НАД + — это важная молекула, которую ваше тело использует для регулирования клеточного метаболизма, старения и восстановления ДНК.
НАД + и старение?Многообещающее исследование группы исследователей из Университета Нового Южного Уэльса выявило возрастных изменений метаболизма НАД + у людей. Их исследование показало, что уровень НАД + снижается на 50% в возрасте от 40 до 60 лет.
Команда обнаружила сильную отрицательную корреляцию между уровнями НАД + и возрастом, наблюдая за ролью НАД в подпитке механизмов, необходимых для борьбы с окислительным стрессом, который вносит значительный вклад в возрастные изменения в организме.
Никотинамид рибозид и окислительный стресс.Помимо воспаления и инфекции, многие процессы в нашей повседневной жизни, такие как расщепление пищи, могут повредить нашу ДНК и клеточные механизмы. Наш метаболизм вызывает это повреждение в процессе, называемом «окислительным стрессом». Ферменты восстановления используют и истощают НАД + для устранения повреждений и предотвращения необратимых осложнений.
Хотя старение естественным образом снижает уровни НАД +, другие факторы стресса, такие как лишение сна , малоподвижный образ жизни , плохое питание и потребление алкоголя также могут истощать уровни НАД +.
Никотинамид рибозид — наиболее эффективная добавка для восстановления уровня НАД +, который может истощиться из-за этих повседневных стрессоров.
Побочные эффекты никотинамид рибозида.Никотинамид рибозид уникально безопасен — он был оценен в 11 опубликованных испытаниях на людях без каких-либо серьезных побочных эффектов, о которых сообщалось в клинических испытаниях.
Однако существует несколько форм никотинамид рибозида. Среди них Niagen® — единственная запатентованная форма, прошедшая нормативные процедуры для оценки безопасности на ключевых рынках по всему миру.
Никотинамид рибозид: многообещающий способ повысить уровень НАД +.Никотинамид рибозид — последний представитель семейства B3. Однако у него нет такого же резюме, как у ниацина, с точки зрения его использования для лечения высокого уровня холестерина или поддержки функции почек. Кроме того, он, как и никотинамид, еще не исследован на предмет помощи при угревой сыпи.
Тем не менее, ученые обнаружили, что роль никотинамид рибозида как наиболее эффективного усилителя НАД + может быть самым многообещающим преимуществом, которое открывает нам понимание здоровья клеток по мере продолжения исследований.
Большие добавки никотиновой кислоты и никотинамида повышают уровни НАД + и поли (АДФ-рибозы) в тканях, но не влияют на вызванные диэтилнитрозамином измененные очаги печени у крыс Fischer-344 | Журнал питания
Аннотация
Поли (АДФ-рибоза) представляет собой гомополимер АДФ-рибозных единиц, синтезируемых из NAD + на ядерных акцепторных белках, и, как известно, участвует в репарации ДНК. Неизвестно, влияют ли большие пероральные дозы клинически используемых предшественников НАД, никотиновой кислоты или никотинамида, на метаболизм поли (АДФ-рибозы) или клеточный ответ на повреждение ДНК.В нашем первом исследовании на крысах Fischer-344 прием никотиновой кислоты в течение 2 недель (диета 500 и 1000 мг / кг) вызывал повышенные уровни NAD + в крови, печени, сердце и почках, тогда как никотинамид вызывал повышенные уровни. только в крови и печени, по сравнению с контрольной группой, получавшей рацион, содержащий 30 мг / кг никотиновой кислоты. И никотиновая кислота, и никотинамид в дозе 1000 мг / кг диеты вызвали повышение уровня NAD + в печени на 44 и 43% соответственно. Однако только никотинамид повышал уровень поли (АДФ-рибозы) в печени (на 63% выше, чем в контрольной группе).После лечения гепатоканцерогеном диэтилнитрозамином у крыс, получавших никотиновую кислоту и никотинамид в дозе 1000 мг / кг, наблюдались более высокие уровни печеночного NAD + , но только добавка никотиновой кислоты вызывала большее накопление поли (АДФ-рибозы) в печени ( 61% выше контрольной группы). Ни один из диетических методов лечения существенно не повлиял на долю печени, занятую плацентарными очагами, положительными по глутатион- S -трансферазе. Эти результаты показывают, что синтез поли (АДФ-рибозы) не зависит напрямую от уровней NAD + в печени во время приема добавок ниацина, и что механизмы действия никотиновой кислоты и никотинамида различны.Наблюдаемые изменения в метаболизме поли (АДФ-рибозы), по-видимому, не вызывают каких-либо изменений восприимчивости к химически индуцированному канцерогенезу в этом органе.
Этот контент доступен только в формате PDF.
© 1995 Американский институт питания
Американский институт питания
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности.Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались.Чтобы принять файлы cookie с этого сайта, используйте кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файле cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
A Молекулярная оценка витаминов-предшественников НАД + в питании человека
ANRV350-NU28-07 ARI 10 июля 2008 г. 14: 6
Источник NR (14), как было показано, противодействует
дефекту роста, наблюдаемому у животных, получающих кукурузное корма (46).
В мясе Na и Nam отсутствуют, а NAD
+
и NADP являются обильными источниками ниацина
(34, 86). Nam продуцируется ферментами слизистой оболочки
, которые расщепляют NAD
+
(86), а Na продуцируется
из Nam путем дезаминирования бактериальной никоти-
намидазой в кишечнике (13). Как Na, так и Nam абсорбируются из пищеварительного тракта
и поступают в кровоток
для распределения в тканях (40,
82, 86).Исследования показывают, что Nam является доминирующей абсорбированной формой ниацина, когда в качестве источников питания
используются NAD
+
и NADP (16, 35, 36, 81).
Однако также сообщалось, что NAD
+
переваривается пирофосфатазами до NMN, а
гидролизуется до NR, что было обнаружено у мужчин lu-
верхней части тонкой кишки (32). Мы предполагаем, что NR включается в клеточный пул
NAD
+
посредством действия пути Nrk (14)
или через спасение Nam после преобразования в Nam посредством фосфолиза
(8).
СИСТЕМНЫЙ АНАЛИЗ
OF NAD
+
БИОСИНТЕЗ
Qprt, Nampt, Naprt1 и Nrk1,2 являются ферментами, участвующими в синтезе NAD
+
p из
9000 , Na и NR. Таким образом, исследуяэкспрессию каждого фермента и изучая метаболические судьбы пищевых входов, можно описать тканеспецифические пути биосинтеза NAD
+
.
Животные на рационе, содержащем достаточное количество
как Trp, так и ниацина, имеют измеряемую концентрацию каждого из них в печени
(9, 10). Однако считается, что
Nam и Na поставляют
только часть NAD
+
, производимого в печени
, при этом большая часть ниацина циркулирует в других тканях. Считается, что Trp является основным предшественником NAD
+
, используемым в печени (9). В дополнение к
, продуцирующему хинолинат для входа в пути биосинтеза NAD
+
, Trp включается в белок
, используется для выработки энергии посредством окисления до
тал и используется для образования кинуреновой кислоты
.Индуцируемые ферменты утилизации Trp reg-
управляют потоком Trp по-разному,
путями в зависимости от диеты и состояния клеточного метаболизма
. В условиях низкого потребления Trp-
уровни циркулирующих Trp снижаются и эн-
ферментов, которые направляют Trp на не-NAD
+
биосинтетические маршруты
, подавляются, что свидетельствует о сдвиге
. всех возможных катаболизма Trp до поколения NAD
+
(75).Добавление больших количеств
Trp обеспечивает больший поток в окислительную ветвь
и позволяет повторно передавать увеличенные уровни Nam в сосудистую сеть (6, 9, 10). Считается, что весь Trp
, который достигает хинолината в печени, превращается
в NAD
+
посредством последующих ферментных реакций
Qprt, Nmnat1-3 и
Nadsyn1, которые высоко экспрессируются в печени
(24, 58).
Помимо печени (27), Qprt экспрессируется
в головном мозге человека и крысы и играет критическую роль
в защите от нейротоксических эффектов хинолината
(23, 45, 58, 93).Хинолинат представляет собой мощный эндогенный нейротоксин
, и повышенные уровни
в мозге связаны с генеративными расстройствами нейрод-
, включая эпилепсию и
болезнь Хантингтона (73, 74). Было обнаружено, что нормальная концентрация хинолината в головном мозге
находится в диапазоне от низкого до среднего наномолярного (37),
и активность Qprt возрастает в ответ на повышение уровня хинолината (25). ), предполагая защитную роль
.Наивысшие уровни лината хино-
обнаруживаются в селезенке, лимфатических узлах, ти-
mus и многих специфических типах иммунных клеток, а
повышаются после стимуляции иммунными активаторами
(57).
Активированные лимфоциты индуцируют экспрессию
Nampt (68), которая также экспрессируется в гладких мышечных клетках
с потерей экспрессии в сен-
центрах (87). Было показано, что у мышей Nampt
циркулирует и высоко экспрессируется
внутриклеточно в коричневой жировой ткани, печени,
и почках, с жиром в качестве источника внеклеточного
Nampt.Человеческий жир также является источником циркулирующего налета (66). Из классических исследований кормления
было обнаружено, что семенники используют Nam, а не
Na или хинолинат (50), а кровь и печень были
, также было обнаружено, что основные места использования Nam
(41). Nam пересекает гематоэнцефалический барьер, и
преобразуется в NAD
+
в головном мозге, хотя не известно, является ли NAM предшественником NAD
+
в нейрональных или ненейронных клетках (78 ).Исследования
с нейронами DRG предполагают, что Nampt
не экспрессируется в нейронах (71). Nam and NR
122 Bogan
·
Brenner
Annu. Rev. Nutr. 2008. 28: 115-130. Загружено с arjournals.annualreviews.org
Дартмутским колледжем 23.09.08. Только для личного пользования.
Ниацин значительно увеличивает НАД + в испытаниях на людях |
Исследователи завершили испытание на людях ниацина, очень старого витамина, открытого более 80 лет назад, и показали, что он может увеличивать присутствие энергетического соединения, необходимого для функционирования клеток.
Ниацин и НАД +
Ниацин — это форма водорастворимого витамина B3, известная с тех пор, как американский биохимик Конрад Эльвехем идентифицировал его в 1937 году. Изначально ниацин назывался никотиновой кислотой, потому что он может быть получен путем окисления никотина азотной кислотой. Однако люди знают, что никотин вызывает привыкание в табаке, поэтому было принято название ниацин, которое происходит от слов NI cotinic AC id vitam IN .
В последние годы наблюдается значительный интерес к добавкам, которые способны повышать уровень НАД +, и ниацин является одной из таких добавок, которые могут это сделать.Биология НАД + играет важную роль в энергетическом метаболизме, поэтому, прежде чем мы погрузимся в результаты нового исследования на людях, которое мы хотим осветить сегодня, мы должны обсудить НАД + и его важность в контексте метаболизма и старения.
Никотинамидадениндинуклеотид (НАД) представляет собой кофермент, обнаруженный во всех живых клетках. Это динуклеотид, что означает, что он состоит из двух нуклеотидов, соединенных своими фосфатными группами. Один нуклеотид содержит основание аденина, а другой — никотинамид.
В метаболизме НАД способствует окислительно-восстановительным реакциям, перенося электроны от одной реакции к другой. Это означает, что НАД находится в клетке в двух формах; НАД + — это окислитель, который забирает электроны у других молекул и превращается в восстановленную форму НАДН. Затем НАДН может стать восстановителем, который отдает переносимые им электроны. Перенос электронов является одной из основных функций NAD, хотя он также выполняет другие клеточные процессы, в том числе действует как субстрат для ферментов, которые добавляют или удаляют химические группы из белков в посттрансляционных модификациях.
НАД + создается из простых строительных блоков, таких как аминокислота триптофан, и создается более сложным образом путем приема пищи, содержащей никотиновую кислоту (ниацин) или другие предшественники НАД +. Эти различные пути в конечном итоге перерабатываются в путь спасения, который рециркулирует их обратно в активную форму NAD +.
Старый дом сдан в новую аренду
Результаты нового испытания на людях с использованием ниацина пролили новый свет на его роль в биологии НАД + [1].
Участникам испытания давали постоянно возрастающую дозу ниацина, начиная с 250 мг / день до 750-1000 мг / день в течение 4-месячного периода, а затем в течение 10-месячного периода последующего лечения. Участники были разделены на исследуемую группу лиц с митохондриальной миопатией и контрольную группу здоровых людей соответствующего возраста, состоящую из двух здоровых людей на каждого пациента с митохондриальной миопатией. Все участники исследования получали один и тот же режим приема добавок ниацина.
Исследователи сообщают, что лечение ниацином увеличивало уровень NAD + в мышцах в 1,3 раза через 4 месяца и в 2,3 раза через 10 месяцев в исследуемой группе. В контрольной группе не наблюдалось увеличения НАД +, что позволяет предположить, что его уровни строго контролируются в ткани скелетных мышц и будут увеличиваться только у пациентов, страдающих от более низких, чем нормальный, уровней НАД +, наблюдаемых в таких условиях, как митохондриальная миопатия и потенциально старение, которое также влияет на функцию митохондрий. Это также важно, так как до этого исследования было неизвестно, улучшило ли добавление ниацина НАД + в мышцах или он отфильтровывался и просто повышал НАД + в печени.
Уровень NAD + в цельной крови также увеличивался при добавлении в 7,1 раза в исследуемой группе и в 5,7 раза в контрольной группе через 4 месяца по сравнению с исходным уровнем участников. Через 10 месяцев рост был в 8,2 раза по сравнению с исходным уровнем. Это показывает, что добавки ниацина не просто отфильтровываются печенью; фактически, они достигают кровотока в значительных количествах, повышая там уровень НАД +.
Добавка ниацина также улучшает композицию тела.Участники отметили снижение процента жира в организме в контрольной группе и увеличение мышечной массы как в контрольной, так и в исследуемой группах. После 10 месяцев приема ниацина пациенты продемонстрировали улучшение мышечной силы.
Исследователи также заметили, что печеночный жир уменьшился вдвое, а висцеральный жир — на четверть. Оба эти типа жировых отложений связаны с повышенным риском метаболического синдрома. Таким образом, хотя ниацин не влиял на поверхностный жир вокруг тела, он оказывал значительное влияние на нездоровый жир, окружающий органы.
Наконец, ниацин был связан с повышением уровня глюкозы в крови, что является фактором риска развития таких состояний, как диабет. Результаты исследования показали, что ниацин действительно повышал уровень глюкозы натощак как в исследуемой, так и в контрольной группах после 4 месяцев приема добавок. Однако гликозилированный гемоглобин, который отражает долгосрочные уровни глюкозы, не пострадал.
Итак, хотя, согласно результатам этого исследования, ниацин действительно повышает уровень глюкозы, его преимущества, по-видимому, значительно перевешивают любые отрицательные стороны, которые может иметь небольшое повышение уровня глюкозы, как подтверждают другие исследования [2].
Другой побочный эффект, отмеченный после 4 месяцев приема ниацина, заключался в том, что у участников наблюдалось небольшое снижение концентрации гемоглобина; однако во время исследования он никогда не опускался ниже нормальных значений для здоровых.
НАД + представляет собой окислительно-восстановительный метаболит, истощение которого, как предполагалось, способствует старению и дегенеративным заболеваниям у грызунов. Однако вопрос о том, происходит ли истощение НАД + у пациентов с дегенеративными расстройствами и улучшает ли их симптомы восполнение НАД +, остается открытым.Здесь мы сообщаем о системном дефиците NAD + у взрослых пациентов с митохондриальной миопатией. Мы вводили возрастающую дозу NAD + -бустера ниацина, формы витамина B3 (до 750–1000 мг / день; Clinicaltrials.gov NCT03973203) для пациентов и их контрольной группы в течение 10 или 4 месяцев соответственно. NAD + в крови увеличился у всех субъектов до 8 раз, а NAD + в мышцах пациентов достиг уровня их контроля. У некоторых пациентов наблюдалась тенденция к анемии, в то время как мышечная сила и митохондриальный биогенез увеличивались у всех испытуемых.У пациентов метаболом мышц сместился в сторону контроля, а жир в печени уменьшился даже на 50%. Наши данные показывают, что анализ крови полезен для выявления дефицита NAD + и указывает на то, что ниацин является эффективным усилителем NAD + для лечения митохондриальной миопатии.
Заключение
Эти результаты дают пищу для размышлений, когда мы рассматриваем биологию НАД + в контексте метаболизма и старения. Цена на другие добавки-предшественники, которые могут повышать НАД + у людей, такие как NR и NMN, очень высоки по сравнению с ниацином, который дешев и легко доступен.Эти результаты показывают, что ниацин может повышать уровень НАД + человека в мышцах и крови, а также потенциально в других тканях.
Излишне говорить, что, хотя эти результаты интригуют, мы не одобряем использование добавок или каких-либо продуктов или поставщиков добавок, и все обсуждения здесь имеют научный интерес.
| ПОМОГИТЕ РАСПРОСТРАНЯТЬ СЛОВО |
| Пожалуйста, свяжитесь с нами в социальных сетях , ставьте лайки и делитесь нашим контентом, а также помогите нам создать массовую поддержку для продления здоровой жизни: |
| Спасибо! |
Литература
[1] Пиринен, Э., Ауранен, М., Хан, Н.А., Брилханте, В., Урхо, Н., Пессия, А.,… и Хаймилахти, К. (2020). Ниацин излечивает системный дефицит NAD + и улучшает работу мышц при митохондриальной миопатии у взрослых. Клеточный метаболизм.
[2] Голдберг, Р. Б., и Якобсон, Т. А. (2008, апрель). Влияние ниацина на контроль глюкозы у пациентов с дислипидемией. В Трудах клиники Мэйо (Том 83, № 4, стр. 470-478). Эльзевир.
ниацина против никотинамида — We Are Feel
Какие формы витамина B3 существуют?
В добавках витамин B3 обычно бывает в следующих формах:
- ниацин
- никотинамид
- никотинамид рибозид
В чем разница?
Большинство людей связывают витамина B3, с ниацином , но никотиновая кислота на самом деле не является той формой, которую естественный витамин B принимает в вашем организме.Будь то под прикрытием ниацина, никотинамида или амида никотинамида, ваше тело неизбежно преобразует витамин B, который вы принимаете в добавках, в никотинамидадениндинуклеотид (НАД). То, как ваше тело превращает диетический витамин B в NAD, имеет решающее значение.
Никотинамид, также известный как ниацинамид, представляет собой амид никотиновой кислоты, широко известный как ниацин. Никотинамид рибозид (NR), с другой стороны, представляет собой химически измененную форму никотинамида, которая имеет уникальные свойства.Однако NR имеет ограниченное применение, поэтому большинство добавок с витамином B3 содержат никотинамид или ниацин.
Выводов:
- Ниацин представляет собой окисленную форму никотина, которую организм может преобразовать в NAD
- Никотинамид представляет собой амид ниацина, который более похож на НАД и имеет меньше побочных эффектов
- Никотинамид рибозид представляет собой синтетическую форму никотинамида с различными свойствами
Почему витамин B3 в форме
никотинамида лучше?Никотинамид больше похож на НАД, чем на ниацин, что может объяснить, почему этот тип витамина B3 имеет такой минимальный профиль побочных эффектов.Хотя пеллагра, медицинский термин, обозначающий дефицит витамина B3, встречается редко, лечение этого состояния ниацином вызывает необъяснимое покраснение кожи. Это покраснение не кажется вредным, но вызывает беспокойство, когда оно происходит. Никотинамид не вызывает покраснения кожи, но, как и другие формы витамина B3, он может быть вредным в высоких дозах. Проконсультируйтесь с врачом, если вы подозреваете, что страдаете пеллагрой.
Похоже, что витамин B3 в никотинамидной форме имеет дополнительное преимущество при лечении прыщей.Никотинамид от прыщей обычно актуален, но есть основания полагать, что пероральный прием этой формы витамина B3 также может уменьшить симптомы этого кожного заболевания.
В целом, организм обрабатывает никотинамид лучше, чем ниацин, поскольку он более похож на НАД, что приводит к большей биодоступности. Независимо от того, в какой форме он находится, витамин B3 растворим в воде, а это означает, что он не задерживается в организме надолго. Когда дело доходит до питательных веществ, которые вам нужно пополнять каждый день, очень важно придерживаться лучших форм добавок.
Хотя NR может иметь некоторые дополнительные преимущества, помимо тех, которые предлагает никотинамид, этому типу витамина B3 также явно не хватает некоторых полезных качеств вещества его происхождения. Никотинамид — самый безопасный и надежный пероральный катализатор производства НАД в организме.
Выводов:
- Как простое производное никотина, никотиновая кислота , по-видимому, имеет серьезные побочные эффекты
- Никотинамид представляет собой амид ниацина, что означает, что его форма больше похожа на НАД, чем на любой другой тип витамина B3
- Необходимо провести дополнительные исследования для NR , чтобы определить его преимущества по сравнению с никотинамидом
Почему мы используем витамин B3
никотинамид вместо других форм?Существует множество качеств, которые могут определять относительную ценность различных форм добавки.Будь то биодоступность или безопасность производства, важно принять во внимание все соответствующие факторы, прежде чем выбирать конкретную форму питательного вещества. Когда дело доходит до перехода с ниацина на никотинамид, ваша безопасность является нашим главным мотиватором.
Похоже, что побочные эффекты ниацина незначительны и проявляются только при высоких дозах. В то же время к любому веществу, вызывающему побочные эффекты, связанные с этой формой витамина B3, следует относиться с осторожностью.С нашим мультивитамином Feel Multivitamin ™ мы делаем следующий шаг вперед, обеспечивая вашу NRV витамина B3 никотинамидом вместо ниацина. Зачем придерживаться всего остального, если можно получить лучшее?
.