Живот
ГРАНИЦЫ, ОБЛАСТИ И ОТДЕЛЫ ЖИВОТА
Сверху живот ограничен реберными дугами, снизу — подвздошными гребнями, паховыми связками и верхним краем лонного сращения. Боковая граница живота проходит по вертикальным линиям, соединяющим концы XI ребер с передневерхними остями.
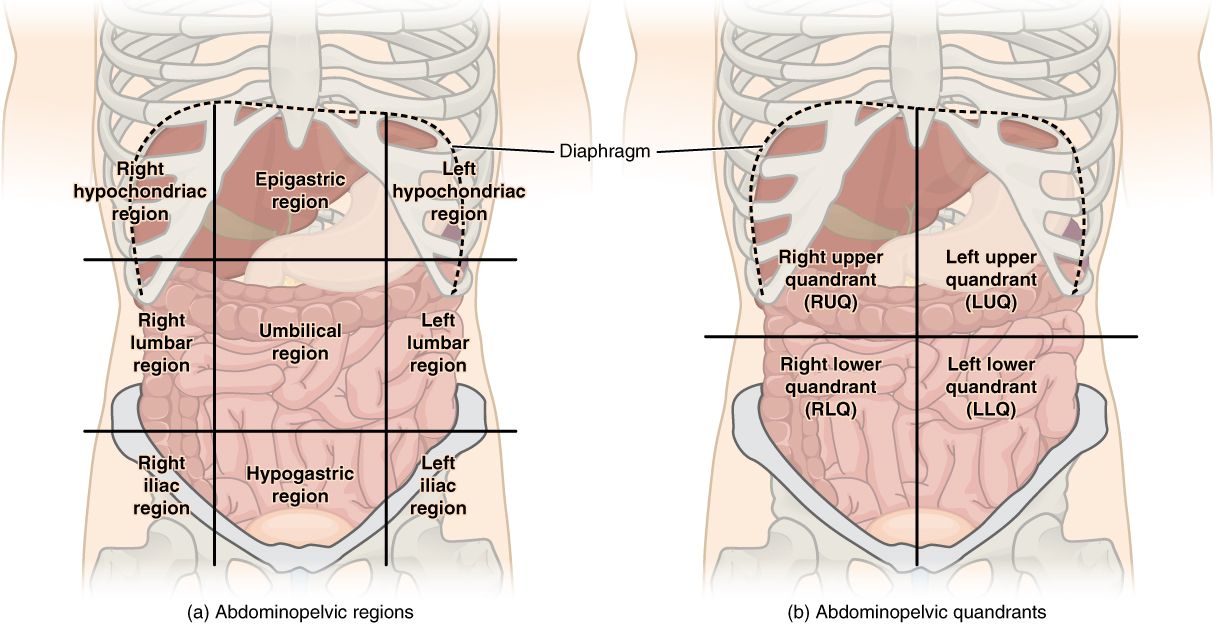
Двумя горизонтальными линиями живот делится на три отдела: надчревье (эпигастрий), чревье (мезогастрий) и подчревье (гипогастрий). Наружные края прямых мышц живота идут сверху вниз и разделяют каждый отдел на три области.
Рис. 15.1. Деление живота на отделы и области:
1 — проекция купола диафрагмы;
2 — linea costarum; 3 — linea spmarum; а — надчревье; б — чревье; в — подчревье; I — собственно эпигастральная область; II и III — правая и левая подреберные области; V — пупочная область; IV и VI — правая и левая боковая области; VIII — надлобковая область; VII и IX — подвздошнопаховые области
ПЕРЕДНЕБОКОВАЯ БРЮШНАЯ СТЕНКА
Переднебоковая
брюшная стенка — комплекс мягких тканей,
расположенных в пределах границ живота
и прикрывающих брюшную полость.
Проекция органов на переднебоковую брюшную стенку
В правую подреберную область проецируются печень (правая доля), часть желчного пузыря, печеночный изгиб ободочной кишки, правый надпочечник, часть правой почки.
В собственно надчревную область проецируются левая доля печени, часть желчного пузыря, часть тела и пилорический отдел желудка, верхняя половина двенадцатиперстной кишки, двенадцатиперстно- тощекишечный переход (изгиб), поджелудочная железа, части правой и левой почек, аорта с чревным стволом, чревное сплетение, небольшой участок перикарда, нижняя полая вена.
В левую подреберную область проецируются дно, кардия и часть тела желудка, селезенка, хвост поджелудочной железы, часть левой почки и часть левой доли печени.
В правую боковую область живота проецируются восходящая ободочная кишка, часть подвздошной кишки, часть правой почки и правый мочеточник.
В
пупочную область проецируются часть
желудка (большая кривизна), поперечная
ободочная кишка, петли тощей и подвздошной
кишки, часть правой почки, аорта, нижняя
полая вена.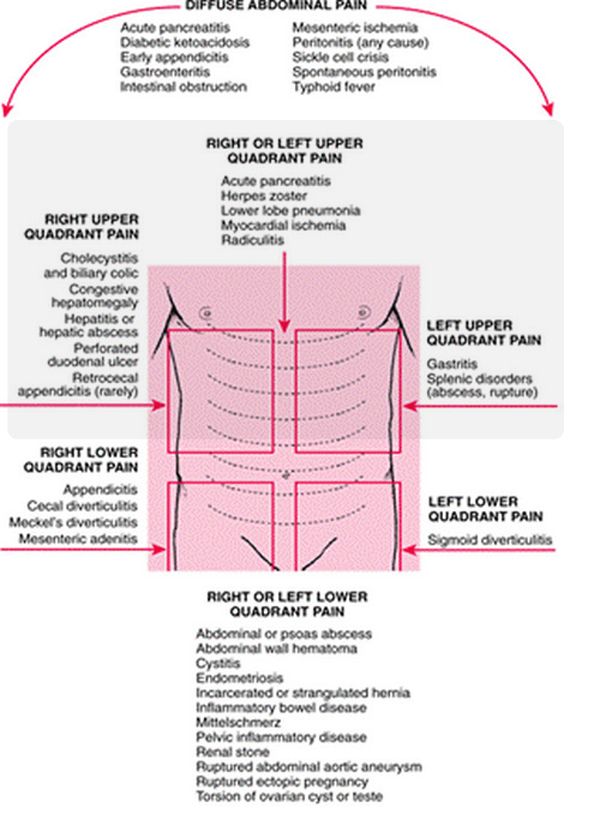
В левую боковую область живота проецируются нисходящая ободочная кишка, петли тощей кишки, левый мочеточник.
В правую подвздошно-паховую область проецируются слепая кишка с червеобразным отростком и конечный отдел подвздошной кишки.
В надлобковую область проецируются петли тощей и подвздошной кишок, мочевой пузырь в наполненном состоянии, часть сигмовидной кишки (переход в прямую).
В левую подвздошно-паховую область проецируются сигмовидная кишка и петли тощей и подвздошной кишки.
Матка в норме не выступает за верхний край лобкового симфиза, но при беременности в зависимости от срока может проецироваться в надлобковую, пупочную или эпигастральную область.
Топография слоев и слабых мест переднебоковой брюшной стенки
Кожа области подвижная, эластичная, что позволяет использовать ее в пластических целях при пластике дефектов лица (метод филатовского стебля). Волосяной покров развит достаточно хорошо.
Подкожная
жировая клетчатка разделена поверхностной
фасцией на два слоя, степень развития
ее может быть различной у разных людей. В области пупка клетчатка практически
отсутствует, вдоль белой линии развита
слабо.
В области пупка клетчатка практически
отсутствует, вдоль белой линии развита
слабо.
Поверхностная фасция состоит из двух листков — поверхностного и глубокого (фасция Томпсона). Глубокий листок гораздо прочнее и плотнее поверхностного и прикрепляется к паховой связке.
Собственная фасция покрывает мышцы живота и срастается с паховой связкой.
Наиболее поверхностно располагается наружная-косая мышца живота. Она состоит из двух частей: мышечной, расположенной более латерально, и апоневротической, лежащей кпереди от прямой мышцы живота и участвующей в формировании влагалища прямой мышцы. Нижний край апоневроза утолщается, подворачивается вниз и внутрь и формирует паховую связку.
Более
глубоко располагается внутренняя косая
мышца живота. Она также состоит из
мышечной и апоневротической части,
однако апоневротическая часть имеет
более сложное строение. Апоневроз имеет
продольную щель, расположенную на уровне
около 2 см ниже пупка (линия Дугласа, или
дугообразная). Выше этой линии апоневроз
состоит из двух листков, один из которых
располагается кпереди от прямой мышцы
живота, а другой — кзади от нее. Ниже
линии Дугласа оба листка сливаются друг
с другом и располагаются кпереди от
прямой мышцы.
Ниже
линии Дугласа оба листка сливаются друг
с другом и располагаются кпереди от
прямой мышцы.
Прямая мышца живота располагается в средней части живота. Волокна ее направлены сверху вниз. Мышца разделена 3-6 сухожильными перемычками и лежит в собственном влагалище, сформированном за счет апоневрозов внутренней и наружной косых и поперечной мышц живота. Передняя стенка влагалища представлена апоневрозом
наружной косой и частично внутренней косой мышц живота. Она рыхло отделена от прямой мышцы, но срастается с ней в области сухожильных перемычек. Задняя стенка сформирована за счет апоневроза внутренней косой (частично), поперечной мышц живота и внутрибрюшной фасции и нигде с мышцей не срастается, формируя клетчаточное пространство, в котором проходят верхние и нижние надчревные сосуды. При этом соответствующие вены в области пупка соединяются друг с другом и формируют глубокую венозную сеть. В ряде случаев прямая мышца живота снизу подкрепляется пирамидальной мышцей.
Поперечная
мышца живота лежит глубже всех остальных.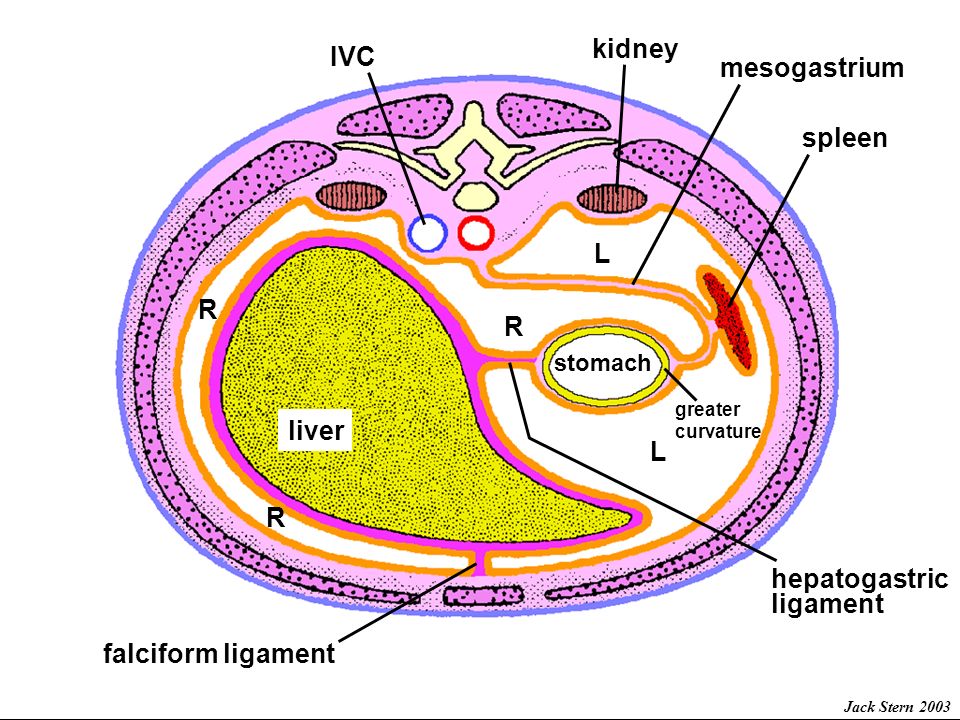
Соответственно линии Дугласа апоневроз поперечной мышцы живота также расщепляется: выше этой линии он проходит под прямой мышцей живота и участвует в формировании задней стенки влагалища прямой мышцы, а ниже линии участвует в формировании передней стенки влагалища.
Под поперечной мышцей располагается внутрибрюшная фасция, которая в рассматриваемой области носит название поперечной (по мышце, на которой лежит).
Необходимо
отметить, что апоневрозы левых и правых
косых и поперечных мышц живота по средней
линии срастаются друг с другом, формируя
белую линию живота. Учитывая относительную
бедность сосудами, наличие связи между
всеми слоями и достаточную прочность,
именно белая линия живота является
местом наиболее быстрого хирургического
доступа при вмешательствах на внутренних
органах живота.
Полость живота— самая большая полость организма человека. Сверху брюшная полость ограничена диафрагмой, внизу она продолжается в полость малого таза, спереди и с боков ограничена мышцами живота, сзади — мышцами поясницы и соответствующим отделом позвоночного столба. Внутренняя поверхность брюшной полости выстлана забрюшинной фасцией, жировой клетчаткой и париетальной брюшиной.
Полость живота подразделяется на брюшинную полость и забрюшинное пространство. Брюшинную полость ограничивает париетальный листок брюшины. Забрюшинное пространство — часть полости живота, лежащая между париетальной фасцией живота у ее задней стенки и париетальной брюшиной.
Брюшина
— серозная оболочка, покрывающая изнутри стенки полости живота (париетальная брюшина) или поверхность внутренних органов (висцеральная брюшина). Оба листка брюшины, переходя один в другой, образуют замкнутое пространство, представляющее собой брюшинную полость. В норме эта полость представляет собой узкую щель, заполненную небольшим количеством серозной жидкости, играющей роль смазки для облегчения движений органов брюшной полости относительно стенок или друг друга. Количество
серозной жидкости обычно не превышает
25—30 мл, давление приблизительно равно
атмосферному.
Количество
серозной жидкости обычно не превышает
25—30 мл, давление приблизительно равно
атмосферному.Лапаротомия (чревосечение) – обязательный этап всех операций на органах брюшной полости. В одних случаях она служит доступом к определенному органу или патологическому процессу, в других — используется для ревизии органов брюшной полости с целью исключения повреждения внутренних органов или определения возможности операции при опухолевом процессе.
Доступы. Чаше всего используют разрез по средней линии живота — срединную лапаротомию.
При
верхнесрединной лапаротомии, т. е.
разрезе по средней линии выше пупка,
рассекают кожу, подкожную клетчатку,
апоневроз (или белую линию живота),
предбрюшинную клетчатку и брюшину.
Этот разрез обеспечивает доступ к
органам верхнего этажа брюшной полости.
Нижнесрединный разрез также проходит
по белой линии, однако после рассечения
белой линии, которая ниже пупка очень
узка, нередко приходится использовать
для отведения краев прямых мышц
пластинчатые крючки Фарабефа.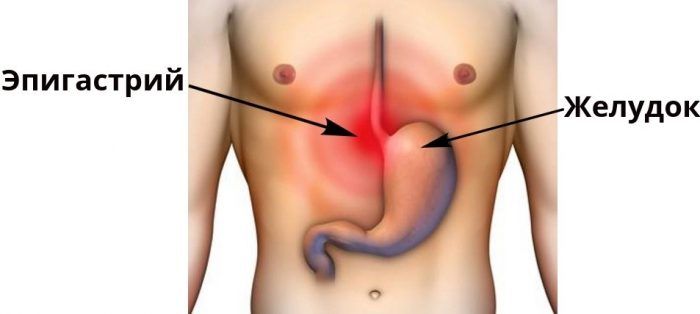 Разрез
обеспечивает доступ к кишечнику и
органам малого таза. При среднесрединной
лапаротомии разрез начинают выше пупка,
обходит пупок слева и кончается ниже
его на 3-4 см. Этот доступ предназначен
для ревизии всей брюшной полости: при
необходимости он может быть продлен
вверх или вниз.
Разрез
обеспечивает доступ к кишечнику и
органам малого таза. При среднесрединной
лапаротомии разрез начинают выше пупка,
обходит пупок слева и кончается ниже
его на 3-4 см. Этот доступ предназначен
для ревизии всей брюшной полости: при
необходимости он может быть продлен
вверх или вниз.
Пути распространения гноя в брюшной полости при перитоните (схема)
Перитонеальный
экссудат может распространяться из
правого подреберья в правую поддиафрагмальную
полость или проникнуть через правый
боковой канал в подвздошную ямку и
спуститься в таз. При прогрессировании
процесса и накоплении экссудата гной
продвигается по левому латеральному
каналу в левую поддиафрагмальную полость
(рис. 95). Значительные изменения
происходят в кровеносных и лимфатических
сосудах кишечника, сальнике и
прилегающих тканях и органах. Вначале
сосуды переполняются кровью, затем
появляются тромбы. Этот процесс может
перейти на крупные венозные стволы
и даже воротную вену. Резвившийся в этих
случаях гнойный тромбофлебит приводит
к образованию множественных абсцессов
печени.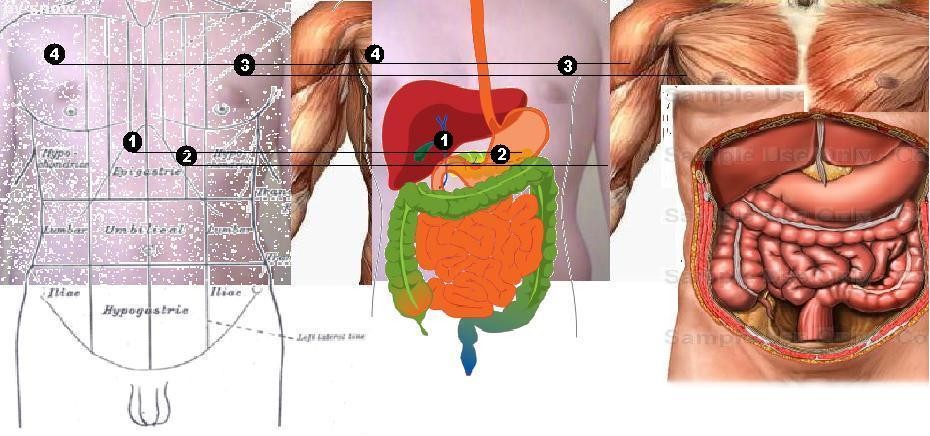 Поражение гнойным процессом
лимфатических сосудов и узлов ведет к
брыжеечным и забрюшинным лимфангитам
и лимфаденитам.
Поражение гнойным процессом
лимфатических сосудов и узлов ведет к
брыжеечным и забрюшинным лимфангитам
и лимфаденитам.
Понятие рационального дренирования брюшной полости включает в себя комплекс приемов, обеспечивающих беспрепятственный отток жидкости из брюшной полости. Прежде всего имеется в виду обеспечение оттока гноя при перитоните — первостепенная задача лечения любого гнойного процесса.
Успешное дренирование брюшной полости возможно лишь при соблюдении условий: дренаж должен стоять в местах скопления жидкости, быть проходимым. Его устанавливают в отлогих участках брюшной полости и некоторых ее карманах, а больному рекомендуют положение в постели, способствующее наилучшему дренированию. При перитоните, как правило, показано возвышенное положение, в ряде случаев требуется положение на боку, спине. Сложнее обеспечить проходимость дренажа. В целях дренирования широко распространено введение резиновых трубочных дренажей, а также дренажей из синтетических материалов.
Страница не найдена
Размер:
AAA
Цвет: C C C
Изображения
Вкл. Выкл.
Выкл.
Обычная версия сайта
RUENBY
Гомельский государственный
медицинский университет
- Университет
- Университет
- История
- Руководство
- Устав и Символика
- Воспитательная деятельность
- Организация образовательного процесса
- Международное сотрудничество
- Система менеджмента качества
- Советы
- Факультеты
- Кафедры
- Подразделения
- Первичная профсоюзная организация работников
- Издания университета
- Гордость университета
- Выпускник-2021
- Первичная организация «Белорусский союз женщин»
- Одно окно
- ГомГМУ в международных рейтингах
- Структура университета
- Абитуриентам
- Приёмная комиссия
- Целевая подготовка
- Заключение, расторжение «целевого» договора
- Льготы для молодых специалистов
- Архив проходных баллов
- Карта и маршрут проезда
- Порядок приёма на 2022 год
- Специальности
- Контрольные цифры приёма в 2022 году
- Стоимость обучения
- Информация о ходе приёма документов
- Приём документов и время работы приёмной комиссии
- Порядок приёма граждан РФ, Кыргызстана, Таджикистана, Казахстана
- Pепетиционное тестирование
- Горячая линия по вопросам вступительной кампании
- Студентам
- Первокурснику
- Расписание занятий
- Расписание экзаменов
- Информация для студентов
- Студенческий клуб
- Спортивный клуб
- Общежитие
- Нормативные документы
- Практика
- Стоимость обучения
- Безопасность жизнедеятельности
- БРСМ
- Профком студентов
- Учебный центр практической подготовки и симуляционного обучения
- Многофункциональная карточка студента
- Анкетирование студентов
- Выпускникам
- Интернатура и клиническая ординатура
- Докторантура
- Аспирантура
- Магистратура
- Распределение
- Врачам и специалистам
- Профессорский консультативный центр
- Факультет повышения квалификации и переподготовки
- Иностранным гражданам
- Факультет иностранных студентов
- Стоимость обучения
- Регистрация и визы
- Полезная информация
- Правила приёма
- Информация о возможностях и условиях приема в 2022 году
- Официальные представители ГомГМУ по набору студентов
- Страхование иностранных граждан
- Приём на Подготовительное отделение иностранных граждан
- Прием иностранных граждан для обучения на английском языке / Training of foreign students in English
- Повышение квалификации и переподготовка для иностранных граждан
- Научная деятельность
- Направления научной деятельности
- Научно-педагогические школы
- Студенчеcкое научное общество
- Инновационные технологии в ГомГМУ
- Научно-исследовательская часть
- Научно-исследовательская лаборатория
- Конкурсы, гранты, стипендии
- Работа комитета по этике
- Научные мероприятия
- В помощь исследователю
- Диссертационный совет
- «Горизонт Европа»
- Патенты
- Инструкции на метод
- Совет молодых ученых
- Госпрограмма (ЧАЭС)
- Главная
Распространенность абдоминальной боли среди студентов
В данной статье авторы провели исследование распространенности абдоминальной боли среди студентов, детализацию болевого синдрома, разбор, принимаемых студентами лекарственных средств для купирования болевого синдрома, обозначили проблемы диагностики причин абдоминальной боли.
Ключевые слова :боль, болевой синдром, абдоминальная боль, студенты.
Введение
Синдром абдоминальной боли является одним из наиболее распространенных клинических синдромов. Причем около половины всех абдоминальных болей связаны с острыми или хроническими заболеваниями кишечника [3]. Боль в животе является особенно актуальной для студентов, так как обучение в высшем образовательном учреждении требует от студента больших эмоциональных и физических затрат. Также на обучающегося действуют такие факторы, как проживание вне дома, необходимость в самостоятельной организации питания, проведении своего досуга, умение преодолевать сложные жизненные ситуации самостоятельно. Не все студенты благополучно справляются со всеми организационными аспектами своей жизни, что зачастую негативно отражается на их здоровье. Так, наиболее частым симптомом, говорящим о функциональных или органических изменениях ряда органов и систем, является абдоминальная боль.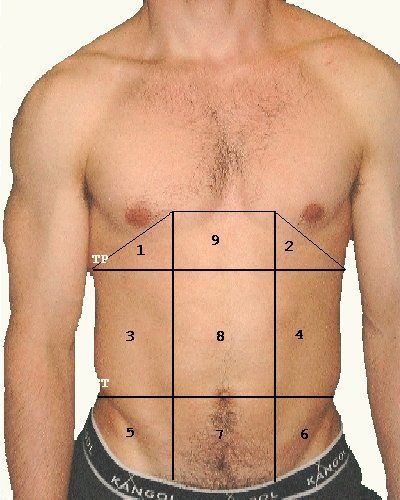 Но определение распространенности абдоминальной боли у населения, как правило, проводится на основании анализа амбулаторных и стационарных медицинских карт, что не может дать полной и достоверной информации о фактической эпидемиологии абдоминальной боли, так как достаточна большая часть населения не обращается за медицинской помощью [1].
Но определение распространенности абдоминальной боли у населения, как правило, проводится на основании анализа амбулаторных и стационарных медицинских карт, что не может дать полной и достоверной информации о фактической эпидемиологии абдоминальной боли, так как достаточна большая часть населения не обращается за медицинской помощью [1].
Определение и классификация боли
Международная ассоциация по изучению боли (IASP) определяет симптом боли как: неприятное ощущение и эмоциональное переживание, связанное с действительным или возможным повреждением тканей; один из видов чувствительности, возникающих вследствие поступления в ЦНС патологических импульсов с периферии без единого универсального раздражителя. Абдоминальная боль представляет собой типовой патологический процесс, который лишен нозологической принадлежности [5].
Клинически абдоминальную боль можно классифицировать следующим образом: висцеральная, париетальная (соматическая), отраженная (иррадиирующая), психогенная.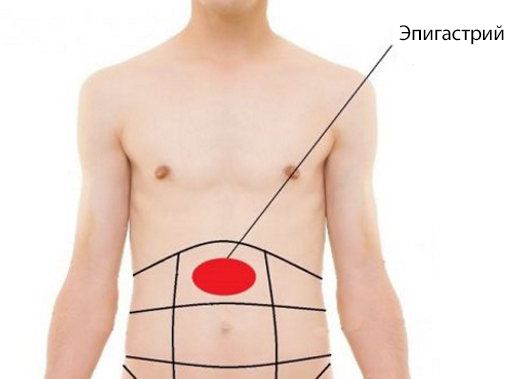 Висцеральная боль возникает при раздражении ноцицепторов органов брюшной полости. Париетальная боль возникает при перфорации и пенетрации органов. Психогенная боль возникает при отсутствии очага раздражения и ее характер определяется особенностями личности (наблюдается у лиц с психоэмоциональными нарушениями) [5]. По продолжительности и течению абдоминальные боли подразделяются на: острые (от нескольких часов до нескольких суток), подострые (от нескольких дней до 6 месяцев), хронические (6 месяцев и более) [6]. Хроническую боль можно также разделить на органическую и функциональную. По механизму возникновения различают следующие разновидности абдоминальной боли: спастическая, возникающая от спазмов гладкой мускулатуры желудочно-кишечного тракта; дистензионная, возникающая от растяжения полых органов брюшной полости, перитонеальная, связанная с патологическим процессом в брюшинном покрове; сосудистая, связанная с ишемией органов брюшной полости [7].
Висцеральная боль возникает при раздражении ноцицепторов органов брюшной полости. Париетальная боль возникает при перфорации и пенетрации органов. Психогенная боль возникает при отсутствии очага раздражения и ее характер определяется особенностями личности (наблюдается у лиц с психоэмоциональными нарушениями) [5]. По продолжительности и течению абдоминальные боли подразделяются на: острые (от нескольких часов до нескольких суток), подострые (от нескольких дней до 6 месяцев), хронические (6 месяцев и более) [6]. Хроническую боль можно также разделить на органическую и функциональную. По механизму возникновения различают следующие разновидности абдоминальной боли: спастическая, возникающая от спазмов гладкой мускулатуры желудочно-кишечного тракта; дистензионная, возникающая от растяжения полых органов брюшной полости, перитонеальная, связанная с патологическим процессом в брюшинном покрове; сосудистая, связанная с ишемией органов брюшной полости [7].
Проблемы диагностики
Очень большую сложность представляет диагностика, направленная на выявление причин абдоминальной боли. Грамотный сбор анамнеза, правильно проведенное физикальное обследование пациента, проведение дифференциальной диагностики, возможности дополнительных исследований позволяют сузить круг причин, вызвавших болевой синдром. Но при все при этом, у трети пациентов причины острых болей в животе даже после тщательного обследования остаются неясными [3]. Также ни в коем случае нельзя забывать, что под «маской» абдоминальной боли могут скрываться такие патологии как депрессия, анемия, инфекции мочевых путей и заболевания позвоночника [5,11]. Наличие хронической абдоминальной боли (как единственного симптома) может приводить к ненужным инвазивным диагностическим процедурам и началу медикаментозной терапии [2].
Грамотный сбор анамнеза, правильно проведенное физикальное обследование пациента, проведение дифференциальной диагностики, возможности дополнительных исследований позволяют сузить круг причин, вызвавших болевой синдром. Но при все при этом, у трети пациентов причины острых болей в животе даже после тщательного обследования остаются неясными [3]. Также ни в коем случае нельзя забывать, что под «маской» абдоминальной боли могут скрываться такие патологии как депрессия, анемия, инфекции мочевых путей и заболевания позвоночника [5,11]. Наличие хронической абдоминальной боли (как единственного симптома) может приводить к ненужным инвазивным диагностическим процедурам и началу медикаментозной терапии [2].
Материалы и методы
При помощи оригинальной анкеты было проведено собственное исследование распространенности абдоминальной боли среди студентов. Вопросы анкеты позволяли детализировать болевой синдром, узнать информацию о принимаемых лекарственных средствах, наличии хронических заболеваний, факте постановки на учет у врачей и прохождении медицинских обследований за последний год (см. рис. 1).
рис. 1).
Рис.1. Макет анкеты
Результаты исследования
В анкетировании приняли участие 75 студентов различных высших и средних учебных заведений и разных курсов, среди них было 32 (42,7 %) представителя мужского пола и 43 (57,3 %) женского, средний возраст опрошенных составил 20,9 лет, у восьми опрошенных также было проведено физикальное обследование-поверхностная пальпация живота по Василенко. Ввиду того, что полученные данные после опроса изобилуют различными вариантами и комбинациями ответов на вопросы, результаты анкетирования для большей наглядности и удобства представлены в виде таблицы (см. табл.1). В тексте будут рассмотрены наиболее часто встречаемые ответы.
Таблица 1
Распространенность абдоминальной боли среди студентов и детализация болевого синдрома
Испытываете ли вы боли в области живота? | Кратность болевого синдрома | Локализация боли | Условия возникновения болевого синдрома | Время появления болевого синдрома, в том числе прием пищи | Условия прекращения болевого синдрома | Характер боли |
Да-70 (93,3 %) Нет-5 (6,7 %) | Беспокоил однократно-15 (20 %) Беспокоит редко (1 раз в месяц)-36 (48 %) Беспокоит с умеренной частотой (1 раз в 5–7 дней)-14 (18,6 %) Беспокоит часто (практически ежедневно)-5 (6,7 %) Боли носят постоянный характер-0 Ответ не указан-5 (6,7 %) | Эпигастрий-11 (14,7 %) Мезогастрий-16 (21,3 %) Гипогастрий-16 (21,3 %) Эпигастрий+Гипогастрий-7 (9,3 %) Эпигастрий+Мезогастрий-7 (9,3 %) Мезогастрий+Гипогастрий-6 (8 %) Эпигастрий+Мезогастрий+ гипогастрий-4 (5,3 %) Ответ не указан-8 (10,7 %) | Физическая нагрузка-5 (6,7 %) Прием пищи-15 (20 %) В состоянии покоя-21 (28 %) Голод-14 (18,7 %) В состоянии покоя, голод-1 (1,3 %) Прием пищи, голод-9 (12 %) В состоянии покоя, голод, физическая нагрузка и прием пищи-1 (1,3 %) В состоянии покоя, голод и прием пищи-1 (1,3 %) Физическая нагрузка, прием пищи-1 (1,3 %) Ответ не указан-7 (9,3 %) | Сразу после приема пищи-10 (13,3 %) Через 20–30 минут после приема пищи-27 (36 %) Ночные боли-5 (6,7 %) Свой вариант-10 (13,3 %): Без видимых причин-2; после определенного положения; менструации; время суток: утро-день; после жирной пищи; на следующие сутки после приема пищи; при длительном голодании; до приема пищи. Через 20–30 минут после приема пищи, ночные боли-1 (1,3 %) Сразу после приема пищи, через 20–30 минут после приема пищи-1 (1,3 %) Сразу после приема пищи, через 20–30 минут после приема пищи, ночные боли-2 (2,7 %) Ответ не указан-19 (25,3 %) | Прием пищи-10 (13,3 %) Боль проходит сама-36 (48 %) Прием лекарственных препаратов-14 (18,7 %) Прием пищи, прием лекарственных препаратов-1 (1,3 %) Прием пищи, боль проходит сама-5 (6,7 %) Прием ЛС, боль проходит сама-3 (4 %) Ответ не указан-6 (8 %) | Жгучая-2 (2,7 %) Острая- 2 (2,7 %) Тупая-11 (14,7 %) Режущая-3 (4 %) Колющая-3 (4 %) Ноющая-18 (24 %) Режущая+ноющая-2 (2,7 %) Тупая+ноющая-4 (5,3 %) Тупая+режущая-2 (2,7 %) Острая+режущая-1 (1,3 %) Острая+тупая+ноющая-1 (1,3 %) Острая+ноющая-1 (1,3 %) Жгучая+ноющая-1 (1,3 %) Колющая+ноющая-5 (6,7 %) Жгучая+режущая+колющая-1 (1,3 %) Жгучая, острая-1 (1,3 %) Острая, колющая-2 (2,7 %) Жгучая, тупая, колющая, ноющая-1 (1,3 %) Режущая, колющая, ноющая-1 (1,3 %) Жгучая, тупая, колющая-1 (1,3 %) Жгучая, тупая, ноющая-1 (1,3 %) Тупая, колющая-1 (1,3 %) Тупая, колющая, ноющая-1 (1,3 %) Острая, колющая, ноющая-1 (1,3 %) Все варианты-1 (1,3 %) Свой вариант-Тянущая (1,3 %) Ответ не указан-6 (8 %) |
Таблица 2
Длительность болевого синдрома | Интенсивность болевого синдрома | Иррадиация боли | Наличие хронических заболеваний | Учет у врача | Прохождение медицинских обследований за последний год |
Несколько: Секунд-14 (18,7 %) Минут (10–15)-34 (45,3 %) Часов-16 (21,3 %) Минут-Часов-6 (8 %) Ответ не указан-5 (6,7 %) | Слабо-21 (28 %) Умеренно-43 (57,3 %) Сильно-3 (4 %) Умеренная боль и сильная боль-3 (4 %) Ответ не указан-5(8,7 %) | Нет-66(88 %) Иррадиирует в (4 %) 1-поясничную область 1-бедро, поясницу 1-в грудную область Ответ не указан-6 (8 %) | Да-14: (32 %) Нет-47 (62,7 %) Ответ не указан-4 (5,3 %) | Да-9 (22,7 %) Нет-54 (72 %) Ответ не указан-4 (5,3 %) | Да-26 (62,7 %) Нет-24 (32 %) Ответ не указан-4 (5,3 %) |
На вопрос “Испытываете ли вы боли в области живота?” 93,3 % ответили “да”, что свидетельствует о большой распространенности синдрома абдоминальной боли среди студентов. Большая часть-48 % испытывают боль редко-1 раз в месяц, боли в животе беспокоили однократно-20 %, беспокоят с умеренной частотой-18,6 %. Среди респондентов боль чаще локализуется в мезогастрии (21,3 %) и гипогастрии (21,3 %), реже в эпигастрии-14,7 %. Важно сказать, что локализация боли в нижней части живота чаще свидетельствует о патологии мочевыделительной системы, кишечника, органов малого таза. Причинами боли в эпигастрии могут быть патологические процессы как со стороны желудка, желчевыводящих путей, поджелудочной железы, так и со стороны сердечно-сосудистой системы [6]. Боль чаще возникала в состоянии покоя (без видимых причин)-28 %, при приеме пищи-20 % и при голодании-18,7 %. 36 % испытывали боль в животе через 20–30 минут после приема пищи.
Большая часть-48 % испытывают боль редко-1 раз в месяц, боли в животе беспокоили однократно-20 %, беспокоят с умеренной частотой-18,6 %. Среди респондентов боль чаще локализуется в мезогастрии (21,3 %) и гипогастрии (21,3 %), реже в эпигастрии-14,7 %. Важно сказать, что локализация боли в нижней части живота чаще свидетельствует о патологии мочевыделительной системы, кишечника, органов малого таза. Причинами боли в эпигастрии могут быть патологические процессы как со стороны желудка, желчевыводящих путей, поджелудочной железы, так и со стороны сердечно-сосудистой системы [6]. Боль чаще возникала в состоянии покоя (без видимых причин)-28 %, при приеме пищи-20 % и при голодании-18,7 %. 36 % испытывали боль в животе через 20–30 минут после приема пищи.
Необходимо заострить внимание на связи абдоминальной боли с приемом пищи. Абдоминальная боль тесно связана с характером питания и пищевыми привычкам [1]. Проблема качества питания широко распространена среди студентов. В эту проблему входят: нерегулярность питания, несбалансированность, низкое качество самих продуктов, недостаточная пищевая ценность продуктов.
Появление боли в животе без видимых причин может быть связано с синдромом функциональной абдоминальной боли (синонимы-«хроническая идиопатическая абдоминальная боль», «неспецифическая функциональная абдоминальная боль»), одним из критериев которого является отсутствие связи с конкретными физиологическими факторами (прием пищи, акт дефекации, менструальный цикл) [6].
У 48 % опрошенных болевой синдром проходит самостоятельно. У 13,3 % боль исчезает после приема пищи. И 18,7 % принимают лекарственные препараты для устранения болевого синдрома. Среди препаратов были выделены следующие: но-шпа, нурофен, найз, омепразол, де-нол, панкреатин, тримедат, одестон, кетарол, анальгин, имодиум.
Краткая характеристика лекарственных средств
Дротаверин (Но-шпа), тримебутин (тримедат) относятся к группе миотропных спазмолитиков [9]. Однако, не смотря на одну групповую принадлежность, они обладают разной фармакодинамикой. Дротаверин является ингибитором фосфодиэстеразы IV (ФДЭ IV). За счет подавления активности этого фермента происходит повышение количества цАМФ в клетке и инактивация киназы легкой цепи миозина, что в дальнейшем вызывает расслабление гладкой мускулатуры. За счет повышения концентрации цАМФ, происходит уменьшение количества внутриклеточных ионов Ca. Побочные эффекты отмечаются достаточно редко, но при длительном применении и в больших дозах могут наблюдаться тошнота, головокружение, тахикардия, гипотензия, запор, бессонница [5].
За счет подавления активности этого фермента происходит повышение количества цАМФ в клетке и инактивация киназы легкой цепи миозина, что в дальнейшем вызывает расслабление гладкой мускулатуры. За счет повышения концентрации цАМФ, происходит уменьшение количества внутриклеточных ионов Ca. Побочные эффекты отмечаются достаточно редко, но при длительном применении и в больших дозах могут наблюдаться тошнота, головокружение, тахикардия, гипотензия, запор, бессонница [5].
Тримебутин (тримедат) взаимодействует с опиатными рецепторами, расположенными на всем протяжении ЖКТ. Они находятся в нервных сплетениях кишечника — подслизистом Мейснеровском и межмышечном Ауербаховском. Выделяют 3 типа таких рецепторов: мю-, дельта- и каппа-. Мю- и дельта-рецепторы проводят возбуждающие импульсы, каппа-рецепторы — тормозящие импульсы. Тримебутин не обладает специфичностью по отношению к конкретному виду рецепторов и взаимодействует с мю-, каппа- и дельта-рецепторами. Таким образом, препарат оказывает двойственный регулирующий эффект. Взаимодействуя с мю- и дельта-рецепторами, он стимулирует моторику ЖКТ, а при связывании с каппа-рецепторами-угнетает. Тримебутин оказывает спазмолитическое или прокинетическое действие в зависимости от исходного состояния моторики ЖКТ [5].
Взаимодействуя с мю- и дельта-рецепторами, он стимулирует моторику ЖКТ, а при связывании с каппа-рецепторами-угнетает. Тримебутин оказывает спазмолитическое или прокинетическое действие в зависимости от исходного состояния моторики ЖКТ [5].
Важно отметить, что согласно клиническим рекомендациям Российской гастроэнтерологической ассоциации по ведению пациентов с абдоминальной болью, спазмолитики применяются для купирования висцеральной абдоминальной боли любого генеза и органического, и функционального, так как мышечный спазм является одним из ключевых механизмов, лежащих в основе висцеральной боли. Они не только купируют боль, но и способствуют восстановлению пассажа кишечного содержимого и улучшению кровоснабжения стенки органа [6]. Назначение спазмолитиков не сопровождается непосредственным вмешательством в механизмы болевой чувствительности, поэтому не «затушевывает» боли и не затрудняет диагностики острой хирургической патологии [5]. Но в настоящее время не имеется систематических доказательств использования спазмолитиков в том случае, когда абдоминальная боль вызвана воспалительными заболеваниями кишечника (неспецифический язвенный колит, болезнь Крона). Считается, что при данной патологии спазмолитики могут усугубить дисмотильность кишечника [2].
Считается, что при данной патологии спазмолитики могут усугубить дисмотильность кишечника [2].
Метамизол натрия (анальгин), кеторолак (кеторол) относятся к ненаркотическим анальгетикам периферического типа действия, ибупрофен (нурофен) относится к нестероидным противовоспалительным средствам (НПВП), неселективные ингибиторы ЦОГ I и ЦОГ II. Нимесулид (найз)-НПВП, ЦОГ II-преимущественные [9]. Их основной механизм действия связан с подавлением активности циклооксигеназ и прекращением синтеза медиаторов воспаления. Обладают обезболивающим, противовоспалительным и жаропонижающим действием.
Омепразол относится к блокаторам АТФ-азы (ингибиторы протонной помпы) [9]. Данный препарат эффективно подавляет секрецию соляной кислоты за счет необратимой блокады , -зависимой АТФазы обкладочных клеток желудка [10].
Висмута трикалия дицитрат (Де-нол) является гастропротектором, средства механической защиты слизистой оболочки, препараты висмута [9]. Представляет собой коллоидный препарат висмута, образующий в кислой среде защитную пленку на поверхности эрозий и язв за счет денатурации белков поверхности язвы. Стимулируя образование простагландина Е2, увеличивает выработку защитной слизи. Угнетает развитие H. Pylori [10].
Стимулируя образование простагландина Е2, увеличивает выработку защитной слизи. Угнетает развитие H. Pylori [10].
Панкреатин относится к ферментным препаратам (средства заместительной терапии [9]. Является препаратом поджелудочной железы крупного рогатого скота, содержащий в 1 г по 25 тыс. ЕД амилазы и протеазы и 200 ЕД липазы [10].
Лоперамид (Имодиум) относится к антидиарейным средствам [9]. Является синтетическим агонистом опиоидных рецепторов [10].
Гимекромон (Одестон) относится к желчегонным препаратам. Увеличивает образование и выделение желчи. Оказывает селективное спазмолитическое действие в отношении желчных протоков и сфинктера Одди (не снижает перистальтику желудочно-кишечного тракта (ЖКТ) и артериальное давление (АД). Уменьшает застой желчи, предупреждает кристаллизацию холестерина и тем самым развитие холелитиаза [12].
По своему характеру боль, среди опрошенных, чаще была тупой (14,7 %), а по своей интенсивности-умеренной (57,3 %). Чаще всего болевой синдром длился 10–15 минут (45,3 %) и в 88,8 % боль не сопровождалась иррадиацией. В 4 % случаев боль иррадировала в: поясничную область, бедро, область груди. У 26,7 % опрошенных болевой синдром сопровождался дополнительными клиническими проявлениями в виде: тошноты (в некоторых случаях присутствовала рвота)-55 %, вздутия-15 %, головной боли, снижении работоспособности, слабости, сонливости, диареи-30 %.
В 4 % случаев боль иррадировала в: поясничную область, бедро, область груди. У 26,7 % опрошенных болевой синдром сопровождался дополнительными клиническими проявлениями в виде: тошноты (в некоторых случаях присутствовала рвота)-55 %, вздутия-15 %, головной боли, снижении работоспособности, слабости, сонливости, диареи-30 %.
У 62,7 % студентов отсутствовали хронические заболевания, у 32 % были следующие, хронические заболевания: гастрит (62,5 %), бронхиальная астма, хронический пиелонефрит, гастродуоденит, хронический тонзиллит, фиброаденома, расстройства вегетативной нервной системы, мочекаменная болезнь, гипотиреоз-37,5 % (причем эти заболевания разделяются поровну). На учете у врачей состоят 22,7 %. 62,7 % проходили медицинские обследования за последний год, причем преобладали медицинские осмотры, связанные с прохождением практики и приемом на работу.
При проведении физикального обследования-поверхностная пальпация живота по Василенко, у 7 из 8 человек никаких изменений выявлено не было. Живот был мягкий, безболезненный, тонус мышц передней брюшной стенки выражен умеренно, патологическое мышечное напряжение отсутствует, опухолевые образования и грыжевые выпячивания не пальпируются. У 1 человека (представитель женского пола) наблюдалась болезненность в левой подвздошной области, правом подреберье с иррадиацией в правую подвздошную область.
Живот был мягкий, безболезненный, тонус мышц передней брюшной стенки выражен умеренно, патологическое мышечное напряжение отсутствует, опухолевые образования и грыжевые выпячивания не пальпируются. У 1 человека (представитель женского пола) наблюдалась болезненность в левой подвздошной области, правом подреберье с иррадиацией в правую подвздошную область.
Заклочение
Синдром абдоминальной боли широко распространен среди студентов и встречается гораздо чаще, чем выставляется диагноз хронического заболевания. Это может быть связано с небольшой обращаемостью за медицинской помощью, отсутствием жалоб со стороны пациента (при наличии хотя бы периодических болей в животе), недооценка этого клинического симптома как со стороны пациента (пассивные жалобы), так и со стороны врача, стигматизация абдоминальной боли (связь ее только с патологией ЖКТ), трудностью диагностики этиологии абдоминальной боли. Частые или периодические умеренные и сильные боли вынуждают человека принимать лекарственные средства, принадлежащие к разным фармакологическим группам, причем в большинстве случаев люди сами назначают себе препараты, не консультируясь с врачом. Зачастую данные лекарственные препараты направлены на симптоматическое лечение и не затрагивают причину боли. Подобное самолечение может приводить к прогрессированию, например, органической патологии, связанной с ЖКТ. Также из-за проблем диагностики может быть назначено неправильное или ненужное медикаментозное лечение, которое либо устраняет боль на определенное время, либо не устраняет вовсе. Достоверно доказано, что наличие хронической боли снижает качество жизни пациента [2]. В связи с этим как врачи, так и студенты должны акцентировать большее внимание на синдроме абдоминальной боли. Проведение санитарно-просветительской работы и повышение компетентности врачей поможет снизить количество студентов, страдающих от болей в животе, повысить качество жизни и сохранить здоровье основной трудоспособной части населения.
Зачастую данные лекарственные препараты направлены на симптоматическое лечение и не затрагивают причину боли. Подобное самолечение может приводить к прогрессированию, например, органической патологии, связанной с ЖКТ. Также из-за проблем диагностики может быть назначено неправильное или ненужное медикаментозное лечение, которое либо устраняет боль на определенное время, либо не устраняет вовсе. Достоверно доказано, что наличие хронической боли снижает качество жизни пациента [2]. В связи с этим как врачи, так и студенты должны акцентировать большее внимание на синдроме абдоминальной боли. Проведение санитарно-просветительской работы и повышение компетентности врачей поможет снизить количество студентов, страдающих от болей в животе, повысить качество жизни и сохранить здоровье основной трудоспособной части населения.
Литература:
- Livzan, M. A., Gaus, O. V., Turchaninov, D. V., & Popello, D. V. (2020). Abdominal Pain Syndrome in Youth: Prevalence and Risk Factors.
 Experimental and Clinical Gastroenterology, 1(10), 12–17.
Experimental and Clinical Gastroenterology, 1(10), 12–17. - Norton, C., Czuber-Dochan, W., Artom, M., Sweeney, L., & Hart, A. (2017). Systematic review: interventions for abdominal pain management in inflammatory bowel disease. Alimentary Pharmacology & Therapeutics, 46(2), 115–125.
- Дорофеев, А. Э., Руденко, Н. Н., Томаш, О. В., Иваненко, А. А., & Элин, А. Ф. (2013). АБДОМИНАЛЬНЫЕ БОЛИ при органической патологии кишечника. 5–14.
- Ивашкин, В. Т., Шелыгин, Ю. А., Баранская, Е. К., Белоусова, Е. А., Бениашвили, А. Г., Васильев, С. В., Головенко, А. О., Головенко, О. В., Григорьев, Е. Г., Костенко, Н. В., Лапина, Т. Л., Лоранская, И. Д., Ляшенко, О. С., Маев, И. В., Полуэктова, Е. А., Румянцев, В. Г., Тимербулатов, В. М., Трухманов, А. С., Фоменко, О. Ю., … Яновой, В. В. (2017). Рга Срк. Российский Журнал Гастроэнтерологии, Гепатологии, Колопроктологии, 27(5), 76–93.
- Минушкин, О. (2012). Патофизиология абдоминальной боли.
 Современные подходы к терапии моторных нарушений. 20–27.
Современные подходы к терапии моторных нарушений. 20–27. - Осипенко, М. Ф., Ливзан, М. А., Гриневич, В. Б., Сас, Е. И., Драпкина, О. М., Шептулин, А. А., Абдулганиева, Д. И., Алексеева, О. П., Корочанская, Н. В., Мордасова, В. И., Полуэктова, Е. А., Прохорова, Л. В., & Трухманов, А. С. (2015). Клинические рекомендации Российской гастроэнтерологической ассоциации по ведению пациентов с абдоминальной. 71–80.
- Волкова, М. П., & Голенко, К. Э. (n.d.). Рецидивирующий болевой абдоминальный синдром у студентов медицинского вуза. 127–130.
- Дроздова М. С., Драгун О. В., Соболева Л. В. (2011) Особенности синдрома абдоминальной боли у студентов ВУЗОВ (на примере УО “ВГМУ”). 84–85
- Волчегорский И. А., Важенина З. П., Рассохина Л. М., Коротовских Л. С., Мирошниченко И. Ю., Тренина Е. А. (2019) Избранные классификации лекарственных средств и основные формы выпуска.
- Аляутдин Р. Н. Фармакология. 5-е изд. 2016.
- Я.
 В. Бородуля, А. В. Круглова, Г. С. Б. (2015). ДАННЫЕ ПАЛЬПАЦИИ ЖИВОТА В ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКЕ ВИСЦЕРАЛЬНОЙ И ВЕРТЕБРОГЕННОЙ АБДОМИНАЛЬНОЙ БОЛИ. Dk, 53(9), 1689–1699.
В. Бородуля, А. В. Круглова, Г. С. Б. (2015). ДАННЫЕ ПАЛЬПАЦИИ ЖИВОТА В ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКЕ ВИСЦЕРАЛЬНОЙ И ВЕРТЕБРОГЕННОЙ АБДОМИНАЛЬНОЙ БОЛИ. Dk, 53(9), 1689–1699. - Официальный сайт Государственного реестра лекарственных средств.
Основные термины (генерируются автоматически): болевой синдром, боль, прием пищи, абдоминальная боль, студент, ответ, прием, состояние покоя, брюшная полость, живот.
Braz J Cardiovasc Surg — Разрыв торакоабдоминальной аневризмы аорты в правой плевральной полости
ВВЕДЕНИЕ
Термин, полученный из греческого слова «дилатация», аневризма соответствует сосуду диаметром в 1,5 раза больше нормального. Аневризмы торакоабдоминального отдела аорты были классифицированы Кроуфордом на типы от I до IV в зависимости от локализации расширения от левой подключичной артерии до брюшного сегмента [1]. В развитии этого заболевания разрывы, непосредственно связанные с увеличением диаметра аневризмы, являются наиболее тяжелыми и наиболее опасными осложнениями.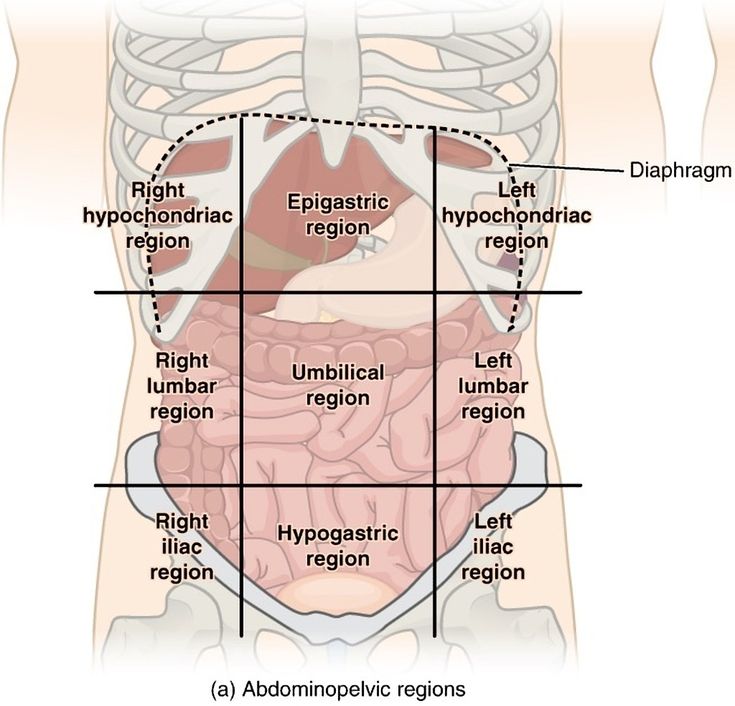 Таким образом, лечение аневризм представляет собой большую проблему [2] с очень точными показаниями из-за высокой заболеваемости и смертности.
Таким образом, лечение аневризм представляет собой большую проблему [2] с очень точными показаниями из-за высокой заболеваемости и смертности.
Целью данного исследования было описание случая 76-летнего пациента с диализной хронической почечной недостаточностью, разрывом аневризмы торакоабдоминального отдела аорты и тампонадой правой плевральной полости.
Клинический случай
76-летний пациент был направлен в отделение неотложной помощи Учебной больницы в Маринге, Бразилия, из-за болей в грудной клетке и сухого кашля во время сеанса гемодиализа. В течение двух лет больная страдала хронической почечной недостаточностью в связи с поликистозом почек. До постановки диагноза курил, артериальной гипертензии не было.
При физикальном обследовании при поступлении у него было выявлено артериальное давление 80 x 50 мм рт. ст., везикулярный шум в правом основании и аускультация сердца показала нормальные ритмичные звуки с митральным систолическим шумом. Живот вялый, безболезненный, с пульсирующим образованием в эпигастрии и мезогастрии, симптом Де Бейки положительный, аускультативно выслушивается систолический шум. Все пульсации пальпировались на обеих верхних конечностях, но на нижних конечностях пальпировались только бедренные пульсации. На этих артериальных путях не было дрожания или шумов.
Живот вялый, безболезненный, с пульсирующим образованием в эпигастрии и мезогастрии, симптом Де Бейки положительный, аускультативно выслушивается систолический шум. Все пульсации пальпировались на обеих верхних конечностях, но на нижних конечностях пальпировались только бедренные пульсации. На этих артериальных путях не было дрожания или шумов.
Дополнительные обследования показали небольшое снижение уровня гемоглобина и гематокрита, высокий уровень креатинина (6,75 мг/дл), электролитов, сахара в крови, холестерина и триглицеридов; артериальная газометрия и ферменты (тропонины, CK-MB и амилазы) без изменений. Рентгенограмма грудной клетки показала небольшое увеличение области сердца и затемнение в правом основании. На электрокардиограмме определяется синусовый ритм без признаков ишемии. Выполнена плевральная пункция справа и собрано 5 мл геморрагической жидкости (2456 эритроцитов/мл).
Пациенту была проведена компьютерная томография грудной клетки, которая показала, что нисходящая грудная аорта была расширена (8,0 см) и извилиста на 4,0 см ниже левой подключичной артерии до брюшной аорты с эксцентрическим тромбом и разрывом в правую плевральную полость (рис. 1).
1).
Рис. 1. Результат компьютерной томографии грудной клетки, показывающий отток контраста из грудной аорты в правую плевральную полость ствол. Его дистальный диаметр составил 3,0 см (рис. 2). Таким образом, рассматриваемая аневризма была классифицирована как тип Кроуфорда III.
Рис. 2. УЗИ органов брюшной полости, показывающее продолжение расширения грудной аорты в верхнюю брыжеечную артерию
Несмотря на тяжесть клинического состояния и наличие почечной недостаточности, пациент был гемодинамически стабилен, и по выбору семьи консервативное лечение было продолжено с высвобождением из стационара на 12-й день.
Состояние пациента было удовлетворительным в течение четырех месяцев с уменьшением боли, клинической стабильностью и отсутствием признаков активного кровотечения, но в конце этого периода у него снова появились торакальные боли и гемодинамическая нестабильность, переходящие в гиповолемический шок и смерть.
ОБСУЖДЕНИЕ
Имеется мало данных об эволюции и характеристиках торакоабдоминальных аневризм аорты, вызванных атеросклерозом, за исключением разрыва [1,3]; даже в этом случае эта этиология считается общей. Чаще встречается у мужчин и рассматривается как фактор риска, аналогичный артериальной гипертензии и курению [1].
Первоначально может протекать бессимптомно и диагностируется при проведении дополнительного обследования другой структуры. В качестве альтернативы, если есть такое осложнение, как разрыв, могут быть выявлены специфические признаки, в зависимости от места кровотечения; более совершенные методы диагностики позволяют легче выявить торакоабдоминальные аневризмы [2]. Если это симптоматично, то основным симптомом является боль в грудной клетке из-за расширения и сжатия соседних структур, как было показано здесь. В этом и в других случаях признаки гемодинамической нестабильности могут привести к диагностике или клиническому подозрению на аневризму аорты [1,3].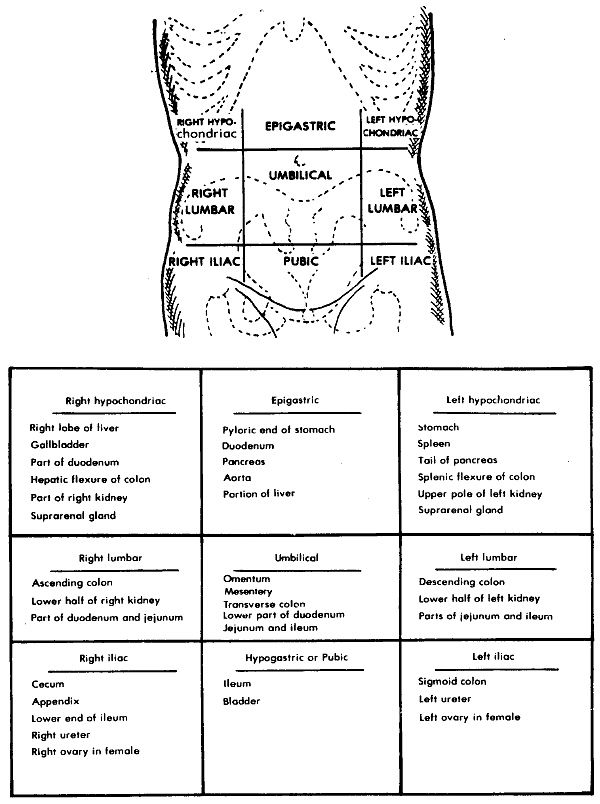
Подтверждение достигается дополнительными обследованиями, сначала простой рентгенограммой грудной клетки, показывающей увеличение средостения, изменение размера области сердца и затенение плевральной полости [3], аналогично представленному здесь случаю. Однако в этом случае плеврит может быть ошибочно принят за следствие хронической почечной недостаточности и аневризма может остаться незамеченной.
Компьютерная томография с контрастом позволяет определить диаметр, проксимальную и дистальную длину, анатомические взаимоотношения аневризмы и наличие расслоения или внутрипросветных тромбов. Ангиография не рекомендуется для измерения аневризмы, но также может предоставить приведенные данные, а также любое место разрыва [1]. Этому пациенту она не проводилась, так как диагноз уже был точно установлен, а также из-за почечной недостаточности.
Появление допплеровской эхокардиографии позволяет оценить инфраренальную часть аорты и поэтому полезно для диагностики, как в этом случае, показывая дистальную протяженность аневризмы.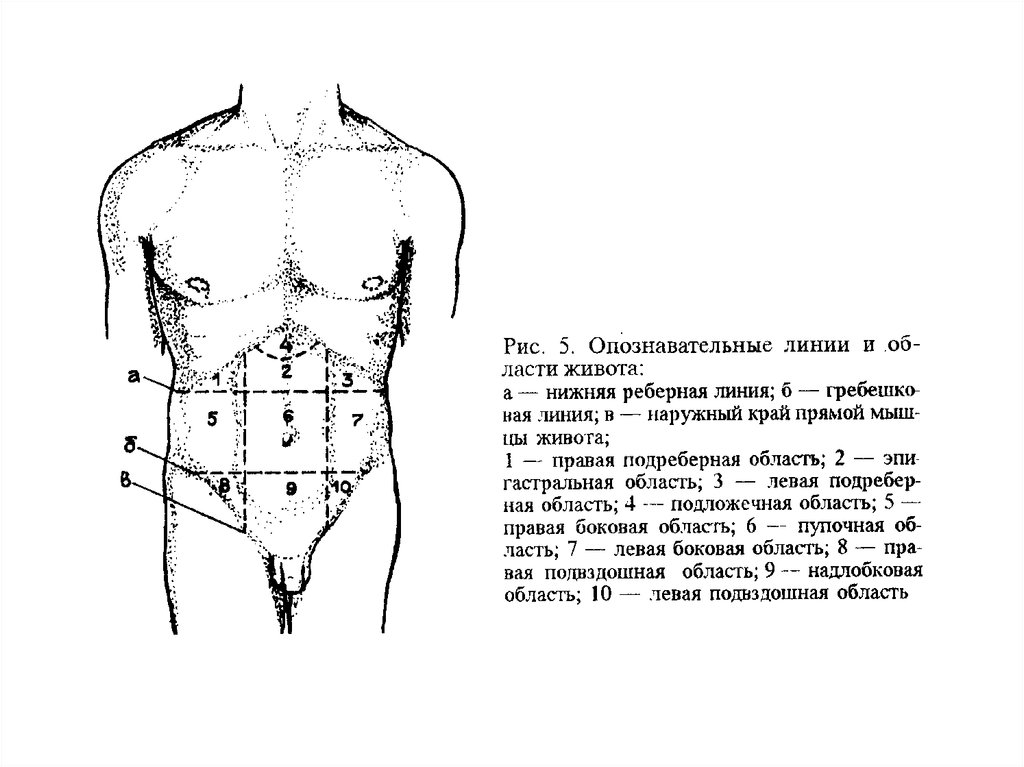
Другими исследованиями, которые также могут помочь в диагностике, являются чреспищеводная эхокардиография для оценки нисходящей аорты при расслоении и магнитно-резонансная томография, которая может предоставить информацию, подтверждающую результаты компьютерной томографии [1].
Разрыв этой аневризмы зависит от ее размера и положения и проявляется симптомами, которые могут свидетельствовать о расслоении: боль в межлопаточной области и иногда кровохарканье или кровавая рвота. При осмотре могут быть признаки нарушения гемодинамики или плеврального выпота [1,3]. В данном случае нисходящая аорта разорвалась во время диагностики, но осталась в правой плевральной полости. В момент смерти разрыв также произошел в правом полутораксе, вызвав необратимый шок.
Для пациентов со спонтанными разрывами грудной аорты срочно требуется оперативное вмешательство [1,2]; но в данном случае хирургическое лечение не проводилось, так как семья не давала согласия на операцию и пациент находился в тяжелом клиническом состоянии.
Плановая операция показана в зависимости от общего состояния больного при достижении диаметра 6 см при наличии недавнего роста или при наличии признаков сдавления соседних структур [1,3].
Принятым стандартом лечения является использование искусственного протеза, но благодаря хорошим результатам, достигнутым при эндоваскулярной коррекции абдоминальных аневризм, для лечения этой аневризмы были разработаны аналогичные методики.
По альтернативному эндоваскулярному лечению Rodrigues Alves et al. [4] описали протокол с клиническими и анатомическими критериями для лучшего определения прогноза пациентов, подвергшихся этой процедуре, и пришли к выводу, что они способны дифференцировать группы пациентов в отношении успеха предлагаемого лечения.
Пальма и др. [5] исследовали результаты эндоваскулярного лечения расслоения аорты типа В и пришли к выводу, что это безопасная альтернатива, которая может заменить традиционное лечение у большинства пациентов, аналогично результатам Dagenais et al. [6], которые продемонстрировали отличные результаты в тщательно отобранных случаях, но сообщили, что требуется больше времени, чтобы увидеть развитие случаев, прежде чем назначить эндоваскулярное лечение пациентам с низким риском.
[6], которые продемонстрировали отличные результаты в тщательно отобранных случаях, но сообщили, что требуется больше времени, чтобы увидеть развитие случаев, прежде чем назначить эндоваскулярное лечение пациентам с низким риском.
Пациент в текущем отчете оставался гемодинамически стабильным в течение четырех месяцев, когда он умер от кровотечения.
Несмотря на то, что хирургическая смертность высока (30%), это часто единственный терапевтический вариант, однако с возможностью новой альтернативы, даже если он не совершенен и не был протестирован, как и хирургический метод, он может предотвратить смерть в случаях разрыва.
РЕФЕРЕНЦИИ
1. Мариньо Дж.С.С., Андраде МФЦ. Аневризма грудно-брюшной аорты. В: Puech-Leão P, Kauffman P, ред. Артериальные аневризмы. Сан-Паулу: Fundo Editorial BYK; 1998. стр.129-46.
2. Palma JH, Miranda F, Gasques AR, Alves CMR, Souza JA, Buffolo E. Лечение торакоабдоминальной аневризмы с помощью саморасширяющихся аортальных стент-графтов. Энн Торак Серг. 2002;74(5):1685-7.
Энн Торак Серг. 2002;74(5):1685-7.
3. Коселли Х.С., де Фигейреду Л.Ф. Естественное течение аневризмы нисходящей и торакоабдоминальной аорты. J Card Surg. 1997; 12 (2 Дополнение): 285-91.
4. Rodrigues Alves CM, Fonseca JH, Souza JA, Carvalho AC, Buffolo E. Эндоваскулярное лечение торакального заболевания: отбор пациентов и предложение оценки риска. Энн Торак Серг. 2002;73(4):1143-8.
5. Palma JH, Souza JA, Rodrigues Alves CM, Carvalho AC, Buffolo E. Саморасширяющиеся аортальные стент-графты для лечения расслоения нисходящей аорты. Энн Торак Серг. 2002;73(4):1138-42.
6. Dagenais F, Normand JP, Turcotte R, Mathieu P. Изменение тенденций в лечении заболеваний грудной аорты: где мы находимся с торакальными эндоваскулярными стент-графтами? Может Джей Кардиол. 2005;21(2):173-8.
15_NC_3970_Acosta.ing.indd
%PDF-1.3
%
1 0 объект
>]/PageLabels 6 0 R/Pages 3 0 R/Type/Catalog/ViewerPreferences>>>
эндообъект
2 0 объект
>поток
2016-11-02T11:08:49+01:002016-11-02T11:08:50+01:002016-11-02T11:08:50+01:00Adobe InDesign CS6 (Macintosh)uuid:a47a81db-a242-bc4c-8186-185a738fa7c2xmp.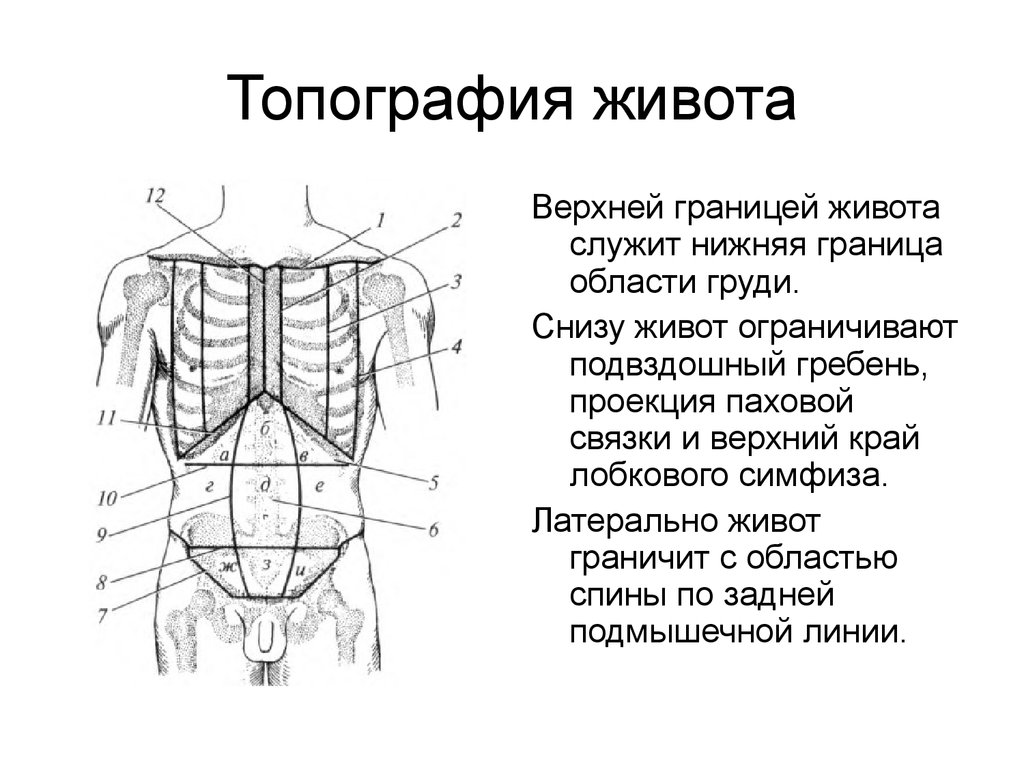 did:F77F11740720681188C6C55CD3F872D5xmp.id :575E668B1820681183D1E61E5AA4A72Eproof:pdf1xmp.iid:6848406032206811822AD0E2FDA9FD03xmp.did:0180117407206811822AE9CAD9598465xmp.did:F77F11740720681188C6C55CD3F872D5default
did:F77F11740720681188C6C55CD3F872D5xmp.id :575E668B1820681183D1E61E5AA4A72Eproof:pdf1xmp.iid:6848406032206811822AD0E2FDA9FD03xmp.did:0180117407206811822AE9CAD9598465xmp.did:F77F11740720681188C6C55CD3F872D5default
 0 0.0 595.276 793.701]/Тип/Страница>>
эндообъект
9 0 объект
>/Шрифт>/ProcSet[/PDF/Text/ImageC]/XObject>>>/TrimBox[0,0 0,0 595,276 793,701]/Тип/Страница>>
эндообъект
20 0 объект
>поток
HWr8}W
i˩Tɒر̬Q Ihx|6
0 0.0 595.276 793.701]/Тип/Страница>>
эндообъект
9 0 объект
>/Шрифт>/ProcSet[/PDF/Text/ImageC]/XObject>>>/TrimBox[0,0 0,0 595,276 793,701]/Тип/Страница>>
эндообъект
20 0 объект
>поток
HWr8}W
i˩Tɒر̬Q Ihx|6Тяжелый острый панкреатит, связанный с инфекцией, вызванной вирусом SARS-CoV-2: история болезни несет ответственность за текущую пандемию, которая затронула более 130 миллионов человек во всем мире, ее патогенез был сообщается о поражении желез эндокринной системы, поджелудочная железа не является исключением, поскольку на фоне поджелудочной железы также поражены другими респираторными вирусами.
Материалы и методы: Мы сообщаем о случае 82-летнего мужчины с диагнозом вирусной пневмонии, вызванной SARS-CoV-2.
у которого были боли в животе во время его эволюции, соответствующие критериям классификации Атланты для подозрения на панкреатит, во время
Во время его пребывания была выполнена абдоминальная аксиальная томография, оценка С по шкале Бальтазар, противовоспалительное лечение было
учитывая, однако результат не был благоприятным, несмотря на уже установленное лечение COVID-19и панкреатит.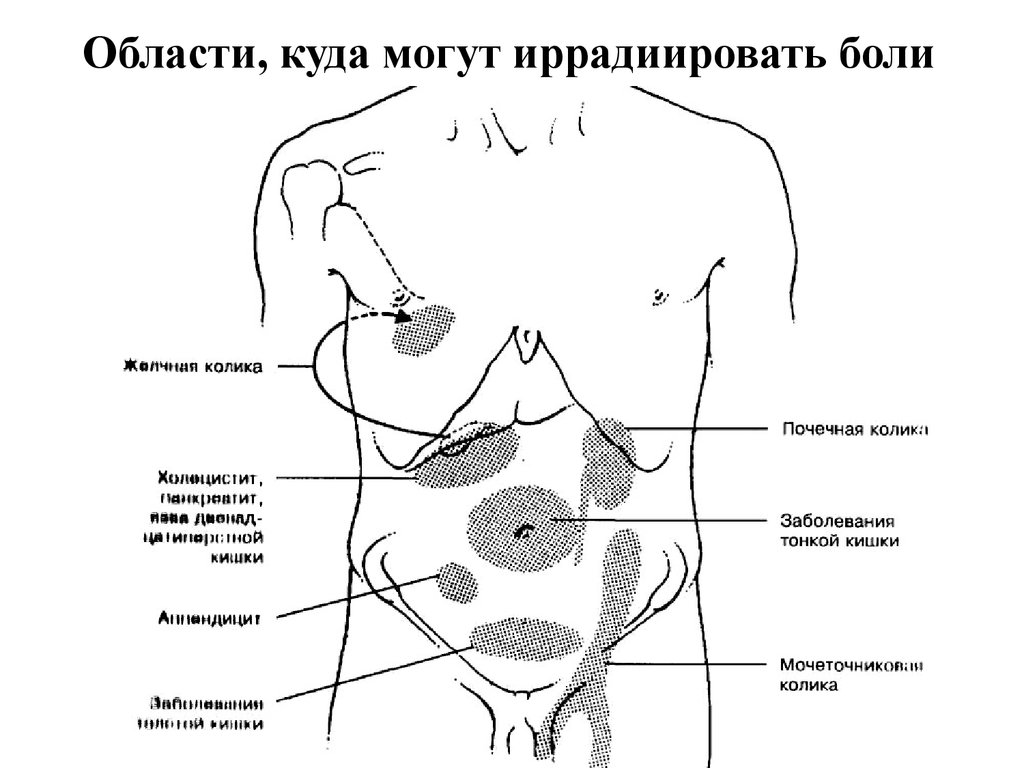 связь между COVID-19 и панкреатитом искали в других задокументированных отчетах о случаях.
наибольшее количество пациентов было сообщено Wang et al. В исследовании с участием 52 пациентов с положительным результатом на SARS-CoV-2 8 пациентов
имелись поражения поджелудочной железы и биохимические изменения (повышенный уровень амилазы и липазы) с бессимптомным течением.
связь между COVID-19 и панкреатитом искали в других задокументированных отчетах о случаях.
наибольшее количество пациентов было сообщено Wang et al. В исследовании с участием 52 пациентов с положительным результатом на SARS-CoV-2 8 пациентов
имелись поражения поджелудочной железы и биохимические изменения (повышенный уровень амилазы и липазы) с бессимптомным течением.
Заключение: Понимание клинических проявлений COVID-19 продолжает прогрессировать, этот случай иллюстрирует, что SARS-CoV-2 может спровоцировать острый панкреатит на фоне COVID-19.
Ключевые слова
Острый панкреатит; пневмония COVID-19; Инфекция SARS-CoV-2
Введение
Тяжелый острый респираторный синдром коронавирус 2 (SARSCoV-2)
вызванный коронавирусом (COVID-19), ответственен за
текущая пандемия, которая затронула более 130 миллионов человек
во всем мире, его патогенез, в тяжелых случаях индуцирует мультиорганное
отказ [1]. В последние месяцы легочные, почечные, сердечные,
прежде всего были изучены эндотелиальные, печеночные и церебральные поражения.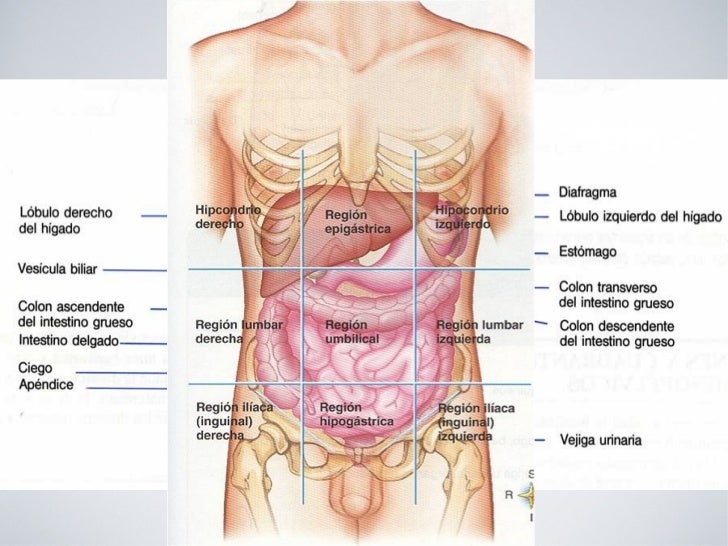
Что касается органов эндокринной системы, то немного сообщений об ассоциации. Что касается щитовидной железы, Было опубликовано исследование THYRCOV, в котором сообщается об ассоциации в 20% случаев тиреотоксикоз связан с коронавирусом [2]. В надпочечники, результаты соответствовали фибриноидному некрозу обнаружено при 5 вскрытиях пациентов с септическим шоком, нуждающихся в стероидной терапии. использовать [3]. Такие проявления, как отек и дегенерация нейронов в ткани гипофиза были связаны с центральным гипокортицизмом, центральный гипотиреоз и снижение дегидроэпиандростерона сульфат [4]. Сообщалось о случаях гипергликемии относительно поджелудочная железа как эндокринный и экзокринный орган у недиабетиков пациенты. является независимым фактором смертности. Панкреатит – это многофакторное заболевание, ассоциированные с ним вирусы парагрипп, корь, коксаки, вирус Эпштейна-Барр и гепатит А, недавно связанные случаи с SARS-CoV-2 [1].
Материалы и методы
Целью клинического случая является документирование ассоциации
между тяжелым идиопатическим острым панкреатитом у больных с активным
Инфекция SARS-CoV-2 и знать ассоциативные переменные, которые
были обнаружены в отчетах о случаях.
Результаты
82-летний мужчина. История болезни была значимой для типа
2 сахарный диабет и системная артериальная гипертензия, алкоголизм отрицает.
На +8 день симптомы лихорадки, сухой кашель, нарастающая одышка,
тошнота, рвота и диарея, развились, и больной
представили в отделение неотложной помощи. Следующие жизненные признаки
были зарегистрированы: Артериальное давление: 84/56 мм рт.ст., ЧСС: 120
ударов в минуту, частота дыхания: 26 об/мин, температура: 36,7 или С, Кислород
Насыщение в окружающем воздухе: 75%, неврологическое сознание, отвечает
на словесный раздражитель с дезориентацией, хотя и сотрудничает.
при исследовании легких — разлитые хрипы без
интегрированный синдром конденсации, рентгенография грудной клетки была
выполнено, что наводило на мысль о пневмонии SARS-CoV-2
(Рисунки 1 и 2). В связи с острой дыхательной недостаточностью ему потребовалось
дополнительный кислород с маской-резервуаром, улучшающий насыщение
до 88% в первый день госпитализации. Мягкий, депрессивный
живот пальпируется, болезненный при средней и глубокой пальпации в
эпигастрии и мезогастрии без раздражения брюшины, перистальтики
подарок. в связи с локализацией болей в животе, лабораторные анализы
были получены отчеты: Амилаза сыворотки: 1534 ЕД/л, сыворотка
липаза: 5117 ЕД/л, Альбумин: 3 г/дл, АСТ: 28 ЕД/л, АЛТ: 16 ЕД/л,
Общий билирубин: 0,49мг/дл, прямой билирубин: 0,14 мг/дл, непрямой
билирубин: 0,35 мг/дл, общий белок: 6,83 г/дл, лейкоциты:
13000/мм3, Нейтрофилы: 11890/мм3, Лимфоциты 980/мм3,
Тромбоциты 338 тыс./мл, гемоглобин: 11,9 г/дл и гематокрит 38,63%.
Из-за повышения ферментов поджелудочной железы происходит поражение печени и желчных протоков.
УЗИ было выполнено на второй день пребывания в стационаре, что
сообщается: Печень в нормальном анатомическом положении, с размерами
в пределах нормы, морфология сохранена, границы правильные,
четкой и отграниченной, паренхима однородная, без
признаки очагового или диффузного поражения, васкуляризация сохранена,
внутри- и внепеченочной дилатации желчного пузыря не наблюдалось.
Мягкий, депрессивный
живот пальпируется, болезненный при средней и глубокой пальпации в
эпигастрии и мезогастрии без раздражения брюшины, перистальтики
подарок. в связи с локализацией болей в животе, лабораторные анализы
были получены отчеты: Амилаза сыворотки: 1534 ЕД/л, сыворотка
липаза: 5117 ЕД/л, Альбумин: 3 г/дл, АСТ: 28 ЕД/л, АЛТ: 16 ЕД/л,
Общий билирубин: 0,49мг/дл, прямой билирубин: 0,14 мг/дл, непрямой
билирубин: 0,35 мг/дл, общий белок: 6,83 г/дл, лейкоциты:
13000/мм3, Нейтрофилы: 11890/мм3, Лимфоциты 980/мм3,
Тромбоциты 338 тыс./мл, гемоглобин: 11,9 г/дл и гематокрит 38,63%.
Из-за повышения ферментов поджелудочной железы происходит поражение печени и желчных протоков.
УЗИ было выполнено на второй день пребывания в стационаре, что
сообщается: Печень в нормальном анатомическом положении, с размерами
в пределах нормы, морфология сохранена, границы правильные,
четкой и отграниченной, паренхима однородная, без
признаки очагового или диффузного поражения, васкуляризация сохранена,
внутри- и внепеченочной дилатации желчного пузыря не наблюдалось.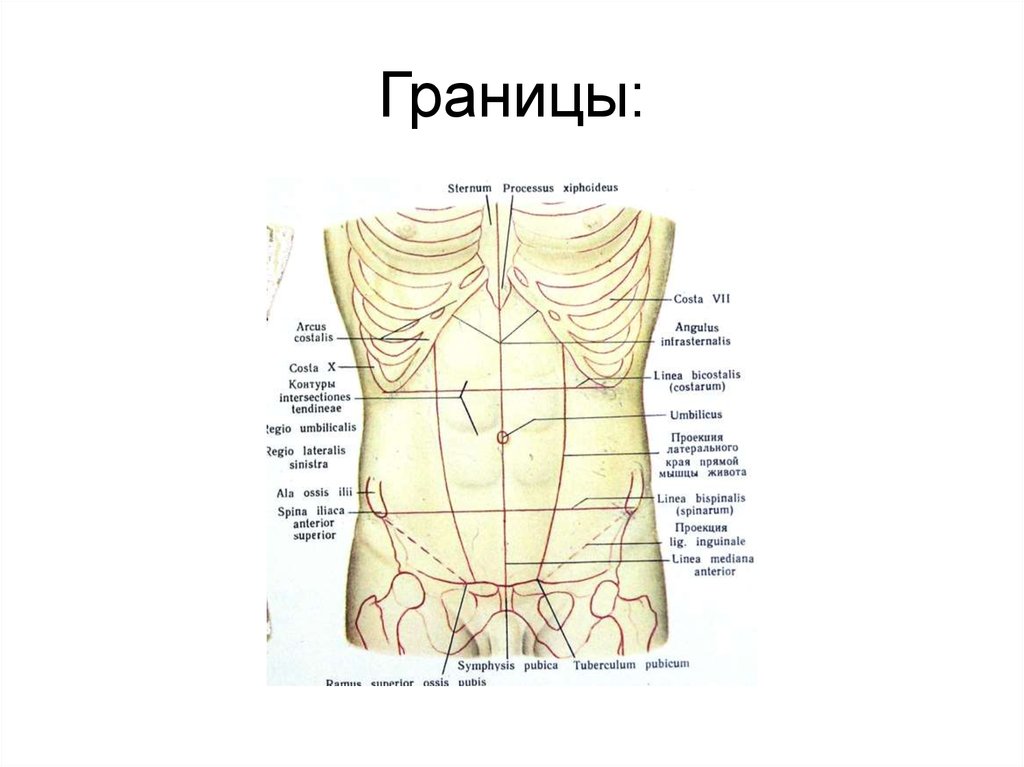 ,
воротная вена 9мм, диаметр холедоха 4 мм, желчный пузырь с
размеры 74х36х33 мм, повреждений не выявлено, тонкая стенка 2,3
мм толщиной. Поджелудочная железа не оценивалась на наличие газа в ее
топография, селезенка без изменений ее паренхимы. Для этого
причина, острый панкреатит был интегрирован, затем инфузионная терапия
начали, наряду с обезболиванием, эмпирическую антибиотикотерапию и
голодание из-за оральной непереносимости. Требуются исследования для определения
степень тяжести: Кальций: 90,3 мг/дл, креатинин: 4,0 мг/дл, АМК
131 мг/дл, мочевина: 280,7 мг/дл, гематокрит: 38,6%, глюкоза:
571 мг/дл, ЛДГ: 252 ЕД/л: оценка BISAP: 5 баллов. АПАЧ II: А
Рэнсон: 3 за первые 48 часов.
,
воротная вена 9мм, диаметр холедоха 4 мм, желчный пузырь с
размеры 74х36х33 мм, повреждений не выявлено, тонкая стенка 2,3
мм толщиной. Поджелудочная железа не оценивалась на наличие газа в ее
топография, селезенка без изменений ее паренхимы. Для этого
причина, острый панкреатит был интегрирован, затем инфузионная терапия
начали, наряду с обезболиванием, эмпирическую антибиотикотерапию и
голодание из-за оральной непереносимости. Требуются исследования для определения
степень тяжести: Кальций: 90,3 мг/дл, креатинин: 4,0 мг/дл, АМК
131 мг/дл, мочевина: 280,7 мг/дл, гематокрит: 38,6%, глюкоза:
571 мг/дл, ЛДГ: 252 ЕД/л: оценка BISAP: 5 баллов. АПАЧ II: А
Рэнсон: 3 за первые 48 часов.
В связи с респираторным статусом пациента был взят мазок из носа.
запросили ОТ-ПЦР на SARS-CoV-2, который был положительным. На
На 4-й день была запрошена КТ брюшной полости,
следующие данные: Отечный панкреатит с перипанкреатической
жидкость во всех карманах брюшины, степень C по шкале Baltazar
шкала.
Во время его пребывания клиническая эволюция была вялой даже при начальную поддерживающую терапию, он представил данные респираторного дистресс, газы крови при поступлении: pH 7,44, PcO2 32 мм рт. ст., pO2 64 мм рт. ст., HCO3 21 мэкв/л, BE –1,5 мэкв/л, O Sat 93%, соотношение PaO2/FiO2 305 мм рт. ст., включая дыхательный тип 1 неудачи, без критериев интубации на момент поступления, это имеет КТ грудной клетки с сообщением о множественных диффузных альвеолярных инфильтратах исходного преобладания, совместимого с вирусной пневмонией, CORADS 5, однако через 2 дня он постепенно прогрессировал до при множественной органической недостаточности больной умер.
Обсуждение
В связи с клиническим случаем в течение недели
госпитализации поступило 67 пациентов с COVID-19 и только это
В данном случае был поставлен окончательный диагноз тяжелого острого панкреатита.
по критериям Атланта, не связанные с основными причинами: камни в желчном пузыре,
алкоголь, гиперкальциемия и гипертриглицеридемия. Результаты, достижения
поддерживают потенциальное повреждение поджелудочной железы вирусом SARS-CoV-2. В исследовании 52 пациентов у 9 было выявлено повреждение поджелудочной железы, определяемое любой аномалией липазы/амилазы без демонстрации
прямое присутствие вируса в ткани поджелудочной железы, 6 пациентов без диабета имели аномальные уровни глюкозы, что свидетельствует о цитопатическом эффекте
на репликацию SARS-CoV-2 и непрямое повреждение системной воспалительной реакцией это наблюдалось при SARS-CoV-1
(2003) [5].
Результаты, достижения
поддерживают потенциальное повреждение поджелудочной железы вирусом SARS-CoV-2. В исследовании 52 пациентов у 9 было выявлено повреждение поджелудочной железы, определяемое любой аномалией липазы/амилазы без демонстрации
прямое присутствие вируса в ткани поджелудочной железы, 6 пациентов без диабета имели аномальные уровни глюкозы, что свидетельствует о цитопатическом эффекте
на репликацию SARS-CoV-2 и непрямое повреждение системной воспалительной реакцией это наблюдалось при SARS-CoV-1
(2003) [5].
Патогенез SARS-CoV-2 опосредуется рецептором ангиотензинпревращающего фермента 2 (ACE-2) в клетках-хозяевах, который ранее высоко экспрессировались в островках поджелудочной железы, острый панкреатит при COVID19 мог возникнуть из-за прямого цитопатического действия локальная репликация SARS-CoV-2 или опосредованно вредным иммунным ответом, индуцированным вирусом [3].
Сообщений о клинических случаях мало, об исследовании с наибольшим числом пациентов сообщили Wang et al [16].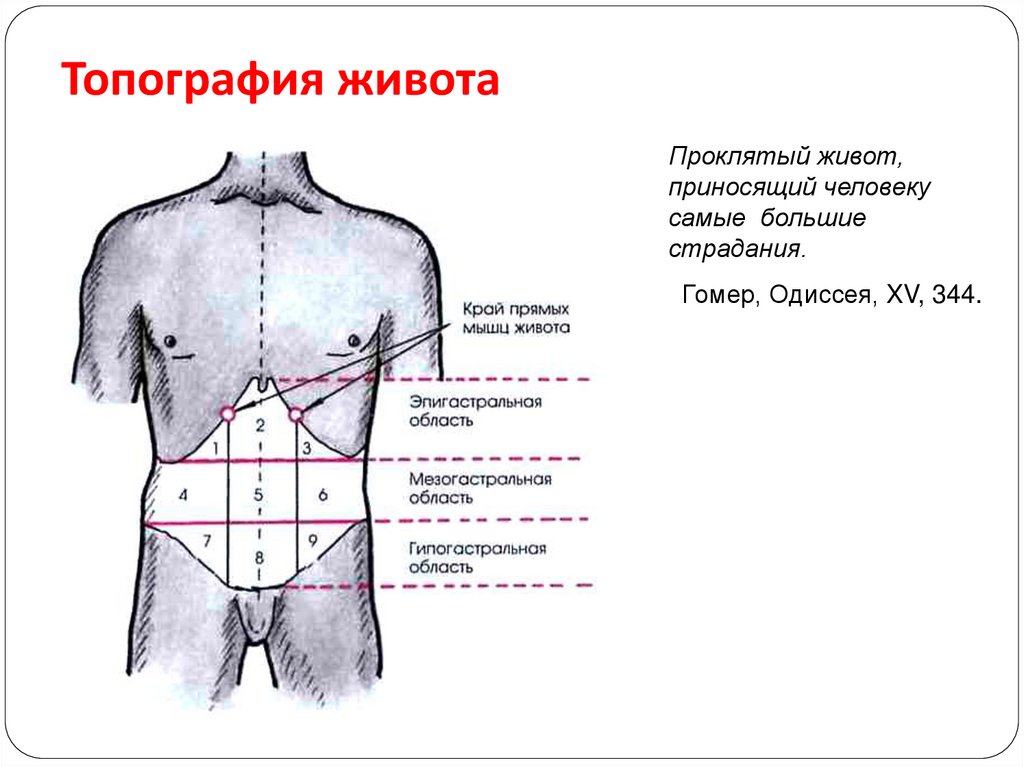
 Experimental and Clinical Gastroenterology, 1(10), 12–17.
Experimental and Clinical Gastroenterology, 1(10), 12–17.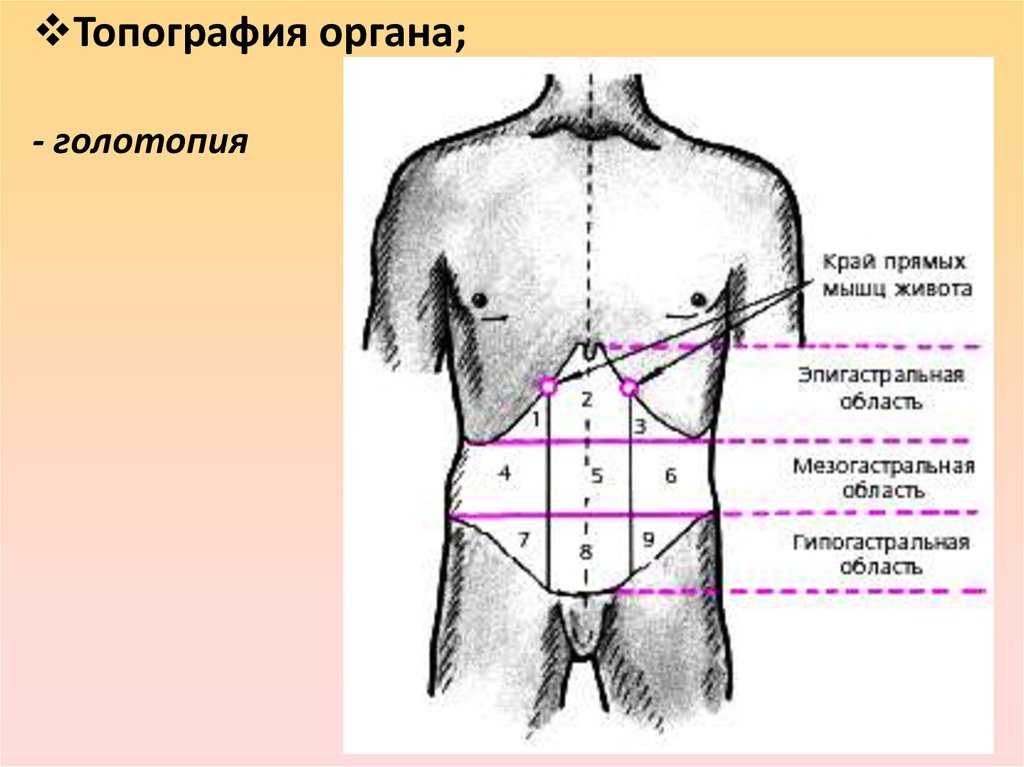 Современные подходы к терапии моторных нарушений. 20–27.
Современные подходы к терапии моторных нарушений. 20–27.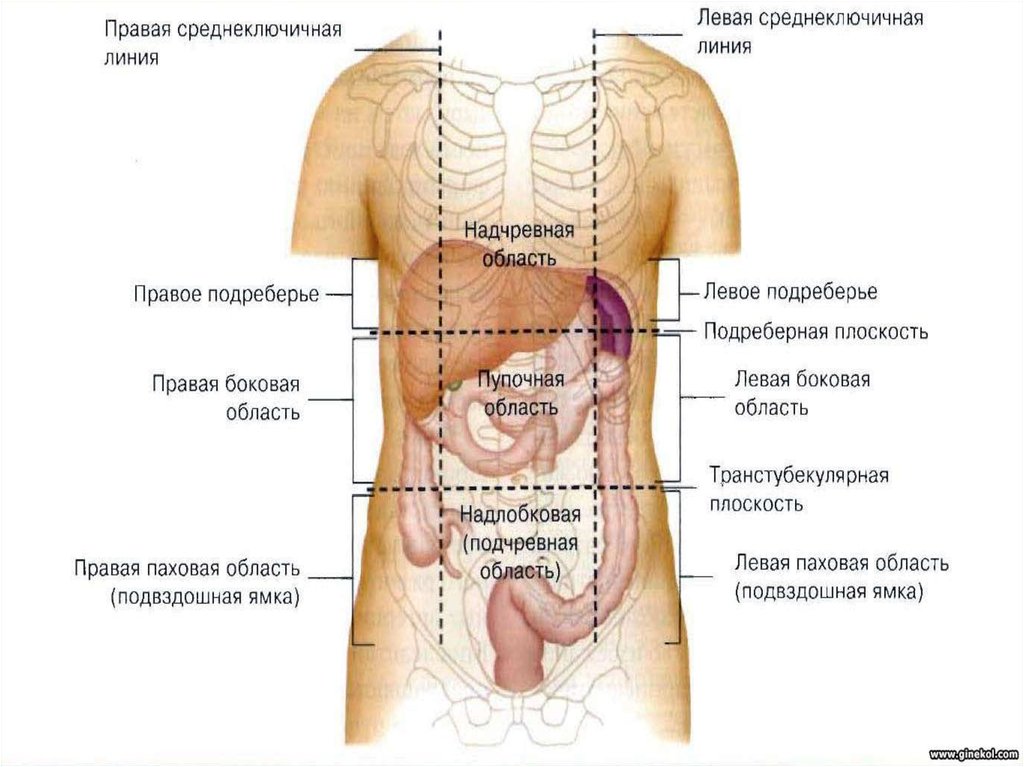 В. Бородуля, А. В. Круглова, Г. С. Б. (2015). ДАННЫЕ ПАЛЬПАЦИИ ЖИВОТА В ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКЕ ВИСЦЕРАЛЬНОЙ И ВЕРТЕБРОГЕННОЙ АБДОМИНАЛЬНОЙ БОЛИ. Dk, 53(9), 1689–1699.
В. Бородуля, А. В. Круглова, Г. С. Б. (2015). ДАННЫЕ ПАЛЬПАЦИИ ЖИВОТА В ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКЕ ВИСЦЕРАЛЬНОЙ И ВЕРТЕБРОГЕННОЙ АБДОМИНАЛЬНОЙ БОЛИ. Dk, 53(9), 1689–1699.