МАТЕРИАЛЫ КОНГРЕССОВ И КОНФЕРЕНЦИЙ: IX РОССИЙСКИЙ ОНКОЛОГИЧЕСКИЙ КОНГРЕСС
IX РОССИЙСКИЙ ОНКОЛОГИЧЕСКИЙ КОНГРЕСС
ОСНОВНЫЕ ПОДХОДЫ И РЕЗУЛЬТАТЫ КОНСЕРВАТИВНОГО ЛЕЧЕНИЯ БОЛЬНЫХ С МЕТАСТАЗАМИ В КОСТИ
В.Е. Каллистов, А.П. Николаев, С.В. Одинцов, Г.Г. Матякин,
Т.П. Чуприк-Малиновская, Н.Н. Виноградова
ФГУ ЦКБ с поликлиникой УДП РФ, Москва
С учетом удельного веса в структуре онкологической заболеваемости и частоты метастазирования в кости особо значимыми для анализа представляются рак молочной и предстательной желез, а также рак легкого и рак почки.
Основными компонентами комплексного лечения метастатического костного поражения являются химиотерапия, гормонотерапия, лучевая терапия, иммунотерапия. Оперативное лечение показано при солитарных метастазах (например, рака почки), либо при угрозе патологического перелома или компрессии спинного мозга.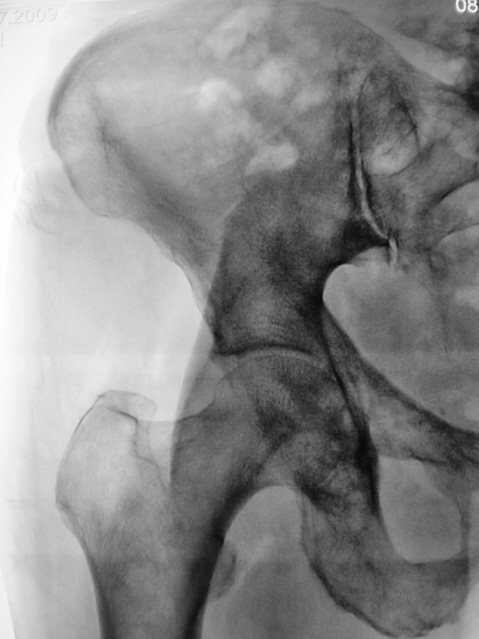
Костные метастазы рака молочной железы. Рак молочной железы (РМЖ) имеет особенную предрасположенность к развитию метастазов в кости. До 90% умерших пациентов, страдавших РМЖ, имеют метастазы в кости.
За 1980-2004 гг. в Центральной клинической больнице МЦ находились на обследовании и лечении 2075 больных РМЖ (табл. 1). Средний возраст составил 59,2 (25-91) года.
Таблица 1.
Распределение больных РМЖ по степени распространенного процесса
(ЦКБ, 1980-2004 гг.).
| Показатели | Всего | Стадии | ||||
|---|---|---|---|---|---|---|
| I | II | III | IV | Инфильтративно-отечная форма | ||
| Количество больных | 2075 | 850 | 802 | 281 | 89 | 53 |
| % от общего числа | 100 | 41,0 | 38,6 | 13,5 | 4,3 | 2,6 |
Из этого числа больных у 232 (11,2%) были выявлены метастазы в кости.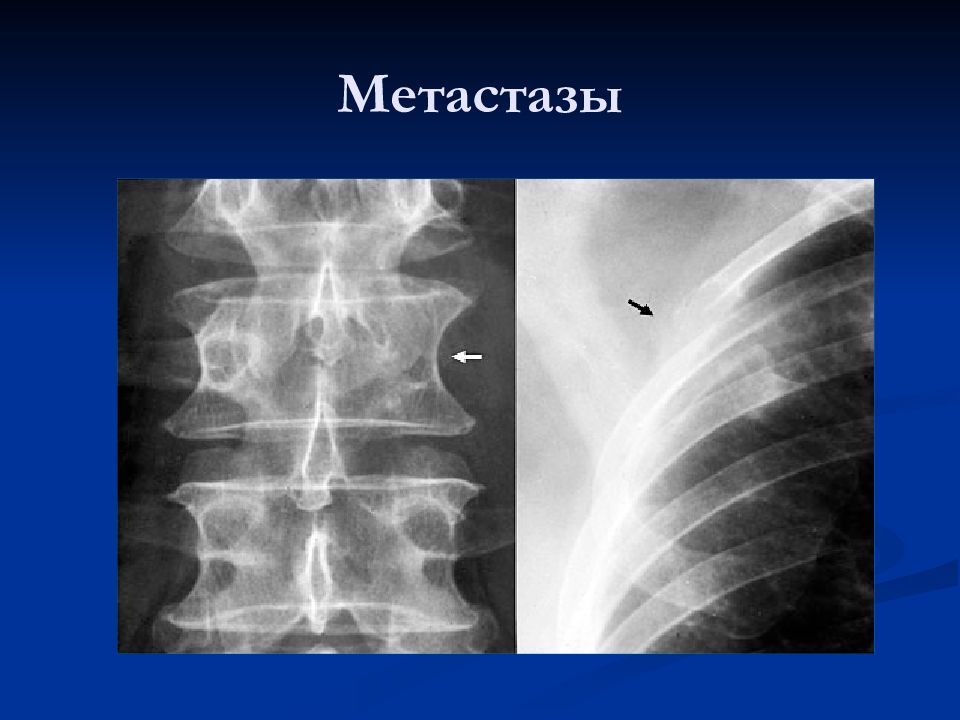 При длительном наблюдении установлено, что метастазы в кости были диагностированы при всех стадиях РМЖ: при I стадии — в 5% случаев, при II – в 10,5%, при III – в 17,6%, при IV – в 45,6%, при инфильтративно-отечной форме — в 28,5% случаев.
При длительном наблюдении установлено, что метастазы в кости были диагностированы при всех стадиях РМЖ: при I стадии — в 5% случаев, при II – в 10,5%, при III – в 17,6%, при IV – в 45,6%, при инфильтративно-отечной форме — в 28,5% случаев.
Средний период до определения метастазов в кости у этих больных составил 36,8 (30,9-42,6) мес. Для определения наиболее вероятных сроков выявления костных метастазов РМЖ рассчитан средний период до их установления при различных стадиях первичной опухоли. При первой стадии он составил 53,2 (39,3-67,1) мес., при IIа стадии – 42,9 (23,5-62,2) мес., при IIб – 50,3 (36,3-64,4) мес., при III стадии — 38,7 (26,5-51,0) мес.
Уровень рецепторов стероидных гормонов в опухоли в значительной степени определяет показания для гормонотерапии при метастатическом поражении костей. По нашему мнению, наиболее целесообразно применение гормонотерапии у больных с метастазами в кости в постменопаузе с признаками гормоночувствительности в следующей последовательности: I линия — тамоксифен; II линия — ингибиторы ароматазы; III линия — прогестины, IV линия — андрогены.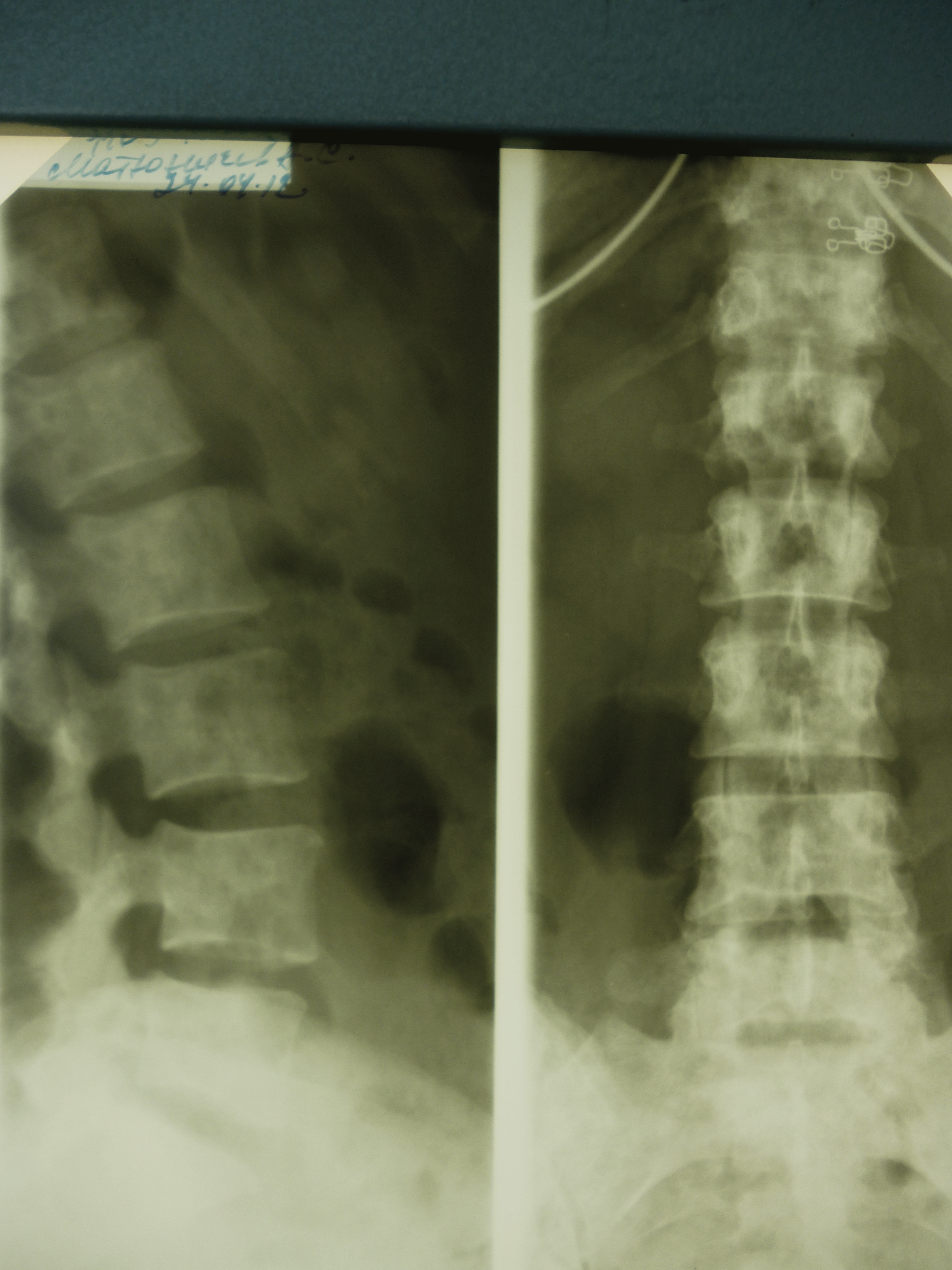
У больных репродуктивного периода и пременопаузы: I линия — овариоэктомия, лучевая кастрация или агонисты рилизинг-гормонов (золадекс) + тамоксифен; II линия — ингибиторы ароматазы; III линия — прогестины; IV линия — андрогены.
Постменопаузальные больные, особенно старше 70 лет, с метастазами РМЖ в кости даже с отрицательными рецепторами подлежали гормонотерапии. У больных репродуктивного периода при отсутствии признаков гормоночувствительности опухоли I линией терапии являлась химиотерапия.
У не леченных больных с метастазами РМЖ в кости в качестве I линии химиотерапии мы в основном используем схему CAF (циклофосфан, доксорубицин и 5-фторурацил). В качестве II-III линии химиотерапии использовались таксаны, гемцитабин, винорельбин в различных сочетаниях или в монорежиме.
У больных, получавших адъювантное лечение по поводу первичной опухоли, при выявлении метастазов в кости лечение начинали с применения таксанов в комбинации с антрациклинами либо в монорежиме в зависимости от состояния пациента.
При достижении объективных эффектов или стабилизации процесса больные в дальнейшем получали поддерживающее лечение (бисфосфонаты) и гормонотерапию. Контроль за метастатическим процессом осуществлялся в среднем 1 раз в три месяца и включал сцинтиграфию, рентгенографию, при необходимости – КТ или МРТ. При наличии признаков прогрессирования процесса применялась следующая линия химиотерапии.
Наряду с системной терапией в лечении костных метастазов РМЖ большую роль играет лучевая терапия. В ряде случаев мы проводим ее параллельно с химио- или гормонотерапией.
Как правило, метастазы в кости сочетаются с прогрессированием во внутренние органы. В табл. 2 представлены результаты проведенной диагностики и лечения.
Таблица 2.
Результаты лечения больных РМЖ в ЦКБ за период с 1980 по 2004 гг. в зависимости от стадии заболевания.
| Вид прогрессирования | I cт. |
II ст. | III ст. | IV cт. | Инфильтративно-отечная форма | Всего |
|---|---|---|---|---|---|---|
| Местный рецидив | 3 | 5 | 3 | — | — | 11 |
| Метастазы в кости | 43 | 84 | 49 | 41 | 15 | 232 |
| Метастазы в другие органы | 13 | 73 | 20 | 48 | 38 | 192 |
| Все случаи прогрессирования | 59 | 162 | 72 | 89 | 53 | 435 |
Изучены показатели выживаемости у группы больных с метастазами в кости скелета у больных в зависимости от возраста. Эти данные представлены на рис. 1. 5-летняя выживаемость больных после диагностики и лечения костных метастазов составила около 25%.
Рис. 1. Выживаемость больных РМЖ различных возрастных групп с метастазами в кости.
Костные метастазы рака предстательной железы. У мужчин наиболее часто в кости метастазирует рак предстательной железы (РПЖ). Метастазы в кости выявляются часто параллельно или вскоре после клинической манифестации болезни. Характер метастазов в костях преимущественно множественный, чаще остеобластического типа, хотя встречаются и литические очаги.
Внедрение в практику агонистов гонадотропин-рилизинг-гормонов, особенно имеющих удобную для применения депо-форму (золадекс, диферелин) позволяет заменить хирургическое вмешательство (орхэктомию) химической кастрацией.
Лечение по схеме максимальной андрогенной блокады вытеснило имевшую длительную историю терапию эстрогенами.
В случае исчерпания возможностей антиандрогенов мы использовали химиотерапию таксанами.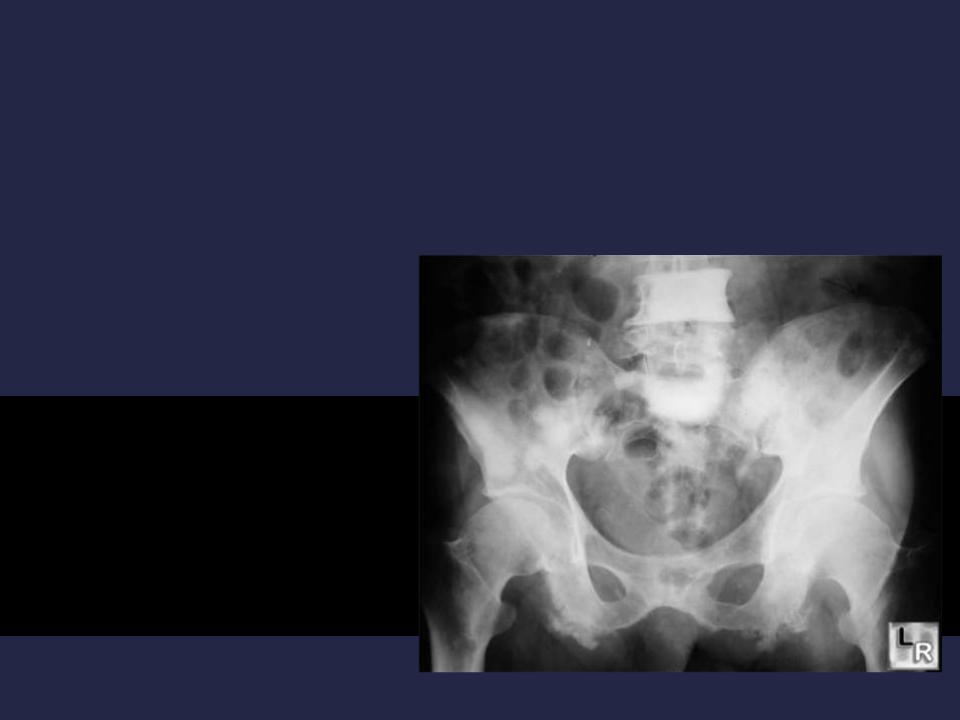
Гормонотерапия или химиотерапия дополняется лучевой терапией на зоны костного поражения, что позволяет ускорить достижение паллиативного эффекта и увеличить его продолжительность.
За 1980-2004 гг. в Центральной клинической больнице МЦ на обследовании и лечении находились 872 больных РПЖ (табл. 3). Средний возраст заболевших составил 72,5 (39-94) года.
Таблица 3.
Распределение больных РПЖ по степени распространенности процесса (ЦКБ, 1980-2004 гг.).
| Всего | Стадии | ||||
|---|---|---|---|---|---|
| I | II | III | IV | ||
| Количество больных | 872 | 299 | 297 | 91 | 185 |
| % от общего числа | 100 | 34,3 | 34,1 | 10,4 | 21,2 |
Из этого числа больных у 252 (28,9%) пациентов были выявлены метастазы в кости: солитарные — у 43 пациентов, множественные – у 209 больных.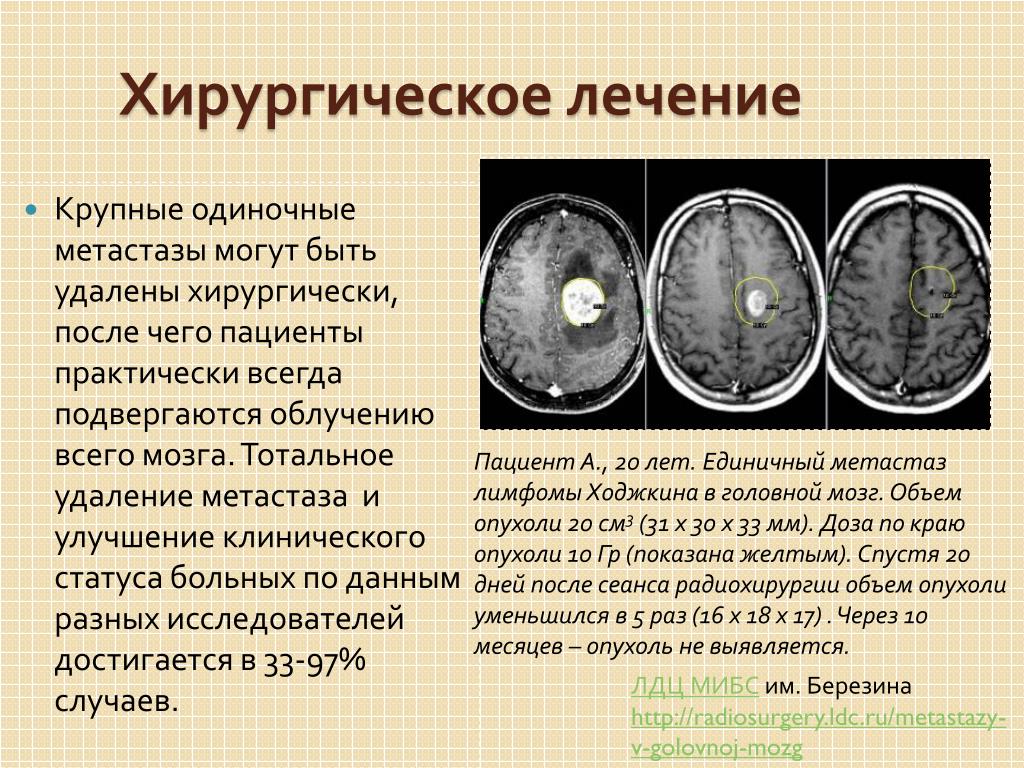 Метастазы в кости были диагностированы при всех стадиях РПЖ: при I стадии – в 13,0% случаев, при II – в 15,2%, при III – в 51,6%, при IV – в 65,3% случаев (табл. 4). Средний период до определения метастазов в кости у больных I-III стадий составил 42,8 (39,9-52,6) мес.; при I стадии — 59,9 (40,3-67,1) мес., при II стадии – 47,4 (33,5-60,2) мес., при III стадии — 28,9 (21,5-41,1) мес.
Метастазы в кости были диагностированы при всех стадиях РПЖ: при I стадии – в 13,0% случаев, при II – в 15,2%, при III – в 51,6%, при IV – в 65,3% случаев (табл. 4). Средний период до определения метастазов в кости у больных I-III стадий составил 42,8 (39,9-52,6) мес.; при I стадии — 59,9 (40,3-67,1) мес., при II стадии – 47,4 (33,5-60,2) мес., при III стадии — 28,9 (21,5-41,1) мес.
Таблица 4.
Результаты лечения больных РПЖ в ЦКБ за период с 1980 по 2004 гг. в зависимости от стадии заболевания.
| Вид прогрессирования | I cт. | II ст. | III ст. | IV ст. | Всего |
|---|---|---|---|---|---|
| Местный рецидив | 1 | 3 | 3 | — | 7 |
| Метастазы в кости | 39 | 45 | 47 | 121 | 252 |
| Метастазы в другие органы | 3 | 7 | 8 | 64 | 82 |
| Все случаи прогрессирования | 43 | 55 | 58 | 185 | 341 |
5-летняя выживаемость больных после выявления метастазов составила при проведении лечения 35% и без лечения — 21%.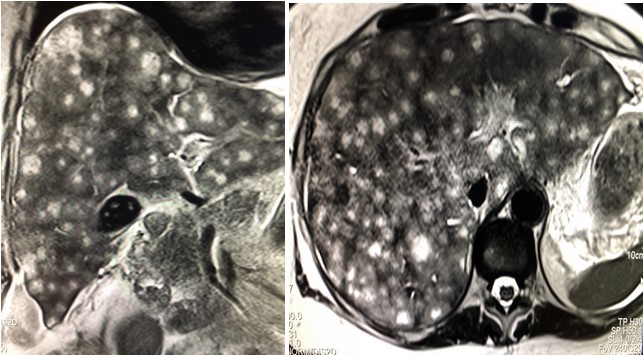
Костные метастазы рака легкого. Метастазы рака легкого (РЛ) в кости имеют в основном остеолитический характер. Они чаще встречаются при мелкоклеточном раке легкого (МРЛ), имеют характер множественного поражения и часто сочетаются с метастазами в лимфоузлах или других органах. При плоскоклеточном раке и аденокарциноме чаще бывают солитарные метастазы. Характер поражения и гистологическая форма опухоли оказывают влияние как на прогноз заболевания, так и на тактику лечения.
При генерализации МРЛ чаще проводилась химиотерапия с использованием различных сочетаний антрациклинов, производных платины, гемцитабина, циклофосфана, метотрексата, винкристина, 5-фторурацила, этопозида и др. Химиотерапию чаще всего сочетали с лучевой терапией на область отдельных метастатических очагов, осложненных болевым синдромом или угрозой переломов.
При солитарных метастазах в кости дифференцированных форм РЛ основным методом лечения являлась лучевая терапия.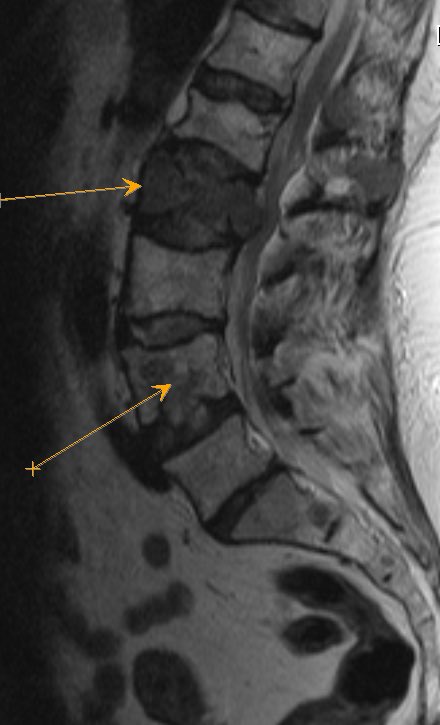
За 1980-2004 гг. в Центральной клинической больнице МЦ на обследовании и лечении находились 1229 больных РЛ (табл. 5). Средний возраст заболевших составил 71,3 (35-89) лет. Центральный рак составил 46,7%, периферический — 53,3%; МРЛ выявлен у 17,9% пациентов.
Таблица 5.
Распределение больных РЛ по степени распространенности процесса (ЦКБ, 1980-2004 гг.).
| Всего | Стадии | ||||
|---|---|---|---|---|---|
| I | II | III | IV | ||
| Количество больных | 1229 | 245 | 304 | 296 | 384 |
| % от общего числа | 100 | 19,9 | 24,7 | 24,1 | 31,3 |
У 120 (9,8%) пациентов были выявлены метастазы в кости, которые диагностировались при всех стадиях РЛ (табл.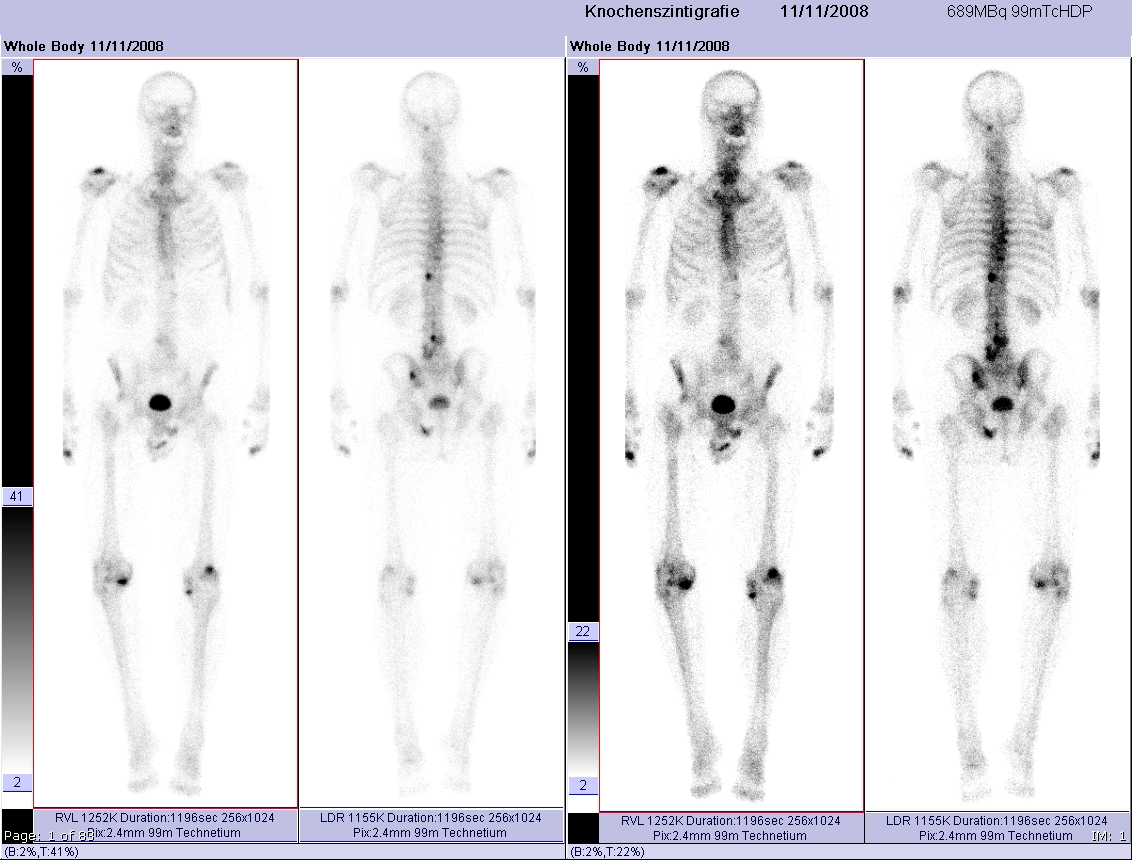 6): при I стадии — у 6,9% больных, при II стадии — также у 6,9%, при III стадии – у 2,3%, при IV – у 19,5% больных. Наиболее частой локализацией метастазов были пояснично-крестцовый отдел позвоночника и кости таза. Солитарные метастазы выявлены у 28 пациентов, множественные – у 92 больных. Источником костных метастазов чаще был МРЛ (55,8% случаев), реже – железистый и плоскоклеточный. Средний возраст больных с метастазами в кости составил 72,6 года. Средний период до определения метастазов в кости у больных I-III стадий составил 16,2 (9,9-22,1) мес.
6): при I стадии — у 6,9% больных, при II стадии — также у 6,9%, при III стадии – у 2,3%, при IV – у 19,5% больных. Наиболее частой локализацией метастазов были пояснично-крестцовый отдел позвоночника и кости таза. Солитарные метастазы выявлены у 28 пациентов, множественные – у 92 больных. Источником костных метастазов чаще был МРЛ (55,8% случаев), реже – железистый и плоскоклеточный. Средний возраст больных с метастазами в кости составил 72,6 года. Средний период до определения метастазов в кости у больных I-III стадий составил 16,2 (9,9-22,1) мес.
Таблица 6.
Результаты лечения больных раком легкого в ЦКБ за период с 1980 по 2004 гг. в зависимости от стадии заболевания.
| Вид прогрессирования | I cт. | II ст. | III ст. | IV ст. | Всего |
|---|---|---|---|---|---|
| Местный рецидив | 12 | 9 | 7 | — | 28 |
| Метастазы в кости | 17 | 21 | 7 | 75 | 120 |
| Метастазы в другие органы | 78 | 112 | 122 | 221 | 533 |
| Все случаи прогрессирования | 107 | 142 | 136 | 296 | 681 |
Средний период до появления костных метастазов при РЛ составил при I стадии 22,0 (29,3-33,1) мес. ; при II стадии – 17,8 (21,5-29,2) мес., при III стадии — 10,6 (6,5-19,2) мес.
; при II стадии – 17,8 (21,5-29,2) мес., при III стадии — 10,6 (6,5-19,2) мес.
Основным методом лечения костных метастазов при РЛ паллиативная химиотерапия на основе производных препаратов платины (цисплатин + гемзар либо цисплатин + таксаны, либо цисплатин + навельбин). При наличии множественных метастазов РЛ в кости, особенно сопровождающихся болевым синдромом, мы использовали бисфосфонаты. При упорном болевом синдроме проводилась симптоматическая лучевая терапия.
Хирургическое лечение метастатического РЛ в кости выполнено у 2 больных с локализацией солитарного метастаза в ребре и плечевой кости.
Средняя продолжительность жизни больных с костными метастазами РЛ, получавших лечение, составила 17,7 мес., без лечения — 5,8 мес.
Костные метастазы рака почки. Клинические симптомы, обусловленные метастазами, при раке почки (РП) нередко являются первым проявлением скрыто протекающего опухолевого процесса. При наличии единичных отдаленных метастазов лечение целесообразно начинать с удаления первичной опухоли, решая в последующем вопрос о хирургическом или консервативном лечении метастаза в зависимости от его локализации.
При наличии единичных отдаленных метастазов лечение целесообразно начинать с удаления первичной опухоли, решая в последующем вопрос о хирургическом или консервативном лечении метастаза в зависимости от его локализации.
За 1980-2004 гг. в Центральной клинической больнице МЦ на обследовании и лечении находились 833 больных РП (табл. 7). Средний возраст заболевших составил 66,1 (37-94) лет. У 13,4% больных РП впервые был диагностирован уже в диссеминированной стадии.
Таблица 7.
Распределения больных РП по степени распространения процесса (ЦКБ, 1980-2004 гг.).
| Всего | Стадии | ||||
|---|---|---|---|---|---|
| I | II | III | IV | ||
| Количество больных | 833 | 238 | 319 | 164 | 112 |
| % от общего числа | 100 | 28,4 | 38,2 | 20,0 | 13,4 |
Метастазы в кости были выявлены у 70 (8,4%) больных и имели место при всех стадиях (табл. 8): при I стадии – у 5,0%, при II – у 3,1%, при III – у 9,8%, при IV– у 28,6% больных. Наиболее частой локализацией метастазов явились: пояснично-крестцовый отдел позвоночника и кости таза.
8): при I стадии – у 5,0%, при II – у 3,1%, при III – у 9,8%, при IV– у 28,6% больных. Наиболее частой локализацией метастазов явились: пояснично-крестцовый отдел позвоночника и кости таза.
Таблица 8.
Результаты лечения больных РП в ЦКБ за период с 1980 по 2004 гг. в зависимости от стадии заболевания.
| Вид прогрессирования | I cт. | II ст. | III ст. | IV ст. | Всего |
|---|---|---|---|---|---|
| Местный рецидив | 2 | 4 | 5 | — | 11 |
| Метастазы в кости | 12 | 10 | 16 | 32 | 70 |
| Метастазы в другие органы | 15 | 18 | 25 | 80 | 138 |
| Всего | 29 | 32 | 46 | 112 | 219 |
Солитарные метастазы обнаружены у 21 пациента, множественные – у 49 больных. Средний период до определения метастазов в кости у этих больных составил 39,6 (31,7-46,5) мес.: при I стадии — 55,9 (41,3-63,1) мес.; при II стадии – 49,9 (33,5-52,2) мес.; при III стадии — 40,7 (29,7-49,0) мес.
Средний период до определения метастазов в кости у этих больных составил 39,6 (31,7-46,5) мес.: при I стадии — 55,9 (41,3-63,1) мес.; при II стадии – 49,9 (33,5-52,2) мес.; при III стадии — 40,7 (29,7-49,0) мес.
В качестве консервативного лечения чаще всего использовались бисфосфонаты (аредия, зомета), а также локальная лучевая терапия на фоне гормональных препаратов (антиэстрогенов, прогестинов или кортикостероидов). При сочетании костных и легочных метастазов наибольшее распространение получило лечение интерфероном (роферон А, интрон А по 3 млн. №10 через 3-4 недели).
Средняя продолжительность жизни больных с костными метастазами РП составила 34,5 мес.
Лучевая терапия метастазов в кости. При возникновении костных метастазов при различных формах злокачественных новообразований лучевая терапия является одним из наиболее эффективных симптоматических лечебных средств. Основные задачи лучевой терапии заключаются в достижении обезболивающего эффекта, профилактике патологических переломов, а также уменьшении признаков компрессии спинного мозга при поражении позвоночника. Уменьшение болевого синдрома наблюдается более чем у 70% больных и сохраняется на протяжении 5-7 мес., полное исчезновение болей — у 36% больных. Наряду с обезболивающим эффектом лучевая терапия способствует профилактике патологических переломов метастатически измененных костей, а также является методом выбора при метастазах в позвоночник со сдавлением спинного мозга перед оперативным вмешательством (ламинэктомия). В результате облучения костных метастазов наблюдается задержка роста опухоли, восстановление костной структуры на месте деструктивного процесса.
Уменьшение болевого синдрома наблюдается более чем у 70% больных и сохраняется на протяжении 5-7 мес., полное исчезновение болей — у 36% больных. Наряду с обезболивающим эффектом лучевая терапия способствует профилактике патологических переломов метастатически измененных костей, а также является методом выбора при метастазах в позвоночник со сдавлением спинного мозга перед оперативным вмешательством (ламинэктомия). В результате облучения костных метастазов наблюдается задержка роста опухоли, восстановление костной структуры на месте деструктивного процесса.
При определении показаний к назначению лучевой терапии при поражении позвоночника следует иметь в виду сроки возникновения и степень компрессии спинного мозга (тотальный или субтотальный блок), локализацию и распространенность поражения. Облучение предпочтительно начинать в первые дни повреждения (2-5 дней) при отсутствии признаков тотального поражения спинного мозга. Объем облучения определяется зоной поражения, при этом наряду с метастатически измененными позвонками в поле лучевого воздействия включаются рядом расположенные позвонки.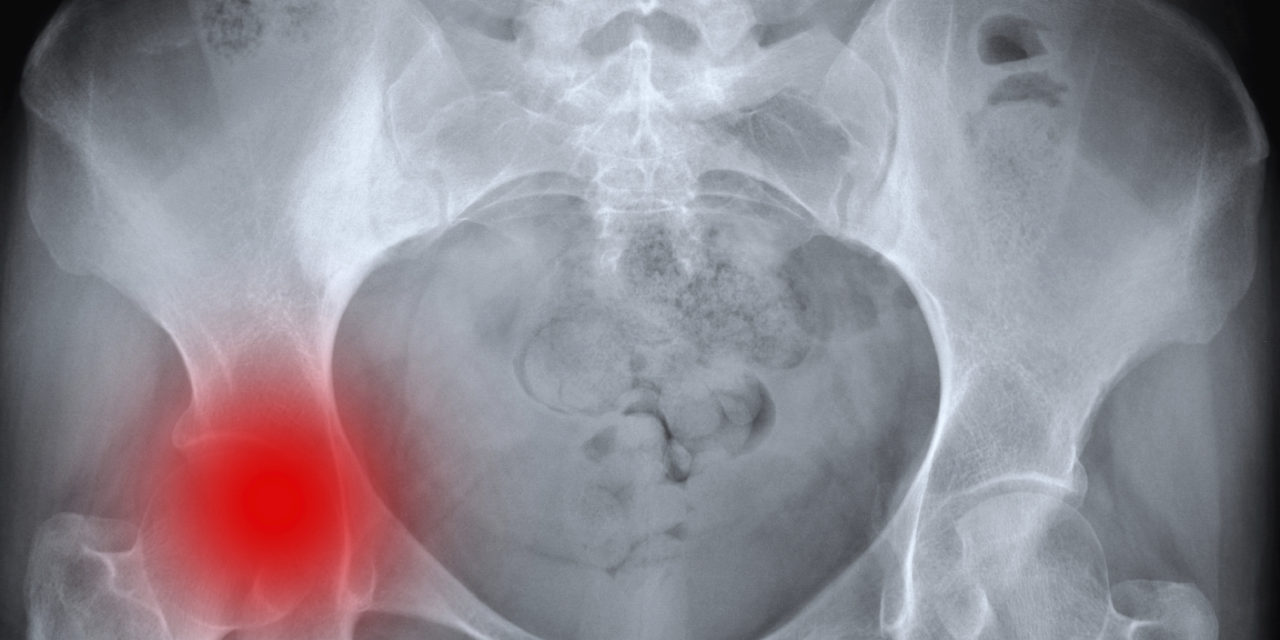 Наиболее часто используется режим фракционирования по 4-5 Гр в сутки, 5-6 фракций до суммарных доз 20-28 Гр, что изоэффективно дозам 36-40 Гр. При локализации метастазов в шейном отделе позвоночника разовая доза уменьшается до 3 Гр и суммарная доза не превышает 18-21 Гр. Важно обеспечить иммобилизацию шейного отдела позвоночника во избежание поражения спинного мозга. Облучение позвоночника целесообразно проводить на фоне дегидратационной терапии кортикостероидами (дексаметазон 8-20 мг/сут.) для профилактики и уменьшения отека спинного мозга. При локализованном единичном поражении позвонка суммарная доза может быть увеличена до суммарных доз 45-50 Гр, при этом предпочтителен режим обычного фракционирования разовой дозой 2 Гр 5 раз в неделю. При множественном поражении позвоночника и выраженных болях у ослабленных больных целесообразно применение ускоренного курса облучения разовыми дозами 6-8 Гр 2-3 фракции с интервалом между ними 2-3 дня. Эти же положения относительно используемого режима фракционирования применимы и к другим локализациям метастазов в кости (ребра, трубчатые кости или кости таза).
Наиболее часто используется режим фракционирования по 4-5 Гр в сутки, 5-6 фракций до суммарных доз 20-28 Гр, что изоэффективно дозам 36-40 Гр. При локализации метастазов в шейном отделе позвоночника разовая доза уменьшается до 3 Гр и суммарная доза не превышает 18-21 Гр. Важно обеспечить иммобилизацию шейного отдела позвоночника во избежание поражения спинного мозга. Облучение позвоночника целесообразно проводить на фоне дегидратационной терапии кортикостероидами (дексаметазон 8-20 мг/сут.) для профилактики и уменьшения отека спинного мозга. При локализованном единичном поражении позвонка суммарная доза может быть увеличена до суммарных доз 45-50 Гр, при этом предпочтителен режим обычного фракционирования разовой дозой 2 Гр 5 раз в неделю. При множественном поражении позвоночника и выраженных болях у ослабленных больных целесообразно применение ускоренного курса облучения разовыми дозами 6-8 Гр 2-3 фракции с интервалом между ними 2-3 дня. Эти же положения относительно используемого режима фракционирования применимы и к другим локализациям метастазов в кости (ребра, трубчатые кости или кости таза). Чем более обширно поражение, тем крупнее используемые разовые дозы и короче курс облучения. При массивном генерализованном поражении костей скелета возможно применение тотального или субтотального облучения половины тела (СТО) с экранированием жизненно важных органов (легкие, сердце, почки). После проведения суммарных доз 15-20 Гр (при СТО) возможно достижение аналгезирующего эффекта в первые дни после облучения.
Чем более обширно поражение, тем крупнее используемые разовые дозы и короче курс облучения. При массивном генерализованном поражении костей скелета возможно применение тотального или субтотального облучения половины тела (СТО) с экранированием жизненно важных органов (легкие, сердце, почки). После проведения суммарных доз 15-20 Гр (при СТО) возможно достижение аналгезирующего эффекта в первые дни после облучения.
При генерализованном поражении костей при РМЖ возможно применение методики последовательного зонного облучения позвоночника, ребер, костей таза и трубчатых костей в сочетании с лучевым воздействием на гипофиз у рецептороположительных больных. Используется режим фракционирования разовой дозой 3-4 Гр 5-6 фракций до суммарных доз 18-24 Гр. При обширном метастатическом поражении костей, особенно при РПЖ, показано использование радиоактивного препарата стронций–89 с периодом полураспада 50,5 дней (метастрон). Введение препарата, содержащего дозу 150 МБк (4 мкюри) в 4 мл раствора приводит к уменьшению или даже полному исчезновению болей у 80% больных на срок 6 мес. Частицы распада радиоактивного стронция с максимальной энергией 1,5 Мэв и проникающей способностью до 8 мм преимущественно накапливаются в патологически измененной кости в местах усиленного обмена. Эффект наступает в сроки от 10 до 20 дней, немаловажным фактором является возможность амбулаторного лечения, а также повторного введения через 3 мес. Токсичность (лейко- и тромбоцитопения) проявляется у 20% больных, носит временный и обратимый характер.
Частицы распада радиоактивного стронция с максимальной энергией 1,5 Мэв и проникающей способностью до 8 мм преимущественно накапливаются в патологически измененной кости в местах усиленного обмена. Эффект наступает в сроки от 10 до 20 дней, немаловажным фактором является возможность амбулаторного лечения, а также повторного введения через 3 мес. Токсичность (лейко- и тромбоцитопения) проявляется у 20% больных, носит временный и обратимый характер.
Таким образом, лечение больных с метастатическим поражением костной ткани должно быть комплексным и основываться на рациональном применении системной терапии и локальных воздействий, которые используются в такой последовательности, чтобы, по возможности, достичь максимальной ликвидации симптомов при наименьшей токсичности используемых препаратов. Лучевая терапия при метастатическом поражении костной системы может быть использована практически у всех больных, и, несмотря на симптоматический характер воздействия, может значительно улучшить качество жизни тяжелого контингента онкологических больных.
Список литературы:
1. Алиев М.Д., Болотина Л.В., Тепляков В.В., Королева Л.А., Карпенко Ю.В., Титов Д.А. Применение зометы в лечении метастатического поражения костей скелета (клинический опыт) Актуальные вопросы клинической онкологии, Том 06/N 3/2004.
2. Давыдов М.И., Аксель Е.М. Злокачественные новообразования в России и странах СНГ в 2000 г.
3. Моисеенко В.М., Семиглазов В.Ф., Тюляндин С.А. Современное лекарственное лечение местно-распространенного и метастатического рака молочной железы. 1997, с. 11–25.
4. Моисеенко В.М. “Естественная история” роста рака молочной железы. Практическая онкология: избранные лекции. Под ред. Тюляндин С.А.а и Моисеенко В.М.. 2004, с. 22.
5. Гарин А.М. Адъювантная и неоадъювантная химиотерапия. Противоопухолевая химиотерапия. Справочник под ред. Н.И. Переводчиковой. 1996, с. 176–7.
6. Тюляндин С.А. Системная терапия операбельного рака молочной железы. Практическая онкология: избранные лекции. Под ред. Тюляндин С.А.а и Моисеенко В.М.. 2004, c. 73–83.
Системная терапия операбельного рака молочной железы. Практическая онкология: избранные лекции. Под ред. Тюляндин С.А.а и Моисеенко В.М.. 2004, c. 73–83.
7. Семиглазов В.Ф. Адъювантная химиотерапия рака молочной железы. Материалы IV Российской онкологической конференции. 2000; с 35–40.
8. Fisher B, Osborne K et al. Neoplasms of the Breast. Cancer medicine 3d edition. Ed. by J Holland et al. Philadelpia: Lea et Febiger, 1993.
9. Fleish H. Bisphosphonates in bone disease. Academic press, 2000.
10. Senartne SG, Pirianov G, Mansi JL et al. Bisphosphonates induce apoptosis in human breast cancer cell lines. Br J Cancer 2000; 82: 1459–68.
11. Bruce E Hillner, James N. Ingle, Roman T. Chlebowski, Julie Gralow et all. American Society of clinical oncology 2003 update on the role of bisphosphonates and bone health issues in women with breast cancer. J Clin Oncol November 1, 2003; 21 (21).
12. Boissier S, Ferrers M, Peyruchaud O et al. Bisphosphonates inhibit breast and prostate carcinoma cell invasion an early event in the formation of bone metastases. Cancer Res 2000; 60: 2949–54.
Метастазы в костях – прогноз, лечение и симптомы при раке 4 степени
Метастазы в костях могут развиться абсолютно при любом злокачественном процессе, для некоторых раков это практически обязательная локализация, при других заболеваниях — редкость. В метастатическом рейтинге первое место по частоте встречаемости достанется метастазам в лёгкие, второе — печеночным очагам и третье — скелетным метастазам.
Метастазы в костях трудно лечатся и обещают боли, тем не менее, скелетные очаги менее прочих локализаций опухоли сокращают жизнь, но способны испортить её переломом или сдавлением спинного мозга.
Какими могут быть метастазы в костях?
По клинико-рентгенологическим признакам все костные очаги подразделяют на три группы:
- остеобластические — с преобладанием уплотнения сверх физиологической меры, но дополнительно наросшая опухолевая ткань не придаёт кости прочности и может сдавливать проходящие по соседству нервы;
- остеолитические — превалирует разрушение структуры и вероятность перелома увеличивается по мере разрастания рака;
- смешанные — сочетание двух видов и это ситуация встречается чаще всего.

Практически не случает такого, чтобы у пациента были исключительно остеолитические или только остебластические очаги, как правило, диагностируется сочетание с превалированием либо разреженной литической, либо избыточной бластической структуры.
При каких раках развиваются?
Лидер среди всех злокачественных процессов, протекающих с метастатическим поражением скелета, миеломная болезнь — разрушение кости начинается в самом начале заболевания и в 100% клинических случаев отмечается множественная деструкция костной ткани.
При раке молочной и предстательной желёз у двух третей больных диагностируются скелетные метастазы, а патологоанатомические наблюдения выявляют вовлечение костей в злокачественный процесс практически у 90% пациентов. При раке молочной железы (РМЖ) превалируют смешанные и остеолитические варианты, при раке простаты — остеобластические.
Высокая частота метастазирования в кости отмечается при раке легкого, но при мелкоклеточном варианте — вдвое чаще и множественные костные дефекты, тогда как при немелкоклеточном — у 40% больных с тяготением к очагам единичным или солитарным, то есть единственному.
Каждый четвёртый, страдающий раком почки, имеет скелетные метастазы, при карциноме мочевого пузыря костные новообразования встречаются много реже.
При раке толстой кишки костное метастазирование выявляется у каждого восьмого больного, при раке желудка — не часто, поскольку раньше и обильнее рак поражает печень и брюшную полость. Рак кишечника тяготеет к мелкоочаговым и множественным вторичным образованиям.
Когда появляются скелетные метастазы?
При злокачественных процессах время появления метастазов в кости различается, тогда как скорость роста очага зависит исключительно от индивидуальных биологических характеристик опухолевой ткани, меняющихся под воздействием лечения и по мере раковой диссеминации.
При первичном обращении костные очаги при отсутствии других проявлений ракового процесса имеются едва ли у 20% пациентов, в подавляющем большинстве случаев опухолевое поражение костей признак диссеминации рака — распространения по системам или генерализации. При РМЖ, немелкоклеточной карциноме легких и раке толстой кишки именно так и происходит.
При РМЖ, немелкоклеточной карциноме легких и раке толстой кишки именно так и происходит.
При раке предстательной железы нередко скелетная патология обнаруживается одновременно с опухолью простаты или в ближайшие сроки после диагностики неблагополучия в половой железе.
При карциноме почки часто сначала находят метастазы в костях и легочной ткани, а после обнаруживается первичная опухоль.
Какие отделы скелета поражаются чаще всего?
Локализация метастаза в кости определяется не нозологической принадлежностью первичной злокачественной опухоли, а функциональной нагрузкой и связанной с нею развитостью кровоснабжения. Множественные очаги в скелете более характерны для высоко агрессивного рака, единичные и тем более один метастаз свидетельствует в пользу благоприятного прогноза заболевания.
- Чаще всего вторичные отсевы рака возникают в обильно питаемых кровью губчатых костях — позвонках, причём преимущественно в испытывающих высокую нагрузку поясничных и грудных отделах позвоночника.

- Далее по частоте следуют метастазы в костях таза — почти половина всех случаев, типичные локализации — подвздошная и лонные кости.
- Вполовину реже отмечается метастазирование в костях черепа и нижней конечности, где превалирует поражение бедренной кости.
- Грудная клетка, преимущественно ребра и грудина, вовлекаются в злокачественный процесс практически в 30% случаев.
Клинические проявления костного метастазирования
Вопреки сложившимся мифам, скелетное метастазирование часто протекает без выраженной боли и даже вовсе без симптомов. Остеобластические очаги реже сопровождаются болевыми ощущениями, нежели остеолитические.
Опасные проявления метастатического костного поражения:
- гиперкальциемия — значительное повышение концентрации кальция из-за разрушения костного матрикса приводит к тяжелейшему состоянию, требующему коррекции метаболизма фактически реанимационными мерами;
- перелом — для возникновения достаточно разрушения половины поперечника кости или позвонка, каждому одиннадцатому пациенту с патологическим переломом необходима срочная хирургическая помощь;
- синдром сдавления или компрессии спинного мозга осколками сломанного грудного или поясничного позвонка осложняется тяжелыми неврологическими нарушениями ниже зоны повреждения;
- нарушение двигательной активности вплоть до паралича возможно при сдавлении спинного мозга в шейном отделе остеобластическим очагом или повреждении отломками при литическом разрушении.

Осложнения метастазирования в кости фатально отражаются на состоянии пациента и активно мешают проведению адекватного лечения, что может сократить срок жизни при безусловном отсутствии качества.
Почему возникает боль?
Боль обусловлена тремя причинами:
- разрушением раковым конгломератом обильно иннервированной надкостницы;
- раздражением в надкостнице болевых рецепторов биологически активными продуктами жизнедеятельности раковых клеток;
- вовлечением в метастатический узел нервных окончаний мышц.
Невыносимая боль далеко не всегда связана со скелетным метастазированием, как правило, это следствие высокой агрессивности опухолевых клеток в терминальной стадии процесса, когда в крови огромна концентрация биологически активных веществ — цитокинов, которые буквально «жгут» нервные окончания даже не поражённых опухолью тканей.
При высокой степени злокачественности первичной опухоли болевой синдром отмечается чаще и более интенсивный. Наиболее наглядный пример, распространенные и постоянные боли в абсолютно целых костях при аденокарциноме легкого, операция с удалением пораженного легкого полностью излечивает боль.
Наиболее наглядный пример, распространенные и постоянные боли в абсолютно целых костях при аденокарциноме легкого, операция с удалением пораженного легкого полностью излечивает боль.
Как обнаруживают метастазы в кости?
Диагностика скелетных повреждений не сложная, но высокотехнологичная, начинают с изотопного обследования — остеосцинтиграфии, выявляющей минимальные раковые новообразования.
Затем засвеченные изотопом «горячие очаги» подвергают рентгенографии или, что лучше, компьютерной томографии (КТ).
ПЭТ — «королева» доказательств, к сожалению, дорогое исследование, поэтому для контроля эффективности терапии не очень подходит.
- Для выявления очагов в скелете маркеры костной резорбции не подходят, в практической онкологии активного применения не нашли.
- Анализы крови позволяют заподозрить опухолевое поражение костного мозга, что часто сопровождает метастазирование в грудину.
Лечение скелетных поражений
Можно ли вылечить метастазы в костях? Однозначно лечением можно продлить жизнь при хорошем самочувствии. С одной стороны, скелетные поражения — манифестация распространения рака по организму, с другой — признак относительно благоприятного прогноза заболевания при отсутствии опухоли в других тканях и висцеральных (внутренних) органах, что даёт годы жизни при стабилизации процесса.
С одной стороны, скелетные поражения — манифестация распространения рака по организму, с другой — признак относительно благоприятного прогноза заболевания при отсутствии опухоли в других тканях и висцеральных (внутренних) органах, что даёт годы жизни при стабилизации процесса.
На этапе костного метастазирования вопрос о радикальном лечении уже не стоит, но операция не исключается при благоприятной гистологической структуре и солитарном — единственном костном поражении.
Так при раке легкого или почки с метастазом в плечевую кость или бедро можно выполнить одномоментное вмешательство с удалением больного органа и резекцией кости с протезированием, но после нескольких месяцев химиотерапии.
Химиотерапия — главный метод лечения костных поражений, лекарственная схема определяется первичной опухолью. При раке молочной и предстательной железы хорошие результаты демонстрирует гормональная терапия.
Дополнение химиотерапии локальным облучением позволяет повысить общий результат терапии, снять боль и уменьшить вероятность перелома.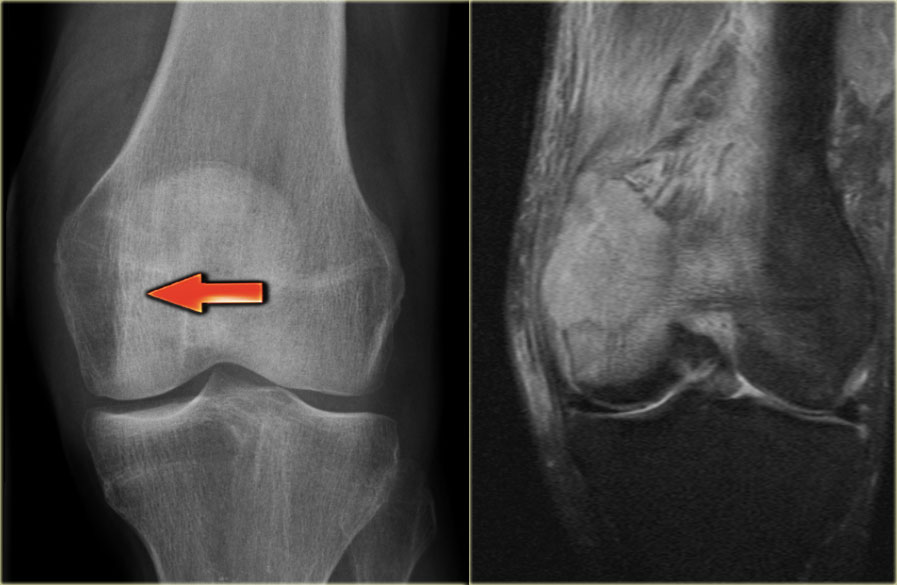 Так при поражении шейных позвонков лучевая терапия обязательна уже на первом этапе.
Так при поражении шейных позвонков лучевая терапия обязательна уже на первом этапе.
Операция необходима при угрозе сдавления (компрессии) спинного мозга поломанным позвонком, как правило, удаляется поражённая часть позвонка — ламинэктомия. При длительной — более полугода стабилизации в результате химиотерапии можно поставить вопрос об удалении поражённой кости конечности с заменой на протез, если больше нет других проявлений рака.
Зачем нужны бисфосфонаты?
Использование бисфосфонатов при метастатическом поражении скелета стало стандартом адекватной терапии.
Человеческие кости постоянно обновляются: остекласты разрушают, а остеобласты наращивают ткани, в норме процессы уравновешены, в присутствии злокачественной опухоли остеокласты приобретают избыточную активность.
Бисфосфонаты по своему строению схожи с костным матриксом, поэтому после введения в организм направляются в кости, где губительно действуют на активизированные раковыми продуктами остеокласты, параллельно снимая боль и оберегая от переломов.
Бисфосфонатами можно лечиться около двух лет, при утрате чувствительности к ним аналогичную роль выполняет моноклональное тело деносумаб. Демосумаб и бисфосфонаты относят к остеомодифицирующим агентам (ОМА).
Для назначения ОМА недостаточно выявления «горячих» очагов при остеосцинтиграфии, их применяют при доказанном рентгенологическими методами опухолевом поражении.
Химиотерапия и ОМА — основные методы лечения скелетных поражений, но не единственные. Лечение костных метастазов должно быть комплексным, только комбинацией облучения и лекарств, с коррекцией метаболизма и присоединением паллиативной хирургии можно избавить от боли и вернуть пациенту активную жизнь.
Когда и что нужно и возможно в каждом конкретном клиническом случае онкологического заболевания знают специалисты нашей клиники. Узнайте больше, звоните:
Список литературы:
- Алиев М.Д., Тепляков В.В., Каллистов В.Е., Валиев А.К., Трапезников Н.Н. / Современные подходы к хирургическому лечению метастазов злокачественных опухолей в кости// Практическая онкология, № 1(5) (март), 2001
- Белозерова М.
 С., Кочетова Т. Ю., Крылов В. В. Практические рекомендации по радионуклидной терапии при метастазах в кости // Злокачественные опухоли, № 4, 2016, Спецвыпуск 2.
С., Кочетова Т. Ю., Крылов В. В. Практические рекомендации по радионуклидной терапии при метастазах в кости // Злокачественные опухоли, № 4, 2016, Спецвыпуск 2. - Кондратьев В.Б., Мартынюк В.В., Ли Л.А. / Метастазы в кости: осложненные формы, гиперкальциемия, синдром компрессии спинного мозга, медикаментозное лечение// Практическая онкология, № 2 (июнь), 2000
- Манзюк Л.В., Багрова С. Г., Копп М.В., Кутукова С.И., Семиглазова Т.Ю/ Использование остеомодифицирующих агентов для профилактики и лечения патологии костной ткани при злокачественных новообразованиях // Злокачественные опухоли: Практические рекомендации RUSSCO #3s2, 2017 (том 7)
- Снеговой А. В., Багрова С. Г., Болотина Л. В., Владимирова Л. Ю., Горбунова В. А., Когония Л. М./ Профилактика и лечение патологии костной ткани остеомодифицирующими агентами (ОМА) при злокачественных новообразованиях // Злокачественные опухоли, № 4, 2016, Спецвыпуск 2.
4 стадия рака: сколько живут, можно ли вылечить, распространение метастазов
Четвёртая стадия рака – самая тяжёлая. Человек страдает не только от физической боли, но и от моральной. Как правило, больной и его родственники уже смирились с тем, что заболевание не вылечить, однако надеются облегчить страдания и снизить болевой синдром.
Человек страдает не только от физической боли, но и от моральной. Как правило, больной и его родственники уже смирились с тем, что заболевание не вылечить, однако надеются облегчить страдания и снизить болевой синдром.
Характеристика 4 стадии онкологии
4 стадия рака – это финал карциномы, когда метастазы начинают распространяться по соседним тканям и органам. Раковые клетки паразитируют по всему организму. Отягчающим обстоятельством клинической картины становится поражение нервной системы и головного мозга, что негативно сказывается на поведении и психоэмоциональном состоянии пациента.
Запущенные случаи онкологии обнаруживают яркие симптомы:
- Воспаление и болезненные ощущения в лимфоузлах. Это органы, куда рак распространяется с метастазами в первую очередь, а к 4 стадии заболевания злокачественная клетка рождает там вторичные опухоли.

- Жёлтый оттенок кожи по причине нарушений в печени.
- Потеря веса, обусловленная сниженным аппетитом, сбоями в работе кишечника. Тошнота и рвота. Ввиду патологического процесса в организме потребность человека в пище и еде снижается. Едва больной стал отказываться от приёмов пищи, следует установить круглосуточное дежурство у постели. Отказ от еды свидетельствует о наступлении терминальной стадии карциномы, придавая заболеванию критический характер. Больной постепенно утрачивает способность к самообслуживанию и нуждается в посторонней помощи.
- Слабость, утомляемость. К апатии и слабости приводит анемия, причина которой в сниженном аппетите. Повышенная утомляемость обусловлена дисфункцией многих внутренних органов в результате онкопоражения, интоксикацией организма и внутренними кровотечениями.
- На фоне раковой интоксикации и в результате воспалительного процесса в организме происходит повышение температуры. Высокая температура держится практически постоянно.

- Ярко выраженный болевой синдром, обусловленный сдавливанием внутренних органов разросшейся опухолью. Внутренняя деформация органов приводит к застою желчи, образованию тромбов, проблемам с печенью и почками. Для облегчения болевого синдрома больному делают инъекции с морфием. В последние дни болезни даже мощные опиаты не снижают болевые ощущения.
- Ишемия, обусловленная дисфункцией почек и нарушением обмена веществ.
Рак 4 стадии поражает кожные покровы.
Запущенность заболевания и игнорирование первых тревожных симптомов влекут непоправимые последствия.
Признаки разновидностей онкологии
Онкологический процесс имеет особые признаки, которые определяются расположением очага опухоли:
- Кашель со сгустками крови характерен при онкологии горла и поражении лёгких. Указанный симптом наблюдается, когда рак поражает носоглотку.
- Дисфагия и кровавые рвотные массы отмечаются, когда опухоль поражает кишечник.
- Поражения кожных покровов незатягивающимися язвочками, вокруг которых присутствует лёгкая припухлость, возможны при меланоме.

- Выделения из женских половых путей, имеющие острый неприятный запах, свойственны раку шейки матки.
- Половая дисфункция характерна при карциноме простаты.
- Ломота мучает больного при онкологии в костных тканях.
- Внезапная слепота и мучительная головная боль, нарушение координации движений и глухота, провалы в памяти свидетельствуют о поражении опухолью головного мозга.
Предсмертные признаки
Если у пациента диагностирована четвёртая стадия рака, значит, отмечаются предсмертные признаки. В последние дни жизни больной много спит, находясь под действием сильнодействующих опиатов. Его близким нужно принять н6еизбежность скорой смерти и знать предвестники приближения печального события:
- Безучастное отношение к событиям окружающей действительности, апатия, отстранённость, равнодушие, негативные мысли. Возникают в результате того, что человек смирился со скорой кончиной.
- Отклонения в работе центральной нервной системы, которые проявляются в неадекватных эмоциональных реакциях, отсутствии физической активности.

- Предкома и кома. Важно то, что в таком состоянии больные продолжают слышать, поэтому близкие должны оказывать им внимание и поддержку.
- Предагония. Состояние длится несколько дней и сопровождается галлюцинациями, резким понижением артериального давления, бледностью кожных покровов и синюшностью слизистых оболочек.
- Клиническая смерть. Данный феномен характеризуется прекращением работы всех органов и систем организма, но продолжается обменный процесс на клеточном уровне. Причина возникновения клинической смерти – ограниченное поступление кислорода к головному мозгу. Если такое состояние возникает при других заболеваниях, есть надежда вернуть человека к жизни в течение 4-5 минут без дальнейших тяжёлых последствий. При раке 4 стадии это сделать невозможно. Клиническая смерть при карциноме, по сути, является летальным исходом.
- Отсутствие признаков работы мозга и функционирования органов и систем.
- В результате кислородного голодания и нарушения циркуляции крови возникает агония, которая появляется перед смертью.
 Кислородное голодание проявляется прерывистым дыханием, которое на 1-2 секунды может пропадать совсем. Дыхание становится поверхностным, выдохи по продолжительности превышают длительность вдоха. Хлюпанье и посвистывающие звуки при дыхании объясняются тем, что дыхательный орган повреждён метастазами.
Кислородное голодание проявляется прерывистым дыханием, которое на 1-2 секунды может пропадать совсем. Дыхание становится поверхностным, выдохи по продолжительности превышают длительность вдоха. Хлюпанье и посвистывающие звуки при дыхании объясняются тем, что дыхательный орган повреждён метастазами.
Для облегчения дыхательного процесса врачи рекомендуют к использованию кислородную подушку – так кислород поступает сразу в лёгкие, минуя верхние дыхательные пути. Кроме того, облегчить состояние человека можно, смачивая его губы и внутреннюю поверхность рта водой.
В агонии люди живут 3-4 часа, потом наступает смерть. Признаком наступления смерти является прекращение функционирования клеток мозга. При этом у больного кожа становится холодной, появляются капельки холодного пота.
Даже в предсмертном состоянии обращение за медицинской помощью помогает облегчить боль и продлить жизнь хотя бы на несколько недель.
Терапия 4 стадии карциномы
На указанной стадии воспрепятствовать патологическому процессу невозможно.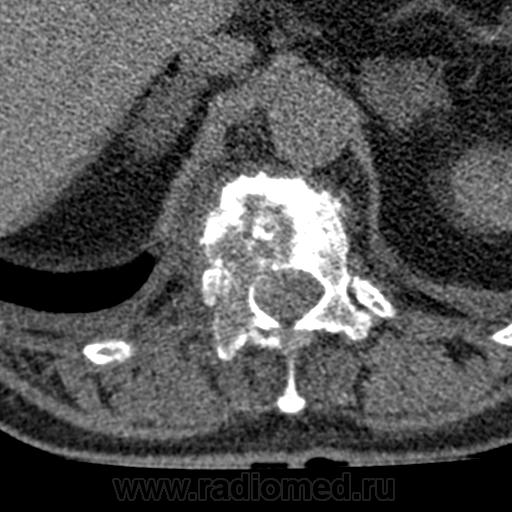 Даже после операции возможны негативные последствия. Но прогноз по заболеванию определяется локализацией основного онкоочага. Применяется паллиативная терапия.
Даже после операции возможны негативные последствия. Но прогноз по заболеванию определяется локализацией основного онкоочага. Применяется паллиативная терапия.
Для уменьшения метастазов применяют химию и радиоактивное облучение. Соблюдение рекомендаций врача и комплексное лечение, сопровождающееся медикаментозной терапией, продлевают жизнь больного на несколько лет.
Важно помнить, что ни одно лекарство от рака не способно гарантированно помочь пациенту. Болезнь не лечится полностью, но терапия способна помочь больному.
Психологическая помощь
Больным с 4 стадией рака требуется поддержка близких. Карцинома поражает тело, все органы – больной чувствует момент приближающейся смерти и собственную ненужность.
Родственники должны создать больному максимально комфортные условия для проживания последних дней жизни.
Тихая фоновая музыка умиротворяет, а беседа с человеком о его жизни помогает ему переосмыслить прожитое, выделить наиболее значимые достижения, насладиться воспоминаниями о приятных событиях.
Больным приятно слушать, когда родственники читают вслух их любимые произведения художественной литературы. Всё это способствует лёгкому отношению к смерти.
Не всегда близкие способны оказать психологическую помощь больному, зная, что победить этот недуг невозможно. Поэтому предусмотрено обслуживание таких пациентов в хосписах – организациях, где психологи и социальные работники оказывают помощь больному и создают условия для комфортного доживания отмеренного срока.
В хосписах оказывают помощь не только онкобольным, но и их родственникам, обучая их правильному уходу за больным, помогая находить с ним общий язык и спокойно реагировать на неприятные поведенческие реакции.
Болезнь взрослого родственника тяжело переживают дети – в хосписах психологи помогают им принять этот неизбежный факт.
Последняя стадия рака крайне тяжёлая. Нельзя оставлять больного наедине со своими болями в последние дни и часы жизни. Зная, что родные его не оставили, чувствуя их заботу и любовь, больной легче отходит в иной мир.
Прогноз по карциноме 4 степени
Больных и их родственников волнует статистика: излечим ли пациент с раком 4 степени? Врачи с осторожностью озвучивают родственникам примерную продолжительность жизни пациента, предпочитая отвечать на вопросы о том, сколько человеку осталось жить, уклончиво. Это раздражает родственников, потому что им хочется конкретики. Однако дать точный ответ врачи не могут, так как последняя стадия рака имеет крайне неблагоприятную клиническую картину.
Финальная стадия карциномы характеризуется бесконтрольным делением онкоклеток, спрогнозировать скорость этого процесса не представляется возможным.
Скорость распространения метастазов по соседним тканям и органам может осуществиться за 30 дней, а возможно прожить с раком много лет, если метастазы прогрессируют слабо.
Выраженность агрессивности при онкологии определяется возрастом пациента, используемой терапией и локализацией первичного очага рака.
Прогнозы врачей на выживаемость утешительны для отдельных типов карциномы. Локализация первичной опухоли имеет определяющее значение при формулировании прогноза.
Так, онкологическое заболевание лёгких на 4 стадии имеет относительно положительный прогноз: на паллиативной терапии и курсах радиоактивного облучения, химиотерапии человек живёт с тяжёлым недугом до 5 лет. Если поражена печень, часть желудка и поджелудочной железы – прогноз неблагоприятный: человек протянет максимум полгода.
Метастазы в костях – прогноз, лечение и сколько живут
Метастазирование в кости это тяжелое раковое осложнение с сильными болевыми симптомами, означающее переход рака в 3, 4 стадию. Прогноз лечения и продолжительность жизни при этом значительно снижаются, сколько живут с метастазами в костях зависит от применяемой терапии и агрессивности первичного очага
Процесс метастазирования это страшное осложнение, которое всегда происходит при раке, если болезнь вовремя не выявлена и не начато ее лечение.
Обычно метастазы образуются в мягких тканях, органах, но иногда ими поражаются и кости.
Метастазу в костных структурах следует рассматривать как еще один эпизод рака, когда аномальные клетки из первичной опухоли, перемещаясь по организму, осаждаются в элементах скелета.
Метастазы в костях появляются на поздних стадиях развития патологии, в 4-х из пяти случаев первичные опухоли это рак молочной железы для женщин и простаты у мужчин.
Такая ситуация не имеет хорошего прогноза, пациент страдает от симптомов сильных болей, ослабленные кости переламываются даже при незначительном воздействии.
Первичное онкологическое поражение почек и щитовидной железы, ведет к метастазированию в структурах черепа.
Причины
Кроме перечисленных видов рака от метастазирования в костные ткани страдают при злокачественных опухолях легких, почек, яичников у женщин, саркоме, лимфоме и поражении органов желудочно-кишечного тракта. В резких случаях бывает миграция атипичных клеток и из других охваченных болезнью органов.
Появление тяжелых признаков и симптомов болезни связано с нарушением постоянного обновления тканей костей, существующее у здорового человека.
Нормальное клеточное взаимодействие, элементами которого выступает резорбция, ремоделирование и костеобразование, нарушается, так как остеобласты и остеокласты, отвечающие за указанный функционал, блокируются раком.
В итоге, в кости наблюдается вытеснение здоровых и полезных тканей, место которых занимает метастаза.
Рак молочной железы частая причина костного метастазирования. При таком женском заболевании злокачественные структуры посредствам лимфогенного или гематогенного перемещения, перемещаются и накапливаются в костях, преимущественно таза и груди.
Течение недуга сопровождается интенсивными болями, свою лепту в которые вносят регулярные переломы. Обычно это означает 4 степень рака, продолжительность жизни и выживаемость при которой небольшая.
Виды метастаз в костях
Исходя из разновидности активизации онкологии, выделяется несколько их типов:
- Остеопластическими называют ситуацию образования плотных участков, внедренных в кость.
- К остеолитическим относят процесс разрушения костной ткани.
Любой случай заболевания это комбинация из двух указанных патологических процессов. Наиболее часто метастазы случаются в костях, активно питаемых кровью, они образуются в:
- Плечевой зоне
- Тазу
- Ребрах
- Черепе, элементах позвоночника
На ранних стадиях образования не имеют никаких признаков, позже появляются симптомы боли и другие проявления.
Симптомы метастаз в костях
Ранняя степень метастазирования протекает бессимптомно, но по мере роста, воздействие онкологии на кость становится более явным, и появляются первые признаки:
- Гиперкальциемия. Так именуют последствие метастазы в кости, встречающееся в более чем трети больных. Патология вызывает повышенную активность остеокластов, из-за чего резко повышается кальций в крови. Это ведет к повышенной нагрузке на почки, что грозит нарушением обратной всасываемости и чрезмерному выделению мочи.
- Патологические переломы.
- Спинномозговая компрессия при опухоли в позвоночнике.
В результате гиперкальцемии и пережатия спинномозговых каналов у человека появляются следующие симптомы:
- Со стороны нервной системы онкобольной с метастазами в костях страдает от заторможенности, неуравновешенной психики, спутанного сознания, аффективных нарушений.
- Сердце и сосуды начинают неправильно функционировать, что заканчивается аритмией, пониженным артериальным давлением, низкой частотой сердечных сокращений. Все это граничит с сердечной недостаточностью и мгновенной смертью.
- Вероятна почечная недостаточность из-за интенсивной нагрузки на них
- Желудочно-кишечный тракт страдает от расстройства, больного часто подташнивает, отсутствует аппетит, запор переходит ведет к кишечной непроходимости и т.д.
В условиях, когда метастазы в костных тканях разрушают больше 50% кортикального слоя, резко возрастает вероятность переломов. От этого страдают кости позвоночного столба в пояснице или грудном отделе и бедра. Незначительное превышение нагрузки заканчивается переломов кости и симптомами сильнейшей боли.
По причине метастазов в костях они настолько ослабевают, что нередко ломаются вообще сами по себе. При этом из-за относительного смещения в месте слома, функционал конечности или костного элемента полностью теряется. Не успев срастись, происходит еще один слом и так далее. В итоге человек практически обездвижен и ему грозит инвалидность с необходимостью постоянного обезболивания.
Дальнейший рост злокачественной опухоли ведет к сдавливанию сломанными костями мягких тканей, располагающихся рядом. Это грозит постоянными сильнейшими болями, слабостью мышц, нарушенной чувствительностью. Продолжительность жизни при таких осложнениях очень мала, терминальная стадия ведет к параличу и отказу органов таза.
В таких условиях жизнь с метастазами в костях становится серьезным испытанием. Речи об излечении уже не идет, задача медиков состоит в улучшении условий существования.
При метастазировании костей позвоночника существует риск спинномозгового пережатия. Часто это явление наблюдается при локализации в грудной части позвоночного столба. Симптомы формируются последовательно, по мере усиления давления на спинной мозг, проходящий в специальном позвоночном канале. Резкое появление признаков происходит при переломе позвоночного элемента.
Если вовремя заметить и начать лечить спинномозговое пережатие, то его последствия обратимы, на поздних стадиях признаки паралича будут становиться все более явными, несмотря лечение.
Статистика говорит, что лишь каждый десятый онкопациент способен к самостоятельному перемещению после развития паралича.
Диагностика
Надежное и информативное диагностирование костного метастазирования возможно при помощи скелетной сцинтиграфии. Метод позволяет понять, насколько распространено образование, и на какой степени оно находится.
Данной процедурой находят метастазы в любых костях человеческого туловища и конечностей. Эффективно выявляются даже начальные стадии недуга, когда симптомы еще не проявлены. Итогом лечения на данном этапе будет значительное улучшение прогноза и продолжительности жизни.
Более доступный и бесконтактный метод это рентген. Однако он выявляет лишь зрелую вторичную метастазу, когда разрушению уже подвергся значительный объем кости. Преимущество рентгенологии заключается возможности дифференцирования вторичного новообразования, исходя из его типа. Разная окраска пятен на фото, будет говорить о различной их природе.
На более поздних этапах диагностики для уточнения диагноза и метода лечения применяют:
- КТ и МРТ
- Радиоизотопное диагностирование
- Остеосцинтиграфию
- Анализы мочи и крови
При обнаружении опухоли в черепе, проводятся дополнительные обследования для исключения поражения соседних органов.
Лечение
То, чем и как лечить метастазы в костях будет зависеть от локализации патологии, степени ее развития и параметров исходного рака. Перечислим основные методы лечения:
- Операции применяются в рамках паллиативной помощи, когда улучшение прогноза выздоровления невозможно и больной уже неизлечим, но нужно максимально продлить срок жизни и улучшить ее качество. Благодаря хирургической удалению опухолей удается уменьшить сдавливание нервных окончаний спинного мозга, уменьшить вероятность сломов костей. Все это значительно снижает болевой синдром и частично возвращает потерянные анатомический функционал.
- Применение лучевой и химиотерапии используется для подготовки пациента к операции, либо после нее, а также как самостоятельное лечение. Путем химического или лучевого уничтожения онкоклеток удается остановить рост метастаз в костях.
- Прием бисфосфонатов. Это специальные препараты, тормозящие разрушение костной ткани.
- При некоторых видах рака эффективно использование радиофармпрепаратов.
- Активизация иммунной системы позволяет продлить продолжительность жизни человека. За счет активизации собственных сил организм лучше начинает бороться со злокачественным распространением, изнутри помогая внешнему лучению.
Бисфосфонатные препараты
Так называют лекарства, защищающие костные структуры от разрушения. Они показаны при остеокластной патологии для компенсации вредного действия метастаз.
Благодаря поглощению басфосфоната в месте, где произошло метастазирование, негативная деятельность замедляется или совсем прекращается.
В дополнение препарат тормозит выработку остеокластов, которые быстро погибают или самостоятельно разрушаются. Механика действия состоит в накапливании активного вещества вокруг образования.
При наборе необходимой массы начинается позитивное воздействие по угнетению разрушающей функции.
Бывает два вида бисфосфонатов. Первые состоят из азотистых соединений и более действенны в отношении метастаз в костях. Вторая группа лишена таких соединений и лечение с ее помощью менее эффективно. Что конкретно назначить будет зависеть от финансовых возможностей больного и стадии развития новообразования.
Прогноз и продолжительность жизни
Сколько конкретно живут пациенты с метастазированием в костях невозможно. Примерно это сделать можно увидев историю болезни. Для точного прогноза выживаемости врачу надо проанализировать много информации о метастазе и других раковых новообразованиях.
Приведем цифры сколько живут люди с метастазами в костной ткани в зависимости от первичной онкологии:
- Метастазирование рака легкого и меланомы дает продолжительность жизни около 6 месяцев.
- Простата – 1-3 года
- Рак молочных желез – 18-24 месяца
- Почки с костным метастазированием дают человеку до 12 месяцев жизни
- Самый лучший прогноз при злокачественном поражении щитовидной железы. С рассматриваемыми в статье осложнениями люди живут еще до 4-х лет.
Рак кости 4 степени с метастазами в кости продолжительность жизни
Кости, как и любая другая ткань человеческого организма подвержена онкологическим заболеваниям. Тем не менее, рак костей в современном мире диагностируется не так часто, как злокачественные образования в других органах.
Обусловлено это спецификой строения костей. На общем фоне онкологических болезней рак костей занимает лишь 1 % от общего числа патологий данной категории.
Если диагностирован рак кости 4 степени с метастазами в кости продолжительность жизни во многом зависит от адекватного лечения.
Несмотря на редкость болезни, она по-своему коварна, так как ее симптомы похожи на другие недуги, либо же их и вовсе можно спутать с накопленной усталостью на протяжении дня.
В связи с этим, много, кто из заболевших обращается за врачебной помощью слишком поздно, когда рак костей уже перешел на четвертый этап своего развития.
По сути это уже финальная стадия заболевания, когда из пораженной кости, идет активное метастазирование перерожденных клеток в здоровую костную ткань.
Пациенты, столкнувшиеся с данной болезнью, задают себе практически всегда один и тот же вопрос: сколько живут с раком костей 4 степени? Конечно же ни один врач онколог не может дать утверждающий ответ, сколько осталось жить тому или иному пациенту. Все зависит от индивидуальных особенностей организма больного, от типа опухоли, и как она реагирует на медицинские препараты.
Симптомы, указывающие на рак костей 4 стадии с метастазами
Злокачественное образование, появившееся в кости — практически всегда ведет себя агрессивно, стремительно развивается и переходит с одной стадии на другую. Первые симптомы, говорящие о том, что у человека есть рак костей — это устойчивые болевые ощущения в области пораженной конечности, повышение температуры до 37.6 градусов.
Боль не является острой, но она практически не прекращается ни на минуту. Это ноющие болевые ощущения, которые могут исходить из одного участка кости, либо же распространяться по всей конечности. Например, если опухоль в коленном суставе, то может тянуть всю ногу до самой пятки.
По мере развития опухоли чувство боли только усиливается. Тогда присоединяются дополнительные симптомы в виде бледности кожных покровов в месте нахождения опухолевого тела, ярко выраженной венозной сетки на коже. Человек начинает стремительно терять вес, пропадает аппетит, появляются головные боли.
Как правило, на 4 стадии рак костей можно нащупать пальцами руки в виде образования. Это говорит о том, что костная ткань полностью поражена опухолью, и по телу больного распространяются метастазы. Окончательный диагноз ставится врачом онкологом после комплексной диагностики костных тканей больного с помощью специальных анализов и медицинского оборудования.
Прогнозы выживаемости для больных раком костей 4 степени с метастазами
Рак кости 4 степени с метастазами в кости продолжительность жизни. В каждом случае длительность последней стадии онкологии составляет разный период времени. Как правило, зависит она от того, насколько обширным является метастазирование, какие еще органы, кроме костной ткани были поражены вторичными опухолевыми образованиями.
Доброкачественные образования костей лечатся гораздо легче, имеют другие симптомы, и больные становятся на ноги в сравнительно короткий промежуток времени.
Рак костей 4 стадии с метастазами — все же относится к категории злокачественных новообразований, и в таком случае опухоль ведет себя в организме человека абсолютно по другому.
Несмотря на это, при правильно сформированном курсе лечения можно добиться положительного эффекта, и продлить жизнь пациента до 5 лет.
В таком случае лечащим врачом может применяться самая разная терапия. В основу курса лечения входят препараты химиотерапии, традиционные противоопухолевые медикаменты, и хирургическое вмешательство в случае необходимости.
Если же метастазы еще не распространились вглубь скелета, а опухоль, например, находится в нижней части конечности, то хирургическая операция по удалению злокачественного образования, либо же конечности в целом — может стать спасением для жизни больного. А уже курс ударной химиотерапии подавит оставшиеся раковые клетки.
В целом же прогноз на выживаемость при раке кости 4 стадии с обширным метастазированием — неблагоприятный. Лишь 20% больных преодолевают пятилетний рубеж жизни с этой болезнью, и то, при условии предоставления им качественной медицинской помощи в условиях стационара, который периодически сменяется на амбулаторный режим лечения.
Остальные пациенты умирают еще на более ранних сроках. Основная причина смерти на последней стадии рака — это метастазы злокачественного образования, которые поражают не только полностью кость с опухолью, но и соседние костные ткани. Более того, раковые клетки вместе с кровотоком способны попадать в здоровые органы человека.
Чтобы не запускать болезнь до четвертой стадии, нужно прислушиваться к сигналам своего организма. Если присутствуют симптомы онкологической болезни костей, то нельзя терять ни минуты. Следует обратиться к врачам за медицинской помощью.
Информативное видео
от рака молочной железы до костных метастазов
Статья на конкурс «био/мол/текст»: Диагностирование рака молочной железы с метастазами в костях — это событие, которое меняет жизнь пациента. Как правило, такую патологию невозможно вылечить, но можно контролировать с помощью постоянного лечения. Что же происходит с костями при метастазировании? Какие методы терапии использует современная медицина?
Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2018.
Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Спонсором приза зрительских симпатий выступил медико-генетический центр Genotek.
«Книжный» спонсор конкурса — «Альпина нон-фикшн»
В 1889 году британский врач Стивен Педжет описал концепцию «семена и почва». Согласно его теории, опухолевые клетки распространяются по организму не случайным образом, а требуют взаимодействия с микросредой органа-хозяина. Злокачественные клетки, или «семена», атакуют только подходящие для роста органы, то есть «почву». Таким образом, очаги роста опухоли в новых органах (метастазы) будут развиваться только тогда, когда определенные «семена» будут высажены на пригодную для них «почву».
Педжет обнаружил, что у женщин с раком молочной железы (РМЖ) метастазы развивались с гораздо большей вероятностью в костях, чем в любых других органах [1].
Наш обзор посвящен метастазам РМЖ в кость, изменениям, которые вызывают опухолевые клетки в кости, а также современной терапии таких метастазов.
Рак молочной железы и кость
Рак молочной железы — злокачественная опухоль железистой ткани молочной железы. Это наиболее распространенная злокачественная опухоль у женщин, а по числу заболевших среди мужского и женского населения она занимает второе место после рака легких. В 2018 году было зарегистрировано более двух миллионов новых случаев [6].
Рисунок 1. Очаги возникновения вторичной опухоли при РМЖ. Первоначально опухоль развивается в груди. Однако по мере роста опухоли раковые клетки отрываются и распространяются по соседним тканям или отправляются в отдаленные органы, такие как легкие. Однажды в другой ткани они могут образовать вторичную опухоль.
Современная медицина разработала эффективные способы лечения РМЖ 1–3 стадии, что значительно увеличило выживаемость пациентов [7]. Однако 9 из 10 смертей от РМЖ обусловлены нарушением функций различных органов, вызванным распространением раковых клеток по организму, то есть метастазированием. Как правило, РМЖ может распространяться на кости, головной мозг, легкие, печень и лимфатические узлы (рис. 1). Согласно статистическим исследованиям, самой частой областью метастазирования является кость [8]. Она — преобладающее место развития метастазов люминального и Her2-позитивного типов РМЖ, при этом существенно менее предпочитаемое метастазами трижды негативного типа РМЖ [9].
На ранних стадиях метастазы РМЖ в костях бессимптомны, в результате их трудно выявить. Однако всем пациентам с РМЖ раз в несколько месяцев проводят биохимический анализ крови и биопсию для обнаружения рецидива заболевания. Для диагностирования метастазов в кости необходимо пройти рентгенографию, компьютерную томографию, магнитно-резонансную томографию, сцинтиграфию [8].
Кость — это динамическая ткань, играющая центральную роль в поддержании гомеостаза всего организма. Основными элементами кости считаются остеобласты, которые участвуют в создании и минерализации кости, остеокласты, обеспечивающие разрушение (резорбцию) костной ткани, и остеоциты, поддерживающие структуру (рис. 2). Все эти клетки костной ткани ответственны за «строительные работы»: поглощение старых клеток кости и порождение новых. Они существуют в равновесии и регулируют работу друг друга, что помогает обеспечить гомеостаз кости. Сбалансированный цикл образования и разрушения костной ткани называют добродетельным циклом (от англ. virtuous cycle) ремоделирования костей [10].
Рисунок 2. Костные клетки. В костной ткани обнаружены четыре типа клеток. Недифференцированные остеогенные клетки могут развиться в остеобласты. Когда остеобласты попадают в кальцинированную матрицу, их структура и функции меняются, и они становятся остеоцитами. Остеокласты по внешнему виду отличаются от других клеток костной ткани.
Кость также содержит красные клетки костного мозга и эндотелиальные клетки, которые образуют капилляры сосудистой системы кости [11].
Все типы клеток разделяют один «дом», следовательно, они взаимодействуют между собой и регулируют функции друг друга. Однако сосудистая система кости направляет метастазирование раковых клеток в эту микросреду [12].
Одиночные клетки могут оторваться от исходной опухоли в груди и распространиться по организму двумя способами: гематогенным (по кровеносным сосудам) и лимфогенным (по лимфатическим сосудам). Лимфогенные метастазы поражают соседние и отдаленные лимфатические узлы, а гематогенные чаще появляются в костном мозге и костях (рис. 3). Более подробно об образовании гематогенных метастазов рассказывает статья «Обнаружены организаторы побега раковых клеток из первичного очага» [13].
Рисунок 3. Схематическое изображение распространения раковых клеток по кровеносной системе.
Как только клетки РМЖ достигают кости, они создают перекрестные помехи в слаженной работе костных клеток. Раковые клетки врываются в добродетельный цикл и приводят к дисбалансу в сторону резорбции кости. В результате возникает порочный цикл (от англ. vicious cycle).
При определенных условиях раковые клетки отделяются от опухоли и становятся мигрирующими. Они интравазируют в соседние кровеносные сосуды и распространяются по организму, в кровотоке клетки могут попасть в ловушку и экстравазировать. При их выходе в подходящую ткань начинается рост вторичной опухоли.
Даже на ранних этапах РМЖ опухолевые клетки могут мигрировать в костный мозг. Они могут бездействовать долгое время и вызвать рецидив спустя годы .
Добродетельный цикл
Процесс ремоделирования костной ткани состоит из пяти основных этапов: покоя, активации, резорбции, реверсии, формирования (рис. 4). В каждом этапе участвуют разные типы клеток кости [15].
Рисунок 4. Ремоделирование кости. Состоит из пяти фаз: 1) фаза покоя — остеоциты неподвижны; 2) фаза активации — дифференцировка остеокластов из преостеокластов; 3) фаза резорбции — разрушение кости остеокластами; 4) фаза реверсии — дифференцировка остеобластов; 5) фаза формирования — остеобласты создают и минерализуют кость.
Межклеточный матрикс на 85–90% состоит из коллагеновых волокон, которые обеспечивают структурную поддержку минерализации кости. Остальная часть — это протеогликаны, карбоксилированные белки, клеточные адгезивные белки и факторы роста.
Остеобласты образуются из мезенхимных стволовых клеток. Во время своей работы они выделяют в костный матрикс смесь факторов роста и белков, образуя специфическую микросреду. Затем они подвергаются запланированной клеточной гибели или дифференцируются в остеоциты (рис. 5).
Рисунок 5. Схема дифференцировки остеобластов, остеоцитов. Остеобласты начинают дифференцироваться из мезенхимных стволовых клеток в костном мозге.
Остеобласты выделяют факторы роста кости, включая трансформирующий фактор роста β (TGF-β), инсулиноподобные факторы роста (IGF), факторы роста фибробластов (FGF), интерлейкины, тромбоцитарный фактор роста (PDFG). Эти факторы остаются внутри костного матрикса и высвобождаются после деградации кости. Этот процесс обеспечивает обратную связь между формированием и резорбцией кости [11].
Остеокласты — фагоциты для кости — дифференцируются из линии моноцитов/макрофагов (рис. 6). Активированные остеокласты собираются на поверхности кости и присоединяются к ней через специальные рецепторы. Они подкисляют микроокружение на границе кость—остеокласт и секретируют ферменты, участвующие в деградации: протеазы, коллагеназу и щелочную фосфатазу.
Рисунок 6. Схема дифференцировки остеокластов. Остеокласты — гигантские многоядерные клетки, дифференцируются из гемопоэтических стволовых клеток линии моноцитов/макрофагов костном мозге.
Развитие зрелых остеокластов — это многоступенчатый процесс, который регулируется сложной системой цитокинов и взаимодействием внутри стромы кости. Соседние стромальные клетки и остеобласты продуцируют колониестимулирующий фактор макрофагов (M-CSF), который действует через рецептор колониестимулирующего фактора 1 (c-FMS) на многоядерных предшественниках, и активируют экспрессию рецептора RANK (рис. 7). Его лиганд, RANKL, так же, как M-CSF, синтезируется остеобластами и стромальными клетками в ответ на действие паратиреоидного гормона (PTH). RANKL — цитокин из семейства факторов некроза опухоли. Связываясь со своим рецептором, он активирует ряд важных факторов, которые регулируют экспрессию генов остеокластов. Это создает условия для финальной дифференцировки, слияния предшественников и функционирования возникших многоядерных остеокластов. Активированные остеокласты разрушают кость и высвобождают TGF-β и другие факторы роста кости, усиливающие пролиферацию остеобластов [11].
Рисунок 7. Модель нормального костного ремоделирования. Кость постоянно реконструируется. Этот процесс требует взаимодействия костеобразующих остеобластов и костеразрушающих остеокластов. Подробности в тексте.
Остеобласты продуцируют остеопротегерин (OPG) — цитокин из семейства факторов некроза опухоли. Он связывается с RANKL, ингибируя взаимодействие RANK—RANKL, и, следовательно, подавляет остеокластогенез и резорбцию кости. Взаимодействие RANK—RANKL—OPG помогает поддерживать добродетельный цикл.
Переключение между добродетельным и порочным циклами связано с деятельностью раковых клеток. Они нарушают баланс костного микроокружения несколькими способами: стимулируют рост и устраняют физический барьер, то есть минерализованную костную матрицу (рис. 8).
Рисунок 8. Порочный цикл костного метастаза РМЖ. В костях клетки РМЖ секретируют факторы (фиолетовые стрелки), которые нарушают дифференцировку и активность остеобластов, увеличивают продукцию RANKL, усиливая образование остеокластов. На остеокласты они влияют и непосредственно. Зрелые остеокласты разрушают в кость, тем самым высвобождая внедренные в костный матрикс факторы роста. Они, попадая в опухолевое микроокружение, способствуют росту опухоли (красная стрелка). Тот же эффект дают факторы, выделяемые остеобластами и остеоцитами (синяя стрелка).
Традиционно костные метастазы делят на две категории: остеолитические и остеобластные. Остеолитические поражения чаще всего встречаются при РМЖ и характеризуются чрезмерной активацией остеокластов. При этом доминирующий процесс в кости — разрушение. Остеобластные поражения чаще встречаются при раке предстательной железы и характеризуются чрезмерной активацией остеобластов.
Однако в последние годы стало ясно, что разделение костных метастазов на чисто остеолитические или остеобластные неправильно, так как примерно у 20% пациентов с метастазами в кости, возникающими из опухолей молочной железы, поражение смешанное [18].
В этом обзоре мы более подробно рассмотрим механизм остеолитического поражения костной ткани.
В резорбции костной ткани участвуют остеокласты, деятельность которых находится под контролем целого ряда клеток костного мозга. Опухолевым клеткам необходимо препятствовать такому контролю и продуцировать собственные факторы, регулирующие активность остеокластов. Ключевым участником является TGF-β, который активирует рост опухоли и подавляет иммунную систему. TGF-β индуцирует синтез белка, связанного с паратиреоидным гормоном (PTHrP), и интерлейкина 11, которые стимулируют активацию остеокластов. В случае с PTHrP это обусловлено его способностью связываться с рецептором РТН и изменять соотношение RANKL/OPG в пользу RANKL [16].
Опухолевые клетки также продуцируют факторы, ингибирующие дифференцировку остеобластов, а значит, подавляют формирование костей [19].
Роль остеокластов
Таким образом, при метастазировании РМЖ опухолевые клетки усиливают резорбцию кости путем прямого секретирования RANKL, что приводит к высвобождению биоактивных молекул. Эти продукты деградации вовлечены в регуляцию добродетельного цикла и стимулируют рост опухоли в случае развития метастаза в кости. Например, кальций — это первый продукт, выделяющийся при разрушении костного матрикса. Опухолевые клетки экспрессируют на своей поверхности кальций-чувствительные рецепторы, которые реагируют на повышение уровня кальция и стимулируют рост опухоли [20].
При метастазах РМЖ костная ткань резорбируется преимущественно собственными нормальными клетками. Прямая деградация костной ткани опухолью встречается редко. Метастатические клетки РМЖ способны продуцировать коллагеназу и другие ферменты, разрушающие кость [21], [22].
Роль остеобластов
Остеобласты проходят сложный многоступенчатый процесс дифференцировки. Все клетки на разных стадиях дифференцировки играют определенную роль в добродетельном/порочном циклах.
Первый этап дифференцировки представлен преостеобластами, которые находятся в стенках гаверсовых и фолькмановских каналов. Для незрелых остеобластов характерна высокая производительность RANKL. При костных метастазах они могут стимулировать остеолиз [20], [21]. Некоторые источники сообщают, что RANKL может стимулировать пролиферацию вторичной опухоли РМЖ в кости [23], [24].
В присутствии раковых клеток преостеобласты усиливают производство провоспалительных цитокинов, таких как интерлейкин-6, моноцитарный хемотаксический белок, фактор некроза опухоли α, макрофагальный воспалительный белок 2 и др. Эти молекулы помогают поддерживать опухолевые клетки и также являются остеокластогенными.
Зрелые остеобласты, в отличие от преостеобластов, расположены на поверхности эндотелия. Во время формирования кости они выделяют биологически активные вещества, которые проявляют свою функцию только после высвобождения из разрушающейся костной матрицы. Среди этих молекул есть факторы, которые стимулируют рост опухоли и неоангиогенез — формирование новых микрососудов для питания опухоли [11]. В конце концов остеобласты дифференцируются в остеоциты или подвергаются апоптозу .
Гибель остеобластов — это не случайное событие, а строго регулируемый процесс, необходимый для обеспечения определенного размера и архитектуры кости. Метастазирующая опухоль РМЖ способна вызывать апоптоз остеобластов, продуцируя индукторы апоптоза [11]. Однако влияние апоптотических остеобластов на добродетельный и порочный циклы описано плохо.
Опухолевые клетки также могут выделять вещества, активирующие остеобласты. В настоящее время факторы, ответственные за этот процесс, не совсем ясны. Основная роль отводится эндотелину-1 (ЕТ-1). Этот фактор секретируется клетками РМЖ и рака предстательной железы и стимулирует возникновение остеобластных метастазов. В результате может начаться процесс ненормального костеобразования [26]. Кости быстро растут, становятся утолщенными, жесткими, негибкими.
Роль остеоцитов
Последний этап дифференцировки остеобластов представлен остеоцитами. Они локализованы в костном матриксе, что делает их идеальными регуляторами ремоделирования кости. Однако это же преимущество становится недостатком при развитии костных метастазов, поскольку они способны подпитывать порочный цикл.
Остеоциты — важные продуценты RANKL. Также они могут контролировать метастатический рост, секретируя факторы, некоторые из которых активируют пролиферацию раковых клеток молочной железы [16].
Терапевтические стратегии
Пациент с костными метастазами испытывает мучительную сильную боль, у него повышается риск переломов, качество жизни катастрофически снижается. Терапия метастазов РМЖ в кости включает в себя различные методы, которые могут влиять как на саму опухоль, так и на ее микроокружение [11].
Чаще всего метастатический РМЖ возникает через несколько месяцев или лет после завершения лечения раннего рака. Риск возникновения вторичной опухоли после лечения РМЖ варьирует от человека к человеку. Но это сильно зависит от характеристики раковых клеток, стадии первичной опухоли, способов лечения. Например, в течение 15 лет вторичная опухоль в кости возникает у примерно 30% пациентов с HER2-позитивным и у 15% — с трижды негативным РМЖ [9].
Наиболее агрессивной вторичной опухолью считается метастатический трижды негативный РМЖ. Он часто поражает пациенток молодого возраста. С таким типом метастазов продолжительность жизни пациентов может не превысить и 6 месяцев [27].
В настоящее время метастатический РМЖ нельзя излечить. Однако это не означает, что его нельзя лечить. Терапия метастазов РМЖ в кости направлена на увеличение продолжительности и качества жизни. Современные методы лечения в США позволяют продлить жизнь 35% таких пациентов по меньшей мере на пять лет, а некоторые пациенты могут прожить 10 и более лет после постановки диагноза [27].
До начала лечения врач объясняет, какие поправки нужно внести в диету и образ жизни пациента. Во-первых, необходимо принимать достаточное количество кальция и витамина D, во-вторых, регулярно выполнять физические упражнения. Соблюдение этих правил позволит пациенту сохранить кости крепкими и минимизировать проявления остеопороза [28].
Тактику лечения врач определяет индивидуально для каждого пациента в зависимости от:
- типа и локализации первичной опухоли;
- количества и расположения вторичных опухолей в кости;
- наличия метастазов в других органах;
- возраста и общего состояния больного;
- предыдущего лечения;
- побочных эффектов.
В лечении костных метастазов можно выделить два основных подхода:
- системную терапию, которая направлена на лечение первичной опухоли;
- местную терапию, которая должна облегчить боли пациентов и уничтожить вторичную опухоль [27].
Системная терапия
Системная терапия включает в себя гормональную терапию, химиотерапию и таргетную терапию.
Гормональная терапия
Гормональная, или эндокринная, терапия — основной способ лечения пациентов с метастатическим РМЖ, положительным по эстрогеновым/прогестероновым рецепторам. Такой способ лечения подразумевает, что лекарственный препарат блокирует действие эстрогена или прогестерона либо снижает их концентрацию в организме. Это может замедлить рост и деление опухолевых клеток.
Существуют различные факторы, позволяющие определить, какой вид гормональной терапии подходит пациенту. К ним относится эффективность и безопасность доступных видов лечения, предшествующая терапия (в том числе гормональная), но в первую очередь — нахождение пациентки в пременопаузе или постменопаузе. Для женщин в пременопаузе гормональная терапия начинается с подавления функции яичников, чтобы остановить производство гормонов. В постменопаузе яичники уже не функционируют, и эстроген производится в жировой ткани и надпочечниках; в этом случае используют ингибиторы ароматаз [27].
Если первый препарат гормональной терапии перестает работать, то назначают второй, и т.д. В какой-то момент — может, через несколько месяцев или лет — гормональная терапия перестает вызывать ответ, и тогда рекомендуют переключиться на химиотерапию.
Побочные эффекты эндокринной терапии зависят от вида лечения и могут включать в себя мышечные боли, чувство усталости, легкую тошноту. К серьезным побочным эффектам относят повышение риска инсульта, рак матки, потерю прочности костей [29].
Химиотерапия
Химиотерапия — это первый этап лечения метастазов РМЖ, если первичная опухоль HER2-положительная и не имеет рецепторов к эстрогену/прогестерону. К химиотерапии обращаются и когда гормональная терапия перестает действовать [27].
Химиотерапевтические препараты, например 5-фторурацил, капецитабин или метотрексат, попадая в кровоток, разносятся по всему организму, уничтожая любые быстрорастущие клетки, в том числе и здоровые.
На выбор вида химиотерапии влияют агрессивность и быстрота роста раковых клеток, предшествующие варианты химиотерапии, побочные эффекты и т.д. [28].
Как и при гормональной терапии, если первый препарат или комбинация препаратов перестали действовать, и опухоль начинает расти, переходят на второй, третий и т.д. препараты. С каждым таким переходом шансов на уменьшение размеров опухоли становится всё меньше.
Побочные эффекты зависят от вида лекарства. К наиболее частым относят усталость, анемию, выпадение волос, тошноту и рвоту, а к самым серьезным — поражения сердца, легких, почек, вероятность возникновения другого вида рака. Пациентам могут назначать лекарственные средства, которые предотвращают или уменьшают выраженность побочных эффектов. Например, некоторые химиотерапевтические препараты повреждают ДНК, и для ее репарации и снижения вероятности возникновения устойчивости к химиотерапии назначают поли(AДФ-рибоза)-полимеразы (PARP) [28].
Таргетная терапия
Таргетная, или молекулярно-таргетная, терапия — активно развивающееся направление лечения рака. Она блокирует рост раковых клеток за счет вмешательства в конкретный молекулярный механизм канцерогенеза.
Таргетная терапия используется как системный подход для лечения костных метастазов РМЖ. Она применяется либо в виде монотерапии, либо в сочетании с гормональной или химиотерапией.
Для лечения положительных по эстрогеновым/прогестероновым рецепторам и HER2-негативных метастазов РМЖ используют ингибиторы киназ CDK4 и CDK6. Ингибиторы CDK4/6 предназначены для прерывания роста опухолевых клеток. FDA одобрило три препарата на их основе: рибоциклиб, палбоциклиб, абемациклиб. Первый из них в начале 2018 года одобрил и Минздрав России.
Для увеличения эффективности эндокринной терапии положительных по гормональным рецепторам и HER2-негативных метастатических опухолей используют ингибиторы mTOR [27].
Для лечения HER2-позитивного метастатического рака активно применяют ингибиторы тирозинкиназы, такие как лапатиниб [27].
Многие таргетные методы лечения относятся к иммунотерапии. Иммунотерапия — это новейший, действенный и перспективный метод лечения многих форм рака. В последнее время ее применяют и для лечения костных метастазов.
Есть два способа действия: усиление иммунной системы, чтобы организм сам боролся с раком, и использование белков, уничтожающих раковые клетки. Иммунотерапия рака предполагает введение в организм противоопухолевых биопрепаратов: цитокинов, моноклональных антител или опухолевых вакцин. Ее используют и в системном, и в местном лечении вторичных опухолей при РМЖ.
Иммунотерапия в качестве системного подхода применяется в лечении HER2-позитивного РМЖ. Опухолевые клетки этого типа выставляют на своей поверхности большое количество рецепторного белка HER2, который важен для их роста. И для лечения используют антитела, которые блокируют внутриклеточные сигналы синтеза этого белка или вмешиваются в его работу. К таким моноклональным антителам относятся трастузумаб и пертузумаб [27].
Побочные эффекты таргетной терапии зависят от вида лекарственного средства. Однако для всех них типичны тошнота, рвота, диарея и слабость. К серьезным побочным эффектам можно отнести снижение сердечной функции и заболевания печени, например гепатит [28].
Местная терапия
Местную, костно-таргетную терапию в сочетании с системной рекомендуют всем пациентам с костными метастазами РМЖ. К ней относят использование бисфосфонатов и деноcумаба, лучевую терапию и хирургические вмешательства. Выбор между этими видами лечения зависит от размера метастазов, осложнений, предпочтений пациента.
Бисфосфонаты
Бисфосфонаты — это стандартная терапия, используемая для уменьшения боли в костях, снижения темпов метастазирования, предотвращения потери костной массы и значительного улучшения качества жизни пациентов.
Рисунок 9. Формула бисфосфоната
Бисфосфонаты представляют собой молекулы, состоящие из двух фосфонатных групп, соединенных атомом углерода (рис. 9). Такая химическая конфигурация позволяет им с высокой степенью сродства связываться с гидроксиапатитной составляющей кости. Дополнительные функциональные группы, присоединенные к центральному атому углерода, придают бисфофонатам различные фармакологические свойства [7].
Бисфосфонаты вводят в организм перорально или путем инфузий. Основной механизм их действия заключается в ингибировании резорбции кости, поскольку после эндоцитоза они стимулируют апоптоз остеокластов. Это разрывает порочный круг сигналов между остеокластами и раковыми клетками в кости [16].
Применение бисфосфонатов может сопровождаться гриппоподобными симптомами и гипокальциемией. Эти препараты обладают выраженной нефротоксичностью и противопоказаны при низком клиренсе креатинина. Их применение, в особенности золедроновой кислоты, повышает риск остеонекроза челюстей.
Лучевая терапия
У пациентов с метастатическим РМЖ радиотерапию используют как способ облегчения боли и профилактики осложнений [33].
Машина фокусирует ионизирующее излучение на метастазах в кости. Облучение, длящееся всего несколько минут, уничтожает раковые клетки.
Побочные эффекты зависят от облучаемого места. К наиболее распространенным последствиям лучевой терапии относятся раздражение кожи и чрезмерная утомляемость [28].
Для радиотерапии могут использоваться и так называемые радиофармацевтические препараты. Обычно это радиоизотопы щелочно-земельных металлов (стронций-89, самарий-153). Их можно избирательно доставлять прямо к метастазу. Во-первых, они могут самостоятельно накапливаться в зонах повреждения кости (как «имитаторы» кальция). Во-вторых, радиоизотопы можно конъюгировать с лигандами, обеспечивающими их направленную доставку в кость [29], [34]. В области костных метастазов исходящее от препарата излучение «убивает» рак.
Препарат усиливает местный эффект лучевой терапии, облегчает боль, иногда сокращает потребность в дальнейшей радиационной терапии.
К основным недостаткам использования радиоизотопов относится уменьшение содержания в крови тромбоцитов и лейкоцитов [28].
Хирургия
Хирургическое вмешательство у пациентов с метастазами в кости проводится редко. Основное показание для него — патологический перелом [7]. С помощью хирургии также можно стабилизировать слабую кость путем вставки винтов, стержней и т.д.
Иммунотерапия
Рисунок 10. Механизм действия деносумаба. Высокоаффинное связывание деносумаба с RANKL ингибирует созревание и активность остеокластов, предотвращая взаимодействие RANKL с рецептором RANK на зрелых и незрелых остеокластах.
Иммунотерапией при местном лечении костных метастазов РМЖ можно назвать применение деноcумаба.
Деноcумаб — человеческое моноклональное антитело (IgG2), которое специфично связывается с RANKL. В результате не образуется связи RANKL—RANK (рис. 10). Лечение денозумабом предотвращает производство остеокластов и, следовательно, останавливает резорбцию кости [7].
На фоне применения деносумаба часто развиваются суставные и мышечные боли, гипокальциемия, инфекционные заболевания [35].
Будущие направления
Сейчас ведется разработка средств для лечения метастатического рака молочной железы, нацеленных на новые мишени. Мишенями могут стать катепсин К, TGF-β, PTHrP, хемокиновые рецепторы и т.д. [30], [34]. Эти молекулы играют важную роль в порочном цикле, следовательно, воздействие на них может остановить рост вторичной опухоли или разрушение кости. Перспективным препаратом остается и деносумаб. Показано, что он улучшает минеральную плотность костей [20]. Однако из-за сложности механизмов костного метастазирования возникает необходимость комбинирования лекарственных препаратов, нацеленных на разные мишени.
Следующая задача состоит в том, чтобы разработать для каждого пациента индивидуальное лечение, предсказывая возможный клинический исход. Геномное и протеомное профилирование имеет прогностический потенциал, коррелирующий с прогрессированием заболевания. Такое профилирование может прогнозировать и исход лечения тем или иным препаратом. В будущем подобные технологии помогут отбирать пациентов, находящихся в группе риска возникновения метастатического РМЖ, и исключать ненужное лечение [20], [21].
Таким образом, РМЖ с метастазами в костях — это уже не приговор. Но, к сожалению, лечение такого рака — сложный, выматывающий процесс. Разумеется, говорить о 100% излечении пока невозможно. Однако использование стандартных терапевтических методов совместно с новыми подходами способно продлить жизнь пациентам и улучшить их состояние, то есть игра всё же стόит свеч.
Важно запомнить, что рак — это не паразит, который колонизирует и разрушает здоровые ткани. Это «умная» группа клеток, которая взаимодействует с нормальными клетками хозяина и использует важные тканевые сигналы ради собственного благополучия.
- Andrew S. Gdowski, Amalendu Ranjan, Jamboor K. Vishwanatha. (2017). Current concepts in bone metastasis, contemporary therapeutic strategies and ongoing clinical trials. J Exp Clin Cancer Res. 36;
- Во власти опухоли: почему метастазы так сложно остановить?;
- Метастазирование опухолей;
- МикроРНК участвуют в регуляции метастазирования опухолей;
- Рак молочной железы с семейной историей;
- Freddie Bray, Jacques Ferlay, Isabelle Soerjomataram, Rebecca L. Siegel, Lindsey A. Torre, Ahmedin Jemal. (2018). Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA: A Cancer Journal for Clinicians;
- Kimberly D. Miller, Rebecca L. Siegel, Chun Chieh Lin, Angela B. Mariotto, Joan L. Kramer, et. al.. (2016). Cancer treatment and survivorship statistics, 2016. CA: A Cancer Journal for Clinicians. 66, 271-289;
- Faustine Williams, Stephen Jeanetta, Aimee S. James. (2016). Geographical Location and Stage of Breast Cancer Diagnosis: A Systematic Review of the Literature. Journal of Health Care for the Poor and Underserved. 27, 1357-1383;
- Hagen Kennecke, Rinat Yerushalmi, Ryan Woods, Maggie Chon U. Cheang, David Voduc, et. al.. (2010). Metastatic Behavior of Breast Cancer Subtypes. JCO. 28, 3271-3277;
- Alfredo Cappariello, Mattia Capulli. (2018). The Vicious Cycle of Breast Cancer-Induced Bone Metastases, a Complex Biological and Therapeutic Target. Curr Mol Bio Rep. 4, 123-131;
- «Структура костной ткани и кровообращение». «Лечение асептического некроза»;
- Daniel L Coutu, Konstantinos D Kokkaliaris, Leo Kunz, Timm Schroeder. (2017). Three-dimensional map of nonhematopoietic bone and bone-marrow cells and molecules. Nat Biotechnol. 35, 1202-1210;
- Обнаружены организаторы побега раковых клеток из первичного очага;
- Одураченные макрофаги, или Несколько слов о том, как злокачественные опухоли обманывают иммунитет;
- «Ремоделирование костной ткани». «Островок здоровья»;
- Gary G. Meadows Integration/Interaction of Oncologic Growth — Springer Netherlands, 2005;
- Опухолевые разговоры, или Роль микроокружения в развитии рака;
- Link Y., Romano A., Bejar J., Schiff E., Dotan Y. (2016). Widespread osteoblastic metastases and marked elevation of CA19-9 as a presentation of signet ring cell gastric carcinoma. J. Gastrointest. Oncol. 7, E1–5;
- Katherine N. Weilbaecher, Theresa A. Guise, Laurie K. McCauley. (2011). Cancer to bone: a fatal attraction. Nat Rev Cancer. 11, 411-425;
- Alfredo Cappariello, Antonio Maurizi, Vimal Veeriah, Anna Teti. (2014). Reprint of: The Great Beauty of the osteoclast. Archives of Biochemistry and Biophysics. 561, 13-21;
- Garrett R.I. (1993). Bone destruction in cancer. Sem. Oncol. 20 (3 suppl 2), 4–9;
- Wende Kozlow, Theresa A. Guise. (2005). Breast Cancer Metastasis to Bone: Mechanisms of Osteolysis and Implications for Therapy. J Mammary Gland Biol Neoplasia. 10, 169-180;
- Shuan Rao, Shane J.F. Cronin, Verena Sigl, Josef M. Penninger. (2018). RANKL and RANK: From Mammalian Physiology to Cancer Treatment. Trends in Cell Biology. 28, 213-223;
- Schuster C., Mo H., Shen C.L., Gollahon L. (2017). RANK/RANKL/ OPG: The Axis of Breast Cancer Bone Metastasis Evil? Ann. Breast Cancer Res. 2, 1008;
- 12 методов в картинках: проточная цитофлуориметрия;
- JA KANIS, N OROURKE, EV MCCLOSKEY. (1994). CONSEQUENCES OF NEOPLASIA INDUCED BONE-RESORPTION AND THE USE OF CLODRONATE (REVIEW). Int J Oncol;
- Komen S.G. (2018). Recommended treatments for metastatic breast cancer. Susan G Komen;
- «Рассказываем историю о метастатическом раке молочной железы». (2017). AstraZeneca;
- Bob Li, Matthew Wong, Nick Pavlakis. (2014). Treatment and Prevention of Bone Metastases from Breast Cancer: A Comprehensive Review of Evidence for Clinical Practice. JCM. 3, 1-24;
- Иммуностимулирующие вакцины;
- Т-клетки — марионетки, или как перепрограммировать Т-лимфоциты, чтобы вылечить рак;
- Прямая атака в центр опухоли;
- Darren Brady, Chris C. Parker, Joe M. O’Sullivan. (2013). Bone-Targeting Radiopharmaceuticals Including Radium-223. The Cancer Journal. 19, 71-78;
- Tomifumi Onishi, Naoki Hayashi, Richard L. Theriault, Gabriel N. Hortobagyi, Naoto T. Ueno. (2010). Future directions of bone-targeted therapy for metastatic breast cancer. Nat Rev Clin Oncol. 7, 641-651;
- European public assessment report (EPAR) for Prolia. (2016). European Medicines Agency;
- Meera Saxena, Gerhard Christofori. (2013). Rebuilding cancer metastasis in the mouse. Molecular Oncology. 7, 283-296;
- Marie-Eve Marquis. (2009). Bone cells-biomaterials interactions. Front Biosci. Volume, 1023.
«Сколько живут при метастазах?» – Яндекс.Кью
К сожалению, у многих пациентов рак обнаруживается на распространенных стадиях, когда имеются либо регионарные, либо отдаленные метастазы. В таком случае полное излечение не всегда возможно, и тогда все усилия врачей направлены на уменьшение опухолевой массы, улучшение качества жизни пациента и снижение тягостных симптомов. Продолжительность жизни в этих случаях определяется видом опухоли и местом ее локализации. Она может составлять он нескольких месяцев до нескольких лет.
Некоторые виды рака прогрессируют очень быстро. Например, рак поджелудочной железы или рак яичников. Время от возникновения опухоли до ее распространения на смежные органы составляет несколько месяцев. В других случаях процесс может протекать годами, даже при наличии метастазов, например, при раке простаты или раке молочной железы.
На продолжительность жизни при наличии метастазов оказывают влияние чувствительность рака к системному лечению, количество метастазов и их локализация.
Чувствительность опухоли к системному медикаментозному лечению
Например, рост рака простаты и гормонозависимого рака молочной железы стимулируется половыми гормонами. Если их «выключить», то рост опухоли прекращается. Такое лечение не обеспечивает выздоровление, но может сдерживать распространение злокачественного процесса на долгое время, в некоторых случаях даже на несколько лет. Такие пациенты ведут вполне активный образ жизни.
В настоящее время активно развиваются новые методы противоопухолевой терапии, например, таргетная терапия или иммунотерапия. Это лечение назначается с учетом специфических особенностей рака у конкретного пациента и позволяет добиться хороших результатов даже у пациентов, которые раньше относились к группе с неблагоприятным клиническим прогнозом. В качестве примера можно привести герцептин при HER2-положительном раке молочной железы.
Локализация метастазов и их количество
Большое значение имеет место локализации метастазов и их количество. Чаще всего при удалении единичных метастазов ряда опухолей прогноз для пациента меняется незначительно.
Например, единичные метастазы печени можно удалить различными способами – хирургическое иссечение, тепловая деструкция под действием лазера или радиоволн, с помощью химиоэмболизации опухоли и др. При единичных метастазах в головной мозг и легкие может применяться гамма-нож или хирургическое лечение.
Совсем другая ситуация развивается при множественных метастазах. В этом случае требуется системное противоопухолевое лечение и паллиативные операции, которые направлены на облегчение симптомов и улучшение качества жизни больных.
Метастазы Печени: Лечение, Продолжительность Жизни, Специалисты
Безусловно, наиболее распространенными злокачественными новообразованиями в печени являются метастазы. Это раковые поражения, образующиеся из отдаленных опухолей.
Чаще всего в печень метастазируют следующие опухоли (в порядке убывания):
Метастазы в печени называются злокачественными вторичными опухолями, поскольку они удалены от первичных опухолей. Опухоли, которые происходят непосредственно из клеток печени, являются первичными опухолями печени, например, рак печени (гепатоцеллюлярная карцинома). Рассеяние опухолевых клеток происходит частично через кровоток (гематогенное рассеяние), частично через лимфатическую систему (лимфогенное рассеяние).
Опухоли органов пищеварения, такие как рак толстой кишки, желудка или поджелудочной железы, в основном распространяются гематогенно (через кровоток) через воротную вену в печень, главный орган, отвечающий за обмен веществ. При постановке диагноза метастазы в печени обычно уже множественные. Количество, внешний вид, размер и положение опухолевых образований имеют решающее значение, прежде всего, для планирования дальнейшего лечения.
Лечение опухолей печени обычно проводится междисциплинарной командой специалистов. К ним относятся абдоминальные хирурги (висцеральные хирурги), специализирующиеся на хирургии печени, радиологи , онкологи и патологи.
Злокачественные новообразования печени, как правило, подвергают хирургии печени с полным удалением опухолевой ткани. Зачастую, особенно при метастазах, что связано с запущенной стадией болезни, операция уже не вполне возможна. Но существуют различные терапевтические подходы, которые можно использовать для улучшения качества и продолжительности жизни пациента.
Особенно при метастазах прежде чем проводить хирургическое удаление, следует убедиться, что первичная опухоль, например, рак толстой кишки, вылечена и в организме нет других метастазов.
При метастазах в печени, например, при колоректальном раке (рак толстой кишки), у пациентов, у которых нет других проблем со здоровьем, может быть предпринята попытка хирургического удаления даже большого количества метастазов. Поскольку печень обладает очень быстрой способностью к регенерации, такое удаление опухолевых образований может быть выполнено в несколько этапов в случае сильного поражения органа (стадия резекции).
Если метастазы не могут быть полностью удалены в первую очередь из-за их большого количества или размера, можно восстановить резектабельность (полное удаление опухоли) с помощью химиотерапии или частичного удаления. Химиотерапия, которая проводится перед удалением опухоли, чтобы уменьшить новообразование, сделать его более операбельным, называется «неоадъювантной химиотерапией».
Метастазы, которые не удаляются хирургическим путем, обычно подвергают паллиативной химиотерапии (не лечит). Кроме того, существуют методы термоабляции, такие как радиочастотная абляция (РЧА) , при которой локальное повышение тепла уменьшает новообразования.
При так называемой «трансартериальной химиоэмболизации» (TACE) химиотерапевтическое средство вводится непосредственно в опухолевую ткань через катетерную систему в кровеносных сосудах. Это позволяет получить максимальное прямое действие с минимальными побочными эффектами для окружающих тканей и пациента.
Другим методом лечения, которое непосредственно воздействует на печень через катетер является селективная внутренняя лучевая терапия (SIRT). В этом случае радиоактивные частицы специально вводят в опухолевую ткань, чтобы действовать как можно более локально с наименьшим сопутствующим ущербом.
Современным методом уменьшения метастазов в печени является HIFU-терапия (фокусированный ультразвук высокой интенсивности). При таком методе опухолевые клетки нагреваются так сильно, что они «спекаются» и опухоль сжимается. Этот процесс все еще находится в состоянии развития, но многочисленные исследования показали, что терапия HIFU является успешным вариантом лечения с небольшим количеством побочных эффектов.
Согласно современному уровню знаний, особенно многообещающими являются концепции мультимодальной терапии, в которых хирургия печени, химиотерапия и тепловая терапия используются в сочетании.
Без хирургического удаления средний срок жизни при постановке диагноза зависит от первичной опухоли (источника метастазирования) и составляет около 4–8 месяцев. При полном хирургическом удалении метастазов в печени при раке толстой кишки, статистика показывает, что 5-летняя выживаемость достигается у 45 %, т.е. через 5 лет после операции живы 45 % онкологических больных.
Источники :
- Внутренняя медицина, Герд Герольд и сотрудники, 2014 (Innere Medizin, Gerd Herold und Mitarbeiter, 2014)
- Хирургия, Зиверт/Штайн, 9-е издание, Springer Verlag (Chirurgie, Siewert/Stein, 9. Auflage, Springer Verlag)
Бисфосфонаты при костных метастазах РМЖ
Девяностые годы прошли под знаком изучения клинического эффекта бисфосфонатов при метастазах РМЖ в кости. Поскольку ибандронат и золедронат появились значительно позже, большинство исследований было посвящено клодронату и памидронату.
Несмотря на довольно продолжительное использование бисфосфонатов, в настоящее время нельзя отдать предпочтение какому-либо из них при лечении осложнений метастазов рака молочной железы.
В 1993 году Paterson А. с коллегами показал, что прием оральной формы клодроната сократил число патологических осложнений метастазов в кости на 27% по сравнению с плацебо, но не повлиял на выживаемость больных [30]. Тем не менее, нельзя не оценить того, что, не увеличив продолжительности жизни, препарат существенно улучшил ее качество.
Тремя годами позже Kanis J.А. подтвердил, что клодронат не просто снижает процент скелетных осложнений, но и уменьшает весьма заметно (32% против 62%) число метастазов [19] . Скептик наверняка скажет, что, если проживешь одинаковое время, неважно, имеешь пять метастазов или десять. Но разница между тем есть, ведь уменьшается интоксикация, легче контролировать боль. А психологическое значение сообщения больному человеку о регрессии части метастатических очагов переоценить трудно, буквально на глазах пациентка превращается в другого человека – активного, доброжелательного, внимательного к близким, готового к продолжению терапевтического сотрудничества.
В 1998 году Diel с соавторами опубликовали результаты проспективного, рандомизированного исследования у 302 больных с подтвержденными микрометастазами в костном мозге [11]. В два раза реже определялись метастазы в костях у больных, получавших клодронат 1600 мг, – 8% против 17%, у 55% больных отмечалась тенденция к снижению отдаленного метастазирования. Так, висцеральные метастазы имелись у 8% против 19% в контроле, что повлияло на выживаемость, умерло только 4%, в контрольной группе – 15%. Отмечено, что редукция метастазов происходит не только в первые 12-14 месяцев, как при терапии другими бисфосфонатами, но и продолжается у 50% после 36 месяцев терапии [11,17,38].
В том же году Powles с коллегами опубликовали результаты мультицентрового, рандомизированного, двойного слепого двухлетнего адьювантного применения клодроната и плацебо у 1079 женщин с последующим клиническим наблюдением на протяжении 2-5 лет [26]. Метастазы в кости появились у 28 (5,2%) больных, принимавших клодронат, тогда как в контроле – у 44 (8,1%). У 20 (7,3%) постменопаузальных пациенток выявлены метастазы в костях в группе «плацебо» и у 9 (3,3%) в другой группе. У пременопаузальных женщин эффект лечения был менее очевиден: 19 (7,1%) клодронат против 24 (9,1%). Тем не менее, предварительный результат показал возможность использования клодроната адьювантно после лечения первичного рака молочной железы у постменопаузальных больных. Теоретически можно прибегнуть к этому, если отбросить экономический аспект, у пожилых женщин, страдающих распространенным остеопорозом, ведь последний является показанием для назначения бисфосфонатов [48]. Таким способом можно было бы «убить двух зайцев», но не в нашей жизни.
Небольшое, по сравнению с предыдущим, исследование Saarto Т. с соавторами продолжительностью 5 лет, результаты которого опубликованы в 2001 году, когда после лечения первичного рака молочной железы (при наличии NL+) 149 женщин 3 года получали клодронат и 150 находились в контроле. Всем проводилась стандартная адьювантная терапия: пременопаузальным – CMF, постменопаузальным – антиэстрогены [33]. Действительно отмечено снижение случаев костного метастазирования на фоне клодроната, не было метастазов у 39 (26%) против 27 (18%), но некостные метастазы выявлены у 67 (45%) в первой группе и у 41 (27%) в контроле, что повлияло на показатели общей выживаемости. Очень важный вывод – возрастает минеральная плотность костей при совместном использовании антиэстрогенов и бисфосфонатов, чего при «гормональных болезнях», к коим относится рак молочной железы, не бывает в принципе.
Hortobagy C. N. с коллегами в 1998 году оценили результаты использования 90 мг памидроната каждые 4 недели или плацебо в течение 2 лет у 382 больных с метастазами в кости (не менее 1 литического очага с минимальным диаметром 1 см) [16,17]. Все больные ранее получали химиотерапию. Памидронат после первого года действительно уменьшил число скелетных осложнений, исключая переломы позвонков. В период от 15 до 24 мес. лечения осложнения в группах были равны или выше при применении памидроната (4% против 3% гиперкальциемии; 17% против 13% вертебральных переломов; 14% против 7% лучевой терапии), что показывало снижение эффективности памидроната на втором году лечения. Также Theriault R.L. с соавторами подтвердили 12-месячную эффективность памидроната, к концу второго года лечения различия с плацебо уменьшались [38].
Ali S.М. с коллегами считают, что снижение эффективности памидроната после двухлетнего приема обусловлено закономерным прогрессированием процесса [3], но это никак не объясняет малую результативность уже на втором году терапии.
Что касается наиболее эффективной дозы памидроната, то единого мнения нет. Lipton с соавторами, сравнив результаты собственных исследований, не обнаружили преимуществ 90 мг перед 45 мг [20]. При сочетании аредии (памидронат) с химиотерапией у пременопаузальных женщин отмечено увеличение времени до прогрессирования по сравнению с плацебо на 1,5 месяца, в группе гормоны + аредия не отмечено различий в длительности ремиссий. Международная группа по изучению аредии сделала вывод, что при сочетании памидроната с химиотерапией склеротические изменения в костях регистрируются у 52% в контрольной группе, у получавших химиотерапию + плацебо – у 44% [53].
Рандомизированное исследование группы Hultborn R. 60 мг памидроната каждые 4 недели (201 больная) и плацебо (203) показало снижение числа скелетных осложнений и гиперкальциемии и более позднее их появление. Но не найдено различий в сравнении случаев переломов длинных трубчатых костей и костей таза, спинальных парезов, необходимости подключения лучевой терапии или хирургии и общей выживаемости [18].
Небольшое исследование Erem Т. с соавторами: сравнение лучевой терапии СД 20 Гр в сочетании с памидронатом 60 мг (группа В – 29 больных) и без (группа А – 20 больных) [13] . Через 3 месяца от начала лечения нуждались в анальгетиках 22% из группы А и 7% из В, через 6 месяцев ситуация не изменилась: в группе, получавшей памидронат, нуждались в обезболивании 8% против 12%, а через 12 месяцев в повторной лучевой терапии испытывали необходимость 33% больных группы А и только 10% группы В, анальгетики требовались соответственно 20% и 15%. Рекомендуемая доза памидроната соответствует 90 мг каждые 4 недели.
Менее изучена эффективность ибандроната при метастазах рака молочной железы. В исследовании Diel с соавторами 462 женщинам, разделенным на три группы, проводилось введение ибандроната 2 мг каждые 4 недели максимально 2 года – 153; 6 мг ежемесячно – 152 и контрольная группа в 157 человек получала плацебо [10]. Отмечено повышение выживаемости для всех больных, получавших ибандронат, – 774,3 дня против 741,7 дня в контроле. Особенно отмечен тот факт, что значительно повысилась выживаемость в группе пациенток с мягкотканными метастазами после 6 месяцев лечения. Качество жизни было тем выше, чем выше доза ибандроната.
В отечественном исследовании также отмечено уменьшение костных осложнений при использовании ибандроната, доза 6 мг признана рациональной [46].
Частота костных осложнений у полутора тысяч больных раком молочной железы, леченных золедронатом или памидронатом, были одинаковы, но процент пациентов, нуждавшихся в лучевой терапии на очаги в костях, был значимо ниже среди пациентов, получавших зомету 4 мг. Не было значимых различий по медиане времени до прогрессирования костных метастазов, частоты объективного ответа, медианы времени выживания [29]. При терапии как памидронатом, так и золедронатом снижался уровень маркеров костной резорбции. Но зомета существеннее снизила соотношение фактора прогноза эффективности NTx к креатинину [36]. Продление исследования на 12 месяцев показало, что риск развития костных осложнения при лечении зометой снижается на 18% по сравнению с группой, получавших памидронат.
Пилотное исследование на 280 больных раком молочной железы показало увеличение минеральной плотности позвонков в передне-заднем направлении на 6,2%-9,6% при ежемесячном лечении золедронатом и 9,2% памидронатом [50].
Таким образом, и в отношении лечения метастазов рака молочной железы в кости, как и при использовании бисфосфонатов при опухоль-ассоциированной гиперкальциемии, нельзя отдать предпочтение какому-либо одному препарату и по совету доктора Herbert Fleisch выбирать наиболее удобный путь введения препарата перорально ежедневно или внутривенно ежемесячно [14].
Мещерякова Н.Г.
Опухолевые поражения костей и вторичные поражения позвоночника
Методики лечения
Лечение опухолевых поражений кости в большинстве случаев требует хирургического вмешательства. После проведения операции, с целью исключения риска рецидива, назначают лучевую или химиотерапию. Такие процедуры могут потребоваться и перед проведением хирургического вмешательства. Они позволяют уменьшить размер опухоли перед операцией.
Вторичные поражения позвоночника
Метастатическое поражение позвоночника обычно свидетельствует о четвертой стадии заболевания. Оно существенного ухудшает медицинские прогнозы.
Метастазы в кости диагностируют при запущенном раке простаты, легких, молочной железы и пр. Обычно они проявляются поражением позвоночника, тазовых костей, ребер и трубчатых костей рук или ног.
Метастазы в позвоночнике — это поражение костной ткани распространившимися по организму раковыми клетками. Они проникают в нее вместе с током лимфы или крови из первичной опухоли. А поскольку кости являются основой опорно-двигательной системы, то такая патология в короткий промежуток времени способна снизить качество жизни пациента и ухудшить прогноз в целом.
Метастазы нарушают функции остеобластов. Эти клетки отвечают за рост кости и репродукцию новых клеток, а также помогают «утилизировать» клетки, которые уже непригодны. Из-за этого метастазы могут вызывать следующие виды поражений:
- остеолитические — возникает постепенное истончение костей, повышается риск переломов даже при легких физических нагрузках;
- остеобластические — патологическое разрастание костной ткани.
Первичным симптомом метастазов является боль. На первых порах она купируется лекарственными препаратами, но со временем становится все более интенсивной. Наблюдается нарушение функциональности суставов. Анализы показывают избыток кальция. Возможно развитие компрессионного синдрома. Возникает сдавливание спинного мозга, что вызывает нарушение опорно-двигательной функции.
Чем раньше было выявлено онкологическое заболевание, тем выше шансы на его излечение. Именно поэтому так важно регулярно проходить плановые медицинские осмотры и при выявлении у себя описанных выше симптомов не затягивать с обращением к хирургу, который при подозрении на развитие новообразования сразу отправляет пациента к онкологу.
Роль сезона в общей выживаемости пациентов с метастазами в кости, подвергающихся лучевой терапии — Cihan
Несмотря на подготовку по ранней диагностике рака, успехи в диагностике и лечении, метастазы в кости (BM) являются одной из наиболее частых проблем в клинической практике. вверх. Хотя костные метастазы являются важным прогностическим фактором при многих опухолях, раннее выявление и оптимальное лечение необходимы для повышения общей выживаемости и улучшения качества жизни (1,2).
Скелетная система является третьим по частоте местом метастазирования после легких и печени (1).Распространение и частота метастазов в кости зависят от метода диагностики. Наиболее распространенные виды рака; грудь, простата и легкие составляют 80% BM. В то время как частота BM у пациентов с раком груди на поздних стадиях составляет 85%, это 50–70% для рака простаты, 32–40% для рака легких. Семьдесят процентов костного мозга составляют осевой скелет (череп, ребра и позвонки), а 30% — длинные кости (2-4). BM чаще всего возникает в результате гематогенного распространения раковых клеток. Микрометастатические опухолевые клетки обнаруживаются в костном мозге онкологических больных в 25–75% случаев.Но не все эти клетки вызывают клинически очевидный костный мозг, нарушая структурную целостность кости. Метастазирование в кости — это многоступенчатый процесс, включающий сложные взаимодействия. При наличии опухолевых клеток баланс между образованием и резорбцией кости нарушается, и образование новой кости не может компенсировать потерю (1,5).
У пациентов с раком легких, молочной железы и простаты с BM нет шансов на выздоровление с помощью сегодняшних подходов к лечению. Следовательно, основная цель лечения — улучшить выживаемость и продлить общее самочувствие до прогрессирования заболевания (1-3).Для лечения BM доступны как системные, так и местные варианты лечения. Выбор лечения зависит от состояния пациента, прогноза заболевания и продолжительности жизни (2). У 65–75% пациентов с метастазами в кости возникают боли в костях и двигательные нарушения. Поэтому важнейшими целями лечения являются обезболивание и сохранение функциональности. Лучевая терапия — лучший вариант лечения, который можно выбрать при метастатической боли в костях. Другие варианты лечения в этой ситуации не так эффективны, как ЛТ.Техника лучевой терапии, назначение доз и фракции определяются в зависимости от общего состояния, ожидаемой продолжительности жизни, мобильности, активов риска переломов, местоположения и количества метастазов, уровня функции костного мозга и предшествующего лечения пациента. Используются различные режимы облучения, такие как 10 × 3, 5 × 4, 1 × 10 и 1 × 8 Гр (6-8).
Хотя есть много опубликованных отчетов о важных прогностических факторах метастазов в кости, таких как пол и состояние здоровья пациента, первичная опухоль и ее гистология, локализация метастазов в кости (например,g., несущая способность) и его тип (например, остеолитический, остеобластический), степень метастазирования, количество болезненных метастазов, степень боли и семейное положение пациентов, нет исследования, которое изучает, является ли сезон важным фактор прогноза метастазов в кости (3-5). Целью этого ретроспективного исследования было выяснить, имеет ли сезон прогностическое значение у онкологических больных с метастазами в кости.
В наше исследование был включен 181 пациент с явными метастазами в кости.Из всех пациентов 116 мужчин и 65 женщин, средний возраст 62,8 года (диапазон от 28 до 85 лет). У 63 пациентов (34,8%) первичным очагом опухоли было легкое, у 61 пациента (33,7%) — грудь, а у 57 пациентов (31,5%) — простата. Среднее время наблюдения составляло от 10 дней до 169 месяцев. Среднее время развития метастазов в кости составило 16,8 ± 3,8 месяца. Средняя общая выживаемость составила 22,1 месяца. В то время как большинство случаев рака диагностировалось зимой, метастазы в кости чаще всего обнаруживались летом.Когда обнаружение метастазов в кости оценивали в соответствии с сезонным распределением, значимый результат был обнаружен только для типа рака (P <0,001). Но по полу, возрасту, типу рака, локализации метастазов в кости, количеству метастазов, количеству пациентов, прошедших лучевую терапию, и дозе фракции облучения, статистически значимых результатов не было ( таблица 1 ). Когда общая выживаемость оценивалась в соответствии с сезоном постановки диагноза, самая высокая выживаемость была обнаружена в весенней группе (78.6 месяцев), а самый низкий — в летней группе (50,5 месяцев) (P = 0,285). Кроме того, общая выживаемость пациентов, которым был поставлен диагноз зимой, была выше, чем в другие сезоны (P = 0,182). В однофакторном и многофакторном анализе факторами, которые значительно влияют на общую выживаемость, были тип рака и пол (P <0,001) (, таблица 2, ).
Таблица 1 Исходные характеристики пациентов с метастазами в кости (BM) в соответствии с квартилями сезона до лечения (n = 181)Полная таблица Таблица 2 Результаты одномерного и многомерного анализа общего выживания (OS)
Полная таблица
В нашем исследовании BM чаще всего возникает при раке легких, за которым следуют рак груди и простаты.Наиболее частым местом метастазов в кости были позвонки, а затем таз. Также чаще встречались множественные БМ. В литературе к раку, который приводит к метастазам в кости, часто указывается, соответственно, рак груди, простаты и легких. В исследовании Tubiana-Hulin et al. анатомическое распределение БМ было следующим; 59% позвонков, 49% таза, 30% ребра, 24% бедра, 20% черепа и 13% плечевой кости (1). Tiwana et al. изучили 1880 пациентов с BM и обнаружили, что наиболее частым местом метастазирования был позвоночник (68.5%), затем конечности (15,2%) и таз (14,4%) (8). В серии из 836 пациентов (33,2% рака молочной железы, 24,6% рака легких), у 285 пациентов были обнаружены метастазы в конечности и у 43 пациентов единственное поражение конечности, причем наиболее частой частью конечности для метастазов в кости был проксимальный отдел бедренной кости (65,2%). а затем плечевая кость (25,6%) (9). В другом отчете одиночное поражение кости было обнаружено у 41% из 703 пациентов с раком молочной железы с метастатическим поражением кости, а множественный BM был обнаружен у 59% (10). Частота и распределение метастазов в этом исследовании соответствуют результатам этих 703 пациентов.
Мы обнаружили, что общая выживаемость при раке легких была меньше, чем при раке груди и простаты (P <0,001). Кроме того, было обнаружено, что общая выживаемость короче у пациентов мужского пола, пациентов с множественными метастазами, пациентов с диагнозом BM летом, с метастазами в нижние конечности и у пациентов с множественными метастазами. При сравнении схем лечения мы не обнаружили значительной разницы между фракционными дозами. В литературе, в то время как общая выживаемость при раке легких измеряется месяцами, у пациентов с раком груди и простаты с BM протекает медленнее, а ожидаемая продолжительность жизни колеблется от 2 до 3 лет.Наличие BM значительно сокращает долгосрочную выживаемость пациентов с раком легких. Согласно исследованиям пациентов с раком молочной железы в литературе, ожидаемая общая выживаемость у пациентов с изолированным BM составляла 5–6 лет, а на поздних стадиях с добавлением других метастазов выживаемость составляла 2 года и 1–20%. из этих случаев наблюдалась общая выживаемость до 5 лет (3-5,8,9). В метаанализе Wu et al. сравнивались различные схемы лечения BM, и не было различий между режимами лучевой терапии (6).
Мы обнаружили, что общая выживаемость пациентов, у которых был диагностирован рак зимой, и больных, у которых диагностировали метастаз в кости весной, имели более высокую общую выживаемость. Robsahm et al. сообщил, что пациенты, у которых зимой диагностировали рак, имели более высокий риск смерти (11). В другом исследовании время диагностики пациентов с раком легких и молочной железы было сгруппировано в соответствии с сезоном, и сравнивалась краткосрочная (1 месяц) и долгосрочная (> 5 лет) выживаемость.При раке молочной железы краткосрочная выживаемость была выше в летней группе, а при раке легких долгосрочная выживаемость была выше в весенней группе (12).
В заключение, наше первоначальное исследование показало, что сезон не влияет на прогноз онкологических больных с метастазами в кости. Однако это исследование должно быть подкреплено дальнейшими исследованиями, в которых участвуют пациенты из разных культур.
Благодарности
Нет.
Конфликт интересов: Авторы не имеют конфликта интересов относительно заявленного.
Список литературы
- Tubiana-Hulin M. Заболеваемость, распространенность и распространение метастазов в кости. Bone 1991; 12 Suppl 1: S9-10. [PubMed]
- Lutz S, Berk L, Chang E, et al. Паллиативная лучевая терапия метастазов в кости: рекомендации ASTRO, основанные на фактических данных. Int J Radiat Oncol Biol Phys 2011; 79: 965-76. [PubMed]
- Ulas A, Bilici A, Durnali A, et al. Факторы риска событий, связанных со скелетом (SRE), и факторы, влияющие на выживаемость без SRE для пациентов с немелкоклеточным раком легкого с метастазами в кости.Tumor Biol 2015. [Epub перед печатью]. [PubMed]
- Nørgaard M, Jensen AØ, Jacobsen JB и др. События, связанные со скелетом, метастазы в кости и выживаемость при раке простаты: популяционное когортное исследование в Дании (1999–2007 гг.). Журнал Урол 2010; 184: 162-7. [PubMed]
- Yong M, Jensen AÖ, Jacobsen JB и др. Выживаемость пациентов с раком груди с метастазами в кости и событиями, связанными со скелетом: популяционное когортное исследование в Дании (1999–2007 гг.). Лечение рака груди 2011; 129: 495-503.[PubMed]
- Wu JS, Wong R, Johnston M, et al. Мета-анализ испытаний лучевой терапии с фракционированием дозы для облегчения болезненных метастазов в кости. Int J Radiat Oncol Biol Phys 2003; 55: 594-605. [PubMed]
- Wong E, Hoskin P, Bedard G, et al. Повторное облучение при болезненных метастазах в кости — систематический обзор. Радиотренажер Oncol 2014; 110: 61-70. [PubMed]
- Tiwana MS, Barnes M, Yurkowski E, et al. Заболеваемость и схемы лечения сложных метастазов в кости в программе лучевой терапии на уровне населения.Radiother Oncol 2015. [Epub перед печатью]. [PubMed]
- Fukuma H, Beppu Y, Chuma H и др. Диагностика и лечение метастатического рака костей конечностей. Ган То Кагаку Риохо 1987; 14: 1729-38. [PubMed]
- Коидзуми М., Ёсимото М., Касуми Ф. и др. Сравнение одиночных и множественных метастатических поражений скелета у пациентов с раком груди. Энн Онкол 2003; 14: 1234-40. [PubMed]
- Robsahm TE, Tretli S, Dahlback A, et al. Витамин D3 от солнечного света может улучшить прогноз рака груди, толстой кишки и простаты (Норвегия).Контроль причин рака 2004; 15: 149-58. [PubMed]
- Ройчоудхури Р., Робинсон Д., Коупленд В. и др. Сезон диагностики рака оказывает различное влияние на краткосрочную и долгосрочную выживаемость. Int J Cancer 2009; 124: 2436-41. [PubMed]
Цитируйте эту статью как: Cihan YB, Sarıgöz T, Arslan A. Роль сезона в общей выживаемости пациентов с метастазами в кости, подвергающихся лучевой терапии. Перевод Cancer Res 2016; 5 (1): 85-88. DOI: 10.3978 / j.issn.2218-676X.2016.01.08
выживаемости при раке костей
Показатели выживаемости могут дать вам представление о том, какой процент людей с таким же типом и стадией рака все еще жив в течение определенного времени (обычно 5 лет) после того, как им был поставлен диагноз.Они не могут сказать вам, сколько вы проживете, но могут помочь вам лучше понять, насколько вероятно, что ваше лечение будет успешным.
Имейте в виду, что показатели выживаемости являются оценочными и часто основываются на предыдущих результатах большого числа людей, у которых был конкретный рак, но они не могут предсказать, что произойдет в конкретном случае. Эта статистика может сбивать с толку и вызывать у вас больше вопросов. Поговорите со своим врачом о том, как эти цифры могут быть применимы к вам, поскольку он или она знакомы с вашей ситуацией.
Что такое 5-летняя относительная выживаемость?
Относительная выживаемость сравнивает людей с одним и тем же типом (и часто стадией) рака с людьми в общей популяции. Например, если относительная 5-летняя выживаемость для определенного типа и стадии рака кости составляет 80%, это означает, что у людей с этим раком вероятность в среднем примерно на 80% выше, чем у людей, не страдающих этим заболеванием. иметь этот рак, чтобы жить не менее 5 лет после постановки диагноза.
Откуда эти числа?
Американское онкологическое общество полагается на информацию из базы данных SEER *, поддерживаемой Национальным институтом рака (NCI), чтобы предоставить статистику выживаемости для различных типов рака.
База данных SEER отслеживает 5-летнюю относительную выживаемость для различных типов рака костей в Соединенных Штатах в зависимости от того, как далеко распространился рак. Однако база данных SEER не группирует раковые заболевания по стадиям AJCC TNM (стадия 1, стадия 2, стадия 3 и т. Д.).). Вместо этого он группирует раковые заболевания на локальные, региональные и отдаленные стадии:
- Локализованный: Нет никаких признаков того, что рак распространился за пределы кости, где он возник.
- Регион: Рак вырос за пределы кости в близлежащие кости или другие структуры или достиг близлежащих лимфатических узлов.
- Отдаленный: Рак распространился на отдаленные части тела, например, на легкие или кости в других частях тела.
5-летняя относительная выживаемость при раке костей
Эти цифры основаны на людях, у которых были диагностированы определенные типы рака костей в период с 2009 по 2015 годы. Информацию о показателях некоторых других наиболее распространенных типов рака костей см. В разделах «Показатели выживаемости при остеосаркоме» или «Показатели выживаемости при опухолях Юинга».
Хондросаркома
SEER стадия | 5-летняя относительная выживаемость |
Локализованный | 91% |
Региональный | 75% |
Дальний | 22% |
Все ступени SEER вместе | 78% |
Хордома
SEER стадия | 5-летняя относительная выживаемость |
Локализованный | 87% |
Региональный | 83% |
Дальний | 55% |
Все ступени SEER вместе | 82% |
Некоторые типы рака костей настолько редки, что показатели выживаемости доступны только для всех стадий вместе взятых, а не для отдельных стадий SEER.Например, 5-летняя относительная выживаемость для гигантоклеточной опухоли кости для всех стадий вместе взятых составляет 79%.
Что такое числа
- Эти цифры относятся только к стадии рака, когда он впервые диагностирован. Они не применяются позже, если рак растет, распространяется или возвращается после лечения.
- Эти числа учитывают не все. Показатели выживаемости сгруппированы в зависимости от того, насколько далеко распространился рак.Но другие факторы, такие как ваш возраст и общее состояние здоровья, тип и расположение рака, а также то, насколько хорошо рак поддается лечению, также могут повлиять на ваше мировоззрение.
- Люди, у которых сейчас диагностирован рак костей, могут иметь лучшее будущее, чем показывают эти цифры. Лечение со временем улучшается, и эти цифры основаны на людях, которым был поставлен диагноз и лечили не менее 5 лет назад.
* SEER = эпиднадзор, эпидемиология и конечные результаты
Метастазы рака простаты в кости: лечение и выживаемость
Рак простаты иногда может распространяться из предстательной железы в кости, что называется метастазами в кости.Хотя метастазы в кости неизлечимы, лечение может помочь облегчить симптомы и продлить жизнь.
Метастазы — это термин, обозначающий распространение рака на другие части тела. Хотя рак простаты может распространиться на любую часть тела, чаще всего он поражает кости.
Даже когда рак распространился с простаты на кости, врачи по-прежнему называют его раком простаты, а не раком костей.
При лечении метастазов в кости врачи стремятся свести к минимуму дальнейшее распространение рака и облегчить боль и другие симптомы.
В этой статье мы обсуждаем симптомы распространенного рака простаты и метастазов в кости. Мы также рассматриваем варианты лечения метастазов в кости, побочные эффекты лечения и выживаемость.
Ранний рак простаты часто протекает бессимптомно. Когда рак распространился за пределы простаты, врачи называют его распространенным раком простаты.
Симптомы распространенного рака простаты могут включать:
- затрудненное мочеиспускание или слабый или медленный поток мочи
- потребность в более частом мочеиспускании, обычно ночью
- кровь в моче или сперме
- эректильная дисфункция
- слабость или ощущение онемения в ногах или ступнях
- потеря контроля над мочевым пузырем или кишечником
Хотя многие из этих симптомов могут возникать не только из-за рака простаты, но и из-за других заболеваний, любой, кто их испытывает, должен обратиться к врачу для обследования.
Когда рак простаты распространился на кости, симптомы могут включать:
- боль в костях
- слабые кости, которые с большей вероятностью сломаются
- боль или скованность в шее или спине
- проблемы с мочеиспусканием
- запор
- онемение и слабость из-за сдавления спинного мозга
Метастазы в кости могут вызывать выброс кальция из костей в кровоток, в результате чего в крови накапливается высокий уровень кальция.Это состояние известно как гиперкальциемия. Нелеченная гиперкальциемия может быть очень опасной, и симптомы могут включать:
- тошноту
- запор
- потеря аппетита
- чувство сильной жажды
- частое мочеиспускание
- усталость и слабость
- головные боли
- боли в костях
- спутанность сознания
- депрессия, потеря памяти и раздражительность
Людям, у которых наблюдается любой из этих симптомов, следует немедленно обратиться к врачу.Раннее лечение метастазов в костях может помочь предотвратить дальнейшие осложнения.
Лечение метастазов в кости может облегчить боль и предотвратить осложнения. Врач будет работать с пациентом, чтобы разработать подходящий план лечения.
Варианты лечения включают:
Бисфосфонаты
Бисфосфонаты — это препараты, которые снижают потерю костной массы и могут помочь:
- укрепляют кости
- снимают боль в костях
- снижают высокий уровень кальция в крови
- снижают риск переломов
- замедляет рост рака в костях
Бисфосфонаты также могут уменьшить побочные эффекты гормональной терапии, которую некоторые люди могут получать для лечения рака простаты.
Золедроновая кислота (Зомета) — это бисфосфонат, который врачи чаще всего назначают людям с раком простаты. Обычно они вводят этот препарат внутривенно каждые 3-4 недели.
Деносумаб
Деносумаб, имеющий торговые марки Xgeva и Prolia, — еще один препарат, снижающий потерю костной массы. Это может помочь:
- снизить риск переломов, особенно если золедроновая кислота не работает.
- замедлить распространение рака, который еще не достиг костей.
Врачи вводят деносумаб под кожу человека каждые 4 недели.
Лучевая терапия
Лучевая терапия использует аппарат для наведения внешнего луча излучения на раковые клетки в теле человека. Это лечение может:
- уменьшить боль в костях
- уменьшить опухоли на позвоночнике для снятия давления
- уменьшить опухоли в других частях тела для облегчения симптомов
радиофармпрепараты
Врачи могут также вводить лекарства, называемые радиофармпрепаратами, для лечения людей с костные метастазы. Попадая в организм, эти лекарства перемещаются к костям и выделяют радиацию, которая может убить раковые клетки.
Радиофармпрепараты воздействуют на все пораженные кости одновременно, а не только на одну область.
Радиофармпрепараты, которые врачи используют для лечения рака простаты, распространившегося на кости, включают:
- хлорид стронция-89 (Метастрон)
- самарий-153 лексидронам (Квадрамет)
- радий-223 (Ксофиго)
Все эти препараты может помочь облегчить боль в костях. По данным Американского онкологического общества (ACS), если рак простаты распространился только на кости, а не на другие органы, радий-223 также может помочь людям жить дольше.
Лечение метастазов в кости может вызывать побочные эффекты у некоторых людей:
Бисфосфонаты и деносумаб
Бисфосфонаты и деносумаб могут вызывать аналогичные побочные эффекты, в том числе:
- гриппоподобные симптомы
- боли в костях или суставах
- диарея
- тошнота
- усталость
Людям, принимающим бисфосфонаты или деносумаб, может потребоваться прием добавок кальция и витамина D, чтобы не допустить слишком низкого уровня кальция.
Бисфосфонаты также могут вызывать проблемы с почками, поэтому врачи могут не рекомендовать эти препараты людям с нарушенной функцией почек.
В редких случаях прием бисфосфонатов или деносумаба может вызвать остеонекроз челюсти (ONJ). ONJ — серьезное заболевание, при котором костная ткань челюсти умирает из-за прекращения кровоснабжения. Это может привести к:
- боли и отеку во рту
- потере зубов
- инфекциям десен
Перед приемом бисфосфонатов или деносумаба важно сообщить врачу о любых стоматологических проблемах.Врачи часто советуют людям обратиться к стоматологу для решения любых стоматологических проблем, прежде чем начинать прием этих лекарств. Соблюдение правил гигиены полости рта, например правильная чистка зубов щеткой и ежедневная чистка зубной нитью, может помочь предотвратить ONJ.
Лучевая терапия
Внешняя лучевая терапия может вызвать некоторые побочные эффекты, в том числе:
- Проблемы с кишечником, такие как диарея, кровянистый стул и ректальное истечение. Некоторым людям может потребоваться соблюдение специальной диеты, чтобы уменьшить эти побочные эффекты.
- Усталость, которая может продолжаться некоторое время после прекращения лечения.
- Лимфедема, которая может вызывать скопление жидкости в определенных частях тела, таких как ноги и пах. Физическая терапия может помочь уменьшить боль и отек.
- Эректильная дисфункция. Врачи могут назначить лекарства, которые помогут при проблемах с эрекцией.
- Затруднения при мочеиспускании, такие как боль при мочеиспускании, случайное подтекание и потеря контроля над мочеиспусканием. При проблемах с мочеиспусканием доступно множество методов лечения, включая катетеры, лекарства, упражнения и хирургическое вмешательство.
Радиофармпрепараты
Радиофармацевтическая обработка может привести к уменьшению количества клеток крови.Низкое количество кровяных телец может увеличить риск инфицирования и кровотечения.
Люди, принимающие радиофармпрепараты, должны поговорить со своим врачом о симптомах, которые могут указывать на низкое количество клеток крови, и о мерах предосторожности, которые они могут предпринять для предотвращения этого.
Обезболивающие могут быть очень эффективными для облегчения боли при раке простаты и метастазах в кости.
Человек должен поговорить с врачом о любой боли, которую он испытывает. Врач может назначить соответствующее обезболивающее и вместе с пациентом разработать план обезболивания.
Обезболивающие наиболее эффективны, когда люди принимают их через регулярные промежутки времени, а не только при сильной боли.
Врачи также могут предложить совет и лечение любых других симптомов или побочных эффектов, которые могут возникнуть у человека.
Поделиться на PinterestВрач может назначить обезболивающее и помочь составить план обезболивания.В настоящее время не существует лекарства от распространенного рака простаты, но достижения в области лечения увеличивают продолжительность жизни и улучшают ее качество.
ACS утверждает, что 5-летняя относительная выживаемость людей с раком простаты, который распространился на удаленные лимфатические узлы, органы или кости, составляет 29 процентов. Соответственно, вероятность того, что люди с этой стадией рака простаты проживут не менее 5 лет после постановки диагноза, примерно на 29 процентов выше, чем у людей без этого заболевания.
Однако выживаемость — это всего лишь оценка, и все разные. Следующие факторы входят в число тех, которые могут повлиять на мировоззрение человека:
- возраст
- общее состояние здоровья
- симптомы
- как рак реагирует на лечение
- насколько далеко распространился рак
Продолжающиеся исследования рака также помогают разработка более эффективных методов лечения и повышение выживаемости.
Рак простаты может распространяться на другие органы тела. Когда рак распространяется на кости, это называется метастазированием в кости.
Хотя в настоящее время не существует лекарства от рака простаты, который распространился на кости, лечение может помочь облегчить боль, улучшить качество жизни и увеличить продолжительность жизни.
Врач будет тесно сотрудничать с человеком, чтобы разработать план лечения. Многие люди также считают полезным присоединиться к группе поддержки и общаться с другими людьми, которые понимают, что они могут чувствовать.Фонд рака простаты предоставляет информацию, чтобы помочь людям найти местную группу поддержки.
Когда рак распространяется на кости
Боль в костях
Сообщите своему врачу, если у вас есть боли в костях или суставах. Метастазы в кости могут быть очень болезненными. Ваше лечение может помочь уменьшить вашу боль, но не избавит от нее полностью. Вам также могут потребоваться другие лекарства или методы лечения самой боли. Если у вас болят кости, сообщите об этом своему лечащему врачу. Вы можете спросить о:
Получение направления к специалисту по боли или паллиативному специалисту ( PA-lee-uh-tiv ) .Паллиативная или поддерживающая терапия используется для лечения боли или других симптомов, вызванных раком и его лечением. Паллиативная помощь — это не то же самое, что уход в хосписе, то есть уход в конце жизни. Вы можете попросить направление к специалисту по паллиативной помощи на любом этапе лечения рака.
Принимаю обезболивающие. Лекарства, отпускаемые без рецепта, такие как Тайленол®, Адвил® или Мотрин®, могут быть всем, что вам нужно. Поговорите со своим врачом, чтобы убедиться, что вы принимаете правильную дозу. Даже если им не нужен рецепт, они все равно могут вызывать вредные побочные эффекты.Если они не уменьшают боль, поговорите со своим врачом о других типах обезболивающих.
Прием стероидов для уменьшения отека, усиливающего боль.
Использование излучения для лечения определенных участков боли в костях.
Компрессия спинного мозга
Одним из частых мест метастазов в кости является позвоночник. Важно, чтобы врач внимательно следил за метастазами в позвоночнике. Если они станут слишком большими, они могут раздавить (или сжать) ваш спинной мозг, что может парализовать вас и лишить вас возможности снова ходить или двигаться.
Позвоните своему врачу или немедленно обратитесь в отделение неотложной помощи, если у вас есть следующие симптомы:
- Усиливающаяся боль в спине
- Боль в спине и боль в ноге одновременно
- Онемение рук, ног или живота
- Проблемы со стоянием из-за слабости ног
- Проблемы с перемещением ног
- Проблемы с удержанием предметов в руках из-за слабости рук
- Потеря контроля над мочеиспусканием (мочой) или дефекацией (какашками).
Лечение компрессии спинного мозга может включать стероиды, лучевую терапию и / или хирургическое вмешательство.
Гиперкальциемия
Раковые клетки влияют на то, как ваше тело строит кости. Это может привести к истончению ваших костей. Это также может вызвать просачивание кальция из костей в кровь. Если уровень кальция в крови становится слишком высоким, у вас может развиться гиперкальциемия ( HY-per-kal-SEE-mee-uh ), поэтому важно лечить ее как можно раньше. Обязательно сообщите своему врачу, если у вас есть:
Если гиперкальциемия усугубляется и вы становитесь более обезвоженным, у вас также может быть мышечная слабость или боль в мышцах и суставах.Гиперкальциемия может быть опасной, если ее не лечить. Это может привести к судорогам, нерегулярному сердцебиению, сердечному приступу, спутанности сознания, потере сознания, коме или почечной недостаточности.
Чтобы предотвратить гиперкальциемию, вы можете:
- Пейте нужное количество жидкости.
- Получите достаточно соли в своем рационе.
- Контроль тошноты и рвоты.
- Оставайтесь активными, ходя пешком.
- Контроль лихорадки.
- Прекратите принимать добавки и лекарства, которые могут вызвать гиперкальциемию или повлиять на ее лечение.Ваша медицинская бригада может сказать вам, какие лекарства вам, возможно, необходимо прекратить.
Изменение диеты для уменьшения содержания кальция не приведет к снижению количества кальция в крови.
Выживание | Рак костей | Исследования рака, Великобритания
Выживание зависит от множества различных факторов. Никто не может сказать вам точно, сколько вы проживете. Зависит от вашего:
- тип и стадия рака
- уровень физической подготовки
- предыдущее лечение
Это общая статистика, основанная на больших группах пациентов.Помните, они не могут сказать вам, что произойдет в вашем конкретном случае.
Ваш врач может дать вам дополнительную информацию о вашем собственном прогнозе. Вы также можете поговорить об этом с медсестрами отдела исследования рака Великобритании по бесплатному телефону 0808 800 4040 с 9 до 17 часов с понедельника по пятницу.
Первичный и вторичный рак кости
Первичный рак кости начинается в костных клетках. Раковые клетки — это костные клетки, ставшие злокачественными.
Большинство людей с раковыми клетками в костях не болеют первичным раком костей.У них есть раковые клетки, которые распространились в кости от рака в другом месте тела. Это называется вторичным или метастатическим раком кости. Так, например, при раке груди, который распространился на кости, раковые клетки в костях будут клетками рака груди.
Все виды первичного рака кости
Обычно для людей с первичным раком кости в Англии:
- почти 85 из каждых 100 человек (почти 85%) выживают после рака в течение 1 года или более после постановки диагноза
- более 60 из каждых 100 человек (более 60%) выживают после рака в течение 5 лет или более после постановки диагноза
- 55 из каждых 100 человек (55%) выживают после рака в течение 10 и более лет после постановки диагноза
Эти статистические данные относятся к людям, у которых в Англии был диагностирован первичный рак кости в период с 2009 по 2013 год.
Чистая выживаемость и вероятность смерти от рака от редких видов рака.
P Muller и другие
Cancer Research UK Cancer Survival Group, Лондонская школа гигиены и тропической медицины
Эти статистические данные относятся к чистой выживаемости. Чистая выживаемость оценивает количество людей, переживших рак, а не количество людей, у которых диагностирован рак, которые еще живы. Другими словами, это выживаемость больных раком с учетом того, что некоторые люди умерли бы от других причин, если бы у них не было рака.
Выживаемость при различных типах первичного рака кости
В Великобритании нет статистических данных о выживаемости при различных типах рака костей.
Приведенные ниже статистические данные относятся к раку костей, диагностированному в Англии в период с 1985 по 2004 год. Они взяты из Национальной сети разведки рака. У нас есть информация о:
- Остеосаркома
- хондросаркома
- Саркома Юинга
- хордома
Пожалуйста, помните, что эти статистические данные относятся ко всем, у кого диагностирован каждый тип рака.Цифры не принимают во внимание другие факторы, влияющие на вашу выживаемость, такие как стадия и степень рака, ваш возраст, место расположения рака или эффективность химиотерапии. Ваш врач может рассказать вам больше о вашем собственном мировоззрении.
Остеосаркома
Более 40 из 100 человек (более 40%) выживают после рака в течение 5 или более лет после постановки диагноза.
Выживание лучше для молодых людей, чем для пожилых людей.
Для тех, кто моложе 40 лет, более 50 из 100 человек (более 50%) переживают рак в течение 5 или более лет. Среди тех, кто старше 40 лет, 25 из 100 человек (25%) переживают рак в течение 5 и более лет.
Выживание лучше для людей с остеосаркомой, начинающейся с черепа, лица, рук или ног, чем для людей с остеосаркомой в основной части тела.
Хондросаркома
Почти 70 из 100 человек (почти 70%) переживают рак в течение 5 или более лет после постановки диагноза.
Выживание лучше для людей с хондросаркомой, начинающейся с черепа, лица, рук или ног, чем для людей с хондросаркомой в основной части тела.
Саркома Юинга
Около 50 из 100 человек (около 50%) выживают после рака в течение 5 и более лет после постановки диагноза.
Выживание лучше для людей с саркомой Юинга, начинающейся с рук или ног, чем для людей с саркомой Юинга в основной части тела.
Хордома
Около 60 из 100 человек (около 60%) выживают после рака в течение 5 и более лет после постановки диагноза.
Заболеваемость и выживаемость саркомы костей: опухоли, диагностированные между 1985 и 2009 годами
Национальная сеть онкологической разведки, октябрь 2012 г.
Эти статистические данные относятся к относительной выживаемости.Относительная выживаемость учитывает, что некоторые люди умрут не от рака, а от других причин. Это дает более точную картину выживаемости при раке.
Что влияет на выживаемость
Ваш прогноз зависит от стадии рака, когда он был диагностирован. Это означает, насколько он велик и распространился ли он.
На выживаемость также влияет местонахождение рака в вашем теле.
Если перед операцией у вас будет химиотерапия, врачи осмотрят вашу опухоль, чтобы узнать, насколько хорошо она реагирует на химиотерапию.Если у вас есть хороший ответ, ваше мировоззрение лучше.
Об этой статистике
Термины 1 год выживания и 5 лет не означают, что вы проживете только 1 или 5 лет. Он относится к количеству людей, живущих 5 и более лет после постановки диагноза. Некоторые люди живут намного дольше 5 лет.
Дополнительная статистика
Определение прогноза для пациентов с неизлечимыми заболеваниями — консультация у Curbside
Сценарий случая
65-летняя женщина получает химиотерапию от рецидивирующего рака груди, который дал метастазы в кости, плевру и печень.Ее врач отложил несколько курсов лечения и изменил дозировку химиотерапии, потому что, несмотря на поддерживающее лечение, у нее развилась стойкая анемия. Биопсия и аспирация костного мозга выявили гиперцеллюлярность с избытком бластных клеток (20 процентов). У пациентки развилась «прелейкемия» (т.е. рефрактерная анемия с избытком бластных клеток), и ее врач сказал ей, что ей осталось жить шесть месяцев или меньше.
Как ее врач определил эти шестимесячные сроки? Мне сказали, что первый вопрос пациента после получения диагноза неизлечимой болезни обычно: «Сколько мне осталось времени?» Насколько точным может быть врач, предсказывая смерть? Какие факторы следует учитывать при определении прогноза?
Комментарий
Врачи часто переоценивают ожидаемую продолжительность жизни неизлечимого пациента.Одно исследование1 показало, что врачи переоценили выживаемость в 5,3 раза. Несколько клинических ориентиров и базовое понимание прогрессирования заболевания могут улучшить способность врача предлагать пациентам и их семьям более точные временные рамки для определения своих приоритетов.
Хотя медицинские решения часто основываются на прогнозе пациента, точный диагноз и окончательное лечение стали более важными в современных медицинских условиях. Пациенты обычно получают мало прогностической информации, и группы защиты традиционно сосредотачиваются только на выживании.Однако это меняется по мере того, как медицина становится все более основанной на доказательствах. Исследователи оценивают результаты лечения на основе факторов, выходящих за рамки простого выживания (например, стоимость лечения, качество жизни, тяжесть симптомов, лицо, осуществляющее уход, и социальное бремя) .2
Наиболее важные прогностические факторы, которые следует учитывать при лечении в зависимости от конкретного случая женщина с рецидивирующим раком груди (например, местным рецидивом в грудной стенке, регионарных лимфатических узлах или, чаще всего, с отдаленными метастазами в кости) — это период без болезни (т.е. время между завершением первичного лечения и рецидивом заболевания), а также степень и расположение метастазов. Эти факторы могут помочь предсказать клиническое поведение и прогрессирование заболевания.
Пациент с длительным периодом отсутствия болезни (например, один год или более) и ограниченными метастазами будет иметь лучший прогноз, чем пациент, который не болел менее одного года и имел более распространенные метастазы. Метастазы в кость или плевру не представляют угрозы для жизни; однако метастазы в печень, легкие или мозг значительно сокращают продолжительность жизни пациента.Средняя продолжительность жизни пациента с метастазами в печень и легкие составляет менее шести месяцев. Ожидаемая продолжительность жизни пациента с обширными метастазами или метастазами в лимфатические узлы составляет менее шести недель. Пациенты с метастазами в головной мозг имеют более вариабельную продолжительность жизни (от одного до 16 месяцев) в зависимости от количества и локализации поражений и специфики лечения. Некоторые осложнения рака (например, рецидивирующая гиперкальциемия и сепсис, злокачественный выпот в перикард и карциноматоз брюшной полости с асцитом и частичной непроходимостью кишечника) связаны с менее благоприятными прогнозами.Многие пациенты с сопоставимыми заболеваниями будут реагировать аналогичным образом; однако у некоторых дела обстоят намного хуже или намного лучше, чем ожидалось. Прогноз пациента также основан на его реакции на лечение.
Помимо гистопатологии рака, метастазов и опухолевых осложнений, двумя наиболее важными факторами, на которые следует обратить внимание при определении прогноза, являются: (1) насколько хорошо пациент может выполнять повседневные действия (например, купаться, одеваться, пользоваться туалетом). ), и (2) насколько обременительны симптомы для пациента.3 Врачи могут использовать шкалу Карновского (KPS) 3, чтобы помочь определить способность пациента выполнять повседневную деятельность. Если пациент ведет сидячий образ жизни в течение 50 или более процентов своего времени бодрствования и становится все более зависимым от лиц, осуществляющих уход, или если у него или у нее показатель KPS менее 50 процентов, ожидаемая продолжительность жизни составляет от двух до трех месяцев3. такие как затрудненное глотание, сухость во рту, одышка, отсутствие аппетита и потеря веса могут предвещать худший прогноз4 и могут сопровождать синдром анорексии-кахексии (истощение).Усиление симптомов и снижение функциональности вызывают прогрессирующее истощение. Прогрессирующее истощение (и его последующие осложнения) — это основной механизм, приводящий к смерти неизлечимых пациентов.
Другие важные прогностические факторы включают сопутствующие заболевания, возраст и статус питания. Также следует учитывать психосоциальные и духовные факторы. Недавние данные5 поставили под сомнение представление о том, что пациенты с сильной «волей к жизни» часто живут дольше, чем те, кто смирился с тем, что они умрут; однако пациенты с недостаточной социальной поддержкой и пациенты, которые бедны или плохо соблюдают предписанные схемы лечения, могут иметь более короткую продолжительность жизни.Нерешенные проблемы в отношениях или экзистенциальный стресс могут продлить процесс умирания.
На последних стадиях рака состояние пациентов обычно быстро ухудшается.6 Пациенты могут прожить несколько месяцев с небольшим потреблением пищи, но они не могут жить без адекватного потребления жидкости. Следовательно, уменьшение потребления жидкости и диуреза может помочь определить, когда пациенту следует получить паллиативную помощь.
В конечном итоге роль семейного врача в определении прогноза зависит от его или ее общения с онкологом пациента и от того, насколько он или она вовлечены в уход за пациентом.В будущих консультациях по Curbside будут рассмотрены вопросы, связанные с плохим прогнозом пациента.
Клинические результаты для пациентов с мелкоклеточным раком легкого с метастазами в кости на момент постановки диагноза
Резюме
Цели
Характеристики и прогностические факторы пациентов с мелкоклеточным раком легкого (МРЛ) с метастазами в кости при первом диагнозе практически не изучены. сообщил. Это исследование было направлено на анализ прогностических факторов этих пациентов и на разработку системы оценки выживаемости, чтобы предоставить доказательства для принятия клинических решений о лечении.
Материалы и методы
Были ретроспективно проанализированы записи 102 пациентов с метастазами в кости с метастазами в кости на момент постановки диагноза, которые находились в нашей больнице в период с мая 2010 года по май 2015 года. Лог-ранговый тест и многомерный регрессионный анализ Кокса использовались для оценки потенциальных клинических предикторов выживаемости. Система оценки была разработана на основе отношения рисков значимых независимых прогностических факторов.
Результат
Наиболее частым местом метастазов в кости был позвоночник (64.7%) и 26 пациентов (25,6%) имели одиночный метастаз в кости. Средняя выживаемость составила 10,4 месяца, а 2-летняя выживаемость — 10,3%. Возраст, количество костных метастазов и наличие внекостных отдаленных метастазов были важными независимыми прогностическими факторами общей выживаемости. На основании полученных баллов пациенты были разделены на три группы. Среднее время выживания в трех группах составляло 6,4 месяца, 8,5 месяца и 12,4 месяца, а 2-летняя выживаемость составила 0%, 2,9% и 19,3% (p = 0.
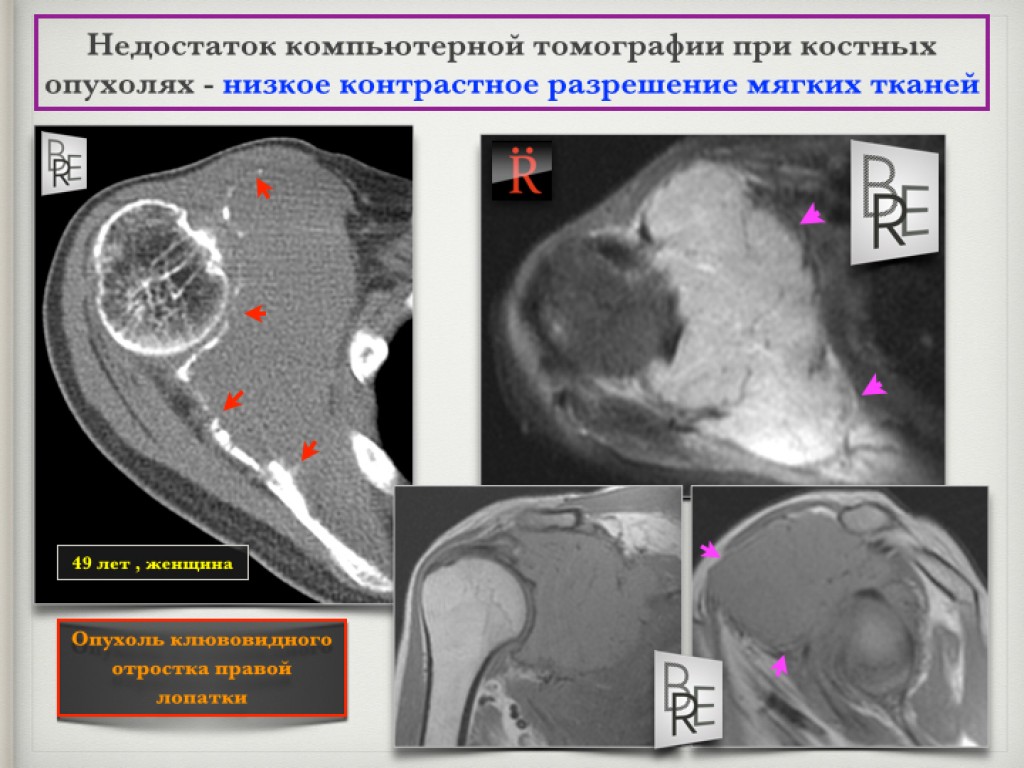
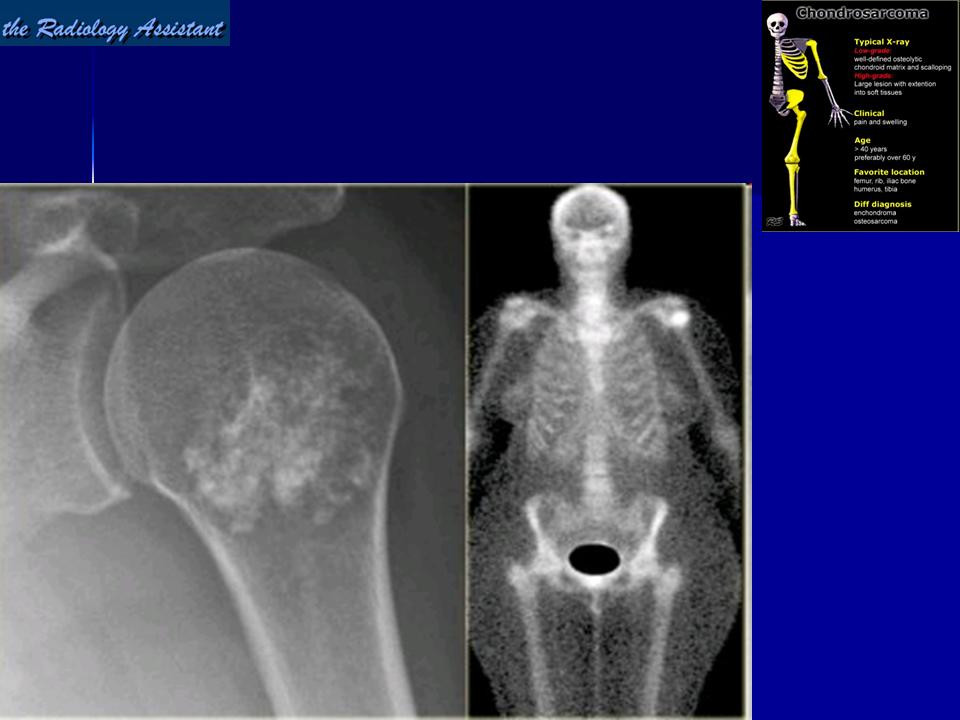
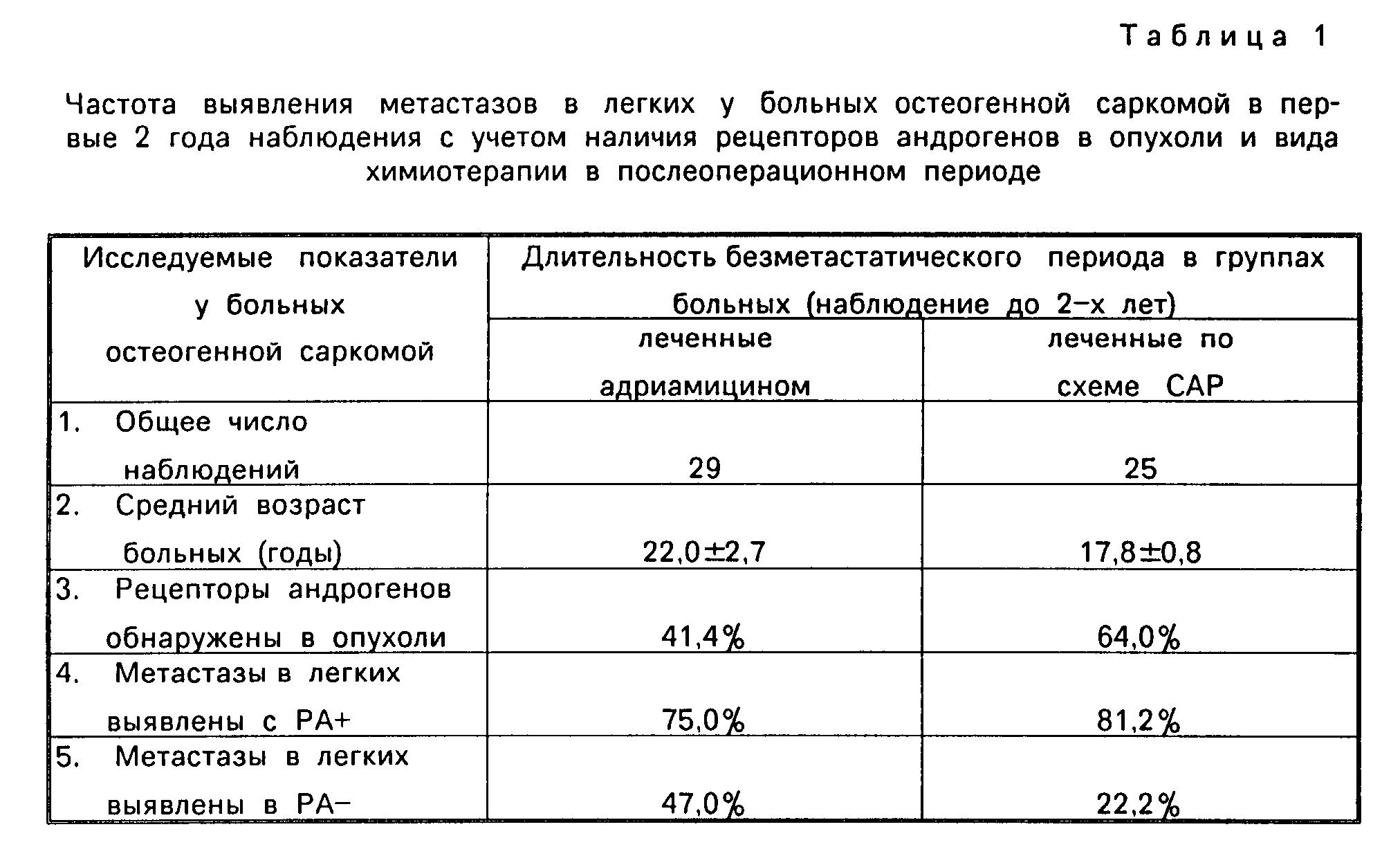 С., Кочетова Т. Ю., Крылов В. В. Практические рекомендации по радионуклидной терапии при метастазах в кости // Злокачественные опухоли, № 4, 2016, Спецвыпуск 2.
С., Кочетова Т. Ю., Крылов В. В. Практические рекомендации по радионуклидной терапии при метастазах в кости // Злокачественные опухоли, № 4, 2016, Спецвыпуск 2.
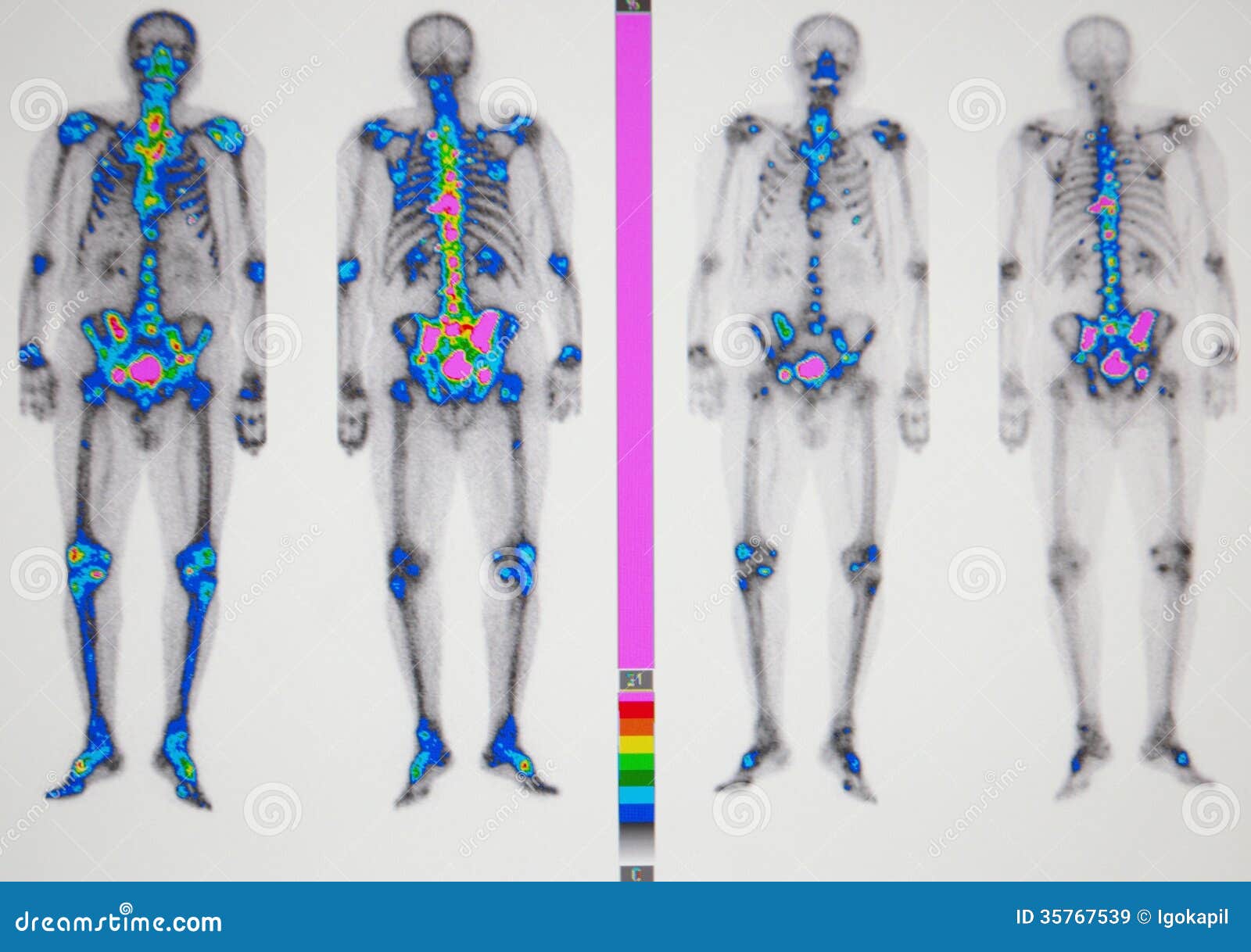

 Кислородное голодание проявляется прерывистым дыханием, которое на 1-2 секунды может пропадать совсем. Дыхание становится поверхностным, выдохи по продолжительности превышают длительность вдоха. Хлюпанье и посвистывающие звуки при дыхании объясняются тем, что дыхательный орган повреждён метастазами.
Кислородное голодание проявляется прерывистым дыханием, которое на 1-2 секунды может пропадать совсем. Дыхание становится поверхностным, выдохи по продолжительности превышают длительность вдоха. Хлюпанье и посвистывающие звуки при дыхании объясняются тем, что дыхательный орган повреждён метастазами.