Углеводы и их роль в жизнедеятельности клетки
1. Какие вещества, относящиеся к углеводам, вам известны?
Ответ. Углеводы (сахариды) — общее название обширного класса природных органических соединений. Название происходит от слов «уголь» и «вода». Углеводы делятся на две группы: простые и сложные. Простые углеводы — глюкоза и фруктоза, дисахарид – сахароза, полисахариды – крахмал и целлюлоза
2. Какую роль играют углеводы в живом организме?
Ответ. Углеводы в живом организме выполняют ряд функций: энергетическую, строительную, защитную, запасающую функции.
Вопросы после §9
1. Какие углеводы называют моно-, олиго– и полисахаридами?
Ответ. Моносахариды (от греч. monos – один) – бесцветные кристаллические вещества, легко растворимые в воде и имеющие сладкий вкус. Из моносахаридов наибольшее значение для живых организмов имеют рибоза, дезоксирибоза, глюкоза, фруктоза, галактоза. Рибоза входит в состав РНК, АТФ, витаминов группы В, ряда ферментов. Дезоксирибоза входит в состав ДНК. Глюкоза (виноградный сахар) является мономером полисахаридов (крахмала, гликогена, целлюлозы). Она есть в клетках всех организмов. Фруктоза входит в состав олигосахаридов, например сахарозы. В свободном виде содержится в клетках растений. Галактоза также входит в состав некоторых олигосахаридов, например лактозы.
Из моносахаридов наибольшее значение для живых организмов имеют рибоза, дезоксирибоза, глюкоза, фруктоза, галактоза. Рибоза входит в состав РНК, АТФ, витаминов группы В, ряда ферментов. Дезоксирибоза входит в состав ДНК. Глюкоза (виноградный сахар) является мономером полисахаридов (крахмала, гликогена, целлюлозы). Она есть в клетках всех организмов. Фруктоза входит в состав олигосахаридов, например сахарозы. В свободном виде содержится в клетках растений. Галактоза также входит в состав некоторых олигосахаридов, например лактозы.
Олигосахариды (от греч. oligos – немного) образованы двумя (тогда их называют дисахариды) или несколькими моносахаридами, связанными ковалентно друг с другом с помощью гликозидной связи. Большинство олигосахаридов растворимы в воде и имеют сладкий вкус. Из олигосахаридов наиболее широко распространены дисахариды: сахароза (тростниковый сахар), мальтоза (солодовый сахар), лактоза (молочный сахар).
Полисахариды (от греч. poly – много) являются полимерами и состоят из неопределённо большого (до нескольких сотен или тысяч) числа остатков молекул моносахаридов, соединённых ковалентными связями.
2. Какие функции выполняют углеводы в живых организмах?
Ответ. Основная функция углеводов – энергетическая. При их ферментативном расщеплении и окислении молекул углеводов выделяется энергия, которая обеспечивает жизнедеятельность организма. При полном расщеплении 1 г углеводов освобождается 17,6 кДж.
Углеводы выполняют запасающую функцию. При избытке они накапливаются в клетке в качестве запасающих веществ (крахмал, гликоген) и при необходимости используются организмом как источник энергии. Усиленное расщепление углеводов происходит, например, при прорастании семян, интенсивной мышечной работе, длительном голодании.
Очень важной является структурная, или строительная, функция углеводов. Они используются в качестве строительного материала. Так, целлюлоза благодаря особому строению нерастворима в воде и обладает высокой прочностью. В среднем 20–40 % материала клеточных стенок растений составляет целлюлоза, а волокна хлопка – почти чистая целлюлоза, и именно поэтому они используются для изготовления тканей.
Хитин входит в состав клеточных стенок некоторых простейших и грибов. В качестве важного компонента наружного скелета хитин встречается у отдельных групп животных, например у членистоногих.
Углеводы выполняют защитную функцию. Так, камеди (смолы, выделяющиеся при повреждении стволов и веток растений, например слив, вишен), препятствующие проникновению в раны болезнетворных микроорганизмов, являются производными моносахаридов.
Твердые клеточные стенки одноклеточных и хитиновые покровы членистоногих, в состав которых входят углеводы, также выполняют защитные функции.
3. Почему углеводы считаются главными источниками энергии в клетке?
Ответ. Углеводы считаются главными источниками энергии в клетке потому, что при их расщеплении выделяется достаточно количества энергии. Углеводы доступны организму. Расщепление углеводов происходит быстрее, чем остальных органических веществ.
► Обычно в клетке животных организмов содержится около 1 % углеводов, в клетках печени их содержание доходит до 5 %, а в растительных клетках – до 90 %. Подумайте и объясните почему.
Ответ. В растительных клетках — большой процент углеводов, т. Так как растения автотрофы и в их клетках постоянно идёт процесс фотосинтеза углеводов.
В печени животных более высокое содержание углеводов, т. к. в её клетках находится запас глюкозы в виде гликогена.
► Углеводы являются производными многоатомных спиртов и состоят из углерода, водорода и кислорода. Химики определяют эти соединения как многоатомные оксиальдегиды или многоатомные оксикетоны. Название «углеводы» хотя и является устаревшим, но и по сей день широко используется, в том числе и в научной литературе. Своё название этот класс соединений получил потому, что у большинства из них соотношение водорода и кислорода в молекуле такое же, как и в воде. Общая формула углеводов Cn(h30)m, где n не меньше 3. Однако не все соединения, относящиеся к классу углеводов, соответствуют данной формуле.
Химики определяют эти соединения как многоатомные оксиальдегиды или многоатомные оксикетоны. Название «углеводы» хотя и является устаревшим, но и по сей день широко используется, в том числе и в научной литературе. Своё название этот класс соединений получил потому, что у большинства из них соотношение водорода и кислорода в молекуле такое же, как и в воде. Общая формула углеводов Cn(h30)m, где n не меньше 3. Однако не все соединения, относящиеся к классу углеводов, соответствуют данной формуле.
Выясните, какие это соединения.
Ответ. Общая формула углеводов Сn(h3O)m. Однако с развитием химии углеводов обнаружены соединения, состав которых не отвечает приведенной общей формуле,но обладающие свойствами веществ своего класса(например,C5h20O4-Дезоксирибоза). Еще одним примером может служить молочная кислота С3Н6 О3.
Углеводы — основные функции в клетке простых и сложных: в чем заключается строительная, защитная и энергетическая роль
Для поддержания нормальной жизнедеятельности человеку необходимо употреблять белки, жиры и углеводы. И ни один элемент нельзя взять и перестать принимать. Недостаток каждого из них может привести к тяжелым последствиям или даже к смерти….
И ни один элемент нельзя взять и перестать принимать. Недостаток каждого из них может привести к тяжелым последствиям или даже к смерти….
Содержание
Что такое углеводы
Углеводы
Так называют органические вещества, состоящие из молекул сахара. Эти соединения получили свое название из-за своего состава – углерод и вода, которые соединяются между собой. По-другому их называют сахаридами. В зависимости от количества молекул сахара их делят на моносахариды, дисахариды, олигосахариды и полисахариды.
Клетки какого организма наиболее богаты ими? Наиболее богаты углеводами растения: содержание сахаров – до 80%, а у животных их не более 3%.
Сахариды играют важную роль. Главными их предназначениями являются:
- энергетическая,
- строительная,
- рецепторная,
- защитная,
- запасающая,
- регуляторная,
- метаболическая.
Следовательно, видна их важность в целом, без них невозможно представить существование животных и растений. А какова роль углеводов в клетке? В чем заключаются их главные миссии – строительная и энергетическая? Рассмотрим подробнее.
А какова роль углеводов в клетке? В чем заключаются их главные миссии – строительная и энергетическая? Рассмотрим подробнее.
Это интересно! Что такое пластический и энергетический обмен
Строительная
Строительная, или структурная, – это основная функция углеводов, которая заключается в том, что это строительный материал для клеток. Какие углеводы выполняют в клетке строительную миссию? В ней участвуют целлюлоза, хитин, рибоза и дезоксирибоза.
Так, например, у грибов и членистоногих строительную функцию выполняет хитин, а целлюлоза (полисахарид) – у растений. Таким образом придается прочность клетке. У растительной содержание целлюлозы достигает 40%, поэтому они хорошо держат форму. Структурная функция мальтозы – обеспечение образования новых клеток прорастающих семян.
Углеводы, роль в клетке
Рибоза и дезоксирибоза участвуют в построении таких молекул, как РНК, ДНК, АТФ и другие. Образование новых молекул происходит постоянно, а с разрушением старых освобождается свободная энергия.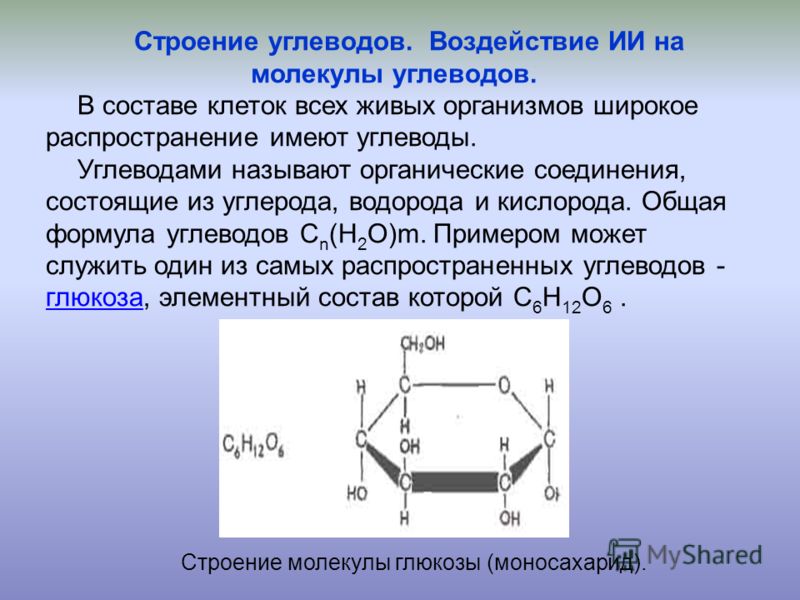 При построении мембраны цитоплазмы также проявляется рецепторная функция углеводов, а именно передаются сигналы из внешнего мира.
При построении мембраны цитоплазмы также проявляется рецепторная функция углеводов, а именно передаются сигналы из внешнего мира.
Таким образом, строительная функция углеводов имеет большое значение для всех процессов, как и энергетическая.
Энергетическая функция
Это основная роль таких органических соединений, и только они дают больше всего энергии. Так, при распаде 1 грамма освобождается 4,1 ккал (38,9 кДж) и 0,4 грамма воды. Такой энергии не может дать ни один другой элемент клетки, поэтому они обеспечивают весь организм нужным ее количеством. Именно они поддерживают тонус, придают жизненные силы и энергию, а главное – позволяют организмам существовать.
Энергетическую миссию выполняют мальтоза, сахароза, фруктоза и глюкоза. Они служат источниками клеточного дыхания, энергией для прорастания семян, фотосинтеза и других важных биологических процессов.
Важно! Шоколадки, конфеты и другие сладости, помимо выделения гормона радости, также содержат огромное количество сахаридов, поэтому и являются отличным источником энергии и заряда бодрости. Это и есть главная функция простых углеводов в клетке.
Это и есть главная функция простых углеводов в клетке.
Такая энергия позволяет человеку активно заниматься спортом, умственной деятельностью, а также участвуют во многих жизненно важных системах:
- газообменная,
- выделительная,
- кровеносная,
- строительная и другие.
Поэтому без энергетической подпитки человек не сможет нормально существовать.
Защитная
Защитная функция очень важна. Практически в каждом органе существуют железы, которые выделяют некий секрет. А он, в свою очередь, большей частью состоит из сахаров. Этот секрет защищает внутренние органы, например выделительные или органы ЖКТ, от внешних факторов – микробов, химических или механических.
Углеводы
Защиту обеспечивают, по большей части, моносахариды – гепарин, хитин, камедь и слизь. А значит, это главная роль моносахаридов. Так, например, простой моносахарид хитин – оболочка панциря членистоногих и грибов. А гепарин выполняет миссию антикоагулянта. Также у растений существуют свои защитные механизмы – шипы и колючки, которые состоят из целлюлозы. Камедь и слизь возникает при травмах оболочки растений, для образования защитного слоя в местах травм.
Также у растений существуют свои защитные механизмы – шипы и колючки, которые состоят из целлюлозы. Камедь и слизь возникает при травмах оболочки растений, для образования защитного слоя в местах травм.
Запасающая
Запасающая роль напрямую связана с энергетической ролью сахаров. Ведь энергия, которая поступает в организм, тратится не полностью, часть ее откладывается. Во время «аварийных ситуаций» она освобождается, например, во время голода или заболевания, для борьбы с вирусом.
Для этого предназначены следующие соединения:
- крахмал (инулин) – содержится в растениях,
- целлюлоза – также в растительных организмах,
- лактоза – в молоке млекопитающих животных,
- гликоген (животный жир) – в организме животных и людей.
Верблюжий жир служит не только запасом нужной энергии, но и может расщепляться в воду.
Таким образом, полисахариды помогают поддерживать нормальную жизнедеятельность.
Регуляторная
Под ней подразумевают способность сахаридов регулировать количество некоторых веществ в организме.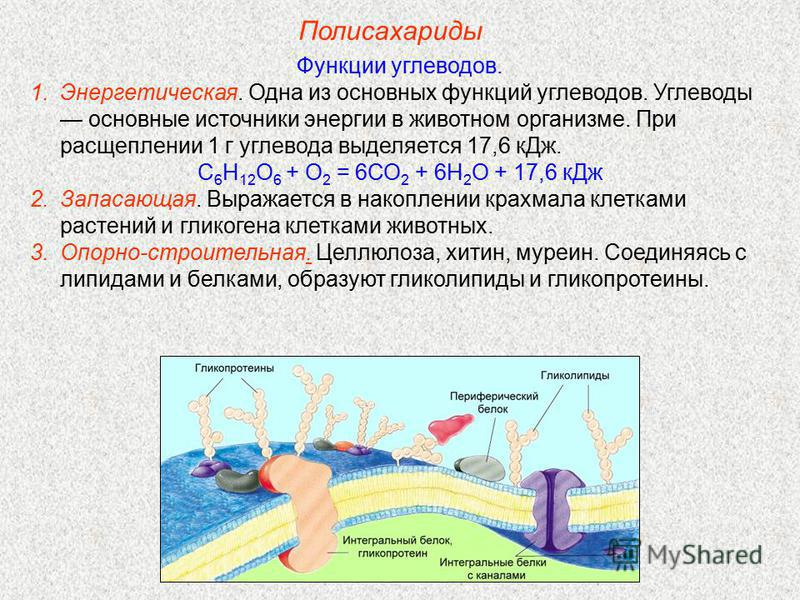 Так, например, глюкоза, которая содержится в крови, регулирует гомеостаз и осмотическое давление. А клетчатка, которая плохо усваивается человеческим организмом, имеет грубую структуру, благодаря чему раздражает рецепторы желудка и быстрее продвигается в нем.
Так, например, глюкоза, которая содержится в крови, регулирует гомеостаз и осмотическое давление. А клетчатка, которая плохо усваивается человеческим организмом, имеет грубую структуру, благодаря чему раздражает рецепторы желудка и быстрее продвигается в нем.
Метаболическая
Проявляется в способности моносахаридов синтезироваться в важные элементы для поддержания жизнедеятельности – полисахариды, нуклеотиды, аминокислоты и другие. Все это жизненно важно, поэтому углеводосодержащие продукты должны быть в рационе всегда.
Продукты с большим количеством сахаридов
Стоит помнить, что у растений сахариды синтезируются при фотосинтезе, но у животных они никак не появляются сами по себе. Получить нужную их дозу можно только с помощью еды.
Углеводы
Самое большое количество сахаридов содержится в рафинаде и меде. Сахар и рафинад целиком углеводны, а мед содержит глюкозу и фруктозу – до 80% от общей массы.
Большое содержание их в продуктах растений. Наибольшее количество во фруктах, ягодах, овощах, корнеплодах. Большой процент содержания в макаронах, сладостях, в мучных изделиях и продуктах брожения (пиве).
Большой процент содержания в макаронах, сладостях, в мучных изделиях и продуктах брожения (пиве).
Важно! В продуктах животного происхождения углеводов очень мало. Например, лактоза – молочный сахар, содержится в молоке млекопитающих животных.
Важно помнить, что сахариды, особенно быстрые, являются источниками ожирения человеческого организма. Поэтому употреблять их нужно в очень ограниченном количестве, так, например, сладкое и хлебобулочные изделия, лучше убрать из рациона или свести к минимуму.
Роль углеводов в жизни клетки
Углеводы их функции, значение, где содержатся
Выводы
Углеводные соединения играют важную роль, без них живое просто перестанет существовать. Растения синтезируют их при фотосинтезе, с помощью хлорофиллов. А вот человек и животные их не синтезируют, именно поэтому нужно потреблять суточную норму из пищи. Наибольшее их количество содержится во фруктах, ягодах, хлебе, сладостях. А чистым сахаридом является сахар.
А вот человек и животные их не синтезируют, именно поэтому нужно потреблять суточную норму из пищи. Наибольшее их количество содержится во фруктах, ягодах, хлебе, сладостях. А чистым сахаридом является сахар.
Углеводы — презентация на Slide-Share.ru 🎓
1
Первый слайд презентации: Углеводы
Биология 10 класс
Изображение слайда
2
Слайд 2
Органические вещества, в состав которых входят три химических элемента: углерод, водород, кислород. Общая формула углеводов: Cn (H 2 O)m (где n не меньше трех) Углеводы
Изображение слайда
3
Слайд 3
Российский химик немецко – балтийского происхождения. Впервые ввел термин «углеводы» в 1844 г.
Углеводы
Карл Генрихович Шмидт
(1822 – 1894)
Впервые ввел термин «углеводы» в 1844 г.
Углеводы
Карл Генрихович Шмидт
(1822 – 1894)
Изображение слайда
4
Слайд 4
Углеводы Содержание в клетке Классификация Функции углеводов Готовимся к ЕРЭ
Изображение слайда
5
Слайд 5
Животные В клетках содержится 2 – 5% углеводов С одержание углеводов в клетках Растения В клетках содержится 70 – 90% от сухой массы (особенно много в клетках клубня картофеля, семенах)
Изображение слайда
6
Слайд 6
Углеводы Простые Полисахариды Олигосахариды Моносахариды Сложные
Изображение слайда
7
Слайд 7
Моносахариды (простые сахара) Состоят из одной молекулы Твердые кристаллические вещества Растворимые в воде Сладкие на вкус
Изображение слайда
8
Слайд 8
Моносахариды (простые сахара) Триозы Молекула содержит три атома углерода Тетрозы Молекула содержит четыре атома углерода Молекула содержит пять атомов углерода Молекула содержит шесть атомов углерода Пентозы Гексозы
Изображение слайда
9
Слайд 9
Триозы Практическое значение имеют глицерин и его производные: молочная и пировиноградная кислоты Молочная кислота Пировиноградная кислота
Изображение слайда
10
Слайд 10
Тетрозы Эритроза – промежуточный продукт фотосинтеза Эритроза
Изображение слайда
11
Слайд 11
Пентозы Рибоза С 5 Н 10 О 5 Дезоксирибоза С 5 Н 10 О 5 Входит в состав РНК Входит в состав ДНК
Изображение слайда
12
Слайд 12
Гексозы Глюкоза – виноградный сахар С 6 Н 12 О 6 Встречается в свободном виде как в клетках растений, так и животных Первичный источник энергии для клеток Обязательно находится в крови (снижение количества глюкозы приводит к нарушению деятельности мышечных и нервных клеток, иногда даже к обморочным и судорожным состояниям)
Изображение слайда
13
Слайд 13
Гексозы Фруктоза – плодовый сахар С 6 Н 12 О 6 Широко распространена в природе В больших количествах находится в плодах Особенно много в меде, сахарной свекле, фруктах Фруктоза очень важна при питании больных сахарным диабетом, когда глюкоза очень слабо усваивается клетками
Изображение слайда
14
Слайд 14
Гексозы Галактоза – пространственный изомер глюкозы С 6 Н 12 О 6 В природе в чистом виде не встречается, образуется при распаде лактозы (молочного сахара)
Изображение слайда
15
Слайд 15
Олигосахариды — дисахариды Сахароза – тростниковый или свекловичный сахар С 12 Н 22 О 11 Состоит из остатков глюкозы и фруктозы Широко распространена в растениях (ягоды, корни, клубни, семена, плоды) Играет огромную роль в питании животных и человека Источники пищевого сахара в промышленности – сахарный тростник и сахарная свекла
Изображение слайда
16
Слайд 16
Олигосахариды — дисахариды Лактоза – молочный сахар С 12 Н 22 О 11 Состоит из остатков глюкозы и галактозы Является основным источником энергии для детенышей млекопитающих Используют в микробиологической промышленности для приготовления питательных сред
Изображение слайда
17
Слайд 17
Олигосахариды — дисахариды Мальтоза – солодовый сахар С 12 Н 22 О 11 Состоит из двух остатков глюкозы Содержится в солоде – проросших, высушенных и размолотых зернах ячменя Менее сладкая, чем сахароза Добавляют в хлебобулочные изделия и продукты детского питания
Изображение слайда
18
Слайд 18
Полисахариды Крахмал (С 6 Н 10 О 5 ) n Состоит из остатков амилозы и амилопектина Резервный полисахарид растений Находится в виде зернышек слоистого строения, нерастворимых в холодной воде В горячей воде образует коллоидный раствор (в быту – клейстер)
Изображение слайда
19
Слайд 19
Полисахариды Гликоген (С 6 Н 10 О 5 ) n Содержится во всех животных тканях, а также в грибах, дрожжах В значительных количествах накапливается в печени, мышцах, сердце Является поставщиком глюкозы в кровь Является «животным крахмалом», сдержит около 30 000 глюкозных остатков
Изображение слайда
20
Слайд 20
Полисахариды Клетчатка (целлюлоза) Главный структурный полисахарид клеточных оболочек растений В ней аккумулировано около 50% всего углерода биосферы Нерастворима в воде (она в ней только набухает)
Изображение слайда
21
Слайд 21
Полисахариды Хитин По структуре близок к целлюлозе Образует покровы тела членистоногих Компонент клеточной стенки грибов
Изображение слайда
22
Слайд 22
Функции углеводов Энергетическая При расщеплении 1 г углеводов выделяется 17,6 кДж энергии Структурная Из целлюлозы состоит клеточная стенка растений, из муреина – клеточная стенка бактерий, из хитина – клеточная сенка грибов, покровы членистоногих
Изображение слайда
23
Слайд 23
Функции углеводов
Запасающая
Резервный углевод животных и грибов – гликоген; у растений — крахмал
Защитная
Вязкие секреты (слизи), выделяемые различными железами состоят из углеводов.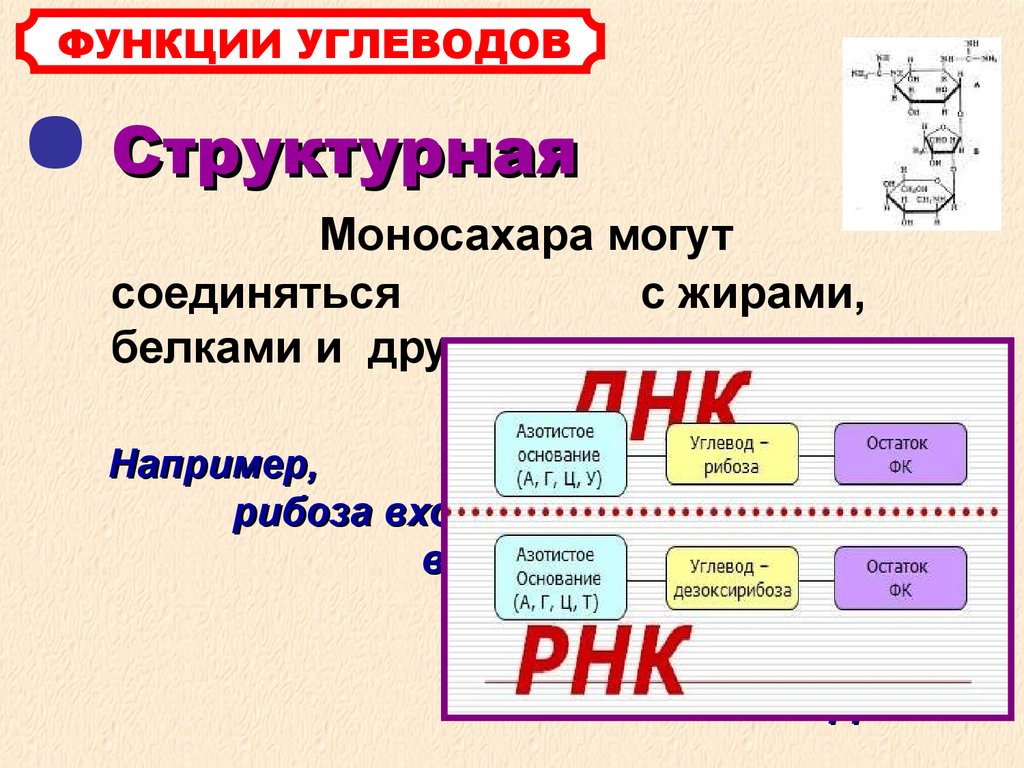 Они предохраняют стенки полых органов (пищевода, кишечника, желудка, бронхов) от механических повреждений, проникновения бактерий и вирусов
Они предохраняют стенки полых органов (пищевода, кишечника, желудка, бронхов) от механических повреждений, проникновения бактерий и вирусов
Изображение слайда
24
Слайд 24
Готовимся к ЕРЭ Какие функции выполняют углеводы в организме животных? 1 ) каталитическую 2) структурную 3) запасающую 4) гормональную 5) сократительную 6) Энергетическую Ответ: 236
Изображение слайда
25
Слайд 25
Готовимся к ЕРЭ Моносахариды в клетке выполняют функции: 1 ) энергетическую 2) составных компонентов полимеров 3) информационную 4) составных компонентов нуклеиновых кислот 5) защитную 6) транспортную Ответ: 124
Изображение слайда
26
Слайд 26
Готовимся к ЕРЭ
Все перечисленные ниже признаки, кроме двух, можно использовать для описания крахмала. Определите два признака, «выпадающих» из общего списка, и запишите в таблицу цифры, под которыми они указаны.
1 ) представляет собой полимер альфа-глюкозы
2) содержится в амилопластах в форме зерен
3) образуется в митохондриях клеток растений
4) представляет собой смесь амилозы и амилопектина
5) накапливается в клетках печени и мышц
Ответ: 35
Определите два признака, «выпадающих» из общего списка, и запишите в таблицу цифры, под которыми они указаны.
1 ) представляет собой полимер альфа-глюкозы
2) содержится в амилопластах в форме зерен
3) образуется в митохондриях клеток растений
4) представляет собой смесь амилозы и амилопектина
5) накапливается в клетках печени и мышц
Ответ: 35
Изображение слайда
27
Слайд 27
Готовимся к ЕРЭ Установите соответствие между особенностями молекул углеводов и их видами: ОСОБЕННОСТИ А ) мономер Б) полимер В) растворимы в воде Г) не растворимы в воде Д) входят в состав клеточных стенок растений Е) входят в состав клеточного сока растений ВИДЫ 1 ) целлюлоза 2 ) глюкоза Ответ: 212112
Изображение слайда
28
Слайд 28
Готовимся к ЕРЭ
Установите соответствие между строением и функцией вещества и его видом. СТРОЕНИЕ И ФУНКЦИЯ
А) молекула сильно разветвлена
Б) имеет четвертичную структуру
В) откладывается в запас в печени
Г) мономерами являются аминокислоты
Д) используется для поддержания уровня кислорода
ВИД ВЕЩЕСТВА 1 ) гемоглобин 2 ) гликоген
Ответ: 21211
СТРОЕНИЕ И ФУНКЦИЯ
А) молекула сильно разветвлена
Б) имеет четвертичную структуру
В) откладывается в запас в печени
Г) мономерами являются аминокислоты
Д) используется для поддержания уровня кислорода
ВИД ВЕЩЕСТВА 1 ) гемоглобин 2 ) гликоген
Ответ: 21211
Изображение слайда
29
Последний слайд презентации: Углеводы
Готовимся к ЕРЭ Найдите три ошибки в приведённом тексте. Укажите номера предложений, в которых они сделаны, исправьте их. 1. Полисахарид целлюлоза выполняет в клетке растения резервную, запасающую функцию. 2. Накапливаясь в клетке, углеводы выполняют главным образом регуляторную функцию. 3. У членистоногих полисахарид хитин формирует покровы тела. 4. У растений клеточные стенки образованы полисахаридом крахмалом. 5. Полисахариды обладают гидрофобностью.
Изображение слайда
Углеводы клеточной поверхности при распознавании и ответе клеток
Обзор
. 1986 г., июль; 40 (1): 97–111.
1986 г., июль; 40 (1): 97–111.
doi: 10.1002/jlb.40.1.97.
Б. К. Брэндли, Р. Л. Шнаар
- PMID: 3011937
- DOI: 10.1002/jlb.40.1.97
Обзор
B K Brandley et al. Дж. Лейкок Биол. 1986 июль
. 1986 г., июль; 40 (1): 97–111.
doi: 10.1002/jlb.40.1.97.
Авторы
Б. К. Брэндли, Р. Л. Шнаар
- PMID: 3011937
- DOI:
10.
 1002/jlb.40.1.97
1002/jlb.40.1.97
Абстрактный
Сложные углеводы покрывают поверхности клеток и могут нести информацию, необходимую для межклеточного распознавания. Сахароспецифические рецепторы (лектины) также присутствуют в клетках и могут взаимодействовать с сахарами на соседних клетках. Это может привести к слипанию двух клеток через углеводы и специфические рецепторы клеточной поверхности. Такая направленная на углеводы клеточная адгезия, по-видимому, важна для многих межклеточных активностей, включая инфекцию бактериями и вирусами, связь между клетками низших эукариот, специфическое связывание сперматозоида с яйцеклеткой; и рециркуляция лимфоцитов, среди прочего. Новые подходы, включающие синтез химически определенных аналогов клеточной поверхности в сочетании с экспериментами по ингибированию, начинают раскрывать механику потенциального углеводного «языка», участвующего в межклеточных взаимодействиях.
Похожие статьи
Углеводы клеточной поверхности и распознавание клеток у Dictyostelium.
Боззаро С. Боццаро С. Ячейка отличается. 1985 авг.; 17(2):67-82. doi: 10.1016/0045-6039(85)90473-7. Ячейка отличается. 1985. PMID: 2412705
Углеводы и распознавание рецепторов.
Габриэль О. Габриэль О. Гориз Биохим Биофиз. 1982; 6:137-56. Гориз Биохим Биофиз. 1982. PMID: 6311714 Обзор. Аннотация недоступна.
Распознавание сперматозоидов и барьеры для межвидового оплодотворения.
О’Рэнд М.Г. О’Рэнд М.Г. Гамет Рез. 1988 апр; 19(4):315-28.
 doi: 10.1002/mrd.1120190402.
Гамет Рез. 1988 год.
PMID: 3058566
Обзор.
Аннотация недоступна.
doi: 10.1002/mrd.1120190402.
Гамет Рез. 1988 год.
PMID: 3058566
Обзор.
Аннотация недоступна.Опосредованное углеводами взаимодействие сперматозоида и яйцеклетки и видовая специфичность: ключ к пониманию модели Unio elongatulus.
Фокарелли Р., Ла Сала ГБ, Балазини М., Розати Ф. Фокарелли Р. и соавт. Клетки Ткани Органы. 2001;168(1-2):76-81. дои: 10.1159/000016808. Клетки Ткани Органы. 2001. PMID: 11114589 Обзор.
Механизмы межклеточной адгезии.
Грейг Р.Г., Джонс М.Н. Грейг Р.Г. и соавт. Биосистемы. 1977 г., июнь; 9 (1): 43–55. doi: 10.1016/0303-2647(77)
- -4. Биосистемы. 1977. PMID: 332245 Обзор.
Посмотреть все похожие статьи
Цитируется
Растительные лектины как мощные антикоронавирусные, противовоспалительные, антиноцицептивные и противоязвенные средства.

Конози Э., Осман М., Дирар А. Конози Э. и др. Саудовская J Biol Sci. 2022 июнь;29(6):103301. doi: 10.1016/j.sjbs.2022.103301. Epub 2022 22 апр. Саудовская J Biol Sci. 2022. PMID: 35475119 Бесплатная статья ЧВК. Обзор.
Фотосенсибилизированный синглетный кислород ( 1 O 2 ) Набор инструментов для биоорганических приложений: Tailoring 1 O 2 Генерация для мечения ДНК и белков, нацеливания и биосенсорного анализа.
Эрсенс Д., Кадони Э., Тэк Л., Мэддер А. Эрсенс Д. и соавт. Молекулы. 2022 25 января; 27 (3): 778. doi: 10,3390/молекулы27030778. Молекулы. 2022. PMID: 35164045 Бесплатная статья ЧВК. Обзор.
Две приятные стороны янус-лектина способствуют перекрестному связыванию липосом с раковыми клетками и поглощению материала.

Сюкштайте Л., Розато Ф., Митрович А., Мюллер П.Ф., Краус К., Нотова С., Имберти А., Ремер В. Siukstaite L, et al. Токсины (Базель). 2021 ноябрь 9;13(11):792. doi: 10.3390/toxins13110792. Токсины (Базель). 2021. PMID: 34822576 Бесплатная статья ЧВК.
Измененная экспрессия гликанов в клетках рака молочной железы способствует инфицированию онколитическим реовирусом сероптипа Т3.
Мохаммед Д., Келер М., Думитру А.С., Аравамудхан П., Сазерленд Д.М., Дермоди Т.С., Алстинс Д. Мохаммед Д. и др. Нано Летт. 2021 24 ноября; 21 (22): 9720-9728. doi: 10.1021/acs.nanolett.1c03608. Epub 2021 11 ноября. Нано Летт. 2021. PMID: 34762801
Что такое Сахарный код?
Габиус Х.Дж., Кудик М., Диркс Т.
 , Кальтнер Х., Копиц Дж., Майо К.Х., Мерфи П.В., Оскарсон С., Рой Р., Шедлбауэр А., Тогель С., Ромеро А.
Габиус Х.Дж. и др.
Химбиохим. 2022 5 июля; 23 (13): e202100327. doi: 10.1002/cbic.202100327. Epub 2021 22 сентября.
Химбиохим. 2022.
PMID: 34496130
Обзор.
, Кальтнер Х., Копиц Дж., Майо К.Х., Мерфи П.В., Оскарсон С., Рой Р., Шедлбауэр А., Тогель С., Ромеро А.
Габиус Х.Дж. и др.
Химбиохим. 2022 5 июля; 23 (13): e202100327. doi: 10.1002/cbic.202100327. Epub 2021 22 сентября.
Химбиохим. 2022.
PMID: 34496130
Обзор.
Просмотреть все статьи «Цитируется по»
Типы публикаций
термины MeSH
вещества
Грантовая поддержка
- CA 08012/CA/NCI NIH HHS/США
- HD 14010/HD/NICHD NIH HHS/США
- HD 20527/HD/NICHD NIH HHS/США
Структура и функция сложных углеводов — компьютерное моделирование
Сложные углеводы очень распространены в животных, растениях и бактериях. Они входят в состав клеточных мембран, а также субклеточного материала клеток. Они также обнаруживаются в физиологических жидкостях, таких как кровь, слезы, молоко и моча. Недавно было подсчитано, что были определены ковалентные структуры от 4000 до 6000 природных углеводов (DOE, 19).87). Многие сложные углеводы незамещены по восстанавливающим концам и называются полисахаридами; примеры включают олигосахариды молока, целлюлозу клеточных стенок растений и запасные формы, такие как крахмал и гликоген. Многие другие встречающиеся в природе сложные углеводы ковалентно связаны с другими молекулами, такими как белки или липиды, гликозидными связями остатков сахара на их восстанавливающих концах с образованием гликоконъюгатов.
Они входят в состав клеточных мембран, а также субклеточного материала клеток. Они также обнаруживаются в физиологических жидкостях, таких как кровь, слезы, молоко и моча. Недавно было подсчитано, что были определены ковалентные структуры от 4000 до 6000 природных углеводов (DOE, 19).87). Многие сложные углеводы незамещены по восстанавливающим концам и называются полисахаридами; примеры включают олигосахариды молока, целлюлозу клеточных стенок растений и запасные формы, такие как крахмал и гликоген. Многие другие встречающиеся в природе сложные углеводы ковалентно связаны с другими молекулами, такими как белки или липиды, гликозидными связями остатков сахара на их восстанавливающих концах с образованием гликоконъюгатов.
БИОЛОГИЧЕСКАЯ ФУНКЦИЯ
Гликопротеины выполняют множество функций в высших организмах. Коллаген является важным структурным элементом внеклеточного пространства, хрящей, костей и базальных мембран. Муцины играют важную роль в качестве смазывающих и защитных агентов в слизистых выделениях.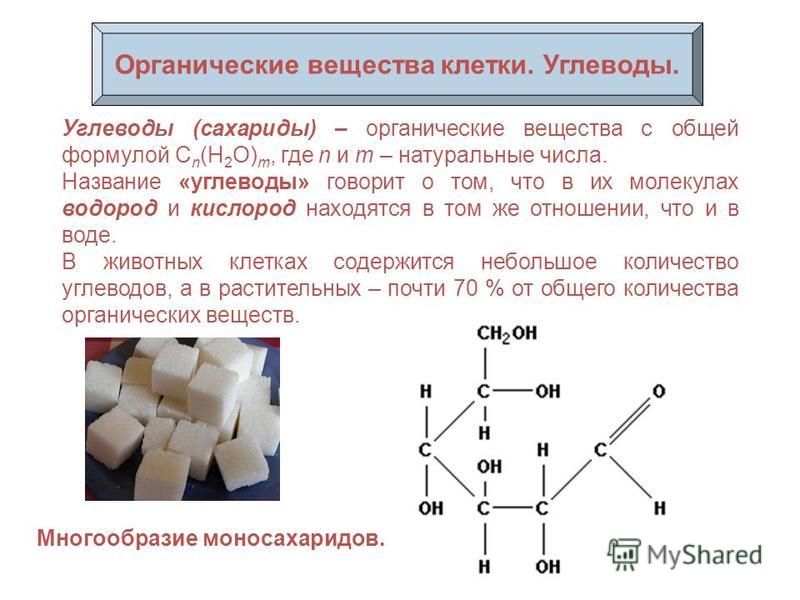 Важные иммунологические молекулы класса гликопротеинов включают иммуноглобулины, антигены гистосовместимости, антигены групп крови типов АВО и Льюиса, комплемент в механизме свертывания крови и интерферон. Многие белки плазмы человека, такие как фетуин, трансферрин и церулоплазмин, являются гликопротеинами, как и некоторые гормоны, такие как хорионический гонадотропин и тиротропин. Большинство животных и растительных лектинов представляют собой гликопротеины, как и лизосомальные ферменты. Распознавание и связывание лизосомальных ферментов со специфическими рецепторами в аппарате Гольджи и на клеточной поверхности включает один или несколько фосфорилированных остатков маннозы на N-связанных олигосахаридных цепях. Сайты узнавания на клеточной поверхности для связывания и поглощения гормонов и для взаимодействия с другими клетками, вирусами и бактериями также являются гликопротеинами.
Важные иммунологические молекулы класса гликопротеинов включают иммуноглобулины, антигены гистосовместимости, антигены групп крови типов АВО и Льюиса, комплемент в механизме свертывания крови и интерферон. Многие белки плазмы человека, такие как фетуин, трансферрин и церулоплазмин, являются гликопротеинами, как и некоторые гормоны, такие как хорионический гонадотропин и тиротропин. Большинство животных и растительных лектинов представляют собой гликопротеины, как и лизосомальные ферменты. Распознавание и связывание лизосомальных ферментов со специфическими рецепторами в аппарате Гольджи и на клеточной поверхности включает один или несколько фосфорилированных остатков маннозы на N-связанных олигосахаридных цепях. Сайты узнавания на клеточной поверхности для связывания и поглощения гормонов и для взаимодействия с другими клетками, вирусами и бактериями также являются гликопротеинами.
Многие функции гликопротеинов на клеточной поверхности также были предложены для нейтральных и кислых гликосфинголипидов. Кроме того, недавно было обнаружено, что некоторые гликосфинголипиды класса ганглиозидов ингибируют митогенный ответ факторов клеточного роста посредством аллостерической модуляции их рецепторов клеточной поверхности (Bremer et al., 1986). Онкогенная трансформация вирусной инфекцией или химическими мутагенами обычно приводит к изменениям структуры гликосфинголипидов на клеточной поверхности, так что количество некоторых типов значительно увеличивается. В некоторых случаях имеются и качественные различия из-за экспрессии генов, молчащих в дифференцированных нормальных клетках. Это особенно важно для опухолевых клеток, где опухолеассоциированные антигены могут служить основой для специфических диагностических анализов на основе моноклональных антител и, в конечном итоге, возможно, для лечения.
Кроме того, недавно было обнаружено, что некоторые гликосфинголипиды класса ганглиозидов ингибируют митогенный ответ факторов клеточного роста посредством аллостерической модуляции их рецепторов клеточной поверхности (Bremer et al., 1986). Онкогенная трансформация вирусной инфекцией или химическими мутагенами обычно приводит к изменениям структуры гликосфинголипидов на клеточной поверхности, так что количество некоторых типов значительно увеличивается. В некоторых случаях имеются и качественные различия из-за экспрессии генов, молчащих в дифференцированных нормальных клетках. Это особенно важно для опухолевых клеток, где опухолеассоциированные антигены могут служить основой для специфических диагностических анализов на основе моноклональных антител и, в конечном итоге, возможно, для лечения.
Связывание между гликозаминогликанами и другими внеклеточными макромолекулами вносит значительный вклад в структурную организацию матрикса соединительной ткани. Все гликозаминогликаны, за исключением тех, в которых отсутствуют сульфатные или карбоксильные группы, электростатически связываются с коллагеном при нейтральном pH из-за их замечательного анионного характера. Дерматансульфат, который, по-видимому, является основным гликозаминогликаном, синтезируемым клетками гладких мышц артерий, сильно связывается с липопротеинами плазмы, а гепарин также взаимодействует с некоторыми белками плазмы, включая факторы свертывания IX и XI и антитромбин III. Интересно, что стехиометрическое связывание гепарина 1:1 с остатками Lys антитромбина III, как полагают, вызывает конформационное изменение антитромбина III, которое увеличивает связывание антитромбина III с тромбином. Это связывание инактивирует тромбин. Гиалуроновая кислота осаждается на поверхности чашек Петри клетками, растущими в культуре тканей, давая им субстрат для прикрепления в процессе роста. Протеогликаны также участвуют в регуляции клеточного роста, возможно, посредством ядерных эффектов на структуру хроматина и активации ДНК-полимеразы, и могут опосредовать межклеточную коммуникацию и потерю рецепторов клеточной поверхности.
Дерматансульфат, который, по-видимому, является основным гликозаминогликаном, синтезируемым клетками гладких мышц артерий, сильно связывается с липопротеинами плазмы, а гепарин также взаимодействует с некоторыми белками плазмы, включая факторы свертывания IX и XI и антитромбин III. Интересно, что стехиометрическое связывание гепарина 1:1 с остатками Lys антитромбина III, как полагают, вызывает конформационное изменение антитромбина III, которое увеличивает связывание антитромбина III с тромбином. Это связывание инактивирует тромбин. Гиалуроновая кислота осаждается на поверхности чашек Петри клетками, растущими в культуре тканей, давая им субстрат для прикрепления в процессе роста. Протеогликаны также участвуют в регуляции клеточного роста, возможно, посредством ядерных эффектов на структуру хроматина и активации ДНК-полимеразы, и могут опосредовать межклеточную коммуникацию и потерю рецепторов клеточной поверхности.
БИОСИНТЕЗ N-СВЯЗАННЫХ ГЛИКОПРОТЕИНОВ И ГЛИКОФИНГОЛИПИДОВ
Роль углеводов в биологических функциях представляет особенно сложную проблему для будущего. Синтез этих гликоконъюгатов происходит во время их внутриклеточного транспорта от места начальной сборки липид-связанного интермедиата (гликопротеины) или церамида (гликосфинголипиды) в эндоплазматическом ретикулуме через аппарат Гольджи на клеточную поверхность, внутриклеточные органеллы или внеклеточные пространство. Для их синтеза требуется семейство активированных доноров сахара, называемых сахарными нуклеотидами, которые синтезируются в цитозольной фракции клеток из сахарофосфатов и нуклеозидтрифосфатов. Интересным исключением является сахарный нуклеотид сиаловой кислоты, называемый цитидинмонофосфат сиаловой кислоты (CMP-NeuAc), который синтезируется в ядре из свободной сиаловой кислоты и CTP. Ферменты, участвующие в биосинтезе гликоконъюгатов, представляют собой гликозилтрансферазы, которые катализируют перенос остатков сахаров от нуклеотидов сахара к невосстанавливающему концу растущей углеводной цепи.
Синтез этих гликоконъюгатов происходит во время их внутриклеточного транспорта от места начальной сборки липид-связанного интермедиата (гликопротеины) или церамида (гликосфинголипиды) в эндоплазматическом ретикулуме через аппарат Гольджи на клеточную поверхность, внутриклеточные органеллы или внеклеточные пространство. Для их синтеза требуется семейство активированных доноров сахара, называемых сахарными нуклеотидами, которые синтезируются в цитозольной фракции клеток из сахарофосфатов и нуклеозидтрифосфатов. Интересным исключением является сахарный нуклеотид сиаловой кислоты, называемый цитидинмонофосфат сиаловой кислоты (CMP-NeuAc), который синтезируется в ядре из свободной сиаловой кислоты и CTP. Ферменты, участвующие в биосинтезе гликоконъюгатов, представляют собой гликозилтрансферазы, которые катализируют перенос остатков сахаров от нуклеотидов сахара к невосстанавливающему концу растущей углеводной цепи.
Различие между биосинтезом гликоконъюгатов и синтезом белка является ключевым; последний происходит на матрице матричной РНК и поэтому определяется генетическим кодом одного структурного гена. 1 В противоположность этому, синтез гликоконъюгатов осуществляется поэтапным добавлением единиц сахара с использованием разных ферментов на каждом этапе. Следовательно, ни одна последовательность ДНК не участвует в определении первичной структуры сложного углевода, поскольку порядок добавления сахаров зависит от специфичности субстрата и кинетических характеристик различных гликозилтрансфераз, каждая из которых кодируется отдельным структурным геном. . Ясно, что невозможно предсказать первичную структуру сложных углеводов по последовательностям ДНК. Следовательно, трехмерные структуры гликопротеинов, гликосфинголипидов и других сложных молекул, содержащих углеводы, невозможно полностью предсказать без экспериментального структурного анализа углеводов.
1 В противоположность этому, синтез гликоконъюгатов осуществляется поэтапным добавлением единиц сахара с использованием разных ферментов на каждом этапе. Следовательно, ни одна последовательность ДНК не участвует в определении первичной структуры сложного углевода, поскольку порядок добавления сахаров зависит от специфичности субстрата и кинетических характеристик различных гликозилтрансфераз, каждая из которых кодируется отдельным структурным геном. . Ясно, что невозможно предсказать первичную структуру сложных углеводов по последовательностям ДНК. Следовательно, трехмерные структуры гликопротеинов, гликосфинголипидов и других сложных молекул, содержащих углеводы, невозможно полностью предсказать без экспериментального структурного анализа углеводов.
Snider (1984) сообщил, что гликопротеины N-связанного типа синтезируются как котрансляционное событие в шероховатой эндоплазматической сети. В то время как полипептидная цепь транслируется на матричной РНК и одновременно проходит через мембрану эндоплазматического ретикулума в цистернальное пространство (просвет), одиночный олигосахарид координированно синтезируется на фосфорилированном полиизопреноидном спирте (долихоле у высших животных и более мелких подобных веществах у насекомых). , дрожжи и растения). Весь олигосахарид-предшественник затем переносится на соответствующие остатки аспарагина в формирующейся полипептидной цепи (вероятно, перед укладкой в третичную структуру) в соответствии с правилами специфичности, которые до конца не поняты. Для переноса требуется последовательность Asn-X-Ser или Asn-X-Thr, но также задействованы дополнительные факторы. Доступность остатка Asn может быть одним из таких факторов, и оценка этой возможности может быть сделана с помощью методов прогнозирования, описанных в этом отчете.
, дрожжи и растения). Весь олигосахарид-предшественник затем переносится на соответствующие остатки аспарагина в формирующейся полипептидной цепи (вероятно, перед укладкой в третичную структуру) в соответствии с правилами специфичности, которые до конца не поняты. Для переноса требуется последовательность Asn-X-Ser или Asn-X-Thr, но также задействованы дополнительные факторы. Доступность остатка Asn может быть одним из таких факторов, и оценка этой возможности может быть сделана с помощью методов прогнозирования, описанных в этом отчете.
Вторая стадия синтеза N-связанного гликопротеина включает обширную посттрансляционную модификацию связанного с белком олигосахарида-предшественника путем удаления и добавления сахаров. Во многих случаях белковая часть также модифицируется частичным протеолитическим расщеплением и/или добавлением модифицирующих функцию групп к определенным аминокислотным остаткам. Посттрансляционная модификация инициируется в шероховатой эндоплазматической сети удалением трех остатков глюкозы двумя специфическими мембраносвязанными глюкозидазами. Эти остатки глюкозы, по-видимому, имеют единственную функцию обеспечения переноса олигосахаридной цепи от долихолпирофосфата к зарождающимся полипептидным цепям. Будет интересно определить по трехмерным структурам и предсказанным конформациям, как эти группы взаимодействуют с ферментом трансферазой, задействованным на этом этапе. Цепи зрелых олигосахаридов с высоким содержанием маннозы синтезируют путем последующего удаления до четырех остатков маннозила из трех ветвей структуры предшественника. В этом процессе участвуют по крайней мере три различных альфа-маннозидазы в аппарате Гольджи. Эти ферменты и две глюкозидазы являются гидролазами, как и лизосомальные гликозидазы, но их активность максимальна при нейтральном рН, в отличие от лизосомальных ферментов, которые проявляют наибольшую каталитическую активность при кислом рН.
Эти остатки глюкозы, по-видимому, имеют единственную функцию обеспечения переноса олигосахаридной цепи от долихолпирофосфата к зарождающимся полипептидным цепям. Будет интересно определить по трехмерным структурам и предсказанным конформациям, как эти группы взаимодействуют с ферментом трансферазой, задействованным на этом этапе. Цепи зрелых олигосахаридов с высоким содержанием маннозы синтезируют путем последующего удаления до четырех остатков маннозила из трех ветвей структуры предшественника. В этом процессе участвуют по крайней мере три различных альфа-маннозидазы в аппарате Гольджи. Эти ферменты и две глюкозидазы являются гидролазами, как и лизосомальные гликозидазы, но их активность максимальна при нейтральном рН, в отличие от лизосомальных ферментов, которые проявляют наибольшую каталитическую активность при кислом рН.
В эукариотических клетках олигосахарид с высоким содержанием маннозы с пятью единицами маннозы (см. ) является прямым предшественником сложных и гибридных структур. Начальным этапом в аппарате Гольджи является добавление остатка N-ацетилглюкозамина к последнему оставшемуся человеку на ветви I (*), после чего оставшиеся два остатка человека на ветвях II и III могут быть удалены альфа-маннозидазами, которые почти определенно отличается от тех, кто участвовал в предыдущих шагах. На этом этапе могут быть сделаны дополнительные разветвления для получения три- и тетраантеннальных структур, а заключительные стадии процессинга осуществляются путем добавления остатков галактозы, N-ацетилглюкозамина, сиаловой кислоты и фукозы для получения зрелых, сложных, N-связанных цепи. Интересная N-ацетилглюкозаминилтрансфераза может добавлять бета-1,4-связанный остаток GlcNAc к разветвленному бета-связанному остатку маннозы внутренней области ядра (0), чтобы получить «разделенную пополам структуру». Этот этап был предметом интенсивного изучения Карвером и его коллегами, которые интересовались структурной специфичностью фермента с различными конформациями предшественников олигосахаридов (Карвер и Бриссон, 19).
Начальным этапом в аппарате Гольджи является добавление остатка N-ацетилглюкозамина к последнему оставшемуся человеку на ветви I (*), после чего оставшиеся два остатка человека на ветвях II и III могут быть удалены альфа-маннозидазами, которые почти определенно отличается от тех, кто участвовал в предыдущих шагах. На этом этапе могут быть сделаны дополнительные разветвления для получения три- и тетраантеннальных структур, а заключительные стадии процессинга осуществляются путем добавления остатков галактозы, N-ацетилглюкозамина, сиаловой кислоты и фукозы для получения зрелых, сложных, N-связанных цепи. Интересная N-ацетилглюкозаминилтрансфераза может добавлять бета-1,4-связанный остаток GlcNAc к разветвленному бета-связанному остатку маннозы внутренней области ядра (0), чтобы получить «разделенную пополам структуру». Этот этап был предметом интенсивного изучения Карвером и его коллегами, которые интересовались структурной специфичностью фермента с различными конформациями предшественников олигосахаридов (Карвер и Бриссон, 19).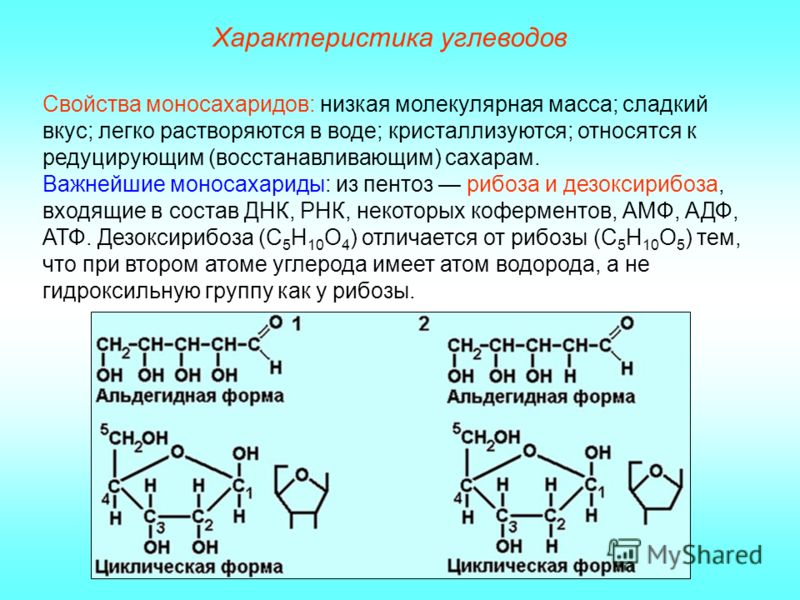 84).
84).
РИСУНОК 8-1
Промежуточный продукт, частично процессированный аспарагином — связанная углеводная цепь гликопротеина.
Вполне вероятно, что в исследованиях путей процессинга и степени процессинга цепей олигосахаридов будут использоваться методы прогнозирования. Если контроль возникает из-за специфичности фермента в отношении конкретной трехмерной структуры субстрата, может оказаться возможным определить эти предпочтения и, исходя из предсказаний распределения трехмерных структур олигосахарида, присоединенного к гликопротеиновому субстрату, предсказать, насколько далеко углеводная цепь будет обработана.
Лизосомальные ферменты содержат одну или несколько фосфатных групп на маннозных остатках олигосахаридных цепей с высоким содержанием маннозы. Маннозо-6-фосфатные группы являются специфическими маркерами распознавания, которые участвуют в транспорте лизосомальных ферментов из аппарата Гольджи или из клеток в лизосомы. В плазматической мембране были обнаружены два мембраносвязанных маннозо-6-фосфатных рецептора; по крайней мере, один из них также находится в мембранах Гольджи. Хотя специфичность их связывания исследована довольно подробно, другие аспекты не определены: природа взаимодействия фосфорилированных остатков маннозы с рецепторами и трехмерные структуры лизосомальных фермент-рецепторных комплексов.
Хотя специфичность их связывания исследована довольно подробно, другие аспекты не определены: природа взаимодействия фосфорилированных остатков маннозы с рецепторами и трехмерные структуры лизосомальных фермент-рецепторных комплексов.
Другой интересный аспект синтеза лизосомальных ферментов включает определение структурных доменов на свернутых белках, распознаваемых ферментом, который инициирует фосфорилирование остатков маннозы, который представляет собой N-ацетилглюкозамин-фосфотрансферазу (GlcNAc-P трансферазу) в аппарате Гольджи. Это механизм, с помощью которого для фосфорилирования отбираются только белки лизосомальных ферментов. Это особенно важно, поскольку одна из форм генетического лизосомного нарушения накопления, называемая муколипидозом II, возникает в результате дефекта связывающего домена GlcNAc-P трансферазы для лизосомальных ферментных белков. Возможно, эту проблему можно решить только с помощью компьютерного моделирования, позволяющего предсказать трехмерные структуры обоих белков.
Гликосфинголипиды синтезируются аналогичным образом, за исключением того, что церамид выполняет функцию долихола для гликопротеинов, а перенос происходит непосредственно от сахарного нуклеотида к акцепторному гликолипиду. Церамид является акцептором либо глюкозы (из UDP-Glc), либо галактозы (из UDP-Gal), образуя глюкозилцерамид или галактозилцерамид. Эти простые гликосфинголипиды преобладают в плазме и головном мозге человека соответственно, а также служат предшественниками более сложных гликосфинголипидов. В большинстве органов, включая головной мозг, основные пути включают превращение глюкозилцерамида в лактозилцерамид, Gal-бета-1,4-Glc-Cer. Лактозилцерамид является субстратом ряда гликозилтрансфераз, продукты которых являются первыми интермедиатами в синтезе родственных гликосфинголипидов, которые можно классифицировать по их общим структурным характеристикам. Уже охарактеризовано более 100 различных гликосфинголипидов, и все еще открываются новые соединения. Хотя некоторые из гликосфинголипидов могут содержать от 15 до 35 или более остатков сахара, большинство широко встречающихся типов имеют от 4 до 10 остатков в олигосахаридной цепи.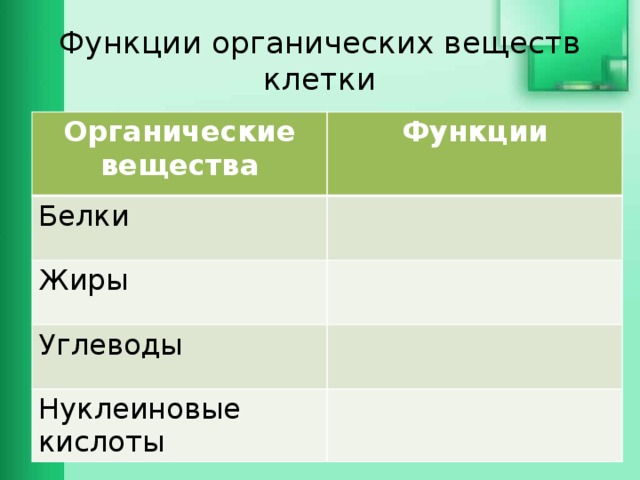
АНАЛИЗ ПЕРВИЧНОЙ И ТРЕТИЧНОЙ СТРУКТУРЫ
Полное понимание взаимодействий между углеводами и белками (ферментами, лектинами, антителами и рецепторами клеточной поверхности) будет зависеть от определения точных трехмерных структур обоих типов молекул. Как было отмечено, первичные структуры олигосахаридных цепей сложных углеводов не могут быть выведены из последовательностей ДНК и поэтому должны быть определены химическим и спектроскопическим анализом. Современные хроматографические методы разделения, наряду с масс-спектрометрией и ядерным магнитным резонансом (ЯМР), позволяют проводить полный анализ первичной структуры на образце в один микромоль. Еще предстоит определить состав; размещение остатков сахара; размер кольца; положения гликозидных связей и их аномерность; и расположение и химическая природа неуглеводных заместителей, таких как липиды, сульфатные и фосфатные группы.
Трехмерные структуры углеводов представляют пространственное расположение отдельных остатков сахара. Наиболее часто встречающиеся сложные углеводы млекопитающих состоят из остатков сахаров, которые существуют в форме пиранозного кольца, наиболее стабильной и жесткой конформацией которого являются формы стула. Когда два остатка сахара ковалентно соединены гликозидной связью, они могут свободно вращаться вокруг гликозидного атома кислорода между двумя кольцами, и поэтому полученный дисахарид может принимать ряд различных конформаций, соответствующих вращениям вокруг этих двух связей. Двугранные углы при гликозидной связи (см. ) принято обозначать греческими символами phi (ϕ) и psi (ψ), где исходной конформацией (ϕ = 0°, ψ = 0°) является тот конформер, в котором C-l Связь -H-1 затмевает O-C’-X’, а связь C-1-O затмевает C’-X’-H-X’.
Наиболее часто встречающиеся сложные углеводы млекопитающих состоят из остатков сахаров, которые существуют в форме пиранозного кольца, наиболее стабильной и жесткой конформацией которого являются формы стула. Когда два остатка сахара ковалентно соединены гликозидной связью, они могут свободно вращаться вокруг гликозидного атома кислорода между двумя кольцами, и поэтому полученный дисахарид может принимать ряд различных конформаций, соответствующих вращениям вокруг этих двух связей. Двугранные углы при гликозидной связи (см. ) принято обозначать греческими символами phi (ϕ) и psi (ψ), где исходной конформацией (ϕ = 0°, ψ = 0°) является тот конформер, в котором C-l Связь -H-1 затмевает O-C’-X’, а связь C-1-O затмевает C’-X’-H-X’.
РИСУНОК 8-2
Двугранные углы, определяющие пространственное соотношение двух остатков сахара в дисахариде.
Относительная ориентация соседних сахарных остатков в олигосахаридной цепи описывается указанием углов вращения (ϕ, ψ) у каждого гликозидного атома кислорода. Когда эти углы одинаковы для каждой связи, цепь имеет спиральную конформацию с n остатками на виток и h единицами перемещения вдоль оси спирали. Если n и h доступны из рентгеновских данных, то можно вычислить ϕ и ψ и наоборот. Если ϕ и ψ различны среди гликозидных связей в олигосахаридной цепи, трехмерная структура становится непериодической и, при крайних вариациях, принимает конформацию случайного клубка. Информация о возмущениях может быть получена с помощью измерений светорассеяния, вязкости, седиментации и диффузии.
Когда эти углы одинаковы для каждой связи, цепь имеет спиральную конформацию с n остатками на виток и h единицами перемещения вдоль оси спирали. Если n и h доступны из рентгеновских данных, то можно вычислить ϕ и ψ и наоборот. Если ϕ и ψ различны среди гликозидных связей в олигосахаридной цепи, трехмерная структура становится непериодической и, при крайних вариациях, принимает конформацию случайного клубка. Информация о возмущениях может быть получена с помощью измерений светорассеяния, вязкости, седиментации и диффузии.
РЕНТГЕНОВСКИЙ АНАЛИЗ КРИСТАЛЛИЧЕСКИХ СТРУКТУР УГЛЕВОДОВ
Из трех основных классов сложных биологических молекул у нас есть наименьшая структурная информация об углеводах с атомным разрешением. Это связано с тем, что они не были кристаллизованы, и, следовательно, нет соответствующей базы данных о кристаллической структуре, кроме базы данных от простых мономеров до тримеров, на основе которой можно было бы моделировать классические или полуэмпирические квантово-механические расчеты. Типичными примерами являются олигосахариды, специфичные для группы крови, кордовые факторы и липиды A и X. Исключением являются циклодекстрины, которые хорошо кристаллизуются, но конформационно относятся к отдельному классу. Структуры, полученные из структуры волокон полисахаридов, зависят от модели и не являются источником окончательных структурных данных. Стахиоза, олигосахарид, состоящий из четырех сахарных остатков, является крупнейшим нециклическим олигосахаридом, для которого проводится анализ кристаллической структуры, но даже в этом случае связанная с ним структура воды не определена.
Типичными примерами являются олигосахариды, специфичные для группы крови, кордовые факторы и липиды A и X. Исключением являются циклодекстрины, которые хорошо кристаллизуются, но конформационно относятся к отдельному классу. Структуры, полученные из структуры волокон полисахаридов, зависят от модели и не являются источником окончательных структурных данных. Стахиоза, олигосахарид, состоящий из четырех сахарных остатков, является крупнейшим нециклическим олигосахаридом, для которого проводится анализ кристаллической структуры, но даже в этом случае связанная с ним структура воды не определена.
Проблема кристалличности присуща только частично. Углеводы сольватируются иначе, чем белки, олигонуклеотиды или нуклеиновые кислоты. Однако было предпринято меньше усилий для получения значительных количеств конфигурационно-однородного материала , необходимого для проведения экспериментов по кристаллизации, чем для белков и нуклеиновых кислот. Другим аспектом кристаллографии гликоконъюгатов является то, что электронная плотность для олигосахаридной части гликопротеинов редко интерпретируется, даже несмотря на то, что было изучено несколько кристаллических гликопротеинов. Это связано с тем, что стандартные программы уточнения не могут работать с олигосахаридами или в месте гликозилирования присутствует микрогетерогенность, поэтому он не учитывается в модели. Таким образом, потенциально ценный источник информации не используется из-за отсутствия надлежащей разработки программ или стратегических подходов к решению проблемы микрогетерогенности.
Это связано с тем, что стандартные программы уточнения не могут работать с олигосахаридами или в месте гликозилирования присутствует микрогетерогенность, поэтому он не учитывается в модели. Таким образом, потенциально ценный источник информации не используется из-за отсутствия надлежащей разработки программ или стратегических подходов к решению проблемы микрогетерогенности.
Стерические соображения о минимальных расстояниях сближения между атомами, полученные из наблюдаемых несвязанных расстояний в различных кристаллических структурах, могут быть использованы для предсказания допустимых конформаций. Этот подход «твердой сферы», первоначально разработанный В.С.Р. Рао в середине 1970-х годов, представляет собой рудиментарный метод теоретических расчетов, который игнорирует электростатические эффекты (водородные связи), но дает качественное предсказание структуры. Впоследствии этот подход был расширен за счет адаптации расчетов энергии, первоначально использовавшихся для пептидов, где потенциальная энергия делится на функции, описывающие дискретные вклады, такие как энергии Ван-дер-Ваальса, электростатические взаимодействия, энергия кручения, энергия водородных связей, деформации связей и углов (Бок , 1983). Данные представлены в виде компьютерных карт энергетических контуров.
Данные представлены в виде компьютерных карт энергетических контуров.
В большей части недавней литературы расчеты конформационной энергии проводились с использованием формы параметров Рао с добавленным торсионным потенциалом относительно одной из гликозидных связей (экзоаномерный эффект). Этот подход, получивший название HSEA (экзоаномерный метод твердых сфер) (Bock, 1983), с успехом использовался Лемье и Боком (1983), Карвером и Бриссоном (1984) и другими, хотя он содержит ряд непроверенных предположений. Добавление потенциала водородной связи (метод HEAH) дает результаты минимизации энергии, которые отличаются от результатов, рассчитанных методом HSEA, из которых можно получить геометрию, отличающуюся от геометрии, полученной методом HSEA.
ЯМР-СТРУКТУРА РАСТВОРОВ УГЛЕВОДОВ
Методы протонного ЯМР предоставляют подробные экспериментальные данные, на основании которых можно определить трехмерные структуры и сравнить их с конформациями, полученными расчетами потенциальной энергии. Карвер и Камминг (1987) создали контурные карты рассчитанных NOE различных олигосахаридов с высоким содержанием маннозы в зависимости от торсионных углов φ и ψ. Затем они связали их с экспериментальными результатами, а также с конформациями минимальной энергии, оцененными с помощью различных расчетов потенциальной энергии (Карвер и Камминг, в печати). Бриссон и Карвер (1983) оценил полезность этого подхода с использованием двух гликопептидов биантеннарного сложного типа (см. ). Поскольку конформации, полученные с помощью NOE, находились в диапазоне, центрированном на конформациях с минимальной энергией, полученных из расчетов потенциальной энергии, был сделан вывод, «что усреднение движения ограничено узким диапазоном около одной стабильной конформации» (Brisson and Carver, 1983). Однако теперь оказывается, что бессмысленно искать единственную конформацию, полученную из NOE, которая удовлетворяет одному минимуму потенциальной энергии, потому что фактически молекулы могут занимать такие минимумы в течение очень небольшой части времени в растворе.
Карвер и Камминг (1987) создали контурные карты рассчитанных NOE различных олигосахаридов с высоким содержанием маннозы в зависимости от торсионных углов φ и ψ. Затем они связали их с экспериментальными результатами, а также с конформациями минимальной энергии, оцененными с помощью различных расчетов потенциальной энергии (Карвер и Камминг, в печати). Бриссон и Карвер (1983) оценил полезность этого подхода с использованием двух гликопептидов биантеннарного сложного типа (см. ). Поскольку конформации, полученные с помощью NOE, находились в диапазоне, центрированном на конформациях с минимальной энергией, полученных из расчетов потенциальной энергии, был сделан вывод, «что усреднение движения ограничено узким диапазоном около одной стабильной конформации» (Brisson and Carver, 1983). Однако теперь оказывается, что бессмысленно искать единственную конформацию, полученную из NOE, которая удовлетворяет одному минимуму потенциальной энергии, потому что фактически молекулы могут занимать такие минимумы в течение очень небольшой части времени в растворе. «Конформационная гибкость должна быть включена в теоретическую трактовку» (Карвер и Камминг, 19).87), и расчет энергетических поверхностей становится чрезвычайно важным. Последние исследования Камминга и Карвера показывают, что трехмерные структуры, определяемые NOE, могут значительно отличаться от любой конформации с минимальной энергией. Из этого они пришли к выводу, что конформации, полученные из NOE, в таких случаях могут соответствовать «виртуальным» конформациям, как определено Jardetzky (1980), как вычисленные структуры, которые на самом деле принимают лишь немногие молекулы в растворе, если вообще какие-либо.
«Конформационная гибкость должна быть включена в теоретическую трактовку» (Карвер и Камминг, 19).87), и расчет энергетических поверхностей становится чрезвычайно важным. Последние исследования Камминга и Карвера показывают, что трехмерные структуры, определяемые NOE, могут значительно отличаться от любой конформации с минимальной энергией. Из этого они пришли к выводу, что конформации, полученные из NOE, в таких случаях могут соответствовать «виртуальным» конформациям, как определено Jardetzky (1980), как вычисленные структуры, которые на самом деле принимают лишь немногие молекулы в растворе, если вообще какие-либо.
РИСУНОК 8-3
Структуры двух частично процессированных аспарагиновых связанных углеводных цепей. Разделение пополам β1,4GlcNAc B вызывает конформационное отличие от A.
Scarsdale et al. (в печати) использовали программу, основанную на молекулярной механике, в попытке смоделировать конформационное усреднение данных ЯМР. Конформации рассчитывали с использованием комбинации молекулярных потенциалов и данных ЯМР для олигосахаридной части эритроцитарного гликолипида, состоящего из трех нейтральных сахаров и аминосахара. Конформер с наименьшей энергией очень напоминал структуру, предложенную ранее. Однако соответствие данным можно улучшить, если рассмотреть два уравновешивающих конформера. Таким образом, можно определить конформации растворов сложных углеводов даже в нежестких случаях, используя комбинацию расчетов и ограничений, налагаемых экспериментальными данными ЯМР.
Конформер с наименьшей энергией очень напоминал структуру, предложенную ранее. Однако соответствие данным можно улучшить, если рассмотреть два уравновешивающих конформера. Таким образом, можно определить конформации растворов сложных углеводов даже в нежестких случаях, используя комбинацию расчетов и ограничений, налагаемых экспериментальными данными ЯМР.
Несмотря на поднятые вопросы об интерпретации результатов ЯМР и ценности потенциальной минимизации энергии, была собрана некоторая важная информация о взаимодействиях углеводных антигенов с антителами (Lemieux et al., 1985), олигосахаридов с лектинами, такими как конканавалин А ( Sekharudu et al., 1986), и олигосахариды с ферментами гликозилтрансферазами (Carver and Cumming, 1987). Дальнейшие уточнения будут зависеть от разработки согласованного набора функций потенциальной энергии, которые можно использовать с экспериментально определенными трехмерными структурами, полученными из NOE, для оценки того, распределяется ли данная молекула между несколькими низкоэнергетическими конформациями или занимает конкретную форму. их подмножество. Твароска и Перес (1986) недавно сравнили несколько расчетов конформационной энергии и предложили общую стратегию для олигосахаридов.
их подмножество. Твароска и Перес (1986) недавно сравнили несколько расчетов конформационной энергии и предложили общую стратегию для олигосахаридов.
Компьютерное время и доступ к соответствующим процессорам массива параллельной обработки являются важными соображениями при определении уровня поддержки исследований в этой области в настоящее время. Доступность машин для очень быстрого расчета межатомных расстояний и вкладов Ван-дер-Ваальса — это вопрос, который должны решать финансирующие агентства. Интересно, что несколько суперкомпьютеров, работающих в настоящее время в кампусах, не используются на полную мощность; возможно, усилия соответствующих консультативных групп в этих центрах должны быть направлены на разработку необходимого программного обеспечения для этих компьютеров и установление политики, которая будет направлять часть их времени на компьютерное моделирование трехмерных структур.
НАДМОЛЕКУЛЯРНАЯ СТРУКТУРА
Структуры, состоящие из более чем одной макромолекулы, взаимодействуют как единое целое в биологических явлениях, таких как катализ многими ферментами, связывание на клеточной поверхности, передача сигнала через клеточные мембраны и другие биологические явления. Любой фермент, состоящий более чем из одной субъединицы, следует рассматривать как надмолекулярную структуру. Когда задействовано большое количество субъединиц и, возможно, они выполняют более одной функции, может потребоваться особое внимание к их относительной пространственной ориентации. Примерами являются репликация ДНК с помощью ДНК-полимераз, когда для инициации репликации требуются комплексы, содержащие 10 или 12 белков (называемые примосомами). Рибосомы еще более сложны: для трансляции матричной РНК требуется не менее 75 белков. Поверхности, состоящие более чем из одной макромолекулы, часто ведут себя как функциональная единица. Например, поглощение холестерина многими клетками требует взаимодействия специфического рецептора клеточной поверхности с полипептидной поверхностью сложной надмолекулярной структуры, называемой липопротеином низкой плотности (ЛПНП), который состоит из белка, холестерина, фосфолипидов и триацилглицеролов. Изменение белка ЛПНП путем ацетилирования остатка Lys блокирует связывание ЛПНП с его рецептором и поглощение холестерина клеткой.
Любой фермент, состоящий более чем из одной субъединицы, следует рассматривать как надмолекулярную структуру. Когда задействовано большое количество субъединиц и, возможно, они выполняют более одной функции, может потребоваться особое внимание к их относительной пространственной ориентации. Примерами являются репликация ДНК с помощью ДНК-полимераз, когда для инициации репликации требуются комплексы, содержащие 10 или 12 белков (называемые примосомами). Рибосомы еще более сложны: для трансляции матричной РНК требуется не менее 75 белков. Поверхности, состоящие более чем из одной макромолекулы, часто ведут себя как функциональная единица. Например, поглощение холестерина многими клетками требует взаимодействия специфического рецептора клеточной поверхности с полипептидной поверхностью сложной надмолекулярной структуры, называемой липопротеином низкой плотности (ЛПНП), который состоит из белка, холестерина, фосфолипидов и триацилглицеролов. Изменение белка ЛПНП путем ацетилирования остатка Lys блокирует связывание ЛПНП с его рецептором и поглощение холестерина клеткой. Некоторые гормоны, в том числе норадреналин и эпидермальный фактор роста (EGF), а также другие сигналы, такие как свет (с родопсином), вызывают фосфорилирование белка. EGF стимулирует рост нормальных фибробластов путем связывания со специфическим трансмембранным белковым рецептором на поверхности клетки. Гормональный сигнал в этом случае передается путем самофосфорилирования рецептора на внутриклеточной стороне после связывания гормона с последующим катализируемым другими киназами фосфорилированием белков, интернализацией комплекса EGF-EGF рецептор и сложным набором последствий. в ядре и в других местах при подготовке к клеточному делению. Бремер и др. (1986) недавно обнаружили, что ганглиозид GM3 ингибирует этот процесс аллостерическим образом, предотвращая самофосфорилирование рецептора EGF после связывания EGF. Для этого GM3 во внешней половине клеточной мембраны должен взаимодействовать с доменом полипептидной цепи рецептора EGF, вероятно, вызывая конформационные изменения, препятствующие фосфорилированию.
Некоторые гормоны, в том числе норадреналин и эпидермальный фактор роста (EGF), а также другие сигналы, такие как свет (с родопсином), вызывают фосфорилирование белка. EGF стимулирует рост нормальных фибробластов путем связывания со специфическим трансмембранным белковым рецептором на поверхности клетки. Гормональный сигнал в этом случае передается путем самофосфорилирования рецептора на внутриклеточной стороне после связывания гормона с последующим катализируемым другими киназами фосфорилированием белков, интернализацией комплекса EGF-EGF рецептор и сложным набором последствий. в ядре и в других местах при подготовке к клеточному делению. Бремер и др. (1986) недавно обнаружили, что ганглиозид GM3 ингибирует этот процесс аллостерическим образом, предотвращая самофосфорилирование рецептора EGF после связывания EGF. Для этого GM3 во внешней половине клеточной мембраны должен взаимодействовать с доменом полипептидной цепи рецептора EGF, вероятно, вызывая конформационные изменения, препятствующие фосфорилированию. Аналогичная ситуация, связанная с липидной мембраной, наблюдается с митохондриальным ферментом бета-гидроксимасляной дегидрогеназой, который каталитически активен только при включении в липидный бислой, состоящий из определенных фосфолипидов. Компьютерное математическое моделирование таких надмолекулярных структур будет необходимо для более глубокого понимания организации биологических материалов для выполнения сложных функций.
Аналогичная ситуация, связанная с липидной мембраной, наблюдается с митохондриальным ферментом бета-гидроксимасляной дегидрогеназой, который каталитически активен только при включении в липидный бислой, состоящий из определенных фосфолипидов. Компьютерное математическое моделирование таких надмолекулярных структур будет необходимо для более глубокого понимания организации биологических материалов для выполнения сложных функций.
Сноски
- 1
На самом деле правильнее говорить «один цистрон — один полипептид». Это также уже не является строго точным, поскольку более чем один ген может вносить вклад в первичную структуру белка, то есть в иммуноглобулины.
Углеводы | Основы биологии
Что вы узнаете на этой странице
- Что такое углеводы
- Почему углеводы важны
- Структура углеводов
- Различия между моносахаридами, дисахаридами и полисахаридами
- Примеры важных углеводов
Углеводы являются одной из четырех основных категорий молекул, встречающихся в живых существах, а остальные три – это белки, липиды и нуклеиновые кислоты. Они жизненно важны для жизни на Земле и выполняют ряд функций, таких как обеспечение энергией, структурная поддержка и сотовая связь.
Они жизненно важны для жизни на Земле и выполняют ряд функций, таких как обеспечение энергией, структурная поддержка и сотовая связь.
Углеводы представляют собой либо сахар, либо полимер сахаров. Полимер представляет собой два или более простых сахара, соединенных вместе. Углеводы — это молекулы на основе углерода, в которых водород и кислород связаны с цепью атомов углерода.
Простой сахар известен как моносахарид. Моносахариды могут связываться вместе, образуя дисахариды и полисахариды. Это три разных типа углеводов, и все три важны для разных целей в мире природы.
Почему важны углеводы?
Вся жизнь на Земле требует углеводов. Они нашли свое место в жизни не только животных и растений, но и грибов, бактерий, архей и простейших.
Самая важная роль углеводов в качестве источника энергии. Химическая энергия сахаров является основным источником энергии для большинства живых существ.
Растения используют солнечную энергию и CO₂ для создания углеводов. Эти углеводы составляют основу почти всех экосистем на Земле.
Эти углеводы составляют основу почти всех экосистем на Земле.
Использование углеводов для получения энергии предотвращает использование белков для получения энергии. Это важно, потому что позволяет использовать белки для других целей, таких как обмен веществ и сокращение мышц.
Некоторые из более сложных углеводов обеспечивают структурную поддержку и защиту. Клетки растений и грибов имеют клеточные стенки, состоящие из углеводов. Эти клеточные стенки обеспечивают защиту и поддержку клетки и всего организма.
Углеводы также участвуют в межклеточном узнавании. Клетки имеют углеводы на внешней поверхности своих клеточных мембран, которые действуют как рецепторы. Рецепторы могут взаимодействовать с углеводами на мембранах других клеток и помогать клеткам идентифицировать друг друга.
Структура углеводов
Химическая структура и состав углеводов относительно просты по сравнению с белками и липидами. Большинство углеводов полностью состоят из атомов углерода, водорода и кислорода.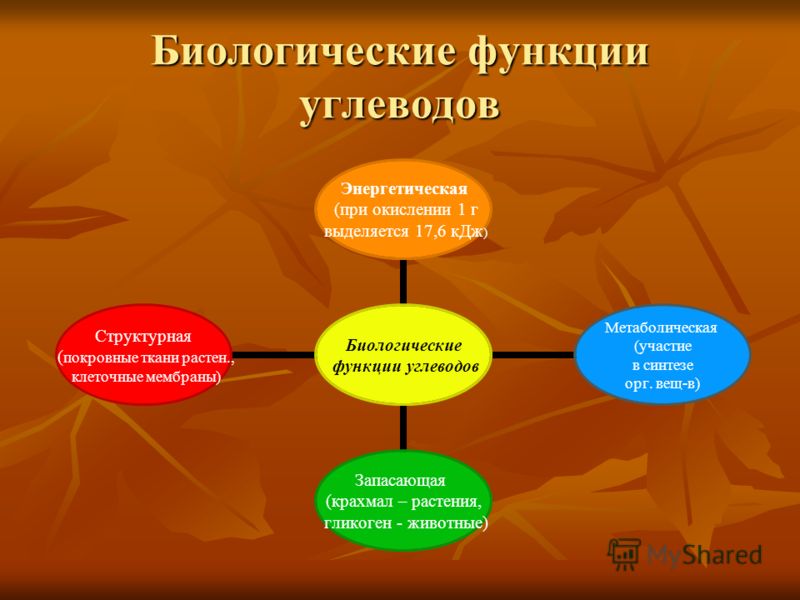 Углеводы имеют три или более атомов углерода, по крайней мере, два атома кислорода и несколько атомов водорода. Некоторые углеводы также содержат атомы азота, например, хитин, который содержится в панцирях насекомых.
Углеводы имеют три или более атомов углерода, по крайней мере, два атома кислорода и несколько атомов водорода. Некоторые углеводы также содержат атомы азота, например, хитин, который содержится в панцирях насекомых.
Атомы углерода могут связываться с четырьмя другими атомами. В углеводах атомы углерода образуют линейную цепь, связываясь с двумя другими атомами углерода. Цепь заканчивается, когда углерод использует три свои связи с кислородом и водородом, а не связывается с двумя атомами углерода.
Атомы кислорода углевода могут быть связаны с углеродом двойными или одинарными связями. Если кислород образует двойную связь с атомом углерода (C=O) вдоль углеродной цепи, это известно как карбонильная группа.
Кислород может быть связан с углеродной цепью в гидроксильной группе (атом кислорода, связанный с атомом водорода -ОН) одинарной связью с атомом углерода из углеродной цепи. Углеводы могут содержать более одной гидроксильной группы.
Атомы водорода занимают большую часть оставшихся углеродных связей. Обычно в углеводе примерно в два раза больше атомов водорода, чем атомов кислорода.
Обычно в углеводе примерно в два раза больше атомов водорода, чем атомов кислорода.
В действительности углеводы не всегда образуют линейные цепочки, а часто образуют кольца. Это происходит потому, что двойная связь между углеродом и кислородом карбонильной группы восстанавливается до одинарной связи, а кислород вместо этого связывается с другим атомом углерода вдоль цепи. Это создает кольцо, содержащее несколько атомов углерода и один атом кислорода.
Моносахариды — простые сахара
Моносахариды представляют собой самые основные углеводы и широко известны как простые сахара. Они включают хорошо известные сахара, такие как глюкоза и фруктоза. Моносахарид включает все необходимые компоненты углевода, то есть углеродную цепь, карбонильную группу и гидроксильную группу.
Моносахариды являются строительными блоками для более крупных углеводов, а также используются в клетках для производства белков и липидов. Сахара, которые не используются для получения энергии, часто хранятся в виде липидов или более сложных углеводов.
Именно моносахариды в основном используются клетками для получения энергии. Глюкоза, возможно, является наиболее важным моносахаридом, поскольку она используется при дыхании для обеспечения клеток энергией. Энергия, хранящаяся в связях молекулы глюкозы, в ходе ряда реакций преобразуется в энергию, пригодную для использования клетками.
Дисахариды
Дисахарид представляет собой углевод, состоящий из двух моносахаридов, соединенных вместе. Они по-прежнему считаются сахарами, но уже не являются простыми сахарами.
Моносахариды связываются друг с другом в так называемой реакции дегидратации, поскольку молекула воды удаляется при связывании двух сахаров. Реакция происходит между двумя гидроксильными группами (-ОН) двух моносахаридов.
У одного моносахарида полностью удалена гидроксильная группа, а у второго моносахарида удален атом водорода из гидроксильной группы. Удаленная гидроксильная группа и водород образуют молекулу воды, т.е. OH + H → H₂O
Из второго моносахарида еще остается кислород из гидроксильной группы. Этот кислород связывается с атомом углерода, где гидроксильная группа была удалена из первого моносахарида. Связь связывает два моносахарида вместе, создавая дисахарид.
Этот кислород связывается с атомом углерода, где гидроксильная группа была удалена из первого моносахарида. Связь связывает два моносахарида вместе, создавая дисахарид.
Наиболее известным дисахаридом является сахароза, которую мы используем дома в качестве сахара из-за ее сладости. Сахароза получается путем связывания одной молекулы фруктозы и одной молекулы глюкозы.
глюкоза + фруктоза = сахароза
Другим хорошо известным дисахаридом является лактоза, сахар, содержащийся в молочных продуктах. Лактоза состоит из одной молекулы глюкозы и одной молекулы галактозы.
Люди нередко испытывают трудности с расщеплением лактозы на глюкозу и галактозу после употребления молочных продуктов. Это является причиной состояния здоровья, известного как непереносимость лактозы, которое может вызвать диарею, вздутие живота, газы и рвоту.
Названия моносахаридов и дисахаридов заканчиваются суффиксом -оза. Например, фруктоза, глюкоза, галактоза, сахароза и лактоза.
Полисахариды
Полисахарид представляет собой три или более моносахаридов, соединенных вместе. Точно так же, как образуются дисахариды, полисахариды образуются в результате множественных реакций дегидратации между углеводами.
Точно так же, как образуются дисахариды, полисахариды образуются в результате множественных реакций дегидратации между углеводами.
Один моносахарид в полисахариде называется мономером. Полисахарид, состоящий из многих мономеров, можно назвать полимером. Некоторые полимеры состоят из более чем 1000 мономеров (или моносахаридов).
мономер = моносахарид; полимер = полисахарид
мономер + мономер + мономер = полимер
Полисахариды выполняют ряд биологических функций. Ключевая функция, которую они выполняют, — временное хранение энергии. Растения хранят энергию в форме полисахарида, известного как «крахмал». Многие культуры, такие как кукуруза, рис и картофель, важны из-за высокого содержания в них крахмала. Люди и другие животные запасают энергию в наших мышцах и печени с помощью полисахарида, известного как «гликоген».
Второй важной функцией полисахаридов является обеспечение структурной поддержки. В растениях есть два очень важных структурных полисахарида: целлюлоза и лигнин.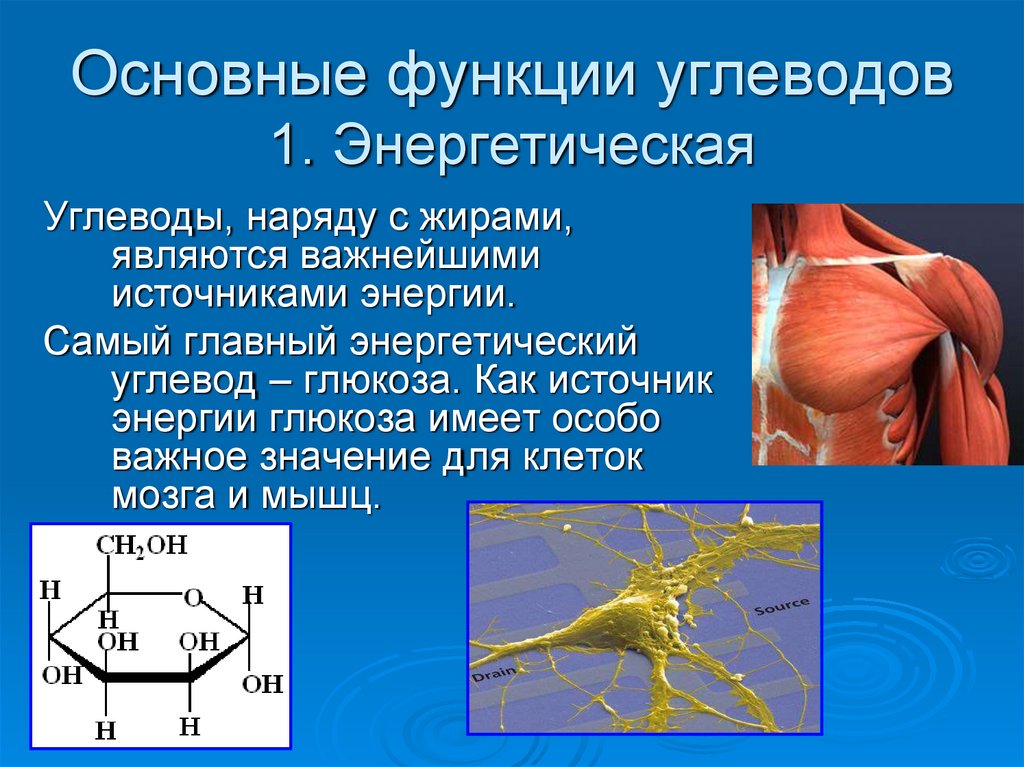
 1002/jlb.40.1.97
1002/jlb.40.1.97 doi: 10.1002/mrd.1120190402.
Гамет Рез. 1988 год.
PMID: 3058566
Обзор.
Аннотация недоступна.
doi: 10.1002/mrd.1120190402.
Гамет Рез. 1988 год.
PMID: 3058566
Обзор.
Аннотация недоступна.

 , Кальтнер Х., Копиц Дж., Майо К.Х., Мерфи П.В., Оскарсон С., Рой Р., Шедлбауэр А., Тогель С., Ромеро А.
Габиус Х.Дж. и др.
Химбиохим. 2022 5 июля; 23 (13): e202100327. doi: 10.1002/cbic.202100327. Epub 2021 22 сентября.
Химбиохим. 2022.
PMID: 34496130
Обзор.
, Кальтнер Х., Копиц Дж., Майо К.Х., Мерфи П.В., Оскарсон С., Рой Р., Шедлбауэр А., Тогель С., Ромеро А.
Габиус Х.Дж. и др.
Химбиохим. 2022 5 июля; 23 (13): e202100327. doi: 10.1002/cbic.202100327. Epub 2021 22 сентября.
Химбиохим. 2022.
PMID: 34496130
Обзор.