Артроз коленного сустава (гонартроз) III-IV стадия | Эндопротезирование коленного сустава. Цены клиник, рейтинг, отзывы
Гонартроз – это дегенеративное заболевание коленного сустава, при котором происходит постепенная деструкция суставного хряща. Заболевание постоянно прогрессирует. В запущенной стадии происходит полное разрушение сустава с его анкилозом (неподвижностью). Проблема решается с помощью операции по эндопротезированию коленного сустава.
Зачем нужно эндопротезирование?
Запущенный артроз коленного сустава не подлежит консервативной терапии. В запущенной стадии не помогут ни хондропротекторы, ни физиотерапия, ни уколы гиалуроновой кислоты. Коленный сустав практически разрушен. Восстановить его невозможно. Всё что остается – удалить собственный сустав и установить на его место искусственный эндопротез.
Такая операция позволяет пациенту получить следующие результаты:
- полное восстановление функции коленного сустава;
- избавление от постоянной боли;
- отсутствие необходимости в приеме обезболивающих препаратов;
- восстановление физической активности, трудоспособности.
При качественно проведенном эндопротезировании коленного сустава, после окончания реабилитационного периода пациент может вести полноценную активную жизнь. Его физические возможности будут близки к тем, что имеет здоровый человек с родными коленными суставами.
Преимущества эндопротезирования за границей
Многие пациенты выезжают для проведения операции по эндопротезированию коленного сустава в другую страну. Там они находят более качественные медицинские услуги. В результате операция проходит более эффективно и безопасно. Недостатком является лишь более высокая цена на лечение. Преимуществ гораздо больше:
Малоинвазивные техники. Разрезы мягких тканей при установлении эндопротеза значительно меньше. Не рассекаются мышцы, что позволяет наилучшим образом сохранить функцию нижней конечности. Уменьшается кровопотеря. Снижается риск осложнений эндопротезирования коленного сустава. Сокращается ранний реабилитационный период. Уменьшаются боли после операции. Соответственно, ниже потребность в обезболивающих препаратах.
Снижается риск осложнений эндопротезирования коленного сустава. Сокращается ранний реабилитационный период. Уменьшаются боли после операции. Соответственно, ниже потребность в обезболивающих препаратах.
Большой опыт. В таких странах как Германия ежегодно проводятся тысячи операций по эндопротезированию колена. Врачи оперируют не только местных жителей, но также иностранных пациентов. Поэтому они имеют огромный опыт установления эндопротезов.
Качественные эндопротезы. Они служат десятки лет и не требуют замены. Качественные эндопротезы не провоцируют иммунных реакций, имеют долгий срок службы и обеспечивают высокую функциональность колена. Некоторые эндопротезы способны сгибаться настолько сильно, что человек даже может сидеть на корточках.
Компьютерная навигация. В немецких клиниках используются современные методы протезирования колена. Для точной установки и регулировки применяются компьютерные системы навигации. При их использовании, как показывают исследования, снижается частота ревизионных (повторных) операций по эндопротезированию.
Сохранение или восстановление надколенника. Патология надколенника становится причиной операции по замене эндопротеза в 8% случаев. В Германии используются качественные эндопротезы, в которых замещается суставная поверхность надколенника (трехкомпонентные тотальные эндопротезы). Они снижают частоту послеоперационной передней боли и нарушения разгибательного механизма.
Где можно поставить эндопротез коленного сустава?
Компания Booking Health поможет определиться с оптимальным выбором. Мы учитываем особенности заболевания, расположение клиники, цели эндопротезирования и цены на лечение. Вот несколько примеров клиник, где вы можете установить эндопротез коленного сустава:
Клиника Норвейк Мария фон ден Апольстен. Находится в городе Мёнхенгладбах, Германия. Хирурги отделения ортопедии ежегодно проводят больше 800 операций по установлению эндопротезов нижней конечности. Здесь доступная стоимость лечения, высокое качество проводимых хирургических вмешательств и полноценный послеоперационный уход.
Здесь доступная стоимость лечения, высокое качество проводимых хирургических вмешательств и полноценный послеоперационный уход.
Академическая клиника Братьев Милосердия. Располагается в Мюнхене, Германия. Считается одной из лучших клиник для лечения болезней опорно-двигательного аппарата по версии журнала «Фокус». Лечение проводят хирурги отделения ортопедии и травматологии. Клиника считается Центром эндопротезирования максимального обеспечения. Здесь устанавливают эндопротезы коленного сустава пациентам любого возраста. Максимальной точности при установке эндопротеза позволяют добиться современные навигационные системы.
Академическая клиника БРК Берлин-Вестэнд. Эндопротезы коленного сустава устанавливаются в отделении ортопедии, травматологии и эндопротезирования. Используются цементные и бесцементные способы фиксации имплантов. В специализированном центре эндопротезирования проводятся первичные или ревизионные операции любой сложности. Используются минимально травматичные вмешательства.
Организация лечения
Чтобы сделать эндопротезирование в Германии, обратитесь к сотрудникам Booking Health. Наши преимущества:
- Выбор лучшей клиники, специализирующейся на проведении эндопротезирования колена.
- Сниженные цены на лечение (стоимость лечения может быть уменьшена до 50% в связи с отсутствием надбавок для иностранных пациентов).
- Помощь в выборе и приобретении импланта.
- Установление коммуникации с врачом.
- Запись пациента на максимально удобные даты.
- Подготовка программы и её контроль на всех этапах.
- Контроль счетов и возврат неизрасходованных средств.
- Коммуникация с клиникой после лечения.
- Помощь в покупке и пересылке препаратов.
- Организация дополнительных обследований или реабилитации.
Компания Booking Health обеспечит сервис высокого уровня. Мы поможем оформить документы, забронируем для вас авиабилеты и гостиницу, встретим в аэропорту и доставим в клинику.
Гонартроз
Гонартроз – это артроз коленного сустава, то есть изменения его хрящевой и костной ткани. Данное заболевание занимает одно из ведущих мест среди всех видов артрозов.
Различают 2 вида гонартроза: первичный (как правило, возникает на фоне сравнительного здоровья коленных суставов у людей пожилого возраста, особенно, женщин) и вторичный (развивается после травм, хирургических операций, воспалительных заболеваний коленного сустава).
Причины данного заболевания разнообразны, к ним относятся:
— избыточная масса тела,
— нарушение обменных процессов,
— различные травмы коленного сустава,
— воспалительные заболевания коленного сустава,
— избыточная нагрузка на суставы (у спортсменов),
— гормональные и эндокринные расстройства,
— наследственные факторы.
Основной жалобой при гонартрозе является боль в коленном суставе. Болезнь развивается постепенно. Возникает ограничение подвижности больного сустава, появляется крепитация, отек, деформация коленного сустава. Развивается прихрамывание на пораженную конечность. Проявление этих симптомов во многом зависит от стадии заболевания.
Диагноз «гонартроз» ставится на основании жалоб пациента, данных объективного осмотра и рентгенологического исследования. Также для диагностики данного заболевания применяют такие методы исследования, как МРТ, КТ, УЗИ.
Лечебные мероприятия должны быть направлены на устранение боли, улучшение питания хрящевой ткани и на ее восстановление. Необходимо улучшить кровообращение в области пораженного сустава и укрепить мышцы этой области.
В наших центрах успешно применяются методики лечения данного заболевания. Помимо медикаментозного лечения специалисты нашего центра подберут оптимальную схему лечения именно для вас. Проведение физиотерапевтических процедур, массажа, ЛФК на тренажерах проводится опытными и высококвалифицированными специалистами под контролем врача.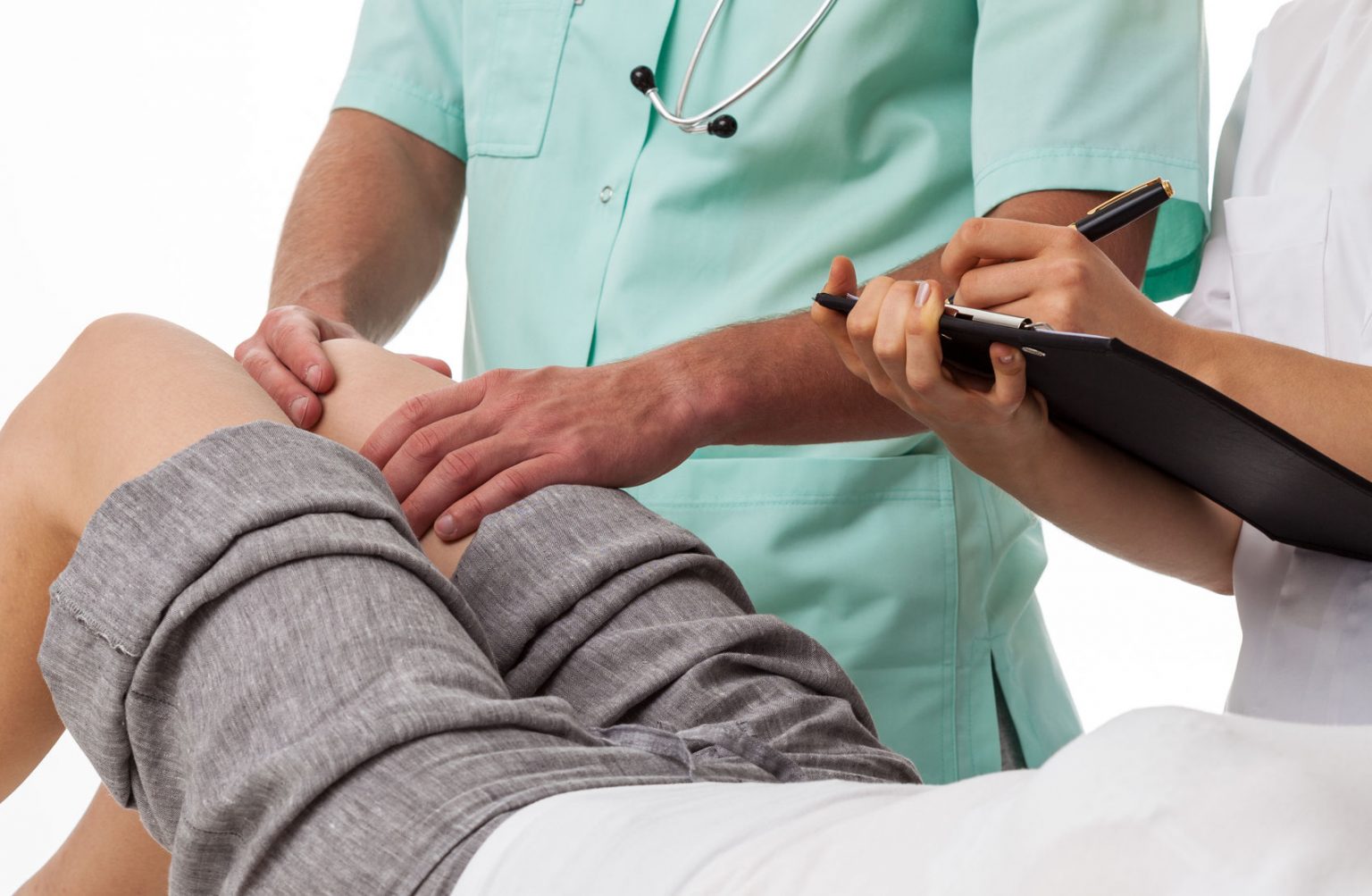
Помните: чем раньше вы начнёте лечение, тем меньше последствий разрушения сустава у вас будет.
Лечение артроза коленного сустава в Германии
Свен Рогманс, травматолог, ортопед
Специализируется по направлениям: ортопедия, травматология, специализированная хирургия несчастных случае, лечение различных видов особо тяжёлых травм.
Подробнее о специалисте →
Артроз коленного сустава (остеоартроз или гонартроз) — дегенеративное хроническое заболевание коленного сустава невоспалительного характера, в результате которого происходит истончение хрящевой и прилагающей к ней костной ткани и, тем самым, нарушение опорно-двигательной функции. Современные методы лечения артроза позволяют максимально замедлить дегенеративные процессы в колене и полностью устранить связанную с ними неприятную симптоматику.
Коленный сустав — самый большой так называемый шарнирный сустав человеческого тела, который создает гибкую связь между бедром (1, бедренная кость), коленной чашечкой (2, коленная чашечка) и голенью (6, голень). Таким образом, в согнутом состоянии возможно не только сгибание и разгибание колена, но и вращательные движения (вращение внутрь и наружу). Такие структуры, как крестообразные связки (3), мениск (4) и боковые связки (5), стабилизируют движения сустава.
Поскольку сустав между бедром и голенью (феморотибиальный/бедренно-большеберцовый) разделен на две части, то сам коленный сустав включает в себя три компонента из трех частей.
- Бедренно-голенной сустав — внутренняя часть
- Бедренно-голенной сустав — наружная часть
- Бедренно-коленный сустав – расположен между бедром и коленной чашечкой
В зависимости от того, сколько компонентов сустава вовлечено в патологический процесс, врачи говорят об одно-, би- или трикомпартиментальном гонартрозе.
Виды артроза коленного сустава
В зависимости от причины развития заболевания различают первичную и вторичную формы гонартроза:
- О первичной форме речь идет, если причина заболевания неизвестна. В таких случаях врачи ссылаются на генетическую предрасположенность, по причине которой хрящевая ткань пациента недостаточно устойчива и изнашивается быстрее, чем это свойственно для человека соответствующего биологического возраста.
- Вторичная форма гонартроза обусловлена одной или несколькими четкими причинами: например, ее развитие может быть следствием механической перегрузки — врожденного смещения сустава (X-образная или O-образная форма ног) или травмы, полученной в результате несчастного случая/спортивной перегрузки, а также осложнением основного заболевания — ревматизма, диабета, нарушения обмена веществ, ожирения и т.д.
Стадии гонартроза
1-я стадия. На ранних стадиях имеются незначительные изменен
2-я стадия. На второй стадии происходит истончение хряща, его поверхность деформируется и становится шероховатой и неровной. Это приводит к нарушению функции сустава, он больше не может равномерно распределять давление тяжести тела, ускоряя тем самым процесс развития артроза. Характерные жалобы на данном этапе: боли во время движения и напряжения суставов, хруст в колене при ходьбе и приседаниях, уменьшение подвижности, что является причиной первого визита к врачу.ия хрящевой ткани, но пациент, как правило, не жалуется на боль и не ощущает дискомфорта.
3-я стадия. Суставное пространство значительно сокращено, давление на кости, в свою очередь, повышено, что ведет к образованию на суставном сочленении костных наростов (остеофитов). Они перенимают на себя функцию хряща, с одной стороны, укрепляя его. Тем не менее, хрящевая составляющая начинает разрушаться из-за разрастания остеофитов, а колено со временем утрачивает свою функциональную подвижность.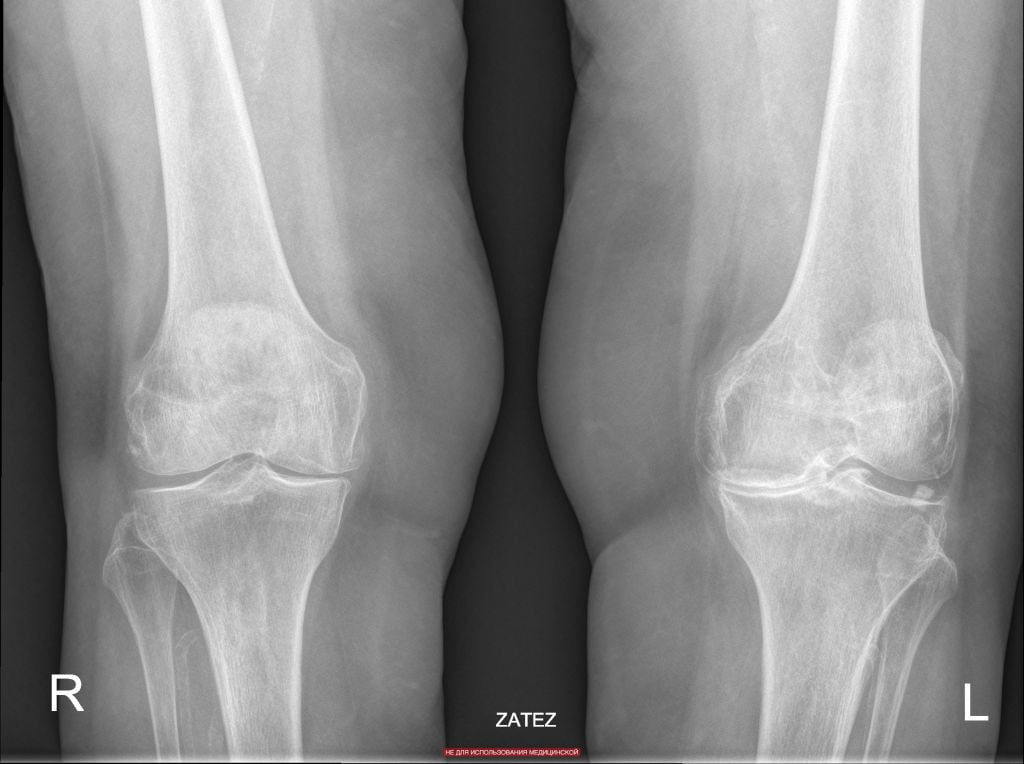
4-я стадия. На поздней стадии артроза коленного сустава хрящевая ткань в нем практически отсутствует, что провоцирует трение костей друг о друга. Пациенты даже в состоянии покоя испытывают острую боль. Подвижность сустава значительно или полностью ограничена, так что пациент вынужден прибегать к помощи костылей или трости.
Лечение гонартроза коленного сустава
К сожалению, гонартроз относится к неизлечимым хроническим заболеваниям. Несмотря на это, данное заболевание требует обязательного проведения поддерживающей терапии, которая направлена на максимально возможное замедление его развития и купирование актуальных жалоб. Чем медленнее будет прогрессировать гонартроз, тем больше времени пациент будет мобилен и сможет вести полноценный образ жизни. Поэтому пациентам с диагнозом «Артроз коленного сустава» следует начинать терапию как можно раньше.
Медикаментозное лечение гонартроза
Возникновение боли в пораженном суставе является одной из первых причин, по которым пациент обращается за медицинской помощью. Так как дегенеративный процесс необратим, то в первую очередь купируется болевой синдром. Какими лекарствами в Германии лечат артроз коленного сустава:
- анальгетики – использование обезболивающих, таких, как парацетамол, особенно эффективно на первом этапе заболевания. Надо отметить, что анальгетики не борются с причиной появления боли, а только блокируют передачу болевых сигналов в головной мозг.
- нестероидные противовоспалительные препараты (НПВП) — АСС, Ибупрофен, Диклофенак и прочие — являются наиболее часто используемыми препаратами в лечении гонартроза. Они обладают не только обезболивающим, но и противовоспалительным эффектом. Данные препараты применяются как местно — в виде мазей, гелей, кремов — так и в форме капсул или таблеток для перорального применения.

- препараты селективных ингибиторов ЦОГ-2— это относительно новая группа препаратов, так называемых коксибов, использование которых по отдельности или в комбинации с НПВП применяется при эндопротезировании тазобедренного и коленного сустава в качестве компонента мультимодального обезболивания. Данный вид препаратов, с одной стороны, позволяет ускорить восстановление и мобилизацию пациента, а с другой — уменьшить его потребность в терапии с применением опиоидных анальгетиков и снизить тем самым частоту побочных эффектов, связанных с ними.
- кортикостероиды – внутрисуставные инъекции препарата кортизона в коленный сустав позволяют быстро и безболезненно доставить лекарственное вещество к повреждённым тканям, без пагубного воздействия на желудочно-кишечный тракт. В краткосрочной перспективе кортизон оказывает быстрое противовоспалительное действие и восстанавливает былую подвижность. Но в долгосрочной перспективе кортизон может стать причиной разрушения хрящевой ткани, поэтому его не рекомендуют применять чаще 4-х раз в год.
- инъекции гиалуроновой кислоты, которая является естественным компонентом синовиальной жидкости и физиологически находится во всех суставах, в том числе и в коленном. Инъекции гиалуроновой кислоты представляют собой внутрисуставные уколы гелеобразной жидкостью, которая помогает смазывать сустав, тем самым амортизируя его при нагрузках. При гонартрозе второй и третьей стадии инъекции «гиалуронки» рекомендуется проводить в комбинации с медикаментозным лечением гонартроза и физиотерапией . Сама инъекция производится амбулаторно с использованием местной анестезии и контроля КТ. Эффект от инъекции длится от шести до двенадцати месяцев и даже превосходит инъекции кортизона: введение в сустав гиалуроновой кислоты не только уменьшает боль и улучшает функционирование сустава, но также зачастую и замедляет течение заболевания.
- Рентгеновское облучение, или ортовольтная рентгенотерапия — это форма лучевой терапии.
 Это полностью безболезненная процедура, с низкой дозой радиационного излучения (по сравнению с облучением при злокачественных образованиях), а ее продолжительность занимает всего несколько секунд. Для равномерного распределения дозы колено облучается с двух сторон одновременно. Рентгенотерапия при остеоартрозе оказывает противовоспалительное действие и снимает боль. Подобное лечение имеет отсроченный во времени эффект, а после первого облучения боль может даже усилиться. Но это лишь свидетельствует о том, что пациент реагирует на терапию. В течение нескольких недель боль в суставе становится заметно менее выраженной.
Это полностью безболезненная процедура, с низкой дозой радиационного излучения (по сравнению с облучением при злокачественных образованиях), а ее продолжительность занимает всего несколько секунд. Для равномерного распределения дозы колено облучается с двух сторон одновременно. Рентгенотерапия при остеоартрозе оказывает противовоспалительное действие и снимает боль. Подобное лечение имеет отсроченный во времени эффект, а после первого облучения боль может даже усилиться. Но это лишь свидетельствует о том, что пациент реагирует на терапию. В течение нескольких недель боль в суставе становится заметно менее выраженной.
Хирургическое лечение артроза коленного сустава
В немецкой клинике «Нордвест» успешно применяются следующие методы хирургического лечения:
- Артроскопия коленного сустава — минимально инвазивная хирургическая манипуляция, осуществляемая в целях диагностики и/или лечения повреждений внутренней части сустава. При артроскопии врач может промыть коленный сустав, а также устранить механические причины болевого синдрома, то есть отполировать шероховатости, удалить малейшие отслоившиеся частички костной и хрящевой ткани, тем самым восстанавливая его статику.
- Эндопротезирование коленного сустава – хирургический метод по восстановлению его подвижной и вращательной функции посредством частичной или полной замены сустава. Данный метод применяется в том случае, если консервативная терапия не дала желаемых результатов и болевой синдром преобладает. Возможна как тотальная, так и частичная замена поврежденного сустава. На сегодняшний день современные эндопротезы изготавливаются с учетом индивидуальных анатомических и терапевтических особенностей пациента из материалов, максимально схожих с собственными тканями человеческого организма, повторяющих форму здорового сустава. Это позволяет подобрать оптимально подходящие типы протезов для женщин, аллергиков, спортсменов и даже для детей. При частичном эндопротезировании производится лишь замена поврежденных отделов коленного сустава, таких, как, например, изношенная хрящевая ткань.
 При этом здоровые участки (кость, боковые и задняя крестообразная связка) сохраняются. Целью является максимально возможное сохранение собственных тканевых структур организма при минимальном внедрении инородного компонента (имплантата). Это позволяет сократить сроки реабилитации и значительно увеличить мобилизацию пациентов и, тем самым, улучшить качество жизни на 20-30 лет.
При этом здоровые участки (кость, боковые и задняя крестообразная связка) сохраняются. Целью является максимально возможное сохранение собственных тканевых структур организма при минимальном внедрении инородного компонента (имплантата). Это позволяет сократить сроки реабилитации и значительно увеличить мобилизацию пациентов и, тем самым, улучшить качество жизни на 20-30 лет.
Возможно, принять решение Вам помогут отзывы пациентов, которые уже прошли лечение артроза коленного сустава в Германии. Не теряйте драгоценное время, пытаясь найти контакты лучших профильных немецких специалистов на форумах в Сети — обращайтесь к нам! С нами Вы сможете осуществить свой первый шаг навстречу здоровью!
ЛЕЧЕНИЕ АРТРОЗА КОЛЕННОГО СУСТАВА СТВОЛОВЫМИ КЛЕТКАМИ
Артроз коленного сустава или изнашивание хрящевой ткани является заболеванием, значительно снижающим качество жизни пациентов, причиняющим сильную боль в коленях и снижающим подвижность. Не стоит думать, что данное заболевание характерно лишь для людей пожилого возраста, артроз стал настоящей проблемой и для людей в возрасте до 35 лет вследствие увеличения частоты случаев ожирения и неконтролируемых занятий спортом. К сожалению, в настоящее время пока не представляется возможным полное излечение от данного заболевания. В лечении артроза применяются различные методы: от лечебной физкультуры до противовоспалительных средств, от физиотерапии до уколов в коленный сустав, последним выходом становится хирургическое вмешательство. Многообещающей и приятной новостью для страдающих артрозом станет возможность лечения стволовыми клетками. Специалист клиники Acıbadem Altunizade в области ортопедии и травматологии Профессор-доктор Альпер Кайя отметил, что, несмотря на то, что в настоящее время метод лечения артроза стволовыми клетками еще не является на 100% эффективным, он приводит к значительному снижению количества жалоб и увеличению амплитуды движения в коленном суставе пациентов, предыдущее лечение которых оказалось безрезультатным, и продолжил: «Мы считаем, что биологические методы лечения, такие как лечение стволовыми клетками, будут широко применяться в ближайшем будущем».
Остерегайтесь боли при подъеме и спуске по лестнице!
Одним из главных признаков наличия артроза в коленном суставе является боль. Проявляющаяся при дополнительной нагрузке, прогрессирующая при подъеме и спуске по лестнице боль постепенно начинает беспокоить даже в состоянии покоя. Специалист в области ортопедии и травматологии Профессор-доктор Альпер Кайя предупредил, что повсеместно с увеличивающейся болью снижается подвижность, и описал следующие симптомы заболевания следующим образом: «Кроме того, артроз сопровождается такими симптомами, как набухание тканей вокруг колена, появление хруста, зависание и застревание сустава при ходьбе. На прогрессирующей стадии заболевания возникает проблема со сгибанием колена. В результате, пациенты прибегают к использованию обезболивающих препаратов и не могут выбраться из дома».
Может потребоваться проведение операции на прогрессирующей стадии заболевания
Не существует определенного способа лечения артроза коленного сустава. Принятие решения о методе лечения пациента основывается на возрасте, тяжести боли, влиянии повседневного образа жизни, других заболеваниях и социальном статусе. На первой стадии заболевания лечение включает восстанавливающую подвижность сустава лечебную гимнастику, специальную диету и прием анальгетиков. Препараты, способствующие нормализации структуры хряща, также снижают тяжесть беспокоящей пациентов боли. Кроме того, применяется физиотерапия и вводятся внутрисуставные инъекции. На более прогрессирующих стадиях заболевания или в случае безрезультатного лечения производится артроскопическая операция без вскрытия коленного сустава, а также корректирующее несущую ось кости хирургическое вмешательство. Эндопротезирование же производится при полном отсутствии хрящевой ткани и на самой последней стадии артроза.
Многообещающий метод лечения стволовыми клетками
Стволовые клетки могут быть получены из костного мозга и жировых тканей. Специалист в области ортопедии и травматологии Профессор-доктор Альпер Кайя подчеркнул отсутствие необходимости в проведении лечения в операционной и пребывании пациента в больнице и продолжил: «Сперва производится забор стволовых клеток из костного мозга или жировых тканей пациента под местной анестезией и их размножение в лаборатории. Процесс размножения занимает несколько часов. Тем временем, пациент пребывает в комнате отдыха отделения введения стволовых клеток. Размноженные стволовые клетки вводятся в коленный сустав в жидкой форме в тот же день. После чего пациент сразу же выписывается из больницы».
Процесс размножения занимает несколько часов. Тем временем, пациент пребывает в комнате отдыха отделения введения стволовых клеток. Размноженные стволовые клетки вводятся в коленный сустав в жидкой форме в тот же день. После чего пациент сразу же выписывается из больницы».
Сокращение жалоб пациентов
Стволовые клетки являются особым видом клеток, которые способны размножаться и трансформироваться в другие клетки. Предполагается, что стволовые клетки, содержащиеся в различных тканях организма, таких как костный мозг, жировые ткани и т.д., восстанавливают поврежденную хрящевую ткань посредством генерации новых клеток. Кроме того, считается, что стволовые клетки препятствуют повреждению хрящевой ткани, секретируя определенные вещества. Специалист в области ортопедии и травматологии Профессор-доктор Альпер Кайя подчеркнул, что благодаря данному методу наблюдается восстановление поврежденной области и сокращение жалоб пациентов, и продолжил: «Несмотря на то, что существующая проблема не устраняется полностью, исследования свидетельствуют о сокращении жалоб на боль, увеличении подвижности сустава и восстановлении здоровья, достаточного для возвращения к привычному образу жизни. Однако, столь многообещающий метод лечения стволовыми клетками требует большего изучения и обоснования, предполагается получение более точных результатов в ближайшем будущем».
Когда стоит прибегать к данному методу?
Специалист в области ортопедии и травматологии Профессор-доктор Альпер Кайя объяснил необходимость применения метода лечения стволовыми клетками следующим образом: «Нехирургический метод лечения стволовыми клетками может стать альтернативой при артрозе с легкой или умеренной степенью износа хряща, а также в случае, если предыдущее лечение оказалось безрезультатным. Кроме того, для более молодых пациентов с износом хрящевой ткани в определенной области производится размещение специальной синтетической ткани со стволовыми клетками в поврежденной области хирургическим путем. Лечение стволовыми клетками противопоказано на поздней стадии заболевания, требующей эндопротезирования, в силу его неэффективности. Однако, последнее слово в данном вопросе принадлежит лечащему врачу».
Лечение стволовыми клетками противопоказано на поздней стадии заболевания, требующей эндопротезирования, в силу его неэффективности. Однако, последнее слово в данном вопросе принадлежит лечащему врачу».
Физиотерапия при гонартрозе
Физиотерапия при артрозе оказывает отличный положительный эффект. Физиотерапевтические сеансы поддерживают и улучшают подвижность коленных суставов, при этом они укрепляют мышцы и оказывают обезболивающее действие. Физиотерапию врач назначает вне обострения, в острой стадии на высоте боли от физиотерапии желательно воздержаться. Так, например, многие пациенты с артрозом любят прогреваться. Тем не менее, при обострении гонартроза активное прогревание может быть небезопасно. Поэтому все прогревающие процедуры, выполняемые в домашних условиях должны быть оговорены с лечащим врачом.
Общие противопоказания к физиотерапии
- лихорадка;
- снижение или отсутствие кожной чувствительности;
- злокачественные новообразования;
- гнойное кожное поражение;
Помимо общих противопоказаний к каждой процедуре могут быть определенные ограничения, поэтому только специалист может назначить необходимый вид физиотерапии.
Наиболее частое физиотерапевтическое воздействие при гонартрозе
- Лечение холодом
Пациенты с острым раздражением или воспалением коленного сустава могут получить пользу от применения холодовых процедур. В домашних условиях это холодные примочки, в стационарных — использование криокамер.
- Электротерапия
Электрические токи предотвращают или замедляют передачу болевых сигналов, стимулируют регенерацию тканей и улучшают кровообращение. Одной из самых известных процедур в этой области является лечение с помощью уникального немецкого прибора «Zimmer» для электростимуляции и ультразвуковой терапии. Врач подбирает индивидуальную схему для каждого пациента. Генерируемые низкочастотные токи передаются через электродные пластины, которые наклеиваются контактной пастой на коленный сустав к коже. Электрофорез помогает доставить препарат «адресно», создавая в тканях сустава лекарственное депо.
Электрофорез помогает доставить препарат «адресно», создавая в тканях сустава лекарственное депо.
- Иглоукалывание
Иглоукалывание может облегчить боль у пациентов с остеоартрозом коленного сустава. При лечении иглоукалыванием, которое обычно происходит в положении лежа, иглы вводятся в кожу в определенных точках в зависимости от заболевания. Стерильные одноразовые иглы специально отшлифованы, поэтому пациент испытывает незначительные, иногда минимальные, начальные пункционные боли. Через некоторое время на обработанных участках может развиться тупое чувство тяжести или тепла. Иглы остаются в коже в течение 20-30 минут. Для достижения определенных эффектов используются специальные методы стимуляции. То есть, иглы могут быть дополнительно нагреты (прижигание) или перемещены вверх и вниз. Есть и другие процедуры, которые влияют на акупунктурные точки. Во время точечного массажа терапевт массирует акупунктурные точки пальцами.
- Магнитно-резонансная терапия- MBST
MBST эффективна при гонартрозе. Она может применяться как отдельный курс лечения, так и в сочетании с другими техниками. Многие больные благодаря данной инновационной технологии избежали скальпеля хирурга. Эффект от процедуры наступает не сразу (необходимо несколько сеансов), но сохраняется в течении нескольких лет.
- Лазерная терапия
Лазерная терапия остеоартроза коленного сустава также может быть полезна в сочетании с двигательной терапией. Благодаря воздействию лазера в тканях происходят оздоровительные процессы – усиливается регенерация клеток, снимается воспаление. Лазер может назначаться даже во время обострения, так как обладает обезболивающим эффектом.
- Аппликации грязевые, озокеритом и парафином
Лечебная грязь, черный воск и парафин обладают целым спектром полезных биологических эффектов – согревающий, компрессионный, регенерирующий, обезболивающий. Благодаря обертыванию суставов химически активными веществами, нижележащие структуры получают необходимые компоненты и лечебные соли. Кроме того, такие аппликации благодаря высокой теплопроводности используемых средств, являются одним из вариантов теплового воздействия, которое усиливает кровообращение в патологической области. Показаны через день, вне обострения. Курс желательно проходить 2 раза в год.
Кроме того, такие аппликации благодаря высокой теплопроводности используемых средств, являются одним из вариантов теплового воздействия, которое усиливает кровообращение в патологической области. Показаны через день, вне обострения. Курс желательно проходить 2 раза в год.
- Плазмотерапия
Технология ArthrexACP System – это аутогемотерапия в модифицированной форме. Плазмотерапия – безопасная процедура, которая обладает локальным стимулирующим эффектом. После сеансов уменьшается боль и воспаление.
- Ультразвук
Ультразвуковые волны, проникающие на глубину до 6 см, улучшают микроциркуляцию, прогревают сустав, усиливают метаболизм, уменьшают отек и улучшают регенерацию хрящевой ткани.
- Бальнеотерапия.
Лечебные ванны широко применяются в лечении гонартроза. Особенно популярны йодо-бромные, солевые, скипидарные и хвойные ванны. Время принятия ванны не должно превышать 20 минут. После ванны желательно отдохнуть.
Для достижения лучшего эффекта физиотерапевт чередует эти сеансы. Он видит динамику процесса и при необходимости корректирует лечение. Перед сеансами выявляются возможные противопоказания, поэтому во время беседы с врачом пациент должен рассказать о всех сопутствующих болезнях.
Заключение.
Физиотерапевтическое лечение считается одним из лучших в терапии гонартроза. Оно стимулирует обменные процессы, восстанавливает местное кровообращение, вызывает локальное прогревание. Некоторые виды физиотерапии можно применять даже в период обострения! Домашнюю физиотерапию можно использовать только по назначению врача, так как самостоятельное прогревание суставов может привести к ухудшению ситуации и обострению процесса.
Методы лечения артроза и артрита за рубежом
Доктор Вадим БережнойОснователь платформы MediGlobus. Медицинский эксперт, Заведующий отделением врачей-координаторов.
С заболеваниями суставов в процессе жизни сталкиваются все больше людей. Многие пациенты имеют недостаточно информации о возможностях современной медицины. Они ежедневно терпят выраженную боль и лечение безрезультативно.
Многие пациенты имеют недостаточно информации о возможностях современной медицины. Они ежедневно терпят выраженную боль и лечение безрезультативно.
Одними из самых распространенных заболеваний опорно-двигательного аппарата являются артриты и артрозы. Обе болезни возникают из-за большого количества этиологических факторов. Они поражают суставы человека и к деформациям, нарушению их функциональности, а как следствие – значительному снижению качества жизни.
АРТРОЗ (ОСТЕОАРТРОЗ, ДЕФОРМИРУЮЩИЙ ОСТЕОАРТРОЗ)
Что такое артроз, какие его симптомы
Артроз (остеоартроз) – дегенеративное заболевание суставов. В его основе лежит поражение хрящевой ткани суставных поверхностей костей. Патология является довольно распространенной. Она признана одной из основных причин нетрудоспособности населения.
В патологический процесс обычно вовлекается не только хрящевая ткань, но и субхондральная кость (участок кости, на котором расположена хрящевая пластина), связочный аппарат сустава, синовиальная оболочка и периартикулярная мышечная ткань.
Дегенеративно-дистрофические процессы начинаются в хряще, но очень быстро затрагивают практически все ткани сустава. Это приводит к изменению его формы, нарушению функциональности или ограничению подвижности, умеренному, а позже выраженному болевому синдрому и воспалительному процессу.
Артроз поражает суставы кистей рук, коленных суставов (гонартроз), тазобедренных (коксартроз), голеностопного и плечевого суставов.
Также известны варианты поражения суставов в шейном и поясничном отделах позвоночника. Основными симптомами артроза является боль, ограничение подвижности, деформация, хруст при движении внутри сустава.
Стадии Артроза
В медицине принято различать 3 стадии (степени) развития артроза.
Стадия 1
Протекает практически незаметно с незначительными изменениями в структуре сустава, происходит истончение хрящевой ткани, меняется состав синовиальной жидкости. Дискомфорт в области больного сустава ощущается только после физической нагрузки.
Стадия 2
На второй стадии уже есть изменения, которые являются причиной легкого хруста и умеренной болезненности при ходьбе и просто движениях. Может иметь место снижение амплитуды движений и быстрая утомляемость во время ходьбы.
Стадия 3
Считается самой тяжелой, здесь пациент испытывает сильный болевой синдром, явное ограничение подвижности сустава, видны деформации. Хрящевые пластины суставных поверхностей костей практически стерты, в процесс вовлекается костная ткань, что причиняет невыносимую боль. Передвижения человека возможны только с тростью или на ходунках.
ПРИЧИНЫ И ФАКТОРЫ РИСКА
Большое количество этиологических факторов влияют на развитие заболевания. Однако на сегодняшний день выделены только 3 основные причины дегенеративных процессов в суставе:
Факторы риска развития болезни очень разнообразны. Они повышают вероятность возникновения проблем с суставами и усугубляют течение заболевания. Среди них выделяют:
ДИАГНОСТИКА и лечение АРТРОЗА
Ни в коем случае не стоит заниматься самодиагностикой и лечением, опираясь на симптомы заболевания и непроверенные источники информации. Лучше обратиться за консультацией к врачу-ортопеду. Доктор назначит необходимые обследования, по результатам которых подберет терапию.
Диагностика артрозов не вызывает особой сложности. Чаще всего для постановки диагноза и определения стадии процесса достаточно осмотра, а также рентгенологического исследования сустава (применяется стандартный или цифровой рентген). В редких случаях может быть назначено проведение МРТ.
Лечение артрозов зависит от стадии развития болезни. Если заболевание диагностировано на раннем этапе, приостановить его прогрессирование можно путем коррекции образа жизни, а также занятиями лечебной физкультурой. В случае полностью разрушенной хрящевой ткани единственный вариант – замена сустава.
Лечение артритов, в особенности ревматоидного, зависит от проявлений заболевания. Как правило, терапия начинается с приема лекарственных препаратов. При деформации крупных суставов проводят эндопротезирование суставов.
Артроскопия
Малоинвазивный хирургический метод, выполняемый с использованием специальной видеоэндоскопической техники. Во время операции с поверхности сустава удаляются лишние и деформированные части хрящевой ткани, поверхность сустава шлифуется, что приводит к улучшению общего состояния пациента и снижению болевого синдрома. Метод применим в большей степени при артрозах, изредка к нему прибегают при артритах.
Протезирование суставов
Самый эффективный метод лечения. Замена сустава может быть как частичной, так и полной (тотальной). Данный метод эффективен в 90% случаев. Пациенты перестают жаловаться на боль. Значительно восстанавливается подвижность сустава. 3 стадия артроза – прямое показание к эндопротезированию сустава. Протезы изготавливаются чаще всего из сплава кобальт-хром, кобальт-хром-молибден или гипоаллергенного титана. Головки суставных поверхностей производятся из высокомолекулярных полимерных соединений или керамики. Тип импланта выбирается исключительно доктором.
Протезирования суставов проводятся как в за рубежом, так и в странах СНГ. По ценам на лечение иностранные госпитали уступают медицинским центрам в странах бывшего СССР, где стоимость будет ниже. При этом, у медицинских центров за рубежом большим преимуществом являются минимально инвазивные хирургические доступы, быстрая и качественная реабилитация, эффективное купирование болевого послеоперационного синдрома и высокий процент успешности лечения. Уже через 1 месяц после операции по замене сустава пациенты могут вернуться к активной жизни и занятиям спортом.
Медикаментозная терапия
Лечение противовоспалительными и гормональными препаратами является основой медикаментозной терапии как артрозов, так и артритов. Целью подобного лечения является остановка воспалительного процесса в тканях сустава и замедление прогрессирования болезни. Также дополнительно назначаются хондропротекторы, которые при длительном применении способствуют улучшению состояния хрящевой ткани. Ортопедия за рубежом имеет целый арсенал лекарственных препаратов нового поколения.
Лечебная физкультура и аппаратное лечение
ЛФК и аппаратные воздействия на сустав применяются исключительно в период ремиссии. На первой стадии болезни ЛФК может быть основной терапией, на более поздних стадиях этот метод разрешается применять как дополнительную терапию к основному лечению.
PRP-терапия (плазмотерапия)
Представляет собой метод лечения, при котором в полость сустава вводятся обогащенные тромбоцитами препараты крови (плазма), изготовленные из собственной крови пациента. Этот метод очень эффективен на начальных стадиях артроза и требует около 3-5 инъекций. PRP-терапия считается безопасной, так как в процессе лечения не используются сторонние препараты, которые могут вызвать осложнения.
Что такое АРТРИТ?
Артрит – это комплексный диагноз, который объединяет несколько патологий, основным механизмом их развития является воспалительный процесс в тканях сустава. Он может быть аутоиммунным или инфекционным.
Под аутоиммунным воспалением подразумевают нарушения в иммунных процессах организма, которые связаны с повышением синтеза ревматоидного фактора – специфических антител. Повышенные концентрации этих антител приводят к поражению тканей суставов. Чаще всего подобный диагноз звучит как ревматоидный артрит. Для диагностики артрита применяют:
Артрит относится к медленно прогрессирующим заболеваниям. Основным методом их лечения является медикаментозная терапия, которая замедляет течение болезни. Рано или поздно дегенеративные процессы в суставе приводят к полной или частичной утрате функций сустава и нетрудоспособности пациента.
Если у Вас возникли вопросы по поводу лечения заболеваний суставов за рубежом, наши координаторы готовы дать развернутые ответы! Оставляйте заявки в форме. Мы в свяжемся с Вами в кротчайшие сроки.
Получить бесплатную консультацию
Доктор Вадим Бережной
Основатель платформы MediGlobus. Медицинский эксперт, Заведующий отделением врачей-координаторов.
Альбина ГоловинаРаботает в сфере медицинского копирайтинга 2 года. Учится на аспирантуре факультета психологии. Автор нескольких научных публикаций в области клинической психологии. Дополнительно изучает физиологию ЦНС, нейропсихологию и психиатрию. В свободное время изучает практики mindfulness и проводит психологические консультации.
Похожие посты
Сколько стоит эндопротезирование плечевого сустава за рубежом?
Читать дальшеЛечение миодистрофии Дюшенна за рубежом — 5 способов продлить жизнь еще на 20 лет
Читать дальшеМедикаментозное лечение остеоартроза | Алексеева Л.И.
Остеоартроз (ОА) – это гетерогенное заболевание, с наибольшей частотой встречающееся у людей старше 60 лет и характеризующееся выраженным болевым синдромом и нередко наличием воспалительных признаков, приводящими больного к врачу. Боль представляет собой самый частый симптом при ОА, поэтому лечение заболевания направлено, в первую очередь, на уменьшение болевого синдрома и, как результат этого, улучшение функции сустава. У 10–30% больных ОА развивается различной степени нетрудоспособность, поэтому возможность воздействовать на естественное течение заболевания имело бы большое социальное и экономическое значение. Традиционное лечение ОА заключается прежде всего в управлении болевым синдромом, которое начинается с различных нефармакологических методов, включающих образование больных, физическую терапию, чрескожную стимуляцию и другие. Однако при недостаточной эффективности нефармакологических методов лечения требуется назначение лекарственной терапии. Действие большинства лекарственных средств направлено, в первую очередь, на лечение симптомов болезни, хотя некоторые из них рассматриваются, как препараты, влияющие на катаболические и анаболические процессы, происходящие при повреждении хряща. Эти лекарства классифицируются, как препараты, модифицирующие симптомы болезни. Выбор препаратов, подбор комбинации различных методов лечения остаются строго индивидуальными (табл. 1). Знание механизмов действия, эффективности, противопоказаний при назначении препаратов, профиля безопасности лекарств чрезвычайно важно.
Несмотря на относительно длительный период применения лекарственных средств, остается большое количество вопросов относительно симптоматического лечения. Иерархически первое место занимают анальгетические препараты. Впервые использование ацетоминофена при ОА рекомендовали Bradley с соавт. [1], которые показали, что прием 4,0 г ацетаминофена в день был сравним по эффективности с двумя дозами ибупрофена (1200 мг и 2400 мг) у больных с ОА коленных и тазобедренных суставов, а переносимость препарата была лучше. Изучение механизма действия препарата выявило наличие высокой анальгетической, жаропонижающей и небольшой противовоспалительной активности [3,4]. In vitro высокие дозы ацетоминофена ингибировали синтез простагландинов [5]. Ацетоминофен, по видимому, влияет на центральную нервную систему через ингибицию синтеза простагландина Е2 и не оказывает действия на синтез простагландинов в периферических тканях [б].
Дальнейшее изучение ацетоминофена с точки зрения его эффективности, риска развития побочных реакций, а также стоимости лечения, показало преимущество его применения у больных ОА с легким и умеренным болевым синдромом, но было отмечено, что клиническая эффективность выше у нестероидных противовоспалительных препаратов (НПВП) [2]. Кроме того, появились данные о гепатотоксичности и потенциальном повреждающем действии ацетоминофена на почки [7], в связи с чем обращается внимание на то, что при приеме около 60 г алкоголя в день доза ацетоминофена не должна превышать 2,0 г в сутки. Преимущество препарата перед другими анальгетическими средствами заключается в его низкой токсичности для желудочно–кишечного тракта (ЖКТ), однако у больных с выраженным болевым синдромом, с наличием воспаления анальгетики оказываются недостаточно эффективными и требуется назначение НПВП.
НПВП, обладая противовоспалительными, анальгетическими и жаропонижающими свойствами, широко используются для уменьшения боли, синдрома «геля», улучшения функции суставов у больных ОА. Выбор НПВП обычно основывается на мнении врача. В терапевтических дозах клиническая эффективность НПВП примерно одинаковая, однако индивидуальный ответ на препараты широко варьирует [8]. На различия в клинической эффективности также оказывают влияние фармакокинетические, фармакодинамические и метаболические свойства препаратов. И хотя вариабельность ответа можно объяснить (частично) адсорбцией, распределением и метаболизмом препарата, наиболее важная причина разной эффективности лежит, по–видимому, в потенциальных различиях механизма действия лекарств [9].
Большинство НПВП представляют собой слабые органические кислоты и полностью адсорбируются при пероральном приеме, около 95% принятого препарата связывается с сывороточным альбумином, поэтому гипоальбуминемия, особенно у пожилых людей с хроническими соматическими заболеваниями, может приводить к повышению концентрации НПВП в сыворотке и, как следствие этого, к увеличению токсичности. Прием НПВП вместе с пищей может уменьшить его адсорбцию, как например, это показано для напроксена, адсорбция которого в этих условиях снижается на 16%. НПВП метаболизируются в основном в печени и экскретируются с мочой, что необходимо учитывать при назначении этих препаратов больным с нарушениями функции печени или почек. Концентрация препаратов в плазме широко варьирует и зависит от клиренса в почках и скорости метаболизма.
Определенное значение для объяснения различных клинических эффектов имеет время нахождения препаратов в плазме, согласно которому НПВП подразделяются на «коротко– и длительноживущие».
Противоспалительная и анальгетическая активность НПВП связана с уменьшением продукции простагландинов Е. Показано также, что НПВП ингибируют образование простациклина и тромбоксана, оказывая комплексное действие на сосудистую проницаемость и агрегацию тромбоцитов. Противовоспалительное действие НПВП обусловлено, по–видимому, подавлением активности циклооксигеназы (ЦОГ) – основного фермента метаболизма арахидоновой кислоты на пути превращения ее в простагландины. Существуют, по крайней мере, две изоформы ЦОГ. И хотя аминокислотная последовательность их на 60% идентична, они представляют собой продукт двух разных генов. ЦОГ–1 регулирует нормальные клеточные процессы и стимулируется гормонами или факторами роста. ЦОГ–1 экспрессируется на большинстве тканей организма и в различной степени ингибируется всеми НПВП, поэтому многие побочные реакции со стороны желудочно–кишечного тракта объясняются именно этой ингибицией [13].
Другая изоформа, ЦОГ–2, которая обычно не определяется в тканях, экспрессируется при воспалении и также ингибируется всеми существующими НПВП в большей или меньшей степени, а также глюкокортикостероидами [34], что отличает ее от ЦОГ–1.
На основании этих данных была создана новая группа препаратов – специфических ингибиторов ЦОГ–2, к которым относятся целекоксиб и рофекоксиб, примерно в 300 раз более эффективно подавляющие ЦОГ–2 по сравнению с ЦОГ–1 [15]. Клинические исследования при ОА показали, что оба препарата оказывали влияние на боль, сравнимое с действием напроксена, ибупрофена и диклофенака, и почти не оказывали повреждающего действия на слизистую желудочно–кишечного тракта и агрегацию тромбоцитов [16,17,18].
Вместе с тем, накапливаются данные о том, что противовоспалительное и анальгетическое действие НПВП не объясняется только ингибицией ЦОГ. Предполагают, что НПВП ингибируют активацию и хемотаксис нейтрофилов и уменьшают продукцию токсических кислородных радикалов в стимулированных нейтрофилах [5], тормозят активность фактора транскрипции NF–kB, таким образом ингибируя стимуляцию синтетазы оксида азота [20].
Кроме того, НПВП, являясь ингибиторами простагландинов, которые, как предполагают, ингибируют апоптоз (программированная гибель клеток), могут способствовать нормализации жизненного цикла клеток в очаге воспаления [14].
Арахидоновая кислота подвергается действию не только ЦОГ, но и 5– и 12–липооксигеназ. К настоящему времени накапливаются данные о том, что механизм развития НПВП–индуцированных гастропатий может включать альтернативные процессы превращения арахидоновой кислоты в лейкотриены под воздействием 5–липооксигеназы (5–ЛОГ). Это послужило поводом для создания новой группы препаратов, способных ингибировать ЦОГ–1 и ЦОГ–2. Первое исследование такого препарата – ликофелона (200 мг х 2 раза в день) проведено у 148 больных ОА в сравнительном испытании с напроксеном (500 мг х 2 раза в день) и плацебо [19]. Ликофелон оказался равным по эффективности НПВП, исключительно хорошо переносился и не вызывал поражения желудочно–кишечного тракта,
Таким образом, изучение механизмов действия НПВП привело к созданию новой классификации препаратов (табл. 2), основанной на селективности действия в отношении ЦОГ, позволяющей врачу индивидуально подобрать наиболее эффективный и безопасный препарат.
Многочисленные контролируемые исследования свидетельствуют о достоверно более высокой эффективности НПВП по сравнению с плацебо, поэтому при выборе препарата необходимо учитывать его безопасность, влияние на хрящ, а учитывая возраст больных ОА, и наличие большого числа сопутствующей патологии, сочетаемость с другими средствами.
Общие принципы применения НПВП при ОА заключаются в использовании минимальной эффективной дозы, приеме одновременно не более одного НПВП, отмене препарата при отсутствии боли и оценке эффективности лечения через 2–4 недели от начала приема.
При ОА наиболее оптимальными считаются «короткоживущие» препараты: ибупрофен, диклофенак, кетопрофен. Применяемые при ОА дозы препаратов обычно ниже, чем при воспалительных заболеваниях суставов (табл. 3). Для быстрого купирования болевого синдрома назначаются препараты с высокой анальгетической активностью: калиевая соль диклофенака (Раптен рапид). Препарат оказывает стойкий анальгетический эффект значительно быстрее и продолжительнее, чем натриевая форма диклофенака и другие НПВП. Кроме того, препарат обладает минимумом побочных эффектов по сравнению с ибупрофеном и индометацином. Раптен рапид может быть также рекомендован для вводной терапии для купирования боли с последующим переходом на другой анальгетик. Уменьшение болевого синдрома на фоне лечения НПВП отмечается примерно у 60–70% больных ОА. Вместе с тем индивидуальные различия в эффективности НПВП колеблются в широких пределах, поэтому на первое место выходит не только подбор наиболее эффективного препарата (Раптен рапид и др.), но и оценка реальных различий в токсичности препаратов. Побочные реакции, наблюдаемые при лечении НПВП, представлены в таблице 4.
Наиболее клинически значимыми являются побочные реакции со стороны ЖКТ, их возникновение, вероятно, обусловлено местной и системной ингибицией синтеза простагландинов. Спектр поражения ЖКТ довольно широк – от развития эзофагитов до кровотечений и перфораций пептических язв, иногда приводящих к смерти [13]. Приводятся данные о повреждении слизистой тонкой и толстой кишок [23]. Эндоскопические исследования показали, что наиболее часто поражаются препилорический и антральный отделы желудка. Как правило, они протекают бессимптомно, поэтому трудно оценить их истинную распространенность. Факторы риска развития НПВП–гастропатий включают в себя возраст больных старше 60 лет, наличие язвенного анамнеза, прием противоязвенных препаратов по любым причинам, сочетанное использование глюкокортикостероидов, наличие тяжелых сопутствующих заболеваний, например, сердечно–сосудистых [21,22]. На основании многочисленных клинических исследований относительный риск для язвы желудка составляет 4,0–5,0; для язвы 12–перстной кишки – 1,1–1,6 и от 4,5 до 5,0 – для язв желудка с кровотечением, перфорацией или смертельным исходом. «Длительноживущие» НПВП, как например, пироксикам, обладают большей ЖКТ–токсичностью,
Значительно лучшие результаты получены при использовании преимущественно селективных ингибиторов ЦОГ–2: мелоксикама и нимесулида. Отдельные клинические исследования свидетельствуют о сходной со стандартными НПВП эффективности, но более высокой безопасности в отношении поражения ЖКТ.
Применение специфических ингибиторов ЦОГ–2 ассоциируется с достоверным снижением частоты развития язвенного поражения ЖКТ по сравнению с диклофенаком и ибупрофеном. Кроме того, тяжелые гастроэнтерологическне побочные реакции (кровотечения, перфорации) встречаются в 2–3 раза реже при приеме рофекоксиба и целекоксиба. В последние годы постоянно дискутируются вопросы о риске/пользе НПВП при ОА, затратах при гастроэнтерологических побочных реакциях. По–видимому, селективные ингибиторы ЦОГ–2 могут существенно повысить безопасность лечения, особенно у пожилых больных с высокими факторами риска.
При недостаточной эффективности и плохой переносимости НПВП назначаются другие анальгетические препараты. Трамадол – синтетический анальгетик центрального действия, не вызывающий физической и психической зависимости, эффективен при боли различного происхождения. Schnitzer с соавт. [24] показали, что препарат эффективен в отношении болевого синдрома, кроме того, сочетанное применение трамадола с напроксеном позволило снизить дозу последнего. Трамадол применяется при ОА в дозах от 50 до 200 мг в сутки. Сравнительно частые побочные реакции при применении препарата (тошнота, головокружения, запоры и сонливость) можно существенно уменьшить при титровании дозы (в течение 3–х дней, увеличивая дозу по 25 мг).
При изолированном суставном поражении для лечения ОА используются местные средства в виде мазей, кремов на основе НПВП, что позволяет избежать системных побочных реакций, особенно у пожилых, и хондроитин сульфата в сочетании с диметилсульфоксидом (Хондроксид). Создана форма НПВП в виде пластыря, содержащая диклофенак, оказавшаяся эффективнее плацебо в 2–х недельном исследовании у 155 больных с гонартрозом [25], что, возможно, позволит уменьшить потребность в системных препаратах.
Moore с соавт. проанализировали 86 исследований для оценки эффективности и токсичности местных средств для лечения острой и хронической боли, в том числе и при ОА. Авторы заключили, что эти препараты достаточно эффективны и безопасны [26].
У больных гонартрозом при наличии суставного выпота используются внутрисуставные введения кортикостероидов. К сожалению, отдельные аспекты этой терапии остаются противоречивыми (ее относительная эффективность, потенциально повреждающее действие и потенциально структурно–модифицирующее действие), поэтому место длительного применения внутрисуставной кортикостероидной терапии для лечения ОА остается пока не ясным – необходимы длительные двойные слепые исследования. В настоящее время считается, что число внутрисуставных введений в один сустав не должно превышать 3–4–х на протяжении одного года.
Несмотря на то, что НПВП уменьшают боль и воспаление, до сих пор не показано, замедляют ли они прогрессирование ОА и защищают ли хрящ от механического или воспалительного повреждения.
Попытки воздействия на болезнь начинались с изучения факторов риска, таких как ожирение, избыточная нагрузка суставов, и ограничивались рекомендациями по снижению веса и применению различных физических упражнений. В настоящее время ведутся разработки средств, способных замедлить прогрессирование ОА. Спектр изучаемых препаратов довольно широк: от антибиотиков с антиколлагенолитической активностью, гиалуроната и полисахаридов до более сложных препаратов, включающих факторы роста и цитокины. Эти препараты называются структурно–модифицирующими, их роль заключается в способности предотвратить, замедлить, стабилизировать или подвергнуть обратному развитию остеоартритический процесс не только в хряще, но и во всем суставе, рассматриваемом в целом, как орган. В настоящее время нет четких доказательств структурно–модифицирующих свойств для человека ни для одного препарата, но определенные данные получены для некоторых из них.
Хондроитин сульфат (ХС) и глюкозамин сульфат (ГС) – сульфатированные гликозаминогликаны, которые находятся в экстрацеллюлярном матриксе суставного хряща. При пероральном приеме они хорошо адсорбируются и обнаруживаются в высоких концентрациях в полости сустава. Механизм их действия до конца не выяснен. Получены доказательства, что ХС и ГС стимулируют синтез гиалуроновой кислоты и протеогликанов и ингибируют действие протеолитических ферментов, тем самым усиливая анаболические процессы в хряще и подавляя катаболические, что может лежать в основе их структурно–модифицирующего действия. Имеются данные об их способности подавлять образование супероксидных радикалов и синтез оксида азота, что обусловливает, по–видимому, их анальгетический эффект. В процессе экспериментальных исследований in vivo было установлено, что введение ХС перорально или внутримышечно кроликам (с дегенерацией хряща, вызванной химопапаином), значительно повышало содержание протеогликанов хряща по сравнению с контрольными животными, что свидетельствует о том, что ХС защищает хрящ при повреждении и обладает способностью поддерживать ресинтез протеогликанов матрикса [27].
Лечение ХС приводит к значительному уменьшению болевого синдрома, улучшению функциональной способности суставов и позволяет снизить дозу принимаемых НПВП. Препарат обладает прекрасной переносимостью, практически не вызывая побочных эффектов [28,29,30]. Мета–анализ двойных слепых плацебо–контролируемых исследований ХС у 372 и 404 больных гон– и коксартрозом подтвердил эффективность препарата по сравнению с плацебо и НПВП [31,32]. Исследование, проведенное в Швейцарии [33] в течение года, затронуло вопрос о наличии у ХС структурно–модифицирующих свойств, поскольку препарат оказывал стабилизирующее влияние на ширину суставной щели и метаболические процессы в субхондральной кости и хряще, а тем самым, по–видимому, и на течение заболевания. На ежегодном Европейском конгрессе ревматологов, проходившем в Стокгольме (2002 г.), были доложены результаты длительного, в течение 2–х лет, применения ХС (800 мг/сутки) у 300 больных с гонартрозом, которые показали способность препарата замедлять прогрессирование ОА [34].
Более ранние краткосрочные исследования выявили эффективность ГС по сравнению с плацебо и НПВП [35,36]. Недавно длительное (в течение 3–х лет) применение ГС (1500 мг/сутки) у 212 больных с гонартрозом подтвердило не только симптоматическое действие препарата (снижение функционального индекса WOMAC), но и его способность замедлять рентгенологическое прогрессирование, которое оценивалось по изменению ширины суставной щели [37].
Относительно недавно стали появляться работы по сочетанному применению этих препаратов. Так, двойное слепое плацебо–контролируемое изучение в течение 16 недель комбинации глюкозамин гидрохлорида (1500 мг/сутки) и ХС (1200 мг/сутки) у 34 мужчин с гонартрозом и болями в нижнем отделе спины показало значительное уменьшение болей в суставах, но не в спине [38]. В другом исследовании сообщалось о сочетанной терапии при ОА височно–челюстных суставов [39]. Вместе с тем многообещающие данные по структурно–модифицирующему действию ХС и ГС требуют дальнейшего подтверждения в длительных контролируемых исследованиях.
Гиалуронат (ГЛ) представляет собой полисахарид, состоящий из длинной цепи дисахаридов, продуцируется в суставах хондроцитами и синовиальными клетками. В настоящее время используются 2 препарата ГЛ, вводимые внутрисуставно: низкомолекулярный (м.в. 500000–730000 дальтон) и высокомолекулярный (м.в. 6000000 дальтон). Клиническое применение ГЛ было обусловлено исследованиями синовиальной жидкости при ОА, показавшими значительное изменение ее реологических свойств по сравнению с синовиальной жидкостью здорового сустава. Поэтому предполагали, что введение ГЛ восстановит защитные и так называемые удар–адсорбирующие свойства синовиальной жидкости [40]. Однако длительный клинический эффект нельзя было объяснить только этими причинами, поскольку период полувыведения препарата составлял 2–8 дней. На основании дальнейших исследований было высказано предположение, что механизм действия препарата связан с ингибицией воспалительных медиаторов (цитокинов и простагландинов), стимуляцией анаболических и замедлении катаболических процессов в матриксе хряща [41,42].
Высокомолекулярный ГЛ [43] при сравнении 3 еженедельных инъекций с НПВП или с комбинацией НПВП и ГЛ оказался эффективнее НПВП, и, вероятно, может использоваться вместо или вместе с НПВП. При ретроспективном изучении 336 больных с гонартрозом хороший ответ наблюдался у 76% [44] при сохранении эффекта терапии в среднем до 8 месяцев. Местные побочные реакции наблюдались у 8% больных, от незначительных до развития острого синовита с выпотом, требовавшего внутрисуставного введения кортикостероидов или короткого курса НПВП.
Сравнительное исследование высоко– и низкомолекулярного ГЛ у 70 больных ОА коленных суставов (по 3 еженедельных инъекции) выявило более высокую эффективность первого препарата, при равном небольшом числе побочных местных реакций [45]. Вместе с тем, применение высоко– и низкомолекулярного ГЛ требует дальнейшего исследования для лучшего определения места этой терапии и особенно – оценки влияния длительного применения на замедление или обратное развитие деградации хряща. В настоящее время ГЛ определяется как средство, модифицирующее симптомы болезни, и рекомендуется для больных, которые не отвечают на другие виды терапии или не переносят НПВП.
Подтвердить структурно–модифицирующие свойства препаратов у человека чрезвычайно трудно, поскольку ОА – обычно очень медленно прогрессирующее заболевание. Необходимо принимать во внимание, что, возможно, любое эффективное в отношении симптомов болезни, средство может потенциально иметь структурно–модифицирующие свойства. Аналогичным образом, известно, что любой препарат со структурно–модифицирующими свойствами обладает небольшим и, как правило, отсроченным по времени действием на симптомы болезни. Кроме того, методы исследования прогрессирования заболевания ограничены, поэтому клиническое испытание структурно–модифицирующих препаратов представляет собой сложную задачу. Для демонстрации структурно–модифицирующих свойств в клинических испытаниях часто используют оценку исходов ОА по рентгенограммам коленных суставов; развиваются методы, способные оценить поверхность и объем хряща.
Некоторое преимущество в оценке эффективности лечения ОА имеют препараты, модифицирующие симптомы заболевания. Тем не менее лечение больных ОА представляет собой сложную задачу. Во–первых, при гетерогенном заболевании с непредсказуемым течением, таком как ОА, важно помнить, что лечение не должно приносить вред больному. Во–вторых, трудно создать единый алгоритм лечения, так как индивидуальные различия течения болезни также велики. Поэтому лечение больных ОА следует рассматривать с учетом оценки пользы/риска от проводимой терапии.
Важным моментом в начале лечения является характеристика болевого синдрома в плане наличия или отсутствия воспалительных изменений. Допущение о том, что значительная часть больных имели только болевой синдром без признаков воспаления, легло в основу создания алгоритма лечения больных ОА коленных и тазобедренных суставов, предложенного Американской коллегией ревматологов в 1995 году [10,11]. При недостаточной эффективности нефармакологических методов лечения в качестве препаратов «первой линии» рекомендовались анальгетики (ацетоминофен 4,0 в сутки), далее – местная терапия (кроме ОА тазобедренных суставов), низкие дозы НПВП или другие анальгетики, такие как трамадол, а затем терапевтические дозы НПВП, внутрисуставные введения глюкокортикостероидов, гиалуроновая кислота, сульфатированные гликозаминогликаны. Для больных с высоким риском развития желудочно–кишечных осложнений назначалось профилактическое лечение мизопростолом, ингибиторами протонного насоса, высокими дозами антагонистов Н2–гистаминовых рецепторов.
И хотя эти рекомендации не потеряли своей актуальности, накапливаются данные о необходимости более раннего назначения противовоспалительной терапии [12]. Кроме того, ацетоминофен оказался не совсем безопасным средством, как сообщалось в ранних работах, a Pincus с соавт. [2] отметили большую эффективность НПВП по сравнению с простыми анальгетиками.
Значительно более высоким отношением польза/риск по сравнению с традиционными НПВП обладают специфические ингибиторы ЦОГ–2. Эти препараты, по–видимому, могут рассматриваться в качестве препаратов «первой линии», в частности, у больных с умеренным и тяжелым болевым синдромом, с и без признаков воспаления, при наличии припухлости сустава и суставного выпота. Больным с недостаточной эффективностью и плохой переносимостью этих препаратов проводить лечение нужно традиционными НПВП с обязательным сочетанием с профилактической терапией, особенно у тех больных, кто имеет факторы риска развития нежелательных явлений. Необходимо учитывать, что большинство больных старше 60 лет имеют, по крайней мере, один фактор риска развития осложнений.
При наличии большого выпота в суставе состояние значительно облегчается внутрисуставным введением стероидов (введение в тазобедренный сустав нежелательно), но не чаще 1–2 раз в год.
Введение гиалуроновой кислоты особенно показано, когда неэффективно лечение анальгетиками и НПВП, также есть противопоказания для их приема.
Весьма перспективными могут оказаться сульфатированные глюкозаминогликаны не только из–за их эффективности и, возможно, структурно–модифицирующего действия, но и за счет их хорошей переносимости, что не требует врачебного мониторинга в отличие от приема НПВП.
Вероятно, время лечения ОА монотерапией уходит в прошлое, а расширение и углубление знаний о патогенезе заболевания, механизмах действия препаратов на разные патогенетические звенья болезни позволяет надеяться, что скоро будут разработаны схемы лечения, новые препараты, которые будут способны изменить естественное течение ОА.
Литература:
1. Bradley ID, Brandt KD, Katz BP et al. Comparison of an antiinflammatory dose of ibuprofen. an analgesic dose of ibuprofen, and acetaminophen in the treatment of patients with osteoarthritis of the knee. N Engi J Med. 1991. 325:87–91.
2. Pincus Т, Callahan LF, Wolfe F et al. Arthrotec compared to acetominophen (ACTA): clinical trial in patients with osteoarthritis (OA) of the hip or knee. Arthritis Rheum 1999. 42–.S404.
3. Towheed ТЕ, Hochberg MC. A systematic review of randomized controlled trials of pharmacological therapy in osteoarthritis of the knee. Semin Arthritis Rheum 1997, 27:755–70.
4. Towheed ТЕ, Hochberg MC. A systematic review of randomized controlled trials of pharmacological therapy in osteoarthritis of the hip. J Rheumatol 1997, 24:349–57.
5. Cryer В. Feldman M. Cyclooxygenase–1 and cyclooxygenase–2 selectivity of widely used nonsteroidal anti–inflammatory drugs. Am J Med 1998, 104:413–21.
6. Simon LS. Mffls JA. Drug therapy: nonsteroidal antiinflammatory drugs. N Engi J Med. 1980, 302:1179–85,1237–43.
7. Schiodt FV, Rjehling FA, Casey DL, Lee WM. Acetominophen toxicity m an urban country hospital. N Engi J Med. 1997, 337:1112–17.
8. Phiffips AC, Simon LS. NSATDs and the elderiy: toxicity and the economic implications. Drugs Aging 1997, 10:119–30.
9. Simon LS, Stand V. Clinical response to nonsteroidal antiinflammatory drugs. Arthritis Rheum 1997, 40:1940–43.
10. Hochberg MC, Altaian RD, Brandt KD et al. Guidelines for medical management of osteoarthritis. L Osteoarthritis of the hip. Arthritis Rheum 1995, 38:1535–40.
11. Hochberg MC, Altman RD, Brandt KD et al. Guidelines for medical management of osteoarthritis. П. Osteoarthritis of the knee. Arthritis Rheum 1995, 38:1541–46.
12. Altman RD, Hochberg MC, Moskowitz RW, Schnitzer TJ. Recommendations for the medical management of osteoarthritis of me Ыр and knee. Arthritis Rheum 2000, 43:1905–15.
13. Wolfe MM, Lichtenstein DR, Singh G. Gasrtointestinal toxicity of me nonsteroidal antiinflammatory drugs. N Engi J Med. 1999, 340:1888–99.
14. Crofford LJ, Lipsky PE, Brooks P et al. Basic biology and clinical application of cyclooxygenase–2. Arthritis Rheum 2000, 43:4–13.
15. Lipsky PE. Abramson SB, Croiford LJ et al. The classification of cyclooxygenase inhibitors. J Rheumatol 1998, 25:2298–2303.
16. Laine L, Haper S, Simon Т et al. A randomized trial comparing the effect ofrofecoxib, a cyclooxygenase–2 specific inhibitor, with that of ibuprofen on gastroduodenal mucosa of patients with osteoarthritis. Gastroenterology 1999, 117:776–83.
17. Hawkey CJ. COX–2 inhibitors. Lancet 1999, 353:307–14.
18. Bensen WG. Flechthner JJ, McMillen Л et al. Treatment of osteoarthritis with celecoxib, a cyclooxygenase–2 specific inhibitor: a randomized controlled trial. Mayo Clin Proc 1999, 74:1095–1105.
19. Reginster J, Bias P, Buchner A. First clinical results oflicofelone (ML3000), an inhibitor of COX–1, COX–2 and %–LOX, for the treatment of osteoarthritis. Ann Rheum Dis 2002. 61 (Suppl):THU0189,pll6.
20. Pelletier IP. The influence of tissue cross–talking on OA progression: role of nonsteroidal antiinflammatoly drugs. Osteoarthritis Cartilage 1999, 7:374–6.
21. Garcia Rodriguerz LA. Nonsteroidal antimflammatory drugs, ulcers and risk: a collaborative meta–analysis. Semin Arthritis Rheum 1997, 26 (suppl):16–20.
22. Simon LS, Hatoum HT, Bittman RM et al. Risk factors for serious nonsteroidal–mduced gastrointestinal complications: regression analysis of the MUCOSA trial. Fam Med 1996. 28:202–208.
23. Wilcox CM, Alexander LN, Cotsonis GA, Clark WS. Nonsteroidal antiinflammatory drugs are associated with both upper and lower gastrointestmal bleeding. Dig Dis Sci 1997, 42:990–97.
24. Schnitzer TJ, Kaniin N, Olson WH. Tramadol allows reduction of naproxen dose among patients with naproxen–responsive osteoarthritis pain: a randomized, double blind, placebo controlled trial. Arthritis Rheum 1999, 42:1370–77.
25. Gallacchi G, Marcolongo R. Pharmacokmetics of diclofenac hydroxyethylpyrrolidine plasters in patients with monolateral knee joint effusion. Drugs Exp Clin Res 1993: 19:95–7.
26. Moore RA, Tramer MR, Carroll D et al. Quantitative systematic review of topically applied non–steroidal anti–inflammatory drugs. BMJ, 1998, 316:333–38.
27. Uebelhart D, Thonar E, Zhang J, Williams J. Protective effect of exogenous 4.6–sulfate in the acute degradation of articular cartilage in the rabbits/ Osteoarthritis Cartilage 1998, 6 (supplement A):6–13.
28. Morreale P, Manopulo R, Galati M et al. Comparison of the anti–inflammatory efficacy of chondroitin–sulfate and diclofenac sodium in patients with knee osteoarthritis. J Rheumatol, 1996.23:1385–91.
29. Uebelhart D, Knussel 0, Theiler R. Efficacy and tolerability of oral chondroitin–sulfate in painful knee osteoarthritis: a double–blind, placebo–controfled, multicentre 6–month trial. Osteoarthritis Cartilage, 1999,7, Suppi A, abstr 144.
30. Алексеева Л.И., Беневоленская Л.И., Насонов Е.Л., Чичасова Н.В., Карякин А.Н.. Структум (хондроитин сульфат) – новое средство для лечения остеозртроза (О А) // Тер. Архив 1999, №5, с. 51–53.
31. Leeb BF, Schweitzer H, Montag K, Smolen JS. A meta–analysis of chondroitmsulfate m the treatment of osteoarthritis. Osteoarthritis Cartilage, 1999, 7, Suppi A. abstr 130.
32. Eugenio–Sarmiento RM, Manapat BHD, Salido EO, The efficacy of chondroitin–sulfate in the treatment of knee osteoarthritis: a meta–analysis. Osteoarthritis Cartilage, 1999, 7, Suppi A, abstr 139.
33. Uebelhart, Thonar E, Delmas P et al. Effects of oral chondroitin sulfate on the progression of knee osteoarthritis: a pilot study. Osteoarthritis Cartilage 1998; 6 (suppl A): 39–46.
34. Michel BA, Bruhlmann P, Stuck! G, Uebelhart D. Chondroprotection through Chondrosutf: the Zurich study. Ann Rheum Dis 2002, 61 (Supp I): 116.
35. Muller–Fasbender H, Bach G, Haase W et al. Glucosamine sulfate compared to ibuprofen m osteoarthritis of the knee. Osteoarthritis Cartilage, 1994,2:61–69.
36. Noack W, Fisher M, Forster KK et al. Glucosamine sulfate in osteoarthritis of the knee. Osteoarthritis Cartilage, 1994,2:51–59.
37. Register J–Y, Deroisy R, Paul I et al. Glucosamine sulfate significantly reduced progression of knee osteoarthritis over 3 years: a large, randomized, placebo–controlled, double–blind, prospective trial. Arthritis Rheum 1999, 42 (suppl):S402.
38. Leffler CN, Phiffipi AF, Lefner SG et al. Glucosamine, chondroitin and magnaese ascorbate for degenerative joint disease of the knee or low back pain: a randomized, double–blind, placebo–controlled pilot study. Mil.Med 1999, 164:85–91.
39. Shanklad WE, The effects of glucosamine and chondroitin sulfate on osteoarthritis of the TMJ: a preliminary report of 50 patients. Cranio 1998, 16:230–235.
40. Balazs EA, Denlinger JL. Viscosupplementation: a new cocept in the treatment of OA. J Rheumatol 1993, Suppl39:3–9.
41. Yasui T, Akatsuka M, Tobetto К et al. The effect ofhyaluronan on interleukin–2 induced prostaglandin–E2 production in human osteoarthritis svnovial cells. Agents Action 1992, 37:155–6.
42. Ghosh P. The role of hyaluronic acid (hyaluronan) m health and disease: interactions with cells, cartilage and components of the synovial fluid. Clin Exp Rheumatol 1994, 12:75–82.
43. Adams ME, Atkinson MH, et al. The role of Viscosupplementation with hylan G–F 20 (Synvisc) in the treatment of osteoarthritis of the knee: a Canadian multicentre trial comparing hylan G–F 20 alone, hylan G–F 20 with non–steroidal anti–inflammatory drugs (NSAIDs) and NSATOs alone. Osteoarthritis Cartilage, 1995, 3:213^225.
44. Lussier AJ, Cividino AA, McFariane CA et al. Viscosupplementanon with hylan for the treatment ofosteoarthritis: findings from clinical practice in Canada. J Rheumatol, 1996, 23:1579–1585.
45. Wobig M, Bach G, Beks P, et al. The role of elastoviscosity in the efficacy of viscosupplementation for osteoarthritis of the knee: a comparison of hylan G–F 20 and a lower– molecular–weight hyaluronan. Clin Ther, 1999 Sep; 21(9): 1549–1562.
.
Гонартроз — причины, симптомы, лечение и т.д.
В обиходе артроз часто путают с артритом. Артрит — это общий термин для воспалений заболеваний суставов . К ним относятся, например, артрит, связанный с инфекцией, и ревматоидный
артрит. Гонартроз также может иногда вызывать воспаление. В этом случае это также будет называться артритом.
Причины гонартроза
В большинстве случаев гонартроз — это возрастное износ хряща в коленном суставе.Основная причина такого износа заключается в том, что способность тела восстанавливать мелкие повреждения со временем снижается.
Артроз также может возникать в более молодом возрасте из-за генетической предрасположенности или перегрузки коленного сустава. Связанные со стрессом причины гонартроза включают:
- ожирение
- неправильное положение ног (например, колени, кривые ноги)
- травмы колена (например, разрыв мениска)
- постоянный стресс в повседневной жизни (например, мастера)
- высокий- ударные виды спорта (например,грамм. футбол)
Люди с генетической предрасположенностью к гонартрозу не обязательно страдают какими-либо жалобами. Предрасположенность может существовать всю жизнь, не вызывая симптомов. Причины возникновения гонартроза чрезвычайно разнообразны. Иногда нет конкретного причина. В этом случае заболевание называется идиопатическим гонартрозом.
Симптомы гонартроза
Гонартроз обычно проявляется болью и ограничением движений коленного сустава, но симптомы не обязательно должны быть заметными.На ранних стадиях заболевания больные обычно ощущают лишь легкую боль при движении. коленка. Боль часто проходит через несколько шагов.
Если гонартроз не проходит, весь хрящевой материал в какой-то момент разрушен. Незащищенные тогда концы костей будут тереться друг о друга. В некоторых случаях это может привести к серьезным ограничениям движений и боли. Эта боль может сохраняться в течение длительного времени и может не иметь прямого отношения к движению.
В связи с тем, что симптомов могут сильно различаться , очень сложно определить прогрессирование.В то время как некоторые пациенты никогда не испытывают боли и страдают лишь от незначительных ограничений движения, другие могут страдать от сильной боли и ограничений. У других симптомы заболевания исчезают сами по себе через некоторое время. Гонартроз не обязательно должен вызывать проблемы даже у человека с генетической предрасположенностью.
Уменьшение хряща в коленном суставе из-за артроза не может быть отменено, но пострадавший может очень эффективно влиять на скорость прогрессирования заболевания и проявление симптомов.Среди прочего, снижение ожирения и Сохранение физической активности может укрепить мышцы колена и значительно замедлить прогрессирование заболевания, тем самым уменьшив ограничения движений и боль.
Лечение гонартроза | Медицинский центр Герцлии
Медицинский центр Герцлии — ведущая частная больница Израиля, предлагающая эффективное лечение гонартроза пациентам со всего мира. Специалисты больницы применяют инновационные методики диагностики и лечения заболеваний суставов.Благодаря непревзойденному уровню знаний и неограниченным технологическим возможностям HMC завоевала репутацию лучшей больницы, выполняющей ортопедические операции в Израиле.
Что такое гонартроз?
Остеоартроз колена, известный как гонартроз, представляет собой дегенеративное повреждение хрящевой ткани, покрывающей поверхность костей. Слой хряща играет важную роль в предотвращении трения и обеспечении плавного движения сустава. Нарушение его целостности неизбежно приводит к хроническим необратимым процессам, уменьшая подвижность сустава и вызывая мучительные боли.Гонартроз — основная причина хирургической замены коленного сустава.
Что вызывает развитие гонартроза?
Установление причин, вызвавших повреждение внутрисуставного хряща, влияет на последующую стратегию лечения. Среди основных причин гонартроза наиболее частыми являются следующие:
- Возрастное ухудшение коленного сустава.
- Последствия физического напряжения или травмы (гонартроз, развивающийся в молодом возрасте, часто возникает из-за профессионального спортивного заболевания).
- Избыточная масса тела и как следствие постоянная нагрузка на колени.
- Острые и хронические воспалительные процессы коленного сустава.
- Врожденная или приобретенная деформация стопы, приводящая к неправильному распределению весовой нагрузки на сустав
Симптомы гонартроза
Основным симптомом, побуждающим пациентов обращаться за медицинской помощью, является боль, возникающая во время физических упражнений, подъема тяжелых грузов или подъема или спуска по лестнице. Боль прогрессирует, а в тяжелых случаях даже сопровождает пациентов в покое.Подвижность сустава значительно снижается. Во время движения возникает характерный хруст. Вторичный воспалительный процесс приводит к отеку колена. Специалисты HMC рекомендуют незамедлительно обратиться за медицинской помощью, прежде чем повреждение станет необратимым и потребует хирургического лечения или полной замены коленного сустава.
Диагностика гонартроза в Израиле
Диагноз «остеоартроз коленного сустава» ставится на основании характерной клинической картины и данных анамнеза. Во время осмотра специалист-ортопед определяет объем движений в суставе.Также необходимо рентгенологическое исследование, так как оно позволяет диагностировать характерные изменения сустава (деформация и сужение суставной щели, наличие остеофитов, утолщение суставных поверхностей). МРТ и эндоскопическая артроскопия используются для дифференциальной диагностики.
Инновационное лечение гонартроза
Современное состояние ортопедии в Израиле позволяет эффективно лечить признаки гонартроза как в легких, так и в тяжелых формах.Ортопеды HMC успешно применяют широкий спектр современных методик, среди которых наиболее заметными являются:
- Физиотерапия для восстановления подвижности сустава и уменьшения боли.
- Обезболивающее.
- Местное и систематическое применение противовоспалительных препаратов, эффективных при острых стадиях заболевания.
- Коррекция распределения нагрузки на суставы при деформациях стопы или голени.
- Минимально инвазивное хирургическое лечение (артроскопия).Эта современная эндоскопическая техника позволяет исключить развитие разрушения хряща за счет удаления поврежденных участков и патологических образований кости (остеофитов), а также укрепления связочного аппарата.
- Операция по замене коленного сустава в случае неудачного консервативного и малоинвазивного лечения.
Индивидуальный подход специалистов HMC к лечению заболеваний коленного сустава гарантирует качественное медицинское обслуживание и отличные клинические результаты.
Рассмотрение подходов, фармакологическое лечение, изменение образа жизни, физическая / профессиональная терапия и другие нефармакологические меры
Информационный бюллетень по остеоартриту. Центры по контролю и профилактике заболеваний. Доступно на https://www.cdc.gov/arthritis/basics/osteoarthritis.htm. 10 января 2019 г .; Доступ: 7 февраля 2020 г.
Kotlarz H, Gunnarsson CL, Fang H, Rizzo JA. Страховая компания и наличные расходы на остеоартрит в США: данные национального опроса. Rheum артрита . 2009 Декабрь 60 (12): 3546-53. [Медлайн]. [Полный текст].
Бакленд-Райт C, Verbruggen G, Haraoui PB. Визуализация: радиологическая оценка остеоартрита кисти. Хрящевой артроз . 2000. 55-6.
Jewell FM, Watt I, Doherty M. Простые рентгенографические признаки остеоартрита. Брандт К.Д., Доэрти М., Ломандер Л.С., ред. Остеоартроз . Нью-Йорк, Нью-Йорк: издательство Оксфордского университета; 1998. 217-37.
Recht MP, Kramer J, Marcelis S, Pathria MN, Trudell D, Haghighi P, et al. Аномалии суставного хряща коленного сустава: анализ доступных методов МРТ. Радиология . 1993 Май. 187 (2): 473-8. [Медлайн].
Хантер DJ. Расширенная визуализация при остеоартрите. Булл Нью-Йоркский университет Госпиталь Дис . 2008. 66 (3): 251-60. [Медлайн].
Keen HI, Wakefield RJ, Conaghan PG. Систематический обзор ультразвукового исследования при остеоартрите. Энн Рум Дис . 2009 Май. 68 (5): 611-9. [Медлайн].
Recht MP, Goodwin DW, Winalski CS, Белый LM. МРТ суставного хряща: пересматривая текущее состояние и будущие направления. AJR Am J Рентгенол . 2005 Октябрь 185 (4): 899-914. [Медлайн].
Kraus VB, McDaniel G, Worrell TW, Feng S, Vail TP, Varju G, et al. Связь сцинтиграфических аномалий костей с деформацией колена и болью. Энн Рум Дис .2009 ноябрь 68 (11): 1673-9. [Медлайн].
Felson DT, Zhang Y, Anthony JM, Naimark A, Anderson JJ. Снижение веса снижает риск симптоматического остеоартрита коленного сустава у женщин. Фрамингемское исследование. Энн Интерн Мед. . 1992 г., 1. 116 (7): 535-9. [Медлайн].
Kraeutler MJ, Mitchell JJ, Chahla J, McCarty EC, Pascual-Garrido C. Внутрисуставная имплантация мезенхимальных стволовых клеток, Часть 1: Обзор литературы по профилактике постменискэктомического остеоартрита. Orthop J Sports Med . 2017 19 января. 5 (1): 2325967116680815. [Медлайн]. [Полный текст].
Лафлин Дж. Генетическая эпидемиология первичного остеоартрита человека: современное состояние. Эксперт Рев Мол Мед . 2005 24 мая. 7 (9): 1-12. [Медлайн].
Dagenais S, Garbedian S, Wai EK. Систематический обзор распространенности рентгенологического первичного остеоартроза тазобедренного сустава. Clin Orthop Relat Res . 2009 Март 467 (3): 623-37. [Медлайн].[Полный текст].
Ли П., Руни П.Дж., Старрок Р.Д., Кеннеди А.С., Дик В. Этиология и патогенез остеоартроза: обзор. Семенной ревматический артрит . 1974 Весна. 3 (3): 189-218. [Медлайн].
Мюррей РО. Этиология первичного остеоартроза тазобедренного сустава. Br J Радиол . 1965, ноябрь 38 (455): 810-24. [Медлайн].
Radin ER, Paul IL, Rose RM. Патогенез первичного остеоартроза. Ланцет . 1972 24 июня. 1 (7765): 1395-6. [Медлайн].
Шарма Л. Эпидемиология остеоартроза. Московиц Р.В., Хауэлл Д.С., Альтман, Р.Д. и др., Ред. Остеоартроз . 3-е изд. 2001. 3-27.
Вейс Э., Вербрюгген Г. Эволюция и прогноз остеоартроза. Reginster JY, Pelletier JP, Martel-Pelletier J, et al, eds. Остеоартроз . 1999. 312-3.
Valderrabano V, Horisberger M, Russell I, Dougall H, Hintermann B.Этиология артроза голеностопного сустава. Clin Orthop Relat Res . 2009 Июль 467 (7): 1800-6. [Медлайн]. [Полный текст].
Jewell FM, Watt I, Doherty M. Простые рентгенографические признаки остеоартрита. Брандт К.Д., Доэрти М., Ломандер Л.С., ред. Остеоартроз . Нью-Йорк, Нью-Йорк: издательство Оксфордского университета; 1998. 217-37.
Манкин HJ. Реакция суставного хряща на травму и остеоартроз (первая из двух частей). N Engl J Med .1974 12 декабря. 291 (24): 1285-92. [Медлайн].
Miller EJ, Van der Korst JK, Sokoloff L. Коллаген суставного и реберного хряща человека. Rheum артрита . 1969 12 (1): 21–9 февраля. [Медлайн].
Фадке К. Регуляция метаболизма хондроцитов в суставном хряще — гипотеза. Дж. Ревматол. . 1983 декабрь 10 (6): 852-60. [Медлайн].
Resnick D, Niwayama G. Дегенеративное заболевание экстраспинальной локализации.Резник Д., изд. Диагностика заболеваний костей и суставов . 3-е изд. 1995. 1263-1371.
Пул AR. Введение в патофизиологию остеоартроза. Передняя панель Biosci . 1999 15 октября. 4: D662-70. [Медлайн].
van Baarsen LG, Lebre MC, van der Coelen D, Aarrass S, Tang MW, Ramwadhdoebe TH. Неоднородный паттерн экспрессии интерлейкина 17A (IL-17A), IL-17F и их рецепторов в синовиальной оболочке ревматоидного артрита, псориатического артрита и остеоартрита: возможное объяснение отсутствия ответа на терапию анти-IL-17? Arthritis Res Ther . 2014. 16 (4): 426. [Медлайн].
Краснокутский С., Ошинский С., Аттур М., Ма С., Чжоу Х., Чжэн Ф. и др. Уровни уратов в сыворотке предсказывают сужение суставной щели у пациентов без подагры с медиальным остеоартритом коленного сустава. Ревматический артрит . 2017 июн.69 (6): 1213-1220. [Медлайн]. [Полный текст].
Hoff P, Buttgereit F, Burmester GR, Jakstadt M, Gaber T, Andreas K и др. Синовиальная жидкость при остеоартрите активирует провоспалительные цитокины в первичных хондроцитах человека. Инт Ортоп . 2013 Январь 37 (1): 145-51. [Медлайн]. [Полный текст].
Радин Э.Л., Пол ИЛ. Реакция суставов на ударную нагрузку. I. Износ in vitro. Rheum артрита . 1971 май-июнь. 14 (3): 356-62. [Медлайн].
Burkitt HG, Stevens A, Lowe JS. Система скелета. Основы гистопатологии . 3-е изд. Нью-Йорк, Нью-Йорк: Черчилль Ливингстон; 1996. 260.
Хамерман Д. Биология остеоартрита. N Engl J Med . 1989 18 мая. 320 (20): 1322-30. [Медлайн].
Hartmann C, De Buyser J, Henry Y, Morère-Le Paven MC, Dyer TA, Rode A. Ядерные гены контролируют изменения в организации митохондриального генома в тканевых культурах, полученных из незрелых зародышей пшеницы. Карр Генет . 1992 Май. 21 (6): 515-20. [Медлайн].
Howell DS. Патогенез остеоартроза. Am J Med . 1986, 28 апреля. 80 (4B): 24-8.[Медлайн].
Буллоу PG. Геометрия диартродиальных суставов, ее физиологическое состояние и возможное значение возрастных изменений в распределении геометрии и нагрузки и развитии остеоартрита. Clin Orthop Relat Res . 1981 Май. 61-6. [Медлайн].
Aigner T, Rose J, Martin J, Buckwalter J. Теории старения первичного остеоартрита: от эпидемиологии до молекулярной биологии. Омоложение .2004 Лето. 7 (2): 134-45. [Медлайн].
OUTERBRIDGE RE. Этиология хондромаляции надколенника. J Bone Joint Surg Br . 1961 г., ноябрь 43-B: 752-7. [Медлайн].
Zgoda M, Paczek L, Bartlomiejczyk I, Sieminska J, Chmielewski D, Górecki A. Возрастное снижение активности коллагеназы в головке бедренной кости у пациентов с остеоартрозом тазобедренного сустава. Clin Rheumatol . 2007 26 февраля (2): 240-1. [Медлайн].
Reyes C, Leyland KM, Peat G, Cooper C, Arden NK, Prieto-Alhambra D.Связь между избыточным весом и ожирением и риском клинически диагностированного остеоартрита колена, бедра и кисти: популяционное когортное исследование. Ревматический артрит . 2016 августа 68 (8): 1869-75. [Медлайн].
Felson DT, Anderson JJ, Naimark A, Walker AM, Meenan RF. Ожирение и остеоартроз коленного сустава. Фрамингемское исследование. Энн Интерн Мед. . 1 июля 1988 г. 109 (1): 18-24. [Медлайн].
Goulston LM, Kiran A, Javaid MK, et al.Предсказывает ли ожирение боль в коленях у женщин в течение четырнадцати лет независимо от рентгенологических изменений? Центр по уходу за артритом (Хобокен) . 2011 Октябрь 63 (10): 1398-406. [Медлайн].
Hurley MV. Роль мышечной слабости в патогенезе остеоартроза. Rheum Dis Clin North Am . 1999 Май. 25 (2): 283-98, vi. [Медлайн].
Felson DT. Факторы риска остеоартрита: понимание уязвимости суставов. Clin Orthop Relat Res .2004 окт. S16-21. [Медлайн].
Williams MF, London DA, Husni EM, Navaneethan S, Kashyap SR. Диабет 2 типа и остеоартрит: систематический обзор и метаанализ. J Осложнения диабета . 2016 июл.30 (5): 944-50. [Медлайн].
Jeon OH, Kim C, Laberge RM, Demaria M, Rathod S, Vasserot AP и др. Местное очищение от стареющих клеток ослабляет развитие посттравматического остеоартрита и создает прорегенеративную среду. Нат Мед . 2017 июня 23 (6): 775-781. [Медлайн]. [Полный текст].
de Boer TN, van Spil WE, Huisman AM, Polak AA, Bijlsma JW, Lafeber FP, et al. Адипокины сыворотки при остеоартрозе; сравнение с контролем и взаимосвязь с местными параметрами синовиального воспаления и повреждения хряща. Хрящевой артроз . 2012 20 августа (8): 846-53. [Медлайн].
Андерсон Д.Д., Чубинская С., Гилак Ф., Мартин Дж. А., Огема Т.Р., Олсон С.А. и др.Посттравматический остеоартрит: лучшее понимание и возможности раннего вмешательства. Дж. Ортоп Рес . 2011 июн.29 (6): 802-9. [Медлайн]. [Полный текст].
Фелсон Д.Т., Ниу Дж., Гросс К.Д., Энглунд М., Шарма Л., Кук Т.Д. и др. Смещение вальгуса является фактором риска заболеваемости и прогрессирования латерального остеоартрита коленного сустава: результаты исследования MOST и инициативы по остеоартриту. Rheum артрита . 2012 30 ноября. [Medline].
Вальдес А.М., Спектор ТД.Генетическая эпидемиология остеоартроза тазобедренного и коленного суставов. Нат Ревматол . 2011 7 января (1): 23-32. [Медлайн].
Felson DT. Развитие клинического понимания остеоартрита. Arthritis Res Ther . 2009. 11 (1): 203. [Медлайн]. [Полный текст].
Поллард Т.С., Батра Р.Н., судья А, Уоткинс Б., МакНалли Э.Г., Гилл Х.С. и др. Генетическая предрасположенность к наличию и 5-летнему клиническому прогрессированию остеоартроза тазобедренного сустава. Хрящевой артроз . 2012 май. 20 (5): 368-75. [Медлайн].
Вальдес А.М., Спектор ТД. Клиническая значимость генетической предрасположенности к остеоартриту. Best Practices Clin Rheumatol . 2010 24 февраля (1): 3-14. [Медлайн].
Джеффрис М.А., Доника М., Бейкер Л.В., Стивенсон М.Э., Аннан А.С., Хамфри МБ. Полногеномное исследование метилирования ДНК выявляет значительные эпигеномные изменения в остеоартрозном хряще. Ревматический артрит .2014 Октябрь 66 (10): 2804-15. [Медлайн].
Chang SC, Hoang B, Thomas JT, Vukicevic S, Luyten FP, Ryba NJ, et al. Морфогенетические белки хрящевого происхождения. Новые члены суперсемейства трансформирующих факторов роста-бета преимущественно экспрессируются в длинных костях во время эмбрионального развития человека. Дж. Биол. Хим. . 1994 11 ноября. 269 (45): 28227-34. [Медлайн].
Lin K, Wang S, Julius MA, Kitajewski J, Moos M Jr, Luyten FP. Богатый цистеином вьющийся домен Frzb-1 необходим и достаточен для модуляции передачи сигналов Wnt. Proc Natl Acad Sci U S A . 1997, 14 октября. 94 (21): 11196-200. [Медлайн]. [Полный текст].
Чепмен К., Такахаши А., Меуленбельт I, Уотсон С., Родригес-Лопес Дж., Эгли Р. и др. Мета-анализ европейских и азиатских когорт показывает глобальную роль функционального SNP в 5 ‘UTR GDF5 с предрасположенностью к остеоартриту. Хум Мол Генет . 2008 15 мая. 17 (10): 1497-504. [Медлайн].
Bos SD, Slagboom PE, Meulenbelt I. Новые взгляды на остеоартрит: особенности раннего развития болезни, связанной со старением. Curr Opin Rheumatol . 2008 20 сентября (5): 553-9. [Медлайн].
Чепмен К., Вальдес AM. Генетические факторы в патогенезе ОА. Кость . 2012 Август 51 (2): 258-64. [Медлайн].
Перейра Д., Пелетейро Б., Араужу Дж., Бранко Дж., Сантос Р.А., Рамос Э. Влияние определения остеоартрита на оценки распространенности и заболеваемости: систематический обзор. Хрящевой артроз . 2011 ноября 19 (11): 1270-85. [Медлайн].
Roberts J, Burch TA.Распространенность остеоартроза у взрослых по возрасту, полу, расе и географическому положению. Vital Health Stat 11 . 1966 июн. 1-27. [Медлайн].
Hoaglund FT, Yau AC, Wong WL. Остеоартроз тазобедренного сустава и других суставов на юге Китая в Гонконге. J Bone Joint Surg Am . 1973, апрель, 55 (3): 545-57. [Медлайн].
Felson DT. Сравнение распространенности ревматических заболеваний в Китае с остальным миром. Arthritis Res Ther .2008. 10 (1): 106. [Медлайн]. [Полный текст].
Джордан Дж. М., Хелмик К. Г., Реннер Дж. Б., Лута Дж., Драгомир А. Д., Вудард Дж. И др. Распространенность симптомов коленного сустава, рентгенологического и симптоматического остеоартрита коленного сустава у афроамериканцев и кавказцев: Проект остеоартрита округа Джонстон. Дж. Ревматол. . 2007, январь, 34 (1): 172-80. [Медлайн].
Chapple CM, Nicholson H, Baxter GD, Abbott JH. Характеристики пациентов, которые предсказывают прогрессирование остеоартрита коленного сустава: систематический обзор прогностических исследований. Центр по уходу за артритом (Хобокен) . 2011 августа 63 (8): 1115-25. [Медлайн].
[Рекомендации] Альтман Р., Аларкон Дж., Аппельрут Д., Блох Д., Боренштейн Д., Брандт К. и др. Критерии Американского колледжа ревматологии для классификации остеоартрита кисти и сообщения о нем. Rheum артрита . 1990 ноябрь 33 (11): 1601-10. [Медлайн].
[Рекомендации] Альтман Р., Аларкон Дж., Аппельрут Д., Блох Д., Боренштейн Д., Брандт К. и др.Критерии Американского колледжа ревматологии для классификации остеоартрита бедра и сообщения о нем. Rheum артрита . 1991 Май. 34 (5): 505-14. [Медлайн].
[Рекомендации] Альтман Р., Аш Э, Блох Д., Боле Г., Боренштейн Д., Брандт К. и др. Разработка критериев классификации и отчетности по остеоартриту. Классификация остеоартроза коленного сустава. Комитет по диагностическим и терапевтическим критериям Американской ассоциации ревматизма. Rheum артрита . 1986, 29 августа (8): 1039-49. [Медлайн].
Marshall M, Peat G, Nicholls E, van der Windt D, Myers H, Dziedzic K. Подгруппы симптоматического остеоартрита кисти у пожилых людей, проживающих в сообществах в Соединенном Королевстве: распространенность, взаимосвязь, профили факторов риска и клинические характеристики на исходном уровне и через 3 года. Хрящевой артроз . 2013 21 ноября (11): 1674-84. [Медлайн].
Brandt KD.Пессимистический взгляд на серологические маркеры для диагностики и лечения остеоартрита. Биохимические, иммунологические и клинико-патологические барьеры. J Rheumatol Suppl . 1989 августа 18: 39-42. [Медлайн].
Patra D, Sandell LJ. Последние достижения в области биомаркеров остеоартрита. Curr Opin Rheumatol . 2011 Сентябрь 23 (5): 465-70. [Медлайн].
[Рекомендации] Макалиндон Т.Э., Баннуру Р.Р., Салливан М.К., Арден Н.К., Беренбаум Ф., Бирма-Зейнстра С.М. и др.Рекомендации OARSI по безоперационному лечению остеоартрита коленного сустава. Хрящевой артроз . 2014 марта 22 (3): 363-88. [Медлайн]. [Полный текст].
Агентство медицинских исследований и качества. Лечение остеоартрита коленного сустава: обновленный обзор. AHRQ. Доступно по адресу https://effectivehealthcare.ahrq.gov/topics/osteoarthritis-knee-update/research-2017. 4 мая 2017 г .; Доступ: 15 марта 2019 г.
Цуй Г.Х., Ван ИЙ, Ли СиДжей, Ши СН, Ван В.С.Эффективность мезенхимальных стволовых клеток в лечении пациентов с остеоартрозом коленного сустава: метаанализ. Эксперт Тер Мед . 2016 12 ноября (5): 3390-3400. [Медлайн]. [Полный текст].
Кристьянссон Б., Хонсавек С. Современные перспективы лечения остеоартрита мезенхимальными стволовыми клетками. Стволовые клетки Инт . 2014. 2014: 1943 18. [Медлайн].
Pas HI, Winters M, Haisma HJ, Koenis MJ, Tol JL, Moen MH. Инъекции стволовых клеток при остеоартрозе коленного сустава: систематический обзор литературы. Br J Sports Med . 2017 Август 51 (15): 1125-1133. [Медлайн].
Чахла Дж., Пьюцци Н.С., Митчелл Дж. Дж., Дин С.С., Паскуаль-Гарридо С., ЛаПрейд РФ и др. Внутрисуставная клеточная терапия остеоартрита и очаговых дефектов хряща коленного сустава: систематический обзор литературы и анализ качества исследований. J Bone Joint Surg Am . 2016 21 сентября. 98 (18): 1511-21. [Медлайн].
Zeng C, Dubreuil M, LaRochelle MR, Lu N, Wei J, Choi HK, et al.Связь трамадола со смертностью от всех причин среди пациентов с остеоартритом. ЯМА . 2019 12 марта. 321 (10): 969-982. [Медлайн].
Келли Дж. Трамадол связан с более высокой смертностью от остеоартрита. Медицинские новости Medscape . 12 марта 2019 г. Доступно по адресу https://www.medscape.com/viewarticle/
Freeman S. Tramadol Риск смертности при остеоартрите может перевесить преимущества. Медицинские новости Medscape. Доступно по адресу https: // www.medscape.com/viewarticle/931904. 8 июня 2020 г .; Дата обращения: 10 июня 2020 г.
Consensi (амлодипин / целекоксиб) [вкладыш в упаковке]. Тель-Авив, Израиль: Китов Фарма Лтд., Июнь 2018 г. Доступно на [Полный текст].
Kingsbury SR, Tharmanathan P, Keding A, Ronaldson SJ, Grainger A, Wakefield RJ, et al. Эффективность гидроксихлорохина в уменьшении симптомов остеоартрита кисти: рандомизированное исследование. Энн Интерн Мед. . 2018 20 февраля. [Medline].
Агентство медицинских исследований и качества. Анальгетики при остеоартрите: обновление сравнительного обзора эффективности 2006 года. AHRQ. Доступно по адресу https://effectivehealthcare.ahrq.gov/topics/osteoarthritis-pain/research. 24 октября 2011 г .; Доступ: 15 марта 2019 г.
Citrome L, Weiss-Citrome A. Систематический обзор дулоксетина для лечения боли при остеоартрите: какое количество нужно лечить, количество, необходимое для нанесения вреда, и вероятность того, что вам помогут или повредят ?. Постградская медицина . 2012 января 124 (1): 83-93. [Медлайн].
Frakes EP, Risser RC, Ball TD, Hochberg MC, Wohlreich MM. Дулоксетин, добавленный к пероральным нестероидным противовоспалительным препаратам для лечения боли в коленях, вызванной остеоартритом: результаты рандомизированного двойного слепого плацебо-контролируемого исследования. Curr Med Res Opin . 2011 27 декабря (12): 2361-72. [Медлайн].
Нойштадт DH. Внутрисуставная терапия. Московиц Р.В., Хауэлл Д.С., Альтман Р.Д. и др., Ред. Остеоартроз . 3-е изд. 2001. 393-409.
Lineker SC, Bell MJ, Boyle J, Badley EM, Flakstad L, Fleming J и др. Внедрение руководств по клинической практике артрита в первичной медицинской помощи. Мед Обучение . 2009 31 марта (3): 230-7. [Медлайн].
Годвин М., Доус М. Внутрисуставные инъекции стероидов при болях в коленях. Систематический обзор с метаанализом. Врач Джан Фам . 2004 Февраль 50: 241-8. [Медлайн]. [Полный текст].
McAlindon TE, LaValley MP, Harvey WF, Price LL, Driban JB, Zhang M, et al. Эффект внутрисуставного триамцинолона по сравнению с физиологическим раствором на объем хряща коленного сустава и боль у пациентов с остеоартритом коленного сустава: рандомизированное клиническое испытание. ЯМА . 2017 16 мая. 317 (19): 1967-1975. [Медлайн].
Haelle T. Инъекции стероидов увеличивают потерю хрящевой ткани при артрите коленного сустава. Медицинские новости Medscape. Доступно на https://www.medscape.com/viewarticle/880072.16 мая 2017 г .; Доступ: 31 октября 2017 г.
Конаган П.Г., Хантер Д.Д., Коэн С.Б., Краус В.Б., Беренбаум Ф., Либерман Дж. Р. и др. Эффекты однократной внутрисуставной инъекции микросферного препарата триамцинолона ацетонида на боль при остеоартрите коленного сустава: двойное слепое, рандомизированное, плацебо-контролируемое многонациональное исследование. J Bone Joint Surg Am . 2018 г. 18 апреля. 100 (8): 666-677. [Медлайн]. [Полный текст].
Ламберт Р.Г., Хатчингс Э.Дж., Грейс М.Г., Джангри Г.С., Коннер-Спейди Б., Максимович В.П.Инъекции стероидов при остеоартрите тазобедренного сустава: рандомизированное двойное слепое плацебо-контролируемое исследование. Rheum артрита . 2007 июль 56 (7): 2278-87. [Медлайн].
Martin CL, Browne JA. Внутрисуставные инъекции кортикостероидов при симптоматическом остеоартрите коленного сустава: что необходимо знать врачу-ортопеду. J Am Acad Orthop Surg . 2019 1. 27 (17): e758-e766. [Медлайн]. [Полный текст].
Kompel AJ, Roemer FW, Murakami AM, Diaz LE, Crema MD, Guermazi A.Внутрисуставные инъекции кортикостероидов в бедро и колено: возможно, не так безопасно, как мы думали ?. Радиология . 2019 15 октября 1. [Medline]. [Полный текст].
Ститик Т.П., Леви Я. Вязкие добавки (биодобавки) при остеоартрите. Am J Phys Med Rehabil . 2006 ноябрь 85 (11 приложение): S32-50. [Медлайн].
Беллами Н., Кэмпбелл Дж., Робинсон В., Джи Т., Борн Р., Уэллс Г. Вискозависимая добавка для лечения остеоартроза коленного сустава. Кокрановская база данных Syst Rev . 2006 г. 19 апреля. CD005321. [Медлайн].
Гольдберг В.М., Баквалтер Дж. А. Гиалуронаны в лечении остеоартрита коленного сустава: данные о модифицирующей болезнь активности. Хрящевой артроз . 2005 марта 13 (3): 216-24. [Медлайн].
Альтман Р.Д., Московиц Р. Внутрисуставной гиалуронат натрия (Гиалган) в лечении пациентов с остеоартрозом коленного сустава: рандомизированное клиническое испытание.Группа изучения Хиалгана. Дж. Ревматол. . 1998 25 ноября (11): 2203-12. [Медлайн].
Stitik TP, Blacksin MF, Stiskal DM, Kim JH, Foye PM, Schoenherr L, et al. Эффективность и безопасность лечения гиалуроновой кислотой в сочетании с домашними упражнениями при боли при остеоартрите коленного сустава. Arch Phys Med Rehabil . 2007 Февраль 88 (2): 135-41. [Медлайн].
Вадделл Д.Д., Коломыткин О.В., Данн С, Марино А.А. Гиалуронан подавляет активность металлопротеиназы, индуцированную IL-1beta, в синовиальной ткани. Clin Orthop Relat Res . 2007 декабрь 465: 241-8. [Медлайн].
Gato-Calvo L, Magalhaes J, Ruiz-Romero C, Blanco FJ, Burguera EF. Плазма, обогащенная тромбоцитами, в лечении остеоартрита: обзор текущих данных. Ther Adv Chronic Dis . 2019. 10: 2040622319825567. [Медлайн]. [Полный текст].
Дай В.Л., Чжоу А.Г., Чжан Х., Чжан Дж. Эффективность богатой тромбоцитами плазмы при лечении остеоартрита коленного сустава: метаанализ рандомизированных контролируемых испытаний. Артроскопия . 2017 Mar.33 (3): 659-670.e1. [Медлайн].
Yaradilmis CYU, Demirkale I, Tagral AS, Okkaoglu MC, Ates A, Altay M. Сравнение двух составов плазмы с высоким содержанием тромбоцитов с добавлением вязкости при лечении гонартроза средней степени тяжести: проспективное рандомизированное контролируемое исследование. Ортопедический журнал . 28 января 2020 г. 20: 240-246. [Полный текст].
Chu CR, Rodeo S, Bhutani N, Goodrich LR, Huard J, Irrgang J, et al.Оптимизация клинического использования биопрепаратов в ортопедической хирургии: согласованные рекомендации конференции AAOS / NIH U-13 2018 г. J Am Acad Orthop Surg . 2019 15 января. 27 (2): e50-e63. [Медлайн]. [Полный текст].
Рабаго Д., Паттерсон Дж. Дж., Мундт М., Кийовски Р., Гретти Дж., Сегал Н. А. и др. Пролотерапия декстрозой при остеоартрите коленного сустава: рандомизированное контролируемое исследование. Энн Фам Мед . 2013 май-июнь. 11 (3): 229-37. [Медлайн]. [Полный текст].
Sawitzke AD, Shi H, Finco MF, Dunlop DD, Bingham CO 3rd, Harris CL, et al.Влияние глюкозамина и / или хондроитинсульфата на прогрессирование остеоартрита коленного сустава: отчет по интервенционному исследованию глюкозаминового / хондроитинового артрита. Rheum артрита . 2008 Октябрь 58 (10): 3183-91. [Медлайн]. [Полный текст].
Clegg DO, Reda DJ, Harris CL, et al. Глюкозамин, хондроитинсульфат и их комбинация для лечения болезненного остеоартрита коленного сустава. N Engl J Med . 2006 г. 23 февраля. 354 (8): 795-808. [Медлайн].
Rutjes AW, Nüesch E, Reichenbach S, Jüni P.S-аденозилметионин при остеоартрозе колена или бедра. Кокрановская база данных Syst Rev . 2009 7 октября. CD007321. [Медлайн].
Ван З., Джонс Дж., Винценберг Т., Цай Дж., Ласлетт Л.Л., Эйткен Д. и др. Эффективность экстракта Curcuma longa для лечения симптомов и синовита выпота при остеоартрите коленного сустава: рандомизированное исследование. Энн Интерн Мед. . 2020 15 сентября [Medline].
Hathcock JN, Shao A. Оценка риска глюкозамина и хондроитинсульфата. Регул Токсикол Фармакол . 2007 Февраль 47 (1): 78-83. [Медлайн].
Gege C, Bao B, Bluhm H, Boer J, Gallagher BM, Korniski B, et al. Открытие и оценка не-Zn хелатирующего селективного ингибитора матриксной металлопротеиназы 13 (MMP-13) для потенциального внутрисуставного лечения остеоартрита. J Med Chem . 2012 26 января. 55 (2): 709-16. [Медлайн].
Брукс М. Смешанные результаты по новому лекарству от остеоартрита. Медицинские новости Medscape.Доступно на https://www.medscape.com/viewarticle/923233. 30 декабря 2019 г .; Доступ: 15 апреля 2020 г.
Brown MT, Murphy FT, Radin DM, Davignon I, Smith MD, West CR. Танезумаб уменьшает боль в коленях при остеоартрите: результаты рандомизированного двойного слепого плацебо-контролируемого исследования III фазы. Дж. Боль . 2012 13 августа (8): 790-8. [Медлайн].
Пирсон Р. Лилли утверждает, что новый тип обезболивающего может уменьшить потребность в опиоидах. Медицинские новости Medscape.Доступно на http://www.medscape.com/viewarticle/863797. 25 мая 2016 г .; Доступ: 8 июля 2016 г.
Родди Э, Доэрти М. Изменение образа жизни и остеоартрит: каковы доказательства ?. Best Practices Clin Rheumatol . 2006 20 февраля (1): 81-97. [Медлайн].
Perrot S, Poiraudeau S, Kabir M, Bertin P, Sichere P, Serrie A и др. Активные или пассивные стратегии купирования боли при остеоартрите тазобедренного и коленного суставов? Результаты национального опроса 4719 пациентов в учреждениях первичной медико-санитарной помощи. Rheum артрита . 2008 15 ноября. 59 (11): 1555-62. [Медлайн].
Беннелл К.Л., Кириакидес М., Ходжес П.В., Хинман Р.С. Влияние двух сеансов бустерной физиотерапии на результаты домашних упражнений у людей с остеоартритом коленного сустава: рандомизированное контролируемое исследование. Центр по уходу за артритом (Хобокен) . 2014 ноябрь 66 (11): 1680-7. [Медлайн].
Anandacoomarasamy A, Leibman S, Smith G, et al. Снижение веса у тучных людей оказывает структурно-модифицирующее воздействие на медиальный, но не латеральный суставной хрящ коленного сустава. Энн Рум Дис . 2012 Январь 71 (1): 26-32. [Медлайн].
Мессье SP. Ожирение и остеоартрит: генезис заболевания и нефармакологическое управление весом. Rheum Dis Clin North Am . 2008 г., 34 (3): 713-29. [Медлайн]. [Полный текст].
Маккарти GM, Маккарти DJ. Эффект местного капсаицина в терапии болезненного остеоартроза рук. Дж. Ревматол. . 1992 апреля 19 (4): 604-7. [Медлайн].
Ватт FE, Кеннеди Д.Л., Карлайл К.Э., Фрейдин А.Дж., Шидло Р.М., Ханифилд Л. и др.Ночная иммобилизация дистального межфалангового сустава снижает боль и деформацию разгибания при остеоартрозе кисти. Ревматология (Оксфорд) . 2014 8 февраля [Medline].
Коэн Р. Ночные шины для пальцев могут облегчить боль при артрите. Medscape [сериал онлайн]. Доступно на http://www.medscape.com/viewarticle/821310. Доступ: 11 марта 2014 г.
Juhl C, Christensen R, Roos EM, Zhang W, Lund H. Влияние типа и дозы упражнений на боль и инвалидность при остеоартрите коленного сустава: систематический обзор и мета-регрессионный анализ рандомизированных контролируемых исследований. Ревматический артрит . 2014 Март 66 (3): 622-36. [Медлайн].
Ян MH, Lin CH, Lin YF, Lin JJ, Lin DH. Влияние нагрузки на нагрузку по сравнению с упражнениями без нагрузки на функцию, скорость ходьбы и чувство положения у участников с остеоартритом коленного сустава: рандомизированное контролируемое исследование. Arch Phys Med Rehabil . 2009 июн 90 (6): 897-904. [Медлайн].
Чайпиньо К., Кароонсупчароен О. Нет разницы между силовой тренировкой в домашних условиях и тренировкой равновесия в домашних условиях при боли у пациентов с остеоартрозом коленного сустава: рандомизированное исследование. Ауст Дж. Физиотер . 2009. 55 (1): 25-30. [Медлайн].
Marks R, Allegrante JP. Хронический остеоартрит и соблюдение физических упражнений: обзор литературы. Закон о физике старения . 2005 октября, 13 (4): 434-60. [Медлайн].
Ван Ч., Шмид Ч., Хибберд П.Л., Калиш Р., Рубенофф Р., Ронес Р. и др. Тайцзи эффективен при лечении остеоартроза коленного сустава: рандомизированное контролируемое исследование. Rheum артрита . 2009 15 ноя.61 (11): 1545-53. [Медлайн].
Wang C, Schmid CH, Iversen MD, Harvey WF, Fielding RA, Driban JB, et al. Сравнительная эффективность тайцзи по сравнению с физиотерапией остеоартрита коленного сустава: рандомизированное исследование. Энн Интерн Мед. . 2016 17 мая. [Medline].
Кан Дж. В., Ли М. С., Посадски П., Эрнст Э. Тайчи для лечения остеоартрита: систематический обзор и метаанализ. BMJ Открыть . 2011 28 марта. 1 (1): e000035.[Медлайн]. [Полный текст].
Гудман А. Коленный бандаж уменьшает повреждение и боль при остеоартрите. Медицинские новости Medscape. Доступно на http://www.medscape.com/viewarticle/813572. Доступ: 4 ноября 2013 г.
[Рекомендации] Hochberg MC, Altman RD, April KT, Benkhalti M, Guyatt G, McGowan J, et al. Рекомендации Американского колледжа ревматологии, 2012 г., по использованию нефармакологических и фармакологических методов лечения остеоартрита кисти, бедра и колена. Центр по уходу за артритом (Хобокен) . 2012 апр. 64 (4): 465-74. [Медлайн]. [Полный текст].
Hinman RS, Wrigley TV, Metcalf BR, Campbell PK, Paterson KL, Hunter DJ и др. Разгрузочная обувь для самостоятельного лечения остеоартрита коленного сустава: рандомизированное испытание. Энн Интерн Мед. . 2016 12 июля [Medline].
Лю Х., Эбботт Дж., Би Дж. А. Импульсные электромагнитные поля влияют на состав внеклеточного матрикса гиалинового хряща, не влияя на молекулярную структуру. Хрящевой артроз . 1996 4 марта (1): 63-76. [Медлайн].
Zizic TM, Hoffman KC, Holt PA, Hungerford DS, O’Dell JR, Jacobs MA, et al. Лечение остеоартроза коленного сустава импульсной электростимуляцией. Дж. Ревматол. . 1995 22 сентября (9): 1757-61. [Медлайн].
Garland D, Holt P, Harrington JT, Caldwell J, Zizic T., Cholewczynski J. Трехмесячное рандомизированное двойное слепое плацебо-контролируемое исследование для оценки безопасности и эффективности высокооптимизированного, емкостно-связанного, импульсного электростимулятор у больных остеоартрозом коленного сустава. Хрящевой артроз . 2007 июн.15 (6): 630-7. [Медлайн].
Fukuda TY, Alves da Cunha R, Fukuda VO, et al. Импульсное коротковолновое лечение у женщин с остеоартритом коленного сустава: многоцентровое рандомизированное плацебо-контролируемое клиническое исследование. Phys Ther . 2011 июл.91 (7): 1009-17. [Медлайн].
Инь К.Н., В то время как А. Обезболивание при остеоартрите и ревматоидном артрите: ДЕСЯТКИ. Br J Сообщество медсестер . 2007 Август.12 (8): 364-71. [Медлайн].
Pietrosimone BG, Saliba SA, Hart JM, Hertel J, Kerrigan DC, Ingersoll CD. Влияние чрескожной электрической стимуляции нервов и терапевтических упражнений на активацию четырехглавой мышцы у людей с тибио-бедренным остеоартритом. J Orthop Sports Phys Ther . 2011 января 41 (1): 4-12. [Медлайн].
Selfe TK, Taylor AG. Иглоукалывание и остеоартрит коленного сустава: обзор рандомизированных контролируемых исследований. Здравоохранение сообщества Fam . 2008 июль-сен. 31 (3): 247-54. [Медлайн]. [Полный текст].
[Рекомендации] Евсевар Д.С., Браун Г.А., Джонс Д.Л., Мацкин Е.Г., Маннер П.А., Муар П. и др. Основанное на фактических данных руководство Американской академии хирургов-ортопедов по лечению остеоартроза коленного сустава, 2-е издание. J Bone Joint Surg Am . 2013 16 октября. 95 (20): 1885-6. [Медлайн]. [Полный текст].
Киркли А., Бирмингем, ТБ, Литчфилд, РБ, Гиффин Дж. Р., Уиллитс К. Р., Вонг CJ и др.Рандомизированное исследование артроскопической хирургии остеоартрита коленного сустава. N Engl J Med . 2008 11 сентября. 359 (11): 1097-107. [Медлайн].
Маркс Р.Г. Артроскопическая хирургия коленного сустава ?. Медицинский журнал Новой Англии . 2008. Vol. 359: 1169-1170. [Полный текст].
Barclay L, Nghiem HT. Артроскопическая хирургия может не помочь при остеоартрите коленного сустава. Medscape. Доступно на http://www.medscape.com/viewarticle/580300.Доступ: 29 сентября 2010 г.
Pagenstert G, Knupp M, Valderrabano V, Hintermann B. Операция по коррекции вальгусного остеоартрита голеностопного сустава. Опер Ортоп Травматол . 2009 21 марта (1): 77-87. [Медлайн].
Pipino G, Indelli PF, Tigani D, Maffei G, Vaccarisi D. Высокая остеотомия большеберцовой кости с открытием клина: исследование продолжительностью от семи до двенадцати лет. Соединения . 2016 13 июня. 4 (1): 6-11. [Медлайн].
Дарас М., Маколей В.Тотальное эндопротезирование тазобедренного сустава у молодых пациентов с остеоартрозом. Am J Orthop (Бель Мид, штат Нью-Джерси) . 2009 Март 38 (3): 125-9. [Медлайн].
Куо А., Эззет К.А., Патил С., Колвелл К.В. Младший. Тотальная артропластика тазобедренного сустава при быстро деструктивном остеоартрите бедра: серия случаев. HSS J . 2009 Сентябрь 5 (2): 117-9. [Медлайн]. [Полный текст].
Reichenbach S, Rutjes AW, Nüesch E, Trelle S, Jüni P. Промывание суставов при остеоартрите коленного сустава. Кокрановская база данных Syst Rev . 2010 12 мая. CD007320. [Медлайн].
Felson DT, Niu J, Clancy M, Aliabadi P, Sack B, Guermazi A, et al. Низкий уровень витамина D и обострение остеоартроза коленного сустава: результаты двух продольных исследований. Rheum артрита . 2007 Январь 56 (1): 129-36. [Медлайн].
Bergink AP, Uitterlinden AG, Van Leeuwen JP, Buurman CJ, Hofman A, Verhaar JA и др. Статус витамина D, минеральная плотность костей и развитие рентгенологического остеоартрита коленного сустава: Роттердамское исследование. Дж. Клин Ревматол . 2009 15 августа (5): 230-7. [Медлайн].
Canter PH, Wider B, Ernst E. Антиоксидантные витамины A, C, E и селен в лечении артрита: систематический обзор рандомизированных клинических испытаний. Ревматология (Оксфорд) . 2007 августа 46 (8): 1223-33. [Медлайн].
Peregoy J, Wilder FV. Влияние добавок витамина С на случайный и прогрессирующий остеоартрит коленного сустава: продольное исследование. Nutr общественного здравоохранения . 2011 г., 14 (4): 709-15. [Медлайн].
Арши А., Петрильяно Ф.А., Уильямс Р.Дж., Джонс К.Дж. Лечение стволовыми клетками дефектов суставного хряща коленного сустава и остеоартрита. Текущие отзывы в костно-мышечной медицине . 21 января 2020 г. [Полный текст].
Kraeutler MJ, Mitchell JJ, Chahla J, McCarty EC, Pascual-Garrido C. Внутрисуставная имплантация мезенхимальных стволовых клеток, Часть 2: Обзор литературы по регенерации мениска. Orthop J Sports Med . 2017 19 января. 5 (1): 2325967116680814. [Медлайн]. [Полный текст].
Харрисон Л. Лечение подозрением на стволовые клетки при артрите коленного сустава. Медицинские новости Medscape. Доступно на https://www.medscape.com/viewarticle/893665. 8 марта 2018 г .; Доступ: 14 марта 2018 г.
[Рекомендации] Коласински С.Л., Неоги Т., Хохберг М.С. и др. Руководство Американского колледжа ревматологии / Фонда артрита по лечению остеоартроза кисти, бедра и колена, 2019 г. Ревматический артрит . 2020 6 января [Medline]. [Полный текст].
[Рекомендации] Баннуру Р.Р., Осани М.К., Вайсброт Э.Е., Арден Н.К., Беннелл К., Бирма-Зейнстра СМА и др. Рекомендации OARSI по безоперационному лечению коленного, тазобедренного и полиартикулярного остеоартрита. Хрящевой артроз . 2019 г. 3 июля [Medline]. [Полный текст].
[Рекомендации] Вебер К.Л., Евсевар Д.С., МакГрори Б.Дж. Руководство по клинической практике AAOS: Хирургическое лечение остеоартрита коленного сустава: Рекомендации, основанные на фактах. J Am Acad Orthop Surg . 2016, 28 июня. [Medline]. [Полный текст].
Хакенталь В. Первые рекомендации по остеоартриту тазобедренного сустава от AAOS. Медицинские новости Medscape. Доступно на http://www.medscape.com/viewarticle/878593. 13 апреля 2017 г .; Доступ: 15 мая 2017 г.
[Руководство] Американская академия хирургов-ортопедов. Управление остеоартрозом тазобедренного сустава: научно обоснованное руководство по клинической практике. AAOS. Доступно на https: //www.aaos.org / uploadedFiles / PreProduction / Quality / Guidelines_and_Reviews / OA% 20Hip% 20CPG_3.13.17.pdf. 13 марта 2017 г .; Доступ: 15 марта 2019 г.
Brooks M. Диклофенак для местного применения 2% (Pennsaid) от боли при остеоартрите коленного сустава очищает FDA. Medscape [сериал онлайн]. Доступно на http://www.medscape.com/viewarticle/819436. Доступ: 26 января 2014 г.
Gibofsky A, Hochberg MC, Jaros MJ, Young CL. Эффективность и безопасность низких доз субмикронного диклофенака для лечения боли при остеоартрите: исследование фазы 3, 12 недель. Curr Med Res Opin . 2014 6. 1–11 августа. [Медлайн].
Миллер М., Штюрмер Т., Азраэль Д., Левин Р., Соломон Д.Х. Опиоидные анальгетики и риск переломов у пожилых людей с артритом. Дж. Ам Гериатр Соц . 2011 Март 59 (3): 430-8. [Медлайн].
Нехирургическое лечение боли в колене у взрослых
1. Нгуен США, Чжан И, Чжу Ю, Ниу Дж, Чжан Б, Felson DT. Растущая распространенность боли в коленях и симптоматического остеоартрита коленного сустава: данные обследований и когорт. Энн Интерн Мед. . 2011; 155 (11): 725–732 ….
2. Бейкер П., Читая I, Купер С, Коггон Д. Коленные расстройства у населения в целом и их отношение к профессии. Оккуп Энвирон Мед . 2003. 60 (10): 794–797.
3. Черри Д.К., Вудвелл Д.А., Рехтштайнер Э.А.; Центры по контролю и профилактике заболеваний. Национальное амбулаторное медицинское обследование: сводка 2005 г. http://www.cdc.gov/nchs/data/ad/ad387.pdf. По состоянию на 1 сентября 2014 г.
4. Бухбиндер Р, Ричардс Б., Харрис И. Остеоартрит коленного сустава и роль хирургического вмешательства: уроки, извлеченные из рандомизированных клинических испытаний и популяционных когорт. Curr Opin Rheumatol . 2014. 26 (2): 138–144.
5. Межов В, Тейхталь AJ, Штрассер Р., Влука А.Е., Cicuttini FM. Патология мениска — доказательства для лечения. Arthritis Res Ther . 2014; 16 (2): 206.
6.Мардохей SC, Аль-Хадифи Н, Посуда HE, Gupte CM. Лечение разрывов мениска: научно обоснованный подход. Мир Дж. Ортоп . 2014. 5 (3): 233–241.
7. Браун Г.А. Руководство по клинической практике AAOS: лечение остеоартроза коленного сустава: научно-обоснованное руководство, 2-е издание. J Am Acad Orthop Surg . 2013. 21 (9): 577–579.
8. Hochberg MC, Альтман Р.Д., Апрель КТ, и другие. Рекомендации Американского колледжа ревматологии, 2012 г., по использованию нефармакологических и фармакологических методов лечения остеоартрита кисти, бедра и колена. Центр лечения артрита (Хобокен) . 2012. 64 (4): 465–474.
9. Дейл Г.Д., Эллисон СК, Матекель Р.Л., и другие. Эффективность физиотерапевтического лечения остеоартроза коленного сустава: рандомизированное сравнение контролируемых клинических упражнений и мануальных терапевтических процедур с программой упражнений в домашних условиях. Phys Ther . 2005. 85 (12): 1301–1317.
10. Brosseau L, Уэллс GA, Тагвелл П., и другие.Оттавская группа научно обоснованных клинических рекомендаций по лечению остеоартрита у взрослых, страдающих ожирением или избыточной массой тела. Phys Ther . 2011. 91 (6): 843–861.
11. Хинман Р.С., Кроссли К.М., МакКоннелл Дж, Bennell KL. Эффективность коленной ленты в лечении остеоартрита коленного сустава: слепое рандомизированное контролируемое исследование. BMJ . 2003. 327 (7407): 135–138.
12. Rutjes AW, Nüesch E, Стерчи Р., Юни П.Лечебное ультразвуковое исследование при остеоартрозе колена или бедра. Кокрановская база данных Syst Rev . 2010; (1): CD003132.
13. Приор MJ, Харрисон Д.Д., Frustaci ME. Рандомизированное двойное слепое плацебо-контролируемое 12-недельное исследование ацетаминофена с пролонгированным высвобождением для лечения признаков и симптомов остеоартрита. Curr Med Res Opin . 2014. 30 (11): 2377–2387.
14. Jawad AS. Анальгетики и остеоартрит: отражены ли рекомендации по лечению в клинической практике? Am J Ther .2005. 12 (1): 98–103.
15. Райхенбах С., Стерчи Р., Шерер М, и другие. Мета-анализ: хондроитин при остеоартрозе колена или бедра. Энн Интерн Мед. . 2007. 146 (8): 580–590.
16. Влад СК, ЛаВалли МП, Макалиндон Т.Е., Felson DT. Глюкозамин от боли при остеоартрите: почему различаются результаты испытаний? Rheum артрита . 2007. 56 (7): 2267–2277.
17.Мишель Б.А., Штуки Г, Фрей Д, и другие. Хондроитины 4 и 6 сульфат при остеоартрозе коленного сустава: рандомизированное контролируемое исследование. Rheum артрита . 2005. 52 (3): 779–786.
18. Провенца JR, Синдзё СК, Сильва Дж. М., Перон CR, Роча Ф.А. Комбинация глюкозамина и хондроитинсульфата один или три раза в день обеспечивает клинически значимое обезболивание при остеоартрите коленного сустава [опубликовано перед печатью 3 августа 2014 г.].По состоянию на 8 июля 2015 г.
19. Jones T, Кельсберг Г, Сафранек С. Клинические запросы FPIN: Внутрисуставные инъекции кортикостероидов при остеоартрите коленного сустава. Ам Фам Врач . 2014. 90 (2): 115–116.
20. Чжан В, Нуки Г, Московиц RW, и другие. Рекомендации OARSI по лечению остеоартрита тазобедренного и коленного суставов: часть III: изменения в доказательствах после систематического кумулятивного обновления исследований, опубликованных до января 2009 г. Хрящевой артроз . 2010. 18 (4): 476–499.
21. Киркли А, Вебстер-Богерт С., Литчфилд R, и другие. Эффект корсета при варусном гонартрозе. J Bone Joint Surg Am . 1999. 81 (4): 539–548.
22. Брауэр RW, Якма Т.С., Верхаген А.П., Верхаар Я.А., Bierma-Zeinstra SM. Подтяжки и ортезы для лечения артроза колена. Кокрановская база данных Syst Rev .2005; (1): CD004020.
23. Rixe JA, Глик Дж. Э., Брэди Дж, Олимпия РП. Обзор лечения пателлофеморального болевого синдрома. Физ Спортмед . 2013. 41 (3): 19–28.
24. Бартон С, Балачандар V, Недостаток S, Моррисси Д. Тейпирование надколенника при пателлофеморальной боли: систематический обзор и метаанализ для оценки клинических исходов и биомеханических механизмов. Br J Sports Med . 2014. 48 (6): 417–424.
25. Heintjes E, Бергер М.Ю., Бирма-Зейнстра С.М., Бернсен Р.М., Верхаар Я.А., Koes BW. Фармакотерапия пателлофеморального болевого синдрома. Кокрановская база данных Syst Rev . 2004; (3): CD003470.
26. D’hondt NE, Струйс П.А., Керкхоффс GM, и другие. Ортопедические устройства для лечения пателлофеморального болевого синдрома. Кокрановская база данных Syst Rev . 2002; (2): CD002267.
27.Биццини М, Чайлдс JD, Пива СР, Далитто А. Систематический обзор качества рандомизированных контролируемых исследований пателлофеморального болевого синдрома. J Orthop Sports Phys Ther . 2003. 33 (1): 4–20.
28. Herrlin S, Холландер М, Ванге П., Weidenhielm L, Вернер С. Артроскопическое или консервативное лечение дегенеративных разрывов медиального мениска: проспективное рандомизированное исследование. Коленная хирургия Sports Traumatol Arthrosc .2007. 15 (4): 393–401.
29. Кац Ю.Н., Брофи РХ, Chaisson CE, и другие. Хирургия в сравнении с физиотерапией при разрыве мениска и остеоартрите. N Engl J Med . 2013. 368 (18): 1675–1684.
30. Visnes H, Бахр Р. Эволюция эксцентрических тренировок как лечения тендинопатии надколенника (прыгающего колена): критический обзор программ упражнений. Br J Sports Med . 2007. 41 (4): 217–223.
31. Mehallo CJ, Дрезнер Я.А., Bytomski JR. Практическое руководство: применение нестероидных противовоспалительных препаратов (НПВП) при спортивных травмах. Clin J Sport Med . 2006. 16 (2): 170–174.
32. Гюнтер П., Schwellnus MP. Местная инъекция кортикостероидов при синдроме трения подвздошно-большеберцовой ленты у бегунов: рандомизированное контролируемое исследование. Br J Sports Med . 2004. 38 (3): 269–272.
33. Лаваньино М, Арноцкий С.П., Доддс Дж. Эльвин Н.Инфрапателлярные ремни уменьшают деформацию сухожилия надколенника в месте повреждения колена прыгуна: вычислительный анализ, основанный на рентгенологических измерениях. Спортивное здоровье . 2011. 3 (3): 296–302.
34. Азар ФМ. Оценка и лечение хронических повреждений медиальной коллатеральной связки колена. Sports Med Arthrosc . 2006. 14 (2): 84–90.
35. ДеФранко М.Дж., Бах Б.Р. мл. Комплексный обзор частичных разрывов передней крестообразной связки. J Bone Joint Surg Am . 2009. 91 (1): 198–208.
36. Беннелл К.Л., Охотник DJ, Hinman RS. Лечение остеоартроза коленного сустава. BMJ . 2012; 345: e4934.
37. Мартин С.Н., Макгоуэн HJ, Смит РФ. Упражнения для лечения остеоартроза коленного сустава. Ам Фам Врач . 2011; 84 (5): 1. https://www.aafp.org/afp/2011/0901/od1.html. По состоянию на 6 мая 2015 г.
38. Bradley JD, Брандт К.Д., Кац Б.П., Каласинский Л.А., Райан С.И.Сравнение противовоспалительной дозы ибупрофена, анальгетической дозы ибупрофена и ацетаминофена при лечении пациентов с остеоартрозом коленного сустава. N Engl J Med . 1991. 325 (2): 87–91.
39. Верклей ИП, Люйстербург PA, Бонен А.М., Koes BW, Bierma-Zeinstra SM. НПВП против ацетаминофена при остеоартрите коленного и тазобедренного суставов: систематический обзор неоднородности, влияющей на результаты. Хрящевой артроз .2011; 19 (8): 921–929.
40. Вегман А, ван дер Виндт Д., ван Тулдер М, Стальман В, де Вриз Т. Нестероидные противовоспалительные препараты или ацетаминофен при остеоартрозе бедра или колена? Систематический обзор доказательств и руководств. Дж. Ревматол . 2004. 31 (2): 344–354.
41. Machado GC, Махер К.Г., Феррейра PH, и другие. Эффективность и безопасность парацетамола при боли в спине и остеоартрите: систематический обзор и метаанализ рандомизированных плацебо-контролируемых исследований. BMJ . 2015; 350: ч2225.
42. Дерри С, Мур Р.А., Рабби Р. Актуальные НПВП при хронической скелетно-мышечной боли у взрослых. Кокрановская база данных Syst Rev . 2012; (9): CD007400.
43. Massey T, Дерри С, Мур Р.А., McQuay HJ. Актуальные НПВП при острой боли у взрослых. Кокрановская база данных Syst Rev . 2010; (6): CD007402.
44. Мейсон Л, Мур Р.А., Дерри С, Эдвардс Дж. Э., McQuay HJ.Систематический обзор местного применения капсаицина для лечения хронической боли. BMJ . 2004; 328 (7446): 991.
45. Парк КС, Цой JJ, Ким ВУ, Мин JK, Парк Ш, Чо CS. Эффективность комбинированных таблеток трамадола и ацетаминофена (Ultracet ® ) в качестве дополнительной и поддерживающей терапии при боли при остеоартрите коленного сустава, недостаточно контролируемой нестероидными противовоспалительными препаратами (НПВП). Clin Rheumatol . 2012. 31 (2): 317–323.
46. Благородный М, Тредуэлл-младший, Tregear SJ, и другие. Долгосрочное лечение опиоидами при хронической нераковой боли. Кокрановская база данных Syst Rev . 2010; (1): CD006605.
47. McAlindon T, ЛаВалли М, Шнайдер Э, и другие. Влияние добавок витамина D на прогрессирование боли в коленях и потерю объема хряща у пациентов с симптоматическим остеоартритом: рандомизированное контролируемое исследование. ЯМА .2013. 309 (2): 155–162.
48. Towheed TE, Максвелл Л, Анастасиадис Т.П., и другие. Глюкозаминовая терапия для лечения остеоартроза. Кокрановская база данных Syst Rev . 2005; (2): CD002946.
49. Сингх Дж. А., Ноорбалучи С, Макдональд Р, Максвелл LJ. Хондроитин при остеоартрозе. Кокрановская база данных Syst Rev . 2015; (1): CD005614.
50. Беллами Н., Кэмпбелл Дж. Робинзон V, Джи Т, Борн Р., Уэллс Г.Внутрисуставные кортикостероиды для лечения остеоартроза коленного сустава. Кокрановская база данных Syst Rev . 2006; (2): CD005328.
51. Divine JG, Shaffer MD. Использование вискозиметров при остеоартрите коленного сустава: обновленная информация. Curr Sports Med Rep . 2011; 10 (5): 279–284.
52. Rutjes AW, Юни П, да Коста BR, Trelle S, Nüesch E, Райхенбах С. Вязкостные добавки при остеоартрите коленного сустава: систематический обзор и метаанализ. Энн Интерн Мед. . 2012. 157 (3): 180–191.
53. Паркс MJ, Марикар Н, Лант М, и другие. Боковые клиновидные стельки как консервативное лечение боли у пациентов с медиальным остеоартрозом коленного сустава: метаанализ. ЯМА . 2013. 310 (7): 722–730.
54. van der Heijden RA, Lankhorst NE, ван Линсхотен Р, Бирма-Зейнстра С.М., ван Мидделкоп М. Упражнения для лечения пателлофеморального болевого синдрома. Кокрановская база данных Syst Rev . 2015; (1): CD010387.
55. Каллаган MJ, Селфе Дж. Тейпирование надколенника при пателлофеморальном болевом синдроме у взрослых. Кокрановская база данных Syst Rev . 2012; (4): CD006717.
56. Коллинз, штат Нью-Джерси, Биссет Л.М., Кроссли К.М., Вичензино Б. Эффективность нехирургических вмешательств при боли в передней части колена: систематический обзор и метаанализ рандомизированных исследований. Sports Med .2012; 42 (1): 31–49.
57. Райан М, Вонг А, Рабаго Д., Лук-порей, Тонтон Дж. Инъекции гиперосмолярной декстрозы под контролем ультразвука при чрезмерной тендинопатии надколенника: пилотное исследование. Br J Sports Med . 2011; 45 (12): 972–977.
58. Маутнер К., Кольберг RE, Маланга Г, и другие. Результаты после инъекций обогащенной тромбоцитами плазмы под контролем УЗИ при хронической тендинопатии: многоцентровый ретроспективный обзор. PM R . 2013. 5 (3): 169–175.
59. Филардо Г, Кон Э, Делла Вилла S, Винчентелли Ф, Форнасари PM, Маркаччи М. Использование богатой тромбоцитами плазмы для лечения рефрактерного колена прыгуна. Инт Ортоп . 2010. 34 (6): 909–915.
60. Rabago D, Паттерсон Дж. Дж., Мундт М, и другие. Пролотерапия декстрозой при остеоартрите коленного сустава: рандомизированное контролируемое исследование [опубликованная поправка опубликована в Ann Fam Med.2013; 11 (5): 480]. Энн Фам Мед . 2013. 11 (3): 229–237.
61. Кон Э, Мандельбаум Б, Буда Р, и другие. Внутрисуставные инъекции плазмы, богатой тромбоцитами, по сравнению с добавками гиалуроновой кислоты в качестве лечения патологии хряща: от ранней дегенерации до остеоартрита. Артроскопия . 2011. 27 (11): 1490–1501.
62. Патель С, Диллон М.С., Аггарвал С, Марваха Н, Джайн А.Лечение остеоартрита коленного сустава плазмой, богатой тромбоцитами, более эффективно, чем плацебо: проспективное двойное слепое рандомизированное исследование. Am J Sports Med . 2013. 41 (2): 356–364.
63. Loew LM, Brosseau L, Тагвелл П., и другие. Массаж глубоким поперечным трением для лечения тендинита бокового локтя или бокового колена. Кокрановская база данных Syst Rev . 2014; (11): CD003528.
Физиотерапия остеоартроза коленного сустава
Укрепляющие упражнения и другие методы лечения остеоартрита
Физическая терапия может быть вашей первой линией защиты при лечении симптомов остеоартрита коленного сустава.
Остеоартроз коленного сустава иногда может показаться обоюдоострым мечом. Чрезмерная нагрузка на колени может ухудшить здоровье суставов и ОА колен, но чем меньше вы двигаете коленями, тем они слабее. Вам нужно найти такой баланс, чтобы ваши коленные суставы двигались ровно настолько, чтобы они были сильными и здоровыми, и физиотерапия поможет вам в этом.
При остеоартрите коленного сустава мышцы, окружающие колено, могут стать слабыми, а коленные суставы — жесткими. Это затрудняет выполнение повседневных задач, например, ходьбу или вставание с постели.
Физическая терапия может помочь уменьшить боль, отек и жесткость при остеоартрите коленного сустава, а также улучшить функцию коленного сустава. Это также может помочь вам ходить, наклоняться, вставать на колени, приседать и сидеть. Фактически, исследование 2000 года показало, что комбинация мануальной физиотерапии и контролируемых упражнений имеет функциональные преимущества для пациентов с остеоартритом коленного сустава и может отсрочить или предотвратить необходимость хирургического вмешательства. 1
Физическая терапия может помочь уменьшить боль, отек и жесткость при остеоартрите коленного сустава, а также улучшить функцию коленного сустава.Это также может помочь вам ходить, наклоняться, вставать на колени, приседать и сидеть. Два основных типа физиотерапии — пассивный и активный — могут помочь сделать ваш коленный ОА более управляемым. При пассивном лечении большую часть работы выполняет физиотерапевт. Но при активном лечении вы выполняете больше работы, например, выполняете домашние упражнения.
Обычные пассивные методы лечения остеоартрита коленного сустава
- Холодная терапия: Холодная терапия уменьшает отек, уменьшая кровообращение.Например, физиотерапевт может приложить холодный компресс к коленному суставу.
- Тепловая терапия: Тепловая терапия увеличивает кровоток, уменьшая жесткость коленных суставов и мышц, окружающих колено. Например, физиотерапевт может положить теплую грелку на коленный сустав, чтобы улучшить кровообращение.
- Гидротерапия: Эта процедура, также иногда называемая водной терапией, использует воду для уменьшения симптомов остеоартрита коленного сустава.Есть несколько преимуществ гидротерапии. Например, вы можете делать легкие упражнения в воде (которые не будут раздражать суставы). Кроме того, просто нахождение в теплой воде может облегчить движение, а также помочь справиться с болью и другими симптомами ОА коленного сустава.
Общие активные методы лечения остеоартрита коленного сустава
- Упражнения для укрепления мышц: Ваш физиотерапевт покажет вам определенные упражнения, которые вы можете выполнять дома для укрепления мышц.Проработка мышц ног поможет укрепить коленные суставы. Одно только укрепление этих мышц может помочь уменьшить боль при ОА коленного сустава.
- Упражнения на гибкость: Поскольку ОА коленного сустава часто затрудняет движение, упражнения на гибкость очень важны. Их регулярное выполнение может помочь увеличить диапазон движений, сделать колени более гибкими и восстановить нормальную функцию коленного сустава.
Упражнения на укрепление и гибкость важны, потому что они могут помочь снять напряжение с колена.Узнайте больше о упражнениях при остеоартрозе коленного сустава в нашей статье о упражнениях для лечения остеоартрита коленного сустава.
Ваш физиотерапевт составит для вас план физиотерапии, который может включать сочетание пассивного и активного лечения остеоартрита коленного сустава.
Поговорите со своим врачом о начале программы физиотерапии для лечения остеоартрита коленного сустава, чтобы вы могли увеличить свою повседневную активность. Чем раньше вы лечите ОА коленного сустава, тем лучше в долгосрочной перспективе.
Обновлено: 17.11.15
Упражнения для лечения артроза коленного сустава
Текущее хирургическое лечение остеоартрита коленного сустава
Остеоатрит (ОА) коленного сустава является обычным явлением, и шансы заболеть ОА увеличиваются с возрастом. Его лечение должно быть изначально консервативным и требует как фармакологических, так и нефармакологических методов лечения. Если консервативная терапия не дает результатов, следует рассмотреть возможность хирургического вмешательства. Хирургические методы лечения ОА коленного сустава включают артроскопию, восстановление хряща, остеотомию и артропластику коленного сустава.Выбор наиболее подходящей из этих процедур зависит от нескольких факторов, включая местоположение, стадию ОА, сопутствующие заболевания с одной стороны и пациентов, страдающих с другой стороны. Часто проводится артроскопический лаваж и дебридмент, но он не влияет на прогрессирование заболевания. Если остеоартроз ограничен одним отделом, можно рассмотреть однокамерное эндопротезирование коленного сустава или остеотомию с разгрузкой. Они рекомендуются молодым и активным пациентам из-за рисков и ограниченной продолжительности полной замены коленного сустава.Тотальное эндопротезирование коленного сустава — распространенный и безопасный метод у пожилых пациентов с далеко зашедшим ОА коленного сустава. В этой статье кратко излагаются текущие стратегии хирургического лечения ОА коленного сустава с акцентом на последние разработки, показания и уровень доказательности.
1. Введение
Остеоартрит (ОА) коленного сустава является наиболее частым заболеванием суставов у пожилых людей, с распространенностью около 30% у взрослых в возрасте> 60 лет [1]. Около половины этих субъектов будут демонстрировать такие симптомы, как боль в суставах, скованность, излияние и ограничение функции суставов.Ожидается, что с нашим стареющим населением распространенность ОА в «развитом» мире будет расти. Ожидается, что в ближайшие десятилетия ОА станет четвертой ведущей причиной инвалидности [2].
Этиология ОА коленного сустава многофакторна и включает обобщенные конституциональные факторы (например, старение, пол, ожирение, наследственность и репродуктивные переменные), местные неблагоприятные механические факторы (например, травма сустава, злоупотребление на рабочем месте и во время отдыха, выравнивание и постменискэктомия) , и географические факторы.Существует значительный генетический компонент распространенности ОА коленного сустава, с оценками наследуемости по данным исследований близнецов 0,39–0,65 независимо от известных факторов окружающей среды или демографических факторов [3]. Генетические вариации приводят к изменениям хондроцитов, что приводит к остеоартриту [4, 5].
Диагностические критерии ОА коленного сустава включают анамнез пациента, физикальное обследование, рентгенологические и лабораторные данные [6]. Однако только стандартная рентгенограмма позволяет большинству пациентов поставить окончательный диагноз ОА коленного сустава.Другие радиологические методы, такие как компьютерная томография, УЗИ, МРТ и сканирование костей, могут предоставить альтернативную или дополнительную информацию [7].
Международное исследовательское общество ОА (OARSI) опубликовало глобальные, основанные на фактах, согласованные рекомендации по лечению ОА бедра и колена [8–10]. Из 51 метода лечения, описанного в рекомендациях OARSI, 35 были систематически пересмотрены, включая широкий спектр нехирургических методов (например, физиотерапия, фиксация, обучение, снижение веса, добавление вязкости, инъекции кортикоидов, анальгезия, другие противовоспалительные методы лечения и т. Д. .). Первоначальное лечение ОА коленного сустава должно быть консервативным. Операция может быть рассмотрена только в том случае, если симптомы сохраняются после соответствующего консервативного лечения. Варианты хирургического лечения: артроскопическая обработка раны, операция по восстановлению хряща, остеотомия с коррекцией оси и однокамерная или тотальная артропластика коленного сустава (TKA). Мы сосредоточимся на последнем.
Показания к операции и выбор лечения основаны на симптомах (например, боли и функции коленного сустава), стадии ОА и факторах, связанных с пациентом, таких как возраст, уровень физической активности и сопутствующие заболевания пациента.Радиологические признаки только ОА (сужение суставной щели, остеофиты и т. Д.) Не оправдывают хирургического вмешательства, которое показано только в сочетании с соответствующими симптомами. Наконец, степень страдания пациента в корреляции с радиологическими данными ОА определяет момент операции. Важно, что показание к операции при ОА всегда является относительным показанием. Только в случае прогрессирующей нестабильности коленного сустава, связанной с хирургическим лечением ОА (тотальное эндопротезирование коленного сустава), не следует излишне откладывать.Однако выбор хирургического лечения в общей практике лежит в основе личных, региональных и отраслевых предпочтений, поскольку показания для различных хирургических и нехирургических методов лечения мешают друг другу.
В данной статье обсуждаются принятые варианты хирургического лечения ОА коленного сустава. Мы ориентируемся на новейшие разработки, показания и эффективность выбранного лечения.
2. Хирургическое лечение ОА
2.1. Артроскопический лаваж и удаление раны
Артроскопические методы включают лаваж и удаление раны колена (например,g., бритье грубого хряща или сглаживание дегенерированного мениска). Теоретически артроскопия при ОА должна облегчить симптомы за счет удаления мусора и воспалительных цитокинов, вызывающих синовит [11, 12]. С помощью дебридмента можно удалить оторванные фрагменты мениска и отслоившиеся хрящевые лоскуты. Однако роль артроскопии в лечении ОА коленного сустава противоречива [8–10]. Несмотря на то, что он широко используется, отсутствуют доказательства, подтверждающие его значительную пользу. Контролируемое исследование Moseley et al. [13] показали, что сравнение артроскопического лаважа и хирургической обработки раны с хирургией стыда не дает никаких преимуществ.В 2007 году Сипарский и др. провел научно обоснованный обзор литературы по артроскопическому лечению ОА коленного сустава и обнаружил ограниченную поддержку его использования [14]. Dervin et al. [15] показали важность отбора пациентов перед артроскопией коленного сустава. Пациентам с явными поражениями мениска или хрящевых лоскутов может быть полезно хирургическое вмешательство. Другое исследование подтверждает, что у тщательно отобранных пациентов среднего возраста с артритом коленного сустава артроскопическая обработка раны может быть полезной для временного облегчения симптомов [16].Пациенты с менее обширным артритом по данным рентгенографии, менее тяжелым поражением суставного хряща и более молодым возрастом на момент операции имеют более высокую вероятность улучшения [17]. Короткая продолжительность боли и механических симптомов, а также рентгенологические стадии артрита от легкой до умеренной коррелируют с лучшим результатом [14, 18]. Однако в двух недавних Кокрановских обзорах [18, 19] артроскопического лаважа и хирургической обработки раны при ОА коленного сустава были выявлены только три хорошо спланированных исследования [10, 13, 16] и сделан вывод о том, что процедура не имеет преимуществ при ОА, возникающем в результате механического или воспалительного процесса. причины.На основании имеющихся данных артроскопический лаваж дает только краткосрочную пользу отдельным пациентам с легким рентгенологическим ОА и выпотом. Артроскопическая санация раны не должна использоваться в качестве рутинного лечения ОА коленного сустава, хотя пациенты с симптоматическими разрывами мениска и дряблым телом с симптомами блокировки могут быть лучше.
Количественная оценка преимуществ ограничена методологическими проблемами и ограниченным анализом во многих исследованиях [20]. Это амбулаторная процедура с менее серьезными потенциальными осложнениями, чем другие хирургические методы лечения ОА.Послеоперационное течение предсказуемо, и риск осложнений для большинства пациентов приемлемо мал. Это не препятствует более позднему окончательному хирургическому вмешательству, поэтому пациент и хирург могут подумать, что это «стоит попробовать». Тем не менее, это не может повлиять на прогрессирование ОА; это может быть только полезным инструментом для уменьшения боли у хорошо отобранных пациентов.
2.2. Методы восстановления хряща
Поврежденный суставной хрящ имеет ограниченную способность к заживлению или не имеет ее вообще [21]. Поэтому было предложено восстановление поверхности хряща.Однако восстановление хряща показано только при очаговых дефектах хряща, которые могут рассматриваться как предшественник ОА. Если дефект связан с расширенным хрящом, восстановление больше не показано. Различные методы можно разделить на методы стимуляции костного мозга, такие как абразия, сверление или микроперелом, а также на методы замены, такие как мозаичная пластика или трансплантация костно-хрящевого аллотрансплантата, а также на трансплантацию и комбинированные методы, такие как трансплантация лоскута надкостницы и имплантация аутологичных хондроцитов (ACI), аутологичная матрикс-индуцированный хондрогенез (AMIC).
2.2.1. Методы стимуляции костного мозга
Было показано, что проникновение в субхондральную пластинку способствует восстановлению хрящевой ткани; действительно, плюрипотентные стволовые клетки, происходящие из субхондрального костного мозга, могут способствовать хондрогенезу в области дефекта. Этот метод улучшает шлифовку хрящей и использует целебный потенциал организма. Приди был первым, кто описал технику, с помощью которой он использовал дрель для проникновения в часто склеротическую субхондральную пластинку [22].Раньше это предусматривалось артротомией сустава. В настоящее время это обычно делается с использованием техники микротрещин, описанной Steadman et al. [23–26]. Шилом проделываются отверстия, которые проникают на 2–4 мм в субхондральную пластинку на расстоянии 3–4 мм друг от друга. Это относительно просто и может быть выполнено артроскопически. Низкая стоимость и простота этой техники позволили ее широко использовать. К недостаткам метода можно отнести ограниченную ткань для восстановления гиалина, переменный объем восстанавливаемого хряща и возможное функциональное ухудшение [27].
2.2.2. Методы костно-хрящевой трансплантации
Реконструкция хрящевой поверхности или костно-хрящевых дефектов может быть выполнена путем трансплантации костно-хрящевых трансплантатов. Трансплантат может быть аутологичным или аллогенным. Аутологический перенос называется «мозаичной пластикой» или костно-хрящевой системой аутопереноса (OATS). Эти термины используются как синонимы. Для этого снимают одну или несколько цилиндрических «пробок» с периферии мыщелков бедренной кости на уровне пателлофеморального сустава и переносят пробки на дефект с помощью специального режущего устройства [28–35].Процедура может быть открытой (при больших дефектах) или артроскопической (при небольших дефектах) [36]. Преимущество этого метода заключается в использовании костно-хрящевого трансплантата, состоящего из гиалинового хряща, который заменяет также часто пораженную нижележащую кость. Незначительная интеграция, ограниченная доступность трансплантата и технические трудности — недостатки процедуры.
2.2.3. Имплантация аутологичных хондроцитов (ACI)
В 1994 году Бриттберг представил технику ACI, при которой культивируемые и пролиферирующие аутологичные хондроциты повторно имплантируются под надкостничный лоскут [37].Хондроциты собирают во время первой процедуры, при которой небольшой хрящевой зонд берется артроскопически. Затем хрящ переваривается, и собранные клетки размножаются в течение 3-4 недель в монослойной культуре перед имплантацией (рис. 1). В настоящее время мембрану надкостницы заменяют коллагеновой мембраной, а культуру клеток улучшают путем применения факторов роста или культивирования клеток в трехмерном коллагеновом каркасе, который можно непосредственно имплантировать [38]. Недостатками метода являются двухэтапная процедура и стоимость культивирования клеток.
Основными показаниями к методам восстановления хряща являются поражения хряща ограниченного размера, особенно у молодых пациентов. Если повреждение хряща имеет тенденцию к остеоартриту, процедуры восстановления хряща не показаны. Исключительное восстановление хряща не будет успешным, если смещение оси, нестабильность связок или надколенник являются основной причиной или связаны с поражением хряща. Еще раз один из ключевых элементов успешной операции — правильное показание.Диагностику способствуют усовершенствованные методы МРТ [39, 40]. Тем не менее, многие изолированные поражения хряща распознаются только при артроскопии [41]. Эти случайные находки (которые обнаруживаются при артроскопии или на основании МРТ) затрудняют выбор правильного лечения. Если присутствует некроз кости, хирургическая обработка раны и костная пластика должны рассматриваться как сопутствующие процедуры. Использование ACI и других методов шлифовки хрящей становится все более распространенным. Было показано, что распространенность симптомов после процедур восстановления хряща уменьшается.Были проведены рандомизированные контролируемые испытания, в которых сравнивали ACI, микропереломы и мозаичную пластику [42–44]. Тем не менее, данные о значительном различии между ACI и другими вмешательствами отсутствуют [45]. Требуются дополнительные рандомизированные контролируемые испытания хорошего качества с долгосрочными функциональными результатами.
2.3. Остеотомия вокруг колена
Остеотомия вокруг колена — общепринятый метод лечения однокамерного остеоартрита с сопутствующей варусной или вальгусной деформацией. Остеотомии проводятся с XIX века [46].Хотя остеотомии выполнялись регулярно в первой половине двадцатого века, настоящий прорыв произошел только с публикациями Джексона, Во, Гариепи, Ковентри и других в конце 1950-х и 1960-х [47–50]. Остеотомия стала стандартным методом лечения однокамерного ОА коленного сустава. Классическая остеотомия Ковентри представляла собой вальгизацию закрытого клина, включающую остеотомию малоберцовой кости, и выполнялась проксимальнее бугристости большеберцовой кости [50]. Долгое время это была наиболее широко используемая техника.В 1980-х и 1990-х годах остеотомия вокруг колена потеряла значение из-за успеха артропластики коленного сустава. По сравнению с артропластикой, остеотомия считалась сложной процедурой с непредсказуемым исходом и была связана со значительными осложнениями. В течение последнего десятилетия разработка новых пластин (особенно пластин с угловой стабильностью) и тенденция к остеотомии с открытым клином без вставки костного трансплантата и отсутствие риска повреждения малоберцового нерва привели к возрождению остеотомии вокруг колена. особенно для более молодых пациентов [51–53].
Остеотомии вокруг колена изменяют опорную ось нижней конечности [54]. Цель состоит в том, чтобы разгрузить поврежденный отсек и перенести весовую нагрузку с пораженных участков путем небольшой чрезмерной коррекции на вальгусную или варусную ось, чтобы уменьшить боль, замедлить дегенеративный процесс и отсрочить замену сустава [50, 55, 56].
Основой для удовлетворительного послеоперационного исхода является надлежащий отбор пациентов, включая оценку всех трех коленных отделов. Классический критерий включения — ОА одного отдела в сочетании с варусным или вальгусным выравниванием.Бедренно-пателлярный отсек не должен поражаться ОА. Обязательным условием является хорошая подвижность колена, а также стабильность связок. Нестабильность не является абсолютным противопоказанием, поскольку крестообразные связки можно реконструировать вместе с коррекцией оси [57, 58]. Возраст — важный фактор, который следует учитывать. Возраст> 60–65 лет является относительным противопоказанием, при этом необходимо учитывать биологический возраст и активность. Ожирение и хондрокальциноз не являются строгими противопоказаниями, но вероятность успеха и прогноз ухудшаются.Перед остеотомией рекомендуется подтвердить клинические и рентгенологические данные с помощью артроскопии коленного сустава, чтобы убедиться, что непораженный отдел здоров. Это можно сделать в той же процедуре.
Для коррекции оси нагрузки при однокомпонентном ОА коленного сустава используются различные методы. Это включает в себя остеотомию проксимальной головки большеберцовой кости и надмыщелковую остеотомию бедренной кости. Оба метода могут быть выполнены аддитивным (открытый клин) или субтрактивным (закрытый клин) методом и считаются установленными процедурами для лечения варусного и вальгусного ОА (рис. 2).Вальгизационная остеотомия обычно выполняется на проксимальном отделе большеберцовой кости, тогда как варизационная остеотомия выполняется на бедренной стороне. Если деформация расположена не возле сустава, а в диафизе длинных костей, коррекция должна производиться на месте деформации [57].
Классическая латеральная операция с закрытием клина требует остеотомии малоберцовой кости. Это связано с риском повреждения малоберцового нерва, составляющим до 11% [52]. Линия сустава имеет тенденцию заканчиваться в наклонном положении, что может затруднить последующее размещение большеберцового компонента при полной замене коленного сустава.
Методы медиального вскрытия головки большеберцовой кости менее сложны, точны и быстрее. Это преимущество, особенно при комбинированных вмешательствах с реконструкцией крестообразной связки. Требуется только один пропил, и корректировки во фронтальной плоскости можно комбинировать с корректировками в сагиттальной плоскости. В последние годы были разработаны новые пластины с угловой стабильностью. Повышенная стабильность этих пластин обеспечивает высокую стабильность, что делает ненужным костную пластику [51–53].Риск для малоберцового нерва незначителен.
Большинство длительных исследований техники вальгизации закрывающего клина показали хорошие результаты [59]. О хороших результатах сообщают в течение первых лет наблюдения с ухудшением со временем. Insall et al. показали, что при двухлетнем наблюдении 97% пациентов сообщают о хороших результатах, тогда как через пять лет удовлетворенность пациентов снижается до 85%, а через 9 лет — до 63% [60]. Только одно японское исследование показало очень высокую выживаемость (90%) через 15 лет [61].Длительное наблюдение за техникой открытого клина с использованием современных имплантатов с фиксирующими винтами недоступно. Тем не менее, доступные среднесрочные результаты обнадеживают, и это может стать новой стандартной процедурой вальгизации варусного ОА.
Остеотомия вокруг колена — эффективная процедура у молодых и активных пациентов с ранним остеоартритом одного отдела с ассоциированной варусной или вальгусной осью. Соответствующий отбор пациентов, хорошее предоперационное планирование, точная хирургическая техника и правильное послеоперационное ведение могут минимизировать частоту осложнений и привести к удовлетворительному результату.
Хотя остеотомия с разгрузкой является общепринятым и безопасным методом лечения, не проводилось исследований, чтобы сравнить ее с плацебо или только консервативным лечением. Однако было показано, что он эффективен для уменьшения боли и улучшения функций [8–10]. Необходимы дальнейшие сравнительные исследования, чтобы определить его показания в отношении однокамерного или тотального эндопротезирования коленного сустава.
2.4. Артропластика сустава
Артропластика сустава — это общепринятый, безопасный и экономичный метод лечения распространенного остеоартрита коленного сустава.Из-за своего необратимого характера артропластика сустава рекомендуется только пациентам, которым другие методы лечения не помогли или противопоказаны. Срок службы компонентов протеза ограничен примерно 15–20 годами, но выживаемость при однокамерном артропластике, как правило, ниже. Поэтому по возможности следует избегать артропластики у пациентов моложе 60 лет. Если ОА ограничивается одним отделом, может быть рассмотрена односторонняя артропластика коленного сустава (UKA) или остеотомия с разгрузкой, в противном случае показана ТКА с или без шлифовки надколенника.
2.4.1. Однокомпонентная артропластика коленного сустава (UKA)
Со времени одного из первых последующих исследований, опубликованных в 1970-х годах Marmor, UKA вызвала повышенный интерес [62]. UKA показан в случаях, когда OA затрагивает только один из трех отделов колена: медиальный тибиофеморальный, латеральный тибиофеморальный или пателлофеморальный отдел. Самый распространенный UKA заменяет контактные поверхности медиального тибиофеморального отсека двумя металлическими протезами и вставляет между ними полиэтиленовый вкладыш (рис. 3).Для успешного медиального UKA начальные условия должны обеспечивать хорошо сохранившийся латеральный отсек по отношению к мениску и хрящу [63]. Имплант не фиксируется в сагиттальной плоскости, поэтому стабильность протеза зависит от сохранности крестообразных связок [64]. Противопоказанием является значительное смещение конечности. Следует избегать чрезмерной коррекции контралатерального компартмента, поскольку это может привести к прогрессированию ОА и сохранению симптомов [65]. В равной степени недостаточная коррекция связана с повышенной вероятностью ревизии и клинической неудачи UKA [66].
Одним из преимуществ UKA является менее инвазивная хирургическая техника [67]. В частности, надколенник не вывернут и не поврежден разгибательный механизм, что позволяет гораздо быстрее выздороветь и раньше выписаться из больницы. Он также обеспечивает сохранение костного материала, более нормальную кинематику коленного сустава и улучшение физиологической функции [68].
Использование современных имплантатов и хирургических методов улучшило исход и выживаемость, связанные с медиальной UKA [67].Десятилетняя выживаемость при медиальной односторонней артропластике коленного сустава (UKA) сильно варьирует и колеблется от 80,2 до 98% [69, 70]. В любом случае UKA имеет значительно более низкую долговременную выживаемость, чем TKA [69]. Целевая группа UKA отличается от целевой группы TKA. UKA обычно проводится более молодым пациентам с менее тяжелым заболеванием, у которых конечная функция лучше, но у которых суставы изнашиваются быстрее.
Результаты лечения бокового однопалатного ОА коленного сустава сообщаются редко [71].Эти результаты менее предсказуемы, чем результаты медиального однопалатного ОА, несмотря на недавние улучшения в конструкции имплантата. Мыщелок бедренной кости подвергается большему смещению, чем медиальный мыщелок во время сгибания, что может привести к нестабильности и вывиху большеберцовой вставки в протезе с подвижной опорой [72]. Кинематика бокового отсека предполагает, что компонент с неподвижной опорой может предложить лучшее решение [73].
Изолированный остеоартрит бедра и надколенника встречается у 10% пациентов с остеоартритом коленного сустава.К основным расстройствам часто относятся предшествующая травма надколенника, нарушение трека надколенника, дисплазия блока и дегенерация, вызванная глубоким изгибом и чрезмерной нагрузкой. Лишь немногим пациентам выполняется изолированное протезирование пателлофеморального сустава, хотя это число увеличивается [74, 75]. Неудача изолированного эндопротезирования бедренно-пателлярной области встречается чаще, чем при замене бедренно-большеберцовой кости, и причины этого до сих пор четко не определены. ТКА следует рассматривать также при изолированном бедренно-пателлярном ОА, особенно у пожилых пациентов.
2.4.2. Тотальная артропластика коленного сустава (TKA) (Рисунок 4)
При распространенном остеоартрите коленного сустава, с вовлечением более чем одного отдела и неэффективностью консервативного лечения, было показано, что TKA является высокоэффективным лечением, которое приводит к значительному улучшению функционирования пациента и качество жизни, связанное со здоровьем [76]. До сих пор это была процедура первой линии при конечной стадии остеоартрита коленного сустава. Долгосрочные результаты ТКА были хорошо задокументированы с показателем выживаемости до 98% через 15 лет.[77]. По сообщениям, результаты у более молодых пациентов в основном хуже: выживаемость 76% через 10 лет [78].
Хотя ТКА эффективна при терминальной стадии артрита коленного сустава, послеоперационная боль возникает или сохраняется у одного из восьми пациентов, несмотря на отсутствие клинических или радиологических отклонений [79]. Основными осложнениями являются проблемы с бедренно-надколенниковой, расшатывание компонентов, инфекции и жесткость колена. Существует корреляция между существующими сопутствующими заболеваниями пациентов и объемом движений и состоянием коленного сустава после операции [80].Тем не менее, понимание лечения осложнений также значительно улучшилось. Показана важность факторов, связанных с пациентом, для исхода ТКА, и эти факторы должны влиять на предоперационное консультирование пациентов, ожидающих ТКА.
Одной из центральных проблем при стойких послеоперационных болях является бедренно-надколенниковый сустав. Однако общая польза от шлифовки надколенника никогда не была доказана, и показания к шлифовке надколенника четко не определены [81, 82].Осложнения, связанные с разгибательным механизмом и бедренно-пателлярным суставом, остаются основными неинфекционными показаниями для ревизии ТКА [83].
Из-за иногда неудовлетворительных результатов в последние годы были предприняты усилия по улучшению результатов тотального эндопротезирования коленного сустава. Эти стратегии включают в себя минимально инвазивную хирургию (MIS), интраоперационный контроль с помощью хирургии с компьютерной навигацией (CAS) или лучшего инструментария, улучшения биомеханического и анатомического дизайна имплантатов и улучшения фиксации имплантатов.
Минимально инвазивная хирургия (MIS)
В большинстве случаев артропластика коленного сустава имплантируется с помощью парапателлярной медиальной артротомии с расщеплением сухожилия четырехглавой мышцы и сетчатки / капсулы рядом с надколенником и сухожилием надколенника. Коленная чашечка обычно вывернута. Так называемая «миниинвазивная хирургия» позволяет избежать расщепления сухожилия четырехглавой мышцы. Доступ становится возможным благодаря подходу к средней части широкой мышцы живота (разделение широкой мышцы живота) или подходу к нижней части широкой мышцы живота. Избегают выворота надколенника.Разрез кожи сокращается до минимума. Считается, что эта стратегия обеспечивает более быстрое восстановление, более короткое пребывание в больнице, меньшее количество проблем с надколенником и улучшенные краткосрочные функциональные результаты [83, 84]. Критики подняли вопросы о смещении ноги, неправильном положении имплантатов и длине кривой обучения процедуре [85, 86]. Недавние РКИ не продемонстрировали существенного преимущества этого метода [87, 88].
Биомеханические и анатомические улучшения в конструкции имплантата
TKA плохо копирует физиологическую биомеханику коленного сустава.Ход движения в физиологическом колене определяется главным образом крестообразными связками, а в TKA — полиэтиленовой вставкой. Доступны различные типы вкладок, среди прочего, вращающиеся вкладки, вкладки с фиксированной опорой и задней стабилизацией [89]. Все они не могут имитировать исходное движение колена с откатом мыщелков бедренной кости на плато большеберцовой кости. Клинические результаты различных типов вкладок очень похожи [90]. Доступен новый дизайн вкладки, имитирующий две крестообразные связки, но отсутствует независимое долгосрочное наблюдение [91].
Анатомический дизайн имплантата был улучшен по следующим пунктам. Во-первых, анатомические исследования показали, что дистальный отдел бедренной кости более изменчив, чем предполагалось при проектировании имплантата. В частности, можно продемонстрировать разницу между мужчиной и женщиной. Были разработаны имплантаты с новым соотношением между лобным и переднезадним диаметром и адаптированными углами Q. Это приводит к расширению ассортимента имплантатов, но клиническая польза не была подтверждена в рандомизированных контролируемых исследованиях. Второе усовершенствование конструкции имплантата — это блокировка более анатомической формы, поддерживающая отслеживание надколенника.В-третьих, доступны имплантаты, которые должны способствовать большему сгибанию коленного протеза до 155 ° из-за большего смещения заднего мыщелка, влияющего на более высокое смещение задней части бедра и диапазон сгибания [92]. Ожидаемой разницы между стандартным коленным протезом и протезом с высокой степенью сгибания в РКИ не наблюдалось [93].
Фиксация имплантата
Цементная фиксация тотального эндопротезирования коленного сустава — стандартная процедура с хорошей долговременной долговечностью. Главное преимущество безцементной фиксации — более короткое время операции.В то время как клинические результаты не показывают существенной разницы между цементной и нецементной фиксацией, недавнее исследование обнаружило статистически значимое преимущество в улучшении выживаемости цементированных компонентов по сравнению с нецементированными компонентами, с периодом наблюдения от 2 до 11 лет [94]. Еще одно преимущество цементной фиксации состоит в том, что она менее сложна с технической точки зрения, поскольку для разрезов кости не требуется идеального прилегания к протезу, а цемент может заполнить дефекты [95]. Это менее затратно и предотвращает раннюю миграцию [96], которая потенциально может привести к поздним клиническим неудачам.Цемент также потенциально может создавать эффективный барьер для полиэтиленовых остатков, образующихся на суставной поверхности, тем самым предотвращая остеолиз и расшатывание имплантата [97].
Интраоперационный контроль
Новой технологией, внедренной в TKA, является компьютерная хирургия (CAS). Компьютерная навигация улучшает точность послеоперационного выравнивания после ТКА [98]. Несмотря на этот эффект, пациенты, перенесшие ТКА с навигацией, не показали улучшенных клинических результатов через два года по сравнению с пациентами, которым проводилась традиционная ТКА.Исследования не выявляют ранних преимуществ управляемой ТКА, и необходимы долгосрочные исследования, чтобы выявить улучшения выживаемости, связанные с улучшением выравнивания конечностей [99]. К недостаткам можно отнести более длительное время работы, время обучения, составляющее около 25–30 операций, и стоимость новой технологии.
Еще один новый метод основан на использовании режущих блоков для конкретного пациента, которые созданы с использованием МРТ пациента или компьютерной томографии в качестве шаблона. Эти отдельные режущие блоки позволяют выполнить точную резекцию кости, адаптированную к уникальным формам и углам сустава.Операция облегчается, уменьшается кровопотеря и сокращается продолжительность операции. Недостатками этой новой технологии являются дополнительные затраты на режущий блок и тот факт, что метод основан исключительно на костных ориентирах, не обращая внимания на баланс связок.
Благодаря развитию хирургических методов и усовершенствованной технологии имплантатов результаты и функция TKA улучшились. Для успешного результата важно хорошее совмещение большеберцовых и бедренных компонентов (а также правильное отслеживание надколенника), что приводит к меньшему износу протеза [100].ТКА стала успешным средством лечения запущенного и симптоматического ОА коленного сустава, особенно у пожилых пациентов. Многие новые разработки и разработки были представлены и выведены на «медицинский рынок» за последние годы. Они интересны с научной точки зрения и требуют тщательного соблюдения. Тем не менее, большинству из них не удается доказать клиническое улучшение за доступный период наблюдения. К сожалению, производители регулярно неправильно используют эти технологии в рекламных целях, даже несмотря на отсутствие доказательств улучшения уровня остаточной боли, долговечности артропластики и функции коленного сустава.
Сравнение гиалуроновой кислоты и богатой тромбоцитами плазмы, внутрисуставной инфильтрации при лечении гонартроза.
HA — это обычно используемая смазка для суставов. — Kelly Cunningham, MD
Abstract
ИСТОРИЯ ВОПРОСА: Артроз особенно распространен в коленном суставе. Инфильтрационное лечение гонартроза — один из наиболее широко используемых методов в ортопедической практике.
ЦЕЛЬ: Сравнить клинический ответ на лечение гиалуроновой кислотой (HA) и плазмой, богатой тромбоцитами (PRP) в 2 группах пациентов с гонартрозом.
ДИЗАЙН ИССЛЕДОВАНИЯ: Рандомизированное контролируемое исследование; Уровень доказательности: 1.
МЕТОДЫ: В это исследование было включено 120 пациентов с клинически и рентгенологически подтвержденным гонартрозом. Гонартроз был классифицирован с использованием шкалы радиографической классификации Келлгрена-Лоуренса. 120 пациентов были рандомизированы в 2 группы исследования в соотношении 1: 1: 60 пациентов получили 4 внутрисуставные инъекции PRP (в частности, аутологичной кондиционированной плазмы [ACP], 5.5 мл), и 60 пациентов получили 4 внутрисуставных инъекции ГК (20 мг / 2 мл). Врач без ослепления выполнял инфильтрацию один раз в неделю в течение 4 недель в колено, пораженное клинически значимым гонартрозом (в обеих группах). Все пациенты были оценены по шкале Western Ontario and McMaster (WOMAC) до инфильтрации и через 4, 12 и 24 недели после первой инъекции.
РЕЗУЛЬТАТЫ: Лечение местной инъекцией ACP оказало значительный эффект вскоре после окончательной инфильтрации и постоянно улучшающийся устойчивый эффект до 24 недель (оценка WOMAC, 65.1 и 36,5 в группах HA и ACP соответственно; P <0,001), где клинические результаты были лучше по сравнению с результатами с HA. В группе HA худшие результаты были получены для гонартроза III степени, тогда как клинические результаты, полученные в группе ACP, не показали статистически значимой разницы в отношении степени гонартроза. Средние баллы WOMAC для гонартроза III степени составили 74,85 в группе HA и 41,20 в группе ACP (P <0,001).
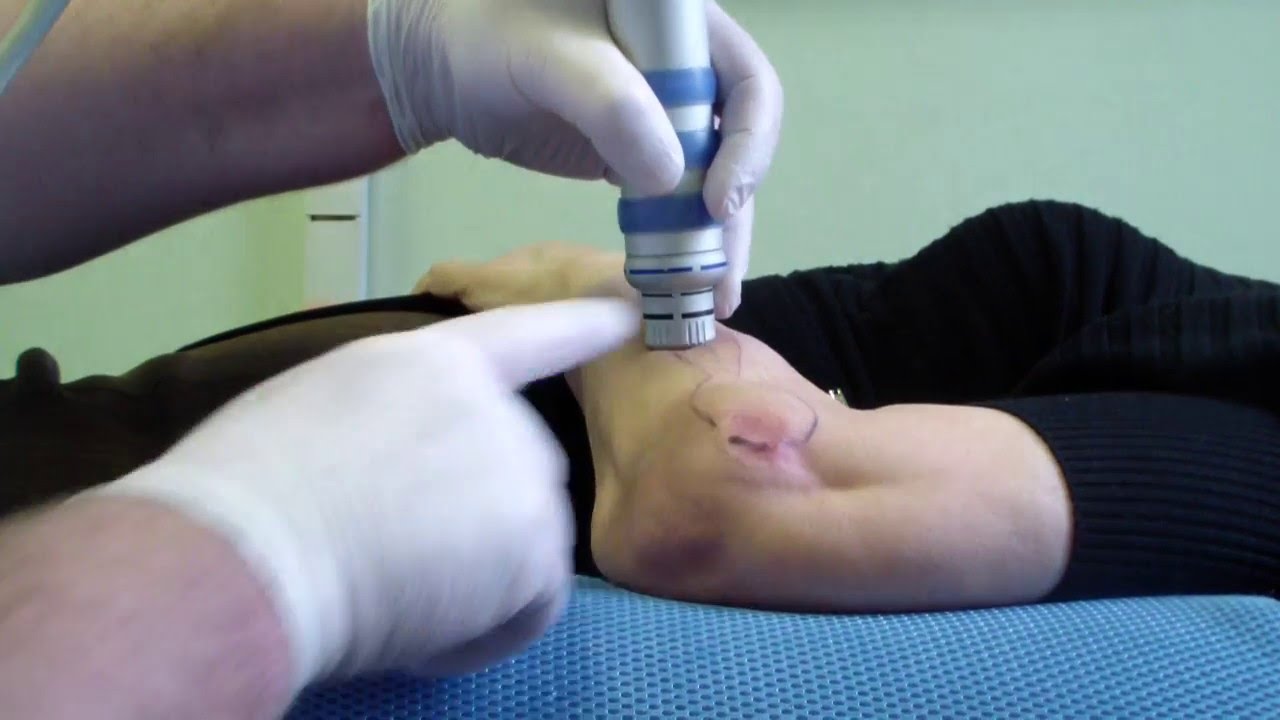
 Это полностью безболезненная процедура, с низкой дозой радиационного излучения (по сравнению с облучением при злокачественных образованиях), а ее продолжительность занимает всего несколько секунд. Для равномерного распределения дозы колено облучается с двух сторон одновременно. Рентгенотерапия при остеоартрозе оказывает противовоспалительное действие и снимает боль. Подобное лечение имеет отсроченный во времени эффект, а после первого облучения боль может даже усилиться. Но это лишь свидетельствует о том, что пациент реагирует на терапию. В течение нескольких недель боль в суставе становится заметно менее выраженной.
Это полностью безболезненная процедура, с низкой дозой радиационного излучения (по сравнению с облучением при злокачественных образованиях), а ее продолжительность занимает всего несколько секунд. Для равномерного распределения дозы колено облучается с двух сторон одновременно. Рентгенотерапия при остеоартрозе оказывает противовоспалительное действие и снимает боль. Подобное лечение имеет отсроченный во времени эффект, а после первого облучения боль может даже усилиться. Но это лишь свидетельствует о том, что пациент реагирует на терапию. В течение нескольких недель боль в суставе становится заметно менее выраженной.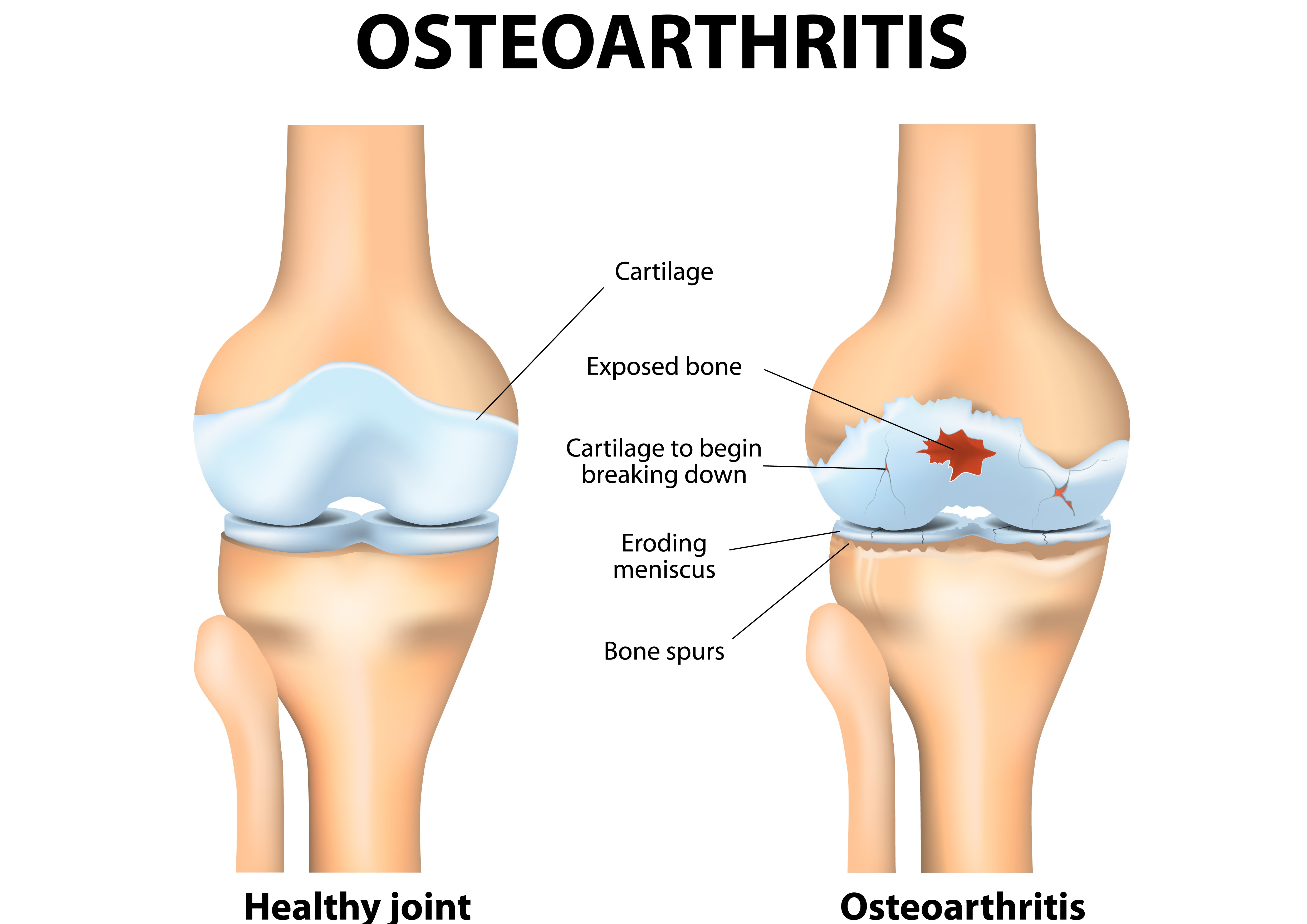 При этом здоровые участки (кость, боковые и задняя крестообразная связка) сохраняются. Целью является максимально возможное сохранение собственных тканевых структур организма при минимальном внедрении инородного компонента (имплантата). Это позволяет сократить сроки реабилитации и значительно увеличить мобилизацию пациентов и, тем самым, улучшить качество жизни на 20-30 лет.
При этом здоровые участки (кость, боковые и задняя крестообразная связка) сохраняются. Целью является максимально возможное сохранение собственных тканевых структур организма при минимальном внедрении инородного компонента (имплантата). Это позволяет сократить сроки реабилитации и значительно увеличить мобилизацию пациентов и, тем самым, улучшить качество жизни на 20-30 лет.