Оптимальный выбор методов лучевой диагностики
Порядок направления пациентов на исследования в кабинеты спиральной рентгеновской и магнитно-резонансной томографии. (специалистам)
1. Лечащим врачам, при направлении больных на данные диагностические методы исследования, необходимо учитывать диагностическую эффективность каждой методики при обследовании различных органов и систем и показания к их проведению.
(При затруднении с выбором наиболее информативного метода диагностики рекомендована консультация со специалистами кабинетов КТ/МРТ.)
2. Все исследования проводятся строго при наличии клинических показаний, либо при сомнительных данных других методик (УЗИ, КТ, МРТ, сцинтиграфия и др.), подготовке к оперативным вмешательствам, контроле проводимого лечения (в том числе ответ на проводимую химиотерапию).
3. Окончательное решение о проведении исследования принимает врач–рентгенолог кабинета КТ/МРТ, он же определяет необходимые методики и объём проводимого исследования (в том числе, выполнение исследования с использованием контрастных веществ).
4. При проведении внутрисосудистых контрастных исследований с применением рентгеноконтрастных веществ обязательным является заполнение направления информированного согласия пациента на исследование установленной формы. В настоящее время в лечебных учреждениях используются следующие методы лучевой диагностики:
1. Рентгенодиагностика традиционная (рентгенография, рентгеноскопия). Метод основан на регистрации рентгеновского излучения, прошедшего через тело пациента в одной проекции.
2. Рентгеновская компьютерная томография (МСКТ/КТ). Метод основан на получения послойных изображений в аксиальной проекции с дальнейшими трёхмерными и мультипланарными реконструкциями.
3. Магнитно-резонансная томография (МРТ). Метод получения послойных и объёмных изображений основан на явлении ядерного магнитного резонанса.
4. Ультразвуковая диагностика (УЗД). Метод получения послойных изображений основан на изучении отражения ультразвуковых волн от тканей.
По способности вызывать ионизацию тканей методы лучевой диагностики делятся на ионизирующие (КТ, рентгеновские и радионуклидные исследования) и неионизирующие (УЗИ, МРТ).
Выбирая для решения конкретной клинической задачи тот или иной метод диагностики, врач должен опираться на следующие критерии:
1. Информативность метода. Диагностика не должна идти от простого к сложному, необходимо сразу выбирать наиболее информативные методы.
2. Вредность для пациента. Во всех случаях применения рентгеновского (ионизирующего) или инвазивного исследования должно быть серьёзное обоснование. Рентгеновское исследование должно быть заменено на радиационно безопасное УЗИ в случаях сопоставимости методов.
3. Экономические затраты. Ценность метода прямо пропорциональна его информативности и обратно пропорциональна вреду и стоимости. Применение дорогостоящих технологий МРТ и МСКТ оправдано только при строгом клиническом обосновании.
4. Доступность метода.
Заболевания центральной нервной системы
Лучевая диагностика патологии позвоночника и спинного мозга
Позвоночник первично исследуют методом рентгенографии (стандартная спондилография в двух проекциях). При необходимости уточнения естественной подвижности в позвоночных сегментах выполняют функциональные снимки.
Противопоказаниями для функциональных проб являются:
· Неврологический дефицит (двигательные и чувствительные нарушения).
· Костные повреждения:
Для определения типа и величины деформации позвоночника проводится спондилография.
МРТ рекомендуется при подозрении на миелопатию.
В диагностике дегенеративно-дистрофических заболеваний (остеохондроз, спондилёз, спондилартроз ) основной метод визуализации – рентгенография.
 КТ и МРТ не должны применяться для диагностики указанной патологии.
КТ и МРТ не должны применяться для диагностики указанной патологии.МРТ — «золотой стандарт» для исследования межпозвонковых дисков -применяется в диагностике грыж межпозвонкового диска.
В поясничном отделе допустимо (при невозможности МРТ) применение КТ для выявления грыж.
В шейном и грудном отделах применение КТ для выявления грыжи межпозвонкового диска не показано из-за низкой информативности. МРТ-метод выбора в дифференциальной диагностике послеоперационных фиброзных изменений от рецидива грыжи, причем применение контрастирования повышает точность.
Методом выбора для исследования связок, нервных корешков, структур позвоночного канала является МРТ. МРТ –«золотой стандарт» диагностики поражений спинного мозга любого генеза.
КТ не применяют для обзорного исследования отделов позвоночника. КТ назначается строго учитывая локализацию изменений в ограниченном числе сегментов позвоночника и изменений паравертебральных мягких тканей исследуемой зоны.

В диагностике опухолей позвоночника при выявлении на спондилограммах изменений, подозрительных на опухоль, применяют КТ и МРТ для уточнения выявленного поражения и стадирования опухоли.
В диагностике воспалительных заболеваний
(специфические и неспецифические спондилиты) позвоночника необходимо комплексное лучевое исследование: рентгенография, КТ, МРТ с учётом информативности и показаний для каждого метода в зависимости от стадии и локализации заболевания.В диагностике туберкулёзного спондилита (спондилитов другой этиологии) необходимо комплексное применение лучевых методов. Первично должны быть выполнены рентгенография и МРТ.
Традиционные рентгенотомографические методы эффективны в развёрнутой стадии заболевания. МРТ информативна уже на ранних фазах спондилита и метод выбора для выявления причин неврологических нарушений. КТ применяется дополнительно после выполнения рентгенографии и МРТ в качестве метода, уточняющего характер патологических изменений.
КТ и МРТ эти методы не конкурирующие, а дополняющие друг друга.
В качестве первичного метода диагностики поражений головного мозга возможно применение КТ.
Внутривенное контрастирование повышает точность диагностики.
МРТ первично рекомендуется в выявлении изменений в задней черепной ямке, стволовых и срединных структурах при наличии соответствующей неврологической симптоматики.
КТ более информативна для диагностики костных поражений черепа, внутричерепных обызвествлений, свежего внутричерепного кровоизлияния.
Черепно-мозговая травма (ЧМТ)
Пациентам с черепно-мозговой травмой в первую очередь проводится КТ как наиболее эффективный метод диагностики повреждений костных структур основания черепа, головного мозга, его оболочек и сосудов. При тяжелой ЧМТ выполняют КТ по срочным показаниям.
Показания к КТ при ЧМТ:
1. Наличие очаговой неврологической симптоматики.
Наличие очаговой неврологической симптоматики.2. Нарушения сознания.
3. Проникающие повреждения.
4. Вдавленные переломы черепа.
5. Выявление крови при люмбальной пункции.
6. Нарастающая симптоматика в первые дни после травмы.
7. Механизм травмы, характерный для повреждения головного мозга.
МРТ применяют в диагностике ушибов головного мозга, подострых и хронических кровоизлияний (с 3-х суток и позднее после травмы), диффузно-аксональных повреждений (ДАП).
МРТ наиболее информативный метод визуализации отёка головного мозга, ДАП у больных, находящихся в коме.
Традиционная краниография информативна в диагностировании переломов костей свода черепа. Рентгенография может не выполняться после проведения КТ, при которой выявлены костные повреждения или показания для экстренной операции.
Опухоли головного мозга
Ни один из методов лучевой диагностики не является всеобъемлющим для диагностики опухоли.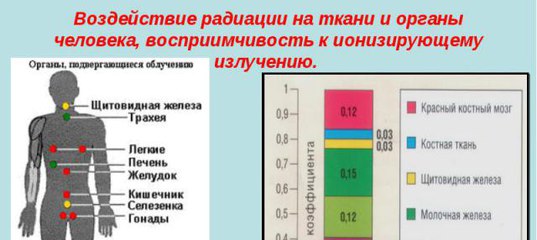
Установление томографическими методами вероятного гистологического строения опухоли не всегда возможно.
В диагностике опухолей задней черепной ямки, гипофиза первично рекомендуется МРТ.
В качестве послеоперационного контроля радикальности удаления опухоли рекомендовано МРТ с контрастированием.
Метастазы в головном мозге
В диагностике метастазов информативны МРТ и КТ с контрастированием. При выявлении одиночного объёмного образования, подозрительного на метастаз, при отсутствии данных за первичную злокачественную опухоль, требуется комплексное обследование, направленное на поиск первичной опухоли.
Опухоли черепно-мозговых нервов
Метод выбора при подозрении на невриному – МРТ.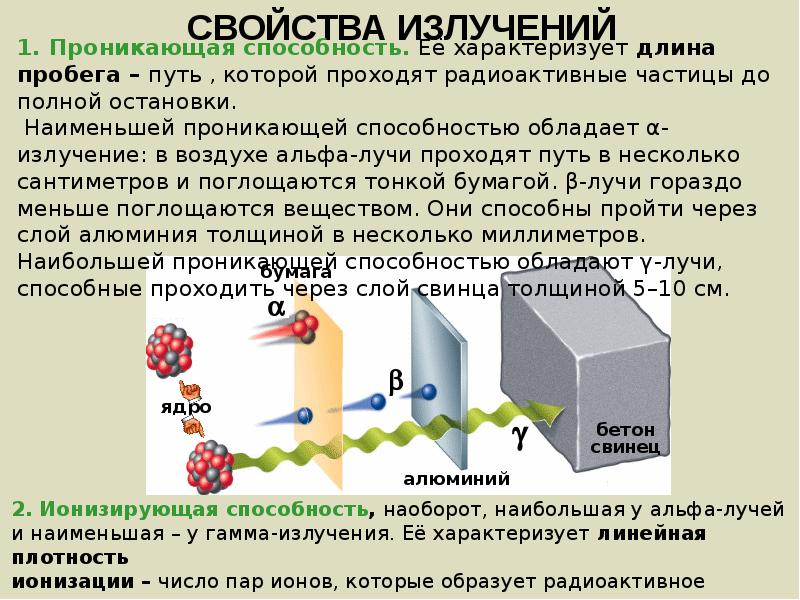 При МРТ визуализируются слуховые (VII-VIII раздельно не дифференцируются) и, не всегда, тройничные нервы (V пара).
При МРТ визуализируются слуховые (VII-VIII раздельно не дифференцируются) и, не всегда, тройничные нервы (V пара).
Для выявления деструкции пирамиды височной кости дополнительно – КТ.
Сосудистые заболевания
При острых нарушениях мозгового кровообращения (ОНМК) любого типа первично показана КТ (дифференциальная диагностика геморрагического и ишемического инсульта). Это принципиально, т.к. при ОНМК по ишемическому и геморрагическому типу лечение различное.
КТ выявляет минимальные кровоизлияния немедленно после образования, поэтому при клинической картине ОНМК и отсутствии на томограммах изменений, характерных для геморрагического инсульта, предполагается ишемический инсульт (ИИ).
Использование КТ или МРТ зависит от момента начала инсульта, т.е. сроки выявления ишемического поражения мозга имеют первостепенное значение для выбора метода визуализации.
В острой стадии развития ишемического инсульта (до 6 часов) повреждение мозговой ткани на нативной КТ определить невозможно. В этот период с целью уточняющей диагностики ишемического инсульта и дифференциации зон необратимого/обратимого повреждения мозговой ткани необходимо проведение перфузионной КТ (при отсутствии КТ-признаков геморрагического инсульта). Кроме того, перфузионная КТ позволяет определить степень снижения мозгового кровотока при ишемическом инсульте. При невозможности перфузионной КТ показана МРТ с оценкой диффузии (МРТ-ДВИ) и состояния интракраниальных артерий (МРА).
В первые сутки заболевания МРТ-ДВИ более информативна, чем нативная КТ. В период с начала вторых суток до 8 суток от начала заболевания информативны как КТ, так и МРТ.
Повторные КТ/МРТ не применяют для наблюдения за течением заболевания в процессе лечения.
 Однако КТ рекомендуется для диагностики осложнений инсульта (объёмное воздействие, вторичное кровоизлияние, развитие гидроцефалии).
Однако КТ рекомендуется для диагностики осложнений инсульта (объёмное воздействие, вторичное кровоизлияние, развитие гидроцефалии).
При подозрении на острое внутричерепное кровоизлияние первично показана КТ
Выявляемость субарахноидальных кровоизлияний (САК) при КТ наиболее максимальна в первые сутки, затем она постоянно снижается и через 1-2 недели признаки кровоизлияния практически не определяются. КТ-ангиография значительно повышает эффективность выявления локализации и причины нетравматического кровоизлияния, однако наличие кровоизлияния затрудняет обнаружение малых артериальных аневризм.
МРТ-диагностика внутримозговых и субарахноидальных кровоизлияний в первые сутки затруднительна. В подострой (3-14 день) и хронической стадиях (больше 14 дней) МРТ высоко информативна.
В диагностике вариантов и пороков развития сосудов головного мозга, в т.ч. артериальных аневризм и сосудистых мальформаций – первично рекомендуется МРТ в сочетании с МР-ангиографией.
КТ-ангиография – метод уточняющей диагностики, особенно при неубедительных данных МРТ.
В сомнительных случаях и при планировании оперативного лечения выполняется церебральная ангиография.
Для исследования экстракраниальных сосудов (ветви дуги аорты) первично применяют дуплексное УЗ-исследование. Уточняющими методами выявленных патологических изменений являются МРА и КТА.
Воспалительные заболевания (абсцесс, менингит) — МРТ или КТ с контрастированием
Вирусные инфекции (энцефалиты) МРТ –метод выбора.
Паразитарные инфекции мозга – КТ. При подозрении на паразитарное поражение мозга необходимо дополнительно КТ-исследование грудной клетки и брюшной полости (диагностика легких и печени).
Демиелинизирующие заболевания (рассеянный склероз и др.) МРТ – метод выбора + контрастирование
Эпилепсия — МРТ и/или КТ.
Гидроцефалия — МРТ или КТ
Дегенеративные и метаболические заболевания — МРТ и КТ.
Заболевания головы и шеи
Заболевания околоносовых пазух. Для визуализации околоносовых пазух первичный метод – рентгенография. При хронических атипично протекающих синуситах, а также при невозможности эндоскопического осмотра, с целью уточнения характера выявленных изменений и дифференциальной диагностики применяют КТ. МРТ для уточняющей диагностики.
Показания для КТ
· Хронический атипично протекающий риносинусит.
· Диагностика вариантов развития пазух.
· Определение распространенности патологического процесса.
· Оценка состояния глубоких мягкотканных структур.
· Осложнения риносинусита (субпериостальный абсцесс, остеомиелит костей черепа и др.).
· Полипы и полипоз полости носа и околоносовых пазух.
· Гранулёматоз Вегенера.
· Опухоли околоносовых пазух.
· Планирование хирургического и/или лучевого лечения.
Показания для МРТ
· Для выявления интракраниального и интраорбитального осложнения и распространения синусита.
· В дифференциальной диагностике грибкового процесса от воспаления другой этиологии.
· Дополняет КТ в комплексной диагностике и оценке распространённости опухолей.
Заболевания глаза
В диагностике заболеваний и повреждений глаза и глазницы применяют УЗИ, КТ и МРТ.
УЗИ и МРТ – методы выбора для выявления отслойки сетчатки. Кроме того, УЗИ применяют в диагностике гемофтальма и внутриорбитальных инородных тел.
КТ и МРТ показаны в диагностике опухолей и воспалительных процессов.
КТ дополняет МРТ в выявлении обызвествлений и костно-деструктивных изменений. МРТ используют для диагностики неметаллических инородных тел глаза, подострых и хронических кровоизлияний (8-21 сутки).
МРТ противопоказана при металлических инородных телах в орбите.
Основные показания для КТ и МРТ
· Сосудистые опухоли орбиты – КТ с контрастированием. МРТ для уточнения.
· Дермоид и эпидермоид орбиты – КТ. МРТ для уточнения.
МРТ для уточнения.
· Идиопатическая псевдоопухоль орбиты – МРТ.
· Опухоли зрительного нерва – МРТ. КТ для уточнения.
· Неврит зрительного нерва – МРТ метод выбора.
· Меланома глазного яблока – первично УЗИ. МРТ для уточнения.
· Ретинобластома –комплексное МРТ/КТ -исследование.
· Опухоли слёзной железы – КТ. МРТ для стадирования злокачественной опухоли.
· Лимфопролиферативные заболевания глазницы -МРТ.
· Абсцесс орбиты – МРТ, особенно при подозрении на внутримозговые осложнения (МРТ), КТ для оценки костных изменений стенок глазницы.
· Травма глаза – КТ метод выбора: определение повреждений стенок глазницы, выявление инородных тел, острых внутриглазничных кровоизлияний.
Заболевания мягких тканей шеи
УЗИ –первичный метод визуализации кист, воспалительных изменений и лимфатических узлов (в т.ч. непальпируемых). При неубедительных УЗ-данных показана КТ.
МРТ с контрастом –метод выбора для выявления и оценки распространённости опухолевого процесса.
КТ с контрастом при невозможности выполнения МРТ.
Заболевания уха
При аномалиях развития и болезнях среднего и внутреннего уха метод выбора –КТ.
Специальные рентгенографические укладки по Шулеру, Майеру, Стенверсу при возможности выполнения КТ второстепенны по информативности.
При подозрении на перелом височной кости метод выбора -КТ.
Для диагностики внутричерепных осложнений заболеваний среднего уха показана и МРТ.
МРТ рекомендуется для выявления поражения вестибуло-кохлеарных нервов у больных с нейросенсорной тугоухостью.
Заболевания глотки и гортани
Для уточнения распространенности опухолевого или воспалительного процесса, оценки регионарных лимфатических узлов и получения дополнительной информации -МРТ или КТ с контрастом.
В лучевой диагностике заболеваний гортани первоначально рекомендуется выполнить боковую рентгенограмму шеи и линейную томографию гортани. Эта методика достаточно информативна, особенно для диагностики подсвязочных стенозов гортани и стенозов трахеи.
Эта методика достаточно информативна, особенно для диагностики подсвязочных стенозов гортани и стенозов трахеи.
Воспалительные заболевания челюстей
Лучевая диагностика остеомиелита зависит от стадии. В острую стадию рентгеновская картина негативна. При УЗИ в этот период возможно выявление скопления гноя под надкостницей и в мягких тканях. Первые рентгенологические признаки появляются через 10-14 дней от начала заболевания.
В подострой и хронической стадиях проводят рентгенографические исследования, при необходимости КТ.
Новообразования челюстей
В диагностике одонтогенных и неодонтогенных кист и доброкачественных опухолей первично показаны рентгенограммы; при необходимости дополнительно используют КТ.
Гемангиома
(в мягких тканях или внутри кости) выявляется рентгенографически, КТ и КТА применяют для определения её распространённости.
Рентгенография –основной метод диагностики фиброзной дисплазии.
Злокачественные опухоли (рак, саркома, метастазы) –основные методы рентгенография и КТ. МРТ позволяет выявить рак слизистой оболочки верхнечелюстной пазухи на ранней стадии (до появления костной деструкции) и на поздней стадии дополняет КТ в оценке распространённости процесса.
В диагностике рецидивов применяют комплексное рентгенологическое исследование: рентгенография, КТ и МРТ.
Заболевания слюнных желез
Лучевая диагностика заболеваний слюнных желез основывается на применении УЗИ (в первую очередь) и сиалографии.
При осложнениях и подозрении на злокачественное поражение применяют МРТ.
Заболевания височно-нижнечелюстного сустава (ВНЧС)
В лучевой диагностике заболеваний ВНЧС (деформирующий артроз, артрит) применяют рентгенографию, КТ и МРТ.
МРТ–метод выбора в диагностике функциональных нарушений ВНЧС.
Травмы челюстно-лицевой области (ЧЛО)
1. Больным с изолированными повреждениями лицевого скелета показана рентгенография в стандартных и/или специальных укладках.
Больным с изолированными повреждениями лицевого скелета показана рентгенография в стандартных и/или специальных укладках.
2. Для поиска рентгеноконтрастных (металлосодержащих) инородных тел ЧЛО первично показана рентгенография.
3. КТ – метод выбора для уточнения локализации инородного тела по отношению к структурам орбиты.
4. КТ показана в случаях внутричерепных инородных тел.
5. КТ — метод выбора при множественной и комбинированной травме, сложных случаях.
6. КТ показана при огнестрельных и взрывных повреждениях лицевого скелета.
7. КТ показана при выборе тактики лечения и планировании пластических операций.
Смирнов В.В. — к.м.н, врач высшей квалификацинной категории.
Саввова М.В. — врач высшей квалификацинной категории.
Радиационная защита помещений с помощью баритовых строительных материалов
Баритобетон и баритовые штукатурные составы АЛЬФВАПОЛ™
- АЛЬФАПОЛ ШТ-БАРИТ — смесь сухая штукатурная магнезиально-баритовая.

- АЛЬФАПОЛ М-БАРИТ — смесь сухая напольная магнезиально-баритовая (баритобетон).
- АЛЬФАПОЛ ВШТ-БАРИТ — смесь сухая штукатурная цементно-баритовая для изоляции рентген-кабинетов и иных помещений с источниками ионизирующего излучения
- АЛЬФАПОЛ В-БАРИТ — смесь сухая напольная цементно-баритовая (баритобетон).
Радиационная защита помещений с помощью магнезиально-баритовых строительных материалов
Радиоактивностью в той или иной степени обладает всё, что нас окружает, даже сам человек. Ионизирующие облучения присутствовали в космосе задолго до возникновения нашей планеты, и радиоактивные вещества входят в её состав с самого рождения. Радиоактивность можно считать естественной средой обитания человека, если она не превышает определённых уровней. На Земле имеются участки территории со значительно повышенным уровнем радиационного фона, однако там не наблюдается серьёзного отрицательного воздействия радиации на здоровье населения, поскольку для них это является естественной средой.
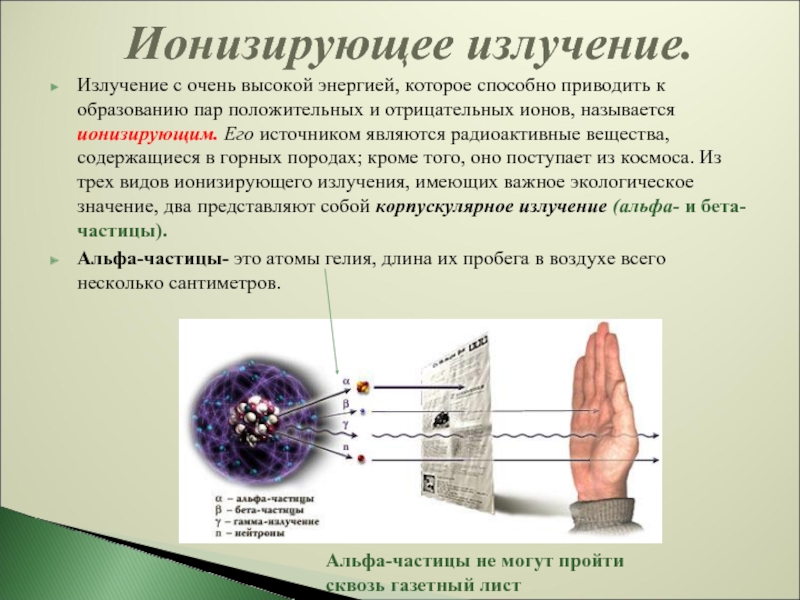
Развитие науки, особенно в области энергетики, космических и ядерных технологий способствует созданию новых, техногенных источников радиоактивного излучения. Они могут содержать радиоактивные вещества, полученные в ядерных реакторах специально или являющиеся побочными продуктами ядерных реакций. Искусственно получаемые радиоактивные изотопы воздействуют на живую ткань посредством испускаемых ими при распаде альфа-, бета- и гамма- лучей и нейтронов. Наибольшей проникающей способностью обладают гамма — лучи, представляющие собой поток фотонов, и нейтронное излучение. Рентгеновское излучение по своим физическим свойствам аналогично гамма — излучению, но отличается по способу генерации. Это электромагнитное излучение образуется в специальной вакуумной трубке при торможении (ударе о мишень) быстрых электронов.
Вопросы защиты от проникающей радиации приходится решать при проектировании любых медицинских учреждений: кабинетов рентгенографии, томографии, стоматологических кабинетов с наличием рентгеновского оборудования. Кроме того, ионизирующее излучение является частым спутником современных исследовательских и испытательных центров, производственных цехов и лабораторий. Материалы, ограждающие людей от вредного воздействия радиации, призваны снижать её уровень до допустимых значений. Эти материалы должны обладать высокой плотностью, поскольку именно от неё главным образом зависит длина пробега радиоактивных частиц в среде распространения. Хорошей защитой от радиоактивных излучений являются экраны из тяжёлых металлов, в частности свинца и свинцовых материалов. Но, надо заметить, они являются достаточно вредными для здоровья человека. Использование специальных радиационнозащитных бетонов и штукатурок в строительных конструкциях является альтернативой свинцовым материалам.
Кроме того, ионизирующее излучение является частым спутником современных исследовательских и испытательных центров, производственных цехов и лабораторий. Материалы, ограждающие людей от вредного воздействия радиации, призваны снижать её уровень до допустимых значений. Эти материалы должны обладать высокой плотностью, поскольку именно от неё главным образом зависит длина пробега радиоактивных частиц в среде распространения. Хорошей защитой от радиоактивных излучений являются экраны из тяжёлых металлов, в частности свинца и свинцовых материалов. Но, надо заметить, они являются достаточно вредными для здоровья человека. Использование специальных радиационнозащитных бетонов и штукатурок в строительных конструкциях является альтернативой свинцовым материалам.
Баритовые рентгенозащитные растворы применяют вместо рольного свинца для изоляции стен, потолков и полов рентгеновских кабинетов и других помещений с источниками излучения. Это тяжелые растворы плотностью свыше 2200 кг/м3. В качестве вяжущих используется портландцемент или шлакопортландцемент и специальные тяжелые заполнители — барит, железные руды (магнезит, лимонит и т. п.) в виде песка крупностью не более 1,25 мм. Барит включается в состав бетонных смесей (баритобетонов, баритовой штукатурки) в силу его способности поглощать рентгеновское излучение. При использовании барито — бетонных составов на портландцементе для обеспечения должной радиационной безопасности помещений требуется весьма значительная толщина слоя. К тому же баритовые составы на цементном вяжущем в процессе эксплуатации осыпаются, растрескиваются, и потому сами нуждаются в дополнительным защитном покрытии толщиной 1 — 1,5 мм. Существенно снизить толщину защитного слоя и значительно улучшить его технологические и эксплуатационные характеристики позволяет использование магнезиально — баритовых смесей вместо барито — бетонных составов.
п.) в виде песка крупностью не более 1,25 мм. Барит включается в состав бетонных смесей (баритобетонов, баритовой штукатурки) в силу его способности поглощать рентгеновское излучение. При использовании барито — бетонных составов на портландцементе для обеспечения должной радиационной безопасности помещений требуется весьма значительная толщина слоя. К тому же баритовые составы на цементном вяжущем в процессе эксплуатации осыпаются, растрескиваются, и потому сами нуждаются в дополнительным защитном покрытии толщиной 1 — 1,5 мм. Существенно снизить толщину защитного слоя и значительно улучшить его технологические и эксплуатационные характеристики позволяет использование магнезиально — баритовых смесей вместо барито — бетонных составов.
Перспективным направлением в области решения задач по обеспечению радиационной безопасности населения является применение композиционных строительных материалов на основе магнезиального вяжущего с добавками шунгита и барита. Специалистами компании «АЛЬФАПОЛ» разработаны современные строительные материалы, эффективно защищающие от сверхнормативного воздействия всех видов источников ионизирующих излучений и сохраняющие при этом основные преимущества строительных материалов на основе магнезиального вяжущего, такие как высокая прочность, повышенная адгезия к любым минеральным основаниям, беспыльность, трещиностойкость, безусадочность, высокая технологичность и др. Баритовые составы «АЛЬФАПОЛ ШТ — БАРИТ» и «АЛЬФАПОЛ М — БАРИТ» относятся к отделочным строительным материалам, предназначенным для
Баритовые составы «АЛЬФАПОЛ ШТ — БАРИТ» и «АЛЬФАПОЛ М — БАРИТ» относятся к отделочным строительным материалам, предназначенным для
- защиты технических средств и человека в медицинских, производственных, научных, административных и жилых помещениях от воздействия ионизирующих излучений
- изготовления контейнеров для хранения и транспортировки радиоактивных материалов и отходов
- отверждения жидких радиоактивных отходов.
Сравнение толщины защитного слоя «АЛЬФАПОЛ ШТ-БАРИТ», «АЛЬФАПОЛ М-БАРИТ» и составов на портландцементе показывает, что рекомендуемая толщина слоя магнезиально — баритовых составов примерно в два раза меньше, чем цементно — баритовых. Это даёт существенный выигрыш в стоимости, сроках проведения работ и весе строительной конструкции в целом. На указанные материалы имеется санитарно-эпидемиологическое заключение для применения в качестве защитного материала от гамма-излучений. Магнезиально-шунгитовая сухая строительная смесь защищена патентом на изобретение № 2233255 от 27 июля 2004 г и заявкой на изобретение Регистрационный номер 2008142229, дата поступления 16. 10.2008 г.
10.2008 г.
Автор статьи: Сазонова Е.Б.
младший научный сотрудник лаборатории легированных кварцевых стёкол
Смотрите еще:
- Рентгенозащита
- Баритовые строительные смеси
Европейское исследование медицинских, промышленных и исследовательских применений ядерных и радиационных технологий
Европейское исследование медицинских, промышленных и исследовательских применений ядерных и радиационных технологий
Обратите внимание, что этот веб-сайт будет проходить техническое обслуживание с 28 по 31 августа. Следовательно, пользователи могут испытывать нестабильность и ограниченную функциональность. Приносим извинения за неудобства.
Для лучшего взаимодействия с пользователем обновите браузер или используйте Браузер Chrome или Firefox .
Главная
Публикации ЕС Загрузка ЗаказЗаключительный отчет
Метаданные публикации
С момента своего открытия более века назад технологии ионизирующего излучения (ИК) стали ключевыми инструментами для изучения материи и биологических строительных блоков. Одно из важнейших открытий 20 века — структура ДНК — стало результатом анализа ее рентгенограммы. За прошедшие годы здравоохранение стало одним из наиболее важных неэнергетических приложений для использования ИК, включая визуализацию и терапию. ИК также используется во многих областях промышленности, от стерилизации и дезинфекции до систем контроля безопасности и от неразрушающего контроля до экологических приложений. Нанотехнологии, наноэлектроника, фотоника, передовые материалы, биотехнологии и передовое производство также используют ИК-инструменты. Эти технологии не только сами по себе приносят высокие доходы, они также создают рабочие места для высококвалифицированных специалистов, ориентированных на инновации, придают дополнительную ценность продуктам и услугам, в которые они встроены, и стимулируют другие технологические разработки. В Европе находится значительная инфраструктура объектов, предназначенных для фундаментальных или прикладных исследований в области IR, широкая сеть передовых университетов и исследовательских центров, а также промышленные корпорации мирового уровня и инновационные МСП, конкурирующие на глобальном уровне.
Одно из важнейших открытий 20 века — структура ДНК — стало результатом анализа ее рентгенограммы. За прошедшие годы здравоохранение стало одним из наиболее важных неэнергетических приложений для использования ИК, включая визуализацию и терапию. ИК также используется во многих областях промышленности, от стерилизации и дезинфекции до систем контроля безопасности и от неразрушающего контроля до экологических приложений. Нанотехнологии, наноэлектроника, фотоника, передовые материалы, биотехнологии и передовое производство также используют ИК-инструменты. Эти технологии не только сами по себе приносят высокие доходы, они также создают рабочие места для высококвалифицированных специалистов, ориентированных на инновации, придают дополнительную ценность продуктам и услугам, в которые они встроены, и стимулируют другие технологические разработки. В Европе находится значительная инфраструктура объектов, предназначенных для фундаментальных или прикладных исследований в области IR, широкая сеть передовых университетов и исследовательских центров, а также промышленные корпорации мирового уровня и инновационные МСП, конкурирующие на глобальном уровне. Такие активы должны поддерживаться и развиваться наряду с их наиболее многообещающими применениями, обеспечивая при этом высочайший уровень безопасности и радиационной защиты. В этом отчете представлена актуальная информация о неэнергетических применениях ядерных и радиационных технологий в ЕС с целью определения их основных преимуществ для общества и перспектив развития. В отчете предлагается ряд действий в этой области, направленных на содействие здоровью граждан Европы и европейской экономике, конкурентоспособности, созданию рабочих мест и росту.
Такие активы должны поддерживаться и развиваться наряду с их наиболее многообещающими применениями, обеспечивая при этом высочайший уровень безопасности и радиационной защиты. В этом отчете представлена актуальная информация о неэнергетических применениях ядерных и радиационных технологий в ЕС с целью определения их основных преимуществ для общества и перспектив развития. В отчете предлагается ряд действий в этой области, направленных на содействие здоровью граждан Европы и европейской экономике, конкурентоспособности, созданию рабочих мест и росту.Показать больше
Показать меньше
Стиль цитирования ЮАПАХАРВАРВАРВАНКУВЕР
Формат экспорта RISBibTeXEndNote
Доступные языки и форматы
Доступные языки и форматы
- Подробности публикации
- Связанные публикации
Пожалуйста, помогите нам улучшить этот портал, приняв участие в нашем опросе.
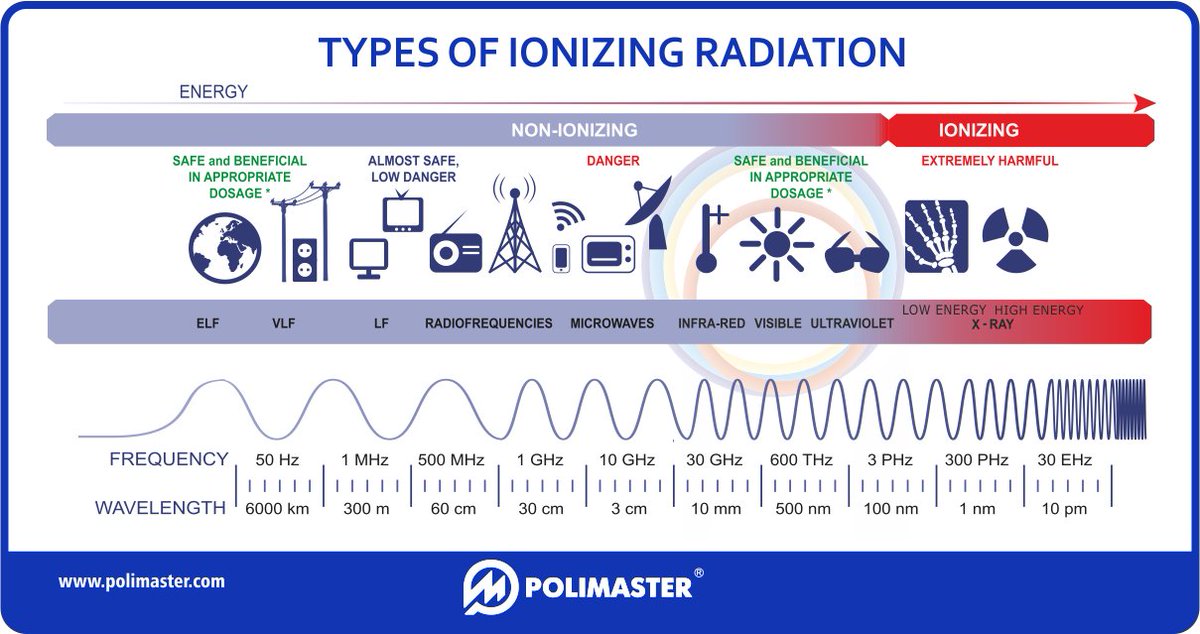
Ионизирующее излучение | Определение, источники, типы, эффекты и факты
- Похожие темы:
- радиация радиоактивность поражение ионизирующим излучением ионизация излучение частиц
См. весь соответствующий контент →
ионизирующее излучение , поток энергии в виде атомных и субатомных частиц или электромагнитных волн, способный высвобождать электроны из атома, заставляя атом заряжаться (или ионизироваться). Ионизирующее излучение включает более энергичную часть электромагнитного спектра (рентгеновские и гамма-лучи) и субатомные частицы, такие как электроны, нейтроны и альфа-частицы (ядра гелия, каждое из которых состоит из двух протонов и двух нейтронов).
Путем смещения электронов (ионизация) ионизирующее излучение эффективно разрушает молекулярные связи. В живых организмах такое разрушение может привести к обширному повреждению клеток и их генетического материала. Характерный тип повреждения ДНК, вызванный ионизирующим излучением, даже при однократном прохождении через клетку, включает близко расположенные множественные повреждения, которые нарушают механизмы репарации клеточной ДНК. Хотя большинство клеток, получивших такие радиационно-индуцированные повреждения, могут быть элиминированы путями реакции на повреждение, некоторые клетки способны избегать этих путей, размножаться и в конечном итоге подвергаться злокачественной трансформации, что является решающим этапом в развитии рака.
Хотя большинство клеток, получивших такие радиационно-индуцированные повреждения, могут быть элиминированы путями реакции на повреждение, некоторые клетки способны избегать этих путей, размножаться и в конечном итоге подвергаться злокачественной трансформации, что является решающим этапом в развитии рака.
Ионизирующее излучение является установленным фактором риска развития рака. Исследования, связанные с облучением клеток и экспериментальных животных, а также эпидемиологические исследования популяций, испытавших необычно высокие уровни радиационного облучения по медицинским или профессиональным причинам, продемонстрировали четкую связь между ионизирующим излучением и раком. Примеры последнего включают Чернобыльскую катастрофу 1986 года и атомные бомбардировки Хиросимы и Нагасаки в Японии в 1945 году. В годы, последовавшие за этими катастрофическими событиями, тысячи людей страдали радиационными заболеваниями и раком.
Риск рака увеличивается примерно пропорционально количеству энергии, депонированной в ткани (доза облучения, обычно измеряемая в единицах грей [Гр] или миллигрей [мГр], где 1 Гр соответствует 1 джоулю энергии на килограмм ткани) . Однако органы и ткани различаются по своей чувствительности к радиационному канцерогенезу (канцерогенной способности). Риск рака также зависит от типа ионизирующего излучения, пола, возраста на момент воздействия, возраста и времени после воздействия, а также факторов образа жизни, таких как репродуктивный анамнез и воздействие других канцерогенов (например, табачного дыма). В среднем основная часть дозы облучения человека приходится на естественные фоновые источники, мало изменившиеся за время существования человечества.
Однако органы и ткани различаются по своей чувствительности к радиационному канцерогенезу (канцерогенной способности). Риск рака также зависит от типа ионизирующего излучения, пола, возраста на момент воздействия, возраста и времени после воздействия, а также факторов образа жизни, таких как репродуктивный анамнез и воздействие других канцерогенов (например, табачного дыма). В среднем основная часть дозы облучения человека приходится на естественные фоновые источники, мало изменившиеся за время существования человечества.
Ионизирующее излучение возникает в результате радиоактивного распада нестабильных изотопов элементов в горных породах, почве и тканях тела, а также в результате ядерных реакций, происходящих на Солнце и далеких звездах. Большая часть всего воздействия такого фонового излучения связана с вдыханием газообразного радона, который образуется в результате радиоактивного распада радия в горных породах и почве и который, просачиваясь в атмосферу, может задерживаться и концентрироваться в плохо проветриваемых помещениях, таких как жилые дома и подземные шахты. Излучение радона и продуктов его радиоактивного распада состоит в основном из альфа-частиц, которые имеют очень ограниченную способность проникать в ткани, но могут повредить клеточную ДНК в легких, если радиоактивный источник вдыхается и попадает в дыхательные пути. Гамма-лучи и рентгеновские лучи, напротив, обладают высокой проникающей способностью и могут воздействовать на клетки, даже если источник излучения находится вне тела. Хотя электроны обладают лишь несколько большей проникающей способностью, чем альфа-частицы, считается, что непосредственная причина большинства связанных с радиацией повреждений ДНК связана с взаимодействием с вторичными электронами, возбуждаемыми за счет переноса электромагнитного излучения или излучения частиц, возникающего вне клетки.
Излучение радона и продуктов его радиоактивного распада состоит в основном из альфа-частиц, которые имеют очень ограниченную способность проникать в ткани, но могут повредить клеточную ДНК в легких, если радиоактивный источник вдыхается и попадает в дыхательные пути. Гамма-лучи и рентгеновские лучи, напротив, обладают высокой проникающей способностью и могут воздействовать на клетки, даже если источник излучения находится вне тела. Хотя электроны обладают лишь несколько большей проникающей способностью, чем альфа-частицы, считается, что непосредственная причина большинства связанных с радиацией повреждений ДНК связана с взаимодействием с вторичными электронами, возбуждаемыми за счет переноса электромагнитного излучения или излучения частиц, возникающего вне клетки.
Различные виды радиации несколько различаются по биологической эффективности на единицу дозы. Например, излучение альфа-частиц, поглощенное тканями, считается примерно в 20 раз более эффективным канцерогеном, чем такая же доза гамма-лучей. Понятие эквивалентной дозы, выраженной в единицах Зиверт (Зв), было введено в целях радиационной защиты. Для гамма-излучения доза 1 мГр соответствует эквиваленту дозы 1 мЗв, тогда как для альфа-излучения доза 1 мГр соответствует эквиваленту дозы 20 мЗв. Среднегодовое воздействие естественного радиационного фона на человека во всем мире составляет 2,4 мЗв в год.
Понятие эквивалентной дозы, выраженной в единицах Зиверт (Зв), было введено в целях радиационной защиты. Для гамма-излучения доза 1 мГр соответствует эквиваленту дозы 1 мЗв, тогда как для альфа-излучения доза 1 мГр соответствует эквиваленту дозы 20 мЗв. Среднегодовое воздействие естественного радиационного фона на человека во всем мире составляет 2,4 мЗв в год.
Оформите подписку Britannica Premium и получите доступ к эксклюзивному контенту.
Подпишитесь сейчас После открытия рентгеновских лучей в 1895 году немецким физиком Вильгельмом Конрадом Рентгеном и открытия радиоактивности в следующем году французским физиком Анри Беккерелем были разработаны медицинские, промышленные и военные методы использования радиационных технологий, которые в конечном итоге привели к заметному увеличению численности населения. воздействие ионизирующего излучения. К началу 21 века в Соединенных Штатах такая антропогенная радиация составляла около 18 процентов от общего годового радиационного облучения населения.
