Болезнь Форестье как причина боли в спине | Кадырова Л.Р., Башкова И.Б., Павлов Ю.И., Акарачкова Е.С.
Статья посвящена проблеме боли в спине и дифференциальной диагностике клинически похожих заболеваний. Рассмотрен клинический случай анкилозирующего диффузного идиопатического скелетного гиперостоза (болезни Форестье)
ВведениеБоль в спине является междисциплинарной медицинской проблемой, тем не менее такие пациенты обращаются первично к терапевтам и врачам общей практики, на которых лежит ответственность за своевременную дифференциальную диагностику и назначение комплекса терапии в тех случаях, когда боль в спине не является проявлением серьезного или угрожающего жизни заболевания.
Однако не всегда назначенная терапия имеет успех, что может быть связано с недостаточным диагностическим поиском [1]. Так, остеохондроз или обнаруженная при проведении магнитно-резонансной томографии (МРТ) грыжа диска могут маскировать заболевания воспалительного, инфекционного, метаболического, онкологического характера. Оценка «симптомов угрозы», или «красных флажков», позволит врачу выявить наличие заболевания, требующего несколько иного подхода к терапевтическим интервенциям.
Оценка «симптомов угрозы», или «красных флажков», позволит врачу выявить наличие заболевания, требующего несколько иного подхода к терапевтическим интервенциям.
В данной статье представлено описание клинического случая — ведение коморбидного пациента с хроническим болевым синдромом.
Пациентка Е., 61 год, обратилась с жалобами на боли в поясничном и грудном отделах позвоночника, которые появлялись и усиливались после физической нагрузки, тугоподвижность позвоночника после физической нагрузки или длительного пребывания в одном положении, снижение в росте на 7 см за жизнь. Также пациентка отмечала боли в суставах нижних конечностей, преимущественно механического характера, боли в своде левой стопы.
Из анамнеза известно, что эпизоды болей в нижней части спины беспокоят с 50-летнего возраста. В дебюте боль была острая, продолжительностью до 1–2 нед. Наблюдалась у невролога по месту жительства с диагнозом «остеохондроз», при обострении проводились короткие курсы терапии нестероидными противовоспалительными препаратами (НПВП), витаминами группы В, что способствовало купированию болей в спине.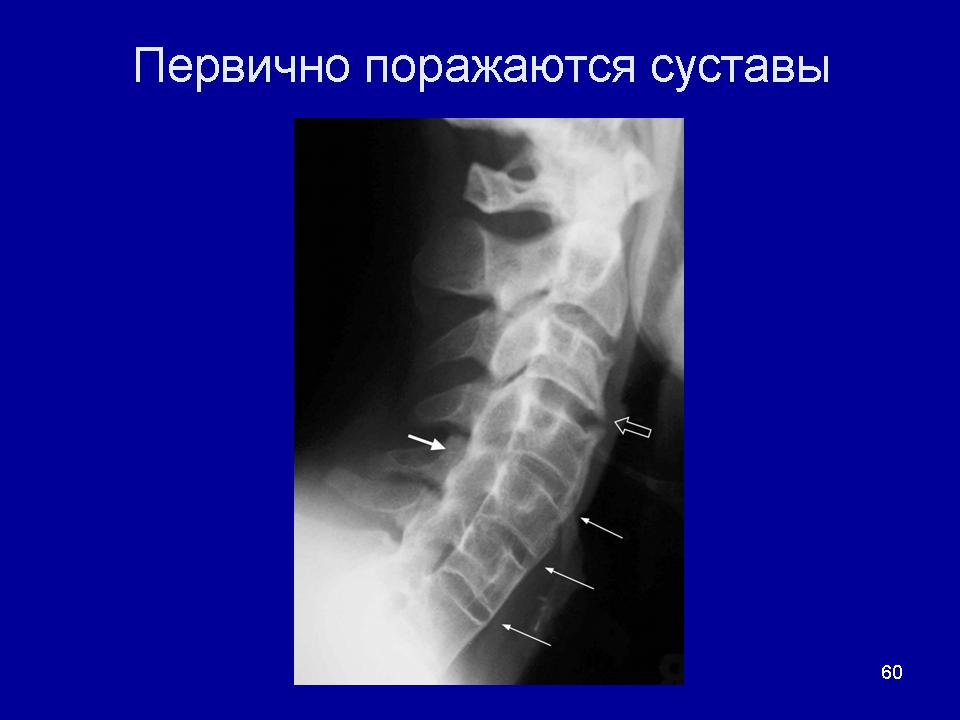
В последние 8–10 лет беспокоят ноющие боли в коленных и тазобедренных суставах, провоцируемые физической нагрузкой. Неоднократно отмечалась припухлость коленных суставов, сопровождаемая утренней скованностью до 30–60 мин, явления синовита купировались приемом НПВП. Поражение крупных суставов нижних конечностей расценивалось как остеоартрит коленных суставов в сочетании с реактивным синовитом.
Пациентка страдает артериальной гипертензией и стенокардией напряжения, по поводу которых принимает антигипертензивные и антиангинальные препараты.
Из-за болей в позвоночнике и рецидивирующих синовитов коленных суставов была отправлена на консультацию к ревматологу с направительным диагнозом «спондилоартрит неуточненный».
При осмотре обращали на себя внимание избыточная масса тела (индекс массы тела 40,7 кг/м2), варикозно расширенные вены нижних конечностей, выраженный грудной кифоз, ограничение движений во всех отделах позвоночника (ротация в шейном отделе позвоночника в пределах 30° в обе стороны, расстояние «затылок — стена» — 5 см, экскурсия грудной клетки — 2 см, проба Шобера — 2 см)..jpg)
С учетом наличия болей в спине, припухлости коленных суставов и суставов предплюсны проведено дообследование на предмет исключения заболевания из группы спондилоартритов. По данным лабораторных методов исследования: СОЭ — 33 мм/ч (по Вестергрену), С-реактивный белок — 8 мг/л, ревматоидный фактор — 2,0 Ед/л, HLA B27 — не обнаружен. Общий анализ мочи и биохимический анализ крови — без особенностей, за исключением повышения уровня сывороточного креатинина до 120 мкмоль/л.
На рентгенограмме костей таза с захватом тазобедренных суставов (рис. 1) выявлен субхондральный остеосклероз суставных поверхностей крестца и подвздошных костей, сужение суставных щелей крестцово-подвздошных сочленений (КПС), начальные признаки двустороннего коксартроза, оссификаты больших и малых вертелов бедренных костей, периостоз (энтезофиты) бугров седалищных костей, крыльев подвздошных костей.
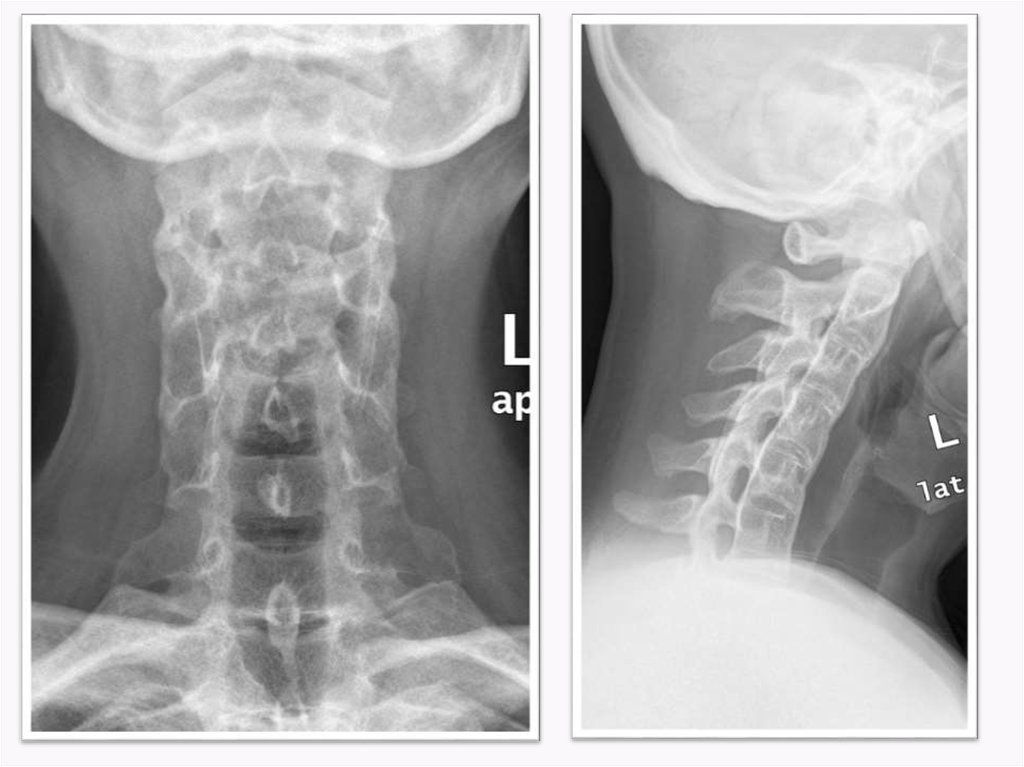
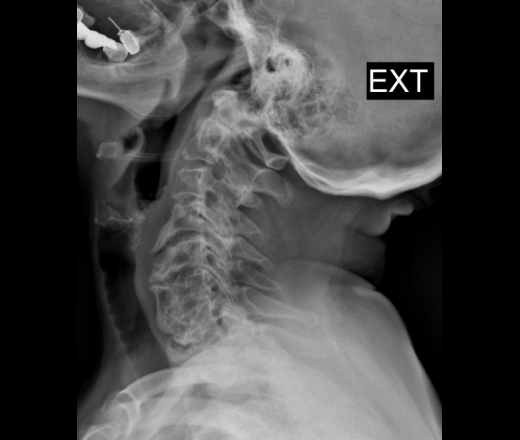
На рентгенограммах шейного (рис. 2), грудного (рис. 3), поясничного (рис. 4) отделов позвоночника обнаружены выпрямление шейного лордоза, выраженный субхондральный склероз замыкательных пластинок тел позвонков в среднегрудном отделе, снижение высоты межпозвоночных дисков, клиновидная деформация тел позвонков в среднегрудном отделе, массивные краевые костные разрастания передних углов тел шейных, грудных и поясничных позвонков с массивным обызвествлением передней продольной связки во всех отделах позвоночника на всем протяжении с клювовидными разрастаниями в шейном и средне-, нижнегрудном отделах, артрозы дугоотростчатых суставов. При проведении ультразвукового исследования коленных суставов выявлены лишь признаки супрапателлярного бурсита с обеих сторон.
Пожилой возраст, указание на наличие болей в спине, невозможность длительное время находиться в вертикальном положении, снижение в росте на 7 см за жизнь требовали настороженности в отношении исключения постменопаузального остеопороза.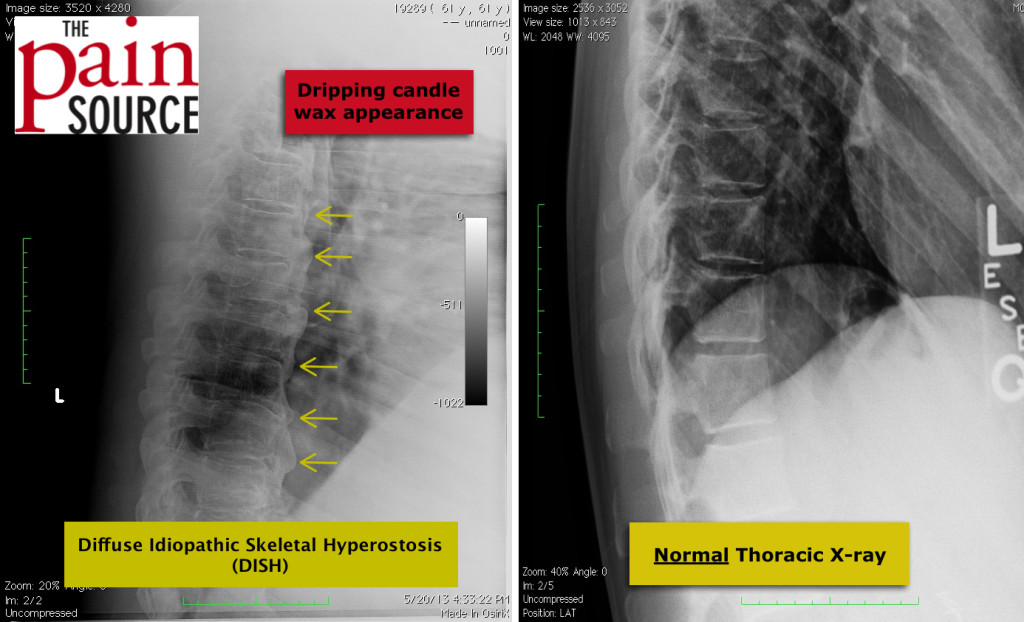 По данным биохимического анализа крови: кальций — 2,19 ммоль/л, фосфор — 0,98 ммоль/л, щелочная фосфатаза — 219 Ед/л. Протеинограмма — без особенностей. При проведении рентгеновской денситометрии центральных отделов скелета выявлено значительное повышение минеральной плотности (МПК) как в поясничном отделе позвоночника (МПК L1-L4–1,908 г/см2, Т-критерий — 5,8 стандартного отклонения), так и в проксимальном отделе бедренной кости (МПК — 1,340 г/см2, Т-критерий — 2,6 стандартного отклонения). Таким образом, лабораторно-инструментальных данных, указывающих на остеопороз, получено не было.
По данным биохимического анализа крови: кальций — 2,19 ммоль/л, фосфор — 0,98 ммоль/л, щелочная фосфатаза — 219 Ед/л. Протеинограмма — без особенностей. При проведении рентгеновской денситометрии центральных отделов скелета выявлено значительное повышение минеральной плотности (МПК) как в поясничном отделе позвоночника (МПК L1-L4–1,908 г/см2, Т-критерий — 5,8 стандартного отклонения), так и в проксимальном отделе бедренной кости (МПК — 1,340 г/см2, Т-критерий — 2,6 стандартного отклонения). Таким образом, лабораторно-инструментальных данных, указывающих на остеопороз, получено не было.
С учетом отсутствия жалоб на боли воспалительного характера в позвоночнике, повышения острофазовых показателей крови, артрита коленных суставов, выявленных дегенеративно-дистрофических изменений в КПС, оссификации передней продольной связки позвоночника во всех отделах позвоночника, множественных периферических гиперостозов, по данным рентгенографического исследования, наиболее вероятным представлялся диагноз анкилозирующего диффузного идиопатического скелетного гиперостоза (болезни Форестье).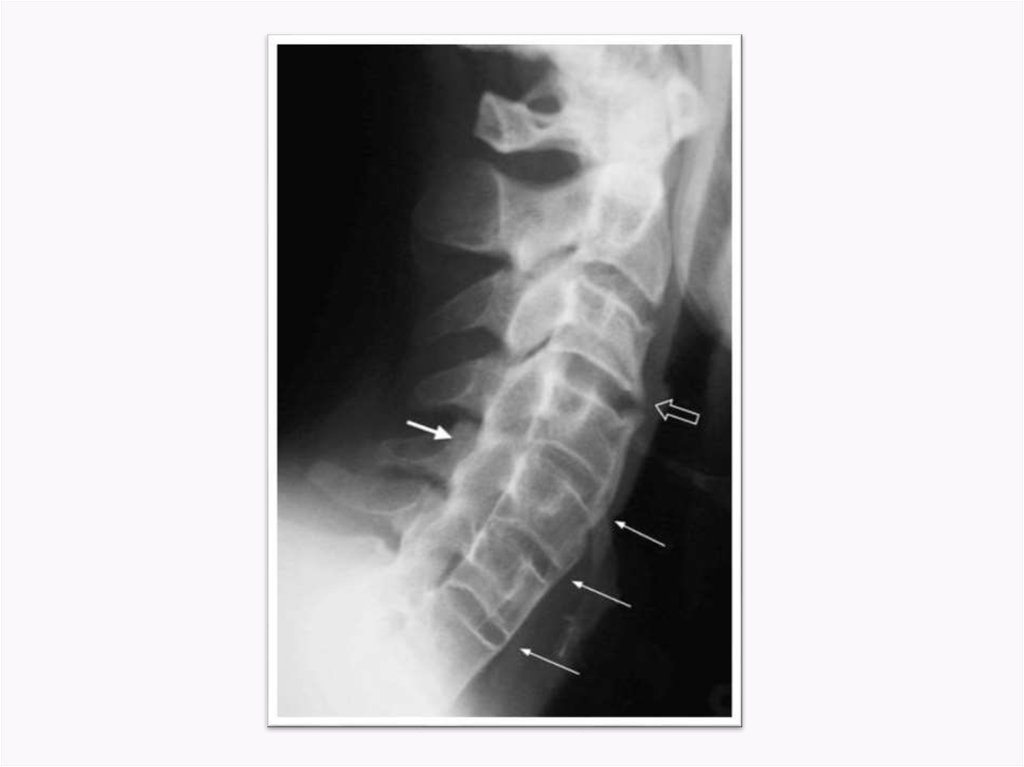
В 1950 г. французский ревматолог J. Forestier (в соавторстве с J. Rotés-Querol) подробно описал не только рентгенологические изменения, характерные для анкилозирующего гиперостоза позвоночника, но и клиническую картину заболевания, которое теперь называют «болезнью Форестье». Спустя четверть века американский радиолог D. Resnick опубликовал статью, в которой показал, что анкилозирующий гиперостоз позвоночника — это только одно из проявлений системной (генерализованной) эктопической оссификации связок, сухожилий и других соединительнотканных структур опорно-двигательного аппарата, и предложил новый термин для обозначения этой патологии — «диффузный идиопатический гиперостоз скелета» [2]. D. Resnick и G. Niwayama в 1982 г. представили диагностические признаки диффузного идиопатического гиперостоза скелета, в основу которых были положены рентгенологические данные [3]. Для постановки диагноза данного заболевания необходимо наличие всех 3 признаков:
непрерывность оссификации передней продольной связки на протяжении не менее чем 4 соседних сегментов позвоночника;
отсутствие (или слабая выраженность) признаков дегенеративных изменений межпозвонковых дисков, таких как сохранение их высоты, отсутствие вакуум-феномена и краевого склероза тел позвонков, в тех сегментах, где оссифицирована передняя продольная связка позвоночника;
отсутствие рентгенологических признаков анкилоза дугоотростчатых суставов и сакроилеита.
Несмотря на достаточно выраженные рентгенологические изменения, жалобы и данные объективного осмотра со стороны позвоночника при диффузном идиопатическом гиперостозе скелета неспецифичны и наблюдаются не чаще, чем у пожилых людей такого же возраста, но без оссификации передней продольной связки позвоночника [4]. Таким образом, нет прямой зависимости между клиникой и рентгенологической картиной.
Пациенты могут предъявить жалобы на дискомфорт, скованность, реже — на боли в грудном отделе позвоночника, усиливающиеся утром после сна, к концу рабочего дня, после физической нагрузки, длительного нахождения в одной позе, на холоде. В случае распространения процесса на шейный и поясничный отделы позвоночника данные ощущения могут отмечаться и в этих отделах. Степень выраженности боли — от слабой до значительной. Нередко, особенно в преклонном возрасте, жалобы могут отсутствовать [5].
Утомляемость спины, изменение осанки, т. е. достаточно бедная клиническая картина, позволяют заподозрить остеопороз, что требует проведения дополнительных исследований.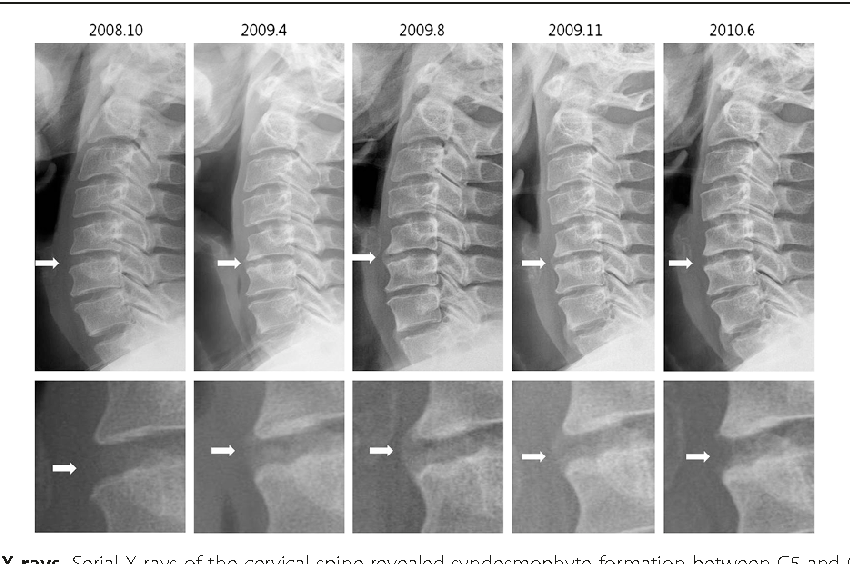
При болезни Форестье оссификация передней продольной связки всегда начинается именно в грудном отделе (причем в 99% случаев — в средне-, нижнегрудном отделах и именно справа), вследствие чего для выявления подобных изменений достаточно выполнить рентгенографию грудного отдела позвоночника в боковой проекции. Это позволит отчетливо разглядеть грубое окостенение преимущественно передней продольной связки. Позже в процесс вовлекаются поясничный и шейный отделы позвоночника.
По мнению Н. В. Бунчука, рентгенологические изменения позвоночника при диффузном идиопатическом гиперостозе скелета нередко интерпретируют как картину «бамбуковой палки», типичной для анкилозирующего спондилита [4]. Ранее ошибочно предполагали, что синдесмофиты при анкилозирующем спондилите формируются вследствие оссификации передней продольной связки. В настоящее время установлено, что формирование синдесмофита при анкилозирующем спондилите начинается с воспаления мест прикрепления волокон фиброзного кольца межпозвонкового диска к телам выше- и нижележащего позвонков, т. е. с энтезита. В дальнейшем происходит хондроидная метаплазия и оссификация наружных слоев фиброзного диска, фронт которой постепенно распространяется от тел позвонков к середине диска. Таким образом, типичные для анкилозирующего спондилита синдесмофиты расположены внутри диска и обычно не выступают за боковые контуры позвонков (рис. 5).
В. Бунчука, рентгенологические изменения позвоночника при диффузном идиопатическом гиперостозе скелета нередко интерпретируют как картину «бамбуковой палки», типичной для анкилозирующего спондилита [4]. Ранее ошибочно предполагали, что синдесмофиты при анкилозирующем спондилите формируются вследствие оссификации передней продольной связки. В настоящее время установлено, что формирование синдесмофита при анкилозирующем спондилите начинается с воспаления мест прикрепления волокон фиброзного кольца межпозвонкового диска к телам выше- и нижележащего позвонков, т. е. с энтезита. В дальнейшем происходит хондроидная метаплазия и оссификация наружных слоев фиброзного диска, фронт которой постепенно распространяется от тел позвонков к середине диска. Таким образом, типичные для анкилозирующего спондилита синдесмофиты расположены внутри диска и обычно не выступают за боковые контуры позвонков (рис. 5).
Оссификация связок, расположенных в задних отделах КПС, а также их капсулы может имитировать частичный анкилоз этих суставов на рентгенограмме.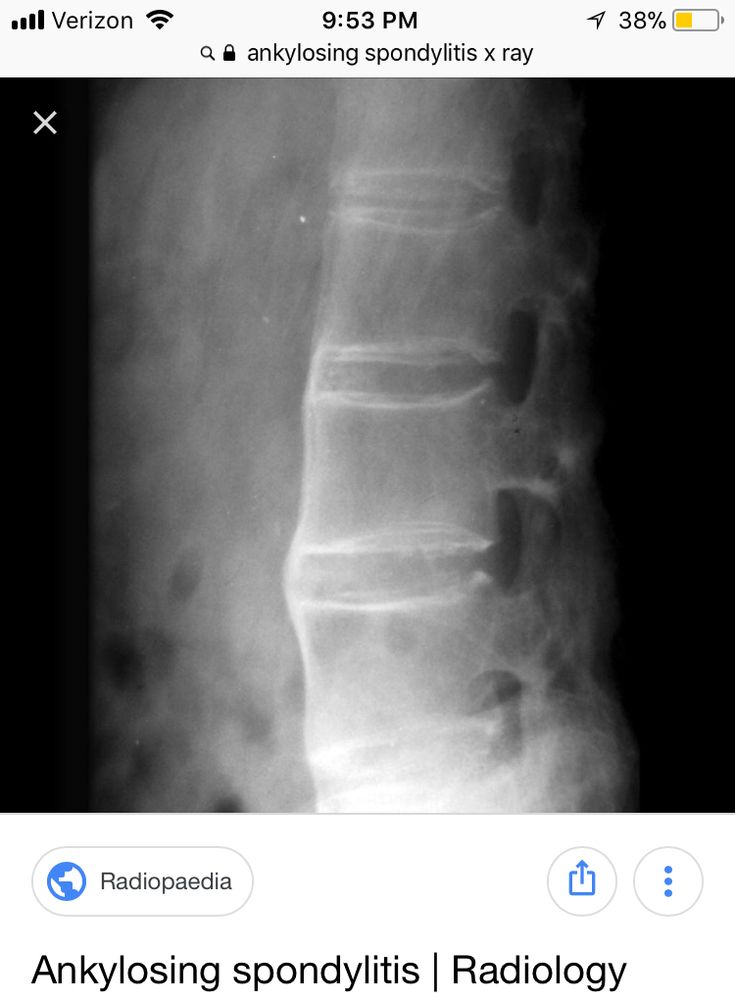 Оссификация связок КПС при дегенеративной патологии (по типу артроза) вплоть до анкилоза наблюдается только в передних отделах.
Оссификация связок КПС при дегенеративной патологии (по типу артроза) вплоть до анкилоза наблюдается только в передних отделах.
Основные дифференциально-диагностические признаки диффузного идиопатического гиперостоза скелета и анкилозирующего спондилита представлены в таблице 1.
В лечении спондилоалгий, возникающих вследствие анкилозирующего гиперостоза позвоночника, обычно эффективны местные тепловые процедуры и массаж мышц спины. Полезны регулярные упражнения для поддержания достаточной подвижности позвоночника. Применение НПВП, эффективных при анкилозирующем спондилите, при диффузном идиопатическом гиперостозе скелета приводит лишь к умеренному снижению болевого синдрома [10]. Знание этого позволит избежать бесконтрольного приема НПВП, учитывая вероятность развития побочных эффектов. Для лечения «периферических» проявлений заболевания, причиной которых является реактивное воспаление структур, подвергающихся кальцификации и оссификации (энтезопатии, тендиниты, лигаментиты), по мнению Н. В. Бунчука, следует использовать локальные методы воздействия, например, инъекционное введение глюкокортикоидов под контролем УЗИ-навигации [4].
В. Бунчука, следует использовать локальные методы воздействия, например, инъекционное введение глюкокортикоидов под контролем УЗИ-навигации [4].
Описанный клинический случай показывает, что поиск причины болевого синдрома в спине требует тщательного анализа анамнеза, клинической картины, инструментальных и лабораторных исследований, т. е. проведения дифференциальной диагностики [11]. Если обратиться к определению, то дифференциальная диагностика в медицине — это способ диагностики, исключающий не подходящие по каким-либо фактам или симптомам заболевания, возможные у больного, что в конечном счете должно привести к правильному диагнозу. Проведение дифференциальной диагностики и постановка точного диагноза позволяют выбрать правильную тактику лечения и реабилитации пациента.
Болезнь Форестье: причины, симптомы и лечение
Болезнь Форестье (анкилозирующий гиперостоз) представляет собой патологическое состояние, вызванное повышенным формированием очагов окостенения связочного аппарата позвоночного столба.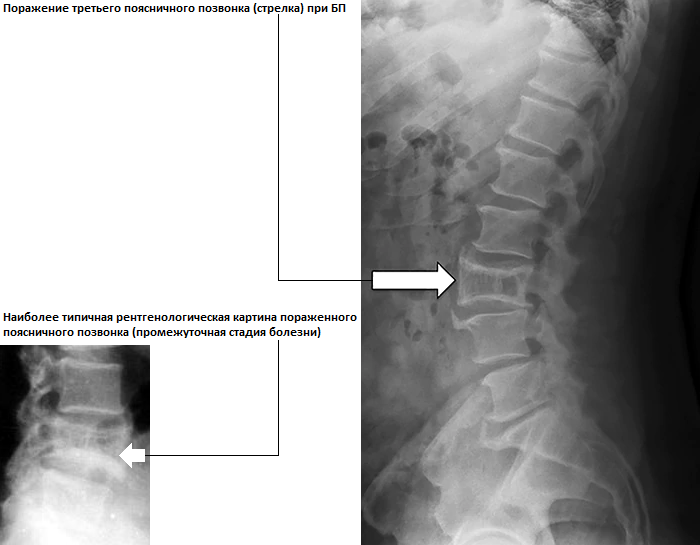 Следует разобраться подробно, что вызывает указанное заболевание, как оно проявляется, существует ли эффективное лечение.
Следует разобраться подробно, что вызывает указанное заболевание, как оно проявляется, существует ли эффективное лечение.
Механизм и причины образования
Анкилозирующий гиперостоз поражает столб позвоночника. Обычно соли кальция начинают заполнять передние межпозвонковые продольные связки грудного или шейного отдела. Со временем они теряют эластичность, костенеют и соединяются с передней частью позвонков. При прогрессировании болезни Форестье костные образования в сухожилиях и связках позвонков увеличиваются в размерах, огибают межпозвоночные диски и прочно срастаются между собой. Происходит полная или частичная утрата подвижности позвонков (анкилоз), позвоночный столб сильно деформируется.
Обычно болезнь начинает развиваться в центральной части позвоночника, постепенно охватывая шейный и поясничный отделы. Патологический процесс со временем распространяется на весь позвоночник и другие части опорно-двигательного аппарата. В результате больному группа инвалидности обеспечена. Болезнь не считается смертельно опасной, но способна значительно ухудшить качество жизни больного.
Болезнь не считается смертельно опасной, но способна значительно ухудшить качество жизни больного.
Причины заболевания точно не установлены. Замечено, что патология поражает людей пожилого возраста, то есть окостенение связок позвоночника происходит в связи с возрастными изменениями, происходящими в организме.
Другими факторами, способствующими формированию анкилозирующего гиперостоза, являются:
- сахарный диабет;
- ожирение;
- гипертония;
- различные хронические интоксикации организма (гнойный отит, туберкулез, синусит и пр.).
Гиперостоз может развиваться постепенно, за длительный промежуток времени охватывая все новые и новые области позвоночника. Чтобы своевременно обратиться к врачу для проведения эффективного лечения, необходимо знать симптоматику указанного заболевания.
Симптомы болезни
Первые проявления гиперостоза начинаются со скованности движений шейного или поясничного отдела позвоночника в утреннее и вечернее время. Периодически возникают болезненные ощущения в тазовых, локтевых, коленных и других костях после чрезмерных нагрузок, а потом и в обычном состоянии.
Периодически возникают болезненные ощущения в тазовых, локтевых, коленных и других костях после чрезмерных нагрузок, а потом и в обычном состоянии.
При болезни Форестье симптомы можно подразделить на следующие синдромы:
- вертебральный;
- экстравертибральный;
- компрессионный.
Вертебральному синдрому характерны определенные признаки:
- нарушение подвижности позвоночника;
- кифоз грудного отдела;
- сколиоз;
- скованность движений.
По мере прогрессирования окостенения тканей позвоночного столба перечисленные признаки болезни Форестье усиливаются.
Значительное искривление позвоночника на поздних этапах развития болезни негативно отражается на положении и работе многих важных внутренних органов, наблюдается их компрессия и смещение. Это выражается в экстравертибральном синдроме, проявления которого могут быть разнообразными. Смещение сердца может привести к опасным сбоям в его функционировании.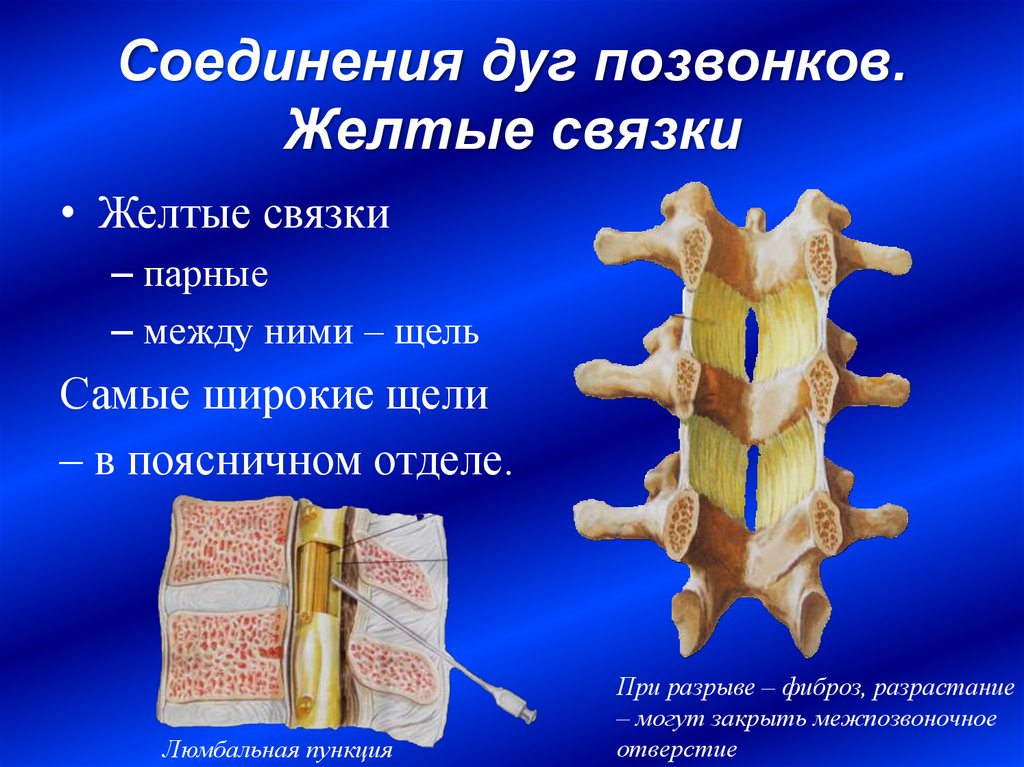 Из-за периодического сдавливания крупных кровеносных сосудов возникают опасные скачки артериального давления.
Из-за периодического сдавливания крупных кровеносных сосудов возникают опасные скачки артериального давления.
При прогрессирующем гиперостозе часто возникают серьезные проблемы с пищеводом, желудком, глоткой, из-за смещения и сдавливания которых у больного нарушаются функции глотания пищи и весь процесс пищеварения.
Компрессионный синдром при указанной патологии выражается в компрессии нервных корешков в стволе спинного мозга или в области межпозвоночных дисков. Ущемление нервных окончаний проявляется в сильных болях в различных участках спины и конечностях, в неврологических нарушениях.
Прогрессирование заболевания может привести к полной обездвиженности пораженных участков позвоночного столба больного. Из-за неравномерного распределения нагрузки на тело происходит поражение всей костно-суставной системы. У возрастных пациентов из-за искривления шейно-грудного отдела позвоночного столба возникает старческий горб. Иногда патологическое изменение позвоночника протекает без видимых проявлений.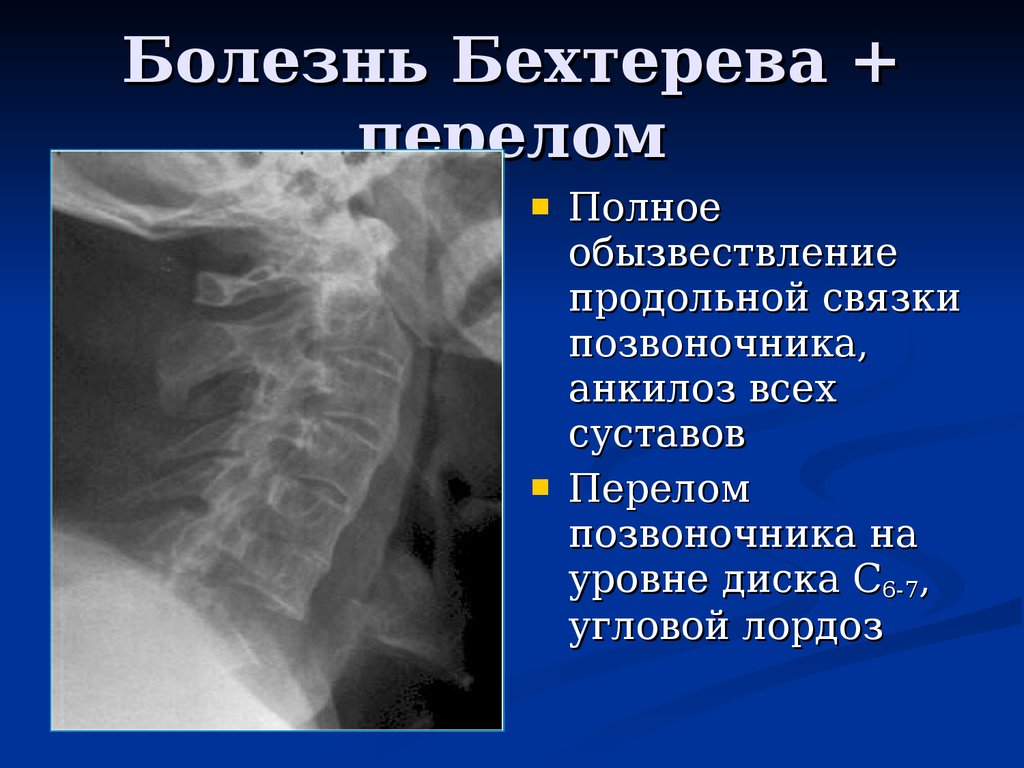 Их можно обнаружить при диагностическом обследовании пациента.
Их можно обнаружить при диагностическом обследовании пациента.
Диагностические исследования при болезни Форестье
Для уточнения диагноза при подозрении на гиперостоз проводят:
- рентгенографию в прямой и боковой проекциях;
- МРТ;
- лабораторные исследования.
Основополагающим исследованием, проводимым для постановки диагноза болезни Форестье, является рентген позвоночника, выполненный в прямой и боковой проекции. Указанный способ простой, доступный, информативный.
На рентгеновских снимках отчетливо видны любые повреждения межпозвоночных дисков, очаги окостенения, некротические участки на развитой стадии болезни. Данной патологии характерно равномерное распределение костных наростов по всему позвоночному столбу, отсутствие поврежденных суставов в крестцовой области. Боковая проекция указанного исследования выявляет патологический процесс, охватывающий тела позвонков.
МРТ позволяет обнаружить начальные видоизменения структуры позвоночника на ранних стадиях гиперостоза, что в дальнейшем значительно облегчает лечение.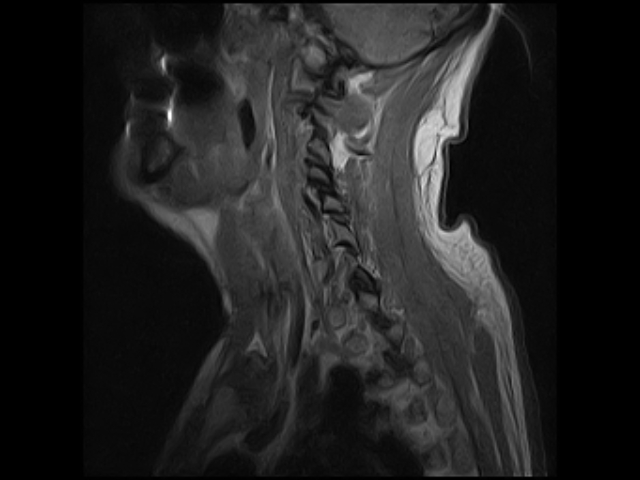
Важно в ходе диагностических исследований провести разграничение указанной патологии со схожими по симптоматике заболеваниями — болезнью Бехтерева, спондилезом, остеохондрозом и др.
Лабораторные анализы крови и мочи при болезни Форестье информативными не являются. Они могут показать отсутствие в организме больного каких-либо воспалительных процессов.
Watch this video on YouTube
Лечение болезни
Лечить костную патологию при болезни Форестье следует консервативными методами с применением комплексного подхода. Полное избавление от заболевания невозможно. Цель борьбы с недугом — улучшение состояния больного.
Лечебные мероприятия могут включать:
- медикаментозную терапию;
- лазеротерапию;
- водолечение;
- массаж;
- магнитотерапию;
- правильное рациональное питание с достаточным количеством кальция;
- лечебную физкультуру на растяжение и гибкость позвоночника;
- ношение ортопедического корсета, снимающего нагрузку с позвоночного столба;
- средства народной медицины.

Симптоматическая медикаментозная терапия при указанной патологии заключается в устранении признаков болезни. Болезненные состояния значительно уменьшаются при помощи НПВС — Ибупрофена, Диклофенака, Индометацина и пр. Стойкий эффект дает комплексное использование препаратов наружного и внутреннего применения — таблеток, компрессов, мазей, гелей и пр. В качестве дополнительного обезболивающего средства хорошо зарекомендовал себя компресс с Димексидом. В тяжелых случаях могут быть использованы спинномозговые блокады.
Часто в лечении патологии назначаются хондопротекторы (Алфлутоп), укрепляющие межпозвоночную хрящевую ткань. Кровоснабжение поврежденных участков позвоночника восстанавливают препараты, улучшающие циркуляцию крови (Пентоксифиллин).
Для улучшения качества жизни пациентов в исключительных случаях может быть проведено хирургическое вмешательство — артопластика, остеотомия и пр.
Watch this video on YouTube
Заключение по теме
Поскольку гиперостоз связан с окостенением и обездвижением позвоночного столба, патологию нельзя оставлять без внимания. Для улучшения качества жизни пожилых людей необходимо проводить симптоматическое лечение.
Для улучшения качества жизни пожилых людей необходимо проводить симптоматическое лечение.
Диффузный идиопатический скелетный гиперостоз шейного отдела позвоночника с дисфагией — молекулярные и клинические аспекты
1. Резник Д., Ниваяма Г. Рентгенологические и патологические особенности поражения позвоночника при диффузном идиопатическом скелетном гиперостозе (DISH) Радиология. 1976; 119: 559–568. дои: 10.1148/119.3.559. [PubMed] [CrossRef] [Google Scholar]
2. Насименто Ф.А., Гатто Л.А., Лагес Р.О., Нето Х.М., Демартини З., Коппе Г.Л. Диффузный идиопатический скелетный гиперостоз: обзор. Surg. Нейрол. Междунар. 2014;5:122–125. doi: 10.4103/2152-7806.130675. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
3. Вайшья Р., Виджай В., Нвагбара И.С., Агарвал А.К. Диффузный идиопатический скелетный гиперостоз (DISH) — распространенная, но менее известная причина болей в спине. Дж. Клин. Ортоп. Травма. 2017; 8: 191–196. doi: 10.1016/j.jcot.2016.11. 006. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
006. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
4. Kuperus J.S., Mohamed Hoesein F.A.A., de Jong P.A., Verlaan J.J. Диффузный идиопатический скелетный гиперостоз: этиология и клиническое значение. Лучшая практика. Рез. клин. Ревматол. 2020;34:101527. doi: 10.1016/j.berh.2020.101527. [PubMed] [CrossRef] [Академия Google]
5. Мадер Р., Верлаан Дж.Дж., Бускила Д. Диффузный идиопатический скелетный гиперостоз: клинические особенности и патогенетические механизмы. Нац. Преподобный Ревматол. 2013; 9: 741–750. doi: 10.1038/nrrheum.2013.165. [PubMed] [CrossRef] [Google Scholar]
6. Мадер Р., Паппоне Н., Баралиакос Х., Эшед И., Сарзи-Путтини П., Ацени Ф., Бибер А., Новофастовский И., Кифер Д. ., Verlaan J.J., et al. Диффузный идиопатический скелетный гиперостоз (DISH) и возможный воспалительный компонент. Курс. Ревматол. Респ. 2021; 23:6. дои: 10.1007/s11926-020-00972-х. [PubMed] [CrossRef] [Google Scholar]
7. Parreira B. Ph.D. Тезис. Университет Алгарве; Фару, Португалия: 2018. Генетические варианты, связанные с эктопическими кальцификатами. [Google Scholar]
Генетические варианты, связанные с эктопическими кальцификатами. [Google Scholar]
8. Грегсон К.Л., Дункан Э.Л. Генетическая архитектура высокой костной массы. Фронт. Эндокринол. 2020;11:595653. doi: 10.3389/fendo.2020.595653. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
9. Frost M., Rahbek E.T., Ejersted C., Hoilund-Carlsen P.F., Bygum A., Thomsen J.S., Andreasen C.M., Andersen T.L., Frederiksen A.L. Формирование кости на основе моделирования трансформирует трабекулы в кортикальную кость в склеротических областях при синдроме Бушке-Оллендорфа. Тематическое исследование двух женщин с вариантами LEMD3. Кость. 2020;135:115313. doi: 10.1016/j.bone.2020.115313. [PubMed] [CrossRef] [Академия Google]
10. Горман С., Джавад А.С., Чиканза И. Семья с диффузным идиопатическим скелетным гиперостозом. Анна. Реум. Дис. 2005; 64: 1794–1795. doi: 10.1136/ard.2004.033852. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Собака как животная модель для DISH? Евро. Спайн Дж. 2010; 19:1325–1329. doi: 10.1007/s00586-010-1280-6. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Спайн Дж. 2010; 19:1325–1329. doi: 10.1007/s00586-010-1280-6. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
12. Warraich S., Bone D.B., Quinonez D., Ii H., Choi D.S., Holdsworth D.W., Drangova M., Dixon S.J., Seguin C.A., Hammond J.R. Потеря равновесного переносчика нуклеозидов 1 у мышей приводит к прогрессирующей эктопической минерализации тканей позвоночника, напоминающих диффузный идиопатический скелетный гиперостоз у человека. Дж. Боун Шахтер. Рез. 2013;28:1135–1149. doi: 10.1002/jbmr.1826. [PubMed] [CrossRef] [Google Scholar]
13. Коуто А.Р., Паррейра Б., Томсон Р., Соарес М., Пауэр Д.М., Станкович Дж., Армас Дж.Б., Браун М.А. Комбинированный подход к поиску генов восприимчивости в DISH/ семьи с хондрокальцинозом: полногеномное сцепление и исследования СРК/ВЗК. Гум. Геном Вар. 2017;4:17041. doi: 10.1038/hgv.2017.41. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
14. Parreira B., Couto A.R., Rocha F., Sousa M., Faustino V., Power DM, Bruges-Armas J.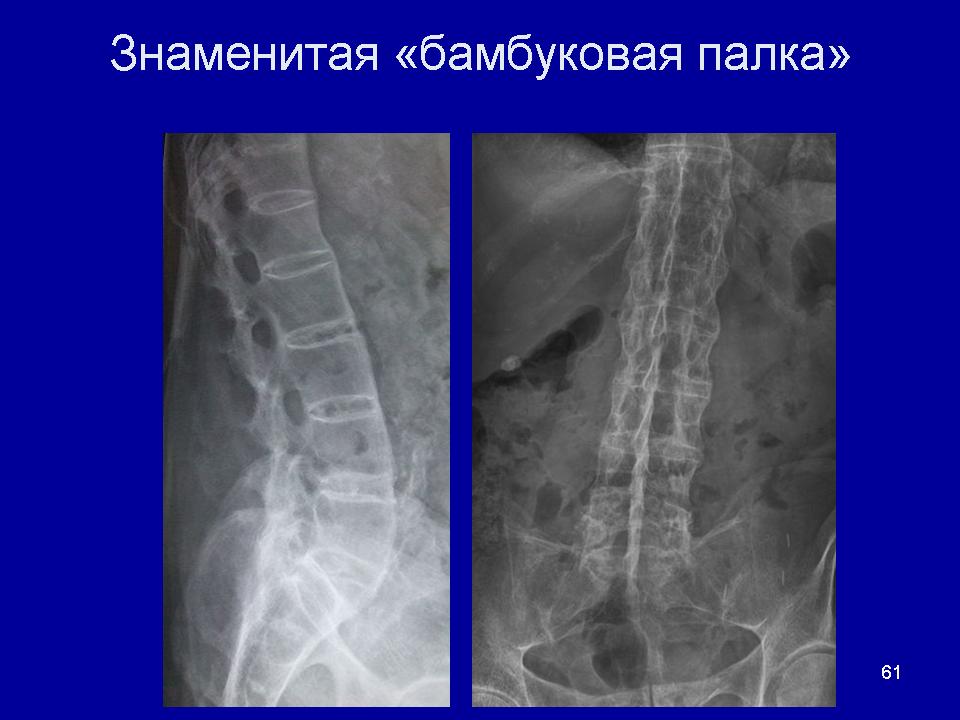 Секвенирование всего экзома у пациентов с диффузным идиопатическим скелетным гиперостозом и хондрокальцинозом кристаллов пирофосфата кальция. Акта Реуматол. Порт. 2020;45:116–126. [PubMed] [Google Scholar]
Секвенирование всего экзома у пациентов с диффузным идиопатическим скелетным гиперостозом и хондрокальцинозом кристаллов пирофосфата кальция. Акта Реуматол. Порт. 2020;45:116–126. [PubMed] [Google Scholar]
15. Джун Дж.К., Ким С.М. Ассоциативное исследование фактора роста фибробластов 2 и полиморфизма генов рецепторов фактора роста фибробластов при корейской оссификации задней продольной связки у пациентов. J. Корейский нейрохирург. соц. 2012;52:7–13. doi: 10.3340/jkns.2012.52.1.7. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
16. Цукахара С., Миядзава Н., Акагава Х., Форейтова С., Павелка К., Танака Т., Тох С., Тадзима А., Акияма И., Иноуэ И. COL6A1, ген-кандидат окостенения задней продольной связки, связан с диффузным идиопатическим скелетным гиперостозом у японцев. Позвоночник. 2005;30:2321–2324. doi: 10.1097/01.brs.0000182318.47343.6d. [PubMed] [CrossRef] [Google Scholar]
17. Servier Medical Art. [(по состоянию на 4 февраля 2021 г.)]; Доступно онлайн: https://smart.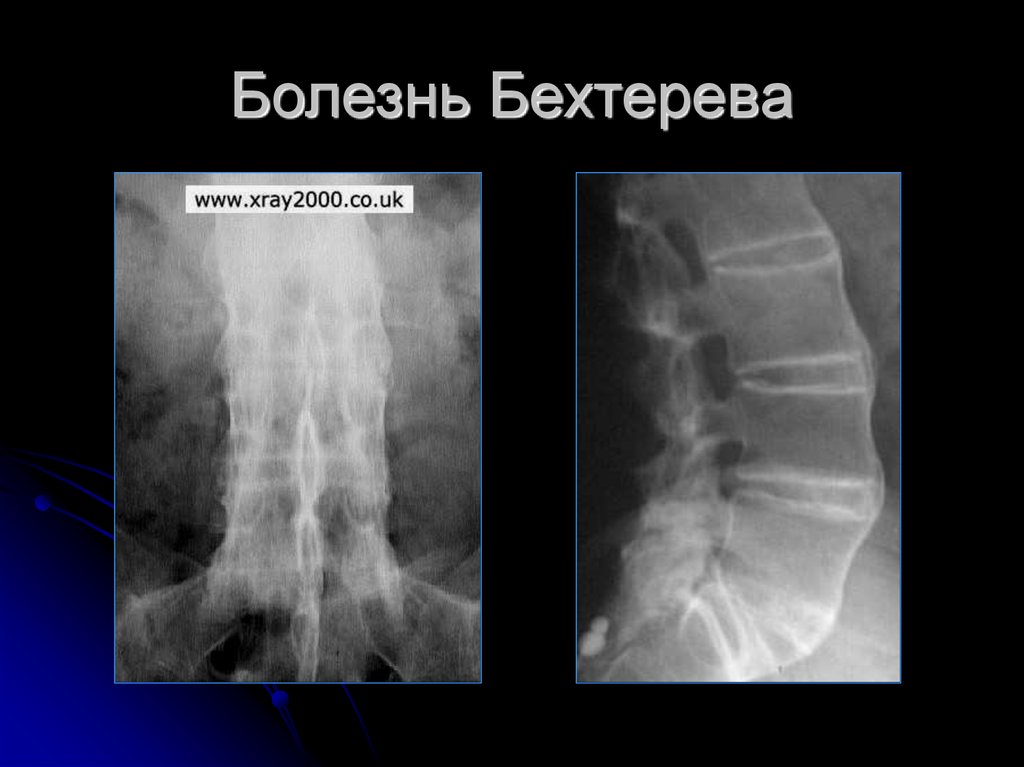 servier.com
servier.com
18. Робертс С.Дж., Ке Х.З. Анаболические стратегии для ускорения заживления переломов костей. Курс. Остеопорос. Отчет 2018; 16: 289–298. doi: 10.1007/s11914-018-0440-1. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
19. Moosa S., Wollnik B. Измененная передача сигналов FGF при врожденных черепно-лицевых и скелетных нарушениях. Семин. Сотовый Дев. биол. 2016;53:115–125. doi: 10.1016/j.semcdb.2015.12.005. [PubMed] [CrossRef] [Google Scholar]
20. Jann J., Gascon S., Roux S., Faucheux N. Влияние суперсемейства TGF-бета на баланс остеокластов/остеобластов при физиологических и патологических состояниях костей. Междунар. Дж. Мол. науч. 2020;21:7597. doi: 10.3390/ijms21207597. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
, и другие. Молекулярная характеристика известных и новых вариантов ACVR1 при фенотипах аберрантной оссификации. Являюсь. Дж. Мед. Жене. А. 2019; 179:1764–1777. doi: 10.1002/ajmg.a.61274. [PubMed] [CrossRef] [Google Scholar]
22. Tsukamoto S., Kuratani M., Katagiri T. Функциональная характеристика уникального мутанта ALK2, p.K400E, связанного с нарушением скелета, диффузным идиопатическим гиперостозом скелета. . Кость. 2020;137:115410. doi: 10.1016/j.bone.2020.115410. [PubMed] [CrossRef] [Академия Google]
Tsukamoto S., Kuratani M., Katagiri T. Функциональная характеристика уникального мутанта ALK2, p.K400E, связанного с нарушением скелета, диффузным идиопатическим гиперостозом скелета. . Кость. 2020;137:115410. doi: 10.1016/j.bone.2020.115410. [PubMed] [CrossRef] [Академия Google]
23. Лопес К.Д., Бекиш Дж.М., Корчиуло К., Медьеро А., Коэльо П.Г., Витек Л., Флорес Р.Л., Кронштейн Б.Н. Местная доставка агонистов аденозиновых рецепторов для стимуляции регенерации костей и заживления дефектов. Доп. Наркотик Делив. 2019; 146:240–247. doi: 10.1016/j.addr.2018.06.010. [PubMed] [CrossRef] [Google Scholar]
24. Corciulo C., Cronstein B.N. Сигнализация пуринергической системы в суставе. Фронт. Фармакол. 2019;10:1591. doi: 10.3389/fphar.2019.01591. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
25. Daniels G., Ballif B.A., Helias V., Saison C., Grimsley S., Mannessier L., Hustinx H., Lee E., Cartron J.P., Peyrard T., et al. Отсутствие переносчика нуклеозидов ENT1 приводит к нулевой группе крови по Августину и эктопической минерализации.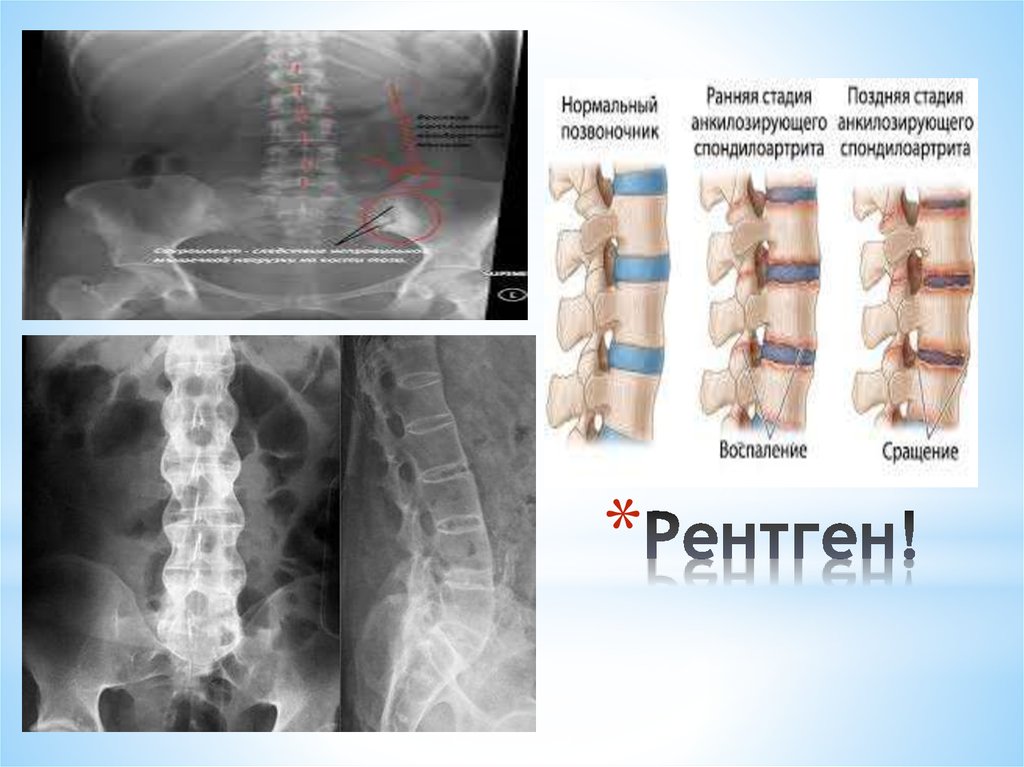 Кровь. 2015;125:3651–3654. doi: 10.1182/blood-2015-03-631598. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Кровь. 2015;125:3651–3654. doi: 10.1182/blood-2015-03-631598. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
26. Dixon J., Beaucage K., Nagao M., Lajoie G., Veras M., Fournier D., Holdsworth D., Bailey C. , Hammond J., Séguin C. Мыши, лишенные переносчика нуклеозидов ENT1: модель диффузного идиопатического скелетного гиперостоза у людей; Материалы ортопедического производства; Монреаль, Квебек, Канада. 17 июля 2020 г.; п. 123. [Google Академия]
27. Стразулла Л.К., Кронштейн Б.Н. Регуляция костей и хрящей с помощью передачи сигналов аденозина. Пуринергический сигнал. 2016;12:583–593. doi: 10.1007/s11302-016-9527-2. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
28. Хусейн А., Джеффрис М.А. Эпигенетика и ремоделирование костей. Курс. Остеопорос. Отчет 2017; 15: 450–458. doi: 10.1007/s11914-017-0391-y. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
29. Чиба Н., Фурукава К., Такаяма С., Асари Т., Чин С., Харада Ю. , Кумагаи Г., Вада К. , Танака Т., Оно А. и др. Снижение метилирования ДНК в промоторной области генов WNT5A и GDNF может способствовать остеогенности мезенхимальных стволовых клеток пациентов с окостеневшими связками позвоночника. Дж. Фармакол. науч. 2015; 127:467–473. doi: 10.1016/j.jphs.2015.03.008. [PubMed] [CrossRef] [Академия Google]
, Кумагаи Г., Вада К. , Танака Т., Оно А. и др. Снижение метилирования ДНК в промоторной области генов WNT5A и GDNF может способствовать остеогенности мезенхимальных стволовых клеток пациентов с окостеневшими связками позвоночника. Дж. Фармакол. науч. 2015; 127:467–473. doi: 10.1016/j.jphs.2015.03.008. [PubMed] [CrossRef] [Академия Google]
30. Yuan X., Shi L., Chen Y. Некодирующие РНК при окостенении связок позвоночника. Евро. Спайн Дж. 2021; 30: 801–808. doi: 10.1007/s00586-020-06687-y. [PubMed] [CrossRef] [Google Scholar]
31. Hong L., Sun H., Amendt B.A. МикроРНК участвуют в формировании, регенерации и восстановлении черепно-лицевой кости. Кость. 2021;144:115789. doi: 10.1016/j.bone.2020.115789. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
32. Zhang H., Xu C., Liu Y., Yuan W. МикроРНК-563 способствует остеогенной дифференцировке клеток задней продольной связки путем ингибирования SMURF1. Чжунхуа Вай Кэ За Чжи. 2017;55:203–207. doi: 10.3760/cma.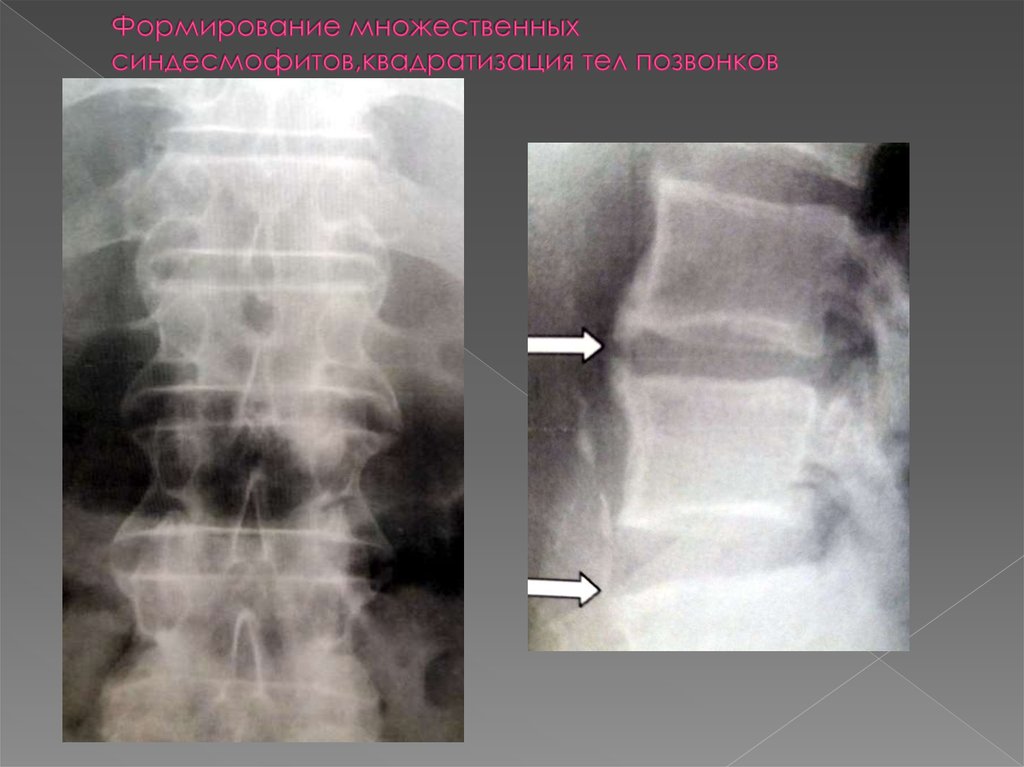 j.issn.0529-5815.2017.03.008. [PubMed] [CrossRef] [Google Scholar]
j.issn.0529-5815.2017.03.008. [PubMed] [CrossRef] [Google Scholar]
33. Esser J.S., Saretzki E., Pankratz F., Engert B., Grundmann S., Bode C., Moser M., Zhou Q. Костный морфогенетический белок 4 регулирует микроРНК. миР-494 и миР-126-5p в контроле функции эндотелиальных клеток при ангиогенезе. тромб. Гемост. 2017; 117:734–749. doi: 10.1160/Th26-08-0643. [PubMed] [CrossRef] [Google Scholar]
34. Pillai S., Littlejohn G. Метаболические факторы при диффузном идиопатическом скелетном гиперостозе — обзор клинических данных. Откройте Ревматол. Дж. 2014; 8: 116–128. дои: 10.2174/1874312
- 8010116. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
- История болезни
- Открытый доступ
- Опубликовано:
- Сима Шривастава 1 ,
- Наталья Чяприна 1 и
- Иньяки Бовилл 1
6025 Доступ
8 цитирований
Сведения о показателях
- БЛЮДО:
Диффузный идиопатический скелетный гиперостоз.
Forestier J, Rotes-Querol J: Старческий анкилозирующий гиперостоз позвоночника. Энн Реум. 1950, 9: 321-330. 10.1136/ард.9.4.321.
Артикул КАС Google ученый
«>Resnick D, Niwayama G: Рентгенологические и патологические признаки поражения позвоночника при диффузном идиопатическом скелетном гиперостозе. Радиология. 1976, 119: 559-568.
Артикул КАС пабмед Google ученый
Резник Д., Шауль С.Р., Робинс Д.М. Диффузный идиопатический скелетный гиперостоз (DISH): болезнь Форестье с экстраспинальными проявлениями. Радиология. 1975, 115: 513-524.
Артикул КАС пабмед Google ученый
Резник Д., Шапиро Р.Ф., Веснер К.
 Б., Ниваяма Г., Утсингер П.Д., Шауль С.Р.: Диффузный идиопатический гиперостоз скелета (DISH). Семин Артрит Реум. 1978, 7: 153-187. 10.1016/0049-0172(78)
Б., Ниваяма Г., Утсингер П.Д., Шауль С.Р.: Диффузный идиопатический гиперостоз скелета (DISH). Семин Артрит Реум. 1978, 7: 153-187. 10.1016/0049-0172(78)-7.
Артикул КАС пабмед Google ученый
Eviatar E, Harell M: Диффузный идиопатический скелетный гиперостоз с дисфагией (обзор). Ж Ларынгол Отол. 1987, 101: 627-632. 10.1017/S0022215100102403.
Артикул КАС пабмед Google ученый
Mader R: Клинические проявления диффузного идиопатического скелетного гиперостоза шейного отдела позвоночника. Семин Артрит Реум. 2002, 32: 130-135. 10.1053/сарх.2002.33726.
Артикул пабмед Google ученый
Ozgocmen S, Kiris A, Kocakoc E, Ardicoglu O: Дисфагия, вызванная остеофитами: отчет о трех случаях. Совместная кость позвоночника. 2002, 69: 226-229.
 10.1016/S1297-319X(02)00377-9.
10.1016/S1297-319X(02)00377-9.Артикул пабмед Google ученый
Умера Б.К., Мукерджи Б.К., Ибекве О.: Шейный спондилез и дисфагия. Ж Ларынгол Отол. 1981, 95: 1179-1183. 10.1017/С0022215100092008.
Артикул КАС пабмед Google ученый
Deutch EC, Schild JA, Mafee MF: Дисфагия и болезнь Форестье. Арка Отоларингол. 1985, 111: 400-402.
Артикул Google ученый
Айдын Э., Акдоган В., Аккузу Б., Кирбас И. Шесть случаев синдрома Форестье, редкой причины дисфагии. Acta Oto-Laryngologica. 2006, 126: 775-778. 10.1080/00016480500504192.
Артикул пабмед Google ученый
Департамент пожилых людей, больница Челси и Вестминстер Фонд, Фулхэм -роуд, Лондон, SW10 9NH, Великобритания
Sema Srivastava, Natalia Ciapryna & Iñaki Bovill
- Наталья Цеприна
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Академия
- Иньяки Бовилл
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
35. Chaput C.D., Siddiqui M., Rahm MD. Ожирение и кальцификация связок позвоночника: комплексный КТ-анализ всего позвоночника в случайная популяция травм. Спайн Дж. 2019; 19:1346–1353. doi: 10.1016/j.spinee.2019.03.003. [PubMed] [CrossRef] [Google Scholar]
36. Сон С., Чанг С. К., Хан И., Парк С.Б., Ким Х. Повышение минеральной плотности костей при диффузном идиопатическом скелетном гиперостозе шейного или грудного отдела (DISH): Случай- Контрольное исследование. Дж. Клин. Денситом. 2018;21:68–74. doi: 10.1016/j.jocd.2016.09.001. [PubMed] [CrossRef] [Google Scholar]
К., Хан И., Парк С.Б., Ким Х. Повышение минеральной плотности костей при диффузном идиопатическом скелетном гиперостозе шейного или грудного отдела (DISH): Случай- Контрольное исследование. Дж. Клин. Денситом. 2018;21:68–74. doi: 10.1016/j.jocd.2016.09.001. [PubMed] [CrossRef] [Google Scholar]
37. Мадер Р., Новофестовский И., Адави М., Лави И. Метаболический синдром и сердечно-сосудистый риск у пациентов с диффузным идиопатическим скелетным гиперостозом. Семин. Ревмирующий артрит. 2009; 38: 361–365. doi: 10.1016/j.semarthrit.2008.01.010. [PubMed] [CrossRef] [Google Scholar]
38. Глик К., Новофастовски И., Шварц Н., Мадер Р. Сердечно-сосудистые заболевания при диффузном идиопатическом скелетном гиперостозе (DISH): от теории к реальности — 10-летнее наблюдение исследование. Артрит Рез. тер. 2020;22:190. doi: 10.1186/s13075-020-02278-w. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
39. Fassio A., Adami G., Idolazzi L., Giollo A., Viapiana O., Bosco E._10.jpg) , Negrelli R., Sani E. , Сандри Д., Мантовани А. и др. Диффузный идиопатический скелетный гиперостоз (DISH) при диабете 2 типа: новая возможность визуализации и новый биомаркер. кальциф. Ткань внутр. 2021; 108: 231–239. doi: 10.1007/s00223-020-00768-2. [PubMed] [CrossRef] [Google Scholar]
, Negrelli R., Sani E. , Сандри Д., Мантовани А. и др. Диффузный идиопатический скелетный гиперостоз (DISH) при диабете 2 типа: новая возможность визуализации и новый биомаркер. кальциф. Ткань внутр. 2021; 108: 231–239. doi: 10.1007/s00223-020-00768-2. [PubMed] [CrossRef] [Google Scholar]
40. Mader R., Lavi I. Сахарный диабет и гипертония как факторы риска раннего диффузного идиопатического скелетного гиперостоза (DISH) Osteoarthr. Хрящ. 2009 г.;17:825–828. doi: 10.1016/j.joca.2008.12.004. [PubMed] [CrossRef] [Google Scholar]
41. Corkill M., Topless R., Worthington A., Mitchell R., Gregory K., Stamp L.K., Brown M., Merriman T.R., Dalbeth N. Exploring the Relationship между подагрой и диффузным идиопатическим скелетным гиперостозом (DISH): эпидемиологическое и генетическое исследование. [(по состоянию на 4 февраля 2021 г.)]; Arthritis Rheumatol. 2018 70 (Приложение 10) Доступно в Интернете: https://acrabstracts.org/abstract/exploring-the-relationship-between-gout-and-diffuse-idiopathic-skeletal-hyperostosis-dish-an-epidemiologic-and-genetic- исследование/ [Google Scholar]
42. Эль Мидани Ю.М., Вассиф Г., Эль Баддини М. Диффузный идиопатический скелетный гиперостоз (DISH): сосудистая этиология? клин. Эксп. Ревматол. 2000; 18: 193–200. [PubMed] [Google Scholar]
Эль Мидани Ю.М., Вассиф Г., Эль Баддини М. Диффузный идиопатический скелетный гиперостоз (DISH): сосудистая этиология? клин. Эксп. Ревматол. 2000; 18: 193–200. [PubMed] [Google Scholar]
43. Паппоне Н., Амброзино П., ди Минно М.Н.Д., Иерволино С. Является ли диффузный идиопатический скелетный гиперостоз заболеванием или синдромом? Ревматология. 2017;56:1635–1636. doi: 10.1093/ревматология/kew451. [PubMed] [CrossRef] [Google Scholar]
44. Bakker J.T., Kuperus J.S., Kuijf H.J., Oner F.C., de Jong P.A., Verlaan J.J. Морфологическая характеристика диффузного идиопатического скелетного гиперостоза шейного отдела позвоночника. ПЛОС ОДИН. 2017;12:e0188414. doi: 10.1371/journal.pone.0188414. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
45. Xu M., Liu Y., Yang J., Liu H., Ding C. Окостенение шейной передней продольной связки является недиагностированной причиной затруднения проходимости дыхательных путей: клинический случай и обзор литературы. БМС Анестезиол.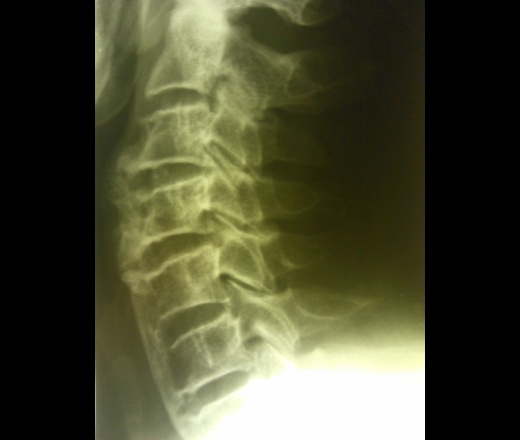 2020;20:161. doi: 10.1186/s12871-020-01077-9. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
2020;20:161. doi: 10.1186/s12871-020-01077-9. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
46. Dell’Era V., Garzaro M., Farri F., Gorris C., Rosa M.S., Toso A., Aluffi Valletti P. Респираторная презентация диффузного идиопатического скелетного гиперостоза (DISH): Управление и обзор литературы. Кранио. 2019: 1–4. doi: 10.1080/08869634.2019.1667044. [PubMed] [CrossRef] [Google Scholar]
47. Souza S., Raggio B., Bareiss A., Friedlander P. Диффузный идиопатический скелетный гиперостоз шейного отдела позвоночника: риск острой обструкции дыхательных путей. Ear Nose Throat J. 2020 doi: 10.1177/0145561320931212. [PubMed] [CrossRef] [Google Scholar]
48. Нисимура Х., Эндо К., Айхара Т., Мурата К., Судзуки Х., Мацуока Ю., Такамацу Т., Маэкава А., Савадзи Ю., Цудзи Х. и др. Факторы риска дисфагии у больных с окостенением передней продольной связки. Дж. Ортоп. Surg. 2020; 28 дои: 10.1177/230949
60564. [PubMed] [CrossRef] [Google Scholar] 49. Garcia Callejo F. J., Oishi N., Lopez Sanchez I., Pallares Marti B., Rubio Fernandez A., Gomez Gomez M.J. Модель дисфагии. Акта Оторриноларингол. особ. 2020; 71: 78–82. doi: 10.1016/j.otoeng.2019.02.002. [PubMed] [CrossRef] [Google Scholar]
J., Oishi N., Lopez Sanchez I., Pallares Marti B., Rubio Fernandez A., Gomez Gomez M.J. Модель дисфагии. Акта Оторриноларингол. особ. 2020; 71: 78–82. doi: 10.1016/j.otoeng.2019.02.002. [PubMed] [CrossRef] [Google Scholar]
50. Lee J.H., Paeng S.H., Pyo S.Y., Kim S.T., Lee W.H. Затрудненное глотание при диффузном идиопатическом скелетном гиперостозе с метаболическим синдромом. Корейский Дж. Нейротравма. 2020;16:90–98. doi: 10.13004/kjnt.2020.16.e4. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
51. Bartalena T., Buia F., Borgonovi A., Rinaldi MF, Modolon C., Bassi F. DISH шейного отдела позвоночника, вызывающий ущемление надгортанника. Индиан Дж. Радиол. Визуализация. 2009; 19: 132–134. doi: 10.4103/0971-3026.50831. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
52. Канделарио Н., Ло К.Б., Наранхо М. Шейный диффузный идиопатический гиперостоз скелета (DISH), вызывающий орофарингеальную дисфагию. BMJ Case Rep. 2017; 2017 doi: 10.1136/bcr-2016-218630.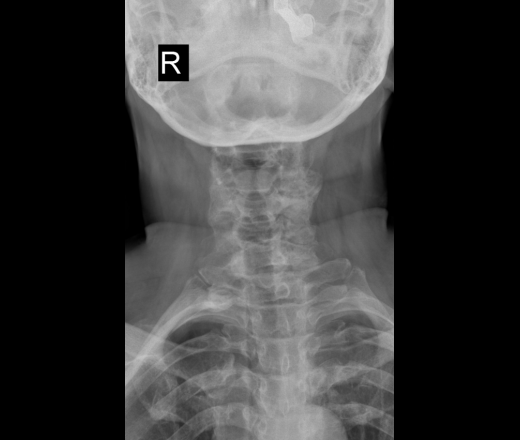 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
53. Домбровский М., Сулевский А., Качмарчик Ю., Кубашевский Л. Хирургическое лечение диффузного идиопатического скелетного гиперостоза шейного отдела позвоночника с дисфагией. Клинический случай. Анна. Мед. Surg. 2020;57:37–40. doi: 10.1016/j.amsu.2020.07.009. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
54. Weglowski R., Piech P. Дисфагия как симптом переднего шейного гиперостоза — клинический случай. Анна. Агр. Окружающая среда. Мед. 2020;27:314–316. doi: 10.26444/aaem/106115. [PubMed] [CrossRef] [Академия Google]
55. Мадер Р., Баралиакос Х., Эшед И., Новофастовский И., Бибер А., Верлаан Дж.Дж., Кифер Д., Паппоне Н., Ацени Ф. Визуализация диффузного идиопатического скелетного гиперостоза (DISH) RMD Open. 2020;6 doi: 10.1136/rmdopen-2019-001151. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
56. Кумар М., Шахи П.Б., Адсул Н., Ачарья С., Калра К.Л., Чахал Р.С. Прогрессирующая дисфагия и дисфония, вторичная по отношению к передним шейным остеофитам, связанным с DISH: клинический случай. Surg. Нейрол. Междунар. 2020;11:69. doi: 10.25259/SNI_61_2020. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Surg. Нейрол. Междунар. 2020;11:69. doi: 10.25259/SNI_61_2020. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
57. Батлер А.Дж., Гасем А., Аль Маайех М. Дисфагия после операции на поясничном отделе позвоночника в условиях невыявленной DISH шейного отдела позвоночника: отчет о клиническом случае. Отчет по делу AME, 2019 г.; 3:13. doi: 10.21037/акр.2019.05.03. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
58. Kuperus J.S., Oudkerk S.F., Foppen W., Mohamed Hoesein F.A., Gielis W.P., Waalwijk J., Regan E.A., Lynch D.A., Oner F.C., de Джонг П.А. и соавт. Критерии диффузного идиопатического скелетного гиперостоза на ранней стадии: разработка и проверка. Радиология. 2019;291:420–426. doi: 10.1148/radiol.2019181695. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
59. Soejima Y., Arima J., Doi T. Диффузный идиопатический скелетный гиперостоз: случай с дисфонией, дисфагией и миелопатией. Являюсь. J. Case Rep. 2019; 20: 349–353. doi: 10. 12659/AJCR.913792. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
12659/AJCR.913792. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
60. Зарей М., Гольбахш М., Ростами М., Моосави М. Дисфония, стридор и дисфагия, вызванные диффузным идиопатическим скелетным гиперостозом: клинический случай и Обзор литературы. Доп. Биомед. Рез. 2020;9:47. doi: 10.4103/abr.abr_50_20. [PMC бесплатная статья] [PubMed] [CrossRef] [Google Scholar]
и другие. Передняя шейная резекция остеофита для лечения дисфагии. Глоб. Spine J. 2020 doi: 10.1177/2192568220912706. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
62. Von der Hoeh N.H., Voelker A., Jarvers J.S., Gulow J., Heyde CE. Результаты после хирургического лечения переднего шейного гиперостоза, вызывающего дисфагию. Евро. Спайн Дж. 2015; 24:489–493. doi: 10.1007/s00586-014-3507-4. [PubMed] [CrossRef] [Google Scholar]
63. Ruetten S., Baraliakos X., Godolias G., Komp M. Хирургическое лечение передних шейных остеофитов, вызывающих дисфагию. Дж. Ортоп. Surg. 2019; 27 doi: 10. 1177/230949
1177/230949
37424. [PubMed] [CrossRef] [Google Scholar]
64. Фон Глински А., Такаянаги А., Элиа С., Исхак Б., Листманн М., Пьер К.А., Блечер Р., Хейман Э., Чепмен Дж.Р., Оскуян Р.Дж. Хирургическое лечение оссификаций передней продольной связки шейного отдела позвоночника: ретроспективное когортное исследование. Глоб. Spine J. 2020 doi: 10.1177/2192568220922195. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
65. Damade C., Masse R., Ghailane S., Petit M., Castelain J.E., Gille O., Mazas S., Bouyer B. ., Kieser D.C. Передний шейный идиопатический гиперостоз и дисфагия: влияние хирургического лечения — исследование серии из 11 случаев. Мировой нейрохирург. 2020; 138: 305–310. doi: 10.1016/j.wneu.2020.02.097. [PubMed] [CrossRef] [Google Scholar]
66. Miyamoto K., Sugiyama S., Hosoe H., Iinuma N., Suzuki Y., Shimizu K. Послеоперационный рецидив остеофитов, вызывающих дисфагию у пациентов с диффузным идиопатическим скелетным гиперостозом . Евро. Спайн Дж. 2009 г.;18:1652–1658. doi: 10.1007/s00586-009-1133-3. [PMC бесплатная статья] [PubMed] [CrossRef] [Google Scholar]
2009 г.;18:1652–1658. doi: 10.1007/s00586-009-1133-3. [PMC бесплатная статья] [PubMed] [CrossRef] [Google Scholar]
Диффузный идиопатический скелетный гиперостоз как недооцененная причина дисфагии: клинический случай | Journal of Medical Case Reports
Диффузный идиопатический скелетный гиперостоз как недооцененная причина дисфагии: отчет о клиническом случае
Скачать PDF
Журнал медицинских историй болезни том 2 , номер статьи: 287 (2008 г.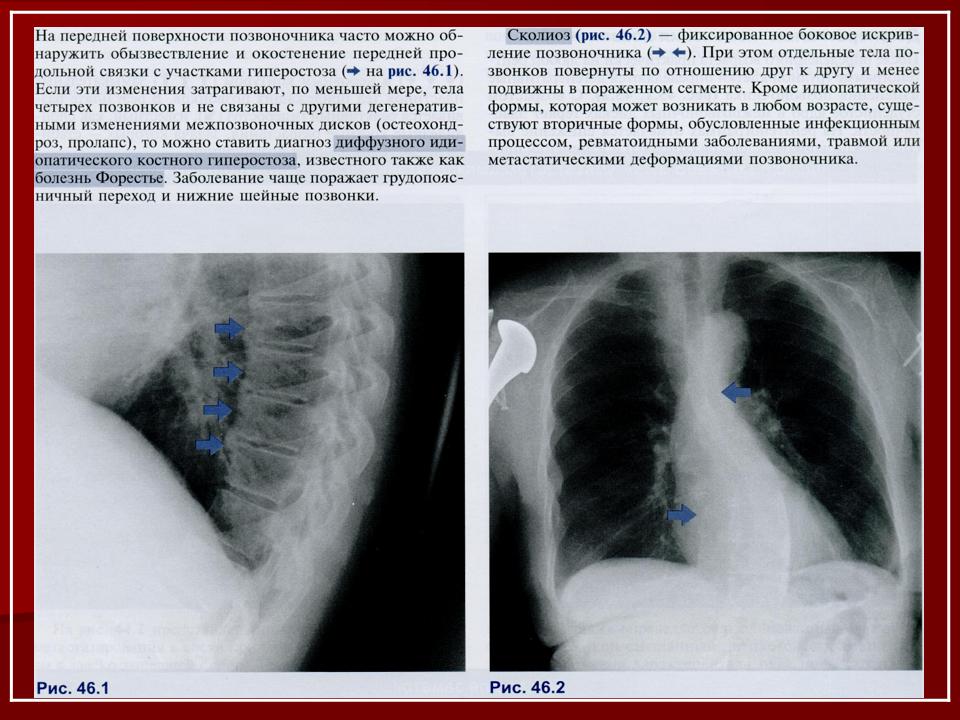 )
Процитировать эту статью
)
Процитировать эту статью
Abstract
Введение
Дисфагия является частым проявлением у пожилых людей. Диффузный идиопатический скелетный гиперостоз, поражающий шейный отдел позвоночника, является редкой причиной дисфагии и может оставаться незамеченным.
Описание случая
Мы представляем случай 88-летнего мужчины с дисфагией и потерей веса. Первоначальное исследование с эндоскопией верхних отделов желудочно-кишечного тракта не дало результатов. Диагноз диффузного идиопатического скелетного гиперостоза как причины дисфагии в конечном итоге был поставлен с помощью видеофлюороскопии. Это показало костный выступ, препятствующий глотанию на уровне C3. Пациент был непригоден для хирургического лечения, поэтому для кормления была вставлена чрескожная эндоскопическая гастростомическая трубка.
Это показало костный выступ, препятствующий глотанию на уровне C3. Пациент был непригоден для хирургического лечения, поэтому для кормления была вставлена чрескожная эндоскопическая гастростомическая трубка.
Заключение
Диагноз диффузного идиопатического скелетного гиперостоза с вовлечением шейного отдела позвоночника часто остается нераспознанным как причина дисфагии, несмотря на его распространенность среди пожилых людей. Диагноз ставится с помощью рентгенографии шейки матки, глотания бария и компьютерной томографии. Существует риск перфорации при эндоскопии у пациентов с диффузным идиопатическим скелетным гиперостозом шейки матки. Консервативное лечение включает нестероидные противовоспалительные препараты и модифицированную диету. Хирургическое вмешательство может быть рассмотрено у некоторых пациентов, у которых консервативное лечение оказалось неэффективным.
Отчеты экспертной оценки
Введение
Диффузный идиопатический гиперостоз был впервые описан в 1950 г. Forestier и Rotes-Querol [1]. Он характеризуется чрезмерной кальцификацией связок и окостенением в спинальной и экстраспинальной локализациях. При поражении шейного отдела позвоночника могут образовываться крупные остеофиты, вызывающие симптомы дисфагии. Мы описываем случай 88-летнего мужчины с дисфагией и потерей веса, вторичными по отношению к диффузному идиопатическому скелетному гиперостозу (DISH).
Forestier и Rotes-Querol [1]. Он характеризуется чрезмерной кальцификацией связок и окостенением в спинальной и экстраспинальной локализациях. При поражении шейного отдела позвоночника могут образовываться крупные остеофиты, вызывающие симптомы дисфагии. Мы описываем случай 88-летнего мужчины с дисфагией и потерей веса, вторичными по отношению к диффузному идиопатическому скелетному гиперостозу (DISH).
История болезни
88-летний мужчина поступил с 6-месячной историей дисфагии при приеме твердой пищи и значительной потерей веса. Он отрицал какие-либо симптомы одинофагии. Охриплость голоса, боль в шее или одышку отрицал. Не было никаких изменений в привычке кишечника или крови в стуле. Его калорийность зависела исключительно от протеиновых добавок. В его предыдущей медицинской истории были диабет 2 типа, гиперхолестеринемия, гипертония, мерцательная аритмия и глаукома.
При осмотре: вялость, бледность. Его вес составлял 54 кг. Остальная часть его физического осмотра была ничем не примечательна.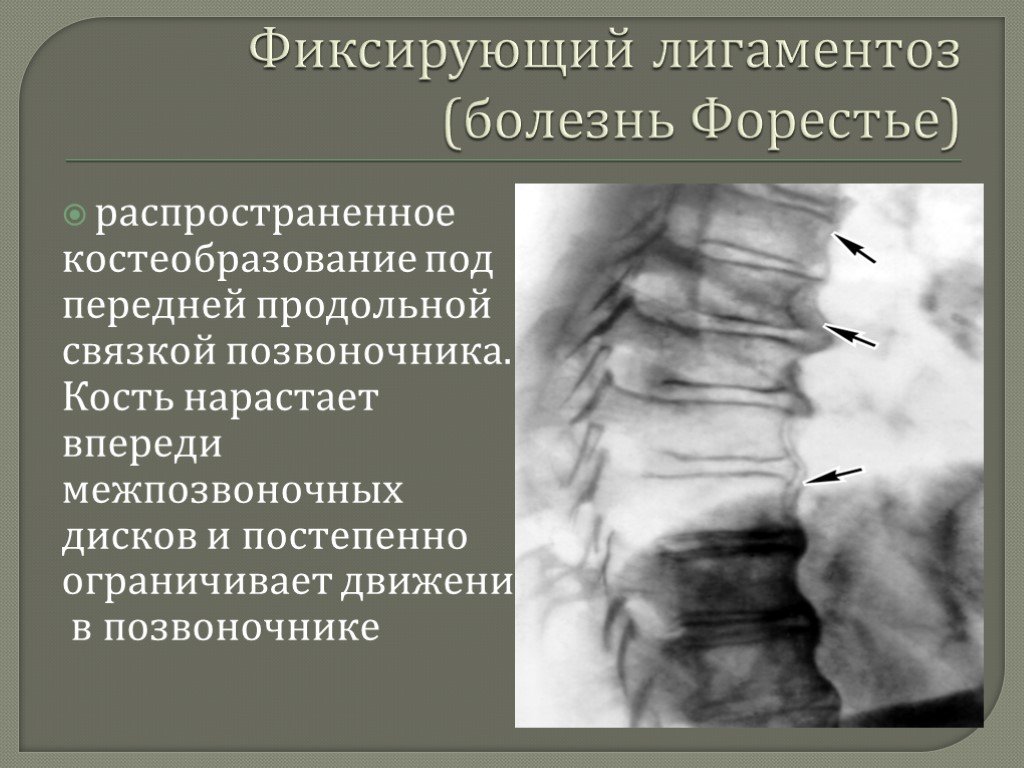 Общий анализ крови показал нормоцитарную анемию (10,3 г/дл) с нормальным уровнем ферритина. Функция печени была нормальной, кроме альбумина 28 г/л. Скорость оседания эритроцитов и уровень тиреотропного гормона в норме. Эндоскопия была выполнена, чтобы исключить внутреннюю причину симптомов пациента. Это показало хронический атрофический гастрит, но не причину дисфагии. Выполнена видеофлюороскопия, которая показала костный выступ, препятствующий глотанию на уровне С3. Рентгенограмма шейного отдела позвоночника в боковой проекции показала образование остеофитов в передней части, наиболее заметное в позвонках С3/С4 и соответствующее DISH (рис. 1).
Общий анализ крови показал нормоцитарную анемию (10,3 г/дл) с нормальным уровнем ферритина. Функция печени была нормальной, кроме альбумина 28 г/л. Скорость оседания эритроцитов и уровень тиреотропного гормона в норме. Эндоскопия была выполнена, чтобы исключить внутреннюю причину симптомов пациента. Это показало хронический атрофический гастрит, но не причину дисфагии. Выполнена видеофлюороскопия, которая показала костный выступ, препятствующий глотанию на уровне С3. Рентгенограмма шейного отдела позвоночника в боковой проекции показала образование остеофитов в передней части, наиболее заметное в позвонках С3/С4 и соответствующее DISH (рис. 1).
Рентгенограмма шейного отдела позвоночника в боковой проекции, показывающая образование передних остеофитов, наиболее заметное на уровне С3/С4 позвонков, и кальцификацию передних продольных связок.
Изображение в полный размер
Ему было начато назогастральное питание, так как при видеофлюороскопии были обнаружены признаки аспирации.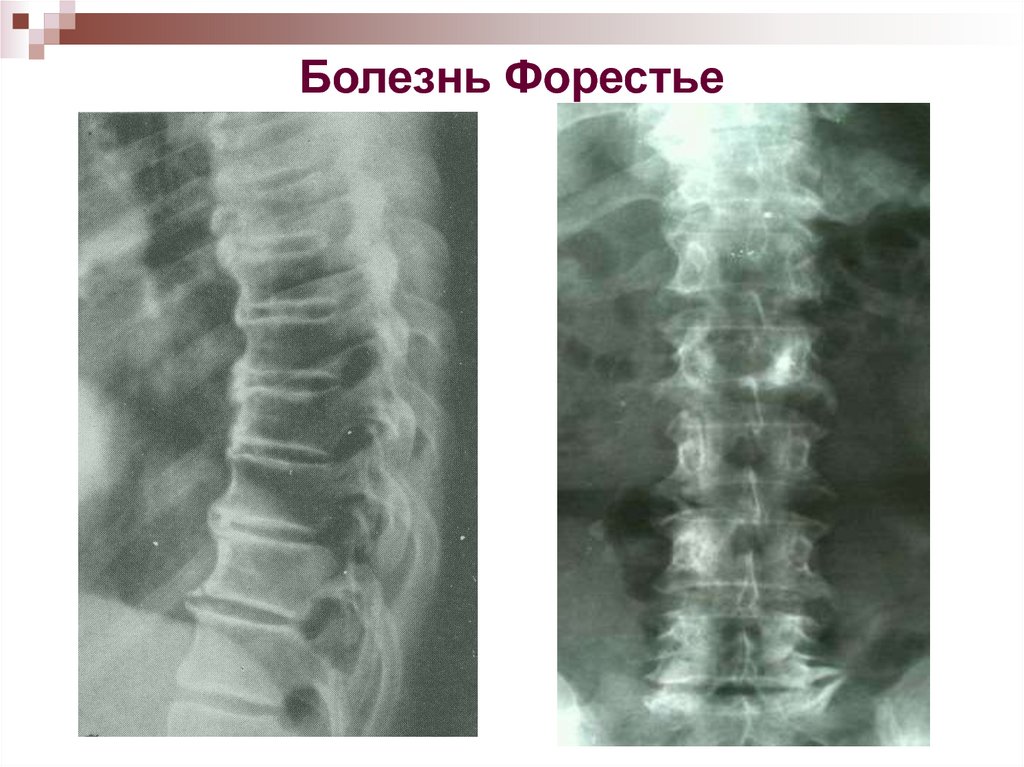 Его направили к спинальным хирургам, но они не сочли операцию целесообразной из-за слабого состояния пациента и сопутствующих заболеваний. Чрескожная эндоскопическая гастростомическая трубка была установлена через 3 недели. Пациент умер через 6 недель после госпитализации от осложнений, вторичных по отношению к несвязанному септическому артриту плеча.
Его направили к спинальным хирургам, но они не сочли операцию целесообразной из-за слабого состояния пациента и сопутствующих заболеваний. Чрескожная эндоскопическая гастростомическая трубка была установлена через 3 недели. Пациент умер через 6 недель после госпитализации от осложнений, вторичных по отношению к несвязанному септическому артриту плеча.
Обсуждение
DISH — распространенное, но игнорируемое заболевание, наблюдаемое у пожилых людей. Он характеризуется образованием новой кости в осевых и периферических энтезиальных областях. Сообщается, что распространенность DISH составляет 10% у пациентов старше 70 лет (см. [2]). Этиология DISH не установлена, но есть ассоциации с диабетом, ожирением [3], гиперхолестеринемией и подагрой. DISH чаще всего поражает грудной отдел позвоночника, хотя вовлечение шейного отдела позвоночника обнаруживается у 76% пострадавших [4]. Распространенность дисфагии, связанной с DISH, поражающей шейный отдел позвоночника, составляет 28% [5].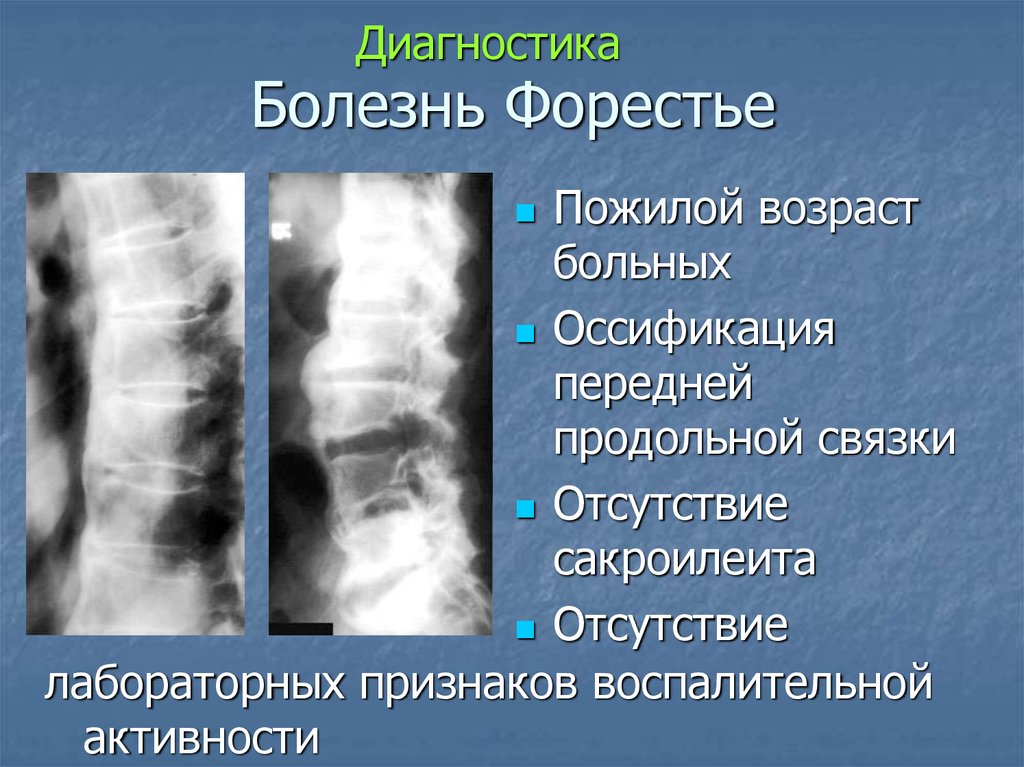 Дисфагия, вызванная DISH, может быть обусловлена несколькими факторами: прямой механической компрессией пищевода крупными передними остеофитами; более мелкие остеофиты, расположенные в местах фиксации пищевода, например, на уровне перстневидного хряща; воспаление околопищеводных мягких тканей в месте контакта с вышележащими остеофитами; или спазм пищевода, вызванный болезненными остеофитами [6].
Дисфагия, вызванная DISH, может быть обусловлена несколькими факторами: прямой механической компрессией пищевода крупными передними остеофитами; более мелкие остеофиты, расположенные в местах фиксации пищевода, например, на уровне перстневидного хряща; воспаление околопищеводных мягких тканей в месте контакта с вышележащими остеофитами; или спазм пищевода, вызванный болезненными остеофитами [6].
Диагноз DISH рентгенологический. Простые рентгенограммы шейного отдела позвоночника обычно показывают текущую кальцификацию и окостенение вдоль передней поверхности по крайней мере четырех смежных позвонков. Большие передние остеофиты обычно обнаруживаются между С4 и С7 [7]. Компьютерная томография является еще одним полезным методом визуализации в диагностике DISH, поскольку размер и форма остеофитов показаны относительно пищевода и других важных структур. Глотание бария или видеофлюороскопия подтвердят компрессию пищевода и обструкцию в связи с большими передними остеофитами. Эндоскопия у этих пациентов сопряжена с риском перфорации, но может быть необходима для исключения других внутренних причин дисфагии, таких как стриктуры пищевода, эзофагит, ткани пищевода, нарушения моторики, опухоли и кандидоз [8]. Другими клиническими проявлениями, связанными с шейным DISH, являются охриплость голоса, стридор, аспирационная пневмония, миелопатия, синдром грудной апертуры и апноэ во сне [7]. Лечение делится на консервативное и хирургическое. Консервативное лечение включает модификацию диеты, нестероидные воспалительные препараты, кортикостероиды и миорелаксанты [9]., 10]. В тяжелых случаях хирургическое лечение может быть единственным вариантом и включает остеофитэктомию. Хирургический доступ может быть переднебоковым, заднелатеральным или трансфарингеальным, когда вовлечены позвонки от С2 до С4. Осложнения включают повреждение гортанного нерва, инсульт, синдром Горнера и нестабильность шейки матки [11].
Другими клиническими проявлениями, связанными с шейным DISH, являются охриплость голоса, стридор, аспирационная пневмония, миелопатия, синдром грудной апертуры и апноэ во сне [7]. Лечение делится на консервативное и хирургическое. Консервативное лечение включает модификацию диеты, нестероидные воспалительные препараты, кортикостероиды и миорелаксанты [9]., 10]. В тяжелых случаях хирургическое лечение может быть единственным вариантом и включает остеофитэктомию. Хирургический доступ может быть переднебоковым, заднелатеральным или трансфарингеальным, когда вовлечены позвонки от С2 до С4. Осложнения включают повреждение гортанного нерва, инсульт, синдром Горнера и нестабильность шейки матки [11].
Заключение
Дисфагия является частым проявлением у пожилых людей. Диагноз DISH с поражением шейного отдела позвоночника часто остается нераспознанным как причина дисфагии, несмотря на его распространенность среди пожилых людей. Диагноз устанавливается с помощью простой рентгенографии шейки матки и глотания бария, особенно когда эндоскопия исключает внутреннюю причину дисфагии.
Согласие
Письменное информированное согласие не может быть получено в этом случае, так как ближайшие родственники пациента не могут быть отслежены. Мы считаем, что этот отчет о клиническом случае содержит полезный клинический урок, который нельзя было бы извлечь столь же эффективно каким-либо другим способом. Мы ожидаем, что ближайшие родственники пациента не будут возражать против публикации, поскольку были предприняты все усилия, чтобы пациент остался анонимным.
Сокращения
Список литературы
Julkunen H, Heinonen OP, Knekt P, Maatela J: Эпидемиология гиперостоза позвоночника вместе с его симптомами и связанной с ними смертностью среди населения в целом. Scand J Ревматол. 1975, 4: 23-27. 10.3109/03009747509095610.
Артикул КАС пабмед Google ученый
Ссылки на скачивание
Информация об авторе
Авторы и организации
AUTHORS 9000.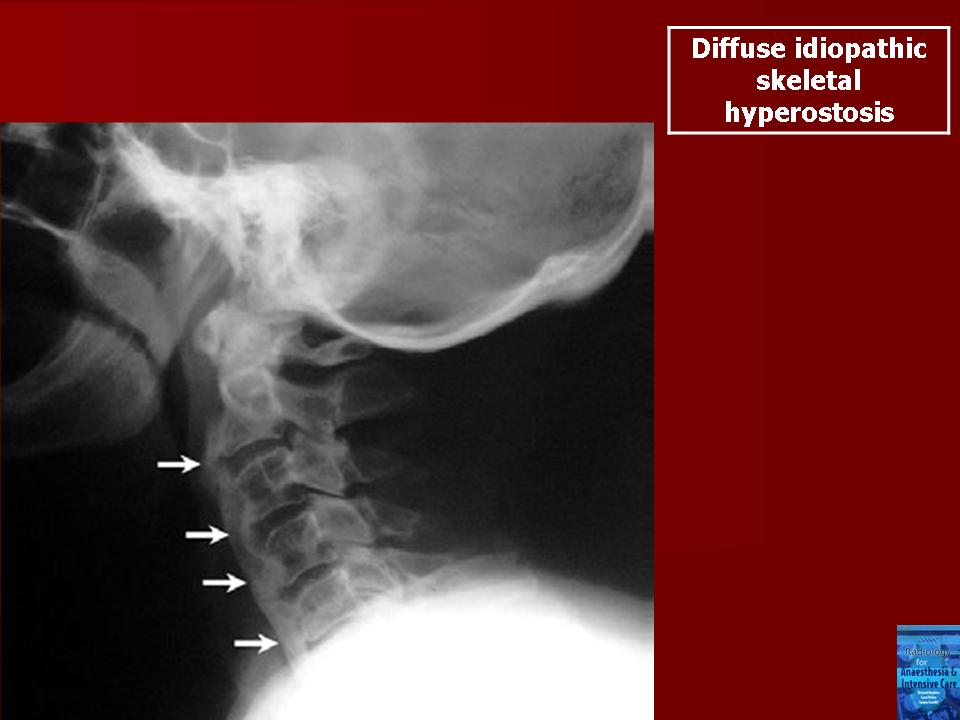
- 293
AUTHORS 9000.
- 2939393143
AUTHOR Вы также можете искать этого автора в PubMed Google Scholar
Автор, ответственный за корреспонденцию
Сима Шривастава.
Дополнительная информация
Конкурирующие интересы
Авторы заявляют об отсутствии конкурирующих интересов.
Вклад авторов
Авторы принимали участие в написании рукописи или клинической помощи пациенту. Все авторы прочитали и одобрили окончательный вариант рукописи.
Оригинальные файлы изображений, представленные авторами
Ниже приведены ссылки на оригинальные файлы изображений, представленные авторами.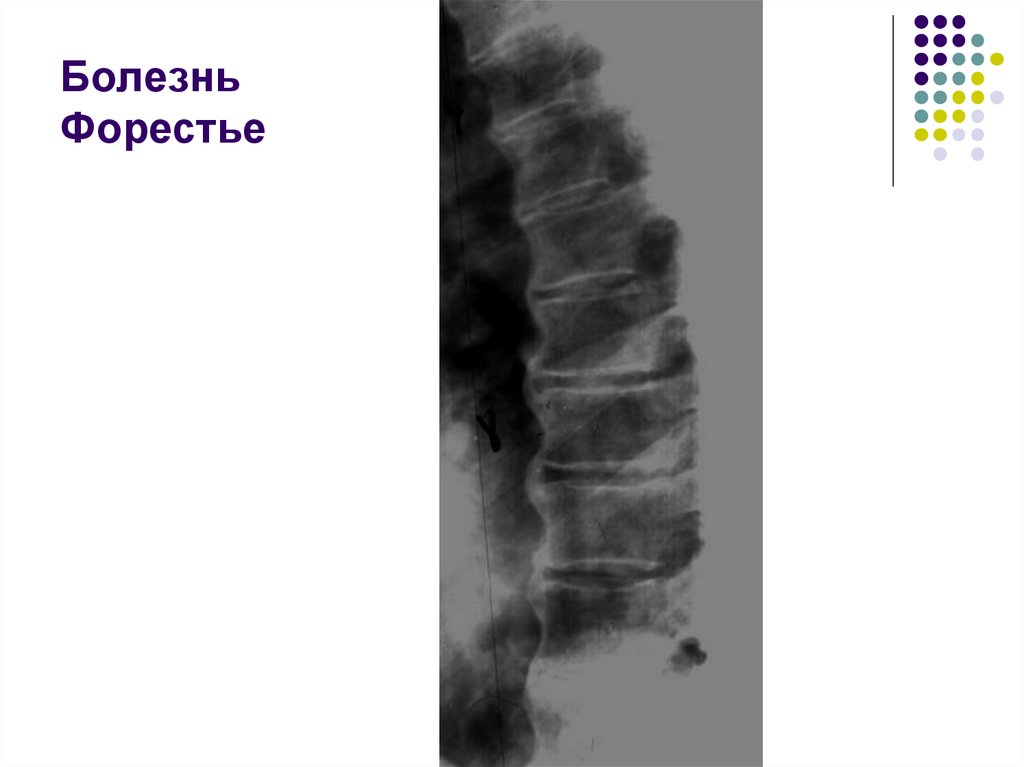
 Б., Ниваяма Г., Утсингер П.Д., Шауль С.Р.: Диффузный идиопатический гиперостоз скелета (DISH). Семин Артрит Реум. 1978, 7: 153-187. 10.1016/0049-0172(78)
Б., Ниваяма Г., Утсингер П.Д., Шауль С.Р.: Диффузный идиопатический гиперостоз скелета (DISH). Семин Артрит Реум. 1978, 7: 153-187. 10.1016/0049-0172(78) 10.1016/S1297-319X(02)00377-9.
10.1016/S1297-319X(02)00377-9.