Лечение остеохондроза банками в Москве
Остеохондроз — патология, связанная с дегенеративными изменениями костной и хрящевой структуры межпозвонковых дисков, сегодня встречается у каждого второго человека в возрасте за 30 лет. Хотя первые симптомы могут проявляться уже в подростковом возрасте. Основными причинами остеохондроза являются неправильная осанка, лишний вес, травмы, врожденные и сопутствующие заболевания.
Симптоматика остеохондроза различна, зависит от области поражения, давности и тяжести заболевания. Характерными симптомами, указывающими на патологию костно-суставной системы позвоночного столба, являются:
- Боли в области спины, сосредоточенные, в основном, в районе позвоночника;
- Ощущение скованности, так называемого «корсета» в позвоночнике и грудной клетке;
- Головные боли непонятной этиологии;
- Онемение и покалывание кончиков пальцев, стоп, кистей рук, слабость конечностей;
- Проблемы с концентрацией внимания;
- Головокружения, шум в ушах.
Многие симптомы затрагивают внутренние органы, и пациенты редко связывают их с поражениями позвоночника.
О методах лечения остехондроза написано достаточно много — как в официально принятой медицине, так и в альтернативной. Лечение может быть консервативным и хирургическим — при необратимости процессов дегенерации хрящевых дисков.
Одним из популярных методов является лечение баночным массажем. Банки при остеохондрозе нужно использовать в комплексе с другими способами лечения и под наблюдением врача-вертебролога или невропатолога.
Эффект баночного лечения достигается путем притока крови к мягким тканям, и приводит к улучшению кровообращения и оттоку лимфы в пораженных областях, что сокращает воспаление и отеки, увеличивает скорость регенерации межпозвонковых дисков, дополнительно нормализует тонус мышц и повышает их эластичность. Метод устраняет болевой синдром, снимает стресс, расслабляет, улучшает работу внутренних органов.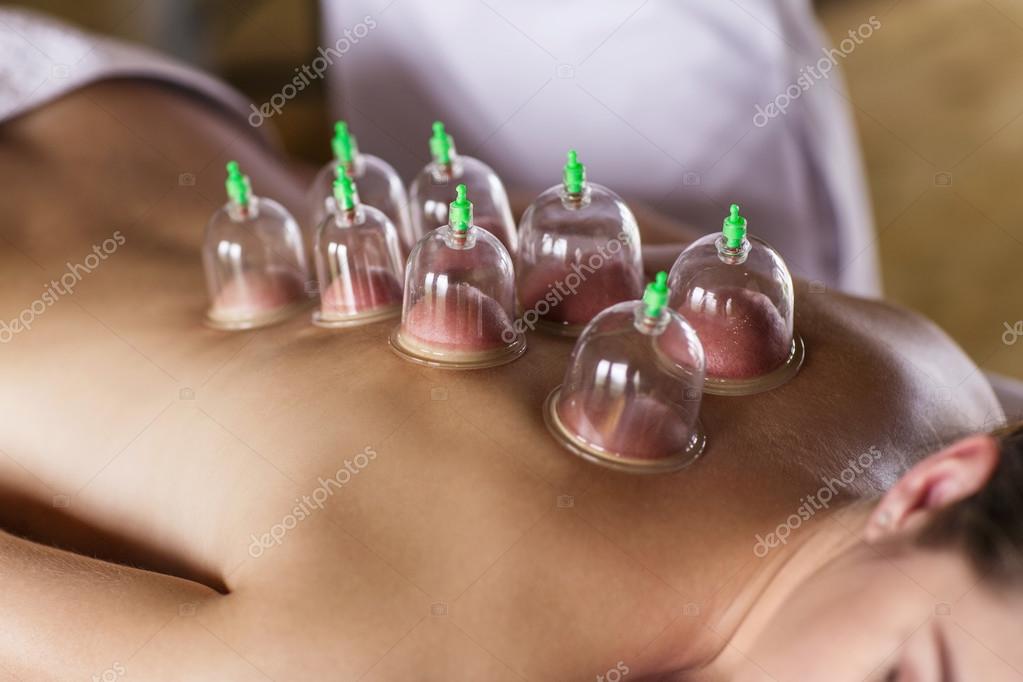
Особенно хорошо работают банки при шейном остеохондрозе, восстанавливая полноценный кровоток шейного отдела и головного мозга.
Лечение банками при остеохондрозе подразумевает обязательное и точное соблюдение рекомендаций, так как, при всех благоприятных воздействиях, метод имеет немало противопоказаний:
- Остеохондроз в острый период
- Артриты, особенно в остром периоде
- Токсикоз и любые интоксикации
- Почечная недостаточность
- Активные формы туберкулеза
- Сердечно-сосудистые патологии в декомпенсации
- Гепатит (любой)
- Артериальная гипертензия
- Послеоперационная реабилитация, ранний послеродовой период
- Психиатрические нарушения
- Все патологии кровеносных сосудов
- Склонность к кровотечениям, заболевания, связанные с нарушением свертываемости крови
- Гематомы и травмы в области спины
- Гнойничковые и любые инфекционные заболевания кожи.
Таким образом, самостоятельное лечение банками при скрытом или явном остеохондрозе обязательно сопровождается посещением врача.
Методика постановки банок
Банки, используемые при остеохондрозе, ставятся в следующей последовательности:
В начале проводится подготовка кожных покровов спины. Кожа обрабатывается небольшим количеством теплого массажного или растительного масла, которое нужно хорошо растереть. Это предотвратит болезненность, дискомфорт от процедуры и уменьшит образование гематом.
Далее необходимо — Взять в руку стеклянную банку. Смочить спиртом вату, удерживаемую пинцетом, или ватную палочку, зажечь ее и провести внутри банки. Долго греть огнем банку не стоит, это нужно для удаления из емкости банки лишнего кислорода и создания вакуумного эффекта, образующего тягу и создающего лечебный эффект.
Палочку удалить быстрым движением и поставить банку на подготовленный участок спины. После этого банку можно двигать по нужной области.
Движения выполняются плавно и неторопливо вдоль позвоночника.
Процедура занимает 5-15 минут. По окончании пациента нужно накрыть пледом, напоить теплым чаем.
Тибетская и китайская медицина доказали свою эффективность в лечении многих хронических заболеваний. В первую очередь за счет своего комплексного подхода. Лечение строго индивидуально во всех случаях. Особенно если у пациента смешанный тип конституции и есть расстройство всех дошей. Важна чуткость врача и союз пациента с врачом, строгая коррекция питания и образа жизни. Эффективно помогает как внутреннее лечение с помощью препаратов тибетской фармакопеи, так и внешнее, включающее методы акупунктуры и акупрессуры.
ᐉ Эффективность баночного массажа при остеохондрозе • ВитаМед в Краснодаре •
Баночный массаж при остеохондрозе может применяться как для купирования острого болевого синдрома, так и в качестве поддерживающего лечения.
Баночный массаж при остеохондрозе относится к локальным массажным воздействиям, что позволяет использовать его у той категории больных, которая имеет противопоказания к проведению общего массажа. Локальному воздействию обычно подвергаются пациенты преклонного возраста, имеющие слабое здоровье и противопоказания к проведению общего массажа (тромбофлебит, мочекаменная болезнь, желчекаменная болезнь, опухоли внутренних органов, в том числе и доброкачественные и др.). В ходе проведения баночного массажа при остеохондрозе, происходит стимуляция регенеративных процессов, улучшается кровообращение, что способствует активизации роста костей и других тканей. Эффективность баночного массажа при остеохондрозе связана с дозированным локальным воздействием во время процедуры на клетки костной, мышечной ткани, фасций, сосудов и нервов, что приводит их в активное состояние, способствует росту тканей и регенерации поврежденных костей, мышц и нервов. Что позволяет использовать баночный массаж при остеохондрозе в качестве восстановительного лечения, позволяющего предотвратить дальнейшее разрушение хряща межпозвоночного диска.
Эффективность хондроксида при лечении неврологических проявлений поясничного остеохондроза
С. С. Василевский Березовское РТМО Chondroxide’s efficiency in treatment of lumbar osteochondritis’ neurologic manifestations S. S. Vasilevsky Остеоартроз — это патологический процесс, заключающийся в нарушении нормального баланса разрушения и восстановления в суставном хряще и подхрящевой кости, что сопровождается фиброзом суставной капсулы, формированием краевых остеофитов и небольшим воспалением. В процессе развития заболевания возникают дегенеративные изменения в хрящевой ткани. Это проявляется деполимеризацией и убылью компонентов протеингликанов. Содержание протеинов в артрозном хряще уменьшается главным образом за счет хондроитинсульфата. Наряду с этим происходит снижение функции и гибель хондроцитов в поверхностных слоях хряща при наличии пролиферации этих клеток в более глубоких слоях. Дегенерация суставного хряща может быть обусловлена несколькими, чаще одновременно действующими причинами и механизмами.
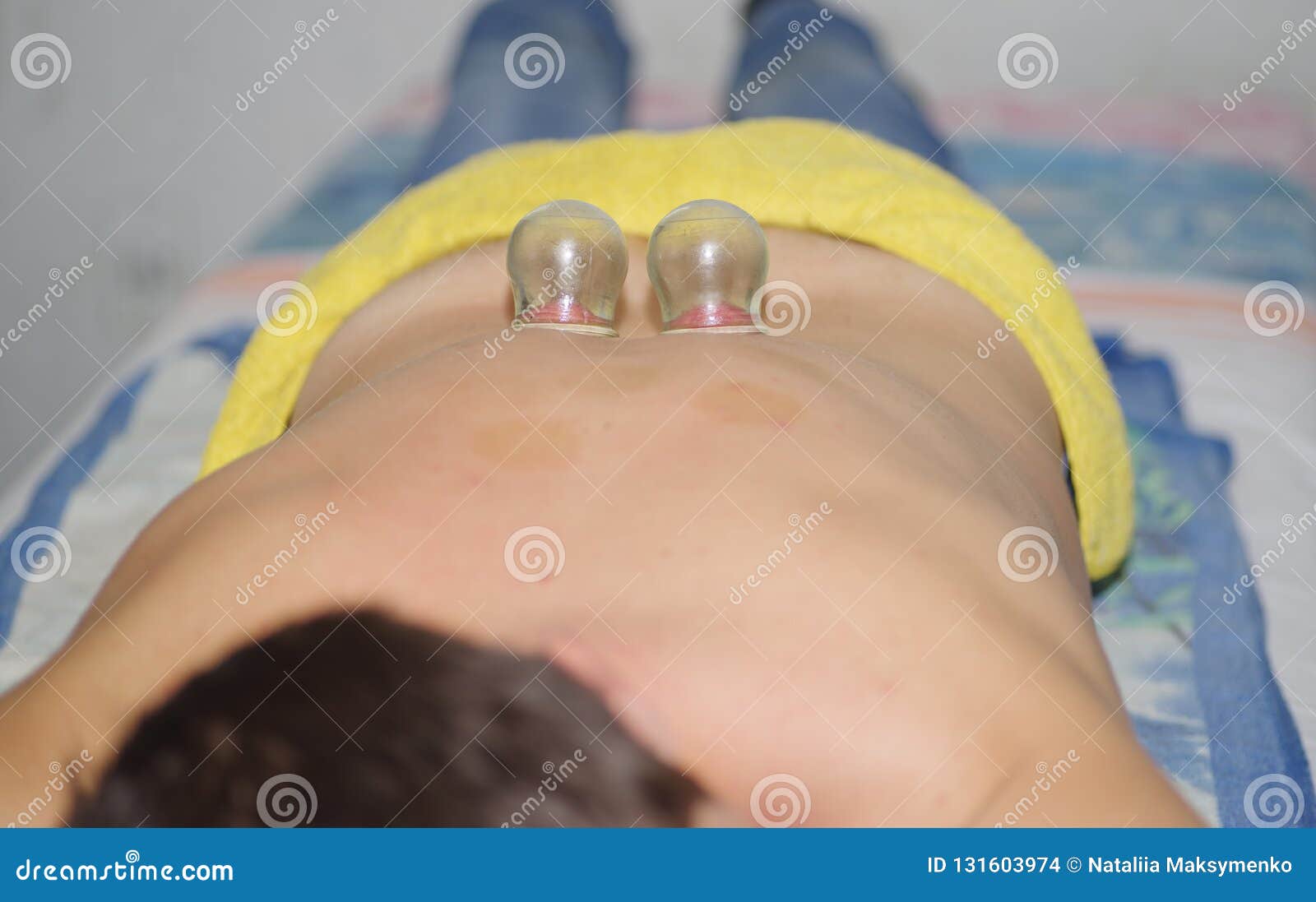
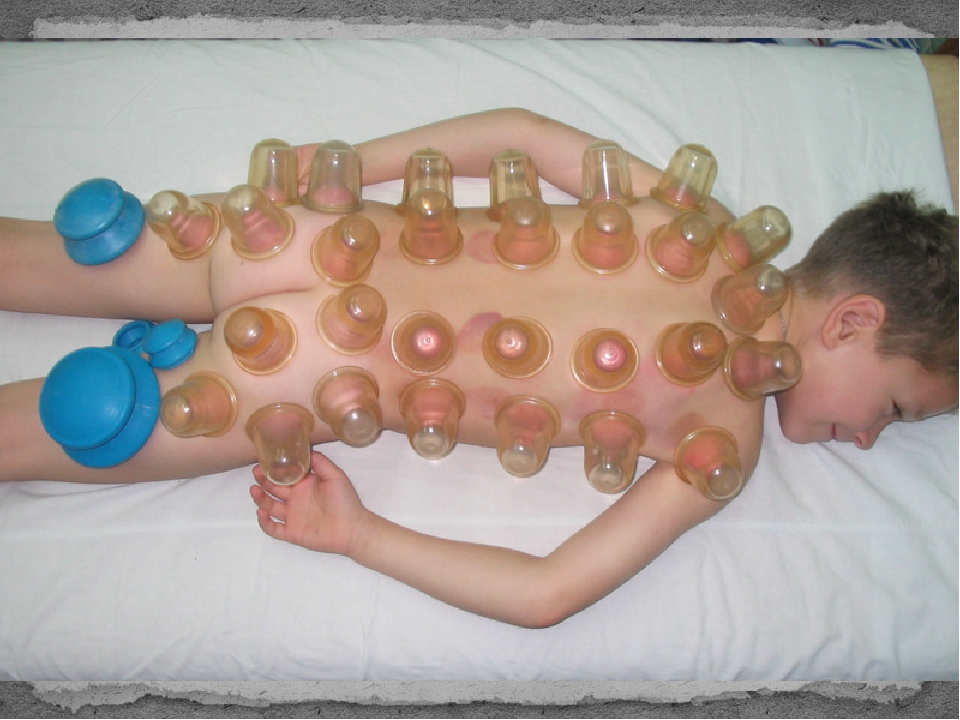
БАНОЧНЫЙ МАССАЖ ПРИ ОСТЕОХОНДРОЗЕ ПОЗВОНОЧНИКА
Баночный массаж при остеохондрозе позвоночника используется с давних времен. Лечебный эффект достигается за счет создания вакуума и теплового воздействия на пораженный участок тела. Такой метод терапии можно использовать при повреждениях различных отделов позвоночника. Ставить банки можно всеми известным способом или же массировать ими поврежденное место.
Баночный массаж и его воздействие
Массаж можно проводить только по назначению врача, учитывая возможные противопоказания и индивидуальные особенности каждого пациента. Он эффективно воздействует при поясничном, шейном и грудном остеохондрозе и совершенно безвреден для организма. Благодаря этому, массаж можно применять и в детском возрасте.
Массаж используется как дополнительное средство в лечении различных недугов, которое улучшает кровообращение, питание поврежденной области и значительно уменьшает выраженность симптомов заболевания.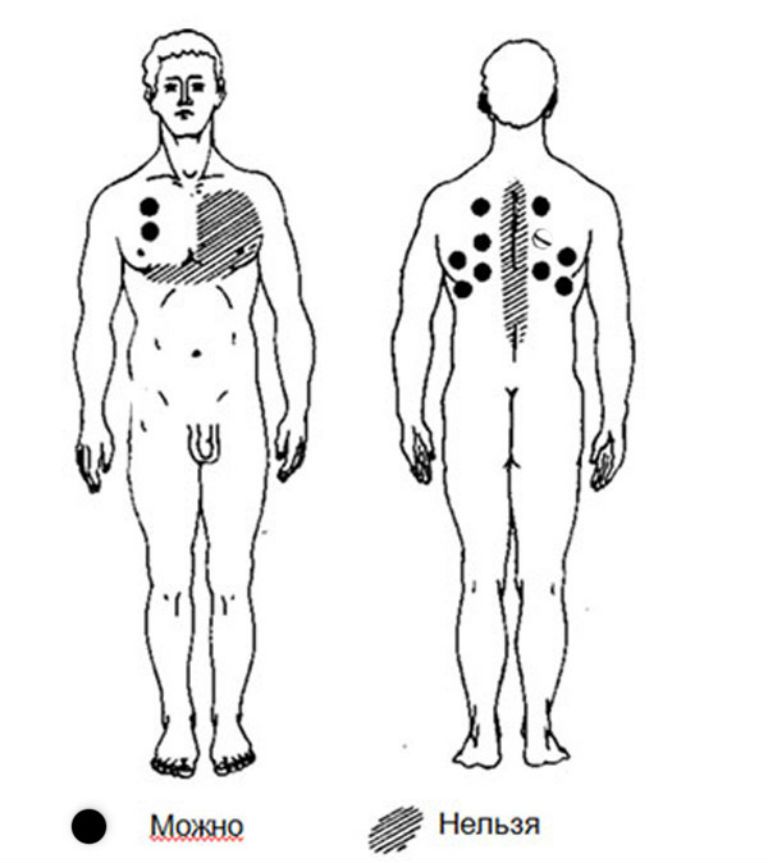
Кроме этого создание вакуума позволяет снять отечность и уменьшить давление на нервные окончания. При нагретом воздухе банка быстро присоединяется к поверхности тела, происходит всасывание кожного покрова внутрь. Это способствует снятию мышечного спазма и нормализации лимфооттока.
Польза и вред
Благодаря комплексному воздействию массаж обладает следующими полезными свойствами:
- за счет улучшения оттока и притока крови улучшается питание мышечных волокон, межпозвоночных дисков, нервных окончаний, тем самым снижая проявление остеохондроза и предотвращая дальнейшее развитие;
- уменьшается давление на нервные окончания, которое распространяется на весь позвоночный столб;
- нормализуется тонус мышц, а благодаря их расслаблению, исчезают болевые ощущения;
- под действием вакуума возникает местное раздражение рецепторов кожного покрова, что позволяет организму вырабатывать активные вещества, способствующие выведению вредных веществ и токсинов из организма;
- при курсовом назначении массажа мышцы, поддерживающие позвоночный столб, укрепляются и становятся более эластичными;
- применение банок помогает справиться со стрессом, так как обладает хорошим релаксирующим эффектом. Кроме этого подобное воздействие на организм способствует выработке эндорфинов и улучшает настроение.Применение массажа в период обострения заболевания может нанести вред организму и усилить болевые ощущения.
Применение массажа в период обострения заболевания может нанести вред организму и усилить болевые ощущения.
- Негативные эффекты также могут возникнуть при повышенной температуре тела пациента.
- Возможно появление синяков, которые исчезают через несколько дней.
Показания
- болевые ощущения в области позвоночника, которые носят постоянный характер и усиливаются при длительном нахождении в сидячем или стоячем положении;
- искривление позвоночника;
- прострелы, которые возникают при резких поворотах;
- слабость в конечностях;
- остеохондроз позвоночного столба в фазе ремиссии;
- миозиты;
- радикулит;
- нарушение кровообращения, вызванное шейным остеохондрозом.

Противопоказания
Вакуумный массаж комплексно воздействует на весь организм, поэтому существуют некоторые ограничения в применении:
- при беременности;
- при повреждении кожного покрова на месте установки банок;
- при патологиях сердца и сосудов;
- при отклонениях в работе ЦНС;
- при активных формах инфекционных заболеваний, туберкулез.
- ·Кроме этого необходимо соблюдать осторожность пациентам с низким и высоким давлением, а также при общем недомогании.
Виды баночного массажа
Существуют 2 основных вида баночного массажа: статический и динамический.
Статический вакуумный массаж
Банки устанавливают на грудной отдел, область поясницы (с обеих сторон от позвоночника) вдоль седалищного нерва, на конечностях. Во время процедуры пациент может находиться в положении лежа или сидя, полностью расслаблен. Сеанс длиться 8-14 минут.
Динамический вакуумный массаж
Динамическая терапия значительно отличается от статической методикой и временем сеанса. Для начала массажист разогревает тело, используя различные массажные кремы и масла. После этого устанавливаю банку стандартным методом. Специалист производит массирующие движения по току лимфатических сосудов или против него. Сеанс длится не более 5-6 минут.
· На завершающем этапе банку снимают и накрывают пациента теплым одеялом, оставляют отдыхать несколько минут.
Профилактика
Баночный массаж применяют не только для лечения, но и для профилактики различных заболеваний. Благодаря ему повышается иммунитет, расслабляются мышца, восстанавливается деятельность клеток, нормализуется давление, замедляется развитие различных заболеваний позвоночника, в том числе и остеохондроз. Профилактический курс массажа также определяется лечащим врачом.
·Для достижения лечебного эффекта необходимо соблюдать все требования к проведению баночного массажа, не пропускать сеансы и вовремя обращаться за помощью.
Массажные банки и остеохондроз: польза и эффективность
Как баночный массаж помогает справиться с болями и ограничению движений при остеохондрозе.
Одним из наиболее эффективных средств, в профилактике и избавлении от симптомов остеохондроза, является массаж вакуумными банками. И прежде чем мы перейдем к рассмотрению данного вида массажа уделим внимание самой проблеме – что же такое остеохондроз?
Остеохондроз: причины, протекание заболевания и последствия
Остеохондроз представляет собой комплекс дистрофических изменений хрящевой ткани. Поражает в основном межпозвоночные диски, а так же может поражать практически любой сустав. При заболевании происходит недостаточное питание хрящевой ткани, что приводит к её дистрофии. Дистрофия межпозвоночных дисков, потеря их эластичности и упругости приводит к целому ряду симптомов: боли различной локализации, онемения, снижения тонуса мышц.
Широкий диапазон локализации болей связан с возможностью защемления нервных корешков располагаемых в области межпозвоночных дисков. Эти корешки иннервируют деятельность отдельных органов и конечностей. Так, например, при шейном остеохондрозе (при защемлении нервных корешков) могут наблюдаться головные боли, боли в верхних конечностях. При остеохондрозе грудного отдела позвоночника боли в груди и области сердца. При пояснично-крестцовом остеохондрозе боли в нижних конечностях и области поясницы.
Остеохондроз как «награда» человеку за прямохождение
Причины возникновения заболевания до конца не изучены. По некоторым убеждениям остеохондроз является «наградой» человеку за прямохождение. Вследствие прямохождения возросла нагрузка на позвоночный столб человека. Межпозвоночные диски в таком положении подвергаются значительным нагрузкам. Осложняет ситуацию в современном мире гиподинамия и принятие долгих неестественных для человеческого опорно-двигательного аппарата положений, самое опасное из которых – сидячее. В неестественном положении нагрузка на позвоночник возрастает, вследствие чего околопозвоночные мышцы находятся в постоянном напряжении и не успевают восстанавливаться. Происходит спазмирование мышц и, тем самым, сжатие кровеносных сосудов питающих околопозвоночные ткани и межпозвоночные диски. Ткани не получают достаточного количества питательных веществ и подвергаются дистрофии. Неправильное питание с малым количеством питательных микроэлементов усугубляет положение. Неадекватные нагрузки в столь пагубных условиях могут приводить к травматизации мышц, которые составляют корсет позвоночника. Таким образом, возникают воспалительные процессы, которые могут переходить в хроническую форму в условиях недостаточного питания тканей. Получается замкнутый круг – гиподинамия, неестественные нагрузки и неправильное питание привели к пагубному состоянию позвоночника – нагрузки, которыми мы можем предпринять для спасения от гиподинамии, могут усугубить ситуацию.
В неестественном положении нагрузка на позвоночник возрастает, вследствие чего околопозвоночные мышцы находятся в постоянном напряжении и не успевают восстанавливаться. Происходит спазмирование мышц и, тем самым, сжатие кровеносных сосудов питающих околопозвоночные ткани и межпозвоночные диски. Ткани не получают достаточного количества питательных веществ и подвергаются дистрофии. Неправильное питание с малым количеством питательных микроэлементов усугубляет положение. Неадекватные нагрузки в столь пагубных условиях могут приводить к травматизации мышц, которые составляют корсет позвоночника. Таким образом, возникают воспалительные процессы, которые могут переходить в хроническую форму в условиях недостаточного питания тканей. Получается замкнутый круг – гиподинамия, неестественные нагрузки и неправильное питание привели к пагубному состоянию позвоночника – нагрузки, которыми мы можем предпринять для спасения от гиподинамии, могут усугубить ситуацию.
Что же делать?
Необходимо восстановить питание подвергшихся голоданию тканей и снять накопившееся напряжение с мышечного корсета позвоночника. В этом нам и помогут вакуумные массажные банки. Но важно помнить, что после курса баночного массажа вам необходимо изменить ваши пищевые привычки и заняться спортом, больше двигаться. Иначе вы рискуете возвращению этого болезненного состояния.
Массажные банки при остеохондрозе: польза и эффективность
При проведении баночного массажа происходит насыщение тканей питательными веществами, усиливается кровоток, стимулируется отток лимфы, а так же расслабляются спазмированные мышцы. Рассмотрим подробнее.
Польза баночного массажа при остеохондрозе:
- Усиление кровотока до стойкой гиперемии. Как мы рассмотрели выше, одной из главных причин недостаточного питания тканей, является сужение кровеносных сосудов и капилляров при спазмации мышц. Под воздействием баночного массажа происходит усиление притока крови вплоть до капиллярного.
 Это можно наблюдать в виде покраснения кожи.
Это можно наблюдать в виде покраснения кожи. - Расслабление спазмированных мышц. Кроме усиления питания тканей непосредственно во время сеанса баночный массаж способствует снятию мышечных спазмов, которые являются причиной недостаточного питания тканей. А так же снятие болей связанных со спазмами.
- Стимуляция оттока лимфы. Ещё один полезный эффект от вакуумного воздействия. Вместе с лимфой из тканей выводятся продукты обмена и различные токсины. Это приводит к ускорению процессов восстановления при воспалении.
Если обобщить, то вся польза баночного массажа сводиться к тому что бы улучшить межклеточный метаболизм тканей. Стимулировать как насыщение питательными веществами, так и выведение продуктов распада и токсинов из организма. Всё это приводить к восстановлению дистрофических тканей, и тем самым устранению различных болей и ограничений в движениях при остеохондрозе.
Где купить массажные банки?
Вы можете купить медицинские вакуумные массажные банки на нашем сайте в разделе «Массажеры»
Вконтакте
Google+
Лечим остеохондроз банками
Волнует вопрос лечения остеохондроза. И еще один вопрос: идет процесс фиброзирования легочной ткани после пневмонии, как с помощью тибетской медицины можно убрать эти проблемы?
Анна Колчина, Москва
Евгения Горяева, врач клиники Тибетской медицины «Наран», Москва:
– В официальной медицине человека поделили между специалистами. И гинеколог, к примеру, не хочет знать, что у пациента есть проблемы с пищеварением или со зрением. Это привело к тому, что такая медицина не видит общих закономерностей в развитии болезней, устраняет следствия, не искореняя причину. А ведь наш организм способен как самостоятельно восстанавливаться, так и разрушаться.
Последствия проблем с позвоночником проявляются на трех уровнях.
Первый уровень – корешковый (болевой): из-за защемления нервных корешков в позвоночнике могут возникнуть боли и спазмы в мышцах спины, шеи, головы, в руках и ногах.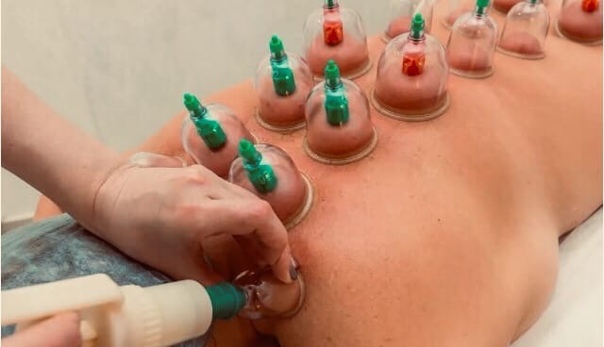
Второй уровень – висцеральный: проблемы, связанные с позвоночником, передаются практически во все внутренние органы, а также органы чувств, получающие через позвоночник команды от головного мозга.
Третий уровень – сосудистый: ощущение мурашек в руках и ногах, быстрый переход то в жар, то в холод. То есть неполадки с позвоночником могут влиять на функционирование сосудистой системы.
У читательницы возникли проблемы на двух уровнях – болевом и висцеральном, что и привело к склерозированию легочной ткани, возможно, после перенесенного воспаления легких. На этом же уровне из-за проблем в грудном отделе позвоночника могут возникнуть еще и сердечные недомогания – сердцебиения, боли в сердце.
Официальная медицина считает, что остеохондроз – дистрофические изменения в позвонках. Но чтобы они появились, нужно сильно постараться. В молодые годы первыми звоночками остеохондроза могут быть вегетососудистая дистония и нейроциркуляторная дистония. Это не что иное, как выход проблем с позвоночником на сосудистый уровень.
Симптомы – головокружение, сердцебиение, потливость, головная боль, боль в шее, то есть, казалось бы, легкие, несерьезные. В лучшем случае врач выпишет кавинтон, аминалон или ноотропил – сосудистые препараты. Но ведь дело не только в сосудах, но и в позвоночнике. Игнорирование этого факта запускает дальнейший механизм развития болезни.
Как решить эту проблему?
Первое: максимально уравновесить свое психологическое состояние. От этого, как ни странно, зависит состояние мышц спины, а следовательно, и позвоночника. Я видела много тибетских монахов, которые, находясь в солидном возрасте, имея даже полноватое строение тела, сохраняли гибкость позвоночника.
Второе: надо помнить, что в основе нарушения обменных процессов лежит мышечный спазм, поэтому стоит обратиться к массажу спины./59a6afe66e7eca8.ru.s.siteapi.org/img/4f89025a2781238bff9de42d7a8ed6c1be4b7773.jpg) При этом делать его следует по всей длине позвоночника, а не только на отдельной его части, например шейной. Обязательно надо хорошо промассировать ягодицы, поясничную область, затем пройтись по грудному отделу и закончить шейным.
При этом делать его следует по всей длине позвоночника, а не только на отдельной его части, например шейной. Обязательно надо хорошо промассировать ягодицы, поясничную область, затем пройтись по грудному отделу и закончить шейным.
Хороши растяжки, висы на турнике, но делать их надо после разогрева мышц спины при помощи массажа или аппликатора Кузнецова.
Можно поставить банки на спину – по всей длине позвоночного столба, симметрично с обеих сторон, 8–10 банок. Делают через день 7, 9 или 11 раз. Курс – раз в квартал.
Хорош и баночный массаж. Больному следует, раздевшись до пояса, лечь на живот. Желательно, чтобы поверхность была относительно твердой. Кстати, и спать на мягком ложе при остеохондрозе не рекомендуется. Обильно натираем спину подогретым растительным маслом. Делаем легкий массаж – похлопывания, затем пощипывания и, наконец, надавливания костяшками пальцев. Идем сверху вниз. Затем берем медицинскую банку (подойдет и небольшая майонезная), смазываем ее спиртом, поджигаем и тут же прикладываем горлышком к спине. Банка мгновенно «присосется» к коже. Начинаем «возить» ею по всей поверхности спины вверх-вниз – от шеи до ягодиц. Периодичность – та же, как для банок. Баночный массаж будет способствовать длительной молодости, поскольку чем гибче позвоночник, тем длиннее жизнь.
Остеохондроз. 7 простых правил, которые помогут вам сохранить спину здоровой
Заведующий нейрохирургическим отделением № 3 Краснодарской краевой клинической больницы № 1 Игорь Басанкин дает советы, которые пригодятся большинству.
Остеохондроз – очень распространенная патология, которая сопровождается болевыми ощущениями и приносит серьезный дискомфорт. Лечение этой болезни далеко не всегда помогает полностью избавиться от ее проявлений, поэтому профилактика здесь особенно актуальна.
Что приводит к остеохондрозу
Игорь Басанкин
Внутренние причины: нарушения внутриутробного формирования позвоночника, генетическая предрасположенность, метаболические нарушения, гормональные патологии, избыточный вес, возрастные изменения.
Внешняя причина, по большому счету, одна – неправильные нагрузки на позвоночник.
В этой ситуации в местах избыточного давления происходит изменение структуры хрящевой ткани.
Это случается при сидячем образе жизни; травматических повреждениях спины; сколиозе, кифозе и прочих патологиях спины; постоянное ношение тяжестей, плоскостопие; некачественная подушка либо матрас, вредные привычки – чрезмерное употребление спиртного, курение.
Как распознать болезнь
Периодическая или постоянная боль в спинной области, шее, онемение конечностей или постоянное напряжение спинных мышц. Стреляющие боли в спине, груди или пояснице. Боль при поднятии рук вверх. Боль при наклоне или повороте головы, головокружения, тянущие боли в руке и/или ноге. Шум в ушах. Неожиданные приступы тошноты.
7 способов облегчить себе жизнь
Важно: Чтобы все перечисленные ниже действия приносили результат, они должны носить комплексный характер
Научитесь держать прямую осанку. Идеальная осанка – это такое положение тела, когда голова находится со спиной на одной линии. Голова – высоко поднята, плечи – расправлены, грудь – приподнята, живот – втянут. Походка должна была ровной и пружинистой. Проявите дисциплину, добейтесь идеальных результатов.
Организуйте свое рабочее место. Многие пренебрегают этим очевидным советом, но зря. Ведь состояние мышц шеи и плечевого пояса оказывает непосредственное влияние на позвоночник. Профилактика шейного остеохондроза невозможна, если плечи за рабочим столом все время напряжены.
Кресло должно быть оснащено комфортной спинкой и подлокотниками. Важно, чтобы клавиатура находилась ниже локтей, угол между предплечьем и плечом – около 120 градусов. Монитор следует расположить так, чтобы глаза смотрели в его верхний край.
Во время работы за компьютером держите спину выпрямленной. Каждые 40–50 минут старайтесь делать перерыв, чтобы пройтись и немного размяться. Лучше всего сделать специальную гимнастику, так как во время длительного пребывания в одном положении нередко отекает шея.
Каждые 40–50 минут старайтесь делать перерыв, чтобы пройтись и немного размяться. Лучше всего сделать специальную гимнастику, так как во время длительного пребывания в одном положении нередко отекает шея.
Правильная посадка за рулем. Автомобилисты часто настраивают водительское кресло не так, как рекомендуется, а так, как им хочется. Через некоторое время они начинают жаловаться на остеохондроз. Поэтому отрегулируйте спинку кресла так, чтобы не только плечи касались его, а вся поясница полностью. Она должна прижиматься к сиденью, а не быть на весу. Спинку сиденья не наклоняйте сильно назад, а фиксируйте в вертикальном положении. Пользуйтесь специальными поясничными подушками, созданными для водительских сидений.
Во время поездки подбородок держите немного поднятым. Следите за коленями: они должны быть выше бедер. Каждые 1,5–2 часа старайтесь делать остановку: выходите из машины и делайте несколько упражнений для поясницы. Так вы вернете тонус спинным мышцам.
Рациональное питание. Несбалансированный рацион является одним из важнейших факторов развития остеохондроза. Поэтому в целях профилактики избегайте сладостей, соленых блюд, белого хлеба, жирной пищи. Особая опасность – это белый рафинированный сахар, именно он вымывает из костей кальций.
Ешьте продукты, богатые витаминами С, Е, В3 (РР): овощи, фрукты, морепродукты, рыбу, бобовые, орехи, мясо курицы, яйца. Они обеспечат высокую эластичность вашей хрящевой ткани. Не забывайте про нежирные кисломолочные продукты – кефир, йогурт, творог. Принимайте витаминные комплексы. Избавляйтесь от лишнего веса.
Физическая активность. Лечебная физкультура (ЛФК) – отличное средство для профилактики остеохондроза. С ее помощью вы укрепите свой мышечный корсет и связочный аппарат. Все упражнения, входящие в комплекс ЛФК, – физиологичны: в ходе их выполнения мышцы не переутомляются.
Настоятельно рекомендуется плавание – вода помогает расслабить мышцы и увеличить амплитуду движений суставов.
Еще один действенный метод – оздоровительная скандинавская ходьба. Во время таких прогулок задействуются основные мышечные группы, увеличивается расход энергии, улучшается функционирование органов дыхания и сердца.
Массаж. Он повысит тонус ваших мышц и устранит чрезмерное мышечное напряжение. Особенно массаж важен в профилактике грудного остеохондроза. Обычно эту процедуру выполняют курсами. Также научитесь самомассажу и выполняйте его ежедневно 10–15 минут.
Правильный сон. На протяжении всего дня на межпозвоночные диски приходится нагрузка всего тела. Только в ночное время удается полностью расслабиться и принять свободное положение. Именно поэтому профилактика остеохондроза позвоночника заключается в организации правильного режима сна.
Основание кровати должно быть ровным и жестким. Старайтесь не спать в гамаках, на раскладушках или надувных матрасах.
Матрас должен иметь хорошую эластичность и среднюю степень жесткости. Благодаря этому удастся сохранить физиологические изгибы позвоночника в естественном положении. Хорошее решение – пробрести ортопедический матрас: он позволит максимально расслаблять мышцы всего тела и снижать степень раздражения нервных волокон.
Пусть ваша подушка будет небольшого размера, прямоугольной формы и умеренной жесткости. Ортопедические подушки помогут устранить болевые ощущения в районе шеи и послужат отличным средством профилактики шейного остеохондроза.
При остеохондрозе позвоночника. Большой атлас целительных точек. Китайская медицина на страже здоровья и долголетия
При остеохондрозе позвоночника
При поясничном и грудном остеохондрозе стеклянные банки статично помещаем на расстоянии 4 пальцев слева и справа от позвоночника, по всей спине (рис.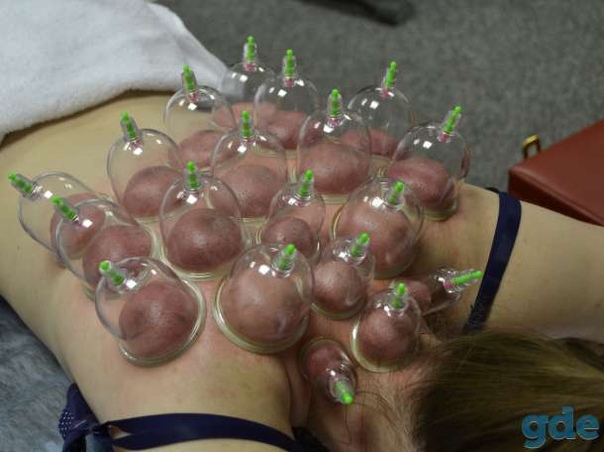 6.5, а). Оставляем их на 10 минут, после чего снимаем и основательно растираем спину массируемого.
6.5, а). Оставляем их на 10 минут, после чего снимаем и основательно растираем спину массируемого.
Рис. 6.5, а, б. Зоны при остеохондрозе позвоночника
Для вакуум-массажа воспользуемся резиновыми и пластиковыми вакуум-банками (фото 6.3). Устанавливаем банку слева или справа от позвоночного столба и двигаем ее вниз, стараясь образовать впереди банки складку кожи. Складка кожи во время массажа все время должна «бежать» впереди банки. Не давите на банку, скольжение должно сбыть мягким.
Фото 6.3. Пластиковая вакуум-банка
Чтобы облегчить остеохондроз шейного отдела позвоночника, надо установить массажную резиновую банку поблизости от 7-го шейного позвонка (рис. 6.5, б). И выполнять круговой массаж вокруг позвонка по часовой стрелке. Надавливать на область позвонка нельзя, не забывайте об этом! Использовать стеклянные банки при шейном остеохондрозе тоже нельзя!
Вакуум-массаж вызовет умеренное покраснение кожи, может дать чувство легкой болезненности или жжения. Это нормальные реакции, их не надо бояться. Сеансы динамичного вакуум-массажа можно повторять каждый день. Статичные стеклянные банки устанавливаем 1 раз в 2–3 суток. Частота зависит от индивидуальных реакций кожи, чем бледнее «синяки» и меньше болезненность после сеанса, тем выше частота. Однако каждые сутки можно устанавливать банки можно не раньше, чем после четвертого сеанса.
Вакуум-массаж для снятия зажима поясницы
Молодым людям поясничные боли практически незнакомы, даже если в сидячем положении приходится проводить много часов за день. Но с возрастом происходят изменения в хрящевой ткани позвоночника, и возникают болезненные зажимы именно в этой области. С помощью рефлексотерапии мы можем изменить жесткое состояние тканей в напряженных точках на «размягченное», не прибегая к опасным гимнастическим и массажным движениям в хрящевой ткани. Вакуум-терапия снимает спазмы и деформации мышц, нервная система успокаивается, и многие процессы в организме приходят в норму.
Работаем следующим образом.
Устанавливаем банки статично или производим вакуум-массаж на расстоянии 4 пальцев слева и справа от позвоночного столба (в районе поясничного и крестцового отделов, см. рис. 6.6) и на ягодичных мышцах.
Рис. 6.6. При зажиме поясницы
При поясничном радикулите для терапии используются эти же зоны.
Смещение межпозвоночных дисков
Если в результате падения и ушиба спины, поднятия чрезмерной тяжести или резкого неестественного поворота корпуса больному поставили диагноз «смещение межпозвоночных дисков», методом вакуум-массажа можно ускорить выздоровление.
1. Укладываем больного на живот. Уточняем локализацию болевого синдрома. При травме, связанной с поднятием тяжести и резком повороте, это чаще всего 4 и 5 поясничные позвонки (но в данном случае это лишь пример, а в конкретной ситуации мы опираемся на диагноз травматолога). Остается только уточнить, в какую сторону от позвоночника распространяется боль: вправо или влево.
Локализация травмы определяется травматологом на основании снимков! Мы помогаем больному ускорить выздоровление при определенном диагнозе, а не ставим собственный диагноз!
2. Сначала мягко массируем напряженную болезненную мышцу около позвонка, чтобы разогреть ее и увеличить подвижность и проводимость мышечной ткани (рис. 6.7, а). Затем воздействуем вакуум-банками на напряженные мышцы слева или справа от позвонков. Время воздействия вакуум-массажем до 15 минут.
3. Пациент переворачивается на спину. Проводим кинетический вакуум-массаж последовательно по всем точкам. Общее время воздействия не более 10 минут для всех точек надчревной области, живота и лобковой зоны.
4. Осторожно пощупайте область пупка. С болезненной стороны (то есть с той стороны, которая проецируется на болезненную область спины) надавите пальцами сбоку от пупка. Оцените реакцию больного на нажатие на расстоянии 1–3 пальца от пупка. Если наблюдается иррадиация боли в поясничную область, поставьте стеклянную банку на указанную зону на 5 минут.
Рис. 6.7, а, б. Вакуум-помощь при смещении дисков
После окончания процедуры больной должен некоторое время полежать неподвижно (10–15 минут). Повторите сеанс через 2 суток. Всего проделайте не менее 7 сеансов, все это время повороты и наклоны спины противопоказаны!
Данный текст является ознакомительным фрагментом.
Продолжение на ЛитРесРассекающий остеохондрит: диагноз, который нельзя пропустить
АЛЛЕН Л. ХИКСОН, доктор медицины, и ЛИЗА М. ГИББС, доктор медицины, Калифорнийский университет, Дэвис, Медицинская школа, Сакраменто, Калифорния
Am Fam Physician. 2000, 1 января; 61 (1): 151-156.
См. Соответствующий информационный бюллетень для пациентов о рассекающем остеохондрите, написанный авторами этой статьи.
Рассекающий остеохондрит — наиболее частая причина дряблости суставной щели у пациентов подросткового возраста.Поскольку клинические данные часто неуловимы, для постановки диагноза требуется высокий показатель подозрительности. Ограниченный диапазон движений может быть единственным заметным клиническим признаком. Диагноз ставится на основании рентгенологического исследования, а магнитно-резонансная томография играет ключевую роль в определении стабильности поражения. Консервативное лечение — основа лечения стабильных поражений. В то время как большинство пациентов поддаются консервативному лечению, пациентам с нестабильными поражениями требуется артроскопическое лечение.
Оценка боли в коленях у подростков представляет собой сложную задачу для врачей первичного звена.Рассекающий остеохондрит (ОКР) является наиболее частой причиной расшатывания суставной щели у подростков1 и может привести к значительной слабости. ОКР — относительно редкое заболевание, характеризующееся некрозом фокальной области субхондральной кости. Исторически это наблюдалось преимущественно у молодых мужчин. В последнее время об этом все чаще сообщается среди молодых спортсменок2. Клинические данные могут быть незаметными, поэтому врачи должны иметь низкий порог подозрения для получения рентгенограмм.Ранняя диагностика и соответствующее лечение могут предотвратить долгосрочные последствия.
Иллюстративный случай
15-летняя девочка обратилась в нашу клинику через неделю после случайного столкновения с раздвижной стеклянной дверью. Она жаловалась на боли в коленях, которые усиливались при переносе веса и разгибании ног. Незначительная опухоль на плато большеберцовой кости, вызванная инцидентом, была стойкой. Хотя нога пациентки никогда не «сдавалась», она чувствовала, что это могло произойти. У нее ранее не было проблем с коленями.В подростковом возрасте она увлекалась баскетболом и футболом, хотя при дальнейших допросах она призналась, что в течение нескольких месяцев у нее наблюдались нечеткие боли в коленях, которые не позволяли ей играть так энергично, как она хотела. Других совместных жалоб у нее не было. Менструации у пациентки были регулярными и начались в 12 лет. В ее семейном анамнезе были отрицательные ревматологические заболевания.
При осмотре были обнаружены отек мягких тканей и болезненность линии суставов. Обследование дало отрицательный результат на подколенный выпот или болезненность.Проба Лахмана была отрицательной, медиальные и боковые коллатеральные связки были стабильными. При неврологическом обследовании выявлены симметричные рефлексы с нормальной чувствительностью и силой. У нее был дискомфорт при нагрузке и ограничении полного разгибания на 5 градусов. Рентгенограммы были получены после выявления ограничения расширения.
На рентгенограммах правого колена обнаружен костный фрагмент в медиальном мыщелке бедренной кости (рис. 1). Магнитно-резонансная томография (МРТ) правого колена была проведена для оценки разрыва хондры.Сканирование выявило остеонекроз, затрагивающий латеральную сторону медиального мыщелка бедренной кости (рис. 2). Хрящ, покрывающий область некроза, был цел, а суставная щель была очищена от рыхлых тел. Вид другого колена был получен для исключения контралатерального поражения и был нормальным.
Просмотр / печать Рисунок
РИСУНОК 1.
Переднезадняя (слева) и боковая (справа) рентгенограммы, показывающие рассекающий остеохондрит поражение (стрелки) латеральной стороны медиального мыщелка бедренной кости.
РИСУНОК 1.
Переднезадние (слева) и боковые (справа) рентгенограммы, показывающие рассекающий остеохондрит поражение (стрелки) латеральной части медиального мыщелка бедренной кости.
Просмотр / печать Рисунок
РИСУНОК 2.
(слева) T 2 -взвешенное МРТ, показывающее поражение (стрелка) размером 1,0 × 0,5 см со сниженной интенсивностью сигнала, соответствующей некрозу кости. (справа) T 2 -взвешенное сканирование, демонстрирующее край костного отека (стрелка), окружающий поражение.
РИСУНОК 2.
(слева) T 2 -взвешенное МРТ, показывающее поражение (стрелка) размером 1,0 × 0,5 см со сниженной интенсивностью сигнала, соответствующей некротизированной кости. (справа) T 2 -взвешенное сканирование, демонстрирующее край костного отека (стрелка), окружающий поражение.
Пациент был впоследствии направлен на осмотр врачом-ортопедом, который согласился с диагнозом. Клинически пациентка не смогла полностью вытянуть правую ногу.Ей сделали артроскопию для выявления нестабильных некротических фрагментов. При обследовании под наркозом выявлена блокада разгибания правого колена на 5 градусов. Артроскопия выявила костно-хрящевое поражение размером 1,0 × 0,5 см, соответствующее рентгенологическим данным медиального мыщелка бедренной кости. На краю костно-хрящевого дефекта был отмечен рыхлый хрящ, который был обработан на этом участке. Признаков обнаженной кости не обнаружено. Само поражение было признано стабильным после механического зондирования, дальнейшие процедуры не выполнялись.
Пациент был направлен на физиотерапию и прошел три сеанса для увеличения объема движений и укрепления квадрицепса. Ее попросили воздержаться от соревновательных видов спорта. Пациентка была потеряна для наблюдения в течение девяти месяцев, после чего ее снова осмотрели в семейной клинике. Она была безболезненной, с полным диапазоном движений и стабильным коленом. Она полностью занималась школьными видами спорта и не имела никаких дополнительных симптомов.
Определение и патология
ОКР относится к фокальной области субхондральной кости, которая подвергается некрозу.Вышележащий хрящ остается неповрежденным в различной степени, питаясь синовиальной жидкостью. Когда некротизированная кость рассасывается, хрящ теряет свою опорную структуру2. Впоследствии костный фрагмент может сместиться в суставную щель. Существует два основных типа ОКР: взрослая форма, которая возникает после закрытия физики, и ювенильная форма, которая возникает у пациентов с открытой эпифизарной пластинкой.3 Многие исследователи считают, что взрослая форма — это недиагностированное стойкое ювенильное ОКР.4
Эпидемиология
Заболеваемость ОКР среди населения в целом оценивается от 15 до 30 случаев на 100 000 человек.1,5 Хотя это и редко, оно считается важной причиной боли в суставах у активных подростков. Известно, что ОКР обычно поражает мужчин в возрасте от 10 до 20 лет. В одном исследовании было отмечено, что у мальчиков в три-четыре раза больше шансов заболеть, чем у девочек3. По всей видимости, заболеваемость увеличивается среди женщин2 и детей младшего возраста 1, возможно, из-за более активного участия в организованных видах спорта.
Наиболее часто поражаются области, в порядке убывания частоты, мыщелки бедренной кости, купол таранной кости и головная часть плечевой кости.6 Колено поражено примерно в 75% случаев.3 Классически медиальная часть бедра, не несущая нагрузки. Мыщелок является локализацией в 85 процентах случаев ОКР коленного сустава.7 ОКР следует исключить в контралатеральном суставе, потому что в 20-30 процентах случаев это двустороннее поражение.3 Множественные поражения, хотя и редкие, иногда отмечались8 Меньше частые локализации включают коленную чашечку, головку бедренной кости, суставной диск лопатки, большеберцовое плато, головку таранной кости и позвонки.8,9 Головные поражения плечевой кости часто встречаются у бейсбольных питчеров и гимнастов-подростков. 9,10
Патофизиология
Наше понимание патофизиологии ОКР не сильно продвинулось за последние 100 лет. Генетическая предрасположенность, ишемия, повторяющиеся травмы и аномальная оссификация — все это теоретизировалось как причины ОКР. Хотя этиология остается неясной, обычно считается, что она многофакторная, с повторяющимися усилиями сдвига и сжатия, играющими подстрекательскую роль.
Многие пациенты не имели в анамнезе серьезных травм, но скорее повторяющиеся микротравмы приводят к стрессу субхондральной кости, особенно у спортсменов.1 При ОКР коленного сустава поражение или соударение большеберцовой кости и надколенника на фрагментах мыщелка бедренной кости было вовлечены.1 Из-за высокой частоты поражений двусторонних и ненагруженных участков нетравматическая этиология может быть более вероятной. Ишемия, вызванная спазмом сосудов, жировой эмболой, инфекцией или тромбозом, может иметь значение.1,3
Педиатрические пациенты могут иметь более высокую вероятность травм с менее серьезной травмой, связанной с пластинами роста, более пористой костью и восприимчивостью к травмам во время всплесков роста у подростков.11 Аномальные центры окостенения, часто встречающиеся у детей в периоды быстрого роста, имеют были вовлечены в качестве предшественников к развитию поражений ОКР.1 Предполагается, что дополнительный костный островок частично восстанавливается со временем. Генетическая предрасположенность — менее вероятный фактор, хотя наследственные заболевания костей могут быть ошибочно приняты за ОКР.3
Клиническая презентация
Пациенты обычно в возрасте от 12 до 20 лет активно занимаются гимнастикой, бейсболом или другими организованными видами спорта. Жалобы часто включают легкий и неопределенный дискомфорт в коленях. Фактически, незначительное ограничение диапазона движений может быть наиболее важным клиническим признаком. Примерно 21 процент пациентов связывают появление симптомов с травмой5. У большинства из них боль связана с активностью5 и скованностью после периодов простоя. Общие жалобы включают ощущение «схватывания» и «уступки» 4, а также невозможность полностью разогнуть конечность.Постоянная или периодическая боль слабого уровня, как правило, плохо локализуется и усиливается с нагрузкой.4 При осмотре могут присутствовать выпоты, крепитация2 и болезненность линии суставов. Пациенты с ОКР коленного сустава могут ходить с внешней ротацией большеберцовой кости, и признак Вильсона может быть положительным.1 Последний вызывается сгибанием колена на 90 градусов, внутренним вращением большеберцовой кости и медленным разгибанием колена, наблюдая за болезненной реакцией. 3
Диагноз
ОКР — это радиологический диагноз.При подозрении на ОКР коленного сустава показаны переднезадние, боковые и туннельные рентгенограммы (колено в сгибании). Одни только переднезадние снимки могут пропустить поражение на задней поверхности медиального мыщелка бедренной кости.1 Если поражение отмечено, следует также обследовать контралатеральное колено. Простые пленки обнаруживают ограниченную область некроза, но являются плохим методом оценки суставного хряща и не могут использоваться для определения стабильности.6 Если обычные рентгенограммы отрицательны, следует рассмотреть другую этиологию и не рекомендовать дальнейшее обследование на ОКР.
Все очаги ОКР, видимые на рентгенограммах, для стабильности необходимо стадировать с помощью МРТ. МРТ имеет 97-процентную чувствительность для обнаружения нестабильных поражений.12 За исключением прямой визуализации, МРТ является наиболее точным методом определения стадии поражений и имеет решающее значение для клинического лечения.13 Стадии I и II представляют собой стабильные поражения, а стадии III и IV описывают нестабильные поражения. при котором не только хрящ поврежден, но и существует синовиальная жидкость между фрагментом и подлежащей костью (Таблица 1).
Просмотр / печать таблицы
ТАБЛИЦА 1Стадия МРТ суставов с рассекающим остеохондритом
Стадия I — утолщение суставного хряща и слабые изменения сигнала (стабильные) |
Хрящ 2-й стадии — разрывы суставов , ободок со слабым сигналом позади фрагмента, указывающий на прикрепление фиброза (стабильный) |
Стадия III — разрыв суставного хряща, высокосигнальные изменения позади фрагмента и подлежащей субхондральной кости (нестабильны) |
Стадия IV — свободное тело (нестабильный) |
Стадия МРТ суставов с рассекающим остеохондритом
Стадия I — утолщение суставного хряща и слабые изменения сигнала (стабильные) |
Нижний суставной хрящ — II стадия -сигнальный ободок за фрагментом, указывающий на прикрепление фиброза (стабильный) |
Стадия III — повреждение суставного хряща, высокосигнальные изменения за фрагментом и подлежащей субхондральной костью (нестабильно) |
Стадия IV — свободное тело (нестабильное) |
Томография, компьютерная томография, артрография и ядерное сканирование кости. также использовался для оценки стабильности и исцеляющего потенциала, но у каждого из них есть ограничения.6 На МРТ наличие изменений с высоким уровнем сигнала на изображениях T 2 означает наличие жидкости между фрагментом и неповрежденной костью. Вышележащий суставной хрящ может быть неповрежденным в нестабильном фрагменте.6 При планировании операции важно различать стадии II и III.13 Если МРТ демонстрирует нестабильное поражение (стадия III или IV), для определения целостности сустава следует использовать артроскопию. хрящевая поверхность.
Клиническое лечение
После определения стадии нестабильные поражения лечат хирургическим путем (рис. 3).Обычно принято консервативное лечение стабильных поражений. Однако не существует проспективных рандомизированных клинических исследований для оценки различных методов лечения4. В существующей литературе часто группируются исследования взрослых и ювенильных форм ОКР, а также различных пораженных суставов, что затрудняет выводы, основанные на доказательствах. Прогноз ухудшается с возрастом и закрытием физического тела. Таким образом, цель лечения подросткового ОКР состоит в том, чтобы способствовать разрешению поражения до закрытия физического состояния. Во взрослом виде терапия направлена на сохранение функции и предупреждение развития раннего дегенеративного остеоартроза.3
Просмотр / печать Рисунок
Лечение рассекающего остеохондрита коленного сустава
РИСУНОК 3.
Алгоритм для определения надлежащего лечения рассекающего остеохондрита коленного сустава. (ОКР = рассекающий остеохондрит; МРТ = магнитно-резонансная томография)
Ведение рассекающего остеохондрита коленного сустава
РИСУНОК 3.
Алгоритм для определения надлежащего лечения рассекающего остеохондрита коленного сустава.(ОКР = рассекающий остеохондрит; МРТ = магнитно-резонансная томография)
Следует учитывать такие факторы, как расположение поражения, отношение к несущей поверхности, стабильность, закрытие физического состояния и клинические проявления. Нехирургическое лечение показано в случаях ювенильного ОКР, особенно у пациентов с открытыми пластинками плода3. При консервативных мерах примерно половина поражений разрешается в течение 10–18 месяцев. Девочки моложе 11 лет и мальчики моложе 13 лет имеют отличные шансы на выздоровление, в то время как пациенты старше 20 лет, как правило, имеют худшие результаты, и вероятность того, что потребуется хирургическое вмешательство, увеличивается.1 Нестабильные поражения (стадии III и IV) у пациентов с закрытым физическим состоянием имеют особенно плохой прогноз. Пациентам старшего возраста с симптомами показано более агрессивное вмешательство3.
Нехирургическое лечение включает наблюдение. Соревновательных видов спорта следует избегать в течение шести-восьми недель. Целью модификации активности является обеспечение бессимптомной повседневной деятельности1. Может быть начата физиотерапия, включая упражнения на растяжку и диапазон движений. Также могут быть полезны упражнения на кондиционирование и укрепление четырехглавой мышцы.Исторически иммобилизация поощрялась; тем не менее, длительное наложение шины приводит к атрофии и ригидности четырехглавой мышцы, что может усложнить состояние.5 Постоянные симптомы у послушного, консервативно леченного пациента или начало защемления или скрежета сустава предполагают отслоение сустава с развитием рыхлого тела и являются показателем для артроскопической оценки.1
В этих случаях артроскопия является обязательной для оценки стабильности поражения и визуализации вышележащего хряща.В зависимости от результатов хирургического вмешательства может быть удалено свободное тело, иссечен фрагмент, удален хрящ или высверлено образование для реваскуляризации. После операции следует как можно раньше начинать упражнения на диапазон движений. Укрепление четырехглавой мышцы может способствовать общей стабильности колена. Пациентов следует наблюдать с трехмесячными интервалами с изучением истории болезни и физического обследования до исчезновения симптомов. Визуализирующие исследования показаны для оценки клинического ухудшения.
Лечение рассекающего остеохондрита в Луисвилле | Хирургия костной пластики KY
Рассекающий остеохондрит — это заболевание сустава, при котором кусок хряща вместе с тонким слоем кости отделяется от конца кости из-за недостаточного кровоснабжения.Разделенные фрагменты иногда называют «суставными мышами». Эти фрагменты могут быть локализованы или могут отделяться и падать в суставную щель, вызывая боль и нестабильность суставов.
Рассекающий остеохондрит может возникнуть в любом суставе, включая локти, лодыжки, плечи и бедра.
Рассекающий остеохондрит чаще встречается среди мальчиков и молодых людей в возрасте от 10 до 20 лет, активно занимающихся спортом. У спортсменов, занимающихся такими видами спорта, как гимнастика и бейсбол, может развиться рассекающий остеохондрит.
Точная причина рассекающего остеохондрита остается неизвестной, и считается, что определенные факторы, такие как травмы, переломы, растяжения или травмы сустава, увеличивают риск развития этого состояния. Рассекающий остеохондрит может быть вызван ограничением кровоснабжения конца пораженной кости, что обычно возникает в сочетании с повторяющейся травмой. После травмы или травмы кости в этой области могут быть лишены кровотока, что приведет к некрозу, и в конечном итоге фрагмент кости может отломиться.Это может инициировать процесс заживления, однако к этому времени суставной хрящ будет сдавлен, уплощен и разовьется субхондральная киста. Все эти изменения, помимо повышенного давления в суставах, вызывают нарушение заживления сустава.
Пациенты с рассекающим остеохондритом обычно имеют боль в локтевом суставе, отек, скованность и снижение диапазона движений. Боль обычно усиливается после активности.
Ваш врач, вероятно, назначит рентген правого и левого локтя, чтобы увидеть аномалию в суставной щели и сравнить их.Вы также можете пройти компьютерную томографию или магнитно-резонансную томографию, которая поможет определить расположение незакрепленных фрагментов в суставе.
Лечение
Ваш врач может порекомендовать различные методы лечения в зависимости от отчетов диагностического сканирования, возраста, степени тяжести, стабильности хряща и других факторов. Цели лечения — облегчить симптомы и остановить или замедлить прогрессирование дегенерации сустава. Консервативные подходы к лечению, такие как подход ожидания и наблюдения, обезболивающие и иммобилизация на 1-2 недели, рекомендуются, если состояние диагностируется на ранних стадиях и если степень тяжести легкая.Однако операция требуется, если заболевание диагностируется на поздней стадии или если состояние тяжелое.
Хирургическая коррекция рассекающего остеохондрита может проводиться как открытым способом, так и артроскопическими методами. Некоторые из хирургических процедур включают сверление, пересадку кости, внутреннюю фиксацию открытой репозиции, костно-хрящевую трансплантацию или имплантацию аутологичных хондроцитов (ACI).
- Сверление — В этом методе в кости просверливается несколько небольших отверстий, что позволяет разрастаться новым кровеносным сосудам в области дефекта.Это способствует притоку крови к области дефекта, тем самым инициируя реакцию заживления и образование новых хрящевых клеток внутри поражения
- Открытая репозиция с внутренней фиксацией — Открытая операция выполняется в тех случаях, когда дефектная область труднодоступна с помощью артроскопа. Следовательно, может потребоваться открытый разрез. При этой процедуре перед суставом делается разрез, чтобы хирург мог увидеть сустав, и удаляются незакрепленные тела. Внутренняя фиксация включает фиксацию отломков с помощью внутренних фиксаторов, таких как металлические винты, шпильки или проволока
- Костная пластика — помогает заполнить промежуток после удаления мертвой или некротизированной кости.В этой процедуре на поврежденный участок накладывается костный трансплантат. Эта процедура может быть выполнена для восстановления поврежденного участка или замены отсутствующей кости. Для роста новой кости может потребоваться аутотрансплантат (взятый у того же человека) или аллотрансплантат (взятый из костного банка)
- Костно-хрящевая пластика — Процедура включает перенос здоровых хрящевых пробок из ненесущих участков сустава и перенос на поврежденные участки сустава в виде мозаики.Это позволяет вновь имплантированной кости и хрящу расти в дефектной области. Трансплантаты могут быть взяты от одного и того же человека (аутотрансплантат) или от донора или костного банка (аллотрансплантат)
- Имплантация аутологичных хондроцитов (ACI) — В этой процедуре здоровые хрящевые клетки собираются из сустава, не несущего нагрузку, и культивируются в лаборатории. Пластырь из культивированной хрящевой ткани будет имплантирован в дефектную область, что также способствует росту нового хряща.
Рассекающий остеохондрит коленного сустава
Суставы. 2014 январь-март; 2 (1): 29–36.
Опубликовано онлайн 8 мая 2014 г.
GIACOMO ZANON
1 Отделение ортопедии и травматологии, Университет Павии, IRCCS Fondazione Policlinico San Matteo, Павия, Италия
GIOVANNI DI VICO
2 Дом престарелых Св. Михаила, Маддалони, Италия
МАТТЕО МАРУЛЛО
1 Отделение ортопедии и травматологии, Университет Павии, IRCCS Fondazione Policlinico San Matteo, Павия, Италия
1 Отделение ортопедии и травматологии, Университет Павии, IRCCS Fondazione Policlinico San Matteo, Павия, Италия
2 ул.Дом престарелых Майкла, Маддалони, Италия
Автор для корреспонденции: Джакомо Занон, доктор медицины, кафедра ортопедии и травматологии, Университет Павии, IRCCS Fondazione Policlinico San Matteo, Павия, Италия, электронная почта: [email protected] Авторские права © 2014, CIC Edizioni InternazionaliЭта статья цитируется в других статьях в PMC.Abstract
Рассекающий остеохондрит (ОКР) коленного сустава является частой причиной боли и дисфункции в коленном суставе среди пациентов с незрелым скелетом и молодых взрослых пациентов.ОКР все чаще встречается у детей, подростков и молодых взрослых спортсменов. Если его не распознать и не лечить надлежащим образом, это может привести к вторичному остеоартриту с болью и функциональными ограничениями. Стабильные поражения у пациентов с незрелым скелетом сначала следует лечить в неоперативном режиме. Нестабильные ювенильные поражения и стабильные ювенильные поражения, которые не заживают при консервативном лечении, требуют хирургического лечения. Напротив, ОКР коленного сустава у взрослых редко поддается консервативным мерам из-за ограниченного потенциала заживления.Оперативное лечение зависит от стадии поражения, и существует несколько хирургических вариантов.
Ключевые слова: хрящ, колено, костно-хрящевой, рассекающий остеохондит
Введение
Рассекающий остеохондрит (ОКР) является частой причиной боли в коленях и дисфункции у пациентов с незрелым скелетом и молодых взрослых пациентов. ОКР — это приобретенное идиопатическое поражение субхондральной кости, которое может вызывать отслоение и секвестрацию с вовлечением суставного хряща или без него (1–5).Этиология OCD остается спорной. Наиболее широко считается, что это происходит из-за повторных микротравм, связанных с сосудистым поражением, что подтверждается тем фактом, что поражение классически расположено на латеральной стороне медиального мыщелка бедренной кости, где оно может быть связано с контактом с гипертрофированным большеберцовым позвоночником ( 6).
Другими возможными причинами являются дефекты окостенения, повторяющиеся механические нагрузки и ишемия (7, 8). Поражение может зажить самопроизвольно или фрагмент может оторваться и смещаться в полости сустава, что приведет к наличию внутрисуставного рыхлого тела (8, 9).
Если ОКР не распознается и не лечится надлежащим образом, это может привести к вторичному остеоартриту (ОА) с болью и функциональными ограничениями. Рентгенография показывает, что у взрослых с ОКР ОА коленного сустава развивается примерно на 10 лет раньше, чем у пациентов с первичным остеоартритом (10).
Классификация
ОКР обычно классифицируется как «ювенильный» или «взрослый» в зависимости от степени зрелости дистального отдела бедренной кости. Считается, что большинство случаев ОКР у взрослых связано с сохранением нерешенного ювенильного ОКР, хотя было описано de novo взрослых ОКР (1).
Поражения ОКР у взрослых имеют склонность к нестабильности и обычно имеют прогрессирующее и неослабевающее клиническое течение. Для сравнения, ювенильные очаги ОКР с неповрежденной суставной поверхностью имеют потенциал к заживлению (11–13). Как взрослые, так и юношеские очаги ОКР, которые не заживают, потенциально могут быть связаны с последующими последствиями, такими как преждевременное дегенеративное заболевание суставов (10).
Поражения, оцениваемые артроскопически, могут быть классифицированы в соответствии с их серьезностью с использованием шкалы ОКР Международного общества восстановления хряща (ICRS) (14):
Тип I: стабильное поражение с непрерывной, но размягченной областью, покрытой неповрежденным суставным суставом. хрящ
Тип II: Поражение с частичным разрывом суставного хряща, стабильное при зондировании
Тип III: Поражение с полным разрывом суставного хряща, но без вывиха ( « мертвый in situ» )8
902 Тип IV: Пустой дефект или дефект с вывихнутым фрагментом или незакрепленным фрагментом в ложе ().Классификация поражений ОКР по ICRS. A: Тип I: стабильное поражение со сплошным, но размягченным участком, покрытым неповрежденным суставным хрящом. B: Тип II: поражение с частичным разрывом суставного хряща, стабильное при зондировании. C: Тип III: поражение с полным разрывом суставного хряща, но без вывиха («мертвый in situ »). D: Тип IV: пустой дефект или дефект с вывихнутым фрагментом или незакрепленным фрагментом внутри ложа.
Прогноз в отношении заживления поражения ОКР зависит как от зрелости скелета, так и от тяжести поражения.У более молодых пациентов с открытым физическим состоянием прогноз более благоприятный.
Эпидемиология
Несмотря на то, что точная распространенность ОКР неизвестна, сообщалось о показателях от 15 до 29 на 100 000 (10, 15).
Состояние показывает преобладание мужчин (соотношение мужчин и женщин 5: 3), хотя его распространенность среди девочек увеличивается. Средний возраст начала ОКР может снижаться, поскольку на заболеваемость, по-видимому, влияет растущее участие детей в спортивных соревнованиях (1).
Более 70% поражений ОКР обнаруживаются в заднебоковой части медиального мыщелка бедренной кости, 15% — в нижней центральной части латерального мыщелка и менее 1% — в блоке. Поражения надколенника, обычно расположенные в нижней медиальной области, встречаются редко (5–10%).
Этиология
Возможные причины ОКР (травматические, ишемические, идиопатические и наследственные) все еще обсуждаются, однако большинство авторов в настоящее время считают, что ОКР имеет многофакторную этиологию (16).
Травма
Травма — самая известная причина ОКР.Хотя прямая травма колена может привести к трансхондральному перелому, классическое расположение ОКР в заднебоковой части медиального мыщелка бедренной кости предполагает, что косвенная травма является более вероятной причиной. Повторное столкновение большеберцовой ости с латеральной стороной медиального мыщелка бедренной кости во время внутренней ротации большеберцовой кости также может быть одним из факторов (6).
Ишемия
Ишемия была исследована как потенциальная причина ОКР.Enneking (17) обнаружил, что кровоснабжение субхондральной кости похоже на кровоснабжение брыжейки кишечника с плохими анастомозами с окружающими артериолами. Эта склонность к ишемии естественным образом приводит к образованию секвестров в субхондральной кости, что делает ее особенно уязвимой для травматического повреждения, последующего перелома и потенциального разделения. Вместо этого Rogers и Gladstone (18) изучили васкуляризацию дистальной части бедренной кости и обнаружили многочисленные анастомозы с интрамедуллярной губчатой костью.
Genetics
Несколько авторов исследовали потенциальную генетическую связь с ОКР. Петри (16) не обнаружил четкой генетической этиологии ОКР.
Клиническая картина
Ранние поражения коленного сустава с ОКР связаны с расплывчатыми и плохо выраженными симптомами, включая различную степень боли и отека. По мере прогрессирования поражения появляются и учащаются такие симптомы, как захват, запирание и уступка.
Постоянные и тяжелые симптомы обычно связаны с расшатыванием тела в колене.Пораженные пациенты могут заметить запирание и могут пальпировать незакрепленное тело в пораженном суставе.
Визуализация
Визуализирующие исследования имеют решающее значение для характеристики поражений ОКР, оценки статуса поражения и прогнозирования прогноза. Идеальный алгоритм визуализации поможет хирургу отличить хирургические случаи от нехирургических.
Рентгенологическое исследование — подходящее исследование первой линии. Как описано Cahill и Berg (19), расположение и размер поражения можно установить по рентгенограмме.Первоначальная визуализация должна включать переднезадний и боковой вид колена. Надрез или туннельная задне-передняя рентгенограмма — лучший способ визуализировать поражение медиального мыщелка бедренной кости. При подозрении на поражение надколенника следует добавить вид на линию горизонта.
Магнитно-резонансная томография (МРТ) — рутинная часть диагностической оценки ОКР. Его можно использовать для визуализации незакрепленных тел и определения степени смещения. МРТ также позволяет оценить границы раздела жидкостей и целостность суставных поверхностей.МРТ можно использовать для точной оценки размера поражения и оценки состояния хряща и субхондральной кости; Поражения ОКР также могут быть идентифицированы на основании наличия зоны высокого сигнала под поражением, распространения костного отека () и наличия рыхлых тел, которые характерны для этих поражений (13).
Боковая рентгенограмма (A), сагиттальная МРТ (B) и аксиальная МРТ (C) рассекающего остеохондрита поражения блока (стрелка). Поражение четко отделено от подлежащей субкондральной кости с очевидным передним отделением суставной поверхности.D: Боковой рентгеновский снимок показывает рыхлое тело (стрелка).
Де Смет и др. (20) описали четыре критерия в Т2-взвешенных МРТ-исследованиях, которые коррелировали со способностью заживать очаги ОКР после неоперативного лечения: i) линия высокой интенсивности сигнала длиной не менее 5 мм между очагом ОКР и подлежащим лечением. кость, ii) область повышенного однородного сигнала диаметром не менее 5 мм под поражением, iii) очаговый дефект размером 5 мм или более на суставной поверхности, и iv) сильная сигнальная линия, пересекающая субхондральную пластинку в поражение.Из этих признаков высокая сигнальная линия за фрагментом, обнаруженная в 72% нестабильных поражений, оказалась наиболее прогностической (20). Pill et al. (21) обнаружили, что высокая сигнальная линия является наиболее частым признаком у пациентов, у которых неоперативное лечение было неудачным.
Внутрисуставное введение гадолиния увеличивает чувствительность и специфичность результатов МРТ (22). Bohndorf (23) продемонстрировал, что усиление высокой сигнальной линии за фрагментом после внутривенного введения гадолиния указывает на заживление грануляционной ткани, а не синовиальной жидкости.Сцинтиграфия кости с технецием — важный инструмент для оценки потенциального заживления костно-хрящевого фрагмента. Повышенное поглощение коррелирует с остеобластической активностью. Визуализация технеция может также выявить оккультное двустороннее поражение. Paletta et al. (24) проанализировали количественное сканирование костей в небольшой серии (12 пациентов) и обнаружили, что повышенная активность предсказывала выздоровление у 100% пациентов с открытыми формами бедренной кости, но не у подростков с закрытыми формами. Компьютерная томография (КТ) может быть полезна в предоперационном планировании и при назначении лечения, когда МРТ недоступна или противопоказана.
Консервативное лечение
Ювенильное ОКР со стабильными поражениями часто поддается лечению без операции, например иммобилизации, отсутствию веса или ограничению активности (25).
Cahill (1) сообщил, что 50% ювенильных очагов ОКР заживают в течение 10–18-месячного периода, при условии, что физика остается открытой, а пациентом сохраняется комплаентность. Симптоматические поражения у детей или пациентов с незрелым скелетом следует сначала лечить консервативными мерами в течение трех месяцев, если при рентгенологическом исследовании нет свободных тел.Однако хирургическое лечение показано, если безоперационное лечение не помогло в течение длительного периода времени (обычно шесть месяцев для ювенильного типа или более короткий период для взрослого типа) или при наличии нестабильного поражения. Напротив, ОКР коленного сустава у взрослых редко поддается консервативным методам.
Хирургическое лечение
Оперативное лечение следует рассматривать у пациентов с незрелым скелетом с отслоившимися или нестабильными поражениями, а также у тех пациентов, которым приближается физическое закрытие, чьи поражения не поддаются консервативному лечению (1, 26, 27).Напротив, большинство поражений ОКР у взрослых нестабильны, а клиническое течение более пагубно, что требует раннего агрессивного хирургического вмешательства (28, 29).
Пациентам с поражением менее 2 см в диаметре должно быть предложено артроскопическое вмешательство в виде субхондрального сверления и, возможно, хирургической обработки раны и стабилизации фрагмента. Может потребоваться костная трансплантация.
Пациентам с высыпаниями> 2 см в диаметре или пациентам с множественными незакрепленными телами () поражения могут быть исправлены с помощью открытой процедуры.Пациентам также может быть предложена имплантация аутологичных хондроцитов или мозаичная пластика.
Удаление хронического дряблого тела.
Пациентам с поражением диаметром 2 см и более может быть предложено радикальное удаление склеротической кости с костной пластикой дефекта и имплантацией аутологичных хондроцитов (сэндвич-метод).
Артроскопическое субхондральное сверление
С помощью этого метода выполняется множественная перфорация поражения спицами Киршнера. В то время как артроскопическое сверление ювенильных поражений ОКР хорошо описано в литературе, его применение при ОКР у взрослых менее известно.Двумя наиболее распространенными методами являются трансартикулярное сверление и ретросуставное сверление, которые служат для создания каналов для возможной реваскуляризации и заживления (30, 31). Хотя трансартикулярное сверление является точным и технически простым, оно создает каналы суставного хряща, которые заживают с помощью фиброзного хряща. С другой стороны, при ретросуставном сверлении такого повреждения суставного хряща можно избежать. Однако эта технически сложная процедура может привести к неадекватному сверлению дефекта и повреждению мягких тканей, и обычно она выполняется в сочетании с костной пластикой (28, 32).Для проведения костной пластики требуется дополнительная инвазивная хирургия для извлечения аутогенного губчатого вещества кости, обычно из гребня подвздошной кости. Ряд авторов обнаружили, что артроскопическое трансартикулярное сверление эффективно при лечении поражений ОКР у пациентов с незрелым скелетом, но менее эффективно у тех, у кого физическое закрытие уже произошло (30, 33–36).
Артроскопическая обработка раны и стабилизация фрагментов
В литературе есть описания ряда хирургических методов оперативной фиксации нестабильных поражений ОКР в колене с использованием биорассасывающихся гвоздей или штифтов и нерассасывающейся винтовой фиксации (37–39).
При нестабильных поражениях фиброзная ткань, обнаруженная между фрагментами, должна быть удалена. Если потеря костной массы значительна, может потребоваться трансплантация губчатой кости. Если в частично нестабильных поражениях наблюдается потеря субхондральной кости, аутогенный костный трансплантат упаковывается в кратер до репозиции и фиксации фрагмента. Винты Герберта и канюлированные винты использовались успешно, для удаления потребовались повторные операции (40, 41).
Хотя несколько авторов сообщили о положительных результатах применения биоабсорбируемых винтов, этот тип хирургического вмешательства не лишен осложнений, связанных с биодеградацией синтетических полимеров и реакцией организма хозяина (42–44).
Трансплантация аутологичных костно-хрящевых пробок для замещения дефектов у пациентов с зрелым скелетом хорошо описана в литературе. Однако у этой процедуры есть потенциальные недостатки, а именно болезненность донорского участка и неконгруэнтное суставное прилегание (45–47).
Аутологичная костно-хрящевая мозаичная пластика
Этот метод включает трансплантацию цилиндрических костно-хрящевых трансплантатов, взятых из ненагруженных участков колена, для восстановления несущей поверхности или пораженного участка.Для увеличения скорости заполнения используются комбинации трансплантатов разных размеров.
Аутологичная костно-хрящевая мозаичная пластика оказалась на 94% эффективной при поражениях ОКР, требующих хирургического вмешательства на мыщелке бедренной кости. Однако проспективное рандомизированное исследование напрямую сравнило имплантацию аутологичных хондроцитов с мозаичной пластикой при ОКР поражений колена и обнаружило, что имплантация аутологичных хондроцитов дала значительно лучшие результаты (45).
При трансплантации костно-хрящевого аллотрансплантата используется только что собранный мыщелок аллотрансплантата.Преимущества заключаются в том, что можно восстановить точную кривизну мыщелка, и во время сбора урожая не создается никаких дополнительных дефектов.
Имплантация аутологичных хондроцитов
Имплантация аутологичных хондроцитов включает диагностическую артроскопию, сбор небольшого количества хрящевых клеток для культивирования клеток и последующую реимплантацию клеток в дефект. В новых хирургических методах лечения, включая одноступенчатые клеточные процедуры, используются мезенхимальные стволовые клетки и увеличение матрикса (48).Имплантация аутологичных хондроцитов использовалась для лечения крупных изолированных дефектов бедренной кости у пациентов с зрелым скелетом. Если помимо суставного хряща не хватает субхондральной кости, перед имплантацией часто требуется костная пластика кратера ОКР.
Peterson et al. (49) сообщили об успешных клинических результатах более чем у 90% пациентов. Bentley et al. (45) сообщили о значительно лучших результатах имплантации аутологичных хондроцитов по сравнению с аутологичными пробками при костно-хрящевых дефектах в коленях у взрослых; кроме того, результаты мозаичной пластики со временем ухудшались.
Радикальное удаление склеротической кости с костной пластикой дефекта и имплантацией аутологичных хондроцитов (сэндвич-метод)
Дефект иссекается до нормального окружающего хряща, а склеротическая кость выкапывается до кровоточащей губчатой кости. Костный дефект заполняется губчатой костью до субхондральной костной пластинки, и берется периостальный лоскут, который используется для фиксации трансплантата. Затем используется второй надкостничный лоскут для имплантации аутологичных хондроцитов, которая выполняется, как описано ранее.
Новые хирургические методы лечения
Новые хирургические методы лечения, в том числе одноэтапные, используют биомиметический костно-хрящевой каркас (трехслойный коллаген-гидроксиапатитовый каркас) (). Filardo et al. (50) пролечили 27 пациентов с симптоматическим ОКР мыщелков бедренной кости с имплантацией трехслойного коллаген-гидроксиапатитового каркаса. Статистически значимое улучшение всех клинических показателей было получено через один и два года наблюдения.
Хирургический вид: имплантация остеоконхондрального каркаса на медиальном мыщелке бедренной кости.
Список литературы
1. Cahill BR. Рассекающий остеохондрит коленного сустава: лечение ювенильной и взрослой форм. J Am Acad Orthop Surg. 1995; 3: 237–247. [PubMed] [Google Scholar] 2. Clanton TO, DeLee JC. Рассекающий остеохондрит. История, патофизиология и современные концепции лечения. Clin Orthop Relat Res. 1982; (167): 50–64. [PubMed] [Google Scholar] 3. Glancy GL. Рассекающий ювенильный остеохондрит. Am J Knee Surg. 1999; 12: 120–124. [PubMed] [Google Scholar] 4. Кочер MS, Micheli LJ. Колено у детей: оценка и лечение.В: Insall JN, Scott WN, редакторы. Хирургия колена. 3-е изд. Нью-Йорк, Нью-Йорк: Черчилль-Ливингстон; 2001. С. 1356–1397. [Google Scholar] 5. Паппас А. Рассекающий остеохондроз. Clin Orthop Relat Res. 1981; (158): 59–69. [PubMed] [Google Scholar] 6. Папе Д., Филардо Г., Кон Е. и др. Клинические проблемы, связанные с заболеваниями подмышечной кости. Коленная хирургия Sports Traumatol Arthrosc. 2010. 18: 448–462. [PubMed] [Google Scholar] 7. Обедиан Р.С., Грелзамер Р.П. Рассекающий остеохондрит дистального отдела бедра и надколенника.Clin Sports Med. 1997. 16: 157–174. [PubMed] [Google Scholar] 8. Шенк Р.С., младший, Спокойной ночи JM. Рассекающий остеохондрит. J Bone Joint Surg Am. 1996. 78: 439–456. [PubMed] [Google Scholar] 9. O’Driscoll SW. Исцеление и регенерация суставного хряща. J Bone Joint Surg Am. 1998; 80: 1795–1812. [PubMed] [Google Scholar] 10. Линден Б. Заболеваемость рассекающим остеохондритом мыщелков бедренной кости. Acta Orthop Scand. 1976; 47: 664–667. [PubMed] [Google Scholar] 11. Кэхилл Б.Р., Филлипс М.Р., Наварро Р.Результаты консервативного лечения рассекающего ювенильного остеохондрита с помощью совместной сцинтиграфии. Перспективное исследование. Am J Sports Med. 1989; 17: 601–606. [PubMed] [Google Scholar] 12. Зеленый WT, Банки HH. Рассекающий остеохондрит у детей. J Bone Joint Surg Am. 1953; 35-А: 26–47. [PubMed] [Google Scholar] 13. Хефти Ф., Бегуристейн Дж., Крауспе Р. и др. Рассекающий остеохондрит: многоцентровое исследование Европейского педиатрического ортопедического общества. Дж. Педиатр Ортоп Б. 1999; 8: 231–245. [PubMed] [Google Scholar] 14.Бриттберг М., Винальски К.С. Оценка повреждений и ремонта хрящей. J Bone Joint Surg Am. 2003. 85 (Дополнение 2): 58–69. [PubMed] [Google Scholar] 15. Хьюстон Дж. К., Хергенродер П. Т., Куртенэ Б. Дж. Рассекающий остеохондрит мыщелков бедренной кости. J Bone Joint Surg Am. 1984; 66: 1340–1348. [PubMed] [Google Scholar] 16. Петри П.В. Этиология рассекающего остеохондрита. Неспособность установить семейное происхождение. J Bone Joint Surg Br. 1977; 59: 366–367. [PubMed] [Google Scholar] 17. Enneking WF. Клиническая Патология опорно-двигательного аппарата.Эд 3. Гейнсвилл, Флорида: Университет Флориды Пресс; 1990. с. 166. [Google Scholar] 18. Роджерс В.М., Гладстон Х. Сосудистые отверстия и артериальное кровоснабжение дистального конца бедренной кости. J Bone Joint Surg Am. 1950; 32 (A: 4): 867–874. [PubMed] [Google Scholar] 19. Кэхилл BR, Берг BC. Сцинтиграфия суставов с фосфатом 99m-технеция в лечении рассекающего остеохондрита мыщелков бедренной кости у несовершеннолетних. Am J Sports Med. 1983; 11: 329–335. [PubMed] [Google Scholar] 20. Де Смет А.А., Илахи О.А., Граф Б.К.Нелеченный рассекающий остеохондрит мыщелков бедренной кости: прогнозирование исхода для пациента с использованием результатов рентгенографии и МРТ. Skeletal Radiol. 1997; 26: 463–467. [PubMed] [Google Scholar] 21. Таблетка С.Г., Гэнли Т.Дж., Милам Р.А. и др. Роль магнитно-резонансной томографии и клинических критериев в прогнозировании успешного безоперационного лечения рассекающего остеохондрита у детей. J Pediatr Orthop. 2003. 23: 102–108. [PubMed] [Google Scholar] 22. Чой Ю.С., Коэн Н.А., Поттер Х.Г. и др. Магнитно-резонансная томография в оценке рассекающего остеохондрита надколенника.Skeletal Radiol. 2007; 36: 929–935. [PubMed] [Google Scholar] 23. Bohndorf K. Рассекающий остеохондрит (остеохондроз): обзор и новая классификация МРТ. Eur Radiol. 1998. 8: 103–112. [PubMed] [Google Scholar] 24. Палетта Г.А., мл., Беднарз П.А., Станицкий С.Л. и др. Прогностическое значение количественного сканирования костей при рассекающем остеохондрите коленного сустава: предварительный опыт. Am J Sports Med. 1998; 26: 7–14. [PubMed] [Google Scholar] 25. Twyman RS, Desai K, Aichroth P. Рассекающий остеохондрит коленного сустава: долгосрочное исследование.J Bone Joint Surg Br. 1991; 73: 461–464. [PubMed] [Google Scholar] 26. Юинг JW, Voto SJ. Артроскопическое хирургическое лечение рассекающего остеохондрита коленного сустава. Артроскопия. 1988; 4: 37-40. [PubMed] [Google Scholar] 27. Guhl JF. Артроскопическое лечение рассекающего остеохондрита. Clin Orthop Relat Res. 1982; (167): 65–74. [PubMed] [Google Scholar] 28. Garrett JC. Рассекающий остеохондрит. Clin Sports Med. 1991; 10: 569–593. [PubMed] [Google Scholar] 29. Майкл Дж. У., Вурт А., Эйзель П. и др. Отдаленные результаты после оперативного лечения рассекающего остеохондрита коленного сустава — результаты 30 лет.Int Orthop. 2008. 32: 217–221. [Бесплатная статья PMC] [PubMed] [Google Scholar] 30. Брэдли Джей, Денди диджей. Результаты бурения рассекающего остеохондрита до созревания скелета. J Bone Joint Surg Br. 1989. 71: 642–644. [PubMed] [Google Scholar] 31. Кавасаки К., Учио Ю., Адачи Н. и др. Сверление из межмыщелковой области для лечения рассекающего остеохондрита коленного сустава. Колено. 2003. 10: 257–263. [PubMed] [Google Scholar] 32. Леболт-младший, Уолл Э.Дж. Просверливание ретросустава и костная пластика при ювенильном рассекающем остеохондрите коленного сустава.Артроскопия. 2007; 23: 794.e1–794.e4. [PubMed] [Google Scholar] 33. Aglietti P, Buzzi R, Bassi PB, et al. Артроскопическое сверление при рассекающем ювенильном остеохондрите медиального мыщелка бедренной кости. Артроскопия. 1994; 10: 286–291. [PubMed] [Google Scholar] 34. Андерсон А.Ф. Антеградное сверление при рассекающем остеохондрите коленного сустава. Артроскопия. 1997. 13: 319–324. [PubMed] [Google Scholar] 35. Гэнли Т.Д.Ф., Амро Р.Р., Грегг Дж. Р. и др. Антеградное сверление при рассекающем остеохондрите коленного сустава. Доклад представлен на Ежегодном собрании педиатрического ортопедического общества Северной Америки в 2002 г .; 3–5 мая 2002 г .; Солт-Лейк-Сити, штат Юта.[Google Scholar] 36. Кочер М.С., Мичели Л.Дж., Янив М. и др. Функциональные и рентгенологические результаты рассекающего ювенильного остеохондрита коленного сустава, леченного трансартикулярным артроскопическим сверлением. Am J Sports Med. 2001; 29: 562–566. [PubMed] [Google Scholar] 37. Weckström M, Parviainen M, Kiuru MJ, et al. Сравнение биорассасывающихся штифтов и гвоздей при фиксации рассекающего остеохондрита взрослых фрагментов коленного сустава: результат 30 колен. Am J Sports Med. 2007. 35: 1467–1476. [PubMed] [Google Scholar] 38.Табаддор Р.Р., Банфи М.Б., Андерсен Дж. С. и др. Фиксация ювенильного остеохондрита рассекает поражения колена с помощью биорассасывающихся имплантатов из сополимера поли 96L / 4D-лактида. J Pediatr Orthop. 2010; 30: 14–20. [PubMed] [Google Scholar] 39. Андерсон А.Ф., Липскомб А.Б., Кулам С. Антеградная кюретка, костная пластика и фиксация рассекающего остеохондрита в скелетно зрелом колене. Am J Sports Med. 1990; 18: 254–261. [PubMed] [Google Scholar] 40. Кугат Р., Гарсия М., Куско Х и др. Рассекающий остеохондрит: исторический обзор и его лечение канюлированными винтами.Артроскопия. 1993; 9: 675–684. [PubMed] [Google Scholar] 41. Джонсон Л.Л., Уитвлугт Г., Остин М.Д. и др. Рассекающий остеохондрит коленного сустава: фиксация артроскопическим компрессионным винтом. Артроскопия. 1990; 6: 179–189. [PubMed] [Google Scholar] 42. Дервин Г.Ф., Кин Г.К., Чисселл Х.Р. Биоразлагаемые стержни при рассекающем остеохондрите коленного сустава у взрослых. Clin Orthop Relat Res. 1998; (356): 213–221. [PubMed] [Google Scholar] 43. Friederichs MG, Greis PE, Burks RT. Подводные камни, связанные с фиксацией рассекающих фрагментов остеохондрита биоабсорбируемыми винтами.Артроскопия. 2001; 17: 542–545. [PubMed] [Google Scholar] 44. Ким SJ, Шин SJ. Дряблые тела после артроскопического костно-хрящевого аутотрансплантата при рассекающем остеохондрите коленного сустава. Артроскопия. 2000; 16: E16. [PubMed] [Google Scholar] 45. Bentley G, Biant LC, Carrington RW и др. Проспективное рандомизированное сравнение имплантации аутологичных хондроцитов и мозаичной пластики при костно-хрящевых дефектах коленного сустава. J Bone Joint Surg Br. 2003. 85: 223–230. [PubMed] [Google Scholar] 46. Аутербридж HK, Аутербридж AR, Аутербридж RE.Использование латерального аутотрансплантата надколенника для восстановления большого костно-хрящевого дефекта колена. J Bone Joint Surg Am. 1995; 77: 65–72. [PubMed] [Google Scholar] 47. Йошизуми Ю., Сугита Т., Кавамата Т. и др. Цилиндрический костно-хрящевой трансплантат при рассекающем остеохондрите коленного сустава: отчет о трех случаях. Am J Sports Med. 2002; 30: 441–445. [PubMed] [Google Scholar] 48. Эриксон Б.Дж., Чалмерс П.Н., Янке А.Б. и др. Хирургическое лечение рассекающего остеохондрита коленного сустава. Curr Rev Musculoskelet Med.2013; 6: 102–114. [Бесплатная статья PMC] [PubMed] [Google Scholar] 49. Петерсон Л., Минас Т., Бриттберг М. и др. Лечение рассекающего остеохондрита коленного сустава трансплантацией аутологичных хондроцитов: результаты через 2–10 лет. J Bone Joint Surg Am. 2003; 85-А (Дополнение 2): 17–24. [PubMed] [Google Scholar] 50. Филардо Дж., Кон Е., Ди Мартино А. и др. Лечение рассекающего остеохондрита коленного сустава бесклеточным биомиметическим костно-хрящевым каркасом: клиническая и визуализирующая оценка через 2 года наблюдения. Am J Sports Med.2013; 41: 1786–1793. [PubMed] [Google Scholar]Рассекающий остеохондрит (ОКР) у лошадей — молекулярная основа его патогенеза и перспективы терапии стволовыми клетками-предшественниками
Джеффкотт, Л. Б. (1996). Остеохондроз — международная проблема коневодства. Журнал ветеринарных наук о лошадях, 16 (1), 32–37.
Артикул Google Scholar
Карлсон, К. С., Каллинз, Л.Д. и Меутен Д. Дж. (1995). Остеохондроз суставно-эпифизарного хрящевого комплекса у молодых лошадей: свидетельство нарушения кровоснабжения хрящевого канала. Ветеринарная патология, 32 (6), 641–647.
Артикул CAS PubMed Google Scholar
Экман С. и Карлсон К. С. (1998). Патофизиология остеохондроза. Ветеринарные клиники Северной Америки: практика мелких животных, 28 (1), 17–32.
Артикул CAS PubMed Google Scholar
Аль-Хизаб, Ф., Клегг, П. Д., Томпсон, К. К., и Картер, С. Д. (2002). Микроскопическая локализация активных желатиназ в хрящах рассекающего остеохондрита (ОКР) лошади. Остеоартрит и хрящ, 10 (8), 653–661.
Артикул CAS PubMed Google Scholar
Ван Верен, П.Р., и Олстад, К. (2016). Патогенез рассекающего остеохондроза: как это влияет на ведение клинического случая? Ветеринарное образование лошадей, 28 (3), 155–166.
Артикул Google Scholar
Троттер, Г. У., и Макилрайт, К. У. (1981). Рассекающий остеохондрит и субхондральные кистозные поражения и их связь с остеохондрозом у лошади. Журнал ветеринарных наук о лошадях, 1 (5), 157–162.
Артикул Google Scholar
Де Грау, Дж. К., Брама, П. А., Вимер, П., Броммер, Х., ван де Лест, К. Х., и ван Верен, П. Р. (2006). Хрящевые биомаркеры и липидные медиаторы воспаления у лошадей с рассекающим остеохондритом дистального промежуточного гребня большеберцовой кости. Американский журнал ветеринарных исследований, 67 (7), 1156–1162.
Артикул PubMed Google Scholar
Стромберг, Б. (1979). Обзор основных особенностей остеохондроза у лошади. Ветеринарный журнал лошадей, 11 (4), 211–214.
Артикул CAS PubMed Google Scholar
Вос, Н. Дж. (2008). Заболеваемость остеохондрозом (рассечением) у голландских теплокровных лошадей, представленных для предварительного обследования. Ирландский ветеринарный журнал, 61 (1), 33–37.
Артикул PubMed PubMed Central Google Scholar
Ральстон, С. Л. (1996). Гипергликемия / гиперинсулинемия после кормления зерновой мукой молодым лошадям с поражениями рассекающего остеохондрита (ОКР). Pferdeheilkunde, 12 (3), 320–322.
Артикул Google Scholar
Сток, К., Хаманн, Х. и Дистл, О. (2005). Преобладание костных отломков в дистальных и проксимальных межфаланговых, пястно-, плюснефаланговых и предплюсневых суставах теплокровных лошадей Ганновера. Журнал ветеринарной медицины. А., физиология, патология, клиническая медицина, 52 (8), 388–394.
Артикул CAS PubMed Google Scholar
Макилрайт, К. У. (2005). Использование синовиальной жидкости и биомаркеров сыворотки при заболеваниях костей и суставов лошадей: обзор. Ветеринарный журнал лошадей, 37 , 473–482.
Артикул CAS PubMed Google Scholar
Бранли, Т., Бертони, Л., Контентин, Р., Ракич, Р., Гомес-Ледук, Т., Десанс, М., Эрвье, М., Лежандр, Ф., Жаке, Ж., Одидже, Ф., Денуа, Дж. М., Демур, М., и Галера, П. (2017). Характеристика и использование мезенхимальных стволовых клеток костного мозга лошади в конструировании хряща лошади. Изучение их потенциала образования гиалинового хряща при культивировании в условиях гипоксии в биоматериале в присутствии BMP-2 и TGF-ß1. Обзоры стволовых клеток и отчеты, 13 (5), 611–630.
Артикул CAS Google Scholar
Джеффкотт, Л. Б., и Хенсон, Ф. М. Д. (1998). Исследования роста хряща у лошади и их применение в этиопатогенезе дисхондроплазии (остеохондроза). Ветеринарный журнал, 156 (3), 177–192.
Артикул CAS PubMed Google Scholar
Кэмпбелл, Дж. Р. (1977). Рост костей у жеребят и сжатие эпифиза. Ветеринарный журнал лошадей, 9 (3), 116–121.
Артикул CAS PubMed Google Scholar
Семеволос С.А. (2017). Развитие рассекающего остеохондрита. Ветеринарные клиники Северной Америки: конная практика, 33 (2), 367–378.
PubMed Google Scholar
Лаверти С. и Жирар К. (2013). Патогенез эпифизарного остеохондроза. Ветеринарный журнал, 197 (1), 3–12.
Артикул CAS PubMed Google Scholar
Sjaastad, Ø. В., Хоув, К., и Санд, О. (2003). Физиология домашних животных. Scandinavian Veterinary Press, 58 (244), 239–241.
Google Scholar
Ван Верен, П. Р. (2006). Этиология, диагностика и лечение ОК (D). Клинические методы в коневодстве, 5 , 248–258.
Артикул Google Scholar
Шинглтон, В.Д., Маки, Э. Дж., Коустон, Т. Э., и Джеффкотт, Л. Б. (1997). Хрящевые каналы в суставном / эпифизарном хряще лошади и возможная связь с дисхондроплазией. Ветеринарный журнал лошадей, 29 , 260–264.
Артикул Google Scholar
Карлсон, К. С., Меутен, Д. Дж., И Ричардсон, Д. К. (1991). Ишемический некроз хряща при спонтанных и экспериментальных очагах остеохондроза. Журнал ортопедических исследований, 9 (3), 317–329.
Артикул CAS PubMed Google Scholar
Фон Линтхудт Д. и Ревель М. (1994). Подобные рентгенологические поражения локализованной болезни Шейерманна поясничного отдела позвоночника у сестер-близнецов. Spine, 19 , 987–989.
Артикул PubMed Google Scholar
Виттвер К., Диркс К., Хаманн Х. и Дистл О. (2008). Связь между маркерами генов-кандидатов в локусе количественных признаков на хромосоме 4 лошади, ответственной за рассекающий остеохондроз в суставных связках хладнокровных лошадей южной Германии. Журнал наследственности, 99 (2), 125–129.
Артикул CAS PubMed Google Scholar
Левчук Д., и Корвин-Косаковска А. (2012). Генетические предпосылки остеохондроза у лошади — обзор. Статьи и отчеты по зоотехнике, 30 (3), 205–218.
CAS Google Scholar
Хилла Д. и Дистл О. (2013).Обзор: Генетические аспекты остеохондроза (рассечения), ладонно-подошвенных костно-хрящевых фрагментов, рентгенологические изменения ладьевидной кости и дегенеративные заболевания суставов у лошадей. Prakt. Tierarzt, 13 , 128–140.
Google Scholar
Ликкьен, С., Олсен, Х. Ф., Долвик, Н. И., Грондал, А. М., Роед, К. Х., & Клеметсдал, Г. (2014). Оценка наследственности предплюсневого остеохондроза и костно-хрящевых фрагментов ладонной / подошвенной первой фаланги у рысаков стандартной породы. Ветеринарный журнал лошадей, 46 , 32–37.
Артикул CAS PubMed Google Scholar
Наккаш, Ф., Мецгер, Дж., & Дистл, О. (2018). Генетические факторы риска остеохондроза у различных пород лошадей. Ветеринарный журнал лошадей, 50 (5), 556–563.
Артикул CAS PubMed Google Scholar
Austbø, L., Røed, K.Х., Долвик Н. И., Скреттинг Г. (2010). Идентификация дифференциально экспрессируемых генов, связанных с остеохондрозом у стандартных породных лошадей, с использованием произвольно примированной РНК ПЦР. Биотехнология животных, 21 , 135–139.
Артикул CAS PubMed Google Scholar
Сертейн, Д., Пикемал, Д., Вандерхейден, Л., Лежен, Ж.-П., Вервилген, Д., и Сандерсен, К. (2010). Профили экспрессии генов лейкоцитов лошадей, пораженных остеохондрозом. Журнал ортопедических исследований, 28 , 965–970.
CAS PubMed Google Scholar
Дежардин, К., Вайман, А., Мата, X., Лежандр, Р., Лаубье, Дж., Кеннеди, С.П., Лало, Д., Барри, Э., Жак, К., Крибиу, Е.П., и Шиблер, Л. (2014). Секвенирование следующего поколения идентифицирует миРНК хряща и субхондральной кости лошади и предполагает их участие в физиопатологии остеохондроза. BMC Genomics, 15 , 798.
Артикул CAS PubMed PubMed Central Google Scholar
Гибсон Г. и Асахара Х. (2013). микроРНК и хрящи. Журнал ортопедических исследований, 31 (9), 1333–1344.
Артикул CAS PubMed Google Scholar
Мартинес-Санчес А., Дудек К. А. и Мерфи К. Л. (2012). Регулирование функции хондроцитов человека посредством прямого ингибирования главного регулятора хряща SOX9 с помощью микроРНК-145 (miRNA-145). Журнал биологической химии, 287 , 916–924.
Артикул CAS PubMed Google Scholar
Барри, Э., Ривьер, Дж., Моргенталер, К., Россиньоль, Ф., Меспуль-Ривьер, К., и Роберт, К. (2016). P3004 Дифференциальная экспрессия микробов в синовиальной жидкости как биомаркеров остеохондроза в скакательных суставах лошади. Журнал зоотехники, 94 , 52–53.
Артикул Google Scholar
Фернандес, Т. Л., Шимомура, К., Асперти, А., Пиньейро, К. К. Г., Каэтано, Х. В. А., Оливейра, К. Р. Г. К. М., Накамура, Н., Эрнандес, А. Дж., И Буэно, Д. Ф. (2018). Разработка новой модели на крупных животных для оценки стволовых клеток пульпы зуба человека для лечения суставного хряща. Обзоры стволовых клеток и отчеты, 14 , 734–743.
Артикул CAS Google Scholar
Хуанг, З., Годкин, О., и Шульце-Танзил, Г.(2017). Проблема использования мезенхимальных стромальных клеток для рецеллюляризации децеллюляризованного хряща. Обзоры стволовых клеток и отчеты, 13 (1), 50–67.
Артикул CAS Google Scholar
Насрабади, Д., Резаиани, С., Эсламинеджад, М. Б., и Шабани, А. (2018). Улучшенный протокол хондрогенной дифференцировки мезенхимальных стволовых клеток костного мозга — влияние PTHrP и FGF-2 на гипертрофию хондроцитов, индуцированную TGFβ1 / BMP2. Обзоры стволовых клеток и отчеты, 14 , 755–766.
Артикул CAS Google Scholar
Келлинг, С., Крюгель, Дж., Ирмер, М., Пат, Дж. Р., Садовски, Б., Миро, X., и Миосге, Н. (2009). Мигрирующие хондрогенные клетки-предшественники из восстанавливающей ткани на поздних стадиях остеоартрита человека. Cell Stem Cell, 4 (4), 324–335.
Артикул CAS PubMed Google Scholar
Марич К., Корницка К., Марендзяк М., Голонка П., Никпонь Ю. (2016). Метаболический синдром лошадей нарушает остеогенную дифференцировку жировых стволовых клеток за счет преобладания аутофагии над избирательной митофагией. Журнал клеточной и молекулярной медицины, 20 (12), 2384–2404.
Редман С. Н., Олдфилд С. Ф. и Арчер К. В. (2005). Современные стратегии восстановления суставного хряща. Европейские клетки и материалы, 9 , 23–32.
Артикул CAS Google Scholar
Джонстон, Б., Алини, М., Куккиарини, М., Додж, Г.Р., Эглин, Д., Гилак, Ф., Мадри, Х., Мата, А., Маук, Р.Л., Семино, К.Э., и Стоддарт , MJ (2013). Тканевая инженерия для восстановления суставного хряща — современное состояние. Европейские клетки и материалы, 25 , 248–267.
Артикул CAS Google Scholar
Барберо А., Плоегерт С., Хеберер М. и Мартин И. (2003). Пластичность клональных популяций дедифференцированных суставных хондроцитов взрослого человека. Артрит и ревматизм, 48 , 1315–1325.
Артикул CAS PubMed Google Scholar
Альсалам, С., Амин, Р., Гемба, Т., & Лотц, М. (2004). Идентификация мезенхимальных клеток-предшественников в нормальном и остеоартрозном суставном хряще человека. Артрит и ревматизм, 50 , 1522–1532.
Артикул PubMed Google Scholar
Цзян Ю. и Туан Р. С. (2014). Происхождение и функция стволовых / предшественников хрящевых клеток при остеоартрите. Nature Reviews Ревматология, 11 (4), 206–212.
Артикул PubMed PubMed Central Google Scholar
Саймон Т. М. и Джексон Д. У. (2006). Суставной хрящ: пути повреждения и варианты лечения. Обзор спортивной медицины и артроскопии, 14 , 146–154.
Артикул PubMed Google Scholar
Сеол Д., МакКейб, Д.Д., Чоу, Х., Чжэн, Х., Ю, Ю., Янг, К., Уолтер, М.В., Леман, А.Д., Дин, Л., Баквалтер, Д.А., и Мартин, JA (2012). Хондрогенные клетки-предшественники реагируют на повреждение хряща. Артрит и ревматизм, 64 (11), 3626–3637.
Артикул CAS PubMed PubMed Central Google Scholar
Уильямс, Р., Хан, И. М., Ричардсон, К., Нельсон, Л., Маккарти, Х. Э., Анальбелси, Т., Сингхрао, С.К., Доутуэйт, Г.П., Джонс, Р.Э., Бэрд, Д.М., Льюис, Х., Робертс, С., Шоу, Х.М., Дудия, Дж., Фэйркла, Дж., Бриггс, Т., и Арчер, К. (2010). Идентификация и клональная характеристика субпопуляции клеток-предшественников в нормальном суставном хряще человека. PLoS One, 5 (10), e13246.
Артикул CAS PubMed PubMed Central Google Scholar
Хуанг, Ю.З., Се, Х.К., Silini, A., Parolini, O., Zhang, Y., Deng, L., & Huang, Y.-C. (2017). Мезенхимальные стволовые клетки / клетки-предшественники, полученные из суставного хряща, синовиальной оболочки и синовиальной жидкости для регенерации хряща: текущее состояние и перспективы на будущее. Обзоры стволовых клеток и отчеты, 13 (5), 575–586.
Артикул CAS Google Scholar
Цзян, Ю., Цай, Ю., Чжан, В., Инь, З., Ху, К., Тонг, Т., Лу, П., Чжан, С., Neculai, D., Tuan, R. S., & Ouyang, H. W. (2017). Клетки-предшественники, полученные из хряща человека, из коммитированных хондроцитов для эффективного восстановления и регенерации хряща. Трансляционная медицина стволовых клеток, 5 (6), 733–744.
Артикул CAS Google Scholar
Чамерник, К., Барлич, А., Дробнич, М., Марк, Дж., Джерас, М., и Зупан, Дж. (2018). Мезенхимальные стволовые клетки в костно-мышечной системе: от моделей животных к регенерации тканей человека? Обзоры стволовых клеток и отчеты, 14 (3), 346–369.
Артикул CAS Google Scholar
Пунвар С., & Хан У. С. (2011). Мезенхимальные стволовые клетки и восстановление суставного хряща: клинические исследования и будущее направление. Журнал «Открытая ортопедия», 5 , 296–301.
Артикул PubMed PubMed Central Google Scholar
Hunziker, E. (2001). Восстановление суставного хряща: фундаментальная наука и клинический прогресс.Обзор текущего состояния и перспектив. Остеоартрит и хрящ, 10 , 432–463.
Артикул Google Scholar
Каплан А. И. и Деннис Дж. Э. (2006). Мезенхимальные стволовые клетки как трофические медиаторы. Журнал клеточной биохимии, 98 , 1076–1084.
Артикул CAS PubMed Google Scholar
Castro-Viñuelas, R., Санджурхо-Родригес, К., Пиньейро-Рамиль, М., Эрмида-Гомес, Т., Фуэнтес-Бокете, И., Де Торо-Сантос, Ф. Дж., Бланко-Гарсия, Ф. Дж., И Диас-Прадо, С. ( 2018). индуцированные плюрипотентные стволовые клетки для восстановления хряща: состояние и перспективы на будущее. Европейские клетки и материалы, 36 , 96–109.
Артикул Google Scholar
Ван, М., Юань, З., Ма, Н., Хао, К., Го, В., Цзоу, Г., Чжан, Ю., Чен, М., Пэн, Дж. , Ванга, А., Ван, Ю., Суй, X., Сюй, В., Лу, С., Лю, С., Го, К. (2017). Достижения и перспективы стволовых клеток для регенерации хрящей. Stem Cells International , 1–16.
Гуццо Р. М., Скэнлон В., Санджай А., Сюй Р.-Х. и Дрисси Х. (2014). Создание типоспецифичных iPS-клеток человека с повышенным хондрогенным потенциалом. Обзоры стволовых клеток и отчеты, 10 (6), 820–829.
Артикул Google Scholar
Oellerich, D., & Miosg, N. (2017). Хондрогенные клетки-предшественники и восстановление хряща. Хрящ , 59–72.
Анасиз, Ю., Озгуль, Р. К., & Уккан-Четинкая, Д. (2017). Новая глава о мезенхимальных стволовых клетках: децеллюляризованные внеклеточные матрицы. Обзоры стволовых клеток и отчеты, 13 (5), 587–597.
Артикул CAS Google Scholar
Уолкер Р. Р. Э. (2007).Остеохондроз у лошади. Ветеринарные туры для крупных животных, 7 (1), 1–6.
Google Scholar
Мирамс, М., Айоделе, Б. А., Татарчух, Л., Хенсон, Ф. М., Пагель, К. Н., и Маки, Э. Дж. (2015). Идентификация новых генов, связанных с остеохондрозом. Журнал ортопедических исследований, 34 (3), 404–411.
Артикул CAS PubMed Google Scholar
Брунс, Дж., Вернер, М., & Хаберманн, К. (2017). Рассекающий остеохондрит: этиология, патология и визуализация с особым вниманием к коленному суставу. Хрящ , 1–17.
Джеффкотт, Л. Б. (1991). Остеохондроз у лошади — в поисках ключа к патогенезу. Ветеринарный журнал лошадей, 23 (5), 331–338.
Артикул CAS PubMed Google Scholar
Ytrehus, B., Карлсон, С., & Экман, С. (2007). Этиология и патогенез остеохондроза. Ветеринарная патология, 44 (4), 429–448.
Артикул CAS PubMed Google Scholar
Олстад, К., Экман, С., и Карлсон, К. С. (2015). Обновленная информация о патогенезе остеохондроза. Ветеринарная патология, 52 (5), 785–802.
Артикул CAS PubMed Google Scholar
Олстад, К., Хендриксон, Э. Х. С. и Карлсон, К. С. (2013). Пересечение сосудов в эпифизарных хрящевых каналах приводит к рассекающему остеохондрозу и рассекающему остеохондрозу бедренно-надколенникового сустава жеребят: потенциальная модель рассекающего остеохондрита у молодых людей. Остеоартрит и хрящ, 21 , 730–738.
Артикул CAS PubMed Google Scholar
Henson, F. M. D., Davies, M. E., & Ieffcott, L.Б. (1997). Дисхондроплазия лошадей (остеохондроз) — гистологические данные и локализация коллагена типа VI. Ветеринарный журнал, 154 , 53–62.
Артикул CAS PubMed Google Scholar
Бриджес, К. Х. и Харрис, Э. Д. (1988). Экспериментально индуцированные переломы хряща (рассекающий остеохондрит) у жеребят, получавших диету с низким содержанием меди. Журнал Американской ветеринарной медицинской ассоциации, 193 (2), 215–221.
CAS PubMed Google Scholar
Hurtig, M., Green, S., Dobson, H., Mikuni-Takagaki, Y., & Choi, J. (1993). Клинические и биохимические корреляты дефектного роста хрящей и костей у жеребят с дефицитом меди. Ветеринарный журнал лошадей, S16 .
Ван де Лест, К. Х. А., Брама, П. А. Дж., Ван Эль, Б., ДеГрут, Дж., И ван Верен, П. Р. (2004). Изменения внеклеточного матрикса при ранних дефектах остеохондроза у жеребят: ключевая роль коллагена? Biochimica et Biophysica Acta (BBA) — Molecular Basis of Disease, 1690 , 54–62.
Артикул CAS Google Scholar
Эрнандес-Видаль, Г., Джеффкотт, Л. Б., и Дэвис, М. Е. (1998). Иммунолокализация катепсина B в дисхондропластическом суставном хряще лошади. Ветеринарный журнал, 156 (3), 193–201.
Артикул CAS PubMed Google Scholar
Lecocq, M., Girard, C.A., Fogarty, U., Beauchamp, G., Ричард Х. и Лаверти С. (2008). Изменения хрящевого матрикса в развивающемся эпифизе: ранние события на пути к остеохондрозу лошадей? Ветеринарный журнал лошадей, 40 (5), 442–454.
Артикул CAS PubMed Google Scholar
Банк, Р. А., Саундри, М., Марудас, А., Мизрахи, Дж., И Текоппеле, Дж. М. (2000). Повышенный отек и мгновенная деформация остеоартрозного хряща тесно связаны с деградацией коллагена. Артрит и ревматизм, 43 , 2202–2210.
Артикул CAS PubMed Google Scholar
Gründer, W. (2006). МРТ-оценка ультраструктуры хряща. ЯМР в биомедицине, 19 (7), 855–876.
Артикул PubMed Google Scholar
Экман С., Родригес-Мартинес Х. и Плоен Л. (1990). Морфология нормального и остеохондрозного суставно-эпифизарного хряща свиней: исследование на домашних свиньях и мини-свиньях происхождения диких свиней. Acta Anatomica (Базель), 139 (3), 239–253.
Артикул CAS Google Scholar
Лиллих, Дж. Д., Бертоне, А. Л., Малемуд, К. Дж., Вейсброд, С. Е., Рагглз, А. Дж., И Стивенсон, С. (1997). Биохимическая, гистохимическая и иммуногистохимическая характеристика дистального остеохондроза большеберцовой кости у лошадей. Американский журнал ветеринарных исследований, 58 , 89–98.
CAS PubMed Google Scholar
Биркедал-Хансен, Х., Мур, У. Г., Бодден, М. К., Виндзор, Л. Дж., Биркедал-Хансен, Б., ДеКарло, А., и Энглер, Дж. А. (1993). Матричные металлопротеиназы: обзор. Критические обзоры по оральной биологии и медицине, 4 (2), 197–250.
Артикул CAS PubMed Google Scholar
Кино, Х., Сато, Х., Цунедзука, Ю., Такино, Т., Кавасима, А., и Окада, Ю. (1996). МТ-ММП, активатор проММП-2 (прогелатиназа а) на клеточной поверхности, экспрессируется с его субстратом в ткани мыши во время эмбриогенеза. Journal of Cell Science, 109 , 953–959.
CAS PubMed Google Scholar
d’Ortho, M. P., Will, H., Atkinson, S., Butler, G., Messent, A., & Gavrilovic, J. (1997). Матричные металлопротеиназы 1 и 2 мембранного типа обладают протеолитическими способностями широкого спектра, сравнимыми со многими матриксными металлопротеиназами. Европейский журнал биохимии, 250 (3), 751–757.
Артикул PubMed Google Scholar
Парч, Г., Матуччи-Чериник, М., Марабини, С., Янч, С., Пиньоне, А., и Каньони, М. (1991). Синтез коллагеназы синовиоцитов ревматоидного артрита: дозозависимая стимуляция веществом P и капсаицином. Скандинавский журнал ревматологии, 20 , 98–103.
Артикул CAS PubMed Google Scholar
Весснер, Дж. Ф. (1991). Матричные металлопротеиназы и их ингибиторы в ремоделировании соединительной ткани. Журнал FASEB, 5 (21), 45–54.
Google Scholar
Исигуро, Н., Ито, Т., Обата, К., Фудзимото, Н., и Ивата, Х. (1996). Определение стромелизина-1, коллагеназы типа IV 72 и 92 кДа, тканевого ингибитора металлопротеиназы-1 (ТИМП-1) и ТИМП-2 в синовиальной жидкости и сыворотке крови пациентов с ревматоидным артритом. Журнал ревматологии, 23 (1), 599–604.
Google Scholar
Постумус, М., Лимбург, П. К., Вестра, Дж., Кэтс, Х. А., Стюарт, Р. Э., ван Леувен, М. А., и ван Рейсвейк, М. Х. (1999). Уровни матриксной металлопротеиназы-3 в сыворотке крови в связи с развитием радиологического повреждения у пациентов с ранним ревматоидным артритом. Ревматология, 38 (108), 1–7.
Google Scholar
Mehraban, F., Lark, M. W., Ahmed, F. N., Xu, F., & Moskowitz, R. W. (1998). Повышенная секреция и активность матриксной металлопротеиназы-3 в синовиальных тканях и хондроцитах при экспериментальном остеоартрите. Osteoarthritis Cart, 6 (2), 86–94.
Google Scholar
Жуглин М., Робер Т., Валетт Дж., Гавар Д. Ф., Квинтин-Колон Ф. и Денуа Дж. (2000). Металлопротеиназы и активность фактора некроза опухолей альфа в синовиальной жидкости лошадей: корреляция с изменениями суставного хряща. Ветеринарные исследования, 31 , 507–515.
Артикул CAS PubMed Google Scholar
Клегг, П. Д., Берк, Р. М., Кофлан, А. Р., Риггс, К. М., и Картер, С. Д. (1997). Характеристика металлопротеиназ 2 и 9: идентификация клеточных источников этих ферментов в суставах. Ветеринарный журнал лошадей, 29 (3), 35–42.
Google Scholar
Клегг П. Д., Кофлан А. Р. и Картер С. Д. (1998). Конские TIMP-1 и 2: Идентификация, характеристика и клеточные источники при заболеваниях суставов. Ветеринарный журнал лошадей, 30 , 416–423.
Артикул CAS PubMed Google Scholar
Суарес, А., Анхела, К., Станек, К., Эдингер, Дж., И Бюхнер, Х. (2017). Измерение уровня металлопротеиназы-3 в синовиальной жидкости лошадей как биомаркера заболевания суставов. Revista Electrónica De Veterinaria, 18 (10), 1–11.
Google Scholar
Бринк, П., Смит, Р. К. У., Твердал, А., и Долвик, Н. И. (2015). Изменения концентраций биомаркеров синовиальной жидкости после артроскопической операции у лошадей с рассекающим остеохондритом дистального промежуточного гребня большеберцовой кости. Американский журнал ветеринарных исследований, 76 (7), 599–607.
Артикул CAS PubMed Google Scholar
Хедбом, Э., Антонссон, П., Хьерпе, А., Эшлиманн, Д., Паулссон, М., Роза-Пиментель, Э., Соммарин, Ю., Вендель, М., Олдберг, А., и Хейнегард, Д. (1992). Белки хрящевого матрикса. Кислый олигомерный белок (COMP) обнаруживается только в хрящах. Журнал биологической химии, 267 (61), 32–36.
Google Scholar
Мисуми, К., Вилим, В., Клегг, П. Д., Томпсон, К. С. М., и Картер, С. Д. (2001). Измерение белка олигомерного матрикса хряща (COMP) в синовиальной жидкости нормальной и больной лошади. Остеоартрит и хрящ, 9 (2), 119–127.
Артикул CAS PubMed Google Scholar
Тейлор, С. Э., Уивер, М. П., Пициллидес, А. А., Уиллер, Б. Т., Уиллер-Джонс, К. П. Д., Шоу, Д. Дж., И Смит, Р. К. У. (2006). Уровни белка олигомерного матрикса хряща и гиалуронана в синовиальной жидкости лошадей с остеоартрозом предплюсне-плюсневого сустава по сравнению с контрольной популяцией. Ветеринарный журнал лошадей, 38 (6), 502–507.
Артикул CAS PubMed Google Scholar
Скиельдебранд, Э., Хейнегард, Д., Элоранта, М. Л., Нильссон, Г., Дудхия, Дж., Сандгрен, Б., и Экман, С. (2005). Повышенная концентрация COMP (олигомерный матричный белок хряща) в костно-хрящевых переломах от гоночных чистокровных животных. Журнал ортопедических исследований, 23 (1), 156–163.
Артикул CAS PubMed Google Scholar
Юн, Дж. К., Нг, А., Ким, Б. Х., Бьянко, А., Ксавьер, Р. Дж., И Элледж, С. Дж. (2010). Передача сигналов Wnt регулирует физиологию митохондрий и чувствительность к инсулину. Гены и развитие, 24 (14), 1507–1518.
Артикул CAS Google Scholar
Xu, M., Stattin, E.-L., Shaw, G., Heinegård, D., Sullivan, G., Wilmut, I., Colman, A., Onnerfjord, P., Khabut , А., Аспберг, А., Докери, П., Хардингем, Т., Мерфи, М., и Барри, Ф. (2017). Хондроциты, полученные из мезенхимальных стромальных клеток и индуцированные плюрипотентные клетки пациентов с семейным остеохондритом Dissecans, проявляют стрессовую реакцию эндоплазматического ретикулума и дефектную сборку матрикса. Трансляционная медицина стволовых клеток, 5 (9), 1171–1181.
Артикул CAS Google Scholar
Verwilghen, D. R., Enzerink, E., Martens, A., Franck, T., Balligand, M., Хенротин, Ю., Детильё, Дж., И Сертейн, Д. (2011a). Связь между артроскопической оценкой суставов и уровнями Coll2-1, Coll2-1NO2 и миелопероксидазы в крови и синовиальной жидкости лошадей, пораженных остеохондрозом предплюсневого сустава. Остеоартрит и хрящ, 19 (11), 1323–1329.
Артикул CAS PubMed Google Scholar
Деберг, М., Лабасс, А., Кристгау, С., Клоос, П., Банг Хенриксен, Д., Шапель, Ж.-П., Зегельс, Б., Регинстер, Дж. Ю., и Хенротин, Ю. (2005). Новые биохимические маркеры сыворотки (Coll 2-1 и Coll 2-1 NO2) для изучения деградации коллагеновой сети типа II, связанной с окислением, у пациентов с остеоартритом и ревматоидным артритом. Остеоартрит и хрящ, 13 (3), 258–265.
Артикул PubMed Google Scholar
Амей, Л. Г., Деберг, М., Оливейра, М., Лабасс, А., Эшлиманн, Дж. М., и Хенротин, Ю. (2007). Химические биомаркеры C2C, Coll2-1 и Coll2-1NO2 предоставляют дополнительную информацию о катаболизме коллагена типа II у здоровых мышей и мышей с остеоартритом. Артрит и ревматизм, 56 (10), 3336–3346.
Артикул CAS PubMed Google Scholar
Verwilghen, D. R., Martens, A., Busschers, E., Franck, T., Deberg, M., Henrotin, Y., Vanderheyden, L., & Serteyn, D.(2011b). Концентрации Coll2-1, Coll2-1NO2 и миелопероксидазы в синовиальной жидкости предплюсневых суставов лошадей, пораженных остеохондрозом. Связь с ветеринарными исследованиями, 35 (7), 401–408.
Артикул PubMed Google Scholar
Лепаж, О. М., Марку, М., Трембле, А., и Дюма, Г. (1992). Пол не влияет на уровень остеокальцина в сыворотке крови у стандартных лошадей разного возраста. Канадский журнал ветеринарных исследований, 56 , 379–381.
CAS PubMed PubMed Central Google Scholar
Биллингхерст, Р. К., Брама, П. А. Дж., Ван Верен, П. Р., Ноултон, М. С., и Макилрайт, К. В. (2004). Оценка сывороточных концентраций биомаркеров метаболизма скелета и результатов рентгенографии как индикаторов тяжести остеохондроза у жеребят. Американский журнал ветеринарных исследований, 65 (2), 143–150.
Артикул CAS PubMed Google Scholar
Фрисби, Д. Д., Аль-Собаил, Ф., Биллингхерст, Р. К., Кавкак, К. Э., и Макилврейт, К. В. (2008). Изменения синовиальной жидкости и биомаркеров сыворотки крови при физической нагрузке и раннем остеоартрите у лошадей. Остеоартрит и хрящ, 16 , 1196–1204.
Артикул CAS PubMed Google Scholar
Димок, А. Н., Сицилиано, П. Д., и Макилрайт, К. В. (2010). Доказательства, подтверждающие повышенное присутствие активных форм кислорода в пораженном суставе лошади. Ветеринарный журнал лошадей, 32 (5), 439–443.
Артикул Google Scholar
Керер, Дж. П. (1993). Свободные радикалы как медиаторы повреждения тканей и болезней. Критические обзоры по токсикологии, 23 (1), 21–48.
Артикул CAS PubMed Google Scholar
Ауэр Д. Э. (1989). Гипотеза об этиопатогенезе воспалительных заболеваний суставов у лошадей. Ветеринарная клиническая патология, 18 (1), 21–26.
Артикул CAS PubMed Google Scholar
Гаттеридж, Дж. М. К. (1993). Свободные радикалы в болезненных процессах: сборник причин и следствий. Сообщения об исследованиях свободных радикалов, 19 , 141–158.
Артикул CAS PubMed Google Scholar
De Franceshi, L., Григоло, Б., Розети, Л., Маркони, Э., Факкини, А., Буда, Р., Ваннини, Ф., и Джаннини, С. (2007). Рассекающий остеохондрит. Гистопатология, 51 (1), 133–134.
Артикул PubMed Google Scholar
Винсент, Ф., Брун, Х., Чейн, Э., Ронто, X., и Адольф, М. (1989). Влияние свободных радикалов кислорода на кинетику пролиферации культивируемых суставных хондроцитов кролика. Журнал клеточной физиологии, 141 , 262–266.
Артикул CAS PubMed Google Scholar
Раткришнан, К., Тику, К., Рагхаван, А., и Тику, М. Л. (1992). Высвобождение кислородных радикалов суставными хондроцитами: исследование люминол-зависимой хемилюминесценции и секреции перекиси водорода. Журнал исследований костей и минералов, 7 , 11–39.
Google Scholar
Сертейн, Д., Пикемаль, Д., Мендоса, Л., Кодрон, И., Ногье, Ф., Бруно, Р., Сандерсен, К., и Лежен, Дж. П. (2014). Экспрессия генов, связанных с остеохондрозом, в лейкоцитах лошадей различается в зависимости от пораженных суставов жеребят. Журнал молекулярных биомаркеров и диагностики, 5 (5), 189.
Google Scholar
Кинсли, М. А., Семеволос, С. А., и Дестердик-Зеллмер, К. Ф. (2015). Передача сигналов Wnt / β-катенином в хрящевых каналах и хондроцитах костно-хрящевого соединения, а также в хрящах полной толщины при раннем остеохондрозе лошадей. Журнал ортопедических исследований, 33 (10), 1433–1438.
Артикул CAS PubMed Google Scholar
Каасик А., Сафиулина Д., Чубей В., Куум М., Жарковский А., Векслер В. (2007). Набухание митохондрий нарушает транспорт органелл в нейронах гранул мозжечка. Журнал биологической химии, 282 (45), 32821–32826.
Артикул CAS PubMed Google Scholar
Халестреп, А. П. (1989). Регулирование объема матрикса митохондрий млекопитающих in vivo и in vitro и его роль в контроле митохондриального метаболизма. Biochimica et Biophysica Acta, 973 (3), 355–382.
Артикул CAS PubMed Google Scholar
Desjardin, C., Chat, S., Gilles, M., Legendre, R., Riviere, J., Mata, X., Balliau, T., Esquerré, D., Cribiu, EP, Бетч, Дж. М., и Шиблер, Л.(2014). Участие митохондриальной дисфункции и ER-стресса в физиопатологии рассекающего остеохондрита лошадей (ОКР). Экспериментальная и молекулярная патология, 96 (3), 328–338.
Артикул CAS PubMed Google Scholar
Руис-Ромеро, К., Лопес-Армада, М. Дж., И Бланко, Ф. Дж. М. Д. (2006). Митохондриальная протеомная характеристика нормальных суставных хондроцитов человека. Остеоартрит и хрящ, 14 , 507–518.
Артикул CAS PubMed Google Scholar
Кэмерон, Т. Л., Белл, К. М., Татарчух, Л., Маки, Э. Дж., Раджпар, М. Х., Макдермотт, Б. Т., Бут-Хэндфорд, Р. П., и Бейтман, Дж. Ф. (2011). Транскрипционное профилирование хрящевой пластинки роста хондродисплазии выявляет адаптивные сети ER-стресса, которые позволяют выжить, но нарушают гипертрофию. PLoS One, 6 (9), e24600.
Артикул CAS PubMed PubMed Central Google Scholar
Браво, Р., Парра, В., Гатика, Д., Родригес, А. Э., Торреальба, Н., Паредес, Ф., Ван, З. В., Зорзано, А., Хилл, Дж. А., Джаймович, Е., Квест, А.Ф. и Лавандеро С. (2013). Эндоплазматический ретикулум и развернутый белковый ответ: динамика и метаболическая интеграция. Международный обзор клеточной и молекулярной биологии, 301 , 215–290.
Артикул CAS PubMed PubMed Central Google Scholar
Яммани Р.Р. (2012). Белки S100 в хрящах: роль при артрите. Biochimica et Biophysica Acta, 1822 (4), 600–606.
Артикул CAS PubMed PubMed Central Google Scholar
Скаген, П. С., Хорн, Т., Круз, Х. А., Стаергаард, Б., Раппорт, М. М., и Николайсен, Т. (2011). Рассекающий остеохондрит (ОКР), болезнь накопления эндоплазматического ретикулума ?: морфологическое и молекулярное исследование фрагментов ОКР. Скандинавский журнал медицины и науки о спорте, 21 (6), e17 – e33.
Артикул CAS Google Scholar
McIlwraith, C.W. (2010). Лечение заболеваний суставов у спортивных лошадей. В: Материалы конференции по исследованию питания лошадей в Кентукки, 2010 г., Кормление и ветеринарное управление спортивной лошади, Лексингтон, штат Кентукки, 26–27 апреля, стр. 61–81.
Макилрайт, К. У. (2013).Хирургическое лечение остеохондроза в сравнении с консервативным. Ветеринарный журнал, 197 (1), 19–28.
Артикул PubMed Google Scholar
Пирс С.Г., Ферт Е.С., Грейс Н.Д. и Феннесси П.Ф. (1998). Влияние добавок меди на признаки ортопедических заболеваний у чистокровных животных Новой Зеландии, получающих пастбищное питание. Ветеринарный журнал лошадей, 30 (3), 211–218.
Артикул CAS PubMed Google Scholar
Спаркс, Х. Д., Никсон, А. Дж., Фортиер, Л. А., и Мохаммед, Х. О. (2011). Артроскопическое прикрепление рассекающего хрящевого лоскута бедренно-пателлярного сустава остеохондрита: отдаленные результаты. Ветеринарный журнал лошадей, 43 , 650–659.
Артикул CAS PubMed Google Scholar
Стек, Дж. Д., Левингстон, Т. Дж., Лалор, В., Сандерс, Р., Кирни, К., О’Брайен, Ф. Дж., И Дэвид, Ф. (2017). Ремонт большого остеохондрита рассекает поражения с использованием новой многослойной тканевой инженерной конструкции у конного спортсмена. Журнал тканевой инженерии и регенеративной медицины, 11 (10), 2785–2795.
Артикул CAS PubMed Google Scholar
Corzani, M., Meccariello, L., Bisaccia, M., Ferrara, P., Rinonapoli, G., Piscitelli, L., Liberata Meccariello, M., & Caraffa, A. (2016) . Современное лечение двустороннего рассекающего остеохондрита в коленях: от описания случая к обзору литературы. Международный журнал хирургии и медицины, 2 (4), 223–229.
Артикул Google Scholar
Рассекающий остеохондрит коленного сустава — Рассекающий остеохондрит
Рассекающий остеохондрит (ОКР) — это приобретенное потенциально обратимое поражение субхондральной кости, которое также влияет на покрывающий хрящ. Причины ОКР неизвестны. Если ОКР прогрессирует, это может привести к нестабильности суставного хряща. Когда ОКР поражает колено, чаще всего его локализация находится в латеральной части медиального мыщелка бедренной кости.У ювенильных поражений ОКР прогноз заживления лучше, чем у взрослых. Обычно ОКР поражает мужчин чаще, чем женщин (от 2: 1 до 3: 1). Однако по мере того, как женщины и дети младшего возраста занимаются спортом, наблюдается рост распространенности среди девочек и более молодой средний возраст начала ОКР.
Этиология / патологоанатомия
Причины ОКР неизвестны, однако повторяющиеся травмы, воспаления, дополнительные центры окостенения, ишемия и генетические факторы показывают причинную корреляцию.). Существуют некоторые семейные тенденции, но наиболее распространено несемейное ОКР. Повторяющиеся травмы, вызванные круглогодичными видами спорта, ранней спортивной специализацией, несколькими видами спорта в одном классе или несколькими командами в одном виде спорта, а также повышенная интенсивность тренировок являются одними из причинных факторов, связанных с ОКР. Было высказано предположение, что хроническая повторяющаяся микротравма приводит к стрессовой реакции внутри субхондральной кости и, в более тяжелых случаях, к некрозу субхондральной кости, когда может произойти расслоение и разделение фрагментов.
Оценка
Пациенты с ОКР коленного сустава изначально предъявляют неспецифические жалобы на боль в передней части колена и периодическую припухлость различной степени. По мере прогрессирования заболевания пациенты могут жаловаться на более стойкую опухоль или излияние, защемление, запирание и / или уступку. К сожалению, боль и припухлость не являются хорошими показателями рассечения. Физические данные могут включать положительный тест Вильсона, который воспроизводит боль за счет внутреннего вращения большеберцовой кости во время разгибания колена между 90 и 30 градусами, а затем облегчения боли за счет наружного вращения большеберцовой кости.Предпосылка для этого теста заключается в том, что возвышение большеберцовой кости соприкасается с поражением ОКР при внутренней ротации и разгибании; тогда как внешнее вращение перемещает возвышение от поражения.
Стандартные рентгенограммы обоих колен с нагрузкой полезны для первоначальной характеристики типа поражения и статуса пластинки роста. Вид сбоку помогает определить передне-заднее расположение поражения и нормальные, доброкачественные дополнительные центры окостенения в скелетно незрелом колене. Осевой вид полезен при подозрении на поражение надколенника или блока, а «вид с надрезом» при 30–50 градусах сгибания колена может помочь идентифицировать поражения заднего мыщелка бедренной кости.
Исследования были выполнены, чтобы попытаться идентифицировать конкретные результаты МРТ, которые связывают способность поражений ОКР заживать после неоперативного лечения.
Безоперационное лечение
Целью безоперационного вмешательства является ускорение заживления субхондральной кости и предотвращение коллапса хряща, последующего перелома и образования кратера. Лечение зависит от зрелости скелета пациента, а также от размера, стабильности и местоположения поражения, поскольку чем более зрелый скелет пациент, тем хуже прогноз.Нехирургическое лечение является методом выбора при небольших стабильных поражениях у незрелого скелета пациентов с широко открытыми физиологическими образованиями и без признаков нестабильности на МРТ. Нехирургическое лечение фокусируется на значительном изменении деятельности за счет ограничения деятельности с высокой степенью воздействия. Кратковременная иммобилизация и защищенная нагрузка могут быть полезны. В качестве альтернативы могут быть полезны упражнения на фиксацию колен и их подвижность. Обычно начинается период от трех до девяти месяцев безоперационного лечения.Хирургическое лечение для ускорения заживления рекомендуется, когда нехирургические методы оказываются неэффективными, а также для пациентов со зрелым скелетом с большими поражениями.
Оперативное лечение
Хирургическое лечение начинается с артроскопии. Следует рассмотреть возможность оперативного лечения пациентов с нестабильными или отслоившимися поражениями, неудачным консервативным лечением и пациентам, приближающимся к зрелости скелета. Цели оперативного лечения — способствовать заживлению субхондральной кости, поддерживать конгруэнтность суставов, фиксировать жестко нестабильные фрагменты и заменять костно-хрящевые дефекты клетками, которые могут замещать и вырастать хрящи.(53) Оптимальное хирургическое лечение обеспечивает стабильную конструкцию субхондральной кости, кальцинированную отметку прилива и восстанавливающий хрящ с жизнеспособностью и биомеханическими свойствами, эквивалентными или подобными нативному гиалиновому хрящу.
Хирургическое лечение стабильных поражений с неповрежденным суставным хрящом включает просверливание субхондральной кости с целью стимуляции врастания сосудов и заживления субхондральной кости. Если поражение нестабильное и шарнирное, показана фиксация. Пациентам с шарнирным поражением без субхондральной поддержки показана костная пластика для восстановления конгруэнтности суставов.Цель состоит в том, чтобы зафиксировать костную часть фрагмента, чтобы обеспечить заживление и стабилизацию вышележащей суставной поверхности. Артроскопическая или открытая репозиция и внутренняя фиксация могут выполняться аппаратными средствами с использованием спиц Киршнера, канюлированных винтов или винтов Герберта. Сопутствующие осложнения включают миграцию имплантата, повреждение соседнего хряща и аппаратный перелом. Костно-хрящевые пробки недавно были представлены как биологическая альтернатива использованию оборудования. Пробки обеспечивают костный трансплантат, а также фиксацию поражения (26,34)
Если фиксация невозможна, существует несколько методов восстановления дефектов полной толщины, включая методы стимуляции костного мозга, такие как микропереломы, а также имплантация аутологичных хондроцитов и трансплантация костно-хрящевого аутотрансплантата.Однако эти методы имеют ограниченные данные о клинических исходах у подростков.
[toggle hide = «yes» border = «yes» style = «white» title_closed = «Открыть ссылки» title_open = «Закрыть ссылки»]
Ссылки
1. Aglietti, P .; Buzzi, R .; Басси, П. Б. и Фиорити, М .: Артроскопическое сверление при рассекающем ювенильном остеохондрите медиального мыщелка бедренной кости. Arthroscopy, 10 (3): 286-91, 1994.
2. Anderson, A. F .; Richards, D. B .; Pagnani, M. J. и Hovis, W. D .: Антеградное сверление при рассекающем остеохондрите коленного сустава.Arthroscopy, 13 (3): 319-24, 1997.
3. Кэхилл, Б. Р. и Берг, Б. С. Сцинтиграфия суставов с фосфатом 99m-технеция в лечении рассекающего остеохондрита мыщелков бедренной кости. Am J Sports Med, 11 (5): 329-35, 1983.
4. Кэхилл Б.Р .: Рассекающий остеохондрит коленного сустава: лечение юношеских и взрослых форм. J Am Acad Orthop Surg, 3 (4): 237-247, 1995.
5. De Smet, A. A .; Илахи, О. А. и Граф, Б. К.: Нелеченный рассекающий остеохондрит мыщелков бедренной кости: прогнозирование исхода для пациента с использованием результатов рентгенографии и МРТ.Skeletal Radiol, 26 (8): 463-7, 1997.
6. Flynn, J.M. Kocher, M.S. Гэнли, Т.Дж. Рассекающий остеоходрит коленного сустава. J. Pediatr. Orthop., 2004, июль-август: 24 (4): 434-43.
7. Гэнли Т.Дж., Флинн Дж.М.: Рассекающий остеохондрит. В: Insall & Scott Surgery of the Knee, четвертое издание, том 2, Elsevier, 1234-1241, 2006.
8. Kocher, M. S., Micheli, L.J .; Янив, М .; Зураковский, Д .; Ames, A .; Адриньоло, А.А.: Функциональные и рентгенографические результаты рассекающего ювенильного остеохондрита коленного сустава, леченного трансартикулярным артроскопическим сверлением.Am J Sports Med, 29 (5): 562-566, 2001.
9. Кохер М.С., Такер Р., Гэнли Т.Дж., Флинн Дж. М.: Лечение рассекающего остеохондрита коленного сустава: Обзор текущих концепций, Американский журнал спортивной медицины, 2006 г. Июль; 34 (7): 1181-1191.
10. Peterson, L .; Минас, Т .; Бриттберг, М. и Линдал, А.: Лечение рассекающего остеохондрита коленного сустава трансплантацией аутологичных хондроцитов: результаты через два-десять лет. J Bone Joint Surg Am, 85-A (Suppl 2): 17-24, 2003.
11. Pill, S.G .; Гэнли, Т.J .; Milam, R.A .; Lou, J. E .; Мейер, Дж. С. и Флинн, Дж. М .: Роль магнитно-резонансной томографии и клинических критериев в прогнозировании успешного безоперационного лечения рассекающего остеохондрита у детей. J Pediatr Orthop, 23 (1): 102-8, 2003.
. 12. O’Connor, M.A .; Palaniappan, M .; Хан, Н. и Брюс, К. Э .: Рассекающий остеохондрит коленного сустава у детей. Сравнение результатов МРТ и артроскопии. J Bone Joint Surg Br, 84 (2): 258-62, 2002.
13. Steadman, J.R .; Бриггс, К.К .; Родриго, Дж.J .; Kocher, M.S .; Гилл; T.J .; Родки У.Г .: Исходы микропереломов при травматических хондральных дефектах коленного сустава: в среднем через 11 лет наблюдения. Arthroscopy, 19 (5): 477-484, 2003.
14. Томсон, Н.Л .: Рассекающий остеохондрит и костно-хрящевые фрагменты, управляемые компрессионной винтовой фиксацией Герберта. Clin Orthop, (224): 71-8, 1987.
15. Twyman, R. S .; Десаи К. и Айхрот П. М .: Рассекающий остеохондрит коленного сустава. Долгосрочное исследование. J Bone Joint Surg Br, 73 (3): 461-4, 1991.
16. Vonstein, D.W. N., H. Laor, T. и др.: Рассекающий ювенильный остеохондрит коленного сустава: прогноз заживления, основанный на рентгеновском снимке и МРТ с усилением гадолиния. Педиатрическое ортопедическое общество Северной Америки: 79, 2003.
17. Уилсон, Дж. Н .: Диагностический признак рассекающего остеохондрита коленного сустава. J Bone Joint Surg Am, 49 (3): 477-80, 1967.
18. Лефорт Дж., Мойен Б., Бофилс П., Де Билли Б., Бреда Р., Кадилхак С., Клаверт П. и др. Рассекающий остеохондрит мыщелков бедренной кости: сообщение о 892 случаях. Rev Chir Orthop Reparatrice Appar Mot.2006 сен; 92 (5 доп.): 97-141.
19. Дин Р., Аннир П., Скэдден Дж. Внутренняя фиксация несмещенных поражений рассекающего остеохондрита в колене. JBJS Br. 2006 июл; 88 (7): 900-4.
20. Micheli LJ, Moseley JB, Anderson AF, et al. Дефекты суставного хряща дистального отдела бедренной кости у детей и подростков: лечение с имплантацией аутологичных хондроцитов. J Pediatr Orthop. Июль-август 2006 г .; 26 (4): 455-460.
21. Кришнан С.П., Скиннер Дж. А. и др. Имплантация покрытых коллагеном аутологичных хондроцитов при рассекающем остеохондрите коленного сустава: результаты от двух до семи лет.JBJS Br. 2006 фев; 88 (2): 203-5.
22. Макино А., Мусколо Д. Л. и др. Артроскопическая фиксация рассекающего остеохондрита коленного сустава: клиническая картина, магнитно-резонансная томография и артроскопическое наблюдение. Am J Sports Med. 2005 Oct; 33 (10): 1499-504.
23. Гебарски К., Эрнандес Р.Дж. Рассекающий остеохондрит I стадии в сравнении с нормальными вариантами окостенения коленного сустава у детей. Pediatr Radiol. 2005 Sep; 35 (9): 880-6.
24. Uematsu K, Habata T, Hasegawa Y. Рассекающий остеохондрит коленного сустава: отдаленные результаты иссечения костно-хрящевых фрагментов.Колено. 2005 Jun; 12 (3): 205-8.
25. Cepero S, ullot R, Sastre S. Остеохондрит мыщелков бедренной кости у детей и подростков: наш опыт за последние 28 лет. J Педиатр Ортоп Б. 2005 Янв; 14 (1): 24-9.
26. Кобаяси Т., Фудзикава К., Оохаши М. Хирургическая фиксация массивного рассекающего остеохонрита поражения с помощью цилиндрических костно-хрящевых пробок. Артроскопия. 2004 ноя; 20 (9): 981-6.
27. Конрад JM, Stanitski CL. Рассекающий остеохондрит: пересмотр симптома Вильсона. Am J Sports Med.2003 сентябрь-октябрь; 31 (5): 777-8.
28. Kawasaki K, Uchio Y, Adachi N, Iwasa J, Ochi M. Сверление межмыщелковой области для лечения рассекающего остеохондрита коленного сустава. Колено. 2003 Sep; 10 (3): 257-63.
29. Арнольд Калифорния, Томас DJ, Сандерс Дж. Двусторонний рассекающий остеохондрит коленного и двустороннего локтевого суставов. Am J Orthop. 2003 May; 32 (5): 237 40.
30. Louisia S, Beaufils P et al. Трансхондральное сверление при рассекающем остеохондрите медиального мыщелка коленного сустава. Коленная хирургия Sports Traumatol Arthrosc.2003 Jan; 11 (1): 33-39.
31. Лайл М., Кертис С. и др. Восстановление суставного хряща у спортсмена-подростка: является ли имплантация аутологичных хондроцитов ответом? Clin J Sports Med. 2006 16 ноября (6)
32. Линден Б., Телхаг Х. Рассекающий остеохондрит. Acta orthop scand. 1977. 48, 682-686.
33. Мюррей Дж. Р., Читнавис Дж. И др. Рассекающий остеохондрит коленного сустава; следующие долгосрочные клинические исходы. артроскопическая обработка раны. Колено. 2007, 9 января.
34. Миньячи, Тайтерли, Фиксация нестабильных ОКР коленного сустава с помощью костно-хрящевых пробок.Артроскопия 2007; 23 (8): 845-851.
35. Фэрбенкс Х. Рассекающий остеохондрит. JBJS Br. 1933; 21B: 67-82
36. Грин У. Т., Бэнкс, ХХ. Рассекающий остеохондрит у детей. JBJS A. 1953; 35A: 26-47.
37. Петри П.В. Этиология рассекающего остеохондрита: неспособность установить семейную предысторию. JBJSB 1977; 59: 366-367.
38. Брэдли Дж., Денди ди-джей. Результаты бурения рассекающего остеохондрита до созревания скелета. JBJS Br 1989; 71B: 642-44.
39. Кэхилл Б. Р., Филлипс М. Р., Наварро Р.Результаты консервативного лечения рассекающего ювенильного остеохондрита с использованием совместной сцинтиграфии: проспективное исследование. Am J Sports Med 1989; 17: 601-606.
40. Clanton TO, DeLee JC. Рассекающий остеохондрит: история, патофизиология и современные концепции лечения. Clin Orthop Relat Res 1982; 167: 50-64
41. Glancy GL. Рассекающий ювенильный остеохонрит. Am J Knee Surg 1999; 12: 120-124.
42. Грин У.Т., Бэнкс ХХ. Рассекающий остеохондрит у детей. JBJS A 1953; 35A: 26-47.
43.Хефти Ф., Бегуристейн Дж., Крауспе Р. и др. Рассекающий остеохондрит: многоцентровое исследование Европейского педиатрического ортопедического общества. J Pediatr Orthop B 1999; 8: 231-245.
44. Кочер М.С., Мичели Л.Дж., Янив М. и др. Функциональные и рентгенологические результаты рассекающего ювенильного остеохондрита коленного сустава, леченного трансартикулярным артроскопическим сверлением. Am J Sports Med 2001; 29: 562-566.
45. Ribbing S. Наследственное множественное эпифизарное нарушение и его последствия для этиогенеза местных малаций, особенно рассекающего остеохондроза.Acta Orthop Scand 1955; 24: 286-299.
46. Брэдли Дж, Денди ди-джей. Результаты бурения рассекающего остеохондрита до созревания скелета. JBJS Br. 1989; 71B: 642-644.
47. Aglietti P, Buzzi R, Bassi PB, et al. Артроскопическое сверление при рассекающем ювенильном остеохондрите медиального мыщелка бедренной кости. Артроскопия 1994; 10: 286-291.
48. Кочер М.С., Мичели Л.Дж., Янив М. и др. Функциональные и рентгенологические результаты рассекающего ювенильного остеохондрита коленного сустава, леченного трансартикулярным артроскопическим сверлением.Am J Sports Med 2001; 29: 562-566.
49. ДеСмет А.А., Илахи О.А., Граф Б.К. Нелеченный рассекающий остеохонрит мыщелков бедренной кости: прогнозирование исхода для пациента с использованием результатов рентгенографии и МРТ. Skeletal Radiol 26: 463-467, 1997.
50. Mubarak SJ, Carroll NC. Семейный рассекающий остеохондрит коленного сустава. Clin Orthop Relat Res. 1979 May; (140): 131-6.
51. Wall EJ, Vourazeris J, Myer GD, Emergy KH, Divine JF, Nick TG, Hewett TE. Исцеляющий потенциал стабильного ювенильного остеохондрита рассекает поражения коленных суставов.JBJS A. 2008 декабрь; 90 (12): 2655-64.
52. Bohndorf K. Рассекающий остеохондрит (остеохондроз): обзор и новая классификация МРТ. Eur Radiol. 1998; : 103-112.
53. Smillie I: Лечение рассекающего остеохондрита. J Bone Joint Surg Br 39: 248-260, 1957.
54. Микели Л., Кертис С., Шервин, Н., Восстановление суставного хряща у спортсмена-подростка: ответом ли является имплантация аутологичных хондроцитов? Clin J Sport Med 16: 465-470.
[/ toggle]
Рассекающий остеохондрит (ОКР) | Upstate Vet
Обзор
Сухой остеохондрит (ОКР) — это наследственное заболевание суставов, которое возникает у некоторых собак на ранней стадии развития.На конце каждой кости находится слой хряща, называемый суставным хрящом. Этот хрящ обеспечивает важную подушку в каждом суставе. ОКР характеризуется развитием трещин в суставном хряще. Из этих трещин часто развиваются свободные лоскуты или фрагменты хряща. Эти свободные лоскуты вызывают воспаление сустава, что приводит к боли и хромоте. Тело будет пытаться компенсировать поврежденный хрящ за счет образования рубцовой ткани или добавления кости вокруг сустава. Эти вторичные изменения называются дегенеративным заболеванием суставов или остеоартритом.
Заболевание чаще встречается у крупных и гигантских пород, таких как лабрадор ретривер, ротвейлер и ньюфаундленд. Некоторые другие крупные породы (например, доберман-пинчер, колли, сибирский хаски) имеют низкую заболеваемость ОКР. ОКР чаще всего встречается в плечевых, локтевых, коленных (коленных) и голеностопных (скакательных) суставах.
Несколько генов от обоих родителей в сочетании с другими факторами определяют, развивается ли у животного ОКР. Какие гены задействованы и как именно возникает ОКР, неизвестно.Питание — наиболее понятный фактор риска. Диета с высоким содержанием кальция увеличивает риск ОКР. Высококалорийные диеты и быстрое увеличение веса в любом возрасте также могут способствовать развитию болезни.
Хромота обычно развивается в возрасте от 4 до 10 месяцев, но иногда может проявляться позже. Степень хромоты может варьироваться от легкой до тяжелой.
Пациентам с ОКР можно вести консервативное или хирургическое лечение. Консервативное лечение часто используется для пожилых собак, особенно со значительными вторичными дегенеративными заболеваниями суставов.Он включает в себя отдых питомца в течение 4-8 недель, а также прием нестероидных противовоспалительных препаратов (НПВП) и пищевых добавок. НПВП уменьшат боль и воспаление; тем не менее, пациенты, получающие эти препараты, должны находиться под тщательным наблюдением за побочными эффектами. Пищевые добавки, предлагаемые для лечения ОКР, называются хондрозащитными средствами и состоят из экстрактов компонентов, необходимых для развития хрящевой ткани.
Хирургия
У молодых собак хирургическое вмешательство часто рекомендуется на ранней стадии заболевания, до развития значительных вторичных дегенеративных изменений.При хирургическом вмешательстве любой рыхлый или поврежденный хрящ удаляется. Хирургическое вмешательство может быть выполнено традиционным или артроскопическим способом. Решение о проведении открытой операции по сравнению с артроскопией принимается индивидуально.
После ухода
Первые 2–4 недели после операции животное должно находиться в покое. Следует контролировать разрез на наличие признаков инфекции, таких как покраснение, отек, жар или боль, в течение 2 недель. Если пациент чрезмерно активен, на месте разреза может образоваться скопление жидкости (серома).Серомы обычно проходят через несколько недель.
Сразу после операции может потребоваться обезболивающее. У старых животных контроль веса важен для уменьшения нагрузки на сустав.
Выздоровление зависит от размера и местоположения поражения, степени эрозии хрящевого ложа, а также от общего состояния здоровья и диеты животного. В течение 8–12 недель большинство животных достигают нормального функционирования.
Прогноз ОКР плеча от хорошего до отличного, функция полностью восстановлена после операции.
Прогноз ОКР в локтевом, коленном и скакательном суставах от умеренного до осторожного в зависимости от размера поражения, тяжести дегенеративного заболевания суставов и возраста животного. При прогрессировании дегенеративного заболевания суставов может возникнуть хромота через несколько месяцев или лет после операции.
(PDF) Рассекающий остеохондрит Гистологические исследования коленного сустава имеют различные результаты и теории этиологии
НЕПРАВИЛЬНОЕ ДОКАЗАТЕЛЬСТВО
52
53 Введение
54 Рассекающий остеохондрит (ОКР) — это заболевание сустава, которое может вызывать прогрессирующие изменения
субхондральная
56 кость и связанный с ней суставной хрящ, включая размягчение,
57 опухоль, раннее расслоение, частичное отслоение или полное
58 костно-хрящевое разделение с рыхлым телом.В 1840 г. Pare
´
59 впервые описал удаление рыхлых тел из суставов,
60, предположительно, из костно-хрящевых поражений [18,23]. Это состояние
61 было описано как «тихий некроз» сэром Джеймсом
62 Пэджетом в 1870 году [17] и позже названо «остеохондритом
63 рассекающего» Ко
Йнига в 1888 году, который предположил, что
64 воспалительная реакция в кости и суставном хряще
65 вызывала спонтанный некроз [11].
66 Были предложены другие причины ОКР, в том числе
67 генетическая предрасположенность, ишемия и повторяющиеся или острые
68 травмы. В нескольких отчетах были идентифицированы пациенты с ОКР
69 внутри семей и среди нескольких поколений, хотя
70 многие из этих отчетов были в семьях с карликовыми или
71 низкорослыми [1,12,19,26,27].
72 ишемия также была предложена как причина ОКР [3,5,14], хотя неясно, является ли
73 первичной причиной, вторичным эффектом травмы или
74 другой патофизиологией.Теория Фэрбэнка [6],
75, которую позже отстаивал Смилли [24], заключалась в том, что повторяющиеся
76 микротравмы вызывают ОКР коленного сустава. Травма, острая
77 или повторяющаяся микротравма, стала более общепринятой
78 причиной ОКР в результате высокой распространенности этого
79 расстройства среди спортсменов [2,4,6,7,10, 13,14,16,
80 28]. Несмотря на текущий консенсус, этиология ОКР
81 остается неизвестной и может быть многофакторной.
82 Целью этого исследования было выполнить обзор
83 текущей литературы по гистологическому и / или иммуно-
84 химическому анализу ОКР поражений колена до
85 определить, дают ли патологические изменения представление о
86 прогрессирования или этиологии этого состояния. Более конкретно
87 фокус этого обзора состоял в том, чтобы ответить на три вопроса —
88 вопросов: (1) Является ли остеонекроз постоянным обнаружением в биоптатах OCD
89? (2) Соответствует ли нормальный суставной хрящ
90 образцам биопсии ОКР? (3) Предлагает ли
91 гистологическое исследование этиологию ОКР на основе данных тканей
92?
93 Стратегия и критерии поиска
94 Для выявления исследований по гистологическому анализу поражений ОКР
95 в колене, двое из нас (KGS, JCJ) выполнили следующий поиск
96 в декабре 2011 года после консультации с исследованием
97 стратег (MM): (гистология ИЛИ гистология ИЛИ гистол * ИЛИ
98 биопсия ИЛИ биопсия) И (рассекающий остеохондрит ИЛИ
99 остеохондроз) (рис.1). Поиск проводился в базах данных
100 Medline (1946-2011), Embase (1947-2011) и CINAHL
101 (1982-2011). Мы оценили исходные ссылки
102
, полученные в результате упомянутых поисков, на предмет критериев включения
103
путем просмотра заголовка статьи и / или аннотации. Поиск по
104
в литературе выявил 1282 исходных ссылки в MED-
105
LINE, 230 в EMBASE и 48 в CINAHL.
106
Мы включили все исследования поражений ОКР около колена
107
, опубликованные на английском языке, в которых использовался гистологический анализ
108
субхондральной кости и связанного с ней суставного хряща.
109
Этот анализ может включать иммунохимию или морфологию
110
, если сообщается. Исторически сложилось так, что другие термины были
111
, связанные с ОКР, включая костно-хрящевые переломы,
112
остеонекроз и костно-хрящевые фрагменты [23].Мы пропустили эти поисковые запросы
113
, потому что предположили, что они
114
с меньшей вероятностью отражают текущее определение
115
OCD. Мы исключили исследования, которые оценивали только суставной хрящ
116
без дополнительного анализа кости или сообщали только о
117
последующем лечении ОКР (т.е. имплантации аутологичного хряща
118
). Исследования не были исключены на основании возраста
119
субъектов или тяжести поражения ОКР.С помощью этих критериев включения / исключения
120
мы идентифицировали 12 статей для
121
, из которых мы получили полные тексты; Затем мы выполнили полнотекстовые обзоры
122
, чтобы убедиться, что статьи соответствуют критериям включения.
123
Двое из нас (сом, JCJ) независимо оценили все заголовки,
124
аннотации и полнотекстовые обзоры. Из этих 12 статей была исключена одна
125
, которая не соответствовала критериям включения.Мы
126
оценили методологии исследования для гистологической оценки
127
, и результаты и выводы исследований были сравнены с
128
. После удаления дубликатов все авторы были в соглашении
129
по 11 исследованиям, которые отвечали критериям включения
130
.
131
11 публикаций были рассмотрены на предмет источника образца
132
, будь то свободный фрагмент ОКР, лежащая кость под
133
или оба.Мы классифицировали образцы, которые возникли
134
из фрагмента ОКР как потомство костной / хрящевой ткани.
135
Образцы из подлежащей кости были классифицированы как
136
родительской кости (рис. 2).
137
В исследованиях, включенных в этот обзор, использовались различные методологии
138
для гистологического и иммуногистохимического
139
анализов. В некоторых исследованиях не сообщалось об их фиксации и /
140
или протоколах декальцификации (если использовались) [3,8–10,16,30,31].
141
Некоторые использовали только микрофотографии (без окрашивания) [3,8,
142
9] и использовали несколько различных гистологических методов.
143
Для фиксации образцов ОКР использовались четыре стандартных агента
144
с различными концентрациями и / или другие химические вещества
145
(Таблица 1). Из 11 исследований в четырех использовался формалин
146
(различных концентраций) [10,14,28,31], в одном исследовании
147
использовался 10% формальдегид [4] или спирт [20], а в четырех
148
не сообщал об агенте фиксации [3,8,9,30].Декальцификация
149
агентов, использованных в разных исследованиях, варьировались: в одном исследовании использовалась 5%
150
азотная кислота и 70% спирт [4], в одном исследовании использовался 40% муравьин
151
кислота и 20% цитрат натрия.
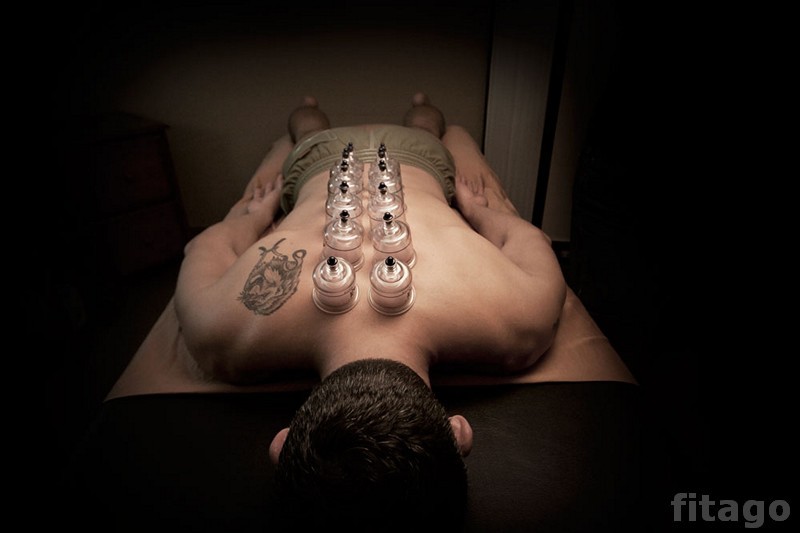
 Это можно наблюдать в виде покраснения кожи.
Это можно наблюдать в виде покраснения кожи.