Артириты | Методжект
Ревматоидный артрит
Ревматоидный артрит (РА) – аутоимунное ревматическое заболевание неизвестной этиологии, характеризующееся хроническим эрозивным артритом(синовитом) и системным воспалительным поражением внутренних органов.
Профилактика.
Этиология РА неизвестна, поэтому первичную профилактику не проводят.
Скрининг.
Скрининг не проводят. Иммунологические нарушения(увеличение титров РФ, АЦЦП и С-РБ) выявляют за несколько месяцев или лет до развития клинических симптомов РА.
Общая характеристика
Характерно разнообразие вариантов начала заболевания. В большинстве случаев заболевание начинается с полиартрита, реже проявления артрита могут быть выражены умеренно, а преобладают артралгии, утренняя скованность в суставах, ухудшение общего состояния, слабость, похудание, субфебрильная температура тела, лимфаденопатия, которые могут предшествовать клинически выраженному поражению суставов.
Развитию артрита за несколько недель или месяцев может предшествовать продромальный период, проявляющийся усталостью, похуданием, периодически возникающими болями в суставах (часто на фоне изменения атмосферного давления), снижением аппетита, повышенной потливостью, субфебрильной температурой тела, умеренной анемией, увеличением СОЭ.
У многих пациентов заболевание дебютирует с неспецифического поражения суставов, и его определяют как недифференцированный артрит (НА). Среди больных НА в течение первого года наблюдения 30-50% развивается достоверный РА. У 40-55%- спонтанная ремиссия, у остальных сохраняется НА или выявляют другое заболевание.
Что происходит в суставах при артрите?
Избыточная стимуляция и нарушение регуляции иммунной системы приводят к избыточной продукции T-клеток
T-клетки проходят в синовий сустава по кровеносным сосудам и выделяют провоспалительные цитокины >запускает каскад реакций в суставах> приводит к развитию воспаления
Синовиальная мембрана начинает пролиферировать и это приводит к избыточной продукции новой жидкости.
Хрящ истончается и это приводит к снижению защиты сустава
Паннус (грануляционная ткань) образуется из синовиальной мембраны
Костная ткань разрушается (эрозии) в областях там, где синовиальная мембрана касается кости (это может быть выявлено при радиографическом обследовании)
В поздних стадиях заболевания полости суставов могут быть полностью заполнены грануляционной тканью
Схема изменения в суставах
Лечение
Цели терапии.
Основная цель терапии – достижение стойкой ремиссии заболевания. Остальные задачи таковы:
- Подавление связанных с воспалением симптомов артрита и внесуставных проявлений.
- Предотвращение деструкции, нарушения функций и деформации суставов.
- Улучшение качества жизни.
- Снижение рисков коморбидных заболеваний.
Лечение больных РА должен проводить ревматолог по следующим причинам:
- Функциональное состояние, находящихся под наблюдением у ревматологов, лучше, чем у курируемых врачом общей практики.
- Применение современных методов фармакотерапии РА требует специальных значений
- Необходимо информирование больных о характере заболевания и побочных эффектах применяемых ЛС
- Используют междисциплинарный подход, основанный на применении нефармакологических и фармакологических методов, привлечение при необходимости специалистов других медицинских специальностей(ортопеда, физиотерапевта, кардиолога, невропатолога, психолога и других)
Медикаментозное лечение.
Для лечение РА используют следующие группы ЛС:
- Ненаркотические анальгетические ЛС-НПВП
- «простые» анальгетики
- ГК
- БПВП и ГИБП
Общие положения
- Для уменьшения болей в суставах назначают НПВП
- НПВП оказывают хороший симпоматический (аналгетический) эффект
- НПВП не влияют на прогрессирование деструкции суставов и прогноз заболевания
- Лечение РА основано на применении БПВП и ГИБП
Терапию БПВП следует начинать как можно раньше (в пределах 3-6 месяцев с момента развития симптомов болезни), даже если пациенты формально не соответствуют диагностическим критериям РА (недифференцированный артрит)
Раннее начало лечение БПВП и ГИБП способствует улучшению функций и замедлению прогрессирования деструкции суставов. Позднее назначение БПВП(через 3-6 месяцев от начала болезни) ассоциируется со снижением эффективности монотерапии БПВП.
Позднее назначение БПВП(через 3-6 месяцев от начала болезни) ассоциируется со снижением эффективности монотерапии БПВП.
Нестероидные противовоспалительные препараты
В зависимости от селективности в отношении ЦОГ-2 НПВП разделяют на две категории – неселективные (Н-НПВП) и селективные (С-НПВП). НПВП более эффективно подавляют боль и воспаление, чем парацетамол. При РА НПВП применяют в комбинации с БПВП.
Глюкортикоиды:
Следует использовать ГК не в виде монотерапии, а в комбинации с БПВП.
Базисные противовоспалительные препараты
Терапию БПВП следует проводить всем больным без исключения. Терапия БПВП и ГИБП уменьшает боль и воспаление, улучшает функции и замедляет прогрессирование деструкции суставов.
При выборе терапии БПВП и ГИБП необходимо учитывать длительность заболевания(< 6 месяцев – ранняя стадия;6-24 месяцев – промежуточная стадия; >24 месяца – развернутая стадия), активность воспаления, наличие факторов неблагоприятного прогноза, коморбидность. К факторам риска неблагоприятного прогноза относят высокие титры РФ, увеличение концентрации АЦЦП, увеличение СОЭ и концентрации СРБ, быстрое развитие деструкции в суставах.
Динамическое наблюдение за эффективностью и побочными эффектами лечения БПВП осуществляет врач-ревматолог и ( в виде исключения) врач общей практики, но при консультативной поддержке врача-ревматолога. *
Метотрексат- наиболее эффективный БПВП, основной компонент комбинированной терапии с другими БПВП и ГИБП. По сравнению с другими БПВП обладает наилучшим соотношением эффективность/токсичность.
Монотерапия показана независимо от длительности заболевания, активности и наличия факторов неблагоприятного прогноза. У больных, впервые начавших лечение метотрексатом.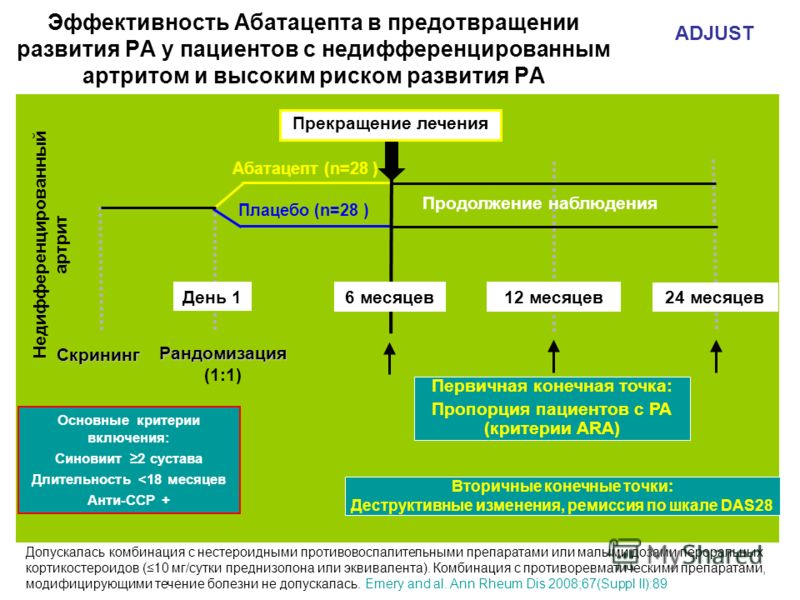 Монотерапия МТ обладает лучшим соотношением эффективность/ токсичность, чем комбинированная терапия МТ и другими БПВП. При неэффективности монотерапии МТ целесообразно проведение комбинированной терапии МТ и БПВП или МТ и ГИБП.
Монотерапия МТ обладает лучшим соотношением эффективность/ токсичность, чем комбинированная терапия МТ и другими БПВП. При неэффективности монотерапии МТ целесообразно проведение комбинированной терапии МТ и БПВП или МТ и ГИБП.
Генно-инженерные биологические препараты (ГИБП)
Это группа лекарственных средств, характеризующихся селективным действием на определенные механизмы развития хронического воспаления и представляющая собой моноклональные антитела к иммунокомпетентным клеткам или провоспалительным цитокинам, гибридные белковые молекулы, ингибирующие активность цитокинов и взаимодействие иммунокомпетентных клеток. В настоящее время зарегистрированы 4 класса ГИБП.
— Ингибиторы ФНО-α: инфликсимаб, адалимумаб, этанерцепт, цертолизумаб пегол, голимумаб
— Анти-В-клеточные препараты: ритуксимаб
— Ингибиторы рецепторов ИЛ-6: тоцилизумаб
— Блокаторы костимуляции Т-лимфоцитов: абатацепт
*Клинические рекомендации. Ревматология, 2-е издание, исправленное и дополненное. Под ред. акад. РАМН Е.Л.Насонова
Возможно ли предотвратить прогрессирование ревматоидного артрита у впервые заболевших?
1. Насонов Е.Л. Почему необходима ранняя диагностика и лечение ревматоидного артрита? // РМЖ. 2002. Т. 10. № 22. С. 1009–1101.
2. Насонов Е.Л. Ревматоидный артрит как общемедицинская проблема // Терапевтич. архив. 2004. Т. 76. № 5. С. 5–7.
3. Каратеев Д.Е., Лучихина Е.Л., Тогизбаев Г. Современные принципы ведения больных ранним артритом // РМЖ. 2008. Т. 16. № 24. С. 1610–1614.
4. Arnett F.C., Edworthy S.M., Bloch D.A. et al. The american rheumatism association 1987 revised criteria for the classification of rheumatoid arthritis // Arthritis Rheum. Vol. 31. 1988. № 3. P. 315–324.
5. Aletaha D., Neogi T., Silman A.J. et al. 2010 Rheumatoid arthritis classification criteria: an American College of Rheumatology/European League Against Rheumatism collaborative initiative // Ann. Rheum. Dis. Vol. 69. 2010. № 9. P. 1580–1588.
Aletaha D., Neogi T., Silman A.J. et al. 2010 Rheumatoid arthritis classification criteria: an American College of Rheumatology/European League Against Rheumatism collaborative initiative // Ann. Rheum. Dis. Vol. 69. 2010. № 9. P. 1580–1588.
6. Hülsemann J.L., Zeidler H. Undifferentiated arthritis in an early synovitis out-patient clinic // Clin. Exp. Rheumatol. Vol. 13. 1995. № 1. P. 37–43.
8. Jansen L.M.A., van Schaardenburg D., van der Horst-Bruinsma I.E., Dijkmans B.A.C. One year outcome of undifferentiated polyarthritis // Ann. Rheum. Dis. Vol. 61. 2002. № 8. P. 700–703.
9. Каратеев Д.Е., Лучихина Е.Л., Тюрина Л.Н. и др. Возможности ранней диагностики ревматоидного артрита в клинической практике на современном этапе (результаты наблюдений за московской когортой больных ранним артритом в рамках программы РАДИКАЛ) // Терапевтич. архив. 2008. Т. 80. № 5. С. 8–13.
10. Quinn M.A., Green M.J., Marzo-Ortega H., Proudman S., Karim Z., Wakefield R.J., Conaghan P.G., Emery P. Prognostic factors in a large cohort of patients with early undifferentiated inflammatory arthritis after application of a structured management protocol // Arthritis Rheum. Vol. 48. 2003. № 11. P. 3039–3045.
11. Van Aken J., van Bilsen J.H.M., Allaart C.F., Huizinga T.W.J., Breedveld F.C. The Leiden Early Arthritis Clinic // Clin. Exp. Rheumatol. 2003. Vol. 21. № 5. Suppl. 31. P. 100–105.
12. Van der Helm-van Mil A.H., le Cessie S., van Dongen H., Breedveld F.C., Toes R.E.M., Huizinga T.W.J. A prediction rule for disease outcome in patients with recent-onset undifferentiated arthritis: how to guide individual treatment decisions // Arthritis Rheum. Vol. 56. 2007. № 2. P. 433–440.
Van der Helm-van Mil A.H., le Cessie S., van Dongen H., Breedveld F.C., Toes R.E.M., Huizinga T.W.J. A prediction rule for disease outcome in patients with recent-onset undifferentiated arthritis: how to guide individual treatment decisions // Arthritis Rheum. Vol. 56. 2007. № 2. P. 433–440.
13. Каратеев Д.Е., Лучихина Е.Л. Ранняя диагностика ревматоидного артрита: проблемы и решения // Росс. мед. вести. 2007. № 4. С. 24–27.
14. Firestein G.S. Evolving concepts of rheumatoid arthritis // Nature. 2003. Vol. 423. № 6937. P. 356–361.
15. Dixon W.G., Symmons D.P.M. Does early rheumatoid arthritis exist? // Best Pract. Res. Clin. Rheumatol. Vol. 19. 2005. № 1. P. 37–53.
16. Александрова Е.Н., Чемерис Н.А., Каратеев Д.Е. и др. Антитела к циклическому цитруллинированному пептиду при ревматоидном артрите // Терапевтич. архив. 2004. Т. 76. № 12. С. 64–68.
17. Avouac J., Gossec L., Dougados M. Diagnostic and predictive value of anti-cyclic citrullinated protein antibodies in rheumatoid arthritis: a systematic literature review // Ann. Rheum. Dis. Vol. 65. 2006. № 7. P. 845–851.
18. Svärd A., Kastbom A., Reckner-Olsson A., Skogh T. Presence and utility of IgA-class antibodies to cyclic citrullinated peptides in early rheumatoid arthritis: the Swedish TIRA project // Arthritis Res. Ther. Vol. 10. 2008. № 4. R75.
19. Каратеев Д.Е., Александрова Е.Н., Демидова Н.В. и др. Антицитруллиновые антитела и данные магнито-резонансной томографии суставов кисти у больных ранним артритом // Терапевтич. архив. 2008. Т. 80. № 10. С. 72–77.
20. Van der Helm-van Mil A.H., Detert J., le Cessie S., Filer A., Bastian H., Burmester G.R., Huizinga T.W.J., Raza K. Validation of a prediction rule for disease outcome in patients with recent-onset undifferentiated arthritis: moving toward individualized treatment decision-making // Arthritis Rheum. Vol. 58. 2008. № 8. P. 2241–2247.
Van der Helm-van Mil A.H., Detert J., le Cessie S., Filer A., Bastian H., Burmester G.R., Huizinga T.W.J., Raza K. Validation of a prediction rule for disease outcome in patients with recent-onset undifferentiated arthritis: moving toward individualized treatment decision-making // Arthritis Rheum. Vol. 58. 2008. № 8. P. 2241–2247.
21. Лучихина Е.Л., Каратеев Д.Е., Новиков А.А., Насонов Е.Л. Прогнозирование развития ревматоидного артрита у больных с ранним недифференцированным артритом // Научно-практич. ревматол. 2009. № 2. С. 31–37.
22. Combe B., Landewe R., Lukas C., Bolosiu H.D., Breedveld F., Dougados M., Emery P., Ferraccioli G., Hazes J.M.W., Klareskog L., Machold K., Martin-Mola E., Nielsen H., Silman A., Smolen J., Yazici H. EULAR recommendations for the management of early arthritis: report of a task force of the European Standing Committee for International Clinical Studies Including Therapeutics (ESCISIT) // Ann. Rheum. Dis. Vol. 66. 2007. № 1. P. 34–45.
23. Каратеев А.Е., Каратеев Д.Е., Лучихина Е.Л. и др. Эффективность и безопасность монотерапии высокими дозами НПВП при раннем артрите (открытое рандомизированное контролируемое 4-недельное исследование эффективности высоких и среднетерапевтических доз нимесулида и диклофенака при раннем артрите) // РМЖ. 2006. Т. 14. № 25. С. 1805–1809.
24. Machold K.P., Landewé R., Smolen J.S., Stamm T.A., van der Heijde D.M., Verpoort K.N., Brickmann K., Vázquez-Mellado J., Karateev D.E., Breedveld F.C., Emery P., Huizinga T.W.J. Extended report: The Stop Arthritis Very Early (SAVE) trial, an international multicentre, randomised, double-blind, placebo-controlled trial on glucocorticoids in very early arthritis // Ann. Rheum. Dis. Vol. 69. 2010. № 3. P. 495–502.
25. Ревматология. Клинические рекомендации / Под ред. Е.Л. Насонова. М.: ГЭОТАР-Медиа, 2006.
Ревматология. Клинические рекомендации / Под ред. Е.Л. Насонова. М.: ГЭОТАР-Медиа, 2006.
26. Каратеев Д.Е., Олюнин Ю.А. О классификации ревматоидного артрита // Научно-практич. ревматол. 2008. № 1. С. 5–16.
27. Van Dongen H., van Aken J., Lard L.R., Visser K., Ronday H.K., Hulsmans H.M.J., Speyer I., Westedt M.-L., Peeters A.J., Allaart C.F., Toes R.E.M., Breedveld F.C., Huizinga T.W.J. Efficacy of methotrexate treatment in patients with probable rheumatoid arthritis: a double-blind, randomized, placebo-controlled trial // Arthritis Rheum. Vol. 56. 2007. № 5. P. 1424–1432.
28. Saleem B., Mackie S., Quinn M., S Nizam, Hensor E., Jarrett S., Conaghan P.G., Emery P. Does the use of tumour necrosis factor antagonist therapy in poor prognosis, undifferentiated arthritis prevent progression to rheumatoid arthritis? // Ann. Rheum. Dis. Vol. 67. 2008. № 8. P. 1178–1180.
29. Emery P., Durez P., Dougados M., Legerton C.W., Becker J.-C., Vratsanos G., Genant H.K., Peterfy C., Mitra P., Overfield S., Qi K., Westhovens R. Extended report: Impact of T-cell costimulation modulation in patients with undifferentiated inflammatory arthritis or very early rheumatoid arthritis: a clinical and imaging study of abatacept (the ADJUST trial) // Ann. Rheum. Dis. Vol. 69. 2010. № 3. P. 510–516.
Лечение недифференцированного артрита в Константиновых Лазнях, Чехия
Недифференцированным называют такой вид артрита, который нельзя отнести к другим известным видам артрита. Данное состояние обычно считается начальной стадией развития ревматического заболевания. Симптомы стандартны для артритов: суставная боль, усиливающаяся во время движения, скованность и ограниченность движений, при длительном течении появляется отечность, сустав деформируется. Лечение направлено на купирование болевого синдрома, остановку разрушения и деформации сустава, ликвидацию воспалительного процесса.
Лечение направлено на купирование болевого синдрома, остановку разрушения и деформации сустава, ликвидацию воспалительного процесса.
Лучшие санатории в Константиновых Лазнях по качеству лечения
Спа-отель Lowenstein
4*От 70 € за 1 ночь 3-х разовое питание с лечением
9,2/10 Посмотреть видеоСанаторий Prusik
3*От 70 € за 1 ночь 3-х разовое питание с лечением
8,4/10Спа-отель Jirasek
3*От 66 € за 1 ночь 3-х разовое питание с лечением
7,4/10Спа-отель Palacky
3*От 62 € за 1 ночь 3-х разовое питание с лечением
7,5/10Спа-отель Manes
3* 7,5/10Спа-отель Purkyne
3*От 62 € за 1 ночь 3-х разовое питание с лечением
6,2/10 Показать все санатории на курорте Константиновы ЛазниСлужба поддержки
Вы не уверены, по каким критериям выбрать курорт или санаторий?
Не знаете как забронировать?
Позвоните нам и сотрудники службы поддержки помогут вам.
Консультация врача
Бесплатная помощь врача-курортолога
Если самостоятельный поиск курорта и санатория, оптимально подходящих для лечения ваших заболеваний, вызывает у вас затруднение,то воспользуйтесь бесплатной консультацией врача-курортолога Елены Хорошевой.
Отправьте свой вопрос здесьКлинические рекомендации Европейской противоревматической лиги по лечению раннего артрита
Представляем Вашему вниманию обновленные рекомендации EULAR по диагностике и лечению раннего артрита, опубликованные в декабре 2016 года.
Рекомендации
- Больные с артритом, у которых отмечается опухание сустава, связанное с болью или скованностью в движении, должны быть проконсультированы врачом-ревматологом в течение 6 недель после появления симптомов.
- Клиническое обследование является основным в выявлении артрита, находки могут быть подтверждены данными ультразвукового обследования.
- В случае раннего недифференцированного артрита, необходимо оценить факторы риска и понять идет ли речь об эрозивной форме заболевания. При этом важно оценить количество пораженных суставов, определить показатели острого воспаления, ревматоидный фактор, антитела к циклическому цитруллиновому пептиду (ACPA) и внимательно изучить данные инструментального обследования.
- У пациентов с высоким риском персистирующего артрита следует начать лечение базисными противоревматическими препаратами как можно раньше (идеально, в первые 3 месяца), даже если симптомы не полностью отвечают диагностическим критериям воспалительных ревматических заболеваний.

- Среди базисных лекарственных препаратов, терапией первой линии считается метотрексат, если на то нет противопоказаний.
- НПВП рассматриваются как эффективные препараты симптоматической терапии, но их следует назначать в минимально эффективной дозе в течение непродолжительного периода, после предварительной оценки гастроэнтерологического, почечного и кардиоваскулярного рисков.
- Системные глюкокортикостероиды эффективны в снижении болевого и отечного симптома, прогрессии заболевания, но в силу частных побочных эффектов должны быть использованы в наименьшей дозе не более 6 месяцев. Внутриартикулярное введение стероидных препаратов эффективно в облегчении локальных воспалительных симптомов.
- Основной целью использования базисных противоревматических препаратов является достижение клинической ремиссии. При этом необходимо регулярно контролировать активность заболевания, проводить мониторинг нежелательных явлений и оценить сопутствующие заболевания, чтобы принять решение о продолжении лечения или о смене препарата.
- Для определения активности заболевания следует проводить подсчет вовлеченных суставов, оценивать функциональный статус, измерять показатели СОЭ и С-реактивного белка. Данные обследования необходимо проводить с промежутком в 1-3 месяца до достижения цели лечения.
- В дополнение к лекарственной терапии больным следует рекомендовать выполнять динамические упражнения.
- Больным нужно рекомендовать отказаться от никотина, контролировать вес, следить за гигиеной полости рта, проходить своевременную вакцинацию. Также важную роль играет лечение сопутствующих заболеваний.
- Очень важно рассказать пациенту о его заболевании, возможных последствиях и методах лечения. Важную роль играют и обучающие программы, в которых специалисты объяснят, как облегчить боль, какие физические упражнения необходимо выполнять.
Источник: Bernard Combe, Robert Landewe, Claire I Daien, et al. Ann Rheum Dis. December 2016./GettyImages-596326788-580690145f9b5805c2774d75.jpg)
Лечение недифференцированного артрита | ACUPUNCTURU.RU
Лечение недифференцированного артрита
Лечение «недифференцированного артрита»
(собственный опыт)
Привели молодого человека 19 лет с диагнозом «недифференцированный артрит». Заболел весной 2013 года, когда на фоне занятий большим теннисом возникли боли в локтевых, а позже и в других суставах тела. При обследовании выявлены изменения, характерные для полимиозита или ревматоидного артрита. Был вынужден прекратить занятия спортом, начать прием преднизолона по 4 таблетки в день (4 × 5 мг). Больному было проведено обследование сердца, поскольку, как известно, «ревматизм лижет суставы, но кусает сердце». Изменений не выявлено. Врачи рекомендовали постепенное снижение дозы преднизолона до возможных пределов, сбрасывая по ¼ таблетки каждую неделю – до тех пор, пока она не станет минимальной, но при этом не будет болей в суставах. Стоит заметить, что прием этого лекарства в данном случае может оказаться пожизненным…
На фоне указанной дозы преднизолона боли в суставах уменьшились, а потом почти прекратились. Но стали проявляться побочные эффекты данного препарата – вырос вес на 5-6 кг, стал отмечать одышку при подъеме на уровень третьего этажа, утомляемость. У больного также изменился внешний вид – появились характерные вздутые щеки.
При обращении в пульсе отмечены характерные изменения – прежде всего на глубоком уровне – признаки патогенной влажности: пульс «стекловидный», уплотненный, плохо движущийся. В лечении применялась тонизация (согревание) селезенки, устранения (высушивание) влажности. Применялись точки да-ду, шан-цю, пи-шу, вэй-шу, шэнь-шу, чжун-вань, ся-вань, шан-вань, да-чжу. Обязательно подключались пары чудесных сосудов: Ян Вэй май – Дай май или Ду май – Ян Цяо май. На фоне лечения признаки влажности в пульсе исчезли.
Больному рекомендовано снижение дозы преднизолона с 2 таблеток, с которыми он пришел, примерно на ½ таблетки каждые три дня. Акупунктура проводилась через день. Примерно на 5 сеансе больной вдруг отметил резкое прекращение болей в суставах, несмотря на снижение дозы преднизолона. К 10-му сеансу осталось ¼ таблетки преднизолона. За время лечения также отметил снижение веса тела на 2-3 кг. Характерная одутловатость щек значительно уменьшилась.
Акупунктура проводилась через день. Примерно на 5 сеансе больной вдруг отметил резкое прекращение болей в суставах, несмотря на снижение дозы преднизолона. К 10-му сеансу осталось ¼ таблетки преднизолона. За время лечения также отметил снижение веса тела на 2-3 кг. Характерная одутловатость щек значительно уменьшилась.
Лечение прекращено.
Спустя примерно 2-3 недели выразил желание придти снова – «на пару сеансов». Отмечает «улучшение качества жизни», которое с его слов проявлено тем, что «жизнь наладилась», смог лучше учиться, то, что раньше давалось с трудом, теперь происходит с меньшими усилиями. Преднизолон больше не принимает. Хорошо переносит физическую нагрузку – «хожу целый день – без проблем!». Иногда бывают незначительные боли в локтевых суставах – особенно в правом, с которого начинался процесс (напомним, что эти боли появились на фоне занятий теннисом).
Ниже приводятся некоторые документы данного больного:
3-е ревматологическое отделение — ФГБНУ НИИР им. В.А. Насоновой
3-е ревматологическое отделение
Заведующий отделением
Алексеева Анна Валерьевна
кандидат медицинских наук, врач-ревматолог высшей квалификационной категории
Об отделении
3-е ревматологическое отделение осуществляет квалифицированную диагностическую и лечебную помощь пациентам с воспалительными заболеваниями суставов.
В отделении развернут стационар на 51 койку, имеются четырехместные палаты, оборудованные душевой кабиной и санузлом, а также одно- и двухместные палаты повышенной комфортности, условия в которых максимально приближены к домашней обстановке (с душевой, санузлом, холодильником и телевизором). Каждая палата оснащена многофункциональными кроватями и звуковой системой экстренного оповещения на круглосуточный пост медицинской сестры.
Приоритетным направлением работы отделения является:
Диагностика и лечение ревматоидного артрита, а также других заболеваний костно-мышечной системы (остеоартрит, серонегативный спондилоартрит, псориатическая артропатия, подагрический артрит), системных заболеваний, протекающих с поражением суставов. Боль и припухлость суставов – это грозные симптомы, нередко являющиеся предвестниками серьезного заболевания. Высокая квалификация специалистов позволяет поставить точный диагноз на самой ранней стадии болезни, чтобы быстро начать патогенетическую терапию и избежать развития суставных деформаций, ведущих к инвалидности.
Отличительной особенностью работы нашего отделения является индивидуальный подход к пациенту и создание уникальной стратегии лечения в каждом отдельном случае с учетом всех особенностей течения болезни и сопутствующей патологии. Наш приоритет — искренняя забота о больных с учетом их интересов.
Совместно с врачами курацию пациентов осуществляют научные сотрудники, что позволяет осуществлять диагностику и лечение на современном и углубленном уровне. Наряду с проверенными временем схемами лечения мы используем инновационные методы терапии, такие как генно-инженерные биологические препараты.
Другой особенностью отделения является командная работа в тандеме с отделением физиотерапии и реабилитации с целью создания разностороннего и наиболее эффективного подхода к лечению ревматических заболеваний. Сотрудниками разрабатывается проект по внедрению санаторно-курортного лечения на амбулаторном этапе наблюдения.
Официальными ценностями сотрудников нашего отделения утверждены профессионализм и ответственность за результат.
Наша миссия – помочь Вам справиться с болезнью и сохранить активный образ жизни!
Вопросы, с которыми к нам чаще всего обращаются:
-
У меня впервые припух(ли) сустав(ы), что с этим делать?
-
Поставлен диагноз «недифференцированный артрит»
-
Мне диагностировали ревматоидный артрит, но нет уверенности в диагнозе
-
Диагноз поставлен, назначенное лечение не помогает
-
Плохо переношу препараты для лечения ревматоидного артрита
-
Развился остеопороз при ревматоидном артрите
-
Диагностировали амилоидоз при ревматоидном артрите
-
«Сухой синдром» (синдром Шегрена) при ревматоидном артрите
-
Врачи подозревают у меня синдром Стилла
-
Прогрессирует деформация суставов, продолжать лечиться препаратами или оперировать….

Специалисты отделения
Демидова Наталья Викторовна
Кандидат медицинских наук, врач-ревматолог высшей квалификационной категории
Касумова Камаля Авязовна
Кандидат медицинских наук, врач-ревматолог высшей квалификационной категории
Муравьёва Наталья Валерьевна
Кандидат медицинских наук, врач-ревматолог
Серикова Галина Владимировна
Врач-ревматолог
Седельникова Мария Андреевна
Врач-ревматолог
Нимесулид при ревматоидном артрите | Лучихина
1. Насонов ЕЛ, Каратеев ДЕ, Чичасова НВ. Рекомендации EULAR по лечению ревматоидного артрита-2013: общая характеристика и дискуссионные проблемы. Научно-практическая ревматология. 2013;51(6):609–20. [Nasonov EL, Karateev DE, Chichasova NV. EULAR recommendations for the treatment of rheumatoid arthritis-2013: general characteristics and disputable problems. Nauchno-prakticheskaya revmatologiya = Rheumatology Science and Practice. 2013;51(6):609–20. (In Russ.)]. DOI: http://dx.doi.org/10.14412/1995-4484-2013-609-22
2. Ziegler S, Huscher D, Karberg K, et al. Trends in treatment and outcomes of rheumatoid arthritis in Germany 1997–2007: results from the National Database of the German Collaborative arthritis Centers. Ann Rheum Dis. 2010 Oct;69(10):1803–8. doi: 10.1136/ard.2009. 122101. Epub 2010 May 6.
122101. Epub 2010 May 6.
3. Crofford LJ. Use of NSAIDs in treating patients with arthritis. Arthritis Res Ther. 2013;15 Suppl 3:S2. doi: 10.1186/ar4174. Epub 2013 Jul 24.
4. Simon LS. Nonsteroidal anti-inflammatory drugs and their risk: a story still in evelopment. Arthritis Res Ther. 2013;15 Suppl 3:S1. doi: 10.1186/ar4173. Epub 2013 Jul 24.
5. Hochberg MC. New directions in symptomatic therapy for patients with osteoarthritis and rheumatoid arthritis. Semin Arthritis Rheum. 2002;15:4–14. doi: 10.1053/sarh.2002.37215.
6. Emery P. Considerations for nonsteroidal anti-inflammatory drug therapy: benefits. Scand J Rheumatol. 1996; 25 (suppl.105):5–12.
7. Kvien TK, Greenwald M, Peloso PM, et al. Do COX-2 inhibitors provide additional pain relief and anti-inflammatory effects in patients with rheumatoid arthritis who are on biological disease-modifying anti-rheumatic drugs and/or corticosteroids? Post-hoc nalyses
8. from a randomized clinical trial with etoricoxib. BMC Musculoskelet Disord. 2015 Feb 13;16(1):26.
9. Moore RA, Derry S, Wiffen PJ, et al. Overview review: comparative efficacy of oral ibuprofen and paracetamol (acetaminophen) across acute and chronic pain condition. Eur J Pain. 2014 Dec 22. doi: 10.1002/ejp.649. Epub ahead of print.
10. Pincus T, Koch G, Lei H, et al. Patient Preference for Placebo, Acetaminophen (paracetamol) or Celecoxib Efficacy Studies (PACES): two randomised, double blind, placebo controlled, crossover clinical trials in patients with knee or hip osteoarthritis. Ann Rheum Dis. 2004 Aug;63(8):931–9. Epub 2004 Apr 13.
Ann Rheum Dis. 2004 Aug;63(8):931–9. Epub 2004 Apr 13.
11. Bjordal J, Klovning A, Ljunggren A, Slшrdal L. Short-term efficacy of harmacotherapeutic interventions in osteoarthritic knee pain: A meta-analysis of randomised placebo-controlled trials. Eur J Pain. 2007 Feb;11(2):125–38. Epub 2006 May 8.
12. Rainsford KD. Anti-inflammatory drugs in the 21st century. Subcell Biochem. 2007;42:3–27.
13. Camu F1, Shi L, Vanlersberghe C. The role of COX-2 inhibitors in pain modulation. Drugs. 2003;63 Suppl 1:1–7.
14. Mehta V, Johnston A, Cheung R, et al. Intravenous parecoxib rapidly leads to COX-2 inhibitory concentration of valdecoxib in the central nervous system. Clin Pharmacol Ther. 2008 Mar;83(3):430–5. Epub 2007 Aug 8.
15. Dembo G, Park SB, Kharasch ED. Central nervous system concentrations of cyclooxygenase-2 inhibitors in humans. Anesthesiology. 2005 Feb;102(2):409–15.
16. Bianchi M, Martucci C, Ferrario P, et al. Increased tumor necrosis factor- and prostaglandin E2 concentrations in the cerebrospinal fluid of rats with inflammatory hyperalgesia: the effects of analgesic drugs. Anesth Analg. 2007 Apr;104(4):949–54.
17. Goldstein JL, Cryer B. Gastrointestinal injury associated with NSAID use: a case study and review of risk factors and preventative strategies. Drug Healthc Patient Saf. 2015 Jan 22;7:31–41. doi: 10.2147/DHPS.S71976. eCollection 2015.
18. Harirforoosh S, Asghar W, Jamali F. Adverse effects of nonsteroidal antiinflammatory drugs: an update of gastrointestinal, cardiovascular and renal complications. J Pharm Pharm Sci. 2013;16(5):821–47.
Harirforoosh S, Asghar W, Jamali F. Adverse effects of nonsteroidal antiinflammatory drugs: an update of gastrointestinal, cardiovascular and renal complications. J Pharm Pharm Sci. 2013;16(5):821–47.
19. Lanas A, Boers M, Nuevo J. Gastrointestinal events in at-risk patients starting non-steroidal anti-inflammatory drugs (NSAIDs) for rheumatic diseases: the EVIDENCE study of European routine practice. Ann Rheum Dis. 2015 Apr;74(4):675–81. doi: 10.1136/annrheumdis-2013-204155. Epub 2013 Dec 18.
20. Burmester G, Lanas A, Biasucci L, et al. The appropriate use of non-steroidal ntiinflammatory drugs in rheumatic disease: opinions of a multidisciplinary European expert panel. Ann Rheum Dis. 2011 May;70(5):818–22. doi: 10.1136/ard.2010. 128660. Epub 2010 Sep 10.
21. Cannon C, Curtis S, FitzGerald G, et al. Cardiovascular outcomes with etoricoxib and diclofenac in patients with osteoarthritis and rheumatoid arthritis in the Multinational Etoricoxib and Diclofenac Arthritis Longterm (MEDAL) programme: a randomised comparison. Lancet. 2006 Nov 18;368(9549):1771–81.
22. Lindhardsen J, Gislason GH, Jacobsen S, et al. Non-steroidal anti-inflammatory drugs and risk of cardiovascular disease in patients with rheumatoid arthritis: a nationwide cohort study. Ann Rheum Dis. 2013 Jun 8. Epub ahead of print.
23. Goodson NJ, Brookhart AM, Symmons DP, et al. Non-steroidal antiinflammatory drug use does not appear to be associated with increased cardiovascular mortality in patients with inflammatory polyarthritis: results from a primary care based inception cohort of patients. Ann Rheum Dis. 2009 Mar;68(3):367–72.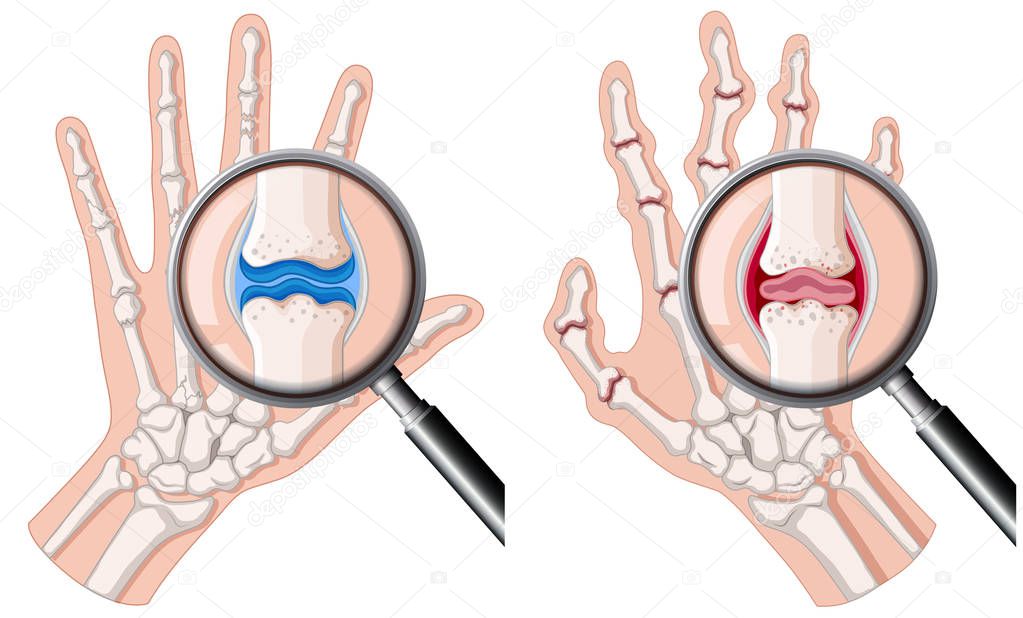 doi: 10.1136/ard.2007.076760. Epub 2008 Apr 13.
doi: 10.1136/ard.2007.076760. Epub 2008 Apr 13.
24. Franklin J, Farragher TM, Lunt M, et al. Excess risk of hospital admission for ardiovascular disease within the first 7 years from onset of inflammatory polyarthritis. Ann Rheum Dis. 2010 Sep;69(9):1660–4. doi: 10.1136/ard.2009.121871. Epub 2010 May 24.
25. Насонов ЕЛ. Эффективность и переносимость нестероидного противовоспалительного препарата. Нимесулид: новые данные. Русский Медицинский Журнал. 2001;(15):6–8. [Nasonov EL. The efficacy and tolerability of a nonsteroidal anti-inflammatory drug. Nimesulide: new data. Russkii Meditsinskii Zhurnal. 2001;(15):6–8. (In Russ.)].
26. Балабанова РМ., Белов БС, Чичасова НВ и др. Эффективность нимесулида при ревматоидном артрите. Фарматека. 2004;(7):55–8. [Balabanova RM., Belov BS, Chichasova NV, et al. The efficacy of nimesulide in rheumatoid arthritis. Farmateka. 2004;(7):55–8. (In Russ.)].
27. Rainsford KD; Members of the Consensus Report Group on Nimesulide. Nimesulide – a multifactorial approach to inflammation and pain: scientific and clinical consensus. Curr Med Res Opin. 2006 Jun;22(6):1161–70.
28. Bennett A. Nimesulide a well established cyclooxygenase-2 inhibitor with many other pharmacological properties relevant to inflammatory diseases. In: Therapeutic Roles of Selective COX-2 Inhibitors. Vein JR, Botting RM, editors. William Harvey Press: 524–40.
29. Pelletier JP, Mineau F, Fernandes J, et al. Two NSAIDs, nimesulide and naproxen, can reduce the synthesis of urokinase and IL-6 while increasing PAI-1, in human OA synovial fibroblasts. Clin Exp Rheumatol. 1997 Jul-Aug;15(4):393–8.
Clin Exp Rheumatol. 1997 Jul-Aug;15(4):393–8.
30. Barracchini A, Franceschini N, Amicosante G, et al. Can non-steroidal antiinflammatory drugs act as metalloproteinase modulators? An in vitro study of inhibition of collagenase activity. J Pharm Pharmacol. 1998 Dec;50(12):1417–23.
31. Wober W. Comparative efficacy and safety of nimesulide and diclofenac in patients with acute shoulder, and a meta-analysis of controlled studies with nimesulide. Rheumatology (Oxford). 1999 May;38 Suppl 1:33–8.
32. Pohjolainen T, Jekunen A, Autio L, Vuorela H. Treatment of acute low back pain with the COX-2-selective anti-inflammatory drug nimesulide: results of a randomized, double-blind comparative trial versus ibuprofen. Spine (Phila Pa 1976). 2000 Jun 15;25(12):1579–85.
33. Барскова ВГ, Якунина ИА, Насонова ВА. Применение нимесила при подагрическом артрите. Терапевтический архив. 2003;(5):60–4. [Barskova VG, Yakunina IA, Nasonova VA. The use of Nimesil in gouty arthritis. Terapevticheskii arkhiv. 2003;(5):60–4. (In Russ.)].
34. Каратеев АЕ, Каратеев ДЕ, учихина ЕЛ и др. Эффективность и безопасность монотерапии высокими дозами НПВП при раннем артрите. Русский Медицинский Журнал. 2006;(16):24–9. [Karateev AE, Karateev DE, Luchikhina EL, et al. The efficacy and safety of monotherapy with high doses of NSAIDs in early arthritis. Russkii Meditsinskii Zhurnal. 2006;(16):24–9. (In Russ.)].
35. Bradbury F. How important is the role of the physician in the correct use of a drug? An observational cohort study in general practice. Int J Clin Pract Suppl. 2004 Oct;(144):27–32.
36. Conforti A, Leone R, Moretti U, et al. Adverse drug reactions related to the use of NSAIDs with a focus on nimesulide: results of spontaneous reporting from a Northern Italian area. Drug Saf. 2001;24(14):1081–90.
37. Laporte JR, Ibanez L, Vidal X, et al. Upper gastrointestinal bleeding associated with the use of NSAIDs: newer versus older agents. Drug Saf. 2004;27(6):411–20.
38. Минушкин ОН. Использование препарата «Найз» у больных, страдающих сочетанной патологией суставов и поражением верхних отделов желудочно-кишечного тракта. Научо-практическая ревматология. 2003;(5):72–6. [Minushkin ON. The use Nise in patients with combined pathology of the joints and lesions of the upper gastrointestinal tract. Naucho-prakticheskaya revmatologiya = Rheumatology Science and Practice. 2003;(5):72–6. (In Russ.)].
39. Каратеев АE, Каратеев ДE, Насонов ЕЛ. Гастродуоденальная переносимость нимесулида (НИМЕСИЛ, BerlinChemie) у больных с язвенным анамнезом: первое проспективное исследование безопасности селективных ЦОГ-2-ингибиторов у больных с высоким риском развития НПВП-индуцированных гастропатий. Научно-практическая ревматология. 2003;(1):45-8. [Karateev AE, Karateev DE, Nasonov EL. Gastroduodenal safety of Nimesulid (Nimesil, Berlin Chemie) in rheumatic patients with history of ulcer. Nauchnoprakticheskaya revmatologiya = Rheumatology Science and Practice. 2003;(1):45–8. (In Russ.)]. DOI: http://dx.doi.org/10.14412/1995-4484-2003-1132
40. Helin-Salmivaara A, Virtanen A, Veslainen R, et al. NSAID use and the risk of hospitalisation for first myocardial infarction in the general population: a national asecontrol study from Finland. Eur Heart J. 2006 Jul;27(14):1657–63. Epub 2006 May 26.
41. Барскова ВГ, Насонова ВА, Цапина ТН и др. Эффективность и безопасность применения нимесила у больных с подагрическим артритом. Клиническая медицина. 2004;82(12):49–54. [Barskova VG, Nasonova VA, Tsapina T, et al. The efficacy and safety of Nimesil in patients with gouty arthritis. Klinicheskaya meditsina. 2004;82(12):49–54. (In Russ.)].
42. Lü cker PW, Pawlowski C, Friedrich I, et al. Double-blind, randomised, multi-centre clinical study evaluating the efficacy and tolerability of nimesulide in comparison with etodalac in patients suffering from osteoarthritis of the knee. Eur J Rheumatol Inflamm. 1994;14(2):29–38.
43. Huskisson E, Macciocchi A, Rahlfs V, et al. Nimesulide versus diclofenac in the treatment of osteoarthritis of the hip or knee: an active controlled equivalence study. Curr Ther Res. 1999;60:253–65.
44. Kriegel W, Korff KJ, Ehrlich JC, et al. Double-blind study comparing the long-term efficacy of the COX-2 inhibitor nimesulide and naproxen in patients with osteoarthritis. Int J Clin Pract. 2001 Oct;55(8):510–4.
45. Каратеев АЕ. Российский опыт применения нимесулида: обзор клинических испытаний. Consilium medicum. 2011;13(9):89–95. [Karateev AE. Russian experience of nimesulide: an overview of clinical trials. Consilium medicum. 2011;13(9):89–95. (In Russ.)].
46. Каратеев АЕ, Алексеева ЛИ, Братыгина ЕА, Аширова ТБ. Оценка частоты развития побочных эффектов при длительном применении нимесулида в реальной клинической практике. Русский Медицинский Журнал. 2009;17(21):1466–72. [Karateev E, Alekseeva LI, Bratygina EA, Ashirova TB. The frequency of side effects with long-term use of nimesulide in real clinical practice. Russkii Meditsinskii Zhurnal. 2009;17(21):1466–72. (In Russ.)].
47. Каратеев АЕ. Сравнительная оценка влияния нимесулида на верхние отделы желудочно-кишечного тракта. Лечащий врач. 2014;(7):51–5. [Karateev AE. Comparative evaluation of the effect of nimesulide on the upper gastrointestinal tract. Lechashchii vrach. 2014;(7):51–5. (In Russ.)].
48. Boelsterli UA. Nimesulide and hepatic adverse affects: roles of reactive metabolites and host factors. Int J Clin Pract Suppl. 2002 Jul;(128):30–6.
49. Boelsterli UA. Mechanisms of NSAIDinduced hepatotoxicity: focus on nimesulide. Drug Saf. 2002;25(9):633–48.
50. Assessment report for Nimesulide containing medicinal products for systemic use. 20 January 2012 EMA/73856/2012 На сайте: http://www.ema.europa.eu
51. Irish Board Suspends Marketing of Drugs Containing Nimesulide http://www.imb.ie.
52. Press release. European Medicines Agency recommends restricted use of nimesulid- containing medicinal products. Doc. Ref. EMEA/432604/2007 На сайте: http://www.emea.europa.eu.
53. Press release. 23/06/2011 European Medicines Agency concludes review of systemic nimesulide-containing medicines. На сайте: http://www.ema.europa.eu/ema/
54. Traversa G, Bianchi C, Da Cas R, et al. Cohort study of hepatotoxity associated with nimesulide and other non-steroidal antiinflammatory drugs. BMJ. 2003 Jul 5;327(7405):18–22.
55. Lee CH, Wang JD, Chen PC. Increased risk of hospitalization for acute hepatitis in patients with previous exposure to NSAIDs. Pharmacoepidemiol Drug Saf. 2010 Jul;19(7):708–14. doi: 10.1002/pds.1966.
56. Gulmez SE, Larrey D, Pageaux GP, et al. Transplantation for acute liver failure in patients exposed to NSAIDs or paracetamol (acetaminophen): the multinational casepopulation SALT study. Drug Saf. 2013 Feb;36(2):135–44. doi: 10.1007/s40264-012- 0013-7.
57. Романов БК. Клинические исследования эффективности и безопасности препарата Нимулид. На сайте: http://www.coralmed-corp.ru [Romanov BK. Clinical studies of the efficacy and safety of Nimulid. http://www.coralmed-corp.ru (In Russ.)].
58. Балабанова РМ, Гришаева ТП, Степанец ОВ. Эффективность и переносимость нимулида у больных ревматическими заболеваниями. Научно-практическая ревматология. 2004;(1):48–50. [Balabanova RM, Grishaeva TP, Stepanets OV. Nimulid efficacy and tolerability in patients with rheumatic diseases. Nauchno-prakticheskaya revmatologiya = Rheumatology Science and Practice. 2004;(1):48–50. (In Russ.)]. DOI: http://dx.doi.org/10.14412/1995-4484-2004-1383
59. Коган КМ, Золотарева ГД, Бернштейн ИЛ и др. Опыт применения препаратов НИМУЛИД и КОНДРОнова® окружными специалистами и врачамиревматологами г. Москвы. Научно-практическая ревматология. 2005;(4):58–62. [Kogan KM, Zolotareva GD, Bernshtein IL, et al. Practical expirience of nimulid and CONDROnova® administration by District specialists and rheumatologists of Moscow. Nauchno-prakticheskaya revmatologiya = Rheumatology Science and Practice. 2005;(4):58–62. (In Russ.)]. DOI: ttp://dx.doi.org/10.14412/1995-4484- 2005-619
60. Каратеев АЕ, Насонов ЕЛ, Яхно НН и др. Клинические рекомендации «Рациональное применение нестероидных противовоспалительных препаратов (НПВП) в клинической практике». Современная ревматология. 2015;(1):4–23. [Karateev AE, Nasonov EL, Yakhno NN, et al. Clinical guidelines «Rational use of nonsteroidal antiinflammatory drugs (NSAIDs) in clinical practice». Sovremennaya revmatologiya = Modern Rheumatology Journal. 2015;(1):4–23. (In Russ.)]. DOI: http://dx.doi.org/10.14412/1996-7012-2015-1-4-23.
Недифференцированный артрит: выявление кандидатов на раннее лечение для предотвращения прогрессирования до RA
Недифференцированный артрит (UA) — распространенная воспалительная форма артрита, сопровождающаяся отеком суставов, болью и ригидностью, которую нельзя классифицировать как конкретное ревматологическое заболевание. По оценкам, от 45% до 55% пациентов достигают спонтанной ремиссии, тогда как до 32% продолжают развиваться ревматоидный артрит (РА). 1 Учитывая существенное совпадение с RA, появляющиеся теории предполагают, что UA представляет собой уникальное окно возможностей для вмешательства в патологию RA до того, как она установится.
«Воспалительный артрит, как правило, является клиническим диагнозом, часто связанным с продолжительной утренней скованностью и улучшением при использовании, высокой температуре и нестероидных противовоспалительных препаратах (НПВП)», — сказал Джон Миллер, доктор медицины, специалист по ревматологии в больнице Джона Хопкинса и инструктор Медицинский факультет Университета Джона Хопкинса в Балтиморе, штат Мэриленд, сообщил советнику по ревматологии . «Синовит при осмотре может быть явным, хотя при исследованиях, включающих МРТ и УЗИ, мы также знаем, что синовит не может быть обнаружен при осмотре.”
Поскольку признаки неспецифические, UA обычно является диагнозом исключения до тех пор, пока не будут выполнены критерии RA. «Чувствительность диагностических критериев ACR 2010 [Американского колледжа ревматологии] для ревматоидного артрита составляет примерно от 80% до 85%, поэтому часто есть пациенты с признаками [РА], которые изначально не соответствуют критериям классификации», — заметил доктор Миллер. – Это подтверждается исследованиями, показывающими, что до трети пациентов с [UA] впоследствии могут быть классифицированы как имеющие [RA].«Клиническая задача состоит в том, чтобы идентифицировать пациентов с UA с риском прогрессирования, которым может быть полезно начало ранних протоколов лечения РА с использованием модифицирующих болезнь противоревматических препаратов (DMARD).
Оценка риска перехода UA к RA
В обзоре 2012 года Пайл изложил начальные критерии для выявления пациентов с UA с высокой вероятностью прогрессирования заболевания до RA, основанные на Правиле прогнозирования клиники раннего артрита Лейдена, включая: 2
- Возраст / женский пол / семейный анамнез РА
- Рано утром скованность
- Повышенная скорость оседания эритроцитов (СОЭ) / С-реактивный белок (СРБ) и количество опухших суставов как свидетельство воспалительного процесса
- Положительные серологические исследования антител к ревматоидному фактору (RF) или антицитруллинированному белку (CP)
- Тип поражения сустава: маленький против большого, только верхняя и нижняя конечность против нижней или симметричный
- Постепенное появление и продолжительность симптомов 8 недель или дольше при первом обращении
Пайл заметил, что «очевидно, что чем больше у вас возможностей RA на презентации, тем больше у вас шансов со временем соответствовать критериям RA.В 2010 году ACR / Европейская лига против ревматизма (EULAR) представила обновленные рекомендации, в которых особое внимание уделялось количеству пораженных суставов, серологическому анализу, острофазному реагенту и продолжительности симптомов. 3 Рекомендации ACR / EULAR вместе с моделью прогнозирования van der Helm-van Mil 4 (которая позволяет оценивать эти критерии) были признаны полезными для выявления пациентов с UA с самым высоким риском прогрессирования заболевания. 2,5
Ключевым фактором в определении риска прогрессирования РА является стойкость воспалительного артрита, особенно при наличии повышенных серологических маркеров, таких как иммуноглобулин M RF и антитела против CP. 6 Поскольку эти 2 маркера напрямую коррелируют с клиническими признаками продолжительной утренней скованности, большим количеством опухших и болезненных суставов, высоким СОЭ и развитием эрозивных изменений, а также указывают на худшие результаты, тестирование этих значений у пациентов с НС значительно улучшает предсказание. 2,6
Показания к лечению UA
Доктор Миллер заявил, что всем пациентам с воспалительным артритом, включая UA, следует рассмотреть возможность раннего лечения.«Терапия DMARD может быть отложена, так как часто требуется дальнейшая оценка кристаллической, инфекционной, злокачественной и метаболической этиологии», — сказал он, добавив, что «поскольку пациенты с [UA] часто проявляют боль и скованность, мы часто используем НПВП или глюкокортикоидов, поскольку мы оцениваем другие процессы ».
Было показано, что использование серологических маркеров в качестве основы для лечения БПВП приводит к снижению прогрессирования на рентгенограммах и МРТ через 1 год. 2 Когда назначается БПВП для лечения UA, данные указывают на то, что метотрексат является лучшим потенциальным лечением в сочетании с другими DMARD или кортикостероидами. 1,7
«Если проводится терапия DMARD, мы пытаемся адаптировать иммуносупрессию к степени воспаления», — пояснил д-р Миллер. «Например, пациента с полиартритом можно лечить метотрексатом или лефлуномидом, а пациента с олигоартритом можно лечить сульфасалазином или гидроксихлорохином. Есть много других факторов, которые влияют на выбор терапии DMARD, включая функцию почек и печени, употребление алкоголя и аллергию ».
Текущие рекомендации предполагают, что терапию РА следует начинать на ранней стадии, когда РА впервые диагностирован, хотя не у всех пациентов, относящихся к группе риска, действительно разовьется РА. 1,2,7,8 Доказательства все еще указывают на необходимость лечения, сказал доктор Миллер. «Несколько групп с ранним артритом показали пользу раннего лечения, и есть доказательства того, что отсрочка терапии может снизить способность традиционных БПВП вызывать ремиссию».
Консультирование пациентов с неподтвержденным диагнозом UA относительно потенциальной потребности в терапии DMARD представляет собой уникальную задачу. «Пациентам часто не нравится диагноз, который включает« недифференцированный », — отмечает д-р Миллер.«Важно научить пациентов, что это означает для уменьшения беспокойства и страха», — сказал он, сосредоточив внимание на преимуществах предотвращения более тревожной перспективы РА. «Я пытаюсь заверить их, что, если симптомы не исчезнут, у нас есть много эффективных лекарств от воспалительного артрита, которые могут уменьшить боль, скованность и улучшить функцию, а также предотвратить прогрессирующее повреждение суставов».
подписаться на @RheumAdvisor
Список литературы
- Wevers-de Boer KV, Heimans L, Huizinga TW, Allaart CF.Медикаментозная терапия недифференцированного артрита: систематический обзор литературы. Ann Rheum Dis. 2013; 72 (9): 1436-1444.
- Пайл К. Лечение раннего недифференцированного артрита. Indian J Rheumatol. 2012; 7: 215-220.
- Aletaha D, Neogi T, Silman AJ и др. Критерии классификации ревматоидного артрита 2010 года: совместная инициатива Американского колледжа ревматологии / Европейской лиги против ревматизма. Энн Рум Дис . 2010; 69: 1580-1588.
- van der Helm-van Mil AHM, Cessie SL, van Dongen H, Breedveld FC, Toes REM, Huizinga TWJ.Правило прогноза исхода заболевания у пациентов с недифференцированным артритом с недавним началом: как принимать индивидуальные решения о лечении. Революционный артрит . 2007; 56: 433-440.
- Зайда Бедран, Кристиан Кирос, Хавьер Роза и др. Подтверждение правила прогноза для диагностики ревматоидного артрита у пациентов с недавно начавшимся недифференцированным артритом. Int J Rheumatol. 2013; 2013: 548502.
- Mjaavatten MD, van der Heijde D, Uhlig T, et al. Вероятность стойкого артрита возрастает с увеличением уровня антител к цитруллинированному пептиду и ревматоидного фактора иммуноглобулина М: продольное исследование 376 пациентов с очень ранним недифференцированным артритом. Arthritis Res Ther. 2010; 12: R76.
- 7. Смолен Дж. С., Ландеве Р., Бредвелд ФК и др. Рекомендации EULAR по лечению ревматоидного артрита с помощью синтетических и биологических противоревматических препаратов, модифицирующих болезнь: обновление 2013 г. Ann Rheum Dis. 2014; 73: 492-509.
- 8. Лопес-Оливо М.А., Какповбиа-Эшаретури В., де Бордес Дж. К. и др. Лечение раннего недифференцированного артрита; систематический обзор и метаанализ прямых и косвенных доказательств испытаний. Arthitis Care Res .2018; 70 (9): 1355-1365.
Чем раньше, тем лучше лечить недифференцированный артрит
Ключевые моменты
• Раннее лечение недифференцированного артрита задерживает развитие ревматоидного артрита (РА) на срок до одного года.
• Метотрексат является препаратом выбора для раннего лечения недифференцированного артрита.
• Внутримышечно можно использовать метилпреднизолон, если метотрексат противопоказан.
• Другие методы лечения могут замедлить прогрессирование недифференцированного артрита, но их эффект не был значительным.
Предпосылки
Артрит, который не полностью соответствует диагностическим критериям РА, считается недифференцированным и может иметь различные проявления. Мария Лопес-Оливо и ее коллеги 1 из Техасского университета в Хьюстоне отмечают, что недифференцированный артрит часто может быть ранним проявлением определенного артрита и может предлагать возможность для раннего лечения.
Присутствие ревматоидного фактора и аллеля HLA-DRB1 может быть ключом к разгадке развития РА при недифференцированном проявлении.Дальнейшие данные свидетельствуют о том, что некоторые характеристики пациента, такие как пожилой возраст, артрит рук и высокая активность недифференцированного артрита, могут предсказывать прогрессирование РА.
Авторы стремились определить, предотвращают ли какие-либо методы лечения недифференцированного артрита или задерживают прогрессирование РА. Недавно они представили свои выводы в Arthritis Care & Research .
Исследование
Авторы провели систематический обзор и метаанализ, в котором изучались доли пациентов, у которых РА развился в течение периода исследования.Вторичные исходы включали ремиссию, оценку активности заболевания в 28 суставах, прогрессирование поражения суставов, синовит и изменения основных переменных для РА. В конечном итоге в анализ были включены 9 испытаний.
Результаты
• Пациенты, получавшие лечение любым типом вмешательства, имели меньшую вероятность развития РА через 12 месяцев (отношение шансов [OR], 0,49; 95% доверительный интервал [CI], 0,26-0,90).
• При рассмотрении каждого отдельного лечения только метотрексат приводил к статистически значимой задержке прогрессирования РА (ОШ, 0.13; 95% ДИ 0,03-0,48).
• У 19% пациентов, получавших метотрексат, развился РА по сравнению с 59% в контрольной группе.
• Никаких различий не наблюдалось через 30 и 60 месяцев (ОШ 0,60; 95% ДИ 0,28–1,3 и ОШ 0,75; 95% ДИ 0,35–1,6, соответственно).
• Незначительная тенденция к замедленному прогрессированию наблюдалась у тех, кто получал внутримышечно метилпреднизолон: 47% с диагнозом РА через 12 месяцев по сравнению с 55% контрольной группы (OR 0,72; 95% ДИ 0,51–1,0).
• Отношение шансов соответствующих курсов лечения, приводящих к РА через 12 месяцев, составляет: метотрексат (OR, 0.16; 95% ДИ 0,08-0,33), абатацепт (ОШ 0,56; 95% ДИ 0,20-1,6), внутрисуставной метилпреднизолон (ОШ 0,57; 95% ДИ 0,09-3,7), метилпреднизолон внутримышечно (ОШ 0,72; 95 % ДИ 0,53–0,99) и инфликсимаб (ОШ 2,0; 95% ДИ 0,49–8,2).
• Все вмешательства улучшили как минимум один вторичный результат.
Значение для врачей
• Когда пациент поступает с недифференцированным артритом, начните лечение как можно раньше, так как это может отсрочить прогрессирование РА.
• Лечение метотрексатом с наибольшей вероятностью предотвратит прогрессирование недифференцированного артрита в РА через 1 год при использовании внутримышечного метилпреднизолона в качестве второго варианта.
• Раннее лечение любой терапией, описанной выше, может привести к снижению активности заболевания, улучшению ремиссии, уменьшению опухших и болезненных суставов, меньшему синовиту, меньшей утомляемости и / или меньшему рентгенологическому прогрессированию повреждения суставов.
• Пациенты с антителами против CCP могут заслуживать особого внимания, поскольку болезнь может прогрессировать быстрее.
Раскрытие информации:
О финансировании не сообщалось.
Ссылки:
1. Lopez-Olivo MA, Kakpovbia-Eshareturi V, des Bordes J, et al.Лечение раннего недифференцированного артрита: систематический обзор и метаанализ прямых и косвенных доказательств испытаний. Резолюция по уходу за артритом . 2017 21 ноя. Doi: 10.1002 / acr.23474. [Epub перед печатью]
Что следует знать о недифференцированном артрите
Недифференцированный артрит (UA) — это общий термин для случаев артрита, который не соответствует конкретному диагнозу. Несмотря на множество типов артрита, которые четко определены медицинским сообществом, симптомы людей не всегда точно соответствуют устоявшейся категории.Например, у вас может быть ранняя стадия воспалительного артрита, но у вас есть набор симптомов, который не согласуется с каким-либо конкретным типом артрита. Кроме того, ревматические заболевания имеют много общих симптомов.
Диагноз UA, вероятно, означает, что еще слишком рано ставить конкретный диагноз, но у вас есть симптомы, которые необходимо лечить.
BSIP / UIG / Getty ImagesРезультаты недифференцированного артрита
Подсчитано, что от 40% до 50% людей с недифференцированным артритом проходят спонтанную ремиссию.Это означает, что симптомы проходят сами по себе.
Примерно у 30% людей с этим диагнозом развивается ревматоидный артрит (РА), а у оставшихся 20–30% развиваются другие типы воспалительного артрита.
РА — хроническое заболевание, которое часто приводит к истощению организма. Ранняя диагностика и лечение имеют решающее значение для замедления или остановки его прогрессирования, поэтому врачам важно предсказать, у каких людей с недифференцированным артритом может развиться РА.
Прогнозирование курса
В 2008 году метод прогнозирования течения UA был разработан в Европе и опубликован в журнале Arthritis & Rheumatism .Он рассматривал несколько факторов, чтобы определить ваш уровень риска.
Факторы включали:
Было обнаружено, что этот метод очень точен в прогнозировании того, кто перейдет от UA к RA.
В 2010 году Американский колледж ревматологии сотрудничал с Европейской лигой против ревматизма, чтобы пересмотреть руководящие принципы, используемые для классификации людей с ревматоидным артритом для целей научных исследований. Поскольку новые рекомендации сосредоточены на более ранних стадиях заболевания, а не на характеристиках поздних стадий стойкого или эрозивного артрита, они также полезны при диагностике и лечении пациентов с РА.Взаимодействие с другими людьми
Согласно пересмотренным руководствам, точный диагноз РА основан на:
- Подтвержденное наличие синовита (воспаления слизистой оболочки сустава) как минимум в одном суставе
- Отсутствие другого диагноза, лучше объясняющего синовит
- Четыре оценивания, в результате которых общая сумма баллов составляет от шести до 10 (см. Таблицу)
| Оценка для диагностики RA | Диапазон оценок |
|---|---|
| Количество и расположение пораженных суставов | 0-5 |
| Положительные анализы крови на ревматоидный фактор или анти-CCP | 0–3 |
| Анализы крови, показывающие высокий уровень СРБ или седиментации | 0-1 |
| Продолжительность симптома | 0-1 |
Это руководство предназначено для улучшения ранней диагностики РА, что приведет к меньшему количеству диагнозов UA и более раннему лечению.
Есть ли роль у исследований изображений?
Методы рентгенографии, такие как рентген и магнитно-резонансная томография (МРТ), предлагают много информации для врача, пытающегося предсказать, перейдет ли UA в РА, особенно когда на изображениях видны эрозии рук и ног.
Лечить или не лечить
Прогрессирование РА схоже, независимо от того, был ли ваш первый диагноз РА или МА, который затем прогрессировал в РА. Возникает вопрос, лучше ли назначать препараты РА пациентам с UA.
Некоторые небольшие исследования оценивали использование модифицирующих заболевание противоревматических препаратов (DMARD) или биопрепаратов для предотвращения прогрессирования UA в RA. Согласно обзору этого исследования, это может быть разумная стратегия с некоторыми лекарствами.
БПВП и биологические препараты фактически являются предпочтительными препаратами первой линии для лечения РА. Они эффективны, но сопряжены с серьезными рисками и побочными эффектами.
Ожидание приема этих препаратов до тех пор, пока у вас не будет точного диагноза РА, означает, что вы не столкнетесь с этими рисками без необходимости, если вы относитесь к тем, у кого симптомы исчезнут спонтанно.
С другой стороны, раннее лечение дает вам наилучшие шансы предотвратить прогрессирование заболевания, инвалидность и снижение качества жизни, если у вас действительно разовьется РА.
Эта дилемма демонстрирует, почему так важно понимать, кто подвергается риску.
Слово Verywell
Если вам поставили диагноз недифференцированный артрит и вы беспокоитесь, что он перерастет в ревматоидный артрит, поговорите со своим врачом о ваших конкретных факторах риска.Как только вы узнаете, какова вероятность, вы сможете лучше вместе работать над оптимальным курсом лечения для защиты вашего здоровья и функциональности.
Спасибо за отзыв!
Как справиться с хроническим воспалением? Может помочь противовоспалительная диета. В нашем бесплатном руководстве по рецептам вы найдете лучшие продукты для борьбы с воспалениями. Получите свой сегодня!
Зарегистрироваться
Ты в!Спасибо, {{form.email}}, за регистрацию.
Произошла ошибка.Пожалуйста, попробуйте еще раз.
Что вас беспокоит?
Другой Неточный Трудно понять Verywell Health использует только высококачественные источники, в том числе рецензируемые исследования, для подтверждения фактов в наших статьях. Прочтите наш редакционный процесс, чтобы узнать больше о том, как мы проверяем факты и обеспечиваем точность, надежность и надежность нашего контента. Verywell Health — часть издательской семьи Dotdash.Клинические и экономические последствия
Введение
В последние несколько лет при лечении ревматоидного артрита (РА) особое внимание уделялось ранней агрессивной терапии с использованием традиционных антиревматических препаратов, модифицирующих болезнь (DMARD), и / или противоревматических биологических агентов.Это стало результатом более глубокого понимания патофизиологии недифференцированного артрита (UA) и RA, а также доступности нескольких биологических агентов, которые подавляют аспекты аутоиммунного ответа, которые способствуют развитию RA.
Примерно от 40% до 50% пациентов с UA испытывают спонтанную ремиссию, в то время как примерно 30% прогрессируют до РА, а у остальных развиваются другие состояния. 1,2 Исследователи изучили критерии, которые могут помочь идентифицировать тех пациентов с UA, у которых есть высокая вероятность прогрессирования до стойкого и / или эрозивного РА.После определения надежных критериев возникает следующий вопрос: может ли активная терапия традиционными БПВП или противоревматическими биологическими агентами быть эффективной для замедления или предотвращения прогрессирования заболевания. Клинические испытания демонстрируют, что раннее лечение может замедлить или остановить прогрессирование заболевания. 3-6 С точки зрения управляемой медицинской помощи, ограничение лечения только теми пациентами с UA, которым больше всего поможет активное вмешательство, имеет серьезные последствия.
В этой статье дается обзор последних исследований в поддержку усилий по выявлению пациентов с UA, которые имеют высокий риск прогрессирования стойкого и / или эрозивного РА, и предлагаются идеи терапевтических подходов для этих пациентов.
Определение недифференцированного артрита
Таблица 1
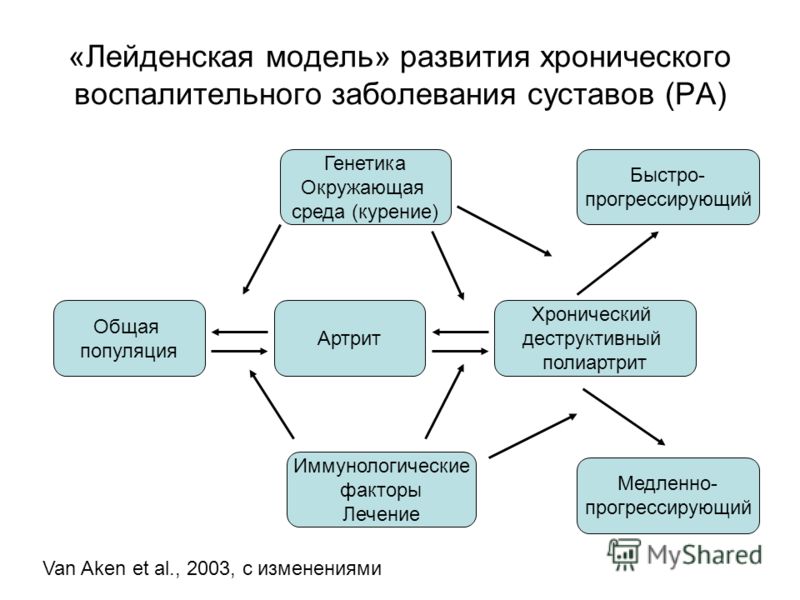
Термин «недифференцированный артрит» был включен в исследования, проведенные Лейденской клиникой раннего артрита в Нидерландах для описания случаев воспалительного артрита, когда не мог быть поставлен конкретный диагноз ( ). 1,7,8 Возникает вопрос, почему UA важен?
Прогрессия от UA к RA
Прогрессирование заболевания у пациентов, изначально поступивших с UA, сравнимо с таковым у пациентов, которым изначально был поставлен диагноз РА.В исследовании van Aken и его коллег сравнивали прогрессирование заболевания у пациентов, которые первоначально поступили с UA и прогрессировали до RA в течение 1 года (группа UA-RA; n = 92), с прогрессированием заболевания у тех, кто изначально поступил с RA (группа RA-RA; n = 62) на основе критериев Американского колледжа ревматологии (ACR) 1987 года. 1 Измерения результатов отслеживались в течение 4 лет после первоначальной презентации.
Никаких существенных различий между двумя группами не наблюдалось в течение любого периода последующего наблюдения (годы 1, 2, 3 и 4) в отношении рентгенологического прогрессирования повреждения сустава (по оценке Шарпа / Ван дер Хейде) или активности заболевания и функционального состояния. способность (измеряемая с помощью анкеты для оценки здоровья [HAQ] или показателя активности заболевания [DAS]).Подобное прогрессирование заболевания наблюдалось в обеих группах, несмотря на то, что большее количество пациентов в группе РА-РА начало лечение DMARD через 3 месяца после обращения (100% против 46%). Это исследование предполагает, что пациенты с UA, которые в конечном итоге прогрессируют до РА, имеют те же результаты, что и пациенты с изначально диагностированным РА.
Прогнозирование прогрессирования UA в RA
Правила прогнозирования — важные инструменты в определении того, у каких пациентов с UA будет прогрессировать RA. Первое подтвержденное правило прогнозирования было разработано в Европе и опубликовано в 2008 году.В нем использовалась информация о пациентах, которая регулярно собирается во время первоначального посещения офиса 9,10 — возраст, пол, количество и типы пораженных суставов, продолжительность утренней скованности, уровень С-реактивного белка и результаты серологического анализа (наличие ревматоидного фактора [RF] и антитело против цитруллинированного белка [ACPA]). Применительно к 3 независимым когортам пациентов с ранним началом UA это правило прогноза точно оценило риск развития РА у более чем 75% пациентов с UA. 10
Критерии классификации ACR / EULAR RA, 2010
Таблица 2
В сентябре 2010 года ACR в сотрудничестве с Европейской лигой борьбы с ревматизмом (EULAR) выпустил обновленные критерии классификации RA с цель — выделить новых пациентов с недифференцированным воспалительным артритом, у которых была высокая вероятность развития стойкого или эрозивного РА (). 11 Они представляют собой значительное изменение по сравнению с критериями ACR 1987 г., которые не были разработаны для выявления пациентов с ранним РА или пациентов с высоким риском прогрессирования РА. 7,12 Авторы подчеркивают, что балльная система 2010 г. требует тестирования на различных когортах пациентов, чтобы продемонстрировать ее валидность. Будет важно определить, работают ли эти критерии для одних групп пациентов лучше, чем для других, и позволяют ли точно индивидуализировать принятие решений о лечении.
Критерии классификации 2010 ACR / EULAR RA могут оказать значительное влияние на ведение пациентов на самых ранних стадиях заболевания. Хотя авторы четко заявляют, что эта классификационная система не предназначена для использования в качестве справочного инструмента для диагностики пациентов с РА, вполне вероятно, что критерии будут включены в клиническую практику как часть общей диагностической процедуры.Это может помочь клиницистам в выявлении пациентов на ранних стадиях РА, которым будет полезно терапевтическое вмешательство и / или направление к специалисту. Также возможно, что эти критерии будут приняты организациями управляемой медицинской помощи для определения целесообразности конкретных вмешательств для пациентов с ранними признаками РА. Есть также экономические преимущества в ограничении терапии теми, у кого высокая вероятность развития стойкого РА, при минимизации терапии для пациентов с низким риском.
Скрининг пациентов с UA, подверженных риску прогрессирования до RA
Скрининг пациентов, которые изначально поступают с UA, для выявления тех, у кого высокая вероятность прогрессирования до RA, может быть полезным для пациента и поставщика медицинских услуг.
Серологические факторы
Серологические факторы — удобная и точная мера для прогнозирования прогрессирования РА. RF использовался в течение нескольких десятилетий и является единственным серологическим фактором, упомянутым в критериях ACR 1987 года. 7,13 Совсем недавно было идентифицировано несколько других биологических маркеров, включая различные ACPA (протестированные как антициклические цитруллинированные пептиды [анти-ЦЦП]). 14,15
Рис. 1
Чтобы проверить прогностическую ценность ACPA для прогрессирования РА, ван Гален и его коллеги сравнили результаты серологических анализов и прогрессирование заболевания у пациентов с UA. 16 Из 318 пациентов с UA 69 были анти-CCP-положительными и 249 были анти-CCP-отрицательными на момент включения в исследование.Через 3 года 93% пациентов с положительной реакцией на КПК соответствовали критериям ACR для РА по сравнению с 25% пациентов с отрицательной реакцией на КПК (отношение шансов 37,8; 95% доверительный интервал [ДИ] 13,8–111,9) (). Авторы пришли к выводу, что наличие антител против CCP помогает дифференцировать тех пациентов с UA, которые подвержены риску развития RA. Прогностическая ценность RF и ACPA была дополнительно подтверждена 4-летним контрольным исследованием пациентов с недифференцированным полиартритом. 17
Хотя для скрининга пациентов с НС можно использовать несколько различных серологических маркеров, исследования окончательно не определили, существуют ли различия в прогностических значениях, связанных с ними.В одном исследовании сравнивалась прогностическая ценность нескольких из этих маркеров, в том числе РФ и анти-ЦКА. 18 Результаты показали, что не было значительных различий в прогностической ценности этих серологических маркеров при различении пациентов с UA, у которых позже развился RA. Кроме того, использование комбинации серологических тестов не улучшило прогностическую ценность, указывая на то, что одного анализа достаточно для определения.
Радиографические критерии
Помимо серологических маркеров, исследователи попытались определить другие меры для прогнозирования прогрессирования от UA до RA.К ним относятся радиологическая оценка исходных эрозий суставов кистей и стоп, магнитно-резонансная томография (МРТ) суставов или комбинация радиологического обследования, серологических анализов и симптомов. 19-22 Хотя эти методы могут оказаться эффективными в прогнозировании того, у каких пациентов с UA может развиться РА, включение рентгенологических критериев, особенно МРТ, может быть недопустимым с точки зрения затрат и времени в качестве инструмента скрининга, а также из-за того, что опытный опорно-двигательный аппарат рентгенолог будет необходим.
Критерии классификации ACR / EULAR RA 2010
Критерии классификации ACR / EULAR RA 2010 обеспечивают стандартизированный алгоритм оценки пациентов с UA. Эти критерии будут важны при разработке критериев включения в клинические испытания с пациентами на самых ранних стадиях заболевания. Они также позволят сравнить когорты пациентов из различных клинических испытаний, в которых приняты эти критерии. Поскольку в этих критериях используется информация, регулярно собираемая при первоначальном представлении в клинике, оценка не увеличит время и стоимость оценки.Хотя эти критерии не предназначены для использования в качестве справочного инструмента для диагностики, они могут быть включены как часть процесса скрининга и диагностики пациентов с UA и помочь в процессе принятия решения о лечении.
Преимущества нацеливания на пациентов с UA для активного лечения
При ведении пациентов с UA важно провести анализ соотношения затрат и выгод при немедленном начале лечения или отсрочке лечения до постановки окончательного диагноза РА.Отсрочка лечения может сохранить ресурсы и уменьшить нецелесообразное или ненужное использование противоревматических средств у пациентов, у которых может быть спонтанная ремиссия и в конечном итоге не прогрессировать до РА. Однако экономическая эффективность отсрочки лечения снижается, если рассматривать долгосрочные последствия — более быстрое прогрессирование заболевания и инвалидности и снижение вероятности ремиссии.
Как упоминалось ранее, прогрессирование заболевания у пациентов с UA, которым в конечном итоге был поставлен диагноз RA, аналогично прогрессированию у пациентов с диагнозом RA при первичном обращении.Следовательно, врачи должны сосредоточиться на предотвращении или замедлении прогрессирования заболевания с помощью терапевтического вмешательства. Имеющиеся данные свидетельствуют о том, что лечение на ранних стадиях заболевания более эффективно, чем лечение пациентов с длительным заболеванием, и связано с большей вероятностью ремиссии заболевания. 6,23 Это приводит к долгосрочным преимуществам, таким как улучшение качества жизни, снижение инвалидности и снижение общих затрат на здравоохранение.
Клинические последствия лечения пациентов с UA
В исследовании PROMPT (PRObable RA: метотрексат по сравнению с лечением плацебо) оценивались клинические последствия отсрочки терапии у пациентов с UA. 4 Это было рандомизированное двойное слепое плацебо-контролируемое исследование, в котором оценивалась эффективность немедленной терапии метотрексатом у пациентов с UA по сравнению с отсрочкой противоревматической терапии до тех пор, пока критерии ACR 1987 года не были удовлетворены для диагноза РА. В общей сложности 110 пациентов, которые соответствовали критериям ACR 1958 года для вероятного РА, были рандомизированы для еженедельного приема метотрексата или плацебо. Первичным критерием оценки был процент пациентов, удовлетворяющих критериям РА 1987 года.
Исследование PROMPT: результаты
Рисунок 2
Через 6 месяцев примерно 10% пациентов в группе метотрексата соответствовали критериям диагноза РА по сравнению с примерно 30% в группе плацебо ().
Через 30 месяцев у 40% пациентов в группе метотрексата и у 53% в группе плацебо развился РА. Все пациенты в группе плацебо, у которых развился РА до РА, сделали это в течение первого года по сравнению с только 50% пациентов в группе метотрексата.
У большинства пациентов рентгенологическое прогрессирование не изменилось, что определено по шкале Шарпа / Ван дер Хейде (73% в группе плацебо и 88% в группе метотрексата). Однако у большего процента пациентов в группе плацебо наблюдалось некоторое прогрессирование заболевания, превышающее наименьшее обнаруживаемое изменение (27.5% против 11,8%; P = 0,046).
РЕЗУЛЬТАТЫ ПРИ НАЛИЧИИ ACPA
Преимущества метотрексата были более выражены у ACPA-положительных пациентов. В общей сложности 14 из 15 ACPA-положительных пациентов, получавших плацебо, прогрессировали до РА, по сравнению с 8 из 12, получавших метотрексат (отношение рисков, 4,9; 95% ДИ, 1,88–12,79; P <0,001). Только 2 из 12 ACPA-положительных пациентов, получавших метотрексат, достигли ремиссии, что позволяет предположить, что метотрексат не вызывает ремиссии, а скорее задерживает начало РА.Несмотря на низкую скорость ремиссии у пациентов, получавших метотрексат, результаты показывают, что раннее лечение может повлиять на прогрессирование заболевания у ACPA-положительных пациентов.
Экономические последствия лечения пациентов с помощью UA
RA связано с затратами не только для системы здравоохранения, но и для пациента и общества из-за потери производительности и сокращения продолжительности жизни с поправкой на качество. 24 Недавнее европейское исследование оценило общие среднегодовые затраты на РА в 14 906 евро, включая затраты на здравоохранение, пациентов и семью, а также производительность. 25 В Соединенных Штатах избыточные расходы на здравоохранение, связанные с РА, оцениваются в 8,4 миллиарда долларов, в то время как другие расходы, относящиеся к РА, составляют дополнительные 10,9 миллиардов долларов (2005 долларов США) — 33% этих затрат относятся на работодателей, 28% — на пациентов. , 20% правительству и 19% опекунам. 26 Любые усилия по значительному снижению бремени этого состояния должны быть сосредоточены на уменьшении числа пациентов, у которых прогрессирует РА.
Рис. 3
Разница в стоимости лечения пациентов с UA и пациентов с RA может быть значительной.Французское исследование с использованием данных 2003 г. показало, что прямые и косвенные затраты UA и RA составили 2424 евро и 5928 евро соответственно (). 27 Двумя сильными предикторами более высоких затрат в целом были усиление боли и присутствие РФ. Хотя наблюдаются различия в ежегодных затратах на UA и RA, необходимы дополнительные исследования, чтобы полностью понять экономическую эффективность раннего вмешательства у пациентов с UA и скрининга пациентов с UA (т. Е. Использование серологических тестов) для выявления тех, кто выиграет от ранней терапии.
Варианты лечения для предотвращения или отсрочки прогрессирования UA в RA
В нескольких клинических испытаниях оценивали использование противоревматических средств для предотвращения прогрессирования UA в RA.
Метотрексат по сравнению с плацебо
Как описано ранее, основное исследование PROMPT продемонстрировало, что у пациентов с UA метотрексат был эффективен в замедлении прогрессирования РА и уменьшении рентгенологического прогрессирования, хотя он не показал каких-либо значительных преимуществ в лечении. ремиссия болезни.
Инфликсимаб по сравнению с плацебо
Инфликсимаб сравнивали с плацебо у пациентов с НК продолжительностью менее 12 месяцев, у которых возник рецидив после однократной инъекции кортикостероидов. 28 Это двойное слепое плацебо-контролируемое испытание включало 17 пациентов, ранее не получавших DMARD. Инфликсимаб вводили 10 пациентам на 0, 2, 6 и 14 неделях, а метотрексат добавляли на 14 неделе в случае отсутствия клинического ответа. На 26 неделе у 1 из 7 пациентов (14%) в группе плацебо и у 2 из 10 (20%) в группе инфликсимаба была достигнута клиническая ремиссия.Не было значительных различий между двумя группами в отношении каких-либо вторичных исходов — скованности ранним утром, оценки болезненности суставов, HAQ или DAS в 28 суставах. К 52 неделе у всех пациентов в группе инфликсимаба и у 5 из 7 пациентов в группе плацебо развился РА. Использование инфликсимаба показало умеренное краткосрочное облегчение у этих пациентов, но не предотвратило развитие РА.
Абатацепт по сравнению с плацебо
В другом исследовании сравнивали абатацепт с плацебо у пациентов с UA, которые также дали положительный результат на ACPA. 5 Пациенты получали абатацепт (n = 28) или плацебо (n = 28) в течение 6 месяцев и были обследованы на 12-м и 24-м месяцах. На 12-м месяце у меньшего числа пациентов в группе абатацепта развился РА, хотя разница не была значимой. (46% против 67%; 95% ДИ, от -47,4% до 7,8%). Абатацепт был связан с задержкой прогрессирования РА. Пациенты в группе абатацепта продемонстрировали более сильное подавление заболевания на рентгенограммах и МРТ, которое сохранялось через 6 месяцев после прекращения лечения. Авторы пришли к выводу, что прогрессирование РА может быть изменено путем модуляции Т-клеточного ответа на очень ранних стадиях заболевания.
Эти 2 небольших исследования предполагают возможность некоторого положительного эффекта биологических агентов у пациентов с UA. Необходимы более масштабные рандомизированные клинические испытания, чтобы ответить на вопрос, оправдана ли биологическая терапия этой популяции пациентов.
Заключение
Выпуск критериев классификации 2010 ACR / EULAR RA может способствовать оценке долгосрочных клинических и экономических результатов, связанных с агрессивным лечением противоревматическими средствами в UA.Скрининг пациентов на серологические маркеры РА может быть точным и рентабельным методом выявления тех, кому фармакотерапия будет полезна, при сведении к минимуму ненадлежащего использования противоревматических средств у пациентов с низким риском.
Принадлежность автора: Медицинский факультет Университета Колорадо, Гринвуд-Виллидж, Колорадо.
Источник финансирования: При поддержке образовательных грантов Genentech и Biogen Idec.
Информация об авторе: Д-р Шифф сообщает о назначениях и грантах консультативных советов Abbott, Amgen, Bristol-Myers Squibb, Horizon, Pfizer и Roche.Он также сообщает об участии рекламного бюро спикера с Abbott.
Информация об авторстве: Концепция и дизайн; сбор данных; анализ и интерпретация данных; составление рукописи; и критический пересмотр рукописи для важного интеллектуального содержания.
Адрес для корреспонденции: Майкл Х. Шифф, доктор медицины, Медицинский факультет Университета Колорадо, 5400 South Monaco St, Greenwood Village, CO 80111.Электронная почта: [email protected].
1. ван Акен Дж., Ван Донген Х., ле Сесси С., Аллаарт К.Ф., Бредвельд ФК, Хейзинга Т.В. Сравнение отдаленных результатов пациентов с ревматоидным артритом с недифференцированным артритом или ревматоидным артритом: наблюдательное когортное исследование. Ann Rheum Dis. 2006; 65 (1): 20-25.
2. Харрисон Б.Дж., Симмонс Д.П., Бреннан П., Барретт Е.М., Силман А.Дж. Естественная ремиссия при воспалительном полиартрите: вопросы определения и прогноза. Br J Rheumatol. 1996; 35 (11): 1096-1100.
3. Goekoop-Ruiterman YP, de Vries-Bouwstra JK, Allaart CF, et al. Клинические и рентгенологические результаты четырех различных методов лечения стратегий у пациентов с ранним ревматоидным артритом (исследование BeSt): рандомизированное контролируемое исследование. Arthritis Rheum. 2005; 52 (11): 3381-3390.
4. van Dongen H, van Aken J, Lard LR, et al. Эффективность лечения метотрексатом у пациентов с вероятным ревматоидным артритом: двойное слепое рандомизированное плацебо-контролируемое исследование. Артрит Ревм. 2007; 56 (5): 1424-1432.
5. Эмери П., Дурез П., Дугадос М. и др. Влияние модуляции костимуляции Т-клеток у пациентов с недифференцированным воспалительным артритом или очень ранним ревматоидным артритом: клиническое и визуализирующее исследование абатацепта (исследование ADJUST). Ann Rheum Dis. 2010; 69 (3): 510-516.
6. Григор Ч., Капелл Х., Стирлинг А. и др. Эффект от стратегии жесткого контроля ревматоидного артрита (исследование TICORA): простое слепое рандомизированное контролируемое исследование. Ланцет. 2004; 364 (9430): 263-269.
7. Арнетт Ф.К., Эдворти С.М., Блох Д.А. и др. Американская ассоциация ревматизма 1987 г. пересмотрела критерии классификации ревматоидного артрита. Революционный артрит . 1988; 31 (3): 315-324.
8. Канаты М.В., Беннетт Г.А., Кобб С., Якокс Р., Джессар Р.А. 1958 г. Пересмотр диагностических критериев ревматоидного артрита. Bull Rheum Dis. 1958; 9 (4): 175-176.
9.ван дер Хельм-ван Мил А.Х., ле Сесси С., ван Донген Х., Бридвелд ФК, Тоес Р.Э., Хейзинга Т.В. Правило прогнозирования болезни исход у пациентов с недифференцированным артритом с недавним началом артритом: как принимать индивидуальные решения о лечении. Артрит Ревм. 2007; 56 (2): 433-440.
10. van der Helm-van Mil AH, Detert J, le Cessie S, et al. Подтверждение правила прогнозирования исхода заболевания у пациентов с недавно начавшимся недифференцированным артритом: переход к индивидуальному принятию решения о лечении. Arthritis Rheum. 2008; 58 (8): 2241-2247.
11. Алетаха Д., Неоги Т., Силман А.Дж. и др. Критерии классификации ревматоидного артрита 2010: совместная инициатива Американского колледжа ревматологии / Европейской лиги против ревматизма. Ann Rheum Dis. 2010; 69 (9): 1580-1588.
12. Bykerk VP, Haes JM. Когда начинается ревматоидный артрит и можно ли его остановить раньше? Ann Rheum Dis. 2010; 69 (3): 473-475.
13. Уокер Д. Д., Паунд Дж. Д., Гриффитс ИД, Пауэлл Р. Дж.. Тесты на ревматоидный фактор в диагностике и прогнозировании ревматоидного артрита. Ann Rheum Dis. 1986; 45 (8): 684-690.
14. van Jaarsveld CH, ter Borg EJ, Jacobs JW, et al. Прогностическое значение антиперинуклеарного фактора, антител против цитруллинированного пептида и ревматоидного фактора при раннем ревматоидном артрите. Clin Exp Rheumatol. 1999; 17 (6): 689-697.
15.Bos WH, Wolbink GJ, Boers M, et al. Развитие артрита у пациентов с артралгией тесно связано со статусом антител к цитруллинированному белку: проспективное когортное исследование. Ann Rheum Dis. 2010; 69 (3): 490-494.
16. van Gaalen FA, Linn-Rasker SP, van Venrooij WJ, et al. Аутоантитела к циклическим цитруллинированным пептидам предсказывают прогрессирование ревматоидного артрита у пациентов с недифференцированным артритом : проспективное когортное исследование. Arthritis Rheum. 2004; 50 (3): 709-715.
17. Каро-Олеас Дж. Л., Фернандес-Суарес А., Ренесес Цестерос С., Поррино С., Нуньес-Ролдан А., Вичманн Шлипф И. Оценка антител против ЦЦП третьего поколения в диагностике ревматоидного артрита от недифференцированного полиартрита через 4 года наблюдения . Clin Exp Rheumatol. 2008; 26 (3): 461-463.
18. van der Linden MP, van der Woude D, Ioan-Facsinay A, et al. Значение антимодифицированного цитруллинированного виментина и антициклического цитруллинированного пептида третьего поколения по сравнению с антициклическим цитруллинированным пептидом второго поколения и ревматоидным фактором в прогнозировании исхода заболевания при недифференцированном артрите и ревматоидном артрите . Arthritis Rheum. 2009; 60 (8): 2232-2241.
19. Курия Б., Ченг С.К., Чен Х.М., Бикерк В.П. Подтверждение правила прогнозирования развития ревматоидного артрита у пациентов с ранним недифференцированным артритом. Ann Rheum Dis. 2009; 68 (9): 1482-1485.
20. Нарваез Дж., Сирвент Э., Нарваез Дж. А. и др. Полезность магнитно-резонансной томографии руки в сравнении с тестом на антитела к антициклическому цитруллинированному пептиду для подтверждения диагноза клинически подозреваемого раннего ревматоидного артрита при отсутствии ревматоидного фактора и рентгенологических эрозий. Semin Arthritis Rheum.
2008; 38 (2): 101-109.
21. Тамай М., Каваками А., Уэтани М. и др. Правило прогнозирования исхода заболевания у пациентов с недифференцированным артритом с использованием магнитно-резонансной томографии запястий и суставов пальцев и серологических аутоантител. Arthritis Rheum. 2009; 61 (6): 772-778.
22. Табет М.М., Хейзинга Т.В., ван дер Хейде Д.М., ван дер Хельмван Мил А.Х. Прогностическая ценность исходных эрозий при недифференцированном артрите . Arthritis Res Ther. 2009; 11 (5): R155.
23. Алетаха Д., Смолен Дж., Уорд ММ. Измерительная функция при ревматоидном артрите: определение обратимых и необратимых компонентов. Arthritis Rheum. , 2006; 54 (9): 2784-2792.
24. Боонен А., Мау В. Экономическое бремя болезни: сравнение ревматоидного артрита и анкилозирующего спондилита. Clin Exp Rheumatol. 2009; 27 (4 доп. 55): S112-S117.
25. Franke LC, Ament AJ, van de Laar MA, Boonen A, Severens JL. Стоимость заболевания ревматоидным артритом и анкилозирующим спондилитом. Clin Exp Rheumatol. 2009; 27 (4 доп. 55): S118-S123.
26. Бирнбаум Х., Пайк С., Кауфман Р., Майнченко М., Кидолези Ю., Цифальди М. Социальные издержки пациентов с ревматоидным артритом в США. Curr Med Res Opin . 2010; 26 (1): 77-90.
27. Flipon E, Brazier M, Clavel G и др. Можно ли определить ранние предикторы будущих издержек хронического артрита? Проект VErA. Фундам Клин Фармакол .2009; 23 (1): 105-113.
28. Салим Б., Маки С., Куинн М. и др. Предотвращает ли использование терапии антагонистами фактора некроза опухоли при плохом прогнозе недифференцированный артрит прогрессирование ревматоидного артрита? Ann Rheum Dis . 2008; 67 (8): 1178-1180.
Недифференцированные спондилоартропатии | Сидарс-Синай
Не то, что вы ищете?Обзор
Когда у человека наблюдаются различные симптомы, которые нельзя классифицировать как конкретное ревматоидное заболевание, считается, что у него недифференцированные спондилоартропатии.
Некоторые врачи не считают это официальным диагнозом. Некоторые считают, что это связано с анкилозирующим спондилитом, псориатическим артритом, спондилитом, связанным с воспалительным заболеванием кишечника или болезнью Крона, и реактивным артритом.
Поскольку симптомы обычно носят общий характер, человеку может быть ошибочно поставлен диагноз тревожности, депрессии или фибромиалгии.
Симптомы
Иногда единственным симптомом у людей с недифференцированной спондилоартропатией является боль.Другие симптомы, которые испытывают люди с недифференцированной спондилоартропатией, включают:
- Длительная, продолжающаяся боль в пояснице, которая появляется постепенно (обычно иррадиирует от ягодиц) в возрасте до 45 лет
- Общая жесткость тела, которая усиливается при пробуждении и улучшается после упражнений
- Отек в ступнях и руках в анамнезе, особенно боль в пятке.
- Общее отсутствие абдоминальных симптомов, хотя до трети пациентов имеют короткие эпизоды диареи или испражняются более двух раз в день.
- Воспаление кишечника, которое можно выявить только при илеоколоноскопии. Симптомы могут напоминать воспалительное заболевание кишечника или бактериальное поражение. При постоянном мониторинге, по-видимому, существует тесная взаимосвязь между воспалением кишечника и суставов.
- Боль в суставах, поражающая как мелкие, так и крупные суставы, в основном в ногах и ступнях. Однако эта боль в суставах может повлиять на одну сторону тела больше, чем на другую.
Воспаление глаза - Бугристая красная сыпь, которая часто возникает при повышении температуры и болях в суставах, которые приходят и уходят
- Симптомы, влияющие на мочевыводящие пути и половые органы
Причины и факторы риска
Как и при реактивном артрите, многие люди с недифференцированными спондилоартропатиями имеют генетический маркер HLA-B27, который предполагает наличие унаследованного элемента этого заболевания.Исследования семей показывают легкое воспаление кишечника или болезнь Крона.
Некоторые данные свидетельствуют о том, что воспаление кишечника может вызывать другие ревматические симптомы, такие как боль в суставах при этом состоянии. Это также может быть вирус, бактерия или микроб.
Диагностика
Природа симптомов недифференцированных спондилоартропатий позволяет легко принять их за другие состояния. Это не так часто, как другие виды ревматоидных заболеваний.Наличие квалифицированного врача, имеющего опыт лечения ревматических состояний, важно для точного диагноза и надлежащего лечения.
Не все врачи осознают, насколько распространена эта проблема, особенно среди женщин. Учитывая, что его часто упускают из виду, становится еще более важным делать домашнюю работу самостоятельно.
Врач проведет физический осмотр и изучит симптомы пациента. Он или она сделает тесты, чтобы исключить инфекции пищеварительной системы. Другие тесты, которые врач может назначить для подтверждения диагноза недифференцированной спондилоартропатии, включают:
- Илеоколоноскопия для определения воспаления в кишечнике
- Анализы крови на различные факторы, включая антитела или реакции иммунной системы
- Тест на ген HLA-B27.Этот тест помогает исключить анкилозирующий спондилит. Этот ген есть у более 95% людей с анкилозирующим спондилитом, тогда как у гораздо меньшего числа людей с недифференцированной спондилоартропатией он есть. (Наличие гена не обязательно означает, что у человека разовьется анкилозирующий спондилит.)
- Может проявляться эрозия суставов кистей и стоп или бедра. Они могут напоминать повреждения суставов, которые часто наблюдаются при ревматоидном артрите
Лечение
Недифференцированные спондилоартропатии, как и связанные с ними ревматические заболевания, являются хроническим заболеванием, которое требует активного участия пациента, а также врача.
Лечение может включать:
- Лекарства — от нестероидных противовоспалительных препаратов, отпускаемых без рецепта, таких как аспирин или ибупрофен, до более сильных обезболивающих и кортикостероидов. Другие препараты, которые могут быть назначены, аналогичны тем, которые используются для лечения симптомов анкилозирующего спондилита, включая альфа-блокатор фактора некроза опухоли
- Тепло для жесткости, включая горячие ванны и теплый душ
- Лед для набухания
- Упражнение
- УЗИ
- Нежный массаж
- Электростимуляторы боли (блоки TENS или TNS)
- Снижение веса для уменьшения нагрузки на суставы
- Улучшение осанки
- Хирургия, в отдельных случаях
Первый год лекарственной терапии впервые возникшего ревматоидного и недифференцированного артрита: общенациональное исследование на основе регистров | BMC Rheumatology
В Финляндии пациентов с ранним артритом лечат в основном ревматологи.Текущее руководство по уходу рекомендует врачам общей практики направлять всех пациентов с подозрением на РА в специализированные клиники. Кроме того, необходима справка ревматолога, чтобы применить специальную компенсацию за противоревматические препараты, по которым мы выявляли наши случаи. Следовательно, в нашу когорту входят те пациенты с артритом, которые были обследованы ревматологами и прописали БПВП и глюкокортикоиды. Очевидно, что не включены все пациенты с UA. Эти факты объясняют, почему в течение одного месяца с даты индексации более 90% пациентов с РА приобрели БПВП и почти 70% метотрексата.У серопозитивных пациентов процент был выше, и в течение одного года только 1,4% серопозитивных и 2,6% серонегативных пациентов с РА не покупали БПВП. Для пациентов с UA охват DMARD был немного меньше. Эти цифры также свидетельствуют о хорошей приверженности к лечению среди финских пациентов с артритом.
Наши результаты могут быть несопоставимы с исследованиями в других условиях. В канадской когорте, изучающей лечение БПВП у 24 942 пациентов с ранним РА в течение года после постановки диагноза в 1997–2006 гг., Только 21% пациентов, лечившихся у терапевта, получали какие-либо БПВП, но 67% из тех, кто лечился у ревматолога, сделали это [ 12].В датской когорте из 1516 пациентов с ранним РА, изучающих начало приема метотрексата в период с 1996 по 2006 год, только 21% пациентов получали метотрексат в течение 90 дней; однако у 13% пациентов было начато повторное БПВП [13]. В исследованиях, основанных на больших когортах РА из коммерческих баз данных США и баз данных заявлений Medicare, начало лечения БПВП в течение одного года после постановки диагноза снизилось с 63 до 56% между когортами 2004–08 и 2009–2012 годов [14, 15]. Другое исследование в США, основанное на базах данных заявлений, показало, что более половины из 63 101 выявленного пациента с РА не получали лечения БПВП в течение 90 дней после постановки диагноза [16].В меньшей канадской когорте из 204 пациентов с ранним РА в 2003–06 гг. Только 23% получали БПВП в течение 3 месяцев и 47% — в течение 6 месяцев [17]. Кроме того, в недавней итальянской когорте из 1336 пациентов с РА менее 40% пациентов начали лечение метотрексатом в течение 3–6 месяцев с момента постановки диагноза [18].
Лучшее покрытие можно найти в современных материалах, леченных ревматологами. В когорте французского ESPOIR из 775 пациентов с ранним воспалительным артритом 77% получили хотя бы один DMARD в среднем через четыре месяца [19].Канадское исследование 339 пациентов с РА показало, что 92% пациентов начали терапию БПВП в течение трех месяцев [20]. В многоцентровой когорте ERAN в Великобритании и Ирландии DMARD были назначены 97% из 808 пациентов с ранним RA; однако среднее время начала БПВП составляло 8 месяцев после появления симптомов [21]. Итальянское исследование показало, что 83% из 10 401 пациента были назначены csDMARD при диагнозе РА, но только 6% из них получали комбинированную терапию [22].
Наш предыдущий анализ финских пациентов с ранним РА в период с 2000 по 2007 год показал, что, хотя в начале периода исследования SSZ был наиболее часто назначаемым DMARD в течение первых 3 месяцев после постановки диагноза, в конце периода наблюдения (2006–2007 гг.) 07) он уступил место метотрексату (69%) и комбинации DMARD (53%) в качестве начального лечения [23].Наши более ранние результаты также показали, что доля пациентов, начинающих тройную комбинацию в течение первого месяца, увеличилась с 6 до 16% в период с 2000 по 07 год. Наши текущие результаты подтверждают, что наблюдается дальнейший рост. Однако только 22% пациентов с ранним серопозитивным РА начали тройную терапию, рекомендованную в последнем Руководстве 2015 г. [8]. Финские рекомендации от 2009 г. одобряли начало тройной терапии и низких доз преднизолона только для пациентов с очень активным РА, но не автоматически в качестве первого выбора для всех пациентов.Кроме того, реальные пациенты с диагнозом РА редко имеют такое активное заболевание, как пациенты в клинических испытаниях [24], и, кроме того, у них могут быть сопутствующие заболевания и полипрагмазия, противопоказанные определенным лекарствам, поэтому возможно, что ревматологи основывают свои решения больше на принципе T2T, чем на рабски следуя определенным рекомендациям [25]. В любом случае, поскольку у нас нет данных об уровнях активности болезни пациентов, нельзя сделать дальнейшие выводы о том, была ли только одна пятая пациентов активным заболеванием, требующим тройной терапии.
Существует различие между руководящими принципами, поощряющими стратегию T2T, с одной стороны, и тем, что действительно происходит на практике. В когорте ESPOIR, где изучалось соблюдение трех рекомендаций EULAR, касающихся начала и ранней корректировки БПВП, уровень соблюдения всех трех рекомендаций среди пациентов с ранним артритом составлял только 23% [26]. Тем не менее, среди тех пациентов, лечение которых соответствовало данным рекомендациям, риск клинического и рентгенологического прогрессирования был ниже.Зная, что выполнение рекомендаций по лечению в реальной жизни всегда неоптимально, строгие национальные рекомендации по лечению, такие как рекомендация о начале тройной терапии при раннем РА в Финляндии, вероятно, приведут к оптимальным результатам.
Количество покупок DMARD может отражать приверженность к лечению, хотя некоторые пациенты не всегда могут покупать лекарства на следующие три месяца, как это обычно бывает. В нашем анализе пациенты, начавшие комбинацию FIN-RACo, в течение первого года совершили в два раза больше покупок DMARD по сравнению с теми пациентами, которые не начали использовать комбинацию FIN-RACo.Частые покупки предполагают регулярное употребление лекарств и хорошую выживаемость комбинации FIN-RACo.
Были опубликованы два финских исследования, основанные на реальных когортах пациентов с ранним артритом. В первый вошли 406 пациентов с ранним РА или НС в период с 2008 по 11 год [27]. Из пациентов с РА через три месяца 20% использовали тройную терапию, 33% — другую комбинацию на основе метотрексата, 36% — монотерапию метотрексатом и 8% — другую монотерапию DMARD; для пациентов с UA соответствующий процент составлял 6, 28, 43 и 17% соответственно.Через год доля пациентов с РА, принимающих различные лекарства, существенно не изменилась. В более поздней (2011–2014 гг.) Когорте FIN-ERA из 611 пациентов с ранним артритом, ранее не имевших DMARD (506 пациентов с РА и 105 пациентов с UA), набранных в пяти финских амбулаторных ревматологических клиниках, комбинированная терапия на основе метотрексата была начата у 68% пациентов и доля тройной комбинации (метотрексат, SSZ и HCQ) составила 31% [28]. Эти результаты, согласующиеся с нашими результатами, показывают, что начало БПВП у пациентов с ранним артритом в Финляндии является комплексным.
В Финляндии нет отдельных рекомендаций по лечению UA, но принцип активного T2T широко используется в клинической практике независимо от диагноза. Рекомендации Европейской лиги EULAR по раннему артриту в 2007 г. рекомендовали пациентам с риском развития стойкого и / или эрозивного артрита как можно раньше назначать БПВП, предпочтительно метотрексат, даже если критерии классификации для конкретного заболевания не выполняются [29]. Последнее обновление рекомендации в 2016 году не внесло серьезных изменений в эти принципы [9].Выполнение рекомендаций EULAR по лечению раннего артрита изучалось у 813 пациентов из когорты ESPOIR в период с 2002 по 2005 год; 78% пациентов начали прием БПВП, 67% — метотрексата и 52% достигли ремиссии [30]. В нашем материале начало DMARD было более полным, но доля на MTX ниже; это можно объяснить тем фактом, что в Финляндии традиционно SSZ назначают при серонегативном олигоартрите.
В нашем исследовании использование самоинъекций биологических DMARD было более распространено среди пациентов с серонегативным RA, чем у пациентов с серопозитивным RA или UA.Серонегативный РА может быть гетерогенной группой заболеваний, как показано в недавнем 10-летнем наблюдательном исследовании [31], что объясняет более низкие результаты лечения csDMARD и большую потребность в переходе на bDMARD.
Недостатком данного исследования является отсутствие клинических данных; у нас нет информации об активности заболевания на момент постановки диагноза или при последующем наблюдении. Кроме того, мы можем упустить пациентов, которых врач не намеревается лечить. Тем не менее, частота серопозитивного РА оставалась стабильной на протяжении этого тысячелетия, частота серонегативного РА несколько снизилась, предположительно из-за изменения диагностики, и по той же причине увеличилась частота возникновения UA [32].Таким образом, маловероятно, что мы упускаем много пациентов. Однако, поскольку это исследование основано на регистрах и у нас отсутствуют данные о продолжительности симптомов до постановки диагноза, возможно, что текущее исследование включает некоторых пациентов, которым поставлен диагноз с опозданием; в этих случаях используемые DMARD представляют собой начальное лечение пациентов, а не лечение раннего ревматического заболевания. Кроме того, мы не знаем, насколько высока доля пациентов с UA позже поставила более конкретный диагноз; это может предложить интересную область для дальнейших исследований.Кроме того, из-за отсутствия клинических данных возможно, что определенная часть пациентов с UA в нашем исследовании может быть несопоставима с пациентами в клиниках так называемого раннего артрита, но иметь хронический воспалительный артрит, требующий специфической противоревматической лекарственной терапии.
Несмотря на то, что у нас нет каких-либо критериев клинического исхода, начало самоинъекции биопрепаратов служило суррогатным маркером неэффективности лечения. Мы ожидали увидеть, что пациенты, получившие комбинированные БПВП в качестве первого курса лечения и, таким образом, по оценке лечащего ревматолога как имеющие активное заболевание, будут теми, кто в конечном итоге начнет принимать биологический препарат раньше и чаще, чем другие пациенты, но, по крайней мере, во время в первый год этого не было.Таким образом, по крайней мере на ранней стадии, комбинированное лечение БПВП оказывается эффективным.
Хотя у нас нет данных о биологических препаратах на основе инфузий, лишь небольшая часть пациентов назначают их в течение первого года после постановки диагноза, периода времени, представляющего интерес для нашего исследования. По данным финского регистрационного исследования ROB-FIN, в 2004–2014 годах первые ингибиторы TNF были назначены пациентам с РА после медианы (IQR) продолжительности заболевания 8,2 (2,4–17) лет, чаще всего с адалимумабом (39%). или этанерцепт (39%), тогда как инфликсимаб был более редким выбором (12%) [33].Согласно последним, но неопубликованным данным регистра ROB-FIN с 2010 по 15 год, использование инфликсимаба в качестве первого биологического препарата снизилось с 7,5 до 4,2% для пациентов с РА (Kalle Aaltonen, личное сообщение). Ритуксимаб был препаратом первого выбора для 20–23% пациентов с РА. Тем не менее, большинство начинало вводить препараты самостоятельно, и средняя точка (IQR) начала приема первого биологического препарата была после 10 (4,4–18) лет продолжительности заболевания. Следовательно, наши результаты первого года лечения вряд ли заметно изменились бы, если бы в него входили препараты на основе инфузий.
Медикаментозная терапия недифференцированного артрита: систематический обзор литературы
Реферат
Недифференцированный артрит (UA) определяется как воспалительный олигоартрит или полиартрит, при котором нельзя поставить окончательный диагноз. Мы провели обзор литературы, чтобы оценить эффективность различных лекарственных препаратов у пациентов с UA. Поиск литературы проводился с использованием электронных баз данных Pubmed, EMBASE и MEDLINE у взрослых с UA или ранним артритом (не соответствует критериям ревматоидного артрита Американского колледжа ревматологии (ACR) 1987 или ACR / Европейской лиги против ревматизма (EULAR) 2010).Медикаментозная терапия состояла из модифицирующих заболевание противоревматических препаратов (DMARD), биологических агентов и пероральных, внутримышечных или внутрисуставных кортикостероидов. Были включены девять публикаций о восьми рандомизированных контролируемых испытаниях (РКИ), две публикации о двух неконтролируемых открытых испытаниях и семь публикаций о трех когортных исследованиях.
/GettyImages-548300647-568f02fc5f9b58eba4855a77.jpg)