Выбор лечебного питания больным диабетом после хирургического вмешательства | partners
Рассмотрен аспект нутриционной поддержки в решении проблемы до- и послеоперационной терапии пациентов с диабетом
Ключевые слова / keywords: Nestle питание после операции, Nestle nutrition after the surgery
Стрелкова ИринаПациенты с сахарным диабетом сталкиваются с необходимостью в хирургическом вмешательстве чаще, чем люди без эндокринных патологий. Согласно статистике, каждый второй больной с таким диагнозом в течение жизни переносит хотя бы одну операцию.
Причиной таких печальных цифр являются, главным образом, осложнения, к которым приводит выраженное нарушение толерантности к глюкозе. Так, снижение иммунитета чревато развитием гнойных воспалений (абсцессов, флегмон), а ангио- и нейропатии провоцируют синдром диабетической стопы, гангрену. Диабетическая ретинопатия также требует оперативного вмешательства – лазерокоагуляции. В то же время у пациентов с диабетом присутствует и обычный риск аппендицита, желчно- и мочекаменной болезни, онкологии, травм, хотя в случае длительного декомпенсированного заболевания эти риски также возрастают в связи с общими системными расстройствами, серьезными метаболическими нарушениями.
Диабетическая ретинопатия также требует оперативного вмешательства – лазерокоагуляции. В то же время у пациентов с диабетом присутствует и обычный риск аппендицита, желчно- и мочекаменной болезни, онкологии, травм, хотя в случае длительного декомпенсированного заболевания эти риски также возрастают в связи с общими системными расстройствами, серьезными метаболическими нарушениями.
Любое хроническое заболевание, требующее радикального метода лечения, а также сопровождающие операцию стресс, кровопотеря и прием сильнодействующих препаратов, включая наркоз, усугубляют течение диабета и состояние пациента в целом. Послеоперационный период часто протекает у таких больных с осложнениями. Катаболические процессы, иммунные нарушения, скомпрометированный статус сердечно-сосудистой и нервной систем в значительной степени замедляют нормальные процессы регенерации. Нередко происходит инфицирование послеоперационных ран, обострение других хронических заболеваний (ИБС, почечной и печеночной недостаточности и т.
Патогенетический механизм метаболического стресса, сопровождающего хирургическую операцию, связан с торможением синтеза инсулина и активацией контринсулиновых факторов, из-за чего чувствительность тканей к инсулину падает, и обычные дозы препарата не могут скомпенсировать дефицит. Гиперадреналинемия, гипергликемия, активная работа калликреин-кининовой системы способствуют развитию обезвоживания и кетоацидоза. На фоне такого нестабильного состояния пациента любой пропуск приема пищи, в частности из-за плохого аппетита, или недостаточная сбалансированность рациона по питательным веществам может привести к резкому изменению уровня глюкозы крови, ухудшению состояния и, соответственно, прогноза.
По приведенным выше причинам на первый план в решении проблемы до- и послеоперационной терапии пациентов с диабетом, выходит аспект нутриционной поддержки.
При грамотном подготовительном питании и адекватной терапии, при компенсации сахарного диабета, этот диагноз не является противопоказанием для операции, и прогноз вмешательства не сильно отличается от соответствующих перспектив у пациентов без нарушения толерантности к глюкозе.
Питание важно как перед большими полостными или ампутационными операциями, так и перед малыми процедурами: удалением вросшего ногтя, атером, лазерокоагуляции и т.д.
Каковы же задачи, стоящие перед универсальной диетой, предназначенной для поддержки пациентов с сахарным диабетом до и после операции?
- Коррекция гликемического и липидного профиля, позволяющая в сочетании с лекарственными средствами добиться компенсации заболевания.
- Снабжение необходимыми нутриентами для обеспечения полноценной регенерации тканей, восполнение образовавшегося белково-энергетического дефицита.
- Стимуляция иммунитета, максимальное снижение риска инфекционных осложнений, обострений хронической патологии.

- Поддержка желудочно-кишечного тракта и активизация процессов всасывания.
- Ускорение восстановительного периода и профилактика рецидивов.
Смесь Ресурс Диабет Плюс от Nestle создана с учетом современных данных об особенностях питания пациентов с диабетом, на основе выведенных совсем недавно диабет-специфических формул. Благодаря уникальному сбалансированному составу продукт выполняет все поставленные перед ним задачи и потому рекомендуется хирургами и эндокринологами для больных с диабетом в послеоперационном периоде.
Состав Resource Diabet Plus представлен медленно всасывающимися углеводами, сывороточными белками и казеином, большим количеством MUFA (мононенасыщенных жирных кислот) при низком содержании SFA (насыщенных жирных кислот), пищевыми волокнами, микроэлементами и витаминами (А, D, K, E, B1, B6, B12, биотин, фолиевая, пантотеновая кислота и пр). Достаточно высокая калорийность продукта – 320 ккал на 200 мл – позволяет утолить чувство голода, но не перегружает ослабленный организм.
Эффекты компонентов Resource Diabet Plus
- Изомальтоза служит источником глюкозы и фруктозы и обеспечивает низкий гликемический индекс продукта. Изомальтоза улучшает контроль гликемии даже у пациентов, находящихся в критическом состоянии, способствуя снижению инсулинового ответа и уровня HbA1. Она положительно влияет не только на углеводный, но и на липидный обмен, уменьшая содержание ЛПНП (липопротеидов низкой плотности) и увеличивая ЛПВП (липопротеиды высокой плотности).
- Сывороточный протеин и казеин содержат полный набор аминокислот, в том числе незаменимых, необходимых для полноценной регенерации и для восстановления мышечной массы при ее дефиците. Кроме того, молочный белок стимулирует выработку инсулина и снижает уровень постпрандиальной гликемии.
- MUFA (мононенасыщенные жирные кислоты) также способствует коррекции гликемического и липопротеинового профиля, положительно сказывается на массе и композиционном составе тела.
 Крайне низкое содержание в составе Ресурс Диабет Плюс транс-жиров уменьшает риск кардиоваскулярных осложнений, что особенно важно при сопутствующем атеросклерозе и диагностированном метаболическом синдроме.
Крайне низкое содержание в составе Ресурс Диабет Плюс транс-жиров уменьшает риск кардиоваскулярных осложнений, что особенно важно при сопутствующем атеросклерозе и диагностированном метаболическом синдроме. - Смесь пищевых волокон Prebio1+ и PHGG (частично гидролизованная гуаровая камедь) оптимизирует работу желудочно-кишечного тракта и благотворно влияет на состояние кишечной стенки, нормализует микрофлору. Пассаж пищи и всасывание углеводов замедляется, снижается концентрация сывороточных транс-жиров, выраженность постпрандиальной гликемии.
Resource Diabet Plus назначается пациентам с сахарным диабетом в пред- и постоперационном периоде. Его применение в качестве добавки к ежедневному питанию или в качестве его полной замены способствует компенсации заболевания, минимизации риска осложнений и ускорению реабилитации.
Хирургия диабета ⋆ Проф Др Альпер Челик
Что такое хирургия диабета?
Диабет является заболеванием, вызванным сидячим образом жизни, несбалансированным питанием или генетическими причинами. Хотя при диабете 1 типа инсулин не производится организмом, у пациентов 2 типа диабета организм производит инсулин, но организм пациента не в состоянии использовать его. Вот почему уровень сахара в крови всегда высокий. Это приводит к повреждению органов. При диабете, классическое лечение это снижение уровня сахара в крови. Хирургия диабета также метод лечения заболевания. Эта операция, которая называется метаболической хирургией, выполняемая для больных сахарным диабетом 2 типа. Таким образом, существующий в организме инсулин используется без проблем. В результате, высокий уровень сахара в крови снижается.
Хотя при диабете 1 типа инсулин не производится организмом, у пациентов 2 типа диабета организм производит инсулин, но организм пациента не в состоянии использовать его. Вот почему уровень сахара в крови всегда высокий. Это приводит к повреждению органов. При диабете, классическое лечение это снижение уровня сахара в крови. Хирургия диабета также метод лечения заболевания. Эта операция, которая называется метаболической хирургией, выполняемая для больных сахарным диабетом 2 типа. Таким образом, существующий в организме инсулин используется без проблем. В результате, высокий уровень сахара в крови снижается.
Цель хирургии диабета
Предполагаемым условием для лечения диабета является устранение резистентности к инсулину в организме. Таким образом, количество гормонов увеличивается. Если тип диабета 1, то лечением является инсулинная терапия. Если 2 тип и испробованы изменения в образе жизни, диета, лекарства, но начались повреждения органов, то необходимо обратиться к хирургии.
Хирургия диабета выполняется тем у кого диабет 2 типа, лишний вес, высокий уровень сахара в крови, несмотря на лекарства используемые и инсулин, сахар крови выше предела. Хирургия диабета выполняется как закрытая операция, через маленькие разрезы. 50% желудка удаляется, делаются изменения в тонкой кишке. После этого изменения, исходит сигнал из поджелудочной железы для секреции инсулина и эффективность увеличивается. Таким образом, диабет 2 типа полностью проходит. Также люди избавляются от ожирения после этой операции. Преимущество данной операции состоит из деталей, таких как не столь болезненным, как открытые операции, не имея проблем с легкими, быстрое возвращение к нормальной жизни, никаких следов от операции.
Могут ли диабетики 1 типа оперироваться?
Диабетики типа 1 не имеют инсулина в организме. Поэтому они не могут выполнить эту операцию. У пациентов с диабетом типа 2, важно, чтобы поджелудочная железа была активна, потому что цель состоит в том, чтобы использовать существующий инсулин правильно и адекватно. Это возможно с операцией.
Это возможно с операцией.
При диабете второго типа такие факторы как, прогрессирование заболевания, повреждения органов, берутся во внимание в процессе принятия решения об операции после тщательных обследований. Должны быть проведены все анализы и обследования пациента. Потому что каждая операция – это риск. Иногда, если классическе методы безуспешны и в конечном счете приводит к потере органов, единственным средством может быть хирургическая операция. Если пациенты не соблюдают диету и невнимательны к образу жизни, то их жизни могут перейти в проблемный период. Несмотря на лечение с помощью лекарств, болезнь не вылечится. И хирургическое вмешательство становится неизбежным.
Метаболическая хирургияВ этой операции, известной как хирургия диабета, применяется процедура лечения диабета 2 типа, возникший из-за нарушения привычек питания и качества жизни у пациента. Цель состоит в том, чтобы убрать резистентность к инсулину. С хирургической процедурой, количество потребляемой еды уменьшается и гормоны становятся гораздо более активными, таким образом проблема диабета и ожирения решается. После уменьшения желудка при сахарном диабете, потеря веса у пациента ускоряется после операции. Для метаболических операций необходимо иметь инсулин в организме, иначе он не работает.
После уменьшения желудка при сахарном диабете, потеря веса у пациента ускоряется после операции. Для метаболических операций необходимо иметь инсулин в организме, иначе он не работает.
Что происходит после лечения диабета хирургии
После операции на диабет, не будет частого чувства голода, как раньше. Из-за отсутствия аппетита, вы столкнетесь недоеданием. Когда эти неприятности уходят, тело привыкает к нормальному порядку, и пациент будет чувствовать себя намного лучше. После операции на лечение диабета, следует пить много воды. Тело нуждается в воде. Потребление воды имеет важное значение, поскольку отсутствие питания и потребления воды будет способствовать чувству вялости пациента. Поскольку привычки питания находятся под контролем врача около 6 месяцев после операции, наименьшее нарушение диеты поспособствует возврату сахара. По этой причине, операция на диабет, который идеально подходит для диабетика.
Лечебное питание у госпитализированных пациентов с диабетом
Недавно опубликованные статьи, представляющие особый интерес, были отмечены как:
• Важные,
•• Важнейшие
1. Correia MI, Waitzberg DL. Влияние недоедания на заболеваемость, смертность, продолжительность пребывания в стационаре и затраты оцениваются с помощью многофакторного модельного анализа. Клиническое питание (Эдинбург, Шотландия) 2003;22:235–9. [PubMed] [Google Scholar]
Correia MI, Waitzberg DL. Влияние недоедания на заболеваемость, смертность, продолжительность пребывания в стационаре и затраты оцениваются с помощью многофакторного модельного анализа. Клиническое питание (Эдинбург, Шотландия) 2003;22:235–9. [PubMed] [Google Scholar]
2•. Циглер ТР. Парентеральное питание у тяжелобольных. Медицинский журнал Новой Англии. 2009 г.;361:1088–1097. Это современная обзорная статья, описывающая современные доказательства использования ПП у госпитализированных пациентов. [Бесплатная статья PMC] [PubMed] [Google Scholar]
3. Daley J, Khuri SF, Henderson W, et al. Корректировка риска послеоперационной заболеваемости для сравнительной оценки качества хирургической помощи: результаты Национального исследования хирургического риска по делам ветеранов. J Am Coll Surg. 1997; 185:328–40. [PubMed] [Google Scholar]
4. Warnold I, Lundholm K. Клиническое значение предоперационного нутритивного статуса у 215 нераковых пациентов. Энн Сург. 1984;199:299–305. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [Google Scholar]
5. Giner M, Laviano A, Meguid MM, et al. В 1995 г. корреляция между недоеданием и плохим исходом у пациентов в критическом состоянии все еще существовала. Питание (Бербанк, округ Лос-Анджелес, Калифорния, 1996; 12:23–9. [PubMed] [Google Scholar]
6. Marik PE. Мониторинг терапевтических вмешательств у пациентов с сепсисом в критическом состоянии. Nutr Clin Pract. 2004; 19:423– 32. [PubMed] [Google Scholar]
7. Martindale RG, Cresci G. Предотвращение инфекционных осложнений с помощью вмешательства в питание, Jpen, 2005; 29.: S53–56. [PubMed] [Google Scholar]
8. Стрикленд С.С. Функциональные последствия недоедания взрослых в развивающихся странах: обзор. J Physiol Anthropol Appl Human Sci. 2002; 21:1–9. [PubMed] [Google Scholar]
9. Вайцберг Д.Л., Торриньяс Р.С., Хасинто Т.М. Новые парентеральные липидные эмульсии для клинического применения. Япония 2006; 30: 351–67. [PubMed] [Google Scholar]
10. Heyland DK, Montalvo M, MacDonald S, et al. Полное парентеральное питание у хирургического больного: метаанализ. Может J Surg. 2001;44:102–11. [PubMed] [Академия Google]
Heyland DK, Montalvo M, MacDonald S, et al. Полное парентеральное питание у хирургического больного: метаанализ. Может J Surg. 2001;44:102–11. [PubMed] [Академия Google]
11. Залога Г.П. Улучшение результатов с помощью специализированной нутритивной поддержки. Япония 2005; 29: С49–52. [PubMed] [Google Scholar]
12. Cresci G. Ориентация на использование специализированных пищевых формул в хирургии и интенсивной терапии. Япония 2005;29:S92–95. [PubMed] [Google Scholar]
13. Baker EH, Janaway CH, Philips BJ, et al. Гипергликемия связана с неблагоприятными исходами у пациентов, госпитализированных с обострением хронической обструктивной болезни легких. грудная клетка. 2006; 61: 284–9.. [Бесплатная статья PMC] [PubMed] [Google Scholar]
14. Falciglia M, Freyberg RW, Almenoff PL, et al. Смертность, связанная с гипергликемией, у пациентов в критическом состоянии зависит от диагноза при поступлении. Крит Уход Мед. 2009; 37:3001–9. [Бесплатная статья PMC] [PubMed] [Google Scholar]
15. Kosiborod M, Inzucchi SE, Spertus JA, et al. Повышенный уровень глюкозы при поступлении и смертность у пожилых пациентов, госпитализированных с сердечной недостаточностью. Тираж. 2009; 119:1899–907. [PubMed] [Google Scholar]
Kosiborod M, Inzucchi SE, Spertus JA, et al. Повышенный уровень глюкозы при поступлении и смертность у пожилых пациентов, госпитализированных с сердечной недостаточностью. Тираж. 2009; 119:1899–907. [PubMed] [Google Scholar]
16. Krinsley JS. Связь между гипергликемией и повышенной госпитальной смертностью в гетерогенной популяции пациентов в критическом состоянии. Мэйо Клин Proc. 2003; 78: 1471–8. [PubMed] [Академия Google]
17. Umpierrez GE, Isaacs SD, Bazargan N, et al. Гипергликемия: независимый маркер госпитальной смертности у пациентов с недиагностированным сахарным диабетом. J Clin Endocrinol Metab. 2002; 87: 978–82. [PubMed] [Google Scholar]
18••. Керлл М., Динардо М., Ношезе М. и др. Выбор меню, гликемический контроль и удовлетворенность стандартными и контролируемыми пациентом планами питания с последовательными углеводами у госпитализированных пациентов с диабетом. Качество и безопасность в здравоохранении. 2010;19:355–359. Это единственное рандомизированное контролируемое исследование, сравнивающее исходы, связанные с диабетом, у пациентов с диабетом, получающих различные планы питания в больнице. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
19. Inzucchi SE. Клиническая практика. Лечение гипергликемии в условиях стационара. N Eng J Med. 2006; 355: 1903–11. [PubMed] [Google Scholar]
20. Американская диабетическая ассоциация. Стандарты медицинской помощи при сахарном диабете–2011. Уход за диабетом. 34 (Приложение 1): S11–61. [Бесплатная статья PMC] [PubMed] [Google Scholar]
21. Клемент С., Брейтуэйт С.С., Маги М.Ф. и др. Ведение диабета и гипергликемии в больницах. Уход за диабетом. 2004; 27: 553–91. [PubMed] [Google Scholar]
22. Schafer RG, Bohannon B, Franz MJ, et al. Рекомендации по питанию при сахарном диабете для учреждений здравоохранения. Уход за диабетом. 2004; 27 (Приложение 1): S55–57. [PubMed] [Google Scholar]
23. Swift CS, Boucher JL. Диетотерапия для госпитализированного больного сахарным диабетом. Эндокр Практ. 2006; 12 (Приложение 3): 61–7. [PubMed] [Академия Google]
24. МакМахон М.М., Рицца Р.А. Нутритивная поддержка госпитализированных больных сахарным диабетом. Мэйо Клин Proc. 1996; 71: 587–94. [PubMed] [Google Scholar]
Мэйо Клин Proc. 1996; 71: 587–94. [PubMed] [Google Scholar]
25. Bantle JP, Wylie-Rosett J, Albright AL, et al. Рекомендации по питанию и вмешательства при диабете: заявление о позиции Американской диабетической ассоциации. Уход за диабетом. 2008; 31 (Приложение 1): S61–78. [PubMed] [Google Scholar]
26. McClave SA, Martindale RG, Vanek VW, et al. Руководство по обеспечению и оценке нутриционной поддержки у взрослых пациентов в критическом состоянии: Общество медицины критических состояний (SCCM) и Американское общество парентерального и энтерального питания (A.S.P.E.N.) Jpen. 2009 г.;33:277–316. [PubMed] [Google Scholar]
27. Warren J, Bhalla V, Cresci G. Улучшение послеоперационной диеты: хирургическая догма против доказательной медицины. Нутр Клин Практ. 2011;26:115–25. [PubMed] [Google Scholar]
28. Андерсон А.Д., Джейн П.К., Макфи Дж. Парентеральное питание у больных в критическом состоянии. Интенсивная терапия Мед. 2003;29:2103. ответ автора 2104. [PubMed] [Google Scholar]
29. Bellantone R, Doglietto G, Bossola M, et al. Предоперационное парентеральное питание истощенных хирургических больных. Акта Чир Сканд. 1988;154:249–51. [PubMed] [Google Scholar]
Bellantone R, Doglietto G, Bossola M, et al. Предоперационное парентеральное питание истощенных хирургических больных. Акта Чир Сканд. 1988;154:249–51. [PubMed] [Google Scholar]
30. Klein S, Kinney J, Jeejeebhoy K, et al. Нутритивная поддержка в клинической практике: обзор опубликованных данных и рекомендации для будущих направлений исследований. Краткое изложение конференции, организованной Национальным институтом здравоохранения, Американским обществом парентерального и энтерального питания и Американским обществом клинического питания. Am J Clin Nutr. 1997; 66: 683–706. [PubMed] [Google Scholar]
31. Марик ЧП. Смерть от полного парентерального питания: part deaux. Крит Уход Мед. 2006; 34:3062. ответ автора 3062–3063. [PubMed] [Академия Google]
32. Schafer RG, Bohannon B, Franz M, et al. Перевод рекомендаций по питанию при сахарном диабете для учреждений здравоохранения. Уход за диабетом. 1997; 20:96–105. [PubMed] [Google Scholar]
33. Kreymann KG, Berger MM, Deutz NE, et al. Руководство ESPEN по энтеральному питанию: Интенсивная терапия. Клиническое питание (Эдинбург, Шотландия) 2006; 25:210–223. [PubMed] [Google Scholar]
Руководство ESPEN по энтеральному питанию: Интенсивная терапия. Клиническое питание (Эдинбург, Шотландия) 2006; 25:210–223. [PubMed] [Google Scholar]
34. Через MA, Mechanick JI. Стационарное энтеральное и парентеральное [корректированное] питание больных сахарным диабетом. Курр Диаб Респ. 2010; 11:99–105. [PubMed] [Google Scholar]
35. Craig LD, Nicholson S, SilVerstone FA, et al. Использование энтеральной смеси с пониженным содержанием углеводов и модифицированным жиром для улучшения метаболического контроля и клинических результатов у резидентов длительного ухода с диабетом 2 типа: результаты пилотного исследования. Питание (Бербанк, округ Лос-Анджелес, Калифорния, 1998; 14:529–34. [PubMed] [Google Scholar]
36. Leon-Sanz M, Garcia-Luna PP, Sanz-Paris A, et al. Контроль гликемии и липидов. у госпитализированных пациентов с диабетом 2 типа: оценка двух формул энтерального питания (с низким содержанием углеводов и высоким содержанием мононенасыщенных жиров или с высоким содержанием углеводов) Jpen, 2005;29: 21–9. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
37. Elia M, Ceriello A, Laube H, et al. Энтеральная нутритивная поддержка и использование специфических для диабета смесей для пациентов с диабетом: систематический обзор и метаанализ. Уход за диабетом. 2005; 28: 2267–79. [PubMed] [Google Scholar]
38•. Алиш С.Дж., Гарви В.Т., Маки К.С. и др. Диабетическая энтеральная формула улучшает вариабельность гликемии у пациентов с диабетом 2 типа. Диабетическая технология и терапия. 2010;12:419–425. Это рандомизированное двойное слепое перекрестное исследование, сравнивающее влияние непрерывного 5-дневного введения нескольких энтеральных смесей на углеводный обмен у амбулаторных пациентов с сахарным диабетом 2 типа. [PubMed] [Академия Google]
39•. Ceriello A, Lansink M, Rouws CH, et al. Введение новой диабетической энтеральной смеси приводит к улучшению 24-часового профиля глюкозы у пациентов с диабетом 2 типа. Исследования диабета и клиническая практика. 2009; 84: 259–266. Это рандомизированное двойное слепое перекрестное исследование, изучающее результаты гликемии у амбулаторных пациентов с сахарным диабетом 2 типа, получающих болюсные энтеральные смеси в течение 24 часов. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
40. Pohl M, Mayr P, Mertl-Roetzer M, et al. Гликемический контроль у пациентов с диабетом II типа, находящихся на искусственном вскармливании, с помощью новой энтеральной смеси с низким содержанием углеводов и высоким содержанием мононенасыщенных жирных кислот: рандомизированное контролируемое исследование. Eur J Clin Nutr. 2005;59: 1221–32. [PubMed] [Google Scholar]
41. Mentec H, Dupont H, Bocchetti M, et al. Непереносимость верхних отделов пищеварительного тракта при энтеральном питании у больных в критическом состоянии: частота, факторы риска, осложнения. Крит Уход Мед. 2001; 29:1955–61. [PubMed] [Google Scholar]
42. Heyland DK, Cook DJ, Schoenfeld PS, et al. Влияние подкисленного энтерального питания на колонизацию желудка у пациентов в критическом состоянии: результаты многоцентрового рандомизированного исследования. Канадская группа испытаний интенсивной терапии. Крит Уход Мед. 1999;27:2399–406. [PubMed] [Google Scholar]
43••. Korytkowski MT, Salata RJ, Koerbel GL, et al. Инсулинотерапия и гликемический контроль у госпитализированных больных сахарным диабетом на фоне терапии энтеральным питанием: рандомизированное контролируемое клиническое исследование. Уход за диабетом. 2009; 32: 594–596. В этом рандомизированном контролируемом исследовании авторы протестировали различные стратегии введения инсулина для контроля гипергликемии у госпитализированных пациентов с диабетом, получающих энтеральное питание. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Korytkowski MT, Salata RJ, Koerbel GL, et al. Инсулинотерапия и гликемический контроль у госпитализированных больных сахарным диабетом на фоне терапии энтеральным питанием: рандомизированное контролируемое клиническое исследование. Уход за диабетом. 2009; 32: 594–596. В этом рандомизированном контролируемом исследовании авторы протестировали различные стратегии введения инсулина для контроля гипергликемии у госпитализированных пациентов с диабетом, получающих энтеральное питание. [Бесплатная статья PMC] [PubMed] [Google Scholar]
44. Умпьеррес Г.Э. Базальный инсулин в сравнении со скользящей шкалой регулярного инсулина у госпитализированных пациентов с гипергликемией во время терапии энтеральным питанием. Уход за диабетом. 2009;32:751–3. [Бесплатная статья PMC] [PubMed] [Google Scholar]
45. Детский А.С., Бейкер Дж.П., О’Рурк К. и соавт. Периоперационное парентеральное питание: метаанализ. Энн Интерн Мед. 1987; 107: 195–203. [PubMed] [Google Scholar]
46. Muller JM, Brenner U, Dienst C, et al. Предоперационное парентеральное питание у больных раком желудочно-кишечного тракта. Ланцет. 1982;1:68–71. [PubMed] [Google Scholar]
Предоперационное парентеральное питание у больных раком желудочно-кишечного тракта. Ланцет. 1982;1:68–71. [PubMed] [Google Scholar]
47. Андерсон А.Д., Палмер Д., Макфи Дж. Периферийное парентеральное питание. Бр Дж Сур. 2003;90:1048–54. [PubMed] [Google Scholar]
48. Bellantone R, Doglietto GB, Bossola M, et al. Предоперационное парентеральное питание у хирургических больных высокого риска. Япония 1988; 12:195–197. [PubMed] [Google Scholar]
49. Klein S, Kinney J, Jeejeebhoy K, et al. Нутритивная поддержка в клинической практике: обзор опубликованных данных и рекомендации для будущих направлений исследований. Лечебное питание (Эдинбург, Шотландия) 1997;16:193–218. [PubMed] [Google Scholar]
50. Cheung NW, Napier B, Zaccaria C, et al. Гипергликемия связана с неблагоприятными исходами у пациентов, получающих полное парентеральное питание. Уход за диабетом. 2005; 28: 2367–71. [PubMed] [Google Scholar]
51. der Voort PH, Feenstra RA, Bakker AJ, et al. Внутривенное потребление глюкозы независимо связано со смертностью в отделениях интенсивной терапии и в больницах: аргумент в пользу токсичности глюкозы у пациентов в критическом состоянии. Клин Эндокринол. 2006;64:141–5. [PubMed] [Академия Google]
Внутривенное потребление глюкозы независимо связано со смертностью в отделениях интенсивной терапии и в больницах: аргумент в пользу токсичности глюкозы у пациентов в критическом состоянии. Клин Эндокринол. 2006;64:141–5. [PubMed] [Академия Google]
52. Лин Л.Я., Лин Х.К., Ли П.С. и др. Гипергликемия коррелирует с исходами у пациентов, получающих полное парентеральное питание. Am J Med Sci. 2007; 333: 261–5. [PubMed] [Google Scholar]
53. Pasquel FJ, Spiegelman R, McCauley M, et al. Гипергликемия при тотальном парентеральном питании: важный маркер неблагоприятного исхода и летальности у госпитализированных пациентов. Уход за диабетом. 2010;33:739–41. [PMC free article] [PubMed] [Google Scholar]
54. Cheung NW, Wong VW, McLean M. Гипергликемия: Интенсивная инфузия инсулина при инфаркте (HI-5): рандомизированное контролируемое исследование инфузионной терапии миокарда инфаркт. Уход за диабетом. 2006;29: 765–70. [PubMed] [Google Scholar]
55. Сингер П., Бергер М. М., Ван ден Берге Г. и др. Руководство ESPEN по парентеральному питанию: интенсивная терапия. Клиническое питание (Эдинбург, Шотландия) 2009; 28:387–400. [PubMed] [Google Scholar]
М., Ван ден Берге Г. и др. Руководство ESPEN по парентеральному питанию: интенсивная терапия. Клиническое питание (Эдинбург, Шотландия) 2009; 28:387–400. [PubMed] [Google Scholar]
56. Ziegler TR. Нутритивная поддержка при критическом заболевании — устранение пробелов в доказательствах. Медицинский журнал Новой Англии. 2011; 365: 562–564. [PubMed] [Google Scholar]
57••. Casaer MP, Mesotten D, Hermans G, et al. Раннее и позднее парентеральное питание у взрослых в критическом состоянии. Медицинский журнал Новой Англии. 2011; 365: 506–517. Результаты этого исследования установили новые стандарты начала питания у госпитализированных пациентов, нуждающихся в ПП. [PubMed] [Академия Google]
58. Buenestado A, Cortijo J, Sanz MJ, et al. Нейтральное влияние липидной эмульсии на основе оливкового масла на функции нейтрофилов и взаимодействие лейкоцитов и эндотелиальных клеток. Япония 2006; 30: 286–96. [PubMed] [Google Scholar]
59. McCowen KC, Friel C, Sternberg J, et al. Гипокалорийное полное парентеральное питание: эффективность в профилактике гипергликемии и инфекционных осложнений – рандомизированное клиническое исследование. Крит Уход Мед. 2000; 28:3606–11. [PubMed] [Google Scholar]
Гипокалорийное полное парентеральное питание: эффективность в профилактике гипергликемии и инфекционных осложнений – рандомизированное клиническое исследование. Крит Уход Мед. 2000; 28:3606–11. [PubMed] [Google Scholar]
60. Siqueira J, Smiley D, Newton C, et al. 2011 Замена стандартного соевого масла липидной эмульсией на основе оливкового масла в парентеральном питании: сравнение сосудистых, метаболических и воспалительных эффектов. Журнал клинической эндокринологии и метаболизма. 2011;96:3207–3216. [Бесплатная статья PMC] [PubMed] [Google Scholar]
61. Якуб П. Липиды и иммунный ответ. Curr Opin Clin Nutr Metab Care. 1998; 1: 153–61. [PubMed] [Google Scholar]
62. Якуб П. Мононенасыщенные жирные кислоты в парентеральном питании; оценка рисков и выгод. Бр Дж Нутр. 2005; 94: 867–8. [PubMed] [Google Scholar]
63. Сала-Вила А., Барбоза В.М., Колдер П.С. Оливковое масло в парентеральном питании. Curr Opin Clin Nutr Metab Care. 2007; 10: 165–74. [PubMed] [Академия Google]
64. Nordenstrom J, Jarstrand C, Wiernik A. Снижение хемотаксиса и случайная миграция лейкоцитов во время инфузии интралипидов. Am J Clin Nutr. 1979; 32: 2416–22. [PubMed] [Google Scholar]
Nordenstrom J, Jarstrand C, Wiernik A. Снижение хемотаксиса и случайная миграция лейкоцитов во время инфузии интралипидов. Am J Clin Nutr. 1979; 32: 2416–22. [PubMed] [Google Scholar]
65. Waitzberg DL, Saito H, Plank LD, et al. Послеоперационные инфекции уменьшаются благодаря специализированной нутритивной поддержке. Мир J Surg. 2006; 30:1592–604. [PubMed] [Google Scholar]
66. Якуб П. Мононенасыщенные жиры и иммунная функция. Proc Nutr Soc. 1998; 57: 511–20. [PubMed] [Академия Google]
67. Госманов А.Р., Смайли Д.Д., Робалино Г. и соавт. Влияние пероральной и внутривенной жировой нагрузки на кровяное давление, функцию эндотелия, симпатическую активность и окислительный стресс у здоровых людей с ожирением. Am J Physiol. 2010; 299:E953–958. [Бесплатная статья PMC] [PubMed] [Google Scholar]
68. Umpierrez GE, Smiley D, Robalino G, et al. Внутривенное повышение артериального давления, индуцированное интралипидами, и дисфункция эндотелия у афроамериканцев с ожирением и диабетом 2 типа. J Clin Endocrinol Metab. 2009 г.;94:609–14. [Бесплатная статья PMC] [PubMed] [Google Scholar]
J Clin Endocrinol Metab. 2009 г.;94:609–14. [Бесплатная статья PMC] [PubMed] [Google Scholar]
69. Garcia-de-Lorenzo A, Denia R, Atlan P, et al. Парентеральное питание, обеспечивающее ограниченное количество линолевой кислоты у пациентов с тяжелыми ожогами: рандомизированное двойное слепое исследование липидной эмульсии на основе оливкового масла и триацилглицеролов со средней/длинной цепью. Бр Дж Нутр. 2005; 94: 221–30. [PubMed] [Google Scholar]
Управление питанием после операции обходного желудочного анастомоза | Diabetes Spectrum
Пропустить пункт назначенияПитание FYI| 01 апреля 2005 г.
Джуди Дауд, Массачусетс, Род-Айленд, LDNDiabetes Spectr 2005;18(2):82–84
https://doi.org/10.2337/diaspect.18.2.82
- Разделенный экран
- Взгляды
- Содержание артикула
- Рисунки и таблицы
- Видео
- Аудио
- Дополнительные данные
- Экспертная оценка
- Нажмите здесь, чтобы открыть pdf в другом окне PDF для
- Делиться
- Фейсбук
- Твиттер
- Электронная почта
Иконка Цитировать Цитировать
Получить разрешения
Цитата
Джуди Дауд; Управление питанием после операции обходного желудочного анастомоза. Diabetes Spectr 1 апреля 2005 г.; 18 (2): 82–84. https://doi.org/10.2337/diaspect.18.2.82
Diabetes Spectr 1 апреля 2005 г.; 18 (2): 82–84. https://doi.org/10.2337/diaspect.18.2.82
Скачать файл цитаты:
- Рис (Зотеро)
- Менеджер ссылок
- EasyBib
- Подставки для книг
- Менделей
- Бумаги
- Конечная примечание
- РефВоркс
- Бибтекс
Расширенный поиск
Операция обходного желудочного анастомоза является высокоэффективным методом снижения веса при морбидном ожирении. Хирургия — это инструмент, с помощью которого отдельные пациенты учатся контролировать потребление калорий, не чувствуя чрезмерного голода. В результате можно значительно снизить вес, чтобы улучшить симптомы многих хронических заболеваний, таких как ишемическая болезнь сердца и диабет. Тот факт, что большинство страховщиков, включая Medicare, оплачивают процедуру, свидетельствует о ее эффективности.
Процесс предоперационного скрининга в Baystate Surgical Associates
Увеличить
Увеличить
Процесс до и после операции чреват ловушками , что возлагало на него большую ответственность. как хирургической бригады, так и пациента. Команда должна состоять из одного или нескольких сертифицированных бариатрических хирургов, опытных диетологов, медсестер и психологов. Обширный предоперационный скрининг важен (таблица 1).
В течение 1–2 лет после операции теряется до 60–70% избыточной массы тела 1 в результате четырех послеоперационных явлений (табл. 2). Потребляется меньше калорий из-за меньшего объема желудка пациентов. Кроме того, пациенты испытывают снижение аппетита , возможно, из-за снижения выработки стимулирующих аппетит гормонов, таких как грелин. Выпивоподобное поведение, как правило, исчезает после операции, поскольку оно приводит к немедленным негативным последствиям в виде боли и рвоты. Нарушение всасывания калорий возникает в результате обхода тонкой кишки. Байпас также вызывает демпинг-синдром у тех пациентов, которые потребляют пищу или напитки, содержащие концентрацию сахара. Этот синдром вызывает симптомы, похожие на гипогликемическую реакцию. Из-за этого пагубного эффекта демпинг-синдром хорошо работает, чтобы отговорить пациентов от употребления сладкого. И, наконец, повышенная физическая активность , которая способствует снижению веса и помогает предотвратить его повторный рост, становится все более возможной по мере того, как пациенты теряют вес. На самом деле, у пациентов, которые не ведут активный образ жизни, вероятно существенное увеличение веса.
Выпивоподобное поведение, как правило, исчезает после операции, поскольку оно приводит к немедленным негативным последствиям в виде боли и рвоты. Нарушение всасывания калорий возникает в результате обхода тонкой кишки. Байпас также вызывает демпинг-синдром у тех пациентов, которые потребляют пищу или напитки, содержащие концентрацию сахара. Этот синдром вызывает симптомы, похожие на гипогликемическую реакцию. Из-за этого пагубного эффекта демпинг-синдром хорошо работает, чтобы отговорить пациентов от употребления сладкого. И, наконец, повышенная физическая активность , которая способствует снижению веса и помогает предотвратить его повторный рост, становится все более возможной по мере того, как пациенты теряют вес. На самом деле, у пациентов, которые не ведут активный образ жизни, вероятно существенное увеличение веса.
Механизмы, вызывающие послеоперационную потерю веса
Увеличить
Увеличить
В отличие от других программ снижения веса, хирургический процесс позволяет пациентам лучше контролировать себя.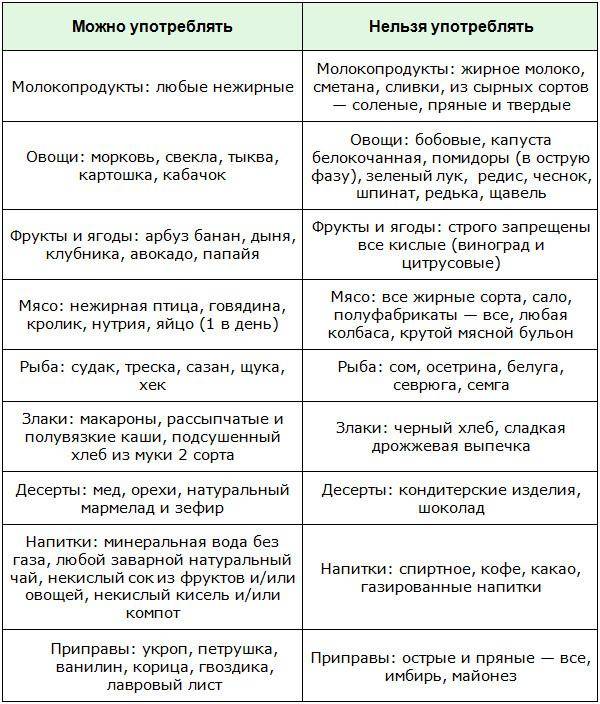 Толерантность к глюкозе улучшается до такой степени, что более 80% пациентов с диабетом сохраняют нормальный уровень глюкозы в плазме, гликозилированного гемоглобина и инсулина после операции. 2 Однако этот процесс требует значительных изменений в привычках образа жизни, которые пациенты должны понять и принять на ранней стадии до операции. Опытный врач-диетолог может помочь пациентам в разработке планов действий и поведенческих целей, которых необходимо достичь до операции, чтобы подготовиться к послеоперационному образу жизни. Полное овладение репертуаром новых привычек со стороны послеоперационных пациентов дает наилучшие долгосрочные результаты.
Толерантность к глюкозе улучшается до такой степени, что более 80% пациентов с диабетом сохраняют нормальный уровень глюкозы в плазме, гликозилированного гемоглобина и инсулина после операции. 2 Однако этот процесс требует значительных изменений в привычках образа жизни, которые пациенты должны понять и принять на ранней стадии до операции. Опытный врач-диетолог может помочь пациентам в разработке планов действий и поведенческих целей, которых необходимо достичь до операции, чтобы подготовиться к послеоперационному образу жизни. Полное овладение репертуаром новых привычек со стороны послеоперационных пациентов дает наилучшие долгосрочные результаты.
Патология морбидного ожирения часто осложняется одним или несколькими психиатрическими диагнозами, такими как посттравматическое стрессовое расстройство, клиническая депрессия, компульсивное переедание или другие состояния, при которых проявляется агрессивное поведение. Самооценка часто держится на трагически низкой отметке. Важным аспектом предварительной оценки является определение способности пациента переносить фрустрацию и проявлять терпение при обучении новым навыкам. Пациенты, страдающие тяжелой депрессией или другими формами психических заболеваний, могут не иметь достаточного самоконтроля, чтобы добиться постоянного изменения привычек. В рамках психиатрической оценки могут быть рекомендованы лекарства и/или психотерапия для стабилизации симптомов.
Важным аспектом предварительной оценки является определение способности пациента переносить фрустрацию и проявлять терпение при обучении новым навыкам. Пациенты, страдающие тяжелой депрессией или другими формами психических заболеваний, могут не иметь достаточного самоконтроля, чтобы добиться постоянного изменения привычек. В рамках психиатрической оценки могут быть рекомендованы лекарства и/или психотерапия для стабилизации симптомов.
1. Частота приема пищи
Многие пациенты в нашей клинике имели привычку есть очень большое количество пищи за один или два приема пищи в день. Емкость в раннем послеоперационном периоде обычно составляет около половины чашки или меньше. Пациенты должны научиться есть частыми небольшими порциями, состоящими из здоровой пищи. Неспособность изменить эту привычку приведет к плохому питанию и недостаточному потреблению калорий. Потребление слишком малого количества калорий может привести к «голодному режиму» обмена веществ, что будет мешать снижению веса. Пациентам рекомендуется завтракать и есть не менее четырех-пяти небольших приемов пищи в день.
Пациентам рекомендуется завтракать и есть не менее четырех-пяти небольших приемов пищи в день.
2. Объем пищи и темп приема пищи
Привычка есть небольшими порциями и медленно и осознанно есть у пациентов, которые должны усвоиться к моменту проведения операции. В противном случае, вероятно, возникнет рвота, что отрицательно скажется на питании пациентов и общем состоянии здоровья.
В краткосрочной перспективе это представляет собой отрицательное подкрепление, которое может помочь сформировать поведение, соответствующее успеху после операции. Однако, если рвота не проходит, это приводит к неудаче хирургического вмешательства. Чтобы избежать последнего результата, пациенты должны очень хорошо пережевывать твердую пищу и избегать употребления жидкости в течение 30–60 минут после приема твердой пищи. Техники релаксации можно использовать для снижения скорости еды и питья. При медленном питании пациенты также могут предвосхищать чувство сытости во время еды. Таким образом, они могут избежать неизбежного «рокового укуса», который приводит к боли и рвоте.
Таким образом, они могут избежать неизбежного «рокового укуса», который приводит к боли и рвоте.
3. Адекватное потребление жидкости
В раннем послеоперационном периоде пациенты часто сообщают о субоптимальном потреблении жидкости, возможно, в результате ограничения жидкости во время еды и перекусов. Обезвоживание может быть очень опасным для общего состояния здоровья и может привести к запорам и плохому усвоению лекарств и питательных веществ. Пациенты должны носить с собой напитки без сахара и часто пить. Они не должны полагаться на жажду как на триггер питья. Многие продукты, такие как супы, способствуют увеличению потребляемой жидкости. Пациентам рекомендуется ежедневно потреблять около 48 унций жидкости.
4. Потребление фруктов, овощей и цельнозерновых продуктов
Пациенты, страдающие морбидным ожирением, обычно не употребляют количество фруктов, овощей и цельнозерновых продуктов, рекомендованное для здорового питания.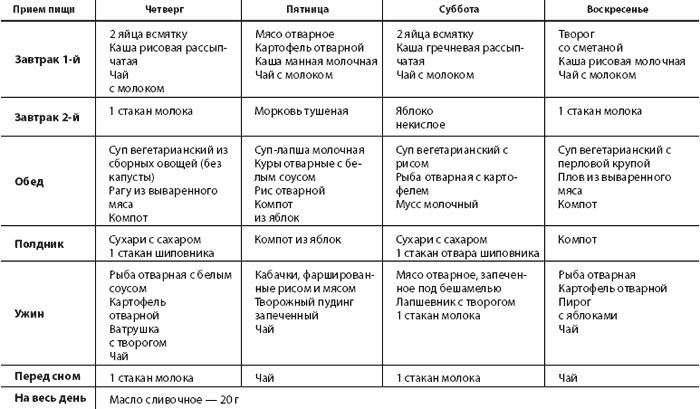 Эта привычка должна быть изменена как часть хирургического процесса, чтобы обеспечить достаточное количество клетчатки и некоторых витаминов и минералов. Низкое потребление клетчатки может привести либо к запорам, либо к хронической диарее из-за недостатка диетической массы. Кроме того, рекомендуется более высокое потребление клетчатки для снижения уровня холестерина в сыворотке. 3 Свежие фрукты можно добавлять в смузи из коровьего молока, йогурта или соевого молока. Овощи можно натирать в супы или томатный соус, а нарезанные или тертые овощи можно добавлять в омлеты.
Эта привычка должна быть изменена как часть хирургического процесса, чтобы обеспечить достаточное количество клетчатки и некоторых витаминов и минералов. Низкое потребление клетчатки может привести либо к запорам, либо к хронической диарее из-за недостатка диетической массы. Кроме того, рекомендуется более высокое потребление клетчатки для снижения уровня холестерина в сыворотке. 3 Свежие фрукты можно добавлять в смузи из коровьего молока, йогурта или соевого молока. Овощи можно натирать в супы или томатный соус, а нарезанные или тертые овощи можно добавлять в омлеты.
5. Адекватное потребление белка
Приблизительно 60–80 г ежедневного белка рекомендуется для адекватного питания и для заживления ран после операции. Этот факт может осложняться непереносимостью больными многих пищевых источников белка, особенно красного мяса и птицы. Также непереносимость лактозы является возможным послеоперационным осложнением, требующим модификации молочных продуктов..jpg)
Белок содержится в рыбе, яйцах и многих растительных продуктах, таких как соевые продукты, орехи и бобовые. Кроме того, в качестве дополнения к диете можно использовать имеющиеся в продаже коктейли с высоким содержанием белка и низким содержанием сахара и батончики для завтрака. Однако многие из них содержат сахароспирты (например, сорбит), которые могут вызывать газообразование и диарею. К счастью, большинство пациентов могут возобновить употребление белковой пищи через несколько месяцев.
Однако самая высокая потребность в белке для лечебных целей приходится на первые несколько недель. Орехи, ореховое масло, сыры и йогурт, если они переносятся, могут быть основными источниками белка до тех пор, пока выбор диеты не расширится. Роль диетолога в этой послеоперационной фазе имеет решающее значение для исхода для каждого пациента. В первые несколько месяцев после операции требуются частые визиты к диетологу, отчасти для обеспечения оптимального белкового питания.
Avoidance of Sweets»> 6. Отказ от сладкогоКак упоминалось выше, средние порции продуктов и напитков, содержащих большое количество сахара, вызывают демпинг-синдром, и их следует избегать. Продукты, наиболее часто связанные с синдромом демпинга, — это подслащенные напитки, такие как газированные напитки, сокосодержащие напитки и молочные коктейли, а также обычное мороженое. Доступно мороженое без добавления сахара, но оно может содержать сахарные спирты.
Старые привычки могут привести пациентов к желанию сладкого, даже если последствия будут пагубными. Пациенты должны иметь в наличии здоровые закуски, такие как орехи, хумус и цельнозерновые крекеры, пищевые смеси, свежие и сушеные фрукты и простой попкорн. Им также нужно быть терпеливыми, поскольку они формируют новые привычки и постепенно избавляются от старых.
7. Витаминно-минеральные добавки
Обходной желудочный анастомоз вызывает мальабсорбцию, вследствие чего питание железом, кальцием и витаминами группы В находится под угрозой. В дополнение к питательной диете необходимы добавки для борьбы с потенциальными недостатками. Железодефицитная анемия, пернициозная анемия и остеопороз (у обоих полов) могут развиваться, хотя обычно не в первый послеоперационный год.
В дополнение к питательной диете необходимы добавки для борьбы с потенциальными недостатками. Железодефицитная анемия, пернициозная анемия и остеопороз (у обоих полов) могут развиваться, хотя обычно не в первый послеоперационный год.
Ежедневный прием поливитаминов взрослой силы с железом, добавки с комплексом витаминов группы В и 1000–1500 мг кальция необходим на всю оставшуюся жизнь пациента. Жевательные витамины теперь доступны для пациентов, которые плохо переносят таблетки. Диагностический анализ крови необходим при ежегодном послеоперационном посещении пациента или раньше, если присутствуют подозрительные симптомы, такие как усталость или одышка.
8. Регулярное посещение собраний группы поддержки
Посещение собраний группы поддержки должно быть обязательным до операции, и пациенты должны продолжать регулярное посещение в течение нескольких месяцев или дольше после операции. Группы поддержки предлагают убежище для пациентов с патологическим ожирением, которые склонны изолировать себя от общественных мероприятий. В таких условиях пациенты, скорее всего, будут чувствовать себя более принятыми, чем в обществе в целом.
Группы поддержки предлагают убежище для пациентов с патологическим ожирением, которые склонны изолировать себя от общественных мероприятий. В таких условиях пациенты, скорее всего, будут чувствовать себя более принятыми, чем в обществе в целом.
Очень важно, что сверстники могут обеспечить заслуживающий доверия и практический инструктаж по преодолению трудностей, связанных с адаптацией к еде и другому образу жизни. Пациенты, достигшие своих целей, служат образцом для подражания и могут стимулировать боевой дух тех, кто более осторожно относится к серьезным изменениям в своих привычках.
Переписка в Интернете часто оказывается полезной для пациентов. Однако информация, доступная в Интернете, иногда неверна. Кроме того, использование Интернета для поддержки исключительно без личного общения со сверстниками может позволить пациентам оставаться в изоляции. Это может привести к продолжению их антиобщественного поведения в ущерб себе.
Compliance With Exercise Program»> 9. Соблюдение программы упражненийАктивность в образе жизни пациента имеет решающее значение для хорошего здоровья и сохранения потери веса. Большинству пациентов требуется не менее 35 минут ежедневных аэробных упражнений, при этом трижды в неделю настоятельно рекомендуется выполнять силовые упражнения для поддержания скорости метаболизма на высоком уровне. 4 Через группы поддержки пациенты часто формируют системы друзей, в которых они вместе тренируются, например, в программе ходьбы или в клубе здоровья. Если ортопедические проблемы сохраняются, программы водных упражнений могут быть единственным вариантом добавления лечебного движения к послеоперационному образу жизни.
Некоторые пациенты очень быстро теряют вес, особенно в раннем послеоперационном периоде. Если у них возникают трудности с питанием, это необходимо решить, чтобы обеспечить питательную диету с достаточным количеством белка. Потеря мышечной массы неизбежна, если кто-то теряет до 1 фунта в день.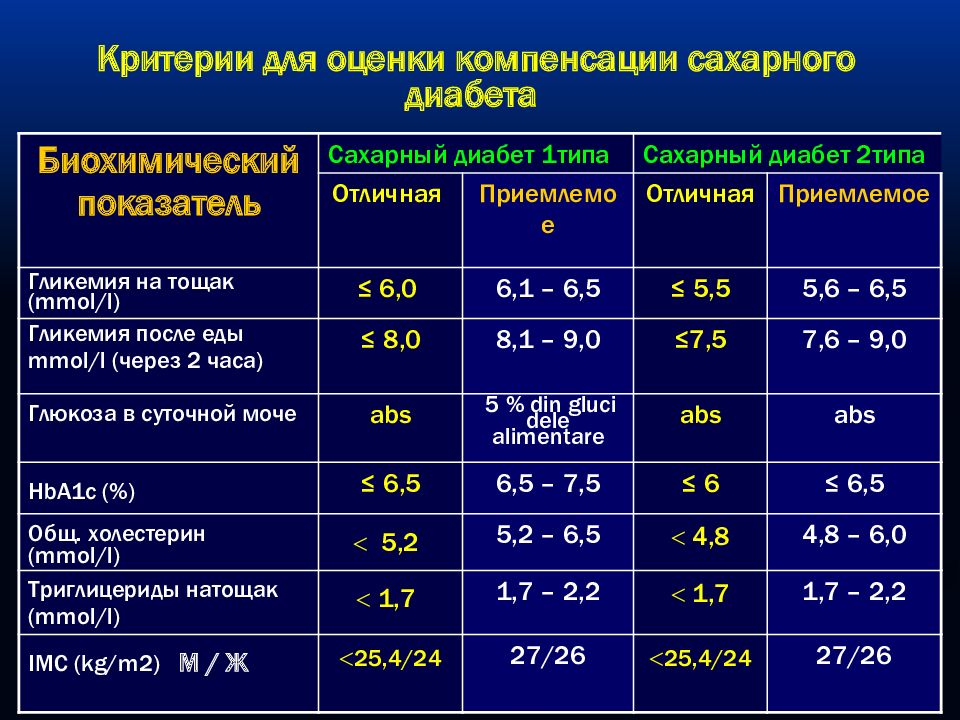 Упражнения, особенно силовые, могут помочь снизить скорость потери мышечной массы. Пациенты могут постепенно увеличивать упражнения с отягощениями, начиная уже через 2–3 недели после операции.
Упражнения, особенно силовые, могут помочь снизить скорость потери мышечной массы. Пациенты могут постепенно увеличивать упражнения с отягощениями, начиная уже через 2–3 недели после операции.
Пациенты сталкиваются со многими драматическими изменениями, которые накладываются на их отношения и поведение. Пища по-прежнему может быть источником эмоционального и физического комфорта для послеоперационных пациентов, но способ, которым этот комфорт достигается, неизбежно будет совсем другим.
Можно ожидать изменений в отношениях. Обязанности, как правило, увеличиваются по мере того, как пациенты теряют вес. Возрастают требования к самообслуживанию. Несмотря на послеоперационные требования, большинство пациентов говорят, что они прошли бы этот процесс снова, если бы им пришлось, потому что они чувствуют, что у них есть второй шанс в жизни.
Джуди Дауд, Массачусетс, доктор медицинских наук, LDN, владелец компании Nutrition Dynamics, Inc., Спрингфилд, Массачусетс.
Обес Сург
2
:61
–68,1992
2 Порис WJ, Swanson MS, MacDonald KG, Long SB, Morris PG, Brown BM, Barakat HA, deRamon RA, Israel G, Dolezal JM: Кто бы мог подумать? Операция оказывается наиболее эффективным методом лечения сахарного диабета у взрослых.

 Крайне низкое содержание в составе Ресурс Диабет Плюс транс-жиров уменьшает риск кардиоваскулярных осложнений, что особенно важно при сопутствующем атеросклерозе и диагностированном метаболическом синдроме.
Крайне низкое содержание в составе Ресурс Диабет Плюс транс-жиров уменьшает риск кардиоваскулярных осложнений, что особенно важно при сопутствующем атеросклерозе и диагностированном метаболическом синдроме.