β — бета | Uatom.org
β — бета
β-излучение – один из видов радиоактивного излучения, которому характерна значительно большая проникающая способность по сравнению с α-излучением.
Природой созданы радиоактивные элементы, способные излучать исключительно β-лучи, например, тритий (3Н или Т), который является одним из изотопов водорода.
Наряду с естественным радиоактивным фоном, окружающий мир существует среди множества искусственно созданных источников ионизирующего излучения.
Техногенные аварии на ядерных объектах гражданского назначения: АЭС Три-Майл-Айленд в США, АЭС Фукусима Даичи в Японии, Чернобыльской АЭС в Украине привели к неконтролируемому поступлению в окружающую среду радионуклидов. В результате чего содержание изотопов, являющихся β-излучающими радионуклидами, таких как изотопы цезия (137Cs, 134Cs), стронция (90Sr), 3H и других, вырос в тысячу раз.
Как бета-излучение воздействует на человека?
При попадании β-частиц на кожу человека может произойти ожог тканей.
Значительные повреждения получают внутренние органы при попадании β-излучающих радионуклидов внутрь организма. При этом происходит ионизация молекул, повреждения органических комплексов и ДНК. В случае длительного поступления значительного количества β-частиц или единовременно при попадании в тело очень сильной дозы – результат плачевный, ведь приводит к смерти.
Защита от β-излучения
Когда речь идет о людях, чья профессиональная деятельность, так или иначе, связана с источниками β-излучения, для их защиты и минимизации последствий негативного воздействия на организм предусмотрены определенные правила поведения:
1) Основная защита от β-излучения заключается в снижении его интенсивности, путем удаления от источника опасности на как можно большее расстояние и уменьшения продолжительности самого контакта с источником.
2) Защититься от внешнего воздействия β-лучей поможет специальная одежда, экраны из стекла, плексигласа, листового алюминия и других металлов.
3) Уберечь внутренние органы (легкие, желудочно-кишечный тракт) от поступления β-частиц вовнутрь организма можно, используя специальные средства защиты, – респираторы, повязки. Также действенным будет – ограничение потребления загрязненной воды и продуктов питания.
Первая помощь при внешнем облучении и попадании бета-частиц вовнутрь организма?
- Срочно покинуть опасную зону и пройти дозиметрический контроль;
- Снять одежду и обувь;
- Загрязненную спецодежду передать для дальнейшей дезактивации;
- При загрязнении кожи необходимо обработать пораженный участок моющими средствами и смыть водой;
- В течение первых 30 мин — 1:00 после поступления в организм бета-частиц – принять препараты, стимулирующие рвотный рефлекс и слабительные средства;
- В дальнейшем использовать сорбенты и употреблять продукты питания, ускоряющие метаболизм организма.

Лечебный эффект бета-лучей
Так же, как и другие виды ионизирующего излучения, β-лучи находят широкое применение в медицине.
При лечении болезней кожи на проблемные участки накладываются аппликаторы, излучающие β-лучи. При злокачественных опухолях организма используют внутритканевую β-терапию, лечебный эффект которой достигается путем разрушительного действия β-лучей на патологически измененные ткани. Также в медицине используется радиоизотопная диагностика для выявления опухолей.
Редакция сайта Uatom.org
Бета излучение – что это кратко, свойства поля и потока электронов, взаимодействие с веществом
3.9
Средняя оценка: 3.9
Всего получено оценок: 179.
3.9
Средняя оценка: 3.9
Всего получено оценок: 179.
Один из видов радиоактивного излучения, существующего в природе, — бета-излучение. Познакомимся с этим видом радиоактивности, с природой бета-лучей, с механизмом их возникновения.
Открытие бета-лучей
После открытия радиоактивности в конце XIX в. многие физики стали изучать природу и свойства радиоактивного излучения. Одним из таких физиков был Э. Резерфорд. В 1899 г. он поставил опыт по определению состава радиоактивного излучения.
Рис. 1. Опыт Резерфорда по радиоактивности 1899.В свинцовом контейнере находится радиоактивный препарат (как правило, соль радия). Через окно в контейнере радиоактивное излучение попадает на фотопластинку. Как и в опытах других физиков, на пластинке появлялась засвеченная область. Теперь, если на пути радиоактивного луча поместить сильное магнитное поле и если радиоактивный луч состоит из заряженных частиц, засвеченная область на фотопластинке сдвинется в сторону.
Опыт показал, что радиоактивное излучение имеет сложный состав. На фотопластинке после включения магнитного поля возникли три пятна. Это доказывало, что в радиоактивных лучах присутствуют частицы всех трех видов: тяжелые положительные, легкие отрицательные и нейтральные (неизвестного веса).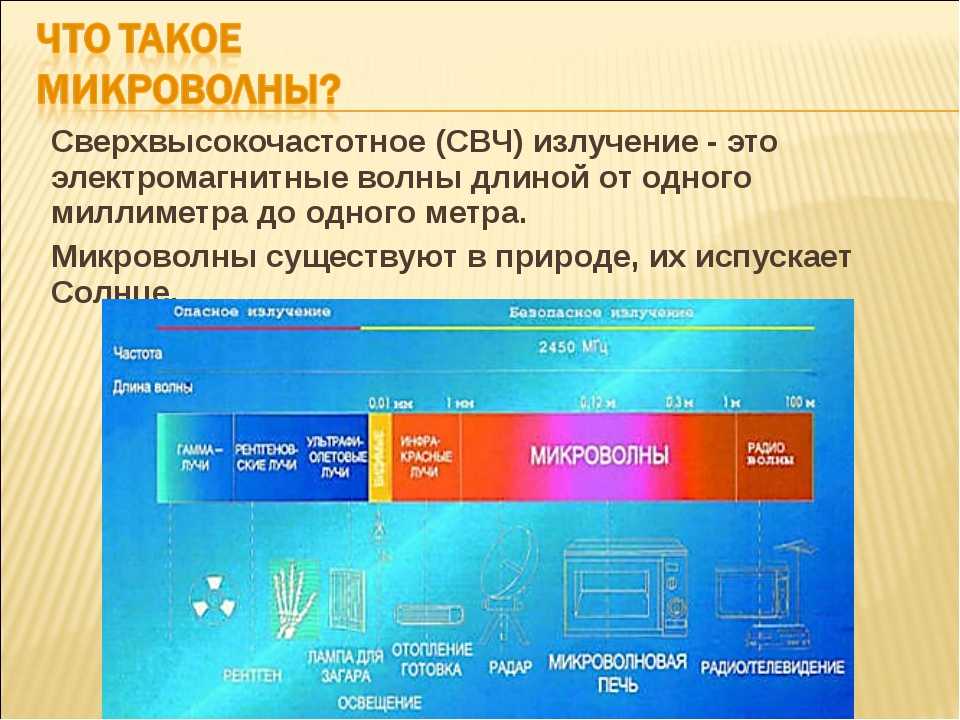
Положительная компонента радиоактивного излучения была названа альфа-лучами, отрицательная — бета-лучами, нейтральная — гамма-лучами.
Свойства бета-лучей
Бета-лучи сильно отклонялись в магнитном поле, следовательно, массы их были невелики. Измеряя степень отклонения бета-лучей магнитным полем с известной индукцией, установили, что эти лучи — не что иное, как поток электронов, движущихся с высокими скоростями.
В дальнейшем выяснилось, что бета-лучи — это результат действия особого, слабого взаимодействия, в результате которого нейтрон распадается на протон, электрон и антинейтрино. Порядковый номер элемента в периодической таблице Менделеева увеличивается на единицу, а массовое число остается прежним (протон и нейтрон весят практически одинаково).
Рис. 2. Бета-распад.Все эти обстоятельства и определяют свойства бета-излучения.
- Генерируется оно радиоактивными ядрами, имеющими избыток нейтронов (по сравнению с энергетически выгодными количествами).

- Электроны, из которых состоят бета-лучи, имеют энергии от нуля до десятков МэВ, летят с околосветовыми скоростями и поэтому достаточно глубоко проникают в вещество, а также способны на взаимодействие с веществом, ионизируя его.
- Для защиты от поля бета-излучения достаточно нескольких сантиметров плотного материала, однако если бета-частицы попадают внутрь организма, они становятся очень опасны. Мощности дозы хватит, чтобы вызвать тяжелые внутренние ожоги.
- Спектр энергии бета-лучей — непрерывный. Бета-частицы обладают всевозможными энергиями от нуля до некоторого максимального значения, которое определяется спецификой распадающегося элемента.
Исходя из квантового характера испускания частиц, спектр энергии бета-лучей должен быть линейчатым (как, например, спектр альфа-частиц). В рамках развивавшейся в то время квантовой теории непрерывность реального бета-спектра была необъяснима, поскольку она нарушала закон сохранения энергии. Поэтому В. Паули в 1930 г. выдвинул предположение, что часть энергии уносится частицей, очень слабо взаимодействующей с веществом. Этой частицей оказалось антинейтрино, зарегистрированное экспериментально в 1956 г. — частица, подтвердившая существование особого, слабого фундаментального взаимодействия.
выдвинул предположение, что часть энергии уносится частицей, очень слабо взаимодействующей с веществом. Этой частицей оказалось антинейтрино, зарегистрированное экспериментально в 1956 г. — частица, подтвердившая существование особого, слабого фундаментального взаимодействия.
Что мы узнали?
Бета излучение — это поток электронов, вылетающих с высокими скоростями из ядер при радиоактивном распаде. Этот распад происходит в результате особого, слабого взаимодействия. Бета-частицы имеют непрерывный энергетический спектр из-за того, что часть энергии уносится легкой безмассовой частицей антинейтрино.
Тест по теме
Доска почёта
Чтобы попасть сюда — пройдите тест.
Пока никого нет. Будьте первым!
Оценка доклада
3.9
Средняя оценка: 3.9
Всего получено оценок: 179.
А какая ваша оценка?
Лечение радиационно-индуцированной тошноты и рвоты
US Pharm. 2019;44(12):HS10-HS13.
2019;44(12):HS10-HS13.
РЕЗЮМЕ: Лучевая терапия является одним из методов лечения злокачественных новообразований. Одним из побочных эффектов лучевой терапии является радиационно-индуцированная рвота; однако противорвотные средства иногда используются недостаточно. Несколько организаций опубликовали рекомендации по лечению радиационно-индуцированной тошноты и рвоты в зависимости от уровня риска. Вызванную облучением рвоту можно хорошо контролировать с помощью антагониста рецептора 5-гидрокситриптамина типа 3, что отражает роль серотонина в этом состоянии. Надлежащая профилактика и лечение радиационно-индуцированной тошноты и рвоты необходимы для завершения курса лучевой терапии, чтобы можно было добиться положительного результата лечения без перерыва.
Вызванные облучением тошнота и рвота как побочный эффект лучевой терапии могут недооцениваться как поставщиком медицинских услуг, так и пациентом. 1,2 Радиация может вызывать тошноту и рвоту, которые могут начаться во время лучевой терапии и продолжаться в течение нескольких дней после завершения лучевой терапии; поэтому он также может влиять на эффективность других методов лечения рака, включая химиотерапию, если она также является частью схемы лечения. 2
2
Тошнота — это серьезный побочный эффект лучевой терапии, который может повлиять на качество жизни пациента. Подсчитано, что радиация вызывает тошноту и рвоту у 50-80% пациентов. Пациенты, проходящие эту терапию, часто получают до 40 фракций облучения в течение 6–8 недель. Пациенты с радиационно-индуцированной тошнотой и рвотой потенциально могут отказаться от дальнейшего лечения или столкнуться с задержками в лечении, что может неблагоприятно повлиять на исход. 1
Факторы риска радиационно-индуцированной тошноты и рвоты Тяжесть тошноты и рвоты, вызванных лучевой терапией, зависит, главным образом, от области, куда доставляется радиация. Облучение всего тела имеет наибольшую вероятность вызвать тошноту и рвоту, а облучение верхней части живота сопряжено со вторым по величине риском. Кроме того, увеличение площади облучаемого тела, используемых фракций облучения и общей общей дозы облучения повысит риск радиационно-индуцированной тошноты и рвоты. 2 Сообщалось, что использование участков облучения, превышающих 400 см 2 , существенно влияет на профилактическое использование противорвотных средств для предотвращения радиационно-индуцированной тошноты и рвоты. 3
2 Сообщалось, что использование участков облучения, превышающих 400 см 2 , существенно влияет на профилактическое использование противорвотных средств для предотвращения радиационно-индуцированной тошноты и рвоты. 3
Патофизиология и механизмы радиационной рвоты сложны. Было высказано предположение, что как уровни серотонина, так и брюшная полость играют важную роль в радиационно-индуцированной тошноте и рвоте. Повышенные уровни активного метаболита серотонина 5-гидроксииндолуксусной кислоты были обнаружены в моче пациентов, испытывающих этот побочный эффект. Кроме того, рвоту, вызванную лучевой терапией, можно хорошо контролировать с помощью введения 5-гидрокситриптамина типа 3 (5-HT 9).0045 3 ) антагонист рецепторов, что подтверждает роль серотонина в радиационно-индуцированной тошноте и рвоте. 4
Практика назначения противорвотных средств Статистически значимыми факторами, влияющими на назначение противорвотных препаратов, являются одновременное применение химиотерапии с лучевой терапией и предшествующая рвота, вызванная химиотерапией. Судя по результатам исследований, радиационно-индуцированная тошнота и рвота, по-видимому, недооцениваются, а противорвотные средства при этом состоянии недостаточно назначаются радиационными онкологами. 3
Судя по результатам исследований, радиационно-индуцированная тошнота и рвота, по-видимому, недооцениваются, а противорвотные средства при этом состоянии недостаточно назначаются радиационными онкологами. 3
Для профилактики и лечения радиационно-индуцированной тошноты и рвоты использовались различные противорвотные средства, но больше всего доказательств имеется в отношении антагонистов 5-HT 3 рецепторов. 5,6
Руководство по лечениюТри различных руководства по лечению радиационно-индуцированной тошноты были разработаны Национальной комплексной онкологической сетью (NCCN), Американским обществом клинической онкологии (ASCO) и Многонациональная ассоциация поддерживающей терапии при раке (MASCC) и Европейское общество медицинской онкологии (ESMO). 7-9
Руководство NCCN: Согласно NCCN, облучение всего тела вызывает самый высокий риск тошноты и рвоты, поскольку оно вызывает это состояние более чем у 90% пациентов ( ТАБЛИЦА 1 ). 7 От 30% до 90% пациентов, получающих лучевую терапию верхних отделов брюшной полости, испытывают тошноту и рвоту. Пациенты, подвергающиеся тотальному облучению тела, должны получать антагонист рецепторов 5-HT 3 — либо гранисетрон 2 мг перорально ежедневно, либо ондансетрон 8 мг перорально два-три раза в день, в зависимости от потребностей пациента — с дексаметазоном 4 мг или без него рот ежедневно. Пациентам, получающим облучение верхней части живота или других локализованных участков, следует назначать либо гранисетрон 2 мг перорально ежедневно, либо ондансетрон 8 мг перорально два раза в день, с дексаметазоном 4 мг перорально ежедневно или без него.
7 От 30% до 90% пациентов, получающих лучевую терапию верхних отделов брюшной полости, испытывают тошноту и рвоту. Пациенты, подвергающиеся тотальному облучению тела, должны получать антагонист рецепторов 5-HT 3 — либо гранисетрон 2 мг перорально ежедневно, либо ондансетрон 8 мг перорально два-три раза в день, в зависимости от потребностей пациента — с дексаметазоном 4 мг или без него рот ежедневно. Пациентам, получающим облучение верхней части живота или других локализованных участков, следует назначать либо гранисетрон 2 мг перорально ежедневно, либо ондансетрон 8 мг перорально два раза в день, с дексаметазоном 4 мг перорально ежедневно или без него.
При одновременном назначении химиотерапии и облучения рекомендуется использовать противорвотный режим, подходящий для химиотерапии. Некоторые химиотерапевтические агенты вызывают более высокий риск эметогенного действия в сочетании с лучевой терапией. Например, считается, что темозоломид в дозе менее или равной 75 мг/м 2 в день при пероральном введении имеет риск эметогенности от минимального до низкого (частота рвоты <30%), но когда его вводят одновременно с лучевой терапией, умеренный эметогенный риск (частота рвоты 30% и выше). Пациентам, у которых наблюдаются обострения тошноты и рвоты, вызванные облучением, следует назначить препарат другого класса, отличный от препарата, который вводят при обострении тошноты и рвоты, вызванных химиотерапией.
Пациентам, у которых наблюдаются обострения тошноты и рвоты, вызванные облучением, следует назначить препарат другого класса, отличный от препарата, который вводят при обострении тошноты и рвоты, вызванных химиотерапией.
Пациентам, у которых наблюдаются прорывные радиационно-индуцированные тошнота и рвота, следует назначить препарат другого класса, отличный от агента, назначаемого для профилактики тошноты и рвоты. 7
Руководства ASCO: Руководства ASCO классифицируют радиационно-индуцированную тошноту и рвоту по четырем категориям риска (высокий, умеренный, низкий и минимальный риск) в зависимости от анатомического места введения радиации ( ТАБЛИЦА 2 ). 8 Облучение всего тела, вызывающее тошноту и рвоту более чем у 90% пациентов, считается фактором высокого риска. Краниоспинальное облучение и облучение верхней части живота представляют умеренный риск, поскольку они вызывают тошноту и рвоту у 30-90% пациентов. Облучение головного мозга, головы и шеи, грудной клетки или таза считается малоопасным, поскольку оно вызывает тошноту и рвоту лишь у 10-30% пациентов. Облучение конечностей или груди представляет минимальный риск, поскольку оно вызывает тошноту и рвоту менее чем у 10% пациентов.
Облучение конечностей или груди представляет минимальный риск, поскольку оно вызывает тошноту и рвоту менее чем у 10% пациентов.
Пациентам, подвергающимся облучению высокого риска (всего тела), рекомендуется предлагать схему из двух препаратов для предотвращения радиационно-индуцированной тошноты и рвоты. Двухкомпонентная схема должна включать либо ондансетрон (перорально, растворяющиеся таблетки для перорального применения, растворимая пленка для перорального применения или внутривенно), либо гранисетрон (перорально или внутривенно) плюс дексаметазон перорально или внутривенно. Ондансетрон можно вводить один или два раза в день в дни лучевой терапии; если его вводят два раза в день, первую дозу следует вводить до облучения. Кроме того, пациент должен получать ондансетрон один или два раза в день на следующий день после каждого сеанса лучевой терапии, если лучевая терапия не запланирована на этот день. Гранисетрон вводят один раз в день в день каждого сеанса лучевой терапии до начала облучения и на следующий день после каждого сеанса лучевой терапии, если в этот день лучевая терапия не планируется. Дексаметазон вводят профилактически один раз в сутки в дни лучевой терапии до ее проведения и на следующий день после каждого сеанса лучевой терапии, если лучевая терапия не запланирована на этот день.
Дексаметазон вводят профилактически один раз в сутки в дни лучевой терапии до ее проведения и на следующий день после каждого сеанса лучевой терапии, если лучевая терапия не запланирована на этот день.
Пациенты, получающие облучение умеренного риска (верхняя часть живота или краниоспинальная область), должны получать профилактическое лечение ондансетроном (перорально, растворимая таблетка для приема внутрь, растворимая пленка для перорального применения или внутривенно), гранисетроном (перорально или внутривенно) или трописетроном (перорально или внутривенно) и, необязательно, пероральный или внутривенный дексаметазон. Профилактически ондансетрон можно вводить один или два раза в день в дни лучевой терапии, причем первую дозу вводят до облучения. Гранисетрон и трописетрон вводят один раз в день перед облучением. Если дексаметазон используется профилактически, его следует вводить один раз в день перед облучением в течение первых 5 дней лучевой терапии.
По данным ASCO, пациентам, подвергающимся облучению с низким риском (голова и шея, грудная клетка или таз) или облучению с минимальным риском (конечности или грудь), следует предложить неотложную терапию ондансетроном или гранисетроном, дексаметазоном или антагонистом дофаминовых рецепторов.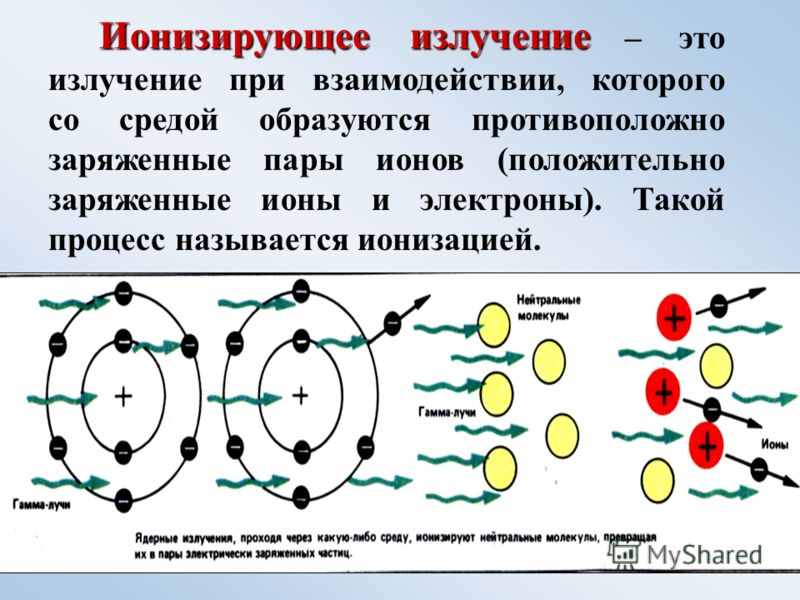 (прохлорперазин или метоклопрамид). Пациентам, перенесшим облучение головного мозга с низким риском, следует предложить дексаметазон в качестве неотложной терапии. Дексаметазон можно вводить в качестве спасательного средства, если пациент еще не принимает кортикостероиды, и дозу дексаметазона следует титровать по мере необходимости до максимальной 16 мг в день (перорально или внутривенно). Прохлорперазин и метоклопрамид, вводимые в качестве неотложных средств при радиационно-индуцированной тошноте и рвоте с низким риском, следует титровать по мере необходимости до максимум 3-4 введений в день. Для взрослых пациентов, получающих лучевую терапию и химиотерапию одновременно, противорвотный режим должен соответствовать риску рвоты химиотерапии, если уровень риска лучевой терапии не превышает уровень риска химиотерапии. Если лучевая терапия продолжается после завершения химиотерапии, противорвотный режим следует скорректировать с учетом риска рвоты при лучевой терапии. 8
(прохлорперазин или метоклопрамид). Пациентам, перенесшим облучение головного мозга с низким риском, следует предложить дексаметазон в качестве неотложной терапии. Дексаметазон можно вводить в качестве спасательного средства, если пациент еще не принимает кортикостероиды, и дозу дексаметазона следует титровать по мере необходимости до максимальной 16 мг в день (перорально или внутривенно). Прохлорперазин и метоклопрамид, вводимые в качестве неотложных средств при радиационно-индуцированной тошноте и рвоте с низким риском, следует титровать по мере необходимости до максимум 3-4 введений в день. Для взрослых пациентов, получающих лучевую терапию и химиотерапию одновременно, противорвотный режим должен соответствовать риску рвоты химиотерапии, если уровень риска лучевой терапии не превышает уровень риска химиотерапии. Если лучевая терапия продолжается после завершения химиотерапии, противорвотный режим следует скорректировать с учетом риска рвоты при лучевой терапии. 8
Руководство MASCC/ESMO: Руководство MASCC/ESMO также классифицирует радиационно-индуцированную тошноту и рвоту на четыре категории в зависимости от места облучения ( ТАБЛИЦА 3 ). 9 Эти категории аналогичны категориям в рекомендациях ASCO. Категория высокого риска включает облучение всего тела; таким пациентам рекомендуется профилактическое лечение антагонистами рецепторов 5-HT 3 в сочетании с дексаметазоном. Считается, что пациенты, подвергающиеся лучевой терапии верхних отделов брюшной полости или краниоспинальной области, имеют умеренный риск развития радиационно-индуцированной тошноты и рвоты. У этих пациентов профилактическое лечение 5-HT 3 антагонист рецептора и дополнительный дексаметазон рекомендуется. Считается, что пациенты, получающие облучение черепа, головы и шеи, области грудной клетки или таза, имеют низкий риск развития радиационно-индуцированной тошноты и рвоты. Пациентам, получающим краниальное облучение, следует назначать дексаметазон в качестве профилактической или экстренной терапии. Те, кто получает лучевую терапию головы и шеи, области грудной клетки или таза, должны получать профилактическую или неотложную терапию дексаметазоном, антагонистом дофаминовых рецепторов или 5-HT 3 антагонист рецепторов.
9 Эти категории аналогичны категориям в рекомендациях ASCO. Категория высокого риска включает облучение всего тела; таким пациентам рекомендуется профилактическое лечение антагонистами рецепторов 5-HT 3 в сочетании с дексаметазоном. Считается, что пациенты, подвергающиеся лучевой терапии верхних отделов брюшной полости или краниоспинальной области, имеют умеренный риск развития радиационно-индуцированной тошноты и рвоты. У этих пациентов профилактическое лечение 5-HT 3 антагонист рецептора и дополнительный дексаметазон рекомендуется. Считается, что пациенты, получающие облучение черепа, головы и шеи, области грудной клетки или таза, имеют низкий риск развития радиационно-индуцированной тошноты и рвоты. Пациентам, получающим краниальное облучение, следует назначать дексаметазон в качестве профилактической или экстренной терапии. Те, кто получает лучевую терапию головы и шеи, области грудной клетки или таза, должны получать профилактическую или неотложную терапию дексаметазоном, антагонистом дофаминовых рецепторов или 5-HT 3 антагонист рецепторов. Пациентам, получающим лучевую терапию с минимальным риском (конечности или грудь), следует предложить неотложную терапию дексаметазоном, антагонистом дофаминовых рецепторов или антагонистом рецепторов 5-HT 3 . Если пациент получает сопутствующую химиотерапию и лучевую терапию, противорвотная терапия должна быть согласована с рвотным риском химиотерапии, за исключением случаев, когда лучевая терапия имеет более высокий риск вызвать тошноту и рвоту. 9
Пациентам, получающим лучевую терапию с минимальным риском (конечности или грудь), следует предложить неотложную терапию дексаметазоном, антагонистом дофаминовых рецепторов или антагонистом рецепторов 5-HT 3 . Если пациент получает сопутствующую химиотерапию и лучевую терапию, противорвотная терапия должна быть согласована с рвотным риском химиотерапии, за исключением случаев, когда лучевая терапия имеет более высокий риск вызвать тошноту и рвоту. 9
Тошнота и рвота, вызванные облучением, могут быть серьезным побочным эффектом лучевой терапии, неблагоприятно влияющим на качество жизни пациента и потенциально ставящим под угрозу лечение, поскольку пациенты, испытывающие сильную тошноту и рвоту, могут отказаться от последующего лечения лучевой терапией. Поэтому профилактика и лечение важны, чтобы помочь избежать или облегчить симптомы радиационно-индуцированной тошноты и рвоты. Доступны различные ресурсы, чтобы помочь практикующим врачам выбрать наиболее подходящее лечение рвоты, вызванной облучением; однако все методы лечения должны быть индивидуализированы в зависимости от потребностей, характеристик и других факторов пациента.
1. Feyer PC, Maranzano E, Molassiotis A, et al. Тошнота и рвота, вызванные лучевой терапией (RINV): руководство MASCC/ESMO по противорвотным средствам при лучевой терапии; обновление 2009 г. Support Care Cancer . 2011;19(доп.1):S5-S14.
2. Урба С. Тошнота и рвота, вызванные облучением. J Natl Compr Canc Netw. 2007;5(1):60-65.
3. Maranzano E, De Angelis V, Pergolizzi S. Проспективное обсервационное исследование рвоты при лучевой терапии: анализ 1020 пациентов, набранных в 45 итальянских центрах радиационной онкологии. Радиотер Онкол. 2010;94(1):36-41.
4. Scarantino CW, Ornitz RD, Hoffman LG, Anderson RF Jr. О механизме радиационной рвоты: роль серотонина. Int J Radiat Oncol Biol Phys. 1994:30(4):825-830.
5. Franzén L, Nyman J, Hagberg H, et al. Рандомизированное плацебо-контролируемое исследование с применением ондансетрона у пациентов, проходящих фракционную лучевую терапию. Энн Онкол. 1996;7(6):587-592.
6. Spitzer TR, Friedman CJ, Bushnell W, et al. Двойное слепое рандомизированное исследование в параллельных группах эффективности и безопасности перорального приема гранисетрона и перорального ондансетрона в профилактике тошноты и рвоты у пациентов, получающих гиперфракционированное облучение всего тела. Пересадка костного мозга. 2000;26(2):203-210.
7. Национальная комплексная онкологическая сеть. Клинические рекомендации NCCN по онкологии (рекомендации NCCN). противорвотные. Версия 1.2019. www.nccn.org/professionals/physician_gls/pdf/antiemesis.pdf. По состоянию на 15 августа 2019 г.
8. Hesketh PJ, Kris MG, Basch E, et al. Противорвотные средства: обновление руководства по клинической практике Американского общества клинической онкологии. J Клин Онкол. 2017;35(28):3240-3261.
9. Ruhlmann CH, Jahn F, Jordan K, et al. Обновленные согласованные рекомендации MASCC/ESMO в 2016 г.: профилактика тошноты и рвоты, вызванных лучевой терапией. Поддержка лечения рака. 2017;25(1):309-316.
2017;25(1):309-316.
Чтобы прокомментировать эту статью, обращайтесь по адресу [email protected].
Ответы на общие вопросы о радиационной безопасности
Онколог-радиолог Мелисса Зиновой (справа) и главный радиотерапевт Бибан Натт с пациентом в MSK Westchester.
Резюме
Эксперты Memorial Sloan Kettering отвечают на распространенные вопросы о безопасности взрослых, проходящих лучевую терапию от рака.
Лучевая терапия является одним из наиболее распространенных и эффективных способов уничтожения раковых клеток и уменьшения размера опухоли. В центре Memorial Sloan Kettering около половины взрослых больных раком проходят лучевую терапию в качестве основного лечения или в рамках более широкого подхода, включающего химиотерапию, хирургическое вмешательство или другие методы лечения. Для многих видов рака лучевая терапия может быть всем, что необходимо для лечения заболевания.
Существуют различные способы лучевой терапии. При дистанционной лучевой терапии лечение проводится аппаратом вне тела. При внутреннем облучении (брахитерапии) закрытые источники радиоактивности размещают вблизи или внутри опухоли. Реже лучевая терапия также может проводиться с использованием жидких материалов в капсулах перорально или инфузией через вену (системное облучение).
При дистанционной лучевой терапии лечение проводится аппаратом вне тела. При внутреннем облучении (брахитерапии) закрытые источники радиоактивности размещают вблизи или внутри опухоли. Реже лучевая терапия также может проводиться с использованием жидких материалов в капсулах перорально или инфузией через вену (системное облучение).
Несмотря на то, что лучевая терапия широко используется в течение десятилетий, до сих пор существует путаница и недопонимание ее безопасности. Мы попросили клинического физика MSK Лоуренса Дауэра и медицинского физика Мэтью Уильямсона рассказать нам о проблемах, которые они чаще всего слышат от пациентов и их семей, а также об ответах и заверениях, которые они дают.
Сделает ли меня внешнее облучение радиоактивным или я стану подвергать облучению других?
Внешняя лучевая терапия, наиболее распространенный вид лучевой терапии, никоим образом не делает человека радиоактивным. Применяется чаще всего в виде рентгеновских лучей на линейном ускорителе. Терапия предназначена для доставки точного количества энергии к опухолевым клеткам, щадя здоровые ткани. Излучение присутствует только при работе линейного ускорителя. Когда вы получаете внешнее облучение, вы не можете заразить или передать это излучение любому другому человеку.
Терапия предназначена для доставки точного количества энергии к опухолевым клеткам, щадя здоровые ткани. Излучение присутствует только при работе линейного ускорителя. Когда вы получаете внешнее облучение, вы не можете заразить или передать это излучение любому другому человеку.
Когда вы получаете внешнее облучение, вы не можете заразить или передать это излучение любому другому человеку.
Лоуренс Т. Дауэр клинический физик
НаверхКак я могу быть уверен, что аппарат внешнего облучения не повреждает нормальные, здоровые ткани моего тела?
Мы тщательно разработали методы калибровки радиационных лучей, чтобы гарантировать, что они достигают областей, на которые они предназначены. Даже когда близлежащие нормальные ткани получают небольшое количество радиации, долговременное повреждение возникает редко. Наши врачи и физики также знают, какое количество радиации может получить здоровая ткань, не причинив при этом значительного вреда. Они используют эту информацию для разработки индивидуального лечения пациента. Мы часто используем специальные маски, слепки или слепки частей тела, чтобы вы оставались неподвижными во время лечения, чтобы мы могли направить лучи излучения точно на область, которую необходимо обработать.
Они используют эту информацию для разработки индивидуального лечения пациента. Мы часто используем специальные маски, слепки или слепки частей тела, чтобы вы оставались неподвижными во время лечения, чтобы мы могли направить лучи излучения точно на область, которую необходимо обработать.
Есть ли риск того, что внутренние радиационные имплантаты (брахитерапия) вытекут или высвободятся из места их установки и будут перемещаться по моему телу?
При брахитерапии мы используем иглу или катетер для введения радиоактивного материала, содержащегося в герметичном источнике, такого как семя, гранула, проволока или капсула. Поскольку радиоактивный материал внутри имплантатов со временем естественным образом распадается, он излучает излучение, которое выделяет энергию для лечения близлежащих раковых клеток. Эта радиоактивность распространяется только на определенное расстояние за пределами имплантата. Через несколько недель или месяцев имплантат перестает излучать излучение. Имплантаты специально тестируются и герметизируются, чтобы предотвратить утечку инкапсулированного радиоактивного материала, и мы размещаем их таким образом, что маловероятно, что они будут двигаться. Мы даем людям особые меры предосторожности, чтобы свести к минимуму воздействие имплантированного радиоактивного материала на других.
Имплантаты специально тестируются и герметизируются, чтобы предотвратить утечку инкапсулированного радиоактивного материала, и мы размещаем их таким образом, что маловероятно, что они будут двигаться. Мы даем людям особые меры предосторожности, чтобы свести к минимуму воздействие имплантированного радиоактивного материала на других.
Должен ли я ограничивать контакты с кем-либо, пока имплантаты для брахитерапии находятся внутри моего тела?
Большинство наших опасений по поводу безопасности связаны с физическим контактом с детьми в течение длительного периода времени, потому что их тела претерпевают такие быстрые изменения и рост. Поскольку мы варьируем дозу облучения в каждом имплантате, а также количество имплантатов, которые мы вставляем, в зависимости от вашего конкретного рака, мы даем вам конкретные советы о мерах предосторожности, которые следует соблюдать, когда вы находитесь в тесном контакте с детьми.
Наверх Семена простаты являются закрытыми источниками. Вы не можете заразить другого человека, находясь рядом с ним или с ней, во время полового акта или любой другой формы интимного контакта. Перед выпиской из больницы ваш врач или сотрудник отдела радиационной безопасности обсудит с вами любые особые меры предосторожности, которые вам следует предпринять в отношении сна. Например, исходя из таких факторов, как ваш возраст и возраст вашего партнера, мы можем попросить вас в течение короткого времени не обнимать своего партнера со спины в позе «ложкой» в течение ночи.
Вы не можете заразить другого человека, находясь рядом с ним или с ней, во время полового акта или любой другой формы интимного контакта. Перед выпиской из больницы ваш врач или сотрудник отдела радиационной безопасности обсудит с вами любые особые меры предосторожности, которые вам следует предпринять в отношении сна. Например, исходя из таких факторов, как ваш возраст и возраст вашего партнера, мы можем попросить вас в течение короткого времени не обнимать своего партнера со спины в позе «ложкой» в течение ночи.
Представляю ли я опасность для окружающих после лечения радиоактивным йодом по поводу рака щитовидной железы?
Лечение радиоактивным йодом включает проглатывание капсулы или жидкой формы радиоактивного йода, который поглощается всеми клетками щитовидной железы, разрушая их. Это эффективно, потому что другие здоровые клетки в организме обычно не поглощают радиоактивный йод.
В течение нескольких дней после этой терапии радиоактивные вещества могут выделяться через жидкости организма, такие как слюна, моча и пот. Мы отправляем пациентов домой с подробными инструкциями по уходу за собой в первые дни — от ограничения контактов с маленькими детьми и домашними животными до использования отдельной посуды и полотенец.
Мы отправляем пациентов домой с подробными инструкциями по уходу за собой в первые дни — от ограничения контактов с маленькими детьми и домашними животными до использования отдельной посуды и полотенец.
Я прохожу визуализирующий тест с использованием радиоактивных материалов. Буду ли я радиоактивным после теста?
Врачи иногда используют небольшое количество радиоактивного материала для диагностики заболеваний. Это называется ядерной медициной. Радиоактивное вещество вводится в ваше тело, обнаруживает определенные клетки или ткани, включая раковые клетки, и связывается с ними. Радиоактивный материал будет оставаться в вашем теле в течение нескольких часов или дней, в зависимости от типа, который используется. В конце концов материал разлагается, и ваше тело естественным образом вымывает его через мочу, пот и другие формы биологического выведения. Мы позаботимся о том, чтобы все детали были вам понятны перед тестом, и мы также можем выдать информационную карточку с объяснением вашего обращения, например, в случае, если вас допросит кто-то из службы безопасности аэропорта.