Табачный дым при вдыхании подавляет активность ресничек эпителия, выстилающего верхние дыхательные пути. Почему это способствует усилению так называемого кашля курильщиков и развитию легочных заболеваний? — Спрашивалка
Светлый
Табачный дым при вдыхании подавляет активность ресничек эпителия, выстилающего верхние дыхательные пути. Почему это способствует усилению так называемого кашля курильщиков и развитию легочных заболеваний? путь заболевание развитие кашель активность дым курильщик ресничка усиление вдыхание эпителий
193
27
0
Ответы
Тятьяна Капитанова
В начале курения у вас появлялось слюнотечение и вы сплевывали, от этого растягивались бронхи, эти ворсинки препятствовали иногородним частичкам, затем они погибают и всякая дрянь попадает не только в бронхи , но безпрепятственно попадает в легкое, при накоплении частичек табака организм пытается их удалить из своего тела и появляется кашель.
0
Светлый
как трогательно
1
ВС
Виктор Сухоруков
Потому что табачный в легких это противоестественно и усиление кашля защитная реакция организма.
0
Артур Маркевич
Здесь, как минимум нужно шесть лет мединститута, чтобы в этом разобраться)))
0
Жоржетта Иудична
у меня знакомая бабулька,ей 90, курит как паровоз и живет себе без ресничек
0
ЕЖ
Евгений Житник
у меня вопрос попроще, где располагается пронатор левого яичка?
0
ЕЖ
Евгений Житник
у меня вопрос попроще,где располагается пронатор левого яичка?
0
Le
Lee-Стричк@
потому что идет постоянное раздражение слизистой, я так думаю
0
Олег Блинов
Никотина вообще относится к алкалойдам. Возможно(я не углублял пока что свои познания о никотине)был каким-то лекарственным препаратом на подобии морфия,героина и т.д. Но любой Яд может быть лекарством,а лекарство ядом. Всё дело в дозе.
Возможно(я не углублял пока что свои познания о никотине)был каким-то лекарственным препаратом на подобии морфия,героина и т.д. Но любой Яд может быть лекарством,а лекарство ядом. Всё дело в дозе.
1
АБ
Андрей Батыгин
не помню,но реально понятно в биологии обЪясняется0
Вера
кашель появляется, когда курящий человек не курит.
0
Светлый
))
1
Вл
Владимир
брось курить не забивай себе голову вопросами
0
Вера Косарева
пейте лучше молоко,намнооооого полезнее.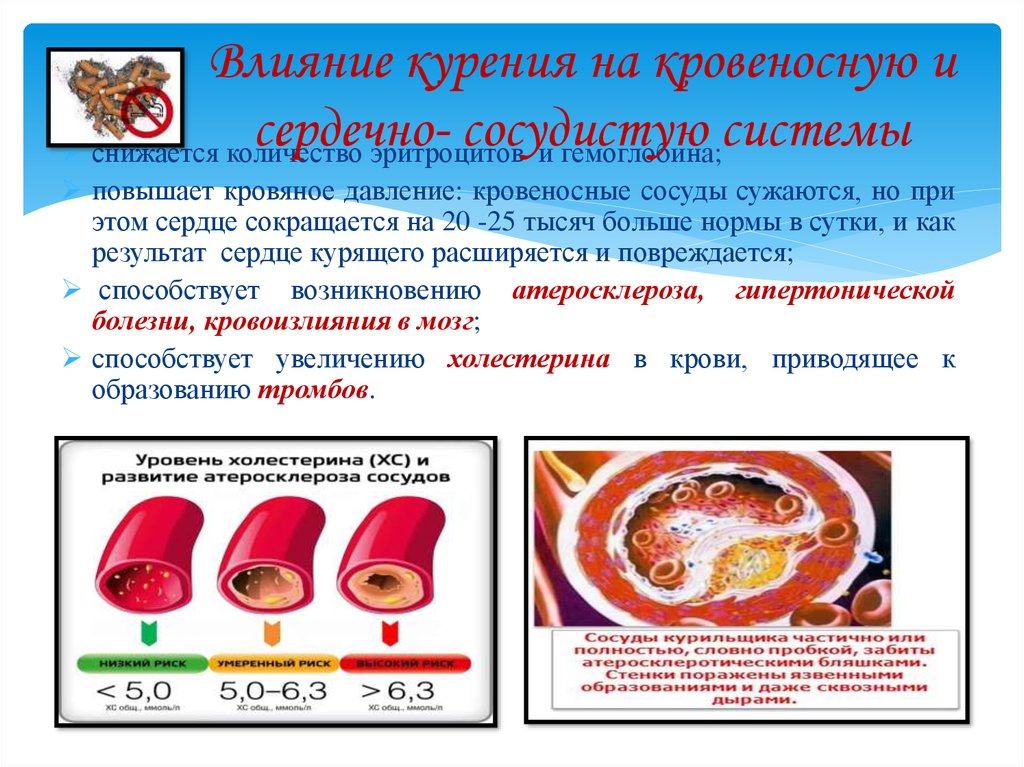
0
МК
Маруся Климова
не курю. и на заболевания аллергия
0
ЛБ
Любовь Бабурина
НЕ ЗНАЮ Я НЕ КУРЮ, И ДРУГИХ РУГАЮ
0
Гордая
Где ты этого бреда начитался ?
0
Марина Киреева
Это вас напрягает?
0
Светлый
очень даже
1
Дарья Томашевская
пойду, покурю
0
Светлый
вот блин а!!!
1
Дарья Томашевская
засада!))))
1
Светлый
и не говори)) одним словом мои руки коротки, не дотянутся до твоих сигарет))
1
Дарья Томашевская
лучше б к другому тянулся)))))))))))
1
Светлый
хах)
1
Другие вопросы
народ, в этом году Мэнни Пакьяо сможет встретиться с Флойдом Мейвезером на ринге?
как стать похожей на папиных дочек (машу? Дашу, Женю, галю? ну или ПУговку?)
Ребят, а что для Вас лучше баскетбол или футбол?
Тарелка Триколор ТВ. Можно ли самим ее установить и подключить?
Можно ли самим ее установить и подключить?
Можно ли самим подключить тарелку Триколор? Отдали тарелку Триколор. Можно ее самим подключить, если можно, то как?
Назовите мне самых известных игроков, которые играют в колхозе.. . тьфу! в сборной Исландии…?
Вопрос 2. Анатомические сведения о человеке. 1. Строение тела человека: его ткани, органы и физиологические системы 2.
Помогите, Какую посудомойку купить? Встраиваемая нужна. Никогда не пользовалась и ни разу не видела их в работе.
Ваши предположения…
Родственики прислали айфон 4с, полностью разблокированный но одно но он на английском, как его русифицировать ?
Подскажите базовую систему тренировок
кто сталкивался с роликами KuzhiLang, копией SEBA High Carbon? почему они на столько дешевле оригинальных?
что значит в волейболе золотая партия и когда она играется ???
какой барабан лучше для стиральной машины?
Сколько стоит iphone5 в Париже сейчас? 8/16/32 гб?
Вред курения на организм — Медицинский портал про здоровье
После того как Колумб открыл Америку, европейцы открыли для себя табак. Однажды мореплаватели пристали к какому-то острову, где встретились с туземцами, которые держали тонкие трубочки из сушеных листочков во рту. Они пускали дым через рот и через нос. Называли они такие трубки “сигаро”.
Однажды мореплаватели пристали к какому-то острову, где встретились с туземцами, которые держали тонкие трубочки из сушеных листочков во рту. Они пускали дым через рот и через нос. Называли они такие трубки “сигаро”.
Мореплаватели стояли и с ужасом наблюдали, как дикари вдыхают этот зловонный, чудовищный дым, который образовывался от горенья листьев. Они, чтобы втянуть дым внутрь использовали длиннющие трубки, изготовленные из коры. Конечную часть такой трубки они вставляли в емкость с горевшими листьями, а противоположный раздвоенный конец, вставляли в ноздри. Такие трубки они называли табако. Листья растения они также разжевывали и глотали.
В середине шестнадцатого века придворный французского короля Жан Нико привез для королевы Екатерины Медичи табачные листья. Она пристрастилась к ним, и утверждала что от них перестает болеть голова. Так в честь посла появилось слово “никотин”. Курение начало распространяться большими темпами, и так как из-за употребления бесконтрольного количества табака люди начали отравляться, то правители начали преследовать людей, которые курили. В разных странах это осуществлялось по разному. К примеру в Британии любителям покурить надевали петлю на шею и так и водили по городу, иногда их даже лишали жизни, а отсеченные головы, со вставленными в рот трубками, выставляли на всеобщее обозрение.
В разных странах это осуществлялось по разному. К примеру в Британии любителям покурить надевали петлю на шею и так и водили по городу, иногда их даже лишали жизни, а отсеченные головы, со вставленными в рот трубками, выставляли на всеобщее обозрение.
О том, как появился табак в России существует несколько версий, но по всей вероятности его привезли купцы из Англии еще при Иване Грозном, а Михаил Романов поставил под запрет курение, так как участились случаи пожаров. Курильщиков жестоко наказывали, вплоть до отрезания ушей. Царь Петр Первый сам любил употреблять табак, а потому отменил наказания.
Как курение может навредить организму
Люди издавна понимали, что это сильная отрава. Ими стали травить клопов и блох. Чтобы справиться с вредителями на деревьях, их опрыскивали раствором из листьев табака. Если курильщику со стажем поставить пиявку, то она, после того как высосет кровь, подыхает.
Вряд ли после каждого глотка табачного дыма курильщик задумывается о том, какой вред ему и его здоровью наносит курение, какие необратимые процессы запускаются с каждой затяжкой.
В одной только обычной сигарете содержится такие токсические вещества как никотин, аммиак, угарный газ, синильная кислота, пиридин, формальдегид, полоний, свинец, висмут, смолы, деготь и другие радиоактивные вещества.
После того. как эти вещества попадают в организм курильщика,они причиняют ему необратимый ущерб. Исследования показали, что курящие люди сокращают среднюю продолжительность жизни на девять лет.
В 1934 году во Франции компания молодых людей устроила нелепое состязание – кто сможет выкурить большее количество папирос за один раз? Двое из «призеров» так и не смогли получить свою награду. Они через некоторое время умерли в клинике, так как получили смертельную дозу никотина. Для взрослого человека смертельная доза составляет от 0,1г до 0,3г, а для этого достаточно выкурить 20 сигарет. Остальным участникам хоть и сало плохо, но после оказания необходимой помощи их удалось спасти.
Если человек только начинает курить, то после того как он сделал первую затяжку у него появляется головокружение, начинает тошнить, его мучает рвота, пульс становится учащенным а тело бледным, то есть налицо все признаки интоксикации.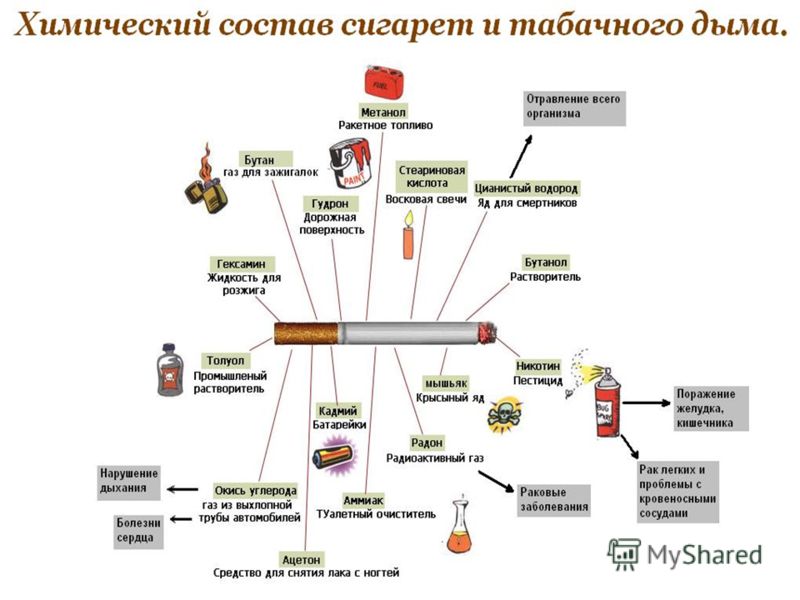 В мировой практике можно найти множество примеров никотиновой интоксикации. Приведем лишь несколько из них.
В мировой практике можно найти множество примеров никотиновой интоксикации. Приведем лишь несколько из них.
Мужчина среднего возраста, куривший по нескольку трубок в день, заключил пари со своим приятелем, кто сможет выкурить больше трубок, но уже после двадцатой ему стало плохо: закружилась голова, появилась тошнота, его вырывало и под конец он упал в обморок. Правда, после оказания медицинской помощи он пришел в себя, но еще долгое время у него не переставала болеть голова.
Другой мужчина, ровесник предыдущего, за пол дня выкурил четырнадцать сигар и две пачки папирос, и при этом ничего не ел. Вследствие дикого эксперимента у него появилась слабость, он весь покрылся холодным потом, у него начались конвульсии, перехватило дыхание и все завершилось летальным исходом.
Трое студентов поспорили, кто сможет без передышки выкурить большее количество папирос, но еще не успев дойти до половины пачки, одному стало плохо. Он потерял сознание, а потом скончался: наступила внезапная коронарная смерть.
Курения наносит необратимый ущерб всему организму в целом и отдельным его органам. Все они подвергаются воздействию канцерогенных веществ, находящихся в табачном дыме. Посмотрим как влияет эта пагубная привычка на отдельные органы курильщика.
Нервная система
Нервная система является самой сложной и хрупкой в нашем организме. Она участвует во всех физиологических процессах, все наши действия производятся с ее помощью. Поэтому курение опасно прежде всего для нервной системы. Когда человек вдыхает продукты горения табака, то они попадают в легкие, затем переносятся в кровь, которая доставляет их прямо в головной мозг, на все это уходит примерно восемь секунд. Никотин “избаловывает” центр удовольствия в головном мозге,и естественно у человека появляется зависимость.
Таким образом нервная система делает нас зависимыми от сигарет. Продукты горения табачных листьев оказывают свое воздействие на многие нервные функции, но большему воздействию подлежит центральная нервная система, скорее головной мозг. Ведь при курении сужаются мозговые сосуды, и вследствие этого уменьшается количество крови приливающей к нервной ткани. По этой причине чаще начинает болеть голова, ухудшается состояние памяти, человек долгое время не может сосредоточиться.
Ведь при курении сужаются мозговые сосуды, и вследствие этого уменьшается количество крови приливающей к нервной ткани. По этой причине чаще начинает болеть голова, ухудшается состояние памяти, человек долгое время не может сосредоточиться.
Органы чувств
Во время курения не избегают негативного воздействия также и органы чувств. Их функции нарушают токсичные вещества, находящиеся в табаке. Большинство курильщиков теряют вкусовые ощущения. Ведь их язык всегда покрыт густой вязкой слизью, перекрывающей доступ еды к тем рецепторам, которые отвечают за ощущения вкуса. Если заядлому курильщику и обычному человеку, который не курит, дать попробовать слегка сладковатую и подсоленную воды, то первый не сможет найти разницы, между тем как второй легко справится с задачей.
У курящего человека также нарушается обоняние. Он начинает плохо воспринимать запахи. Вследствие курения у него воспаляется слизистая оболочка носа, последствием чего может стать хронический насморк. Чтобы наглядно увидеть, как влияет курение на обоняние, проведите небольшой эксперимент. Поднесите зажженную сигарету к носу собаки: вдохнув ее дым, она тут же теряет нюх.
Чтобы наглядно увидеть, как влияет курение на обоняние, проведите небольшой эксперимент. Поднесите зажженную сигарету к носу собаки: вдохнув ее дым, она тут же теряет нюх.
От курения может пострадать также зрение: табачный дым негативно влияет на сетчатку глаза и зрительный нерв. При этом может развиться дальтонизм. И конечно же при курении могут пострадать органы слуха. Ведь ядовитые вещества приводят к воспалению носоглотки, которая соединена с барабанной полостью. Вследствие этого воспаление может перейти и на слуховой нерв.
Хотя органы чувств сложно устроены, но это всего лишь начальный этап, в процессе ощущения внешнего мира. Все эти восприятия передаются посредством нервов в головной мозг, и там подвергаются анализу. А значит курение негативно влияет и на органы чувств, и на центральную нервную систему. При этом нарушается вся система ощущения внешнего мира.
Органы дыхания
Больше всего страдают от курения конечно же органы дыхания, ведь это на них приходится первый удар токсинов. Табачный дым, который вдыхает курильщик при раскуривании обычной сигареты приводит к воспалению дыхательной системы и поэтому большая часть курящих людей страдают хроническим бронхитом, у них появляются частые выделения мокроты слизисто-гнойного типа. Все это сопровождается постоянным мучающим кашлем, который особо усиливается в утреннее время, человек все время пытается отхаркиваться, а мокрота при этом имеет грязный серый цвет. Иногда инфекция может пойти дальше, и проникнуть в лёгочную ткань, и из-за этого может развиться пневмония или нарыв легких.
Табачный дым, который вдыхает курильщик при раскуривании обычной сигареты приводит к воспалению дыхательной системы и поэтому большая часть курящих людей страдают хроническим бронхитом, у них появляются частые выделения мокроты слизисто-гнойного типа. Все это сопровождается постоянным мучающим кашлем, который особо усиливается в утреннее время, человек все время пытается отхаркиваться, а мокрота при этом имеет грязный серый цвет. Иногда инфекция может пойти дальше, и проникнуть в лёгочную ткань, и из-за этого может развиться пневмония или нарыв легких.
Так как у курильщика голосовые связки все время раздражаются, то от этого у него грубеет голос. Он становится хриплым и не очень приятным. От этого может также пострадать профессиональная деятельность человека, если к примеру курильщик певец, ведущий и тому подобное.
В течение года легкие курильщика пропускают через себя около восьмисот граммов табачной смолы. Их легкие от этого темнеют, по сравнению с легкими обычного человека.
Если человек продолжает активно употреблять табачные изделия, то соединительная ткань лёгких теряет свою упругость, дыхательные трубки растягиваются и выпячиваются, а это может привести к образованию бронхоэктазов. Бронхоэктаз — хроническое воспалительное заболевание, которое длится много лет.
Вследствие этих болезней легкие могут уплотниться, а это может привести к пневмосклерозу. Из-за хронического кашля ткани легких могут потерять свою упругость, вследствие чего образуется эмфизема легких. Исследования показали, что работа легких страдает во всех отношениях, и они уже не в состоянии бороться с внешними инфекциями. При этом также повышается вероятность заболевания туберкулезом, ведь курильщики болеют им в два раза чаще обычных людей. В конечном итоге курение может стать причиной образования онкологических заболеваний, и чем больше папирос за день вы курите, тем больше вероятность рака легких.
Если человек перестал курить вероятность онкологических заболеваний становится меньше. Изучив привычки больных раком легкого врачи сделали вывод: почти все они любители табака. Табак может вызвать также рак желудка. Ведь при глотании слюны все ядовитые вещества попадают прямо в желудок. Можно при помощи опытов доказать, что в табачных листьях сконцентрированы канцерогенные вещества. Если в течение года смазывать ухо кролика веществом, которое получено из табачной смолы, то у кроликов начинается онкологическое заболевание. Ведь табачный дым содержит сильнейший канцероген, который называется бензапирен, который и приводит к развитию раковых образований. Это вещество первого класса опасности. И это не единственное опасное вещество, содержащееся в табачном дыму. Онкологические образования могут вызвать хризен, дибензантрацен, дибензапирен и другие.
Изучив привычки больных раком легкого врачи сделали вывод: почти все они любители табака. Табак может вызвать также рак желудка. Ведь при глотании слюны все ядовитые вещества попадают прямо в желудок. Можно при помощи опытов доказать, что в табачных листьях сконцентрированы канцерогенные вещества. Если в течение года смазывать ухо кролика веществом, которое получено из табачной смолы, то у кроликов начинается онкологическое заболевание. Ведь табачный дым содержит сильнейший канцероген, который называется бензапирен, который и приводит к развитию раковых образований. Это вещество первого класса опасности. И это не единственное опасное вещество, содержащееся в табачном дыму. Онкологические образования могут вызвать хризен, дибензантрацен, дибензапирен и другие.
В табачном дыму содержатся также органические соединения, являющиеся производными аммиака. Они растворяясь в слюне попадают прямо в желудок, где образуются нитрозамиды, вызывающие злокачественные опухоли. Интересно то, что табачные листья могут содержать как натуральные, так и искусственные химические элементы, все изотопы которых радиоактивны, причем в готовой продукции (сигареты, сигары, папиросы) изотопов гораздо меньше, чем в самих листьях. Это можно объяснить тем, что во время переработки табака на заводах радиоактивный полоний начинает распадаться, и продолжает это делать при хранении готовых продуктов на складах. В общих числах табачная зола содержит примерно девять процентов изотопа, окурок двадцать процентов, фильтр восемь процентов, а дым аж целых пятьдесят.
Это можно объяснить тем, что во время переработки табака на заводах радиоактивный полоний начинает распадаться, и продолжает это делать при хранении готовых продуктов на складах. В общих числах табачная зола содержит примерно девять процентов изотопа, окурок двадцать процентов, фильтр восемь процентов, а дым аж целых пятьдесят.
Таким образом половина изотопов сконцентрирована в табачном дыме, откуда попадает в человеческий организм. Исследователи провели следующий эксперимент: они сделали надрез между гортанью и бронхами собаке, и каждый день надували дым от нескольких папирос. В итоге после двух лет у собаки сформировался рак легких.
Сердечно-сосудистая система
Курение наносит непоправимый ущерб сердечно-сосудистой системе. Если человек курит, то сразу после того как он в первый затягивается, у него пульс становится частым, вследствие чего увеличивается нагрузка на сердце. Сердце здорового человека может справиться с ней, а если у курильщика проблемы с сердцем, то оно с трудом будет справляться.
Исследования показывают, что при курении повышается артериальное давление. Это происходит потому, что надпочечники начинают выделять особые гормоны, и от этого увеличивается нагрузка на сердце. Оно начинает затрачивать больше сил для перегонки крови через просвет сосудов, который несравнимо уменьшился. Вследствие этого кровь начинает плохо поступать в органы, понижается температура кожи, руки и ноги становятся холодными.
Из-за курения у человека также может образоваться атеросклероз. Давайте посмотрим как он возникает.
При курении образуется огромное количество фенилэтиламинов. Эти фенилэтиламины благоприятствуют увеличению плотности содержания жиров в крови, вследствие чего в сосудах образуются атеросклеротические бляшки. Кроме того ядовитые вещества, которые попадают в кровь при курении мешают усвоению аскорбиновой кислоты, а из-за ее нехватки на стенках сосудов может отлагаться холестерин, сужающий просвет сосудов.
Если к сердцу поступает недостаточно крови, то может произойти ожирение сердца. Итак, курение может способствовать формированию атеросклероза, а последний к патологическому состоянию, при котором абсолютно или относительно нарушается кровоснабжение миокарда, из-за поражения коронарных артерий. может К таким заболеваниям относятся болезни сердца и нарушению его функционирования, которые связаны с недостаточным поступлением крови в сосуды, питающие сердце. Основная причина развития таких заболеваний — атеросклероз и часто повышающееся давление, а последние развиваются наиболее часто вследствие курения. Согласно статистике Всемирной Организации Здравоохранения ишемическая болезнь сердца у курильщиков встречается более часто, чем у тех, кто не курит.
Итак, курение может способствовать формированию атеросклероза, а последний к патологическому состоянию, при котором абсолютно или относительно нарушается кровоснабжение миокарда, из-за поражения коронарных артерий. может К таким заболеваниям относятся болезни сердца и нарушению его функционирования, которые связаны с недостаточным поступлением крови в сосуды, питающие сердце. Основная причина развития таких заболеваний — атеросклероз и часто повышающееся давление, а последние развиваются наиболее часто вследствие курения. Согласно статистике Всемирной Организации Здравоохранения ишемическая болезнь сердца у курильщиков встречается более часто, чем у тех, кто не курит.
Органы пищеварения
Как только табачный дым попадает в ротовую полость, начинается его разрушительная работа. Дыхание курильщика всегда несвежее, плохо пахнущее, язык всегда покрыт сероватым налётом. Из-за воздействия с никотином и веществами, находящихся в табачном дыме начинают желтеть и портиться зубы. Табачный дым поступает в ротовую полость при температуре пятьдесят-шестьдесят градусов, а вот температура окружающей среды чуть пониже. Такие перепады температуры портят зубы. Трескается зубная эмаль, начинают кровоточить десны, развивается кариес, который может послужить основой для занесения заразы.
Такие перепады температуры портят зубы. Трескается зубная эмаль, начинают кровоточить десны, развивается кариес, который может послужить основой для занесения заразы.
Токсичные вещества при курении попадают в органы пищеварения разным способом. Они могут попасть как через ЦНС, так и через слюну и кровеносную систему.
Существует прямая связь между употреблением табака и язвой желудка, причем курильщики умирают от нее намного чаще. При попадании в рот, никотин способствует усиленному выделению слюны. Человек начинает глотать ее, и тут никотин начинает свое разрушительное воздействие на пищеварительный тракт. Он начинает раздражать слизистую оболочку желудка, вследствие чего начинается интенсивная выработка желудочного сока с очень высокой кислотностью, а если к этому присоединятся бактерии, то может возникнуть хронический гастрит.
Никотин препятствует нормальному сокращению желудка, а также кишечника. Если человек выкуривает сигарету, от этого желудок начинает сокращаться реже.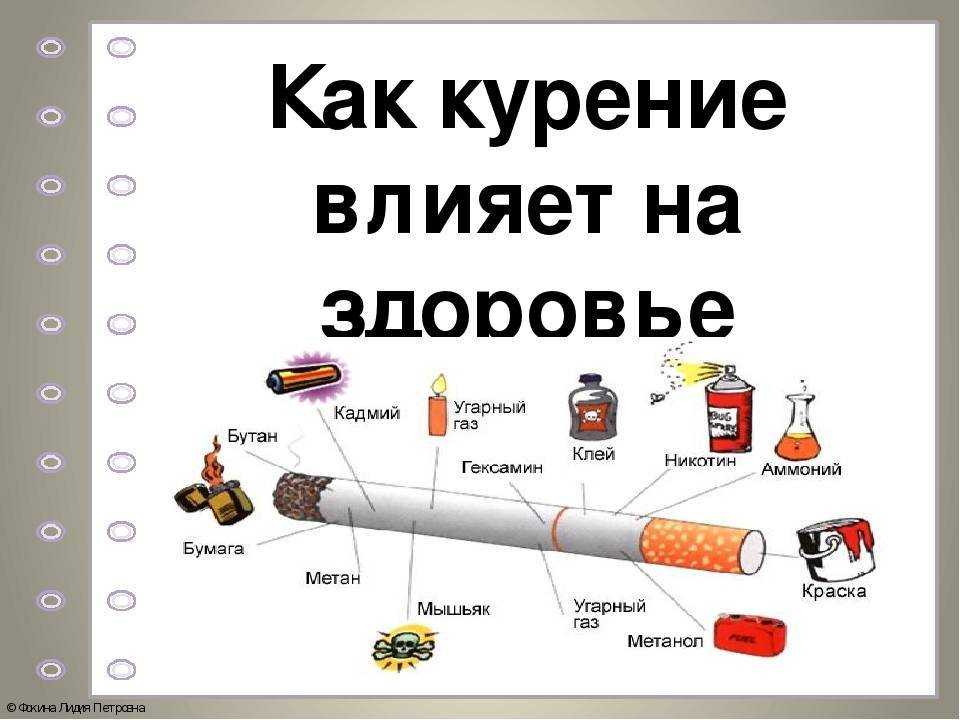 Поэтому почти у всех курящих людей наблюдаются проблемы с пищеварением. Непоправимый ущерб наносится также печени. У курильщиков она увеличивается в размерах, при этом она возвращается к своим прежним размерам, если перестать курить. Не остается в стороне также и поджелудочная железа, ведь длительное раскуривание табачных изделий может привести к раку поджелудочной железы. Все это относится также и к пассивным курильщикам. Если они вынуждены долгое время находиться в закрытом помещении вместе с курящими, то они рискуют с ними в равной степени.
Поэтому почти у всех курящих людей наблюдаются проблемы с пищеварением. Непоправимый ущерб наносится также печени. У курильщиков она увеличивается в размерах, при этом она возвращается к своим прежним размерам, если перестать курить. Не остается в стороне также и поджелудочная железа, ведь длительное раскуривание табачных изделий может привести к раку поджелудочной железы. Все это относится также и к пассивным курильщикам. Если они вынуждены долгое время находиться в закрытом помещении вместе с курящими, то они рискуют с ними в равной степени.
Эндокринная система
Табачный дым и токсины, которые содержатся в нем, оказывают негативное влияние на эндокринную систему. Частое курение может привести к нарушению функционирования желез внутренней секреции: щитовидной, половой. Люди, у которых поражена щитовидная железа, бывают вспыльчивыми, раздражительными. У курильщиков со стажем сперва возникает половая слабость, а затем может наступить импотенция.
Табачный дым содержит окись углерода, который нарушает нормальную доставку кислорода в организм человека. Вследствие нехватки кислорода поражаются сосуды и развивается окклюзия. Тонкие кровеносные сосуды находящиеся в тканях полового члена закупориваются, кровь к половому органу начинает поступать в меньших количествах и развивается нарушение эрекции. Кроме этого табачный дым содержит углеводороды, убивающие женские яйцеклетки. Все это приводит к тому, что у женщин, которые курят наблюдается более раннее наступление менопаузы, чем у женщин, которые не курят.
Вследствие нехватки кислорода поражаются сосуды и развивается окклюзия. Тонкие кровеносные сосуды находящиеся в тканях полового члена закупориваются, кровь к половому органу начинает поступать в меньших количествах и развивается нарушение эрекции. Кроме этого табачный дым содержит углеводороды, убивающие женские яйцеклетки. Все это приводит к тому, что у женщин, которые курят наблюдается более раннее наступление менопаузы, чем у женщин, которые не курят.
Органы слуха
Курение также может быть причиной нарушений работы органов слуха. У людей, часто употребляющих табак, острота слуха понижается. Токсины, содержащиеся в табаке, могут вызвать у человека воспаление носоглотки. Это воспаление затем становится хроническим. Носоглотка соединена с барабанной полостью, и следовательно воспалительный процесс передается и сюда, а затем распространяется на слуховой нерв. Барабанная перепонка утолщается, и из-за этого снижается подвижность слуховых косточек. Все это вредит слуху.
Итак, как мы видим, курение способно навредить как всему организму, так и его отдельно взятым органам. Если человек курит по одной пачке сигарет в день, то он тем самым вводит смертельную дозу никотина, и он не умирает только из-за того, что он выкуривает эту пачку не сразу, а постепенно. Вам решать курить дальше или принять здоровый образ жизни и пройти лечение от табакокурения.
Если человек курит по одной пачке сигарет в день, то он тем самым вводит смертельную дозу никотина, и он не умирает только из-за того, что он выкуривает эту пачку не сразу, а постепенно. Вам решать курить дальше или принять здоровый образ жизни и пройти лечение от табакокурения.
Употребление наркотиков наносит невосполнимый вред здоровью и представляет опасность для жизни!
Ни для кого не секрет, что курильщики часто болеют и рано умирают. По статистике ежегодно погибает от 3,4 до 5,4 млн. человек в результате острых и хронических болезней, вызванных пристрастием к табачной продукции. Во вдыхаемом дыме содержится около 250 соединений, которые вредят здоровью, из них более трети вызывают развитие раковых опухолей.
Список заболеваний
Множественные научные исследования доказали, что курение способствует развитию таких заболеваний, как:
- рак гортани, губ, языка, пищевода, легких, желудка и других органов
- эмфизема легких, астма, ХОБЛ (хроническая обструктивная болезнь легких), бронхит, пневмония
- стенокардия, инфаркт миокарда, инсульт
- облитерирующий эндартериит или тромбоз нижних конечностей
- аневризма аорты
- гастрит, язвенная болезнь, панкреатит
- катаракта
- остеопороз
- эректильная дисфункция и бесплодие
Кроме того, постоянное присутствие токсинов в организме снижает иммунную защиту. Поэтому вероятность заражения туберкулезом и другими инфекциями повышается во много раз. Вредная привычка способствует появлению ревматоидного артрита, диабета второго типа. У каждого курильщика возникает тяжелая зависимость. Многие не могут бросить сигарету даже после развития опасного для жизни заболевания.
Поэтому вероятность заражения туберкулезом и другими инфекциями повышается во много раз. Вредная привычка способствует появлению ревматоидного артрита, диабета второго типа. У каждого курильщика возникает тяжелая зависимость. Многие не могут бросить сигарету даже после развития опасного для жизни заболевания.
Табачный дым содержит более семидесяти химических веществ, которые вызывают рак. Табак также содержит никотин, являющийся высоко аддиктивным психоактивным веществом. При курении табака, никотин вызывает физическую и психологическую зависимость. Сигареты, продаваемые в менее развитых странах, имеют более высокое содержание смол и редко снабжены фильтрами, тем самым они потенциально повышают уязвимость организма к болезням, связанным с курением табака в этих регионах.
Органы дыхания
Первый удар ядов табака приходится на органы дыхания. Сажа, никотин и другие компоненты проходят через слизистые оболочки гортани, трахеи, бронхиального дерева и оседают в легких. В результате возникает реакция раздражения и воспаления. Поэтому у курильщиков наблюдается:
Поэтому у курильщиков наблюдается:
- постоянный кашель, усиливающийся по утрам во время пробуждения
- осиплость голоса
- одышка
- легочная недостаточность
Самым страшным последствием является необратимая умственная деградация
Необходимо как можно раньше распознать зависимость и начать ее лечить.
Под воздействием токсинов (монооксид углерода и цианидиум) происходит растяжение альвеол и гибель эпителия, а акролеин провоцирует воспаление. В результате этих процессов постепенно развивается эмфизема, ХОБЛ и снижается сопротивляемость попавшей внутрь инфекции. В 8 из 10 случаев обструктивные заболевания вызываются вредной привычкой. Они сопровождаются значительным снижением объема легких.
В настоящее время точно установлена связь между курением и вероятностью заражения туберкулезом. У людей с никотиновой зависимостью это тяжелое заболевание наблюдается намного чаще, чем у других. А появление рака легких и гортани у курильщиков в 10 раз выше, поскольку канцерогенные вещества табачного дыма. Особенно это касается любителей глубоких затяжек и тех, кто использует второй раз недокуренные сигареты.
Особенно это касается любителей глубоких затяжек и тех, кто использует второй раз недокуренные сигареты.
Сердечно-сосудистая система
Курение приводит к высокому риску развития заболеваний сердца и сосудов. Именно такие острые состояния как инфаркт и инсульт являются причиной повышенной смертности среди курильщиков. По статистике у них вероятность летального исхода в результате острой коронарной или мозговой ишемии повышается в 4 раза, по сравнению с некурящими людьми.
Исследования, проведенные с 1995 до 1999 год, показали, что у людей с пристрастием к никотину жизнь сокращается примерно на 10 лет. И при этом более 70% из них умирает от онкологии или сердечно-сосудистых заболеваний.
Ишемическая болезнь сердца
Под воздействием никотина усиливается продукция надпочечниковых гормонов. Они вызывают тахикардию и повышают артериальное давление. Сердце испытывает постоянные перегрузки и ему требуется больше кислорода и энергии. Однако суженные коронарные артерии не могут обеспечить миокард, а поступающая с дымом окись углерода снижает способность крови переносить кислород. Одновременно увеличение вследствие вредной привычки холестерина низкой плотности приводит к атеросклерозу. На фоне этого развивается стенокардия и инфаркт.
Одновременно увеличение вследствие вредной привычки холестерина низкой плотности приводит к атеросклерозу. На фоне этого развивается стенокардия и инфаркт.
Заболевания сосудов
Постоянное действие на сосуды токсинами приводит к хрупкости их стенок, отложению бляшек, сужающих просвет, и спазму. Курильщики с большим стажем часто проходят лечение по поводу облитерации и тромбозов артерий (из-за повышенной выработки фибриногена). Чаще всего страдают нижние конечности, где в результате резкого нарушения кровообращения возникают такие симптомы:
- бледность и сухость кожи
- снижение локальной температуры
- трофические язвы
- гангрена
Исследования американских биологов показало, что в результате постоянного курения у человека нарушается процесс деления клеток и изменяется форма сердца. Повышается риск развития аневризмы брюшного отдела аорты.
Нервная система и формирование зависимости
Многие курильщики полагают, что сигарета позволяет им расслабиться и сосредоточиться. На самом деле это всего лишь иллюзия, поскольку зависимые от никотина отличаются от остальных повышенной нервозностью, часто паникуют и раздражаются по пустякам. Поэтому важно знать, что происходит под действием сигареты на самом деле:
На самом деле это всего лишь иллюзия, поскольку зависимые от никотина отличаются от остальных повышенной нервозностью, часто паникуют и раздражаются по пустякам. Поэтому важно знать, что происходит под действием сигареты на самом деле:
- постепенно атрофируются и отмирают клетки головного и спинного мозга
- скорость передачи импульсов по нервным волокнам и в синапсах замедляется
- без перекура становится трудно решать сложные задачи, требующие высокой концентрации
Первичный эффект никотина заключается в ускорении процессов возбуждения. Он становится стимулятором, к которому развивается привыкание. Но после его действия наступает фаза расслабления, так как мозгу требуется отдых. Позднее он уже не может полноценно функционировать без привычного допинга.
Курильщики, которым нужно работать начинают проводить время с сигаретой все чаще. При этом переутомление все больше нарастает, так как табачные ингредиенты не добавляют энергии, а только лишь подхлестывают организм. С годами у зависимых снижается память, нарушается сон, наблюдается частая смена настроения. Атрофические изменения нервных волокон и нарушение питания тканей позвоночника приводит к развитию радикулита, полиневрита.
С годами у зависимых снижается память, нарушается сон, наблюдается частая смена настроения. Атрофические изменения нервных волокон и нарушение питания тканей позвоночника приводит к развитию радикулита, полиневрита.
Страдает также вегетативная нервная система, которая напрямую связана с функцией внутренних органов. Поэтому при частом курении наблюдается:
- расстройство пищеварения
- нарушения сердечного ритма
- выраженная потливость, перемежающаяся с ознобом
- скачки давления
Нарушению подвергаются органы чувств. Поражается роговица глаз, появляется конъюнктивит как реакция раздражения на дым, снижается острота зрения, повышается вероятность развития катаракты. У многих курящих снижается слух, восприятие запахов и вкуса пищи.
Органы пищеварения
При попадании дыма от сигарет в полость рта происходит раздражение слизистых. Часть токсических веществ сглатывается, и вместе с пищей и слюной проходит в желудок и кишечник.
Капля никотина не только «убивает лошадь», но и помогает предотвратить развитие болезни Альцгеймера. Щелчок зажигалки, несколько затяжек – и вот уже через 7 секунд человек молекулы вещества преодолевают гематоэнцефалический барьер и начинают действовать на головной мозг. Эффект никотина заключается не только в возникновении расслабленности, приподнятого настроения. Вещество также влияет на ритмы сна и бодрствования, аппетит, восприятие боли, пищеварение и сердечно-сосудистую систему.
Щелчок зажигалки, несколько затяжек – и вот уже через 7 секунд человек молекулы вещества преодолевают гематоэнцефалический барьер и начинают действовать на головной мозг. Эффект никотина заключается не только в возникновении расслабленности, приподнятого настроения. Вещество также влияет на ритмы сна и бодрствования, аппетит, восприятие боли, пищеварение и сердечно-сосудистую систему.
Регулярное курение приводит к формированию синдрома зависимости и хроническим изменениям в тканях и органах.
Свойства никотина
Что же такое никотин? Это алкалоид — органическое гетероциклическое вещество, состоящее из атомов углерода, азота и водорода. Своим названием группа соединений обязана своими слабощелочными химическими свойствами. Большинство алкалоидов оказывают влияние на нервную систему, среди тех. что «на слуху» у людей – кофеин, кокаин, морфин.
По физическим и органолептическим свойствам никотин — это горькая маслянистая жидкость. При определенных температурах легко смешивается с водой, их плотности практически одинаковы – около 1 г/ см3.
Никотин хорошо растворяется в средах, имеющих низкую полярность. Это обуславливает его быстрое всасывание через кожу и гематоэнцефалический барьер. При высоких значениях pH среды без труда проникает сквозь слизистые.
Где содержится никотин? Алкалоид выделяют из побегов растений семейства пасленовых (табак, помидоры, баклажан, картофель). Концентрация в табаке максимальна – до 14 %. Никотин синтезируется в корнях растений, транспортируется и накапливается в листьях. В организме человека и теплокровных животных соединение распадается с образованием безопасных метаболитов.
Сколько никотина содержится в сигаретах
Диапазон смертельной дозы вещества находится в пределах от 50 до 100 мг. Вспоминая о капле никотина, убившей лошадь, токсикологи отмечают, что человеку достаточно 2-3 капель. Такое количество алкалоида человек может получить из 1,5 пачках сигарет.
Сколько никотина содержится в 1 сигарете? Табачная промышленность выпускает изделия различной крепости. Количество никотина в них находится в диапазоне от 0,3 мг до 1,26 мг. Например, одна сигарета Parliament может «снабдить» курильщика 0,5 мг никотина, а «раковая палочка» Marlboro из красной пачки – 1,1 мг.
Количество никотина в них находится в диапазоне от 0,3 мг до 1,26 мг. Например, одна сигарета Parliament может «снабдить» курильщика 0,5 мг никотина, а «раковая палочка» Marlboro из красной пачки – 1,1 мг.
Интересно, что крепость изделий в линейке одного производителя может определяться исключительно как субъективное ощущение. Фильтр у так называемых легких сигарет имеет большее число перфораций, чем у их крепких. Это позволяет курильщику втягивать больше воздуха, за счет чего концентрация никотина и других ядовитых веществ во вдыхаемом воздухе становится ниже, а вкус – не таким «грубым».
Еще один секрет «легкой» продукции: такие изделия тлеют самостоятельно. Количество табака постепенно уменьшается, даже если человек не делает затяжку и просто держит сигарету в руке.
Сама идея градации сигарет была связана с попыткой табачных корпораций сохранить потребителей: курение легких изделий преподносилось как процесс отказа от пагубной привычки. В действительности люди увеличивали суточное число сигарет, так как считали, что получают меньше смол и никотина. Согласно Рамочной конвенции ВОЗ маркировка «легкие», «мягкие» на пачке запрещена.
Согласно Рамочной конвенции ВОЗ маркировка «легкие», «мягкие» на пачке запрещена.
Как быстро никотин покидает организм
После вдыхания никотин быстро всасывается в кровеносное русло и уже через несколько секунд попадает в головной мозг. Период полувыведения (то время, за которое концентрация вещества падает вдвое) составляет около 2 часов. В зависимости от стажа курения, способа употребления табака скорость поступления и метаболизма может различаться. Информация об этом помогает понять:
- с какой частотой человек испытывает потребность «затянуться»;
- как правильно подбирать терапию для облегчения синдрома отмены.
Около 30% никотина, поступившего в организм, выводится в неизмененном виде, оставшиеся 70% — в виде нетоксичного котинина. Полный цикл распада никотина занимает около 6-8 часов. Отвечая на вопрос, сколько выводится никотин из организма, специалисты, называют сроки 1-2 дня.
Интересно, что название метаболита котинина — анаграмма слова «никотин». Вещество имеет сродство к Н-холинорецепторам, оказывая слабое противотревожное и антипсихотическое действие. Его период полувыведения занимает до 20 часов. Изучение давности последнего употребление медицинских препаратов или курения оценивают по наличию котинина и никотина в моче.
Вещество имеет сродство к Н-холинорецепторам, оказывая слабое противотревожное и антипсихотическое действие. Его период полувыведения занимает до 20 часов. Изучение давности последнего употребление медицинских препаратов или курения оценивают по наличию котинина и никотина в моче.
Никотин встречается с рецептором
Воздействие никотина на организм реализуется через связь с никотиновыми холинорецепторами (или Н-холинорецепторами) и частично — адренорецепторами.
Вегетативная нервная система отвечает за автономную работу внутренних органов. Она состоит из 2 частей – симпатической и парасимпатической. Работа биологически активных веществ происходит на уровне синапсов – мест контакта нейронов с нейронами или клетками органов. Каждый из них состоит из пресинаптической. постсинаптической мембран клеток и щели между ними.
Передача импульсов в парасимпатическом отделе осуществляется за счет медиатора ацетилхолина. При взаимодействии его с пресинаптической мембраной рецептора:
- сужаются зрачки;
- снижается артериальное давление;
- снижается частота сердечных сокращений;
- расширяются периферические кровеносные сосуды;
- сокращаются мышечные волокна внутренних органов;
- усиливается секреция потовых, бронхиальных, пищеварительных, слезных желез.

Но работа ацетилхолина не ограничивается только парасимпатической системой. К симпатическому отделу медиатор тоже «прикладывает руку». Соединяясь с рецептором на пресинаптической мембране, он оказывает действие, напоминающее работу адреналина. А именно:
- учащается сердцебиение;
- повышается артериальное давление;
- увеличивается концентрация глюкозы в крови;
- активируется распад жиров;
- снижается аппетит.
Никотин имеет схожее строение с важной C-петлей молекулы ацетилхолина, но связь алкалоида с холинорецептором более прочна. Химики утверждают, что его молекула идеально замещает ацетилхолин во всех отделах вегетативной нервной системы. Влияние никотина на организм человека практически идентично и складывается из его воздействия на рецепторы в различных тканях.
Никотин и головной мозг
Воздействие алкалоида на мозг связано с активацией α4β2-рецепторов. Они составляют более 80% от всех Н-холинорецепторов ЦНС. Сродство никотина к ним так высоко, что даже ацетилхолин не может с ним конкурировать. Эти рецепторы принимают участие в выделении таких медиаторов, как дофамин, ГАМК, глутамат. Так курение улучшает внимание, память.
Эти рецепторы принимают участие в выделении таких медиаторов, как дофамин, ГАМК, глутамат. Так курение улучшает внимание, память.
Влияние никотина на мозг человека заключается:
- в стабилизации эмоционального фона;
- в снижении тревожности;
- в повышении устойчивости к стрессам;
- в ускорении реакции;
- в улучшении восприятия зрительной и слуховой информации.
Кроме того, алкалоид активизирует метаболизм в ткани мозга и позволяет отсрочить гибель клеток. Это обстоятельство легло в основу клинических исследований, доказавших эффективность никотина как средства профилактики атрофических поражений головного мозга (например, болезни Альцгеймера).
Эффект расслабления и повышения стрессоустойчивости,за который отвечает ацетилхолин, играет злую шутку при формировании зависимости. Так как никотин лучше связывается с рецепторами, организм перестает вырабатывать медиатор самостоятельно. Если человек решает отказаться от сигарет или в силу различных обстоятельств не может утолить никотиновый голод сиюминутно, появляется беспокойство, раздражительность. Постепенно зависимый начинает прибегать к курению не для того, чтобы чувствовать себя замечательно, а для того, чтобы устранить дискомфорт.
Постепенно зависимый начинает прибегать к курению не для того, чтобы чувствовать себя замечательно, а для того, чтобы устранить дискомфорт.
Симптомы физической зависимости отчасти связаны с эндогенными опиатами в головном мозге. Постоянное поступление никотина способствует высвобождению эндорфинов, энкефалинов, играющих важную роль в снижении болевых ощущений.
Никотиновая «бодрость» и «привлекательная стройность» — результат воздействия алкалоида на определенную группу нейронов головного мозга. Эти клетки выделяют вещества, принимающие участие в снижении аппетита, расщеплении жиров и поддержании высокого уровня активности. При отказе от курения человек может ощущать потребность в больших количествах пищи, становится вялым и сонливым.
Никотин и сердечно-сосудистая система
Как было описано ранее, воздействие никотина на оба отдела вегетативной нервной системы, реализуется через изменение просвета сосудов, частоты сердечных сокращений, колебание артериального давления. Спазм артерий, тахикардия и рост давления — результат выброса адреналина. Сердце начинает работать в авральном режиме, проталкивая кровь по суженным сосудам. Оно вынуждено справляться с возросшей нагрузкой. Если человек курит непрерывно, сосуды постоянно спазмированы.
Спазм артерий, тахикардия и рост давления — результат выброса адреналина. Сердце начинает работать в авральном режиме, проталкивая кровь по суженным сосудам. Оно вынуждено справляться с возросшей нагрузкой. Если человек курит непрерывно, сосуды постоянно спазмированы.
Также никотин снижает уровень вещества простациклина, помогающего крупным и мелким артериям расслабиться после сокращения. Ухудшается кровоснабжение всех органов, включая важнейшие из них – мозг и сердце. Фактически курильщик живет в состоянии гипоксии.
Активное и пассивное курение разрушает мембраны клеток, расположенных на внутренней поверхности сосудов. Так изменения эндотелия аорты наблюдаются даже у младенцев 1 месяца жизни, если их мать не расстается с сигаретой. Опасное влияние никотина на сосуды человека может привести к внезапной смерти. Риск острого коронарного синдрома у взрослых пассивных курильщиков по сравнению с теми, кто изолирован от табачного дыма, увеличивается почти на 100%.
Активация липолиза и повреждение стенок сосудов ускоряют развитие атеросклероза любых локализаций.
Кроме того, никотин влияет на реологические свойства крови. Он увеличивает способность тромбоцитов к склеиванию. В сосудах образуются мелкие сгустки. Вязкость крови растет, скорость течения снижается. Наличие повреждений сосудистой стенки приводит к адгезии форменных элементов и образованию пристеночных тромбов.
Так влияние никотина на сердце и сосуды человека заключается в увеличении риска развития:
- артериальной гипертензии;
- ишемической болезни сердца;
- инфаркта, инсульта;
- гангрены.
Как формируется зависимость от никотина
Начиная курить, человек преодолевает естественное неприятие сигареты (высокая температура дыма, вкус, запах). Кроме того, часто первой реакцией на попадание никотина в кровь становится слюнотечение и противная тошнота, которая может продолжаться до получаса. Ее возникновение связано с активацией Н-холинорецепторов и наиболее выражено у «новичков». Если человек справляется с этим ощущением и продолжает «дымить», его шансы стать заядлым курильщиком возрастают.
Регулярное использование табачных изделий вне зависимости от способа доставки никотина (сигареты, нюхательный или жевательный табак) вызывает комфортные субъективные ощущения. Их вид и предвкушение потребления ассоциируются с чувством спокойствия, расслабленности.
Это наблюдение было подтверждено результатами двойного слепого исследования. В ходе него курильщикам предлагали сначала пастилку с никотином или плацебо, а затем сигарету с никотином или сигарету без никотина. Получилось, что:
- Сам процесс курения был связан с удовольствием, вне зависимости от того, содержался ли в сигарете никотин.
- Предварительное «насыщение» никотином в пастилке приводило к снижению влечения, исследуемые делали меньше затяжек.
Затем было доказано, что именно ингаляционный способ применения обеспечивает самую быструю доставку вещества к тканям головного мозга. Такая скорость воспринимается как немедленное вознаграждение и становится одной из причин формирования зависимости.
Размышляя, почему так трудно бросить курить, наркологи подчеркивают, что имеют дело не с вредной привычкой, а с настоящей зависимостью. С течением времени потребление начинает отвечать следующим критериям:
- человек увеличивает число сигарет в сутки;
- при отказе развивается синдром отмены;
- курильщик не может контролировать количество сигарет;
- были неудачные попытки бросить;
- человек понимает, что сигареты вредны, но не может от них отказаться.
Инструментальная диагностика доказывает это утверждение. Медики исследовали функциональную МРТ (фМРТ) головного мозга у курильщиков, вынужденных отказываться от никотина в течение 2 суток. Были обнаружены изменения активности структур, идентичные таковым у кокаиновых и амфетаминовых наркоманов.
Наркологи отмечают, что при самостоятельном отказе от курения в состояние ремиссии входит не более 5% зависимых. Достаточным сроком для оценки воздержания считают интервал 3 года.
Никотин – органическое соединение, имеющее высокое сродство к рецепторам нервной системы. Он действительно улучшает когнитивные способности, но вред, который приносит организму курение, выше предполагаемой пользы.
Он действительно улучшает когнитивные способности, но вред, который приносит организму курение, выше предполагаемой пользы.
Любая форма зависимости оказывает пагубное воздействие на жизнь человека. Будь это алкоголь, сигареты или наркотики. Разберем подробнее, как курение влияет на желудок и другие органы желудочно-кишечного тракта (ЖКТ).
Механизм действия
Употребление табачных изделий в любом виде хорошо изучено. Всемирная организация здравоохранения (ВОЗ) заявляет о существовании массовой эпидемии, наносящей самый тяжелый урон численности населения. После первого вдыхания дыма уже в течение 15 секунд действующее вещество попадает в зону действия чувствительных рецепторов. Происходит выброс дофамина — гормона удовольствия. После выведения никотина из крови, наступает своеобразный «голод», и организм начинает требовать новую дозу. Новая выкуренная папироса лишь замыкает рефлекторную дугу: сигарета — удовольствие — сигарета. Постепенно никотин встраивается в физиологические процессы, и его отсутствие выливается в ряд неприятных симптомов. В совокупности они называются синдромом отмены, абстиненцией. Появление абстинентных проявлений — свидетельство развития не только психологической, но физической формы пристрастия.
В совокупности они называются синдромом отмены, абстиненцией. Появление абстинентных проявлений — свидетельство развития не только психологической, но физической формы пристрастия.
Влияние курения на ЖКТ
Вместе с дымом в кровь попадает не только никотин, но и целый комплекс химических компонентов. По последним исследованиям ученых — до 7 тысяч. Каждый из них оседает в органах и тканях и оказывает на них неблагоприятное действие.
Самые распространенные:
- 69 канцерогенов — средства, дающих сильный толчок к образованию опухолей, в том числе — злокачественных;
- 250 компонентов, запускающих процесс прогрессии опухолей и их мутации;
- никотин — вещество, способствующее привыканию к указанному выше составу.
Среди продуктов горения — деготь, выделяемый угарный газ, ядовитый мышьяк, формальдегид, синильная кислота и другие элементы.
Люди добровольно дают доступ ядовитым веществам к своему организму.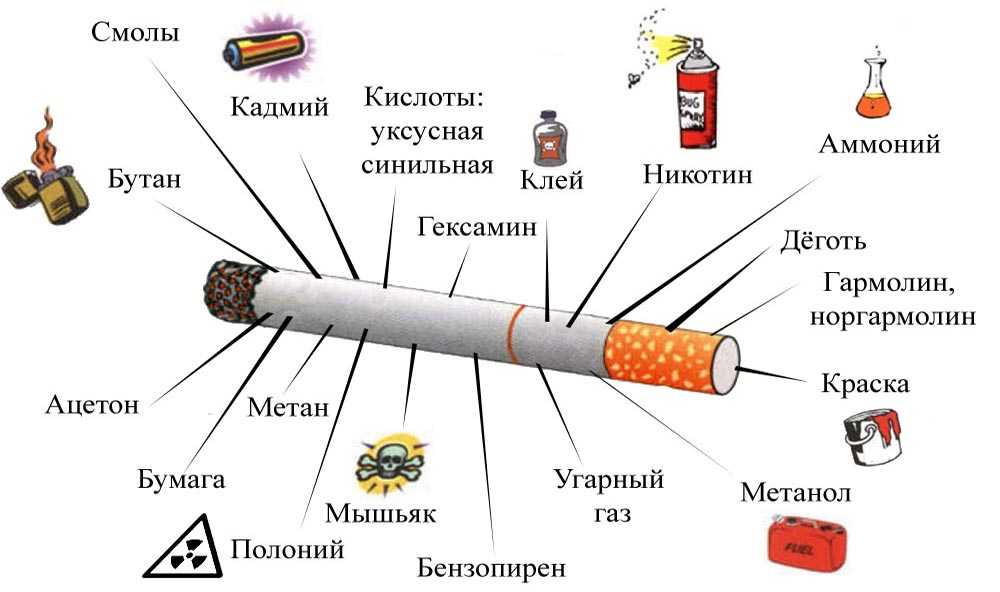 Первый удар приходится на кровеносную систему. Она доносит компоненты до сердца, сосудов, артерий, почек, печени. И, конечно, при курении поражается желудочно-кишечный трак, и так страдающий от некачественных пищевых продуктов, алкогольных напитков, курение и ЖКТ — сочетание, несущее угрозу не только нормальной жизнедеятельности, но и самой жизни.
Первый удар приходится на кровеносную систему. Она доносит компоненты до сердца, сосудов, артерий, почек, печени. И, конечно, при курении поражается желудочно-кишечный трак, и так страдающий от некачественных пищевых продуктов, алкогольных напитков, курение и ЖКТ — сочетание, несущее угрозу не только нормальной жизнедеятельности, но и самой жизни.
Ротовая полость
Температура дыма, поступающего внутрь около 50 градусов. Под горячим воздействием разрушается зубная эмаль, появляется налет, развивается кариес, страдают десны. При этом:
- нарушается деятельность желез, выделяющих слюну;
- повышается отделение мокроты;
- минимизируется чувствительность вкусовых рецепторов;
- нарушается обоняние;
- снижается аппетит.
Пищевод
Дым, поступая внутрь, негативно воздействует на всю зону пище. Снижается тонус нижней части, возникает почва для развития рефлюкса, неполного закрытия клапана. Что влечет за собой целый ряд негативных последствий:
- неприятный запах изо рта;
- изжога;
- боль в области грудины;
- тошнота;
- трудности прохождения пищи.

Как влияет курение на желудочную секрецию
Это одна из причин появления язвы желудка и 12-перстной кишки. Дым сигарет снижает выработку бикарбонатов, нейтрализующих соляную кислоту. Что в свою очередь поражает слизистый слой желудка. Суженные кровеносные сосуды не доносят к органам ЖКТ нужное количество крови, а вместе с ней — кислород и питательные вещества, Негативный процесс способствует застойным явлениям, образованию язв в основных органах пищеварения.
Лечение пациентов, которые даже после обнаружения проблем со здоровьем продолжают курить, значительно затягивается. Лекарства к проблемной области не доносятся в полной дозе. Часто повторяются рецидивы, вызывающие необходимость повторной терапии. У пациентов с затянувшейся зависимостью и выраженным злоупотреблением повторные язвы открываются уже через 3 месяца после окончания лечения. Смертность от указанных заболеваний среди людей из группы риска выше.
Отказаться от пагубной привычки никогда не поздно. Нужно лишь обратиться за консультацией к узким специалистам — наркологам и психологам.
Нужно лишь обратиться за консультацией к узким специалистам — наркологам и психологам.
Как курение влияет на перистальтику желудка
Сужение сосудов, отсутствие снабжения органов ЖКТ жизненно важными компонентами ведет к снижению перистальтики. Появляются:
- запоры или поносы;
- спазмы прямой кишки;
- затруднения кровообращения;
- геморрой.
Развивается язвенный колит, а также болезнь, сопровождающаяся сегментным поражением пищеварительного тракта.
Поджелудочная железа
На протяжении жизнедеятельности происходит нарушение секреции веществ, участвующих в переработке пищи. Табак способствует развитию атеросклероза в кровоснабжающих сосудах поджелудочной железы.
На фоне токсичного действия сохраняются воспалительные процессы, способствующие появлению сахарного диабета.
Как курение влияет на ЖКТ и печень
Дым от сигарет:
- осложняет уже имеющиеся заболевания;
- тормозит выработку противовоспалительных цитокинов;
- способствует разрушению органа в целом;
- параллельно активизирует ферменты, усиливающие токсичное действие лекарственных препаратов.

Нарушается механизм иммунного ответа, что отрицательно влияет на печень. При гепатитах и циррозе прекращают выполняться обеззараживающие функции, от чего страдает весь организм.
Токсины практически напрямую внедряются внутрь. Негативно воздействуют на нервную систему, вызывают тяжелые заболевания головного мозга.
Желчный пузырь
Говоря о том, что при курении поражается желудочно-кишечный тракт, необходимо отметить усиление воспалительных процессов, приводящих к застою желчи. Это неизменно влияет на показатель холестерина, а также способствует образованию камней в желчном пузыре.
Возможность выздоровления
Понятно, чем быстрее человек откажется от вредной привычки, тем скорее организм получит шанс на восстановление. После прекращения вредоносного воздействия запускаются внутренние процессы, способствующие общему оздоровлению. Включаются очищающие механизмы. И если болезни не запущены и не перешли на хронический или необратимый уровень, то вполне возможен обратный ход.
Обращение к специалистам
Больной и его родные на любом уровне заболевания, прежде всего, должны осознать сам факт существования проблемы. То есть — наличие болезни и существование зависимости. Нужно выяснить стадию болезни — психологическая или уже физическая.
Лечение подразумевает комплексный подход. На первом этапе чаще всего будет достаточно работы психолога. Один из методов — это гипноз. Для преодоления физической тяги используют:
- Иглотерапию, воздействующую на целевые акупунктурные точки. Это позволяет снизить тягу к употреблению.
- Лекарственную терапию — это пластыри, жевательные препараты, растворимые таблетки, спреи для полости рта.
- Лечение сопутствующих симптомов — головной боли, тошноты, бессонницы. Принимаются успокаивающие средства с целью снятия тревожности.
Лучше, если лечение проходит в спокойной психологической обстановке. Для снижения риска рецидива и прекращения негативного влияния курения на ЖКТ человеку нужно изменить прежние привычки, найти новые источники радости и уделить время устранению имеющихся патологий.
Бронхит курильщика — КГБУЗ Горбольница №12, г. Барнаул: статьи
Бронхит курильщика – это хроническое воспалительное заболевание слизистой оболочки бронхов, обусловленное систематическим повреждающим воздействием табачного дыма. Проявляется продуктивным кашлем, продолжающимся более 3 месяцев в течение одного года на протяжении не менее двух лет. Диагноз устанавливается на основании данных рентгенографии, КТ грудной клетки, лабораторных анализов, спирометрии, бронхоскопии. Назначается консервативное лечение муколитиками и отхаркивающими средствами. В период обострения применяются антибиотики и бронходилятаторы. Рекомендуется отказ от курения.
МКБ-10
Общие сведения
Бронхит курильщика является хронической патологией, развивается на фоне длительного интенсивного табакокурения. В англоязычных статьях по пульмонологии хронический бронхит позиционируется как одно из проявлений ХОБЛ. Заболевание встречается у 7% населения, 70-80% пациентов приобретают его в связи с курением табака. Удельный вес бронхита среди всех хронических болезней лёгких составляет 60-70%. Первые симптомы появляются в возрасте от 30 до 40 лет. Индекс курения у таких больных составляет приблизительно 10-15 пачка/лет. Мужчины заболевают в 2-4 раза чаще женщин. Продолжение курения на стадии необструктивного хронического бронхита часто приводит к формированию ХОБЛ.
Удельный вес бронхита среди всех хронических болезней лёгких составляет 60-70%. Первые симптомы появляются в возрасте от 30 до 40 лет. Индекс курения у таких больных составляет приблизительно 10-15 пачка/лет. Мужчины заболевают в 2-4 раза чаще женщин. Продолжение курения на стадии необструктивного хронического бронхита часто приводит к формированию ХОБЛ.
Причины
В качестве основной причины возникновения бронхита курильщика выступает вдыхаемый человеком табачный дым. Установлено, что эта субстанция содержит более 4 000 компонентов, оказывающих токсическое влияние на респираторную систему. Интенсивность повреждающего действия табачного дыма в отношении слизистой оболочки респираторного тракта зависит от глубины затяжки, количества выкуриваемых в сутки сигарет и стажа курения.
Хронический бронхит также диагностируется у лиц, вынужденных длительно находиться в прокуренных помещениях. Симптомы болезни у активных и пассивных курильщиков появляются приблизительно через 10-15 лет регулярного вдыхания табачного дыма, однако не все курящие одинаково подвержены развитию данной патологии. Дополнительные факторы риска, способствующие формированию воспалительного процесса в бронхах, делятся на:
Дополнительные факторы риска, способствующие формированию воспалительного процесса в бронхах, делятся на:
- Экзогенные. Наряду с курением повреждающее действие на бронхиальную стенку оказывают вредные условия труда. К ним относятся ингаляции растительной или металлической пыли, токсичных паров и сварочного аэрозоля. Неблагоприятные климатические условия (частые переохлаждения) также способствуют возникновению заболевания, развитию обострений.
- Эндогенные. Данному заболеванию больше подвержены пациенты с затруднением носового дыхания, возникающим из-за хронических заболеваний носа или его придаточных пазух, лица с нарушением функций иммунной системы. Существует наследственная предрасположенность к болезням органов дыхания. Бронхит курильщика нередко дебютирует на фоне симптомов острой респираторной инфекции, пневмонии.
Патогенез
Компоненты табачного дыма оказывают негативное действие на слизистую оболочку трахеобронхиального дерева, факторы местного иммунитета. Страдают клетки реснитчатого эпителия, гипертрофируются бронхиальные железы. Увеличивается продукция секрета, изменяются его реологические свойства – повышается вязкость. Повреждённый мерцательный эпителий не справляется с большим количеством густой мокроты, которая застаивается в бронхах, удаляется только с кашлем. Клетки мерцательного эпителия постепенно атрофируются.
Страдают клетки реснитчатого эпителия, гипертрофируются бронхиальные железы. Увеличивается продукция секрета, изменяются его реологические свойства – повышается вязкость. Повреждённый мерцательный эпителий не справляется с большим количеством густой мокроты, которая застаивается в бронхах, удаляется только с кашлем. Клетки мерцательного эпителия постепенно атрофируются.
Табачный дым губительно действует на нормальную микрофлору носоглотки. Верхние дыхательные пути колонизируются пневмококком, гемофильной палочкой и другими условно патогенными микроорганизмами. Попадая в бронхи, патогены прикрепляются к участкам слизистой с атрофированным эпителием. Снижение функций факторов локальной защиты приводит к дальнейшему распространению инфекции. Развивается ответная воспалительная реакция. Формируется тотальный эндобронхит. Происходит ремоделирование бронхов, появляется и становится необратимой бронхообструкция.
Симптомы бронхита курильщика
Заболевание развивается постепенно, медленно. Основный симптом болезни – кашель с мокротой появляется у пациентов с 10-15-летним стажем курения. На начальном этапе больные предъявляют жалобы на необходимость откашляться утром после сна. Кашель носит интермиттирующий характер, усиливается в период обострений, ослабевает или полностью исчезает во время ремиссии. Отходит светлая мокрота.
Основный симптом болезни – кашель с мокротой появляется у пациентов с 10-15-летним стажем курения. На начальном этапе больные предъявляют жалобы на необходимость откашляться утром после сна. Кашель носит интермиттирующий характер, усиливается в период обострений, ослабевает или полностью исчезает во время ремиссии. Отходит светлая мокрота.
Обострения болезни возникают на фоне переохлаждения, провоцируются респираторной инфекцией. Кроме кашля в этот период присутствуют симптомы общего недомогания, повышение температуры до субфебрильных или фебрильных значений. Иногда бронхит курильщика сопровождается бронхообструктивным синдромом, проявляющимся экспираторной одышкой. Признаки обструкции дыхательных путей на ранних стадиях болезни наблюдаются только во время обострения.
По мере прогрессирования болезни кашель становится постоянным, беспокоит больного в период ремиссии. Он может носить приступообразный характер, возникать в любое время суток. Изменяется цвет мокроты. Бронхиальное отделяемое приобретает коричневый оттенок, иногда наблюдается кровохарканье. При присоединении инфекции мокрота становится гнойной жёлто-зелёной. Появляется одышка при значительном физическом напряжении.
При присоединении инфекции мокрота становится гнойной жёлто-зелёной. Появляется одышка при значительном физическом напряжении.
Симптомы поздней стадии заболевания соответствуют клиническим проявлениям ХОБЛ. Прогрессирует одышка. Пациенты жалуются на затруднённый выдох, чувство нехватки воздуха при ходьбе, малейшей физической нагрузке. Мокрота откашливается с трудом. У больных с длительно персистирующим бронхитом курильщика появляются признаки дистальной гипертрофической остеоартропатии, к кашлю и одышке присоединяется тахикардия, нарушения сердечного ритма.
Осложнения
Бронхит курильщика прогрессирует медленно, в 90% случаев приводит к необратимой обструкции бронхов. Формируется ХОБЛ – самое часто встречающееся осложнение данного патологического процесса, заканчивающееся развитием хронического лёгочного сердца. Инфекционные обострения нередко сопровождаются возникновением бронхопневмонии с последующим образованием участков пневмофиброза, бронхоэктазов. Иногда наблюдаются эпизоды кровохарканья. В 20-30% случаев бронхит курильщика осложняется бронхогенным раком лёгкого.
В 20-30% случаев бронхит курильщика осложняется бронхогенным раком лёгкого.
Диагностика
Пациенты с подозрением на бронхит курильщика обследуются у терапевта и пульмонолога. При сборе анамнеза уточняется стаж курения, количество сигарет, выкуриваемых в течение суток, учитываются наследственность и профессиональные вредности. Осмотр пациентов с поздней стадией болезни выявляет цианоз кожных покровов, бочкообразную форму грудной клетки и деформации ногтевых фаланг пальцев по типу барабанных палочек.
Перкуторно определяется укорочение лёгочного звука. Аускультативные симптомы изменяются в зависимости от стадии патологического процесса. Выслушивается жёсткое или ослабленное дыхание, сухие свистящие и жужжащие, а также влажные хрипы. Простой (необструктивный) бронхит следует дифференцировать с ХОБЛ, необходимо исключить бронхиальную астму, туберкулёз и онкопатологию лёгких. Для уточнения диагноза и с целью дифференциальной диагностики назначаются:
- Лучевые методы исследования.
 В первые годы заболевания изменения на рентгенограмме лёгких могут отсутствовать. Позднее визуализируются рентгенологические признаки эмфиземы и пневмосклероза. КТ грудной полости выявляет бронхоэктазы, наличие интерстициальных изменений. В стадии ХОБЛ определяется саблевидная деформация трахеи.
В первые годы заболевания изменения на рентгенограмме лёгких могут отсутствовать. Позднее визуализируются рентгенологические признаки эмфиземы и пневмосклероза. КТ грудной полости выявляет бронхоэктазы, наличие интерстициальных изменений. В стадии ХОБЛ определяется саблевидная деформация трахеи. - Эндоскопическая диагностика.Фибробронхоскопия является одним из основных методов исследования. С её помощью обнаруживаются симптомы диффузного эндобронхита, бронхоэктазии, устанавливается степень воспаления бронхиальной стенки. При подозрении на неопластический процесс выполняется биопсия.
- Функциональные исследования. Анализ функции внешнего дыхания осуществляется с помощью спирометрии, бодиплетизмографии. Эти методики помогают подтвердить бронхиальную обструкцию, дифференцировать хронический бронхит с бронхиальной астмой. Оценивается обратимость, вариабельность обструкции. При необходимости производятся провокационные тесты. На ЭКГ определяются признаки перегрузки правых отделов сердца.

- Лабораторные анализы. Относятся к дополнительным методам диагностики. Воспалительные изменения со стороны периферической крови характерны для обострения процесса или наличия инфекционных осложнений. Посевы мокроты выявляют патогенные микроорганизмы, позволяют установить их чувствительность к антибактериальным препаратам.
Лечение бронхита курильщика
Лечение осуществляется преимущественно консервативными методами. Обязательным условием успешной терапии является полный отказ от табакокурения. Статистически установлено, что у пациентов, бросивших курить, замедляется или останавливается прогрессирование симптомов болезни. У больных в терминальной стадии ХОБЛ возможно хирургическое лечение – одно- или двусторонняя трансплантация лёгких или пересадка комплекса сердце-лёгкие.
Консервативная терапия
Объём терапевтических мероприятий зависит от стадии патологии, наличия осложнений. Назначаются патогенетические и этиотропные лекарственные препараты, реабилитационные процедуры. Лечение проводится как во время обострений, так и в состоянии ремиссии. На ранних этапах необходимо мотивировать больного бросить курить, санировать хронические очаги инфекции. Пациент обучается дыхательной гимнастике, занимается лечебной физкультурой. Фармакологическое лечение включает в себя следующие группы препаратов:
Лечение проводится как во время обострений, так и в состоянии ремиссии. На ранних этапах необходимо мотивировать больного бросить курить, санировать хронические очаги инфекции. Пациент обучается дыхательной гимнастике, занимается лечебной физкультурой. Фармакологическое лечение включает в себя следующие группы препаратов:
- Антибиотики. Применяются в качестве этиотропной терапии при инфекционном обострении бронхита. Предпочтительны антибактериальные препараты широкого спектра действия, эффективные в отношении пневмококка, гемофильной палочки и атипичных (внутриклеточных) микроорганизмов. Рекомендованы защищённые аминопенициллины, цефалоспорины 3 поколения, макролиды. При наличии анализа на чувствительность микрофлоры к антибиотикам учитываются его результаты.
- Бронходилататоры. Лечение бронхорасширяющими средствами назначается при появлении признаков бронхиальной обструкции при обострении патологии и в качестве базисной терапии на поздних стадиях бронхита.
 Препаратами первой линии являются антихолинергические средства в качестве монотерапии или в комбинации с бета-2-агонистами. Также можно использовать метилксантины.
Препаратами первой линии являются антихолинергические средства в качестве монотерапии или в комбинации с бета-2-агонистами. Также можно использовать метилксантины. - Кортикостероиды. Лечение ингаляционными кортикостероидами дополняет базисную терапию антихолинергическими препаратами при низкой эффективности последних. Показанием для коротких курсов системных глюкокортикостероидных гормонов являются выраженные симптомы бронхоконстрикции на фоне обострений.
- Мукорегуляторы. Мукорегулирующие средства применяются как патогенетическое лечение, показаны на любом этапе развития бронхита курильщика. К препаратам выбора относятся лекарственные средства группы амброксола, ацетилцистеин и карбоцистеин. Не исключается использование фитосборов.
Хирургическое лечение
Трансплантация лёгких как оперативное лечение последней стадии ХОБЛ, к которой в конечном итоге приводит бронхит курильщика, относится к экспериментальным методам, осуществляется крайне редко. Временной интервал, в течение которого следует выполнить вмешательство, очень трудно определить. Сроки выживаемости после ранней трансплантации лёгких ниже, чем продолжительность жизни при естественном течении патологии. Из-за применения иммунодепрессантов в послеоперационном периоде у курильщика существенно увеличивается риск возникновения лёгочной карциномы.
Временной интервал, в течение которого следует выполнить вмешательство, очень трудно определить. Сроки выживаемости после ранней трансплантации лёгких ниже, чем продолжительность жизни при естественном течении патологии. Из-за применения иммунодепрессантов в послеоперационном периоде у курильщика существенно увеличивается риск возникновения лёгочной карциномы.
Прогноз и профилактика
Бронхит курильщика отличается относительно благоприятным течением. Обычно симптомы заболевания прогрессируют в течение нескольких десятков лет. Исключение вредного воздействия табачного дыма на органы дыхания значительно улучшает прогноз. Продолжение курения, несвоевременно начатое лечение становятся причиной формирования лёгочно-сердечной недостаточности, инвалидизации и гибели больного. Превентивные меры сводятся к отказу от табакокурения. К вторичной профилактике наряду с обязательным прекращением курения относятся реабилитационные мероприятия, сезонная вакцинация против респираторных инфекций.
1. Влияние курения на течение хронической обструктивной болезни легких: Автореферат диссертации/ Ракита Д.Д. — 2004.
4. Особенности микробиоты дыхательных путей у курящих пациентов: факторы-предикторы формирования резистентной микрофлоры/ Фролова А.К., Карамова Ф.А., Шоломов И.Ф.// Consilium Medicum – 2015 — №11.
Курение приобрело вид табачной эпидемии как во всем мире, так и в нашей стране. По статистике 60,7% мужчин и 21,7% женщин в России являются курильщиками, причем треть из них моложе 25 лет. О вреде курения знают все, но мало кто задумывается – опасно ли пассивное курение?
Пассивное курение – это состояние, когда некурящий человек вынужден вдыхать воздух с продуктами горения табака от сигарет курильщика.
Медико-социальные исследования, проведенные в последние годы, доказали, что вредное влияние на здоровье курение оказывает не только на самих курильщиков, но и на людей, которые находятся рядом.
Состав сигаретного дыма
В химическом составе табачного дыма обнаружено несколько тысяч вредных компонентов, которые оказывают на организм токсическое, канцерогенное и мутагенное действие.
Основные составляющие сигаретного дыма:
- угарный газ или окись углерода;
- смола;
- никотин;
- нафтален;
- фенол, крезол;
- N-нитрозамины;
- ароматические углеводороды;
- аргон;
- мышьяк;
- метан;
- оксид азота;
- синильная кислота;
- аммиак;
- сероводород;
- пирены, альдегиды;
- алкоголи;
- неорганические соединения: свинец, кадмий, никель.
К самым опасным веществам относят:
- Алкалоид никотин – сильнодействующий универсальный яд, разрушающий все органы и ткани организма.
- Синильная кислота (цианистый водород) – яд, поражающий дыхательную систему.
- Мышьяк – токсическое вещество, используемое в быту для отравления грызунов.
- Полоний – радиоактивное вещество, при накапливании в организме оказывает канцерогенное действие.
- Никель – металл, ядовит, приводит к астме, действуя на почки, провоцирует развитие злокачественных опухолей.

- Смола – органический минерал, поражает ткани легкого, вызывая рак.
При сгорании табака образуются 3 потока дыма:
- Основной вырабатывается во время затяжки дыма, вдыхается курильщиком.
- Боковой – это дым, который выделяется из тлеющей сигареты между затяжками.
- Дым, выдыхаемый курящим человеком.
90% основного потока составляют 350-500 газообразных компонентов, особенно опасными из них считаются окись и двуокись углерода. Остальная часть представлена твердыми микрочастицами с различными токсическими включениями.
При пассивном курении происходит вдыхание воздуха, смешанного с боковым табачным потоком и с дымом, выдыхаемым курильщиком.
Вред пассивного курения
Находясь в одном помещении с активным курильщиком в течение часа, некурящий человек вдыхает порцию табачного дыма, которая равноценна выкуриванию половины сигареты.
Вредное воздействие пассивного вдыхания табачного дыма условно делят на 2 группы.
Немедленное действие – то, что человек ощущает сразу после пребывания в прокуренном помещении:
- Раздражение слизистых носоглотки, бронхов, глаз: першение в горле, кашель, слезотечение.

- Сухость во рту.
- Воздействие табачных токсинов на центральную нервную систему: головная боль, головокружение, тошнота.
- Расстройство работы сердечно-сосудистой системы с симптомами гипоксии: учащение пульса, появление одышки, подъем артериального давления из-за снижения содержания кислорода во вдыхаемом воздухе.
- Аллергические реакции на компоненты табачного дыма.
Отсроченные, которые развиваются через продолжительное время:
- Патологии бронхолегочной системы: астма, бронхиты, эмфизема легких.
- Хронические болезни уха, горла, носа.
- Заболевания сердца и сосудов: ранний атеросклероз, ишемические расстройства, нарушения сердечного ритма, гипертония.
- Аллергические болезни.
- У детей – задержка психомоторного развития.
- Повышенный риск возникновения злокачественных новообразований.
- Высокий процент инвалидности и смерти.
По данным американских исследователей отсроченный результата пассивного курения вызывает 46 тысяч летальных исходов в год, причем 14 тысяч смертей приходится на онкологию, а 32 тысячи на заболевания сердца и сосудов.
Влияние пассивного курения на органы дыхания
Постоянное раздражение слизистой дыхательных путей табачным дымом ведет к формированию хронических ринитов, фарингитов, бронхитов. Бронхиальная астма развивается при пассивном курении в 5 раз чаще, чем у людей, огражденных от действия табачного дыма.
Проблемы с носовым дыханием вызывают воспаление евстахиевой трубы, соединяющей ротовую полость с ухом. В результате наблюдаются частые средние отиты, снижение слуха.
Радиоактивные изотопы табачного дыма, признанные сильнейшими канцерогенами, попадая в ткани легкого, вызывают метаплазию альвеолярных клеток с образованием злокачественных опухолей.
Центральная нервная система
Помимо алкалоида никотина, который оказывает нейротоксическое действие, в табачном дыме содержится много других ядовитых и токсических веществ (окись углерода, фенол, аммиак), которые повреждают различные структуры головного мозга.
Результатами воздействиями становятся:
- Психоэмоциональные нарушения, быстрая смена настроения: возбуждение, апатия
- Расстройство сна: бессонница, дневная сонливость.

- Изменение вкусовых ощущений.
- Потеря аппетита, тошнота.
- Головные боли, головокружения.
- Слабость, повышенная утомляемость.
- Снижение функций мозга: рассеянность, забывчивость, ухудшение памяти.
Сердце, сосуды
Под влиянием токсических веществ табачного дыма развивается выраженное нарушение функции сердечно-сосудистой системы. Это способствует развитию раннего атеросклероза, стенокардии, гипертонии, что в конечном итоге провоцирует инфаркты и инсульты.
Окись углерода, образующийся при сгорании табака, поступая в кровь, снижает способность эритроцитов к доставке кислорода клеткам организма, приводит к тромбообразованию. Закупоривание артерий тромбами вызывает поражение сердца (инфаркт) и нарушение кровообращения в нижних конечностях (облитерирующий эндартериит).
При уже имеющихся сердечно-сосудистых заболеваниях даже кратковременное воздействие табачного дыма может привести к тяжелым приступам стенокардии.
Органы зрения
Компоненты табачного дыма раздражают и сушат слизистую глаз, сужают сосуды, что ведет к нарушению трофики роговицы. Помимо частых конъюнктивитов, длительное пребывание в задымленном помещении вызывает снижение остроты зрения.
Помимо частых конъюнктивитов, длительное пребывание в задымленном помещении вызывает снижение остроты зрения.
Репродуктивная система
Пассивное курение оказывает негативное влияние на репродуктивную систему как мужчин, так и женщин. У жен курящих мужчин чаще развивается синдром истощенных яичников, что значительно снижает их способность к зачатию. У 40–50% женщин, вынужденных дышать токсичными продуктами горения табака, во время беременности возникают те или иные проблемы.
У мужчин компоненты табачного дыма подавляют активность сперматозоидов, что может являться причиной бесплодия.
Влияние пассивного курения на детей
Одним из доказательств вредного влияние на детей пассивного курения служит тот факт, что в семьях, где курит один или оба родителя, в несколько раз увеличивается заболеваемость ребенка респираторными заболеваниями, бронхитами, пневмониями. Компоненты дыма проникают в грудное молоко кормящей матери, то есть происходит постепенное отравление ребенка, следствием которого является угнетение или возбуждение ЦНС: ребенок заторможен, вялый, много спит, либо, наоборот, кричит, плачет, плохо ест, срыгивает, не прибавляет в весе.
Формирование минимальных мозговых дисфункций, которые проявляются задержкой речевого развития и мелкой моторики, что в дальнейшем вызывает проблемы с усвоением учебного материала, плохую адаптацию в коллективе, особенности поведения в школе. Повышается склонность к аллергическим заболеваниям: атопический дерматит, бронхиальная астма.
Отдаленные последствия никотиновой интоксикации ребенка: повышенный риск развития сахарного диабета, ожирения, аутизма, сердечно-сосудистых заболеваний, гипертонии.
Так как детский организм находится в стадии активного роста и развития, его клетки более подвержены мутациям из-за действия табачных токсинов.
Влияние пассивного курения на беременных женщин
Негативное влияние на беременных женщин, которое оказывает пассивное курение, трудно переоценить.
Никотин оказывает сосудосуживающее действие на сосуды матки и плаценты.
Снижается усвоение организмом витаминов С, В, фолиевой кислоты, которые необходимы для нормального роста и развития плода.
Происходит ослабление иммунитета, который у беременной и так подавлен, чтобы организм не отторгнул зародыш, который наполовину состоит из чужого (отцовского) генетического материала. Это вызывает повышенную заболеваемость беременной острыми инфекциями обостряет течение хронических патологий.
Компоненты табачного дыма обладают мутагенным действием на яйцеклетки, что может вызвать генетические дефекты у потомства.
Часто на фоне табачной интоксикации плацента располагается аномально (предлежание плаценты) в нижней части матки у внутреннего маточного зева. Женщина в таком случае не сможет родить естественным путем, так как плацента механически перекрывает выход из матки.
Преждевременная отслойка плаценты – осложнение, когда в результате повреждения сосудов отделение плаценты происходит до момента рождения плода. Нахождение плода в матке препятствует сокращению мышечного слоя, поэтому сосуды в зоне отслойки плаценты кровоточат, развивается внутриматочное кровотечение, угрожающее жизни матери и плода.
Патология, развивающиеся у плода, под воздействием табачного дыма:
- Плацентарная недостаточность, из-за которой плод получает мало питательных веществ и кислорода. В результате возможны самопроизвольные выкидыши, преждевременные роды, рождение ребенка в состоянии гипоксии и с малым весом.
- Синдром задержки развития плода. У детей отмечается гипотрофия при доношенной беременности (масса тела менее 2500 г), неврологические отклонения, склонность к инфекционным заболеваниям, отставание в физическом и психическом развитии.
- Увеличивается риск врожденных аномалий плода.
- Высокая вероятность развития синдрома внезапной детской смертности.
Какое курение опаснее: пассивное или активное
Вопрос о том, что вреднее: пассивное или активное курение еще находится на стадии изучения.
У курильщика уже развиты механизмы адаптации к компонентам дыма и никотину, а вред пассивного курения у человека, не имеющего этой привычки, выражен сильнее, так как у него организм более болезненно реагирует на токсичный дым.
Вредные компоненты дыма, оседающие и накапливающиеся на волосах, одежде, мебели, предметах обстановки, постепенно отравляют организм человека.
Как избежать пассивного курения
Курильщики в угоду пагубной привычки сами выбирают путь хронической интоксикации организма, но почему окружающие должны подвергаться вместе с ними опасным последствиям для здоровья и жизни?
Самый радикальный способ решения вопроса пассивного курения – это полный отказ от курения. Но в силу различных причин не каждый человек способен бросить курить, поэтому разработаны меры по ограничению вредного воздействия табачного дыма.
Если курят дома
В квартире местом курения обычно является кухня или туалетная комната. Для снижения задымления этих помещений следует установить дополнительные вентиляционные устройства: на кухонную вытяжку и в отверстие воздуховода в туалете.
Необходимо часто проветривать квартиру и проводить влажную уборку.
Если курят на работе
Курить в рабочих помещениях категорически запрещено. Администрация обязана выделить курящим сотрудникам специальное помещение, оборудованное мощной вентиляционной установкой и поглотителями табачного дыма.
Администрация обязана выделить курящим сотрудникам специальное помещение, оборудованное мощной вентиляционной установкой и поглотителями табачного дыма.
Если курят в общественных местах
В общественных местах: учебных заведениях, медицинских организациях, кафе, гостиницах и других учреждениях наложен запрет на курение. В случае нарушения необходимо требовать от администрации заведений соблюдения Федерального закона «Об охране здоровья граждан от воздействия окружающего табачного дыма и последствий потребления табака».
В исследованиях, проведенных во многих странах мира о влиянии пассивного курения на здоровье человека доказано, что некурящие, живущие или работающие вместе с курильщиками, имеют высокий риск развития патологических процессов в организме, как и при активном табакокурении.
Во второй половине ноября отмечается Всемирный день борьбы с ХОБЛ (хроническая обструктивная болезнь легких). Зачастую люди узнают об этом заболевании только тогда, когда кашель, затруднение дыхания и хрипы в легких становятся нестерпимыми. Ирина Павловна Белоглазова, врач-пульмонолог, руководитель 4-ого терапевтического отделения ГКБ № 52, рассказывает, чем опасна ХОБЛ, как она возникает, почему ее нельзя не лечить. Врач подчеркивает: курение — основной фактор риска развития ХОБЛ. Знание о последствиях коварной болезни, возможно, кому-то поможет избавиться от вредной привычки.
Ирина Павловна Белоглазова, врач-пульмонолог, руководитель 4-ого терапевтического отделения ГКБ № 52, рассказывает, чем опасна ХОБЛ, как она возникает, почему ее нельзя не лечить. Врач подчеркивает: курение — основной фактор риска развития ХОБЛ. Знание о последствиях коварной болезни, возможно, кому-то поможет избавиться от вредной привычки.
Аббревиатуру ХОБЛ в последнее время приходится слышать все чаще. Однако мы мало знаем об этой болезни.
Хроническая обструктивная болезнь легких (ХОБЛ) была выделена в качестве отдельного заболевания только в самом конце ХХ века. Проявления ХОБЛ и бронхиальной астмы похожи, но природа заболеваний разная. Сейчас мы больше знаем о специфике ХОБЛ и используем специальные методы для ее диагностики и лечения. Понимание особенностей развития болезни помогает врачу отслеживать состояние пациента. Наблюдение специалиста важно — ХОБЛ может привести к очень тяжелым последствиям.
Чем опасна ХОБЛ? Как она возникает?
Слово «обструкция» обозначает помеху, преграду. И при бронхиальной астме, и при ХОБЛ происходит сужение просвета бронхов, то препятствует нормальному прохождению воздуха в легкие. В результате возникает одышка, кашель, затрудненное дыхание, хрипы, удушье. При астме сужение бронхов — иммунный ответ организма на попавший в бронхи раздражитель-аллерген. Потом (например, после того, как человек подышал ингалятором), просвет бронха снова расширяется, и неприятные симптомы исчезают. Астма — хорошо контролируемое заболевание при разумном поведении пациента. Иная ситуация при ХОБЛ.
И при бронхиальной астме, и при ХОБЛ происходит сужение просвета бронхов, то препятствует нормальному прохождению воздуха в легкие. В результате возникает одышка, кашель, затрудненное дыхание, хрипы, удушье. При астме сужение бронхов — иммунный ответ организма на попавший в бронхи раздражитель-аллерген. Потом (например, после того, как человек подышал ингалятором), просвет бронха снова расширяется, и неприятные симптомы исчезают. Астма — хорошо контролируемое заболевание при разумном поведении пациента. Иная ситуация при ХОБЛ.
Если посмотреть на бронх в электронном микроскопе, можно увидеть эпителий (слизистую оболочку) с ворсинками, которые движутся, выгоняя всё ненужное наружу и очищая легкие. Если ворсинки повреждаются, очищение не происходит или происходит недостаточно. Потом повреждается и сама стенка бронхов, становится толстой и жесткой. Сужение бронхов при ХОБЛ в отличие от астмы — необратимый процесс.
ХОБЛ — очень коварная болезнь. Большинству астматиков, если они следят за собой, с возрастом не грозит дыхательная недостаточность. При ХОБЛ процесс повреждения бронхов и легких продолжается. Когда воздух проходит точку, где бронх уже сужен, возможен экспираторный коллапс: воздух не может полностью выйти из легких. В результате лёгочная ткань растягивается, теряет эластичность, начинает постепенно разрушаться, что сопровождается возникновением булл (воздушных пузырьков) и развитием эмфиземы. Легкие пациента оказываются перераздутыми. Это не только препятствует нормальному дыханию, но и способствует развитию патологических процессов в органах дыхательной и других систем, поскольку все в организме взаимосвязано.
При ХОБЛ процесс повреждения бронхов и легких продолжается. Когда воздух проходит точку, где бронх уже сужен, возможен экспираторный коллапс: воздух не может полностью выйти из легких. В результате лёгочная ткань растягивается, теряет эластичность, начинает постепенно разрушаться, что сопровождается возникновением булл (воздушных пузырьков) и развитием эмфиземы. Легкие пациента оказываются перераздутыми. Это не только препятствует нормальному дыханию, но и способствует развитию патологических процессов в органах дыхательной и других систем, поскольку все в организме взаимосвязано.
Каковы причины заболевания?
Основной причиной возникновения ХОБЛ является курение. Воздействие продуктов горения на бронхиальную стенку приводит к ее изменениям. Вероятность возникновения ХОБЛ у курильщика крайне высока. Тем, кто курит и не боится онкологических заболеваний, точно стоит бояться ХОБЛ. Исследования показывают, что смертность от дыхательной недостаточности в результате рака легких — примерно 20%, по причине ХОБЛ — более 23%.
Если пациент не курит, врач, скорее заподозрит другую болезнь. Однако фактором риска для ХОБЛ является и частое пребывание в зоне сжигания биосырья. Повышенная вероятность заболеть есть у поваров, у людей, которые живут или проводят много времени в домах с печным отоплением, там, где продукты сгорания могут попадать в воздух жилого помещения.
Почему надо обращаться к врачу? Многие пациенты с ХОБЛ этого не делают.
Возможно, люди не знают симптомы, на которые стоит обратить внимание. Кто-то боится, что доктор скажет не самые приятные вещи. Первым делом, предложит бросить курить. Узнать, что болезнь неизлечима — тоже невесело. Однако врач, во-первых, правильно диагностирует заболевание. Не все обструктивные нарушения являются проявлениями ХОБЛ или астмы, причиной может быть и онкологическое заболевание, и вирусная инфекция. Во-вторых, врач назначит лечение, которое затормозит прогрессирование ХОБЛ и те страшные последствия, с которыми люди попадают в стационар.
В каких случаях пациенты с ХОБЛ попадают в стационар?
Курильщикам было бы полезно посмотреть на больных с ХОБЛ, вынужденных жить с кислородной подушкой «в обнимку». В больницы попадают люди с инфекционными обострениями, с температурой, кашлем, с гнойной мокротой, усилением одышки, приступами удушья. Со временем болезнь переходит в стадию, когда справиться с ней дома своими силами уже не удается. Мы пытаемся пациентов убедить, объясняем, что будет просто нечем дышать, будут ощущения как у рыбы, выброшенной на берег. Инсультом и инфарктом напугать можно, многие, узнав, что угроза серьезна, бросают курить. ХОБЛ боятся меньше, а зря!
В больницы попадают люди с инфекционными обострениями, с температурой, кашлем, с гнойной мокротой, усилением одышки, приступами удушья. Со временем болезнь переходит в стадию, когда справиться с ней дома своими силами уже не удается. Мы пытаемся пациентов убедить, объясняем, что будет просто нечем дышать, будут ощущения как у рыбы, выброшенной на берег. Инсультом и инфарктом напугать можно, многие, узнав, что угроза серьезна, бросают курить. ХОБЛ боятся меньше, а зря!
Каковы первые признаки заболевания? Когда надо обращаться к врачу и как диагностируется ХОБЛ?
Первый признак заболевания — одышка, которая возникает сначала при интенсивной, а затем и при обычной физической нагрузке. С развитием болезни одышка беспокоит уже и в покое. Затем появляются признаки кислородной недостаточности — синеют руки, губы, иногда меняется даже внешний вид ногтей и пальцев. Может появится свист и жужжание в легких.
Люди с одышкой далеко не всегда осознают и признают, что у них есть дыхательные проблемы — вроде бы нормально себя чувствуют, надо работать, не хочется болеть. Врачу часто удается понять, что проблемы есть, только путем наводящих вопросов. Однако если человек курит больше 20 лет, и него есть одышка, ХОБЛ весьма вероятна. Всем курящим людям в возрасте после 40 лет (учитывая, что курить начинают примерно в 20 лет) необходимо делать спирометрию — измерение показателей дыхания. Один из параметров, вычисляемых при спирометрии — индекс Тиффно — указывает на возможное наличие необратимой обструкции бронхов. Обструкция может быть вызвана разными причинами, и иногда мы просим пациента прийти на повторный текст через год. Однако, если индекс Тиффно менее 70%, есть одышка и пациент курит, диагноз ХОБЛ не вызывает сомнений. Тогда на основании остальных показателей спирометрии мы обсуждаем выбор ингаляторов для постоянного приёма.
Врачу часто удается понять, что проблемы есть, только путем наводящих вопросов. Однако если человек курит больше 20 лет, и него есть одышка, ХОБЛ весьма вероятна. Всем курящим людям в возрасте после 40 лет (учитывая, что курить начинают примерно в 20 лет) необходимо делать спирометрию — измерение показателей дыхания. Один из параметров, вычисляемых при спирометрии — индекс Тиффно — указывает на возможное наличие необратимой обструкции бронхов. Обструкция может быть вызвана разными причинами, и иногда мы просим пациента прийти на повторный текст через год. Однако, если индекс Тиффно менее 70%, есть одышка и пациент курит, диагноз ХОБЛ не вызывает сомнений. Тогда на основании остальных показателей спирометрии мы обсуждаем выбор ингаляторов для постоянного приёма.
Как лечить ХОБЛ?
Как я уже сказала, полностью остановить процесс нельзя, но можно его существенно замедлить. Делать это надо обязательно, не теша себя примерами знакомых, которые всю жизнь курили и «дожили до 100 лет». У каждого своя генетика, у кого-то процесс идет медленнее, а у кого-то очень быстро и приводит к необходимости постоянной кислородотерапии.
У каждого своя генетика, у кого-то процесс идет медленнее, а у кого-то очень быстро и приводит к необходимости постоянной кислородотерапии.
Основной метод терапии при ХОБЛ, так же как при астме — ингаляторы. Ни капельницы, ни таблетки, а ингаляторы. Их должен подобрать врач. Но если у больных астмой эффект от использования ингалятора чувствуется практически сразу, то с ХОБЛ это не так. Пациентам надо понимать, что даже если принципиальных изменений нет, применять ингаляторы надо все равно, это поможет отсрочить кислородотерапию, избежать осложнений и снизить риск обострений заболевания.
Если бросить курить — это поможет?
ХОБЛ в среднем развивается после 20 лет курения. Если бросить курить раньше, заболевания можно избежать. Если бросить курить при первых признаках заболевания, изменения можно замедлить. Если ХОБЛ диагностирована, отказаться от вредной привычки надо обязательно!
По данным ВОЗ, от заболеваний, связанных с курением, в мире ежегодно умирают 5 миллионов человек. Если рост потребления табачных изделий будет продолжаться такими темпами, то уже к 2030 году курение станет одной из главных причин смертей во всем мире.
Если рост потребления табачных изделий будет продолжаться такими темпами, то уже к 2030 году курение станет одной из главных причин смертей во всем мире.
Учитывая тяжелые последствия, которые вызывает пристрастие к табаку, многие страны на законодательном уровне разработали и приняли программы об охране здоровья граждан, предусматривающие ограничение курения в общественных местах. Это относится не только к обычным сигаретам, но и к электронным, а также к системам нагревания табака: IQOS (айкос) и GLO (гло).
Последствия курения сигарет
При сгорании табака образуется более 4 тысяч опасных химических соединений, которые и становятся виновниками патологических процессов, запускаемых в организме.
Вместе с табачным дымом в организм попадают:
- Смолы – мельчайшая взвесь твердых частиц оседает в тканях легких. Большинство относятся к канцерогенам.
- Мышьяк – провоцирует развитие раковых опухолей и заболевания сердца и сосудов.
- Бензол – химическое соединение с выраженным токсическим действием.
 Вызывает лейкозы и другие формы онкологии.
Вызывает лейкозы и другие формы онкологии. - Полоний – обладает радиоактивным действием.
- Формальдегид – провоцирует заболевания дыхательных путей и легких.
Множество других высокотоксичных веществ табачного дыма через кровеносную систему разносятся по организму и наносят серьезный вред внутренним органам.
Алкалоидом, входящим в состав табака и вызывающим у человека физическую и психическую зависимость, является никотин.
Негативные последствия утяжеляются день ото дня, а вред курения отражается на всех органах и тканях курящего человека.
Периферическая и центральная нервная система
- Расстройство функций высшей нервной деятельности, проявляющееся в снижении памяти, работоспособности, головокружении, эпилептических припадках.
- При воспалении корешков спинномозговых нервов: радикулиты, невриты, парестезии (покалывание, онемение).
- Поражение вкусового анализатора приводит к потере вкусового восприятия пищи.
- Нарушение зрения.

- Снижение слуха.
- Повышенный риск инсультов из-за тромбозов или разрывов артерий, кровоснабжающих мозг.
Сердечно-сосудистая система
Так как окись углерода табачного дыма блокирует гемоглобин крови, нарушается транспортировка кислорода к миокарду. Сердце вынуждено усиленно сокращаться, это приводит к гипертрофии желудочков, повышению артериального давления, тахикардии, нарушениям сердечного ритма.
Кроме того, при курении расстраивается жировой обмен, повышается уровень холестерина в крови. Это ведет к отложению атеросклеротических бляшек на стенках сосудов. Вероятность развития инфарктов у курящих в 4-5 раз выше, чем у тех, кто не курит.
Дыхательные пути и легкие
Длительное курение вызывает хронические обструктивные заболевания респираторного тракта и легких: бронхит, легочную эмфизему, обструктивную болезнь легких.
К самым страшным последствиям курения относят рак легких, причем вероятность развития заболевания находится в прямой зависимости от стажа курения и количеством сигарет. Так, при курении более 20 лет по 1-2 пачки в день риск заболеть раком легких увеличивается на 70% по сравнению с некурящими.
Так, при курении более 20 лет по 1-2 пачки в день риск заболеть раком легких увеличивается на 70% по сравнению с некурящими.
Желудочно-кишечный тракт
Снижается секреция слюнных желез, слизистая ротовой полости становится сухой. Так как слюна выполняет защитную роль, то ее недостаток приводит к ряду патологий: кариесу, воспалению десен, пародонтозу. За счет канцерогенного влияния табачных смол во рту могут развиваться раковые образования.
Стимуляция никотином обкладочных клеток желудка приводит к гиперпродукции соляной кислоты, что приводит к разъеданию защитного слоя слизистой и образованию эрозий и язв. Длительно незаживающие язвы способны трансформироваться в раковые опухоли.
Недостаточность мышечного сфинктера в нижней части пищевода вызывает формирование гастроэзофагеального рефлюкса, который характеризуется забросом желудочного содержимого в пищевод. Клетки слизистой часто перерождаются в злокачественные, приводя к раку пищевода.
Мочевой пузырь
После 40 лет у курильщиков увеличивается риск заболеть раком мочевого пузыря, причем у мужчин он развивается в 4 раза чаще, чем у женщин.
Кожные покровы
Во время курения на кожу, особенно лица, оказывают неблагоприятное воздействие сразу несколько факторов: горячий дым, смолы, никотин. Все это нарушает нормальный процесс дыхания кожи, вызывает спазм сосудов, разрушает коллагеновые волокна. Кожа теряет тургор, появляется много морщин, цвет приобретает сероватый или желтоватый оттенок.
Костная ткань и конечности
Курение служит причиной остеопороза – уменьшения плотности костной ткани, что увеличивает риск переломов.
Для курящих характерно поражение мелких сосудов нижних конечностей – облитерирующий эндартериит. Это заболевание приводит к омертвению тканей, лишенных питания – гангрене с последующей ампутацией конечности.
Все эти негативные последствия присущи как мужчинам, так и женщинам. Но есть и такие последствия, которые разные в зависимости от пола.
Последствия у мужчин
Никотин, являясь нервным ядом, разрушает зоны мозга, отвечающие за половое поведение человека и его способность к воспроизведению потомства. С увеличением лет курения последствия становятся более выраженными: с возрастом вероятность иметь здоровое потомство значительно уменьшается.
С увеличением лет курения последствия становятся более выраженными: с возрастом вероятность иметь здоровое потомство значительно уменьшается.
У мужчин последствиями курения на половую систему являются:
- Ухудшение кровоснабжения детородных органов.
- Сниженная секреция половых гормонов.
- Плохое качество спермы.
- Эректильная дисфункция.
- Ослабление либидо.
По статистике, более 10% эректильной дисфункции у мужчин связано с курением. Уровень мужского фактора в бесплодии у курящих молодых мужчин в 2 раза превышает показатель у некурящих.
Последствия для женщины
Вред, наносимый курением, женщине намного сильнее, чем мужчине. Длительный спазм сосудов под влиянием никотина порождает расстройство кровоснабжения органов внутренней секреции, которые вырабатывают женские половые гормоны. Дисбаланс гормонов вызывает:
- Расстройство менструальной функции.
- Бесплодие.
- Невынашивание беременности: самопроизвольные выкидыши, преждевременные роды.

- Ранний климакс.
- Преждевременное старение, потеря женственности.
- Отсутствие либидо.
У женщин, зависимых от табака, количество зачатых и выношенных детей составляет 72% по сравнению с некурящими. Дети у них рождаются недоношенными, с маленьким весом, чаще подвержены риску погибнуть от синдрома внезапной детской смерти.
Американские ученые подсчитали, что пачка сигарет, выкуриваемая беременной женщиной в течение дня, увеличивает риск смерти плода на 20%.
Под воздействием токсичных компонентов табачного дыма происходят разрывы в молекуле ДНК, в половых клетках появляются дефектные гены. При передаче потомству мутированных генов развиваются различные аномалии развития плода, вплоть до уродств.
Это относится к половым клеткам и мужчин, и женщин.
Компоненты табака обнаруживаются даже в цервикальной слизи (на шейке матки) курящей женщины, что является провоцирующим фактором развития злокачественных опухолей половых органов.
Последствия для детей
Одним из коварных свойств табака является то, что он наносит вред не только тем, кто сам курит, но и тем, кто вынужден пассивно вдыхать дым, находясь рядом с курящим.
При проведении эпидемиологических исследований было доказано, что частота заболеваемости у детей напрямую зависит о того, в какой семье воспитывается ребенок. Если в семье есть курящие, – это значительно увеличивает процент детей, страдающих частыми простудными заболеваниями, бронхиальной астмой, бронхитами, пневмониями, гастритами и многими другими патологиями.
Особенно опасно, когда ребенок подвергается воздействию табака еще внутриутробно. В основном поражается нервная система: снижается интеллектуальный потенциал, нарушается развитие зон мозга, отвечающих за речь и слух.
Такие дети отстают в физическом и психическом развитии от сверстников, не умеют руководить эмоциями, хуже овладевают школьной программой, у них имеются проблемы с поведением и социальной адаптацией в обществе.
Последствия курения IQOS (айкос), травы, вейпа
Система нагревания табака IQOS (айкос) в электронных сигаретах представляет такую же опасность, как курение обычного табака. Система IQOS также является поставщиком в организм никотина, который является сильнейшим нейротоксином и наркотиком.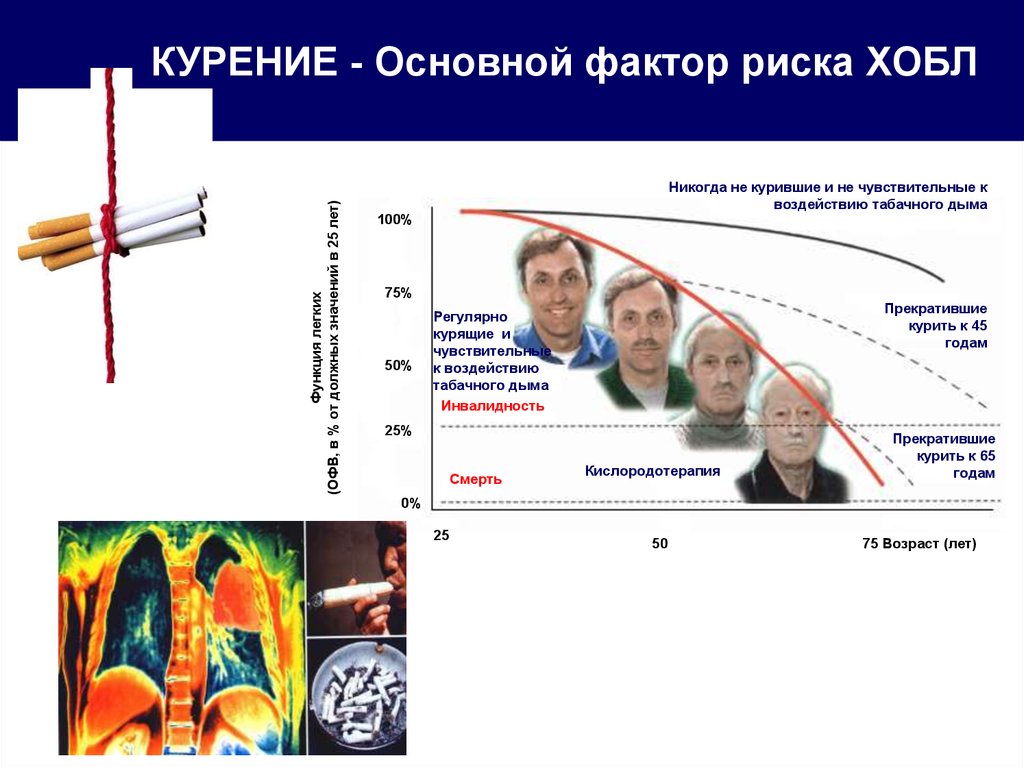 Система позиционировалась как альтернатива табакокурению, якобы она безвредна, так как из нее убрали смолы и некоторые другие токсичные вещества.
Система позиционировалась как альтернатива табакокурению, якобы она безвредна, так как из нее убрали смолы и некоторые другие токсичные вещества.
Медики пришли к выводу, что айкос не только не снимает никотиновой зависимости, но и приводит к ряду серьезных осложнений: дерматиту, болезням горла, головокружению, тахикардии.
Иллюзия безопасности ведет к тому, что количество выкуриваемых сигарет увеличивается, развивается никотиновое перенасыщение: тошнота, головная боль.
Иногда вместо табака для курения используют траву – марихуану (каннабис). Это психоактивное соединение, получаемое из конопли. Обладает выраженным наркотическим эффектом, поэтому относится к запрещенным веществам. У нас в стране выращивание, продажа марихуаны наказывается уголовной ответственностью.
Марихуана отрицательно влияет на психику, приводит к угнетению умственной деятельности, вызывает чувство тревоги и беспокойства. По влиянию на органы дыхания сходен с табаком, также повышен риск развития бронхитов, астмы, простуд, частых ангин. Марихуана повышает артериальное давление, что опасно развитием инсультов и инфарктов у больных гипертонией.
Марихуана повышает артериальное давление, что опасно развитием инсультов и инфарктов у больных гипертонией.
Дым, при сгорании марихуаны, оказывает вредное воздействие на слизистую желудка (гастриты), на моторику кишечника (поносы), страдает печень (гепатит).
Многие молодые люди, выкуривают сигарету с марихуаной для усиления оргазма во время секса. Но немногие из них знают, что злоупотребление вызывает ухудшение половой функции и снижению потенции у мужчин.
У женщин снижается способность к зачатию, а если марихуану курит беременная, то это утяжеляет процесс вынашивания плода (выкидыши, мертворождения), а у родившихся детей наблюдаются различные патологии.
Вейпы или аэрозоли ЭСДН (электронные системы доставки никотина) по виду напоминают ингалятор, в составе которого находится картридж с жидкостью и распылитель. Компонентами раствора являются пропиленгликоль, акролеин, формальдегид, ароматизаторы. При вдыхании образуется пар, содержащий взвесь микрочастиц никотина.
Картриджи сменные, после использования вставляются новые, причем они классифицируются, как табачные изделия: суперлегкие, легкие, крепкие.
Пропиленгликоль вызывает раздражение слизистой дыхательных путей, что может привести к аллергической реакции.
- Акролеин, воздействуя на слизистые глаз и респираторного тракта, усиливает слезотечение и кашель.
- Формальдегид – канцерогенное вещество.
- Ароматизаторы в составе пара глубоко проникают в структуру легких и повреждают ткани альвеол.
Переход на электронные сигареты не снижает никотиновой зависимости, а курильщики вскоре вновь начинают курить обычные сигареты.
Резкий отказ от курения не означает мгновенного выздоровления, но положительный эффект отказа от вредной привычки все же значительный. Так, опасность смерти в течение 5 лет по любой причине снижается на 13%, опасность заболеть раком на 21%, уберечься от инфаркта удается более 61% бывших курильщиков, а от инсульта в 42%.
И хотя отказаться от табакокурения действительно сложно, человек должен понять, что сама жизнь бесценна и разменивать ее на сомнительное удовольствие – затянуться сигаретой, по меньшей мере, глупо.
О курении — Учреждение здравоохранения «Витебский областной эндокринологический диспансер»
Жизнь в XXI веке ставит перед нами много новых проблем, среди которых самой актуальной на сегодняшний день является проблема сохранения здоровья. Если несколько десятилетий назад эта проблема больше касалась людей старшей возрастной группы, то сейчас, к сожалению, состояние здоровья наших подростков оставляет желать лучшего. Каждый пятый житель Земли является подростком и все они подвергаются ряду важных психосоматических изменений, в результате которых формируется личность и закладывается ее здоровье. Не секрет, что здоровые подростки — успешное будущее любой страны. Учеными давно доказано, что здоровье человека лишь на 10 % зависит от успехов здравоохранения, а на 50% — от образа жизни. На фоне небывалого роста болезней «цивилизации», распространенности поведенческих факторов риска, особенно в молодежной среде, чтобы быть здоровым, нужно овладеть искусством его сохранения и укрепления — овладеть навыками здорового образа жизни. Одним из главных составляющих здорового образа жизни является отказ от вредных привычек: курения, потребления алкоголя, наркотиков. Эти «нарушители здоровья» являются причиной многих заболеваний, резко сокращают продолжительность жизни, снижают работоспособность, пагубно отражаются не только на здоровье молодежи, но и на здоровье будущих поколений.
Одним из главных составляющих здорового образа жизни является отказ от вредных привычек: курения, потребления алкоголя, наркотиков. Эти «нарушители здоровья» являются причиной многих заболеваний, резко сокращают продолжительность жизни, снижают работоспособность, пагубно отражаются не только на здоровье молодежи, но и на здоровье будущих поколений.
Что такое привычки? Привычками называют формы поведения человека, возникающие в процессе обучения и многократного повторения различных жизненных ситуаций, выполняемых автоматически. Сформировавшись, привычка становится неотъемлемой частью образа жизни. В настоящее время к вредным привычкам относят все виды токсикоманий (от греч. toxicon- ядовитый, mania- безумие, сумасшествие) – болезней, возникающих от злоупотребления некоторыми лекарственными веществами (наркотическими, снотворными, успокаивающими, возбуждающими и др.), а также алкоголем, табаком и другими токсическими веществами и комплексными составами. Привычки, которые небезопасны для здоровья, называются вредными, хотя специалисты называют их иначе – зависимостями. Но на стадии формирования, когда привычка еще не дошла до автоматизма и не стала неотъемлемой потребностью, от нее еще можно отказаться самостоятельно. Но для этого необходима очень серьезная мотивация, т.е. желание отказаться, которая может выработаться только тогда, когда подросток осознает опасность для здоровья потребления табака, алкоголя и наркотиков. Так в чем же их опасность, как они воздействуют на ткани, органы и системы растущего, еще не сформировавшегося и неокрепшего организма подростка? В этой лекции поговорим об опасности потребления табака.
Но на стадии формирования, когда привычка еще не дошла до автоматизма и не стала неотъемлемой потребностью, от нее еще можно отказаться самостоятельно. Но для этого необходима очень серьезная мотивация, т.е. желание отказаться, которая может выработаться только тогда, когда подросток осознает опасность для здоровья потребления табака, алкоголя и наркотиков. Так в чем же их опасность, как они воздействуют на ткани, органы и системы растущего, еще не сформировавшегося и неокрепшего организма подростка? В этой лекции поговорим об опасности потребления табака.
ТАБАКОКУРЕНИЕ
Одна из самых опасных привычек, хотя многим она кажется совсем безопасной: ведь курят многие и не все болеют, а многие доживают до глубокой старости. Так рассуждают и подростки, протягивая руку за своей первой сигаретой. Но мнения ученых однозначны: с курением связаны самые серьезные болезни сердца, сосудов, легких. Курение — не безобидное занятие, которое можно бросить без усилий. Это настоящая наркомания, и тем более опасная, что многие не принимают ее всерьез.
Это настоящая наркомания, и тем более опасная, что многие не принимают ее всерьез.
Курение не только подтачивает здоровье, но и забирает силы в самом прямом смысле. Как установили специалисты, через 5-9 минут после выкуривания одной только сигареты мускульная сила снижается на 15%, спортсмены знают это по опыту, и потому, как правило, не курят.
Компоненты табачного дыма по-разному влияют на организм: одни приводят к изменениям постепенно, а другие вызывают реакцию организма на свое присутствие уже при первом «появлении».
Курение табака и нервная система
Нервная система управляет работой всех органов и систем, обеспечивает функциональное единство организма человека и взаимодействия его с окружающей средой. Как известно, нервная система состоит из центральной (головной и спинной мозг), периферической (нервы, выходящие из спинного и головного мозга) и вегетативной, регулирующей деятельность внутренних органов, желез и кровеносных сосудов. Вегетативная нервная система в свою очередь подразделяется на симпатическую и парасимпатическую.
Вегетативная нервная система в свою очередь подразделяется на симпатическую и парасимпатическую.
Работа головного мозга, вся нервная деятельность обусловлены процессами возбуждения и торможения. В процессе возбуждения нервные клетки головного мозга усиливают свою деятельность, в процессе торможения – задерживают. Процесс торможения играет роль в ответной реакции организма на соответствующую обстановку и раздражитель. Кроме того, торможение выполняет защитную функцию, предохраняя нервные клетки от перенапряжения и истощения.
Постоянное и правильное сбалансирование процессов возбуждения и торможения обусловливает нормальную высшую нервную деятельность человека.
Чем выше развита нервная система, тем она менее устойчива к никотину — одному из самых опасных ядов растительного происхождения. Влияние никотина на головной мозг было исследовано советским ученым А.Е. Щербаковым. Он установил, что малые дозы никотина повышают возбудимость коры головного мозга на очень короткое время, а затем угнетают и истощают деятельность нервных клеток. При курении электроэнцефалограмма отмечает снижение биоэлектрической активности, что свидетельствует об ослаблении нормальной деятельности головного мозга. Представление некоторых о курении как стимуляторе работоспособности основано на том, что курильщик вначале действительно испытывает кратковременное возбуждение. Однако оно быстро сменяется торможением. Мозг привыкает к никотиновым «подачкам» и начинает требовать их, иначе появляется беспокойство, раздражительность. И человек опять начинает курить, т. е. все время «бьет свой мозг», ослабляя процесс торможения. Равновесие возбуждения и торможения нарушается вследствие перевозбуждения нервных клеток, которые, постепенно истощаясь, снижают умственную деятельность головного мозга. Нарушение процессов возбуждения и торможения вызывает симптомы, характерные для невроза (при неврозах тоже нарушаются процессы возбуждения и торможения под влиянием неблагоприятных внешних психогенных факторов).
При курении электроэнцефалограмма отмечает снижение биоэлектрической активности, что свидетельствует об ослаблении нормальной деятельности головного мозга. Представление некоторых о курении как стимуляторе работоспособности основано на том, что курильщик вначале действительно испытывает кратковременное возбуждение. Однако оно быстро сменяется торможением. Мозг привыкает к никотиновым «подачкам» и начинает требовать их, иначе появляется беспокойство, раздражительность. И человек опять начинает курить, т. е. все время «бьет свой мозг», ослабляя процесс торможения. Равновесие возбуждения и торможения нарушается вследствие перевозбуждения нервных клеток, которые, постепенно истощаясь, снижают умственную деятельность головного мозга. Нарушение процессов возбуждения и торможения вызывает симптомы, характерные для невроза (при неврозах тоже нарушаются процессы возбуждения и торможения под влиянием неблагоприятных внешних психогенных факторов).
Никотин действует на вегетативную нервную систему и прежде всего на ее симпатический отдел, ускоряя работу сердца, суживая кровеносные сосуды, повышая артериальное давление; отрицательно сказывается действие никотина на работе органов пищеварения, обмене веществ.
В первое время при курении наблюдаются неприятные ощущения: горьковатый привкус во рту, кашель, тошнота, головокружение, головная боль, усиленное сердцебиение, повышенная потливость. Это не только защитная реакция организма, но и явления интоксикации. Однако постепенно организм курильщика привыкает к никотину, явления интоксикации исчезают, а потребность в нем перерастает в привычку, т. е. превращается в условный рефлекс, и остается все время, пока человек курит.
Под действием никотина наступает сужение периферических сосудов, и кровоток в них снижается на 40-45 %. После каждой выкуренной сигареты сужение кровеносных сосудов сохраняется около получаса, следовательно, у человека, выкуривающего по одной сигарете через 30-40 минут, сужение сосудов сохраняется почти непрерывно.
Вследствие раздражающего действия никотина на гипоталамическую область головного мозга происходит выделение антидиуретического гормона, уменьшающего выделение с мочой воды из организма. Снижение диуреза отмечается после выкуривания одной сигареты, и это действие продолжается 2-3 часа, что приводит к появлению отеков.
В результате курения снижается насыщение крови кислородом и развивается кислородное голодание, от которого страдает нервная системы, прежде всего, головной мозг.
Окись углерода, находящаяся в табачном дыме, также оказывает неблагоприятное влияние на психомоторные функции. Так, под воздействием окиси углерода у человека снижается способность выполнять тонкие операции руками, оценивать высоту звука, интенсивность освещения, длительность временных интервалов. Происходит это потому, что окись углерода вступает в соединение с гемоглобином, а это препятствует усвоению организмом кислорода.
Если учесть, что 20 % общего количества поступающего в организм кислорода поглощается мозгом (при массе мозга 2 % от массы тела), то можно себе представить, к чему ведет такое искусственное кислородное голодание.
Нервная система страдает и от того, что витамин С, необходимый для ее деятельности, разрушается под влиянием никотина, что само по себе уже может привести к появлению раздражительности, быстрой утомляемости, снижению аппетита, нарушение сна. Например, подсчитано, что одна выкуренная сигарета нейтрализует половину того количества витамина С, который организм человека должен получить за сутки. Кроме того, под воздействием никотина нарушается усвоение других витаминов: в организме курильщика возникает дефицит витаминов А, В1, В6, В12.
Например, подсчитано, что одна выкуренная сигарета нейтрализует половину того количества витамина С, который организм человека должен получить за сутки. Кроме того, под воздействием никотина нарушается усвоение других витаминов: в организме курильщика возникает дефицит витаминов А, В1, В6, В12.
И всем компонентам табачного дыма нет никакой разницы, в каком организме они «творят все эти бедствия» — в 50-летнем, или в организме подростка 14 -15 лет. Последствия, конечно, более разрушительны для еще не окрепшего организма.
С возрастом и ростом «стажа курения» у курильщиков больше, чем у не курящих, увеличивается количество холестерина в крови, повышается проницаемость стенок сосудов. В табачном дыме обнаружено вещество, которое способствует склеиванию клеток крови (тромбоцитов) и образованию ее сгустков. Все это обусловливает развитие атеросклероза сосудов головного мозга. Атеросклероз у курильщиков развивается на 10-15 лет раньше, чем у не курящих. Учеными обнаружены тяжи холестерина в крупных артериях подростков, что говорит о раннем развитии атеросклероза, которые потом превращаются в холестериновые бляшки и нарушают кровоток. Последствия раннего атеросклероза — инсульты.
Учеными обнаружены тяжи холестерина в крупных артериях подростков, что говорит о раннем развитии атеросклероза, которые потом превращаются в холестериновые бляшки и нарушают кровоток. Последствия раннего атеросклероза — инсульты.
Курение часто становится причиной развития невритов, полиневритов, плекситов, радикулитов. Чаще при этом поражаются плечевой, лучевой, седалищный, бедренный нервы. В ряде случаев у курильщиков наблюдается нарушение болевой чувствительности в конечностях. Интересно, что лица, страдающие невритами и полиневритами, даже если они не курят сами, могут ощущать боль в руках и ногах, находясь в накуренном помещении.
Курение может играть определенную роль в возникновении такого тяжелого, прогрессирующего заболевания нервной системы, как рассеянный склероз, которое ведет к стойкой утрате трудоспособности и характеризируется нарушением координации движений, появлением парезов и параличей, психических нарушений, поражением зрительного нерва и др.
Никотин усиливает функцию желез внутренней секреции. После выкуренной сигареты в крови резко увеличивается количество гормонов — кортикостероидов, адреналина. Это приводит к повышению артериального давления. Известно, что гипертоническая болезнь у курильщиков наблюдается в 5 раз чаще, чем у некурящих, развивается она в более молодом возрасте, протекает тяжелее.
После выкуренной сигареты в крови резко увеличивается количество гормонов — кортикостероидов, адреналина. Это приводит к повышению артериального давления. Известно, что гипертоническая болезнь у курильщиков наблюдается в 5 раз чаще, чем у некурящих, развивается она в более молодом возрасте, протекает тяжелее.
У курящих подростков из-за высокой чувствительности нервной системы к табаку чаще, чем у некурящих, встречаются нервные и психические нарушения. Такие подростки нередко раздражительны, невнимательны, плохо спят, быстро утомляются, у них снижены память, внимание, работоспособность.
Раннее курение нередко приводит к развитию так называемой юношеской гипертонии. Если вначале артериальное давление повышается периодически, ненадолго, то через 4-6 лет курения оно уже стойко держится на высоких цифрах.
Курение табака и сердечно-сосудистая система
Сердечно-сосудистые заболевания – одна из важных проблем, которой занимается современная медицинская наука, потому что они занимают 1 место в Мире среди всех причин смерти населения. В развитии болезней сердечно-сосудистой системы немаловажную и далеко не безвредную роль играет курение. Из продуктов табачного дыма на сердечно-сосудистую систему особенно вредно действует никотин и окись углерода, как и на нервную систему.
В развитии болезней сердечно-сосудистой системы немаловажную и далеко не безвредную роль играет курение. Из продуктов табачного дыма на сердечно-сосудистую систему особенно вредно действует никотин и окись углерода, как и на нервную систему.
За сутки сердце курильщика, под воздействием компонентов табачного дыма, делает около 10-15 тыс. лишних сокращений. Какую огромную дополнительную нагрузку выполняет при этом сердце! Необходимо учесть еще и то, что при систематическом курении сосуды сердца склерозированы (сужены) и снижено поступление кислорода в сердечную мышцу, что приводит ее к хроническому переутомлению.
Доказано, что одна выкуренная сигарета кратковременно повышает давление примерно на 10 мм. рт. ст. При систематическом курении артериальное давление повышается в среднем на 20-25 %. Исследования показали, что имеющиеся у юных курильщиков нарушения обмена веществ в мышце сердца является предпосылкой к будущим болезням сердца.
Нанося большой вред сердцу и сосудам, курение является причиной развития многих заболеваний.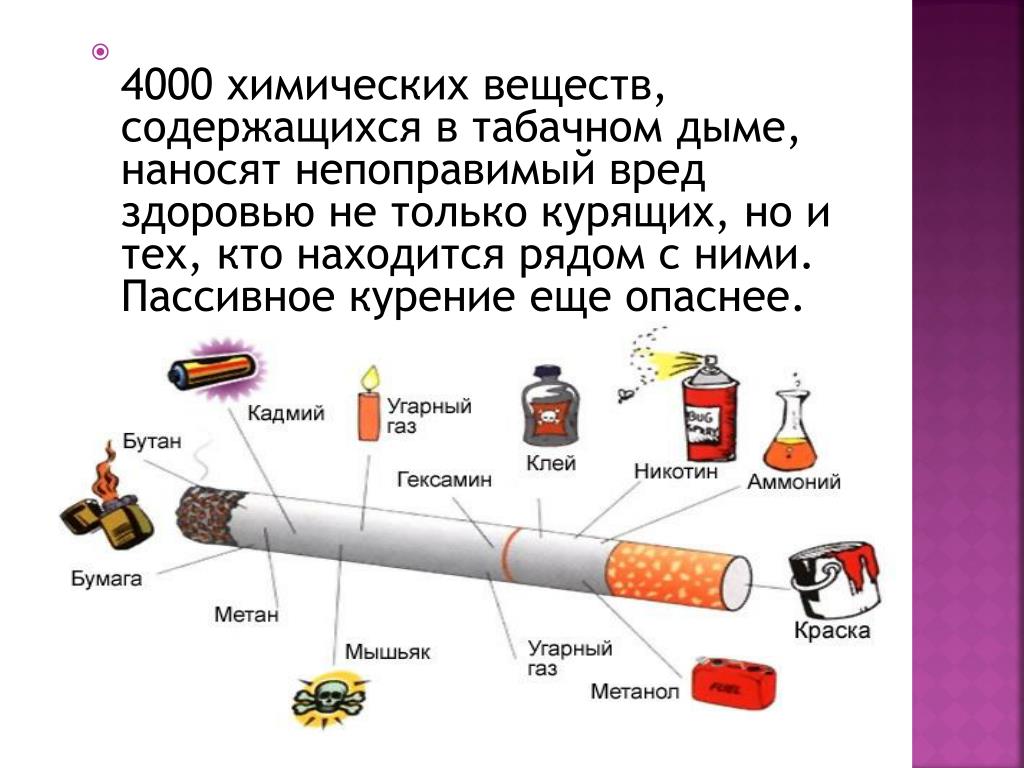 Так, у курящих наблюдаются явления «сердечного невроза». После физического или психического напряжения возникают неприятные ощущения в области сердца, стеснение в груди, усиленное сердцебиение, может наблюдаться аритмия. И все это не зависит от возраста!
Так, у курящих наблюдаются явления «сердечного невроза». После физического или психического напряжения возникают неприятные ощущения в области сердца, стеснение в груди, усиленное сердцебиение, может наблюдаться аритмия. И все это не зависит от возраста!
В настоящее время многие страдают ишемической болезнью сердца, которая связана с недостаточным кровоснабжением сердечной мышцы. Ранним проявлением ишемической болезни сердца является стенокардия. Приступы стенокардии наблюдаются у курящих в 2 раза чаще, чем у некурящих. При воздержании от курения явления стенокардии уменьшается или полностью исчезают.
При ишемической болезни сердца может наступить инфаркт миокарда. Он является следствием атеросклероза сосудов сердца и развивается в результате их тромбоза. Внезапно обескровливается участок сердечной мышцы, что ведет к его некрозу и в дальнейшем развитию на этом месте рубца.
Курение в значительной степени способствует развитию инфаркта миокарда, так как оно является одной из причин развития атеросклероза и ишемической болезни сердца.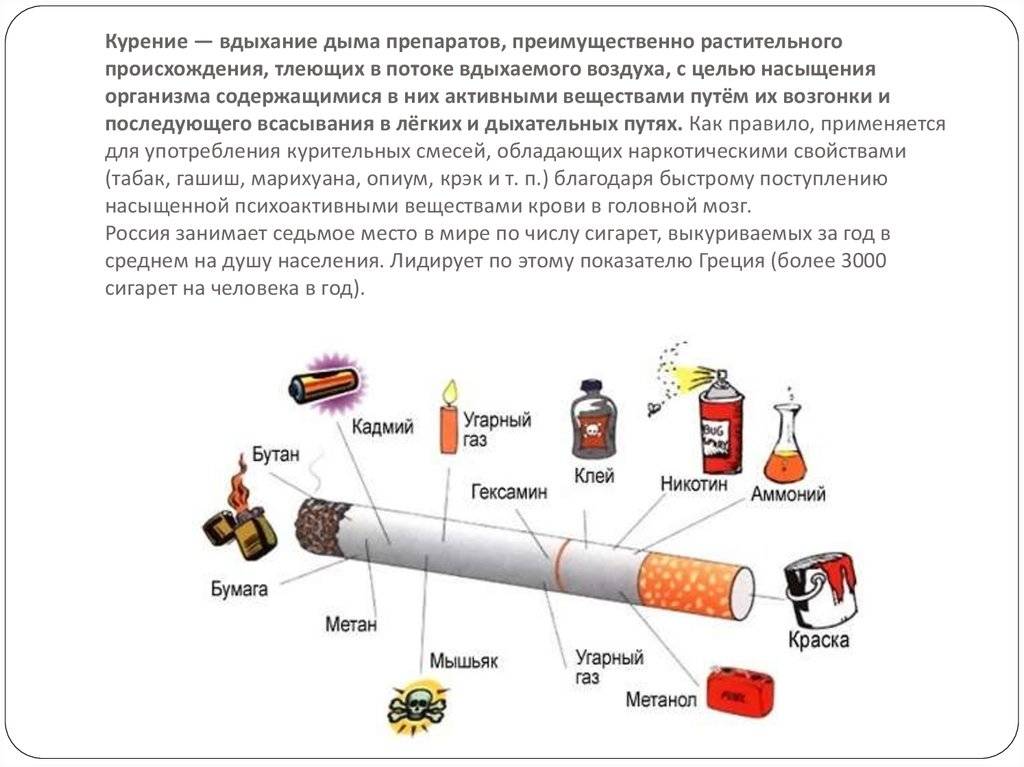 Никотин держит сосуды сердца в состоянии спазма, сердце – в повышенной нагрузке (учащается частота его сокращений), повышается артериальное давление. К сердцу поступает меньше кислорода из-за образования карбоксигемоглобина и сниженной дыхательной деятельности легких. Карбоксигемоглобин повышает вязкость крови и способствует развитию тромбоза.
Никотин держит сосуды сердца в состоянии спазма, сердце – в повышенной нагрузке (учащается частота его сокращений), повышается артериальное давление. К сердцу поступает меньше кислорода из-за образования карбоксигемоглобина и сниженной дыхательной деятельности легких. Карбоксигемоглобин повышает вязкость крови и способствует развитию тромбоза.
Сочетание курения с гипертонической болезнью дает шестикратный риск развития инфаркта миокарда. Врачи с тревогой отмечают, что в последнее десятилетие инфаркт значительно «помолодел» – случаи инфаркта зафиксированы у 24-25 летних мужчин, в анамнезе которых – начало курения в подростковом возрасте. Отказ от курения после перенесенного инфаркта миокарда снижает опасность его повторения в течение 3-6 лет. Но если человек продолжает курить, сердце не вынесет дополнительной нагрузки от компонентов табачного дыма и развивается второй инфаркт, который чаще заканчивается печально. По данным ученых, через год после перенесенного инфаркта миокарда среди продолжающих курить остаются в живых только 5 %.
У курильщиков вследствие атеросклероза и повышения артериального давления чаще, чем у некурящих, развиваются расстройства мозгового кровообращения, в частности инсульт (кровоизлияние в головной мозг и тромбоз мозговых сосудов, вызывающие параличи лица, руки и ноги, часто расстройство речи).
Многие исследования показывают, что курение активизирует процессы свертывания крови и ослабляет ее антисвертывающую систему и приводит к возникновению тромбоза в различных сосудах.
Раннее развитие атеросклероза в периферических сосудах ног приводит к облитерирующему эндартерииту, проявляющегося в перемежающейся хромоте. При прогрессировании болезни может развиться гангрена (омертвение) пальцев, и если их вовремя не удалить, может произойти заражение крови. Доказано, что основной причиной облитерирующего эндартериита является хроническое отравление никотином. У большинства больных симптомы этого заболевания исчезают от одного лишь прекращения курения и появляются снова при его возобновлении. В связи с этим нет более эффективного лечения, чем помочь им бросить курить. А в предупреждении заболевания самое действенное – не начинать курить.
В связи с этим нет более эффективного лечения, чем помочь им бросить курить. А в предупреждении заболевания самое действенное – не начинать курить.
Курение табака и органы дыхания
Органы дыхания – это первая система в организме, которая принимает на себя удар при затяжке курильщика. Через органы дыхания в организм поступают все компоненты табачного дыма: — аммиак вызывает раздражение слизистых оболочек полости рта, носа, гортани, трахеи, бронхов и в результате развивается хроническое воспаление дыхательных путей;
-никотин раздражает слизистые оболочки носа и вызывает хронический катар, который, распространяясь на ход, соединяющий нос и ухо, может привести к снижению слуха;
— табачный дым действует на голосовые связки и продолжительное курение ведет к тому, что в них разрастается фиброзная ткань, сужается голосовая щель. Хроническое раздражение голосовых связок изменяет тембр и окраску произносимых звуков, голос утрачивает чистоту и звучность, становится хриплым, что может трагически изменить планы подростка при выборе профессии: у певцов, актеров, преподавателей, лекторов голос должен быть чистым и звучным;
— попадая в трахею и бронхи, табачный дым действует на верхний слой слизистых оболочек, который имеет колеблющиеся реснички, очищающие воздух от пыли и мелких частиц. Никотин парализует реснички, и частицы табачного дыма оседают на слизистой оболочке трахеи и бронхов. Мельчайший их размер позволяет им глубоко проникать и оседать в легких. Слизистые оболочки гортани, трахеи и бронхов от частого курения раздражаются и воспаляются. Поэтому хронический трахеит и хронический бронхит – обычные для курящих заболевания, которые развиваются всего через пару лет после начала курения. Типичная примета курильщика – кашель с выделением слизи темного цвета от частиц табачного дыма, особенно мучающий по утрам. Кашель – это естественная защитная реакция, с помощью которой происходит освобождение трахеи и бронхов от слизи, усиленно вырабатывающейся железами бронхов под влиянием курения и вследствие воспалительного отека слизистой оболочки бронхов, а также от осевших твердых частиц табачного дыма. Закуривая утром первую сигарету, курильщик раздражает верхние дыхательные пути и этим вызывает кашель. Никакие лекарства в таких случаях не помогают. Единственное средство – прекратить курение.
Никотин парализует реснички, и частицы табачного дыма оседают на слизистой оболочке трахеи и бронхов. Мельчайший их размер позволяет им глубоко проникать и оседать в легких. Слизистые оболочки гортани, трахеи и бронхов от частого курения раздражаются и воспаляются. Поэтому хронический трахеит и хронический бронхит – обычные для курящих заболевания, которые развиваются всего через пару лет после начала курения. Типичная примета курильщика – кашель с выделением слизи темного цвета от частиц табачного дыма, особенно мучающий по утрам. Кашель – это естественная защитная реакция, с помощью которой происходит освобождение трахеи и бронхов от слизи, усиленно вырабатывающейся железами бронхов под влиянием курения и вследствие воспалительного отека слизистой оболочки бронхов, а также от осевших твердых частиц табачного дыма. Закуривая утром первую сигарету, курильщик раздражает верхние дыхательные пути и этим вызывает кашель. Никакие лекарства в таких случаях не помогают. Единственное средство – прекратить курение.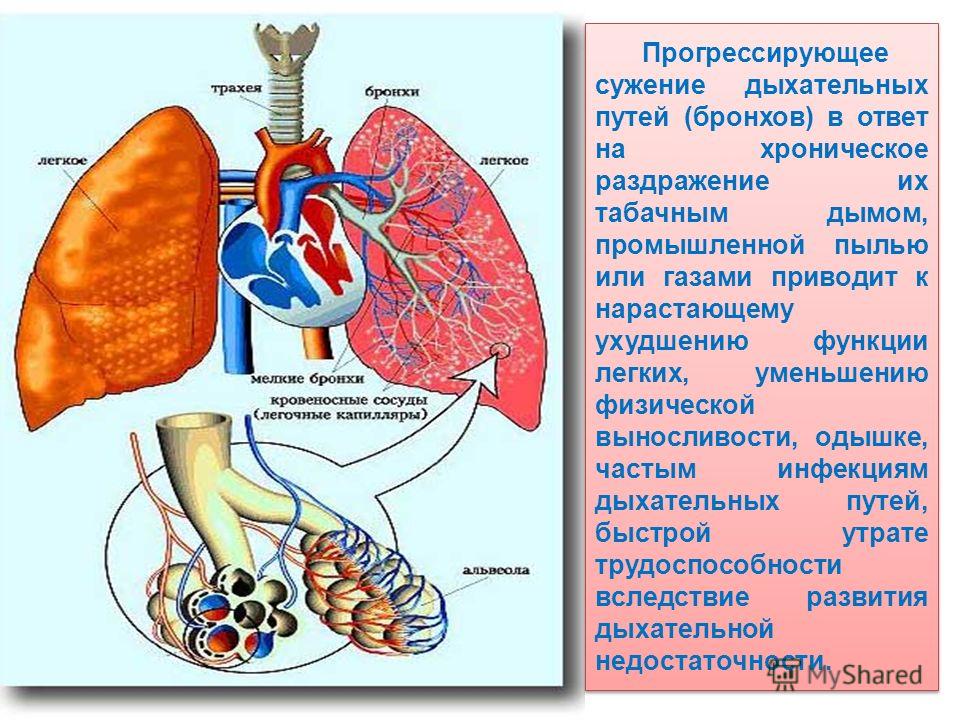
Кашель вызывает эмфизему легких, проявляющуюся в виде отдышки, затруднения дыхания. Степень выраженности хронического бронхита, эмфиземы легких зависит от продолжительности курения, количества выкуриваемых сигарет, а также от глубины затяжки.
Легкие курильщика менее эластичны, более загрязнены, вентиляционная функция их снижена, и они раньше стареют. Длительное хроническое воспаление дыхательных путей и легких приводит к понижению их сопротивляемости и развитию острых и хронических заболеваний, например пневмонии, бронхиальной астмы, повышает чувствительность организма к гриппу.
Курение способствует развитию туберкулеза легких. Французский ученый Пти установил, что из 100 заболевших туберкулезом 95 % курили.
Курение является основной причиной развития около трети всех заболеваний органов дыхания. Даже при отсутствии признаков заболевания может возникнуть нарушение функции легких. У молодого человека, выкуривающего 10 сигарет в день, дыхание примерно такое же, как у человека старше его на 20 лет, но не курящего.
Изменения в легких курящего подростка наступают гораздо быстрее и повреждения органов дыхания масштабнее, поскольку защитные функции еще в стадии формирования и противостоять разрушающему воздействию компонентов табачного дыма организм не в состоянии.
Курение табака и органы пищеварения
Табачный дым, имеющий высокую температуру, попадая в полость рта, начинает свою разрушительную работу. Изо рта курильщика неприятно пахнет, язык обложен серым налетом (один из показателей неправильной деятельности желудочно-кишечного тракта). Под влиянием никотина и частиц табачного дыма желтеют и портятся зубы. Температура табачного дыма во рту около 50-60 С, а температура воздуха, поступающего в рот, намного ниже — значительная разница температур отражается на зубах: портится эмаль, разрыхляются и кровоточат десны, развивается кариес, открывая, образно говоря, ворота для инфекции.
Бытует мнение, что курение уменьшает зубную боль. Это связано с токсическим действием табачного дыма на зубной нерв, что является практическим подтверждением того, что никотин является нервнопаралитическим ядом и опасность его для организма человека очень велика, тем более для организма подростка.
Раздражая слюнные железы, никотин вызывает усиленное слюноотделение. Курильщик не только выплевывает излишнюю слюну, но и проглатывает ее, усугубляя вредное действие никотина на пищеварительный аппарат. Проглатываемая слюна с никотином не только раздражает слизистую оболочку желудка, но и заносит инфекцию. Это может привести к развитию гастрита.
Двигательная и сократительная деятельность желудка спустя 15 минут после начала курения прекращается, и переваривание пищи задерживается, тем самым приводя к воспалительным заболеваниям желудка. А ведь есть люди, которые курят перед едой и во время еды. Многие курят после еды, создавая дополнительные проблемы своему желудку.
Никотин нарушает процесс выделения желудочного сока и его кислотность: во время курения сосуды желудка суживаются, слизистая оболочка обескровливается, количество желудочного сока и его кислотность повышены, да еще заглатываемый со слюной никотин раздражает стенку желудка. Все это приводит к развитию язвенной болезни.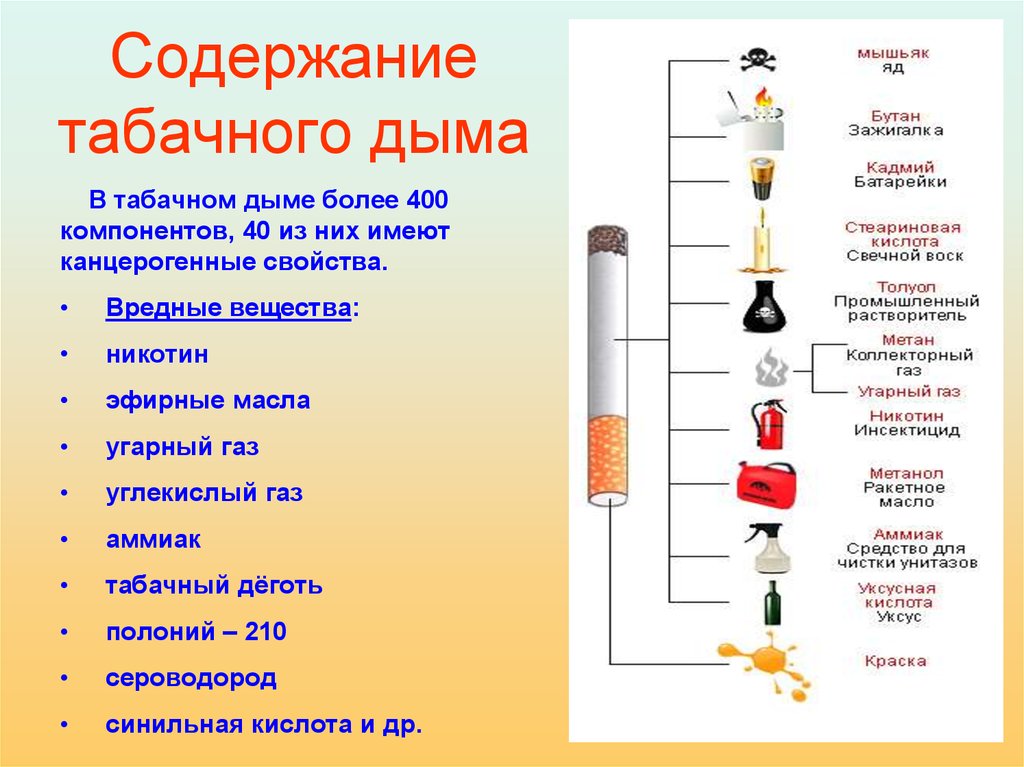 Аналогичен механизм развития и язвенной болезни двенадцатиперстной кишки. Профессор С.М. Некрасов (РФ) при массовом обследовании мужчин на выявление язвенной болезни желудка обнаружил, что она в 12 раз чаще встречается у курящих. Позднее им при обследовании 2280 человек была установлена язвенная болезнь желудка и двенадцатиперстной кишки среди курящих у 23 % мужчин и 30 % женщин, а среди некурящих – только у 2 % мужчин и 5 % женщин. Если при язвенной болезни желудка и двенадцатиперстной кишки человек продолжает курить, болезнь обостряется, могут возникнуть кровотечения, что вызывает необходимость операции. Следует учитывать и то, что язва желудка и двенадцатиперстной кишки может перерасти в рак.
Аналогичен механизм развития и язвенной болезни двенадцатиперстной кишки. Профессор С.М. Некрасов (РФ) при массовом обследовании мужчин на выявление язвенной болезни желудка обнаружил, что она в 12 раз чаще встречается у курящих. Позднее им при обследовании 2280 человек была установлена язвенная болезнь желудка и двенадцатиперстной кишки среди курящих у 23 % мужчин и 30 % женщин, а среди некурящих – только у 2 % мужчин и 5 % женщин. Если при язвенной болезни желудка и двенадцатиперстной кишки человек продолжает курить, болезнь обостряется, могут возникнуть кровотечения, что вызывает необходимость операции. Следует учитывать и то, что язва желудка и двенадцатиперстной кишки может перерасти в рак.
Чувствителен к никотину и кишечник: курение вызывает раздражение и усиливает его перистальтику. Нарушение функции кишечника выражается периодически сменяющимися запорами и поносами. Кроме того, спазмы прямой кишки, вызываемые действием никотина, затрудняют отток крови и способствуют образованию геморроя. Кровотечение из геморроидальных узлов курением поддерживается и даже усиливается.
Кровотечение из геморроидальных узлов курением поддерживается и даже усиливается.
Особо следует сказать о влиянии табака на печень. Печень выполняет защитную, барьерную роль в обезвреживании ядов, поступающих в наш организм. Синильную кислоту из табачного дыма она переводит в относительно безвредное состояние – роданистый калий, который выделяется со слюной 5-6 дней, и в течение этих дней можно определить, что человек недавно курил. Курение как хроническое отравление, вызывая усиление обезвреживающей работы печени, способствует развитию многих заболеваний. В свою очередь при некоторых заболеваниях печени курение играет роль отягощающего фактора. В опытах, когда кроликам вводили никотин, у них возникал цирроз печени.
У курильщиков наблюдается увеличение печени в размере.
Курение приводит к повышению содержание сахара в крови, что отражается на функции поджелудочной железы, развиваются ее заболевания, в том числе сахарный диабет.
Никотин угнетает деятельность желез пищеварительного тракта, снижая аппетит. Многие боятся, что бросив курить, они пополнеют. Небольшое увеличение массы тела (не более 2 кг) возможно, и объясняется это оздоровлением организма, освобождением его от токсических веществ табачного дыма, восстановлением нормальных функций организма и в том числе и органов пищеварения, а также более интенсивным питанием вследствие повышения аппетита.
Многие боятся, что бросив курить, они пополнеют. Небольшое увеличение массы тела (не более 2 кг) возможно, и объясняется это оздоровлением организма, освобождением его от токсических веществ табачного дыма, восстановлением нормальных функций организма и в том числе и органов пищеварения, а также более интенсивным питанием вследствие повышения аппетита.
Необходимо отметить, что курение не только способствует развитию заболеваний органов пищеварения, но и изменяет характер заболеваний, повышает частоту обострений и осложнений, удлиняет сроки лечения.
Курение табака и органы чувств
Органы зрения
Человек воспринимает все разнообразие мира благодаря органам чувств, но курение отнимает и эту возможность у человека, неблагоприятно влияя на них.
Глаза курящего человека часто слезятся, краснеют, края век отекают. Появляется быстрая утомляемость при чтении, мелькание мушек, двоение в глазах. Никотин, действуя на зрительный нерв, вызывает его хроническое воспаление, вследствие чего снижается острота зрения.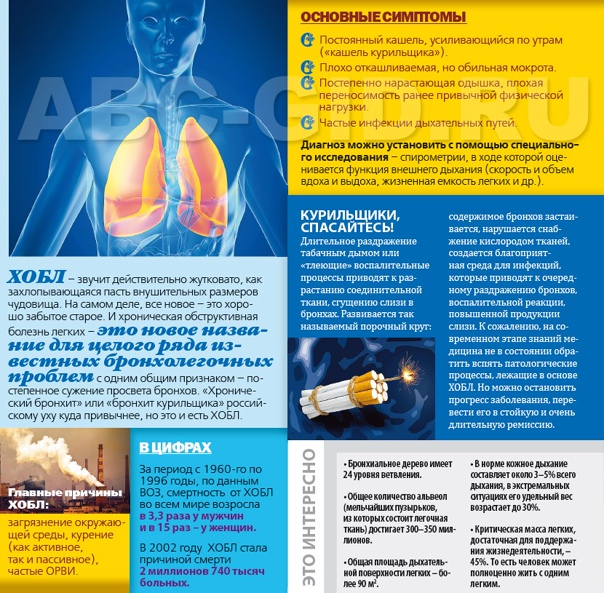 Никотин влияет и на сетчатку глаза: сужаются сосуды, изменяется сетчатка, что ведет к дегенерации ее в центральной области, нечувствительности к световым раздражителям и может привести к слепоте.
Никотин влияет и на сетчатку глаза: сужаются сосуды, изменяется сетчатка, что ведет к дегенерации ее в центральной области, нечувствительности к световым раздражителям и может привести к слепоте.
У курильщиков часто меняется цветоощущение сначала на зеленый, в дальнейшем на красный и желтый и в последнюю очередь на синий цвет.
Следует особо подчеркнуть, что никотин повышает внутриглазное давление и в связи с этим может развиться глаукома и привести к слепоте.
Принимая во внимание, насколько подростки увлечены компьютерными играми, просмотрами видеоматериалов на различных гаджетах, можно понять, насколько велика у них нагрузка на глаза, что и приводит к снижению остроты зрения. Если прибавить еще и потребление табака, то становится понятно, насколько возрастает риск развития заболеваний глаз и проблем со зрением.
Органы слуха
Небезопасно потребление табака для органов слуха. В ходе научных экспериментов учеными установлено, что под действием никотина барабанная перепонка утолщается и втягивается вовнутрь, подвижность слуховых косточек уменьшается.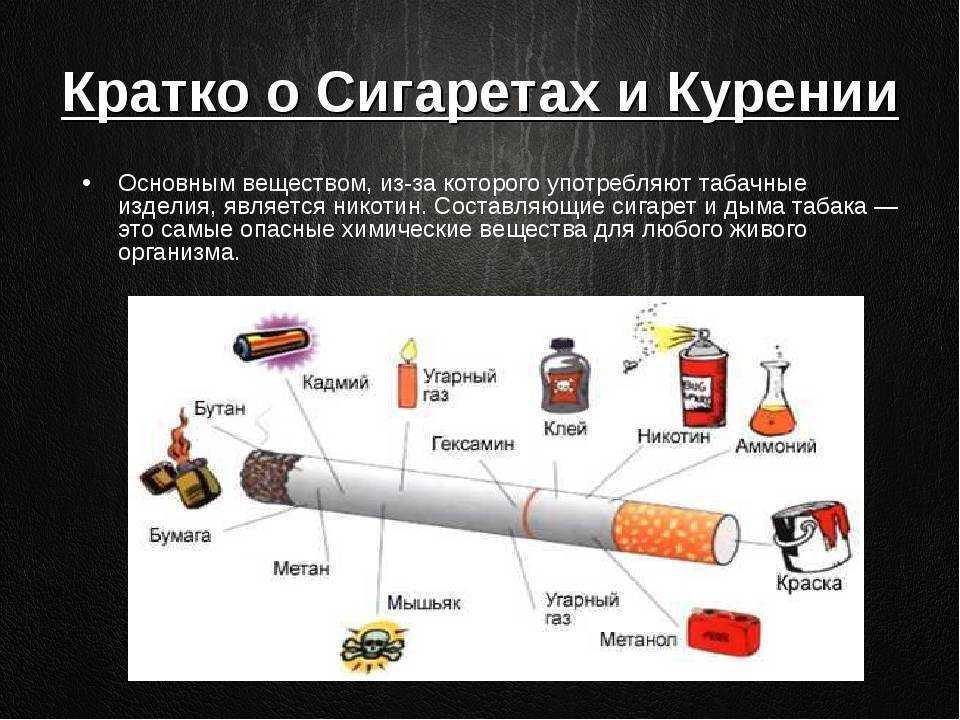 Одновременно слуховой нерв испытывает токсическое воздействие никотина, что и становится причиной снижения остроты слуха у курящих людей. Причем эта патология выявляется и у лиц молодого возраста. После прекращения курения возможно частичное восстановления слуха.
Одновременно слуховой нерв испытывает токсическое воздействие никотина, что и становится причиной снижения остроты слуха у курящих людей. Причем эта патология выявляется и у лиц молодого возраста. После прекращения курения возможно частичное восстановления слуха.
Органы обоняния
Очень важными для всех нас являются органы чувств. Обоняние человека способно сделать восприятие мира намного ярче. Орган обоняния – нос, который служит нам, чтобы мы могли наслаждаться прекрасными запахами, ароматами. Он также предупреждает нас о различного рода опасностях (пожар, утечка газа). Хорошее обоняние очень важно для любого человека, так как без него невозможно воспринимать мир на все 100%. Так, при плохом обонянии жизнь может стать серой и тусклой, лишенной всех красок. И серый табачный дым способствует этому: воздействуя раздражающе на обонятельный нерв и рецепторные клетки, которые находятся на обонятельном эпителии (эпителий находится на слизистой оболочке верхнезадней части полости носа, в области носовой перегородки и верхнего носового хода).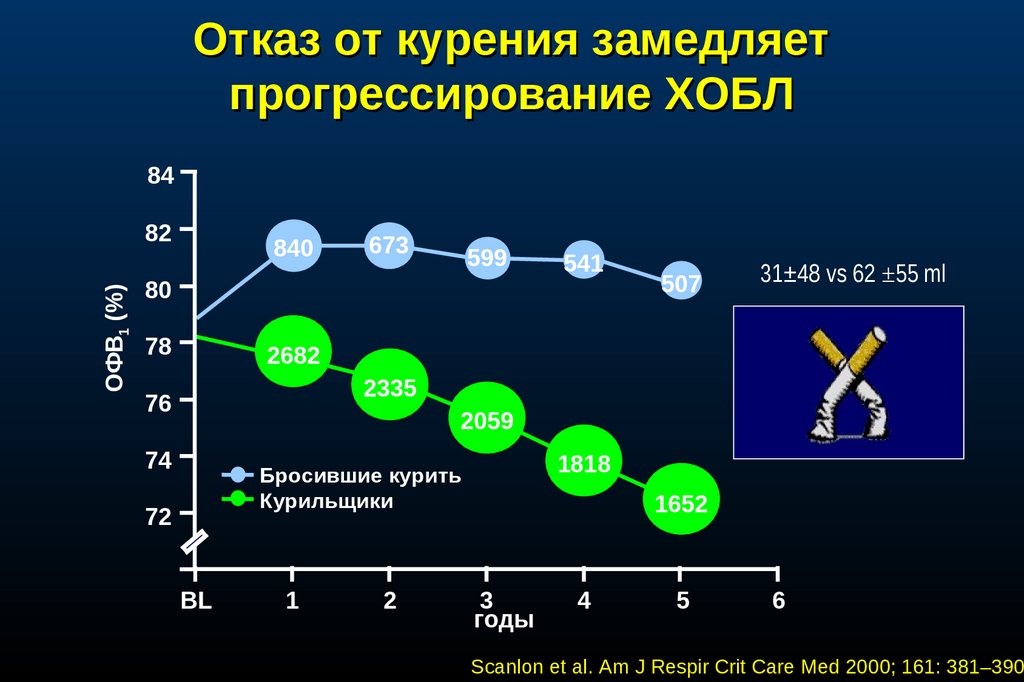 Площадь эпителия всего 4 см2 и его гибель лишает нас ароматов. Единственный выход спасти себя от «обонятельной глухоты» — отказаться от курения и знать об этой опасности нужно уже в детстве.
Площадь эпителия всего 4 см2 и его гибель лишает нас ароматов. Единственный выход спасти себя от «обонятельной глухоты» — отказаться от курения и знать об этой опасности нужно уже в детстве.
Органы вкуса
Благодаря органу вкуса, человек способен оценить пищу, употребляемую им в данный момент. Вкус пищи воспринимают специальные сосочки, расположенные на языке, а также вкусовые луковицы, имеющиеся в небе, надгортаннике и верхней части пищевода. Орган вкуса тесно взаимосвязан с органом обоняния, поэтому неудивительно, что мы хуже ощущаем вкус еды, когда страдаем каким либо простудным заболеванием. На языке существуют определенные зоны, ответственные за определение того или иного вкуса. Например, кончик языка определяет сладкое, середина – соленое, края языка ответственны за определение кислоты продукта, а корень – за горечь. Уже понятно, что на все эти зоны воздействует табачный дым при курении и шанс воспринимать вкус без изменений у курящего человека минимальный: действуя на вкусовые сосочки языка, никотин вызывает спазм сосудов, что способствует снижению обоняния и остроты вкусовых ощущений. Курящие нередко плохо различают вкус горького, сладкого, соленого, кислого.
Курящие нередко плохо различают вкус горького, сладкого, соленого, кислого.
Курение табака и эндокринная система
Эндокринная система регулирует деятельность всего организма за счет выработки особых веществ — гормонов, образующихся в железах внутренней секреции. Поступающие в кровь гормоны вместе с нервной системой обеспечивают регуляцию и контроль жизненно важных функций организма, поддерживая его внутреннее равновесие, нормальные рост и развитие. Уже из одного определения стало понятно, что эндокринная система не может правильно функционировать у курящего человека, поскольку она работает в «паре» с нервной системой. А как влияет табак на нервную систему мы уже знаем. Но все-таки…
Никотин нарушает работу эндокринных желез: гипофиза, щитовидной и околощитовидных желез, надпочечников, половых желез.
При курении больше всего страдает функция надпочечников. Так, при хроническом отравлении никотином кроликов в течение 6-9 мес. масса надпочечников увеличилась примерно в 2,5 раза.
Выкуривание 10 сигарет в день усиливает функцию щитовидной железы: повышается обмен веществ, учащается сердцебиение. В дальнейшем никотин может привести к угнетению функции щитовидной железы и даже прекращению ее деятельности. Говоря про 10 сигарет в день, мы имеем ввиду взрослого человека, а для подростка «хватит» и 1-2 х сигарет для возникновения проблем со щитовидной железой и железами внутренней секреции в целом.
Установлено, что курение табака пагубно влияет на деятельность половых желез. У мужчин никотин угнетает половые центры, расположенные в крестцовом отделе спинного мозга. Угнетение половых центров и невроз, который все время поддерживается курением, приводят к тому, что у курильщиков развивается половое бессилие (импотенция). Курящий мужчина при прочих равных условиях с некурящими укорачивает время нормальной половой жизни в среднем на 3-7 лет. Имеются данные, свидетельствующие о том, что в 11 % случаев половое бессилие у мужчин связано со злоупотреблением табаком. При лечении импотенции вне зависимости от причин, которыми она вызвана, прекращение курения – обязательное условие.
При лечении импотенции вне зависимости от причин, которыми она вызвана, прекращение курения – обязательное условие.
Многочисленными лабораторными исследованиями установлено, что курение неблагоприятно влияет на хромосомы половых клеток, как у мужчин, так и у женщин и может стать причиной бесплодия.
Интересное исследование в этом направлении проводились учеными. Они обнаружили, что курильщиков со стажем 10-15 лет в 1 мл семенной жидкости содержится меньшее количество сперматозоидов, они менее подвижны, чем у некурящих. Причем если мужчина выкуривает по 10 сигарет в сутки (взрослый мужчина!), эти изменения более выражены. Уменьшение количества сперматозоидов и их подвижности особенно заметно у лиц, начавших курить до 18 лет, т. е. до завершения формирования половой функции.
Курение табака и онкологические заболевания
Рак называют болезнью ХХ века. В настоящее время выявлены новые причины риска развития злокачественных опухолей, среди которых особое место принадлежит курению.
Известно, что в табачном дыме содержатся компоненты: смолы, бензпирен, радиоактивные изотопы, и другие вещества, оказывающие канцерогенное действие. Из 1000 сигарет выделяется около 2 мг бензпирена.
Из радиоактивных изотопов наиболее опасен полоний-210. Период его полураспада длительный, а у курильщика он накапливается в бронхах, легких, печени и почках. Выкуривая ежедневно более 10 сигарет, в год человек получает дозу облучения, равную примерно 500 Р (для сравнения – при рентгеновском снимке желудка доза составляет 0.76 Р). Длительно курящий человек получает дозу облучения, достаточную для того, чтобы вызвать такие изменения в клетках бронхов и легких, какие можно рассматривать как предраковые. У тех, кто бросил курить, наблюдалось их обратное развитие, что указывает на обратимость предраковых состояний.
За год человек вводит в свой организм 700-800 г. табачного дегтя при условии, что в день он выкуривает 10 сигарет и более.
Две трети табачного дыма попадают в легкие и покрывают до 10 % легочной поверхности.
На клетки легких продукты табачного дыма действуют в 40 раз сильнее, чем на любую другую ткань. При горении сигареты в ее конечной трети канцерогенные вещества концентрируются в большем количестве, чем в начальной ее части. Поэтому при докуривании сигареты до конца в организм попадает наибольшее количество вредных веществ.
Известный хирург академик АМН СССР Б.В. Петровский считает, что риск развития рака тесно связан не только с количеством ежедневно выкуриваемых сигарет, но и со «стажем» курильщика и значительно увеличивается для тех, кто стал курить в молодом возрасте. Вывод напрашивается сам: если в ваших планах на жизнь есть графа «Стать курящим», то хотя бы отложите начало претворения в жизнь этого действа лет до 20 — 22 в надежде, что: 1) организм полностью сформировался, окреп и готов к неравной битве с табаком или 2) уровень осознания ценности здоровья достигнет таких высот, что даже сама мысль о курении покажется нелепой.
Возможно, эти данные смогут убедить вас в опасности табака в развитии онкологических заболеваний: в середине 20 века американские ученые наблюдали за большой группой мужчин в возрасте 50-69 лет, из которых курили 31 816 и 32 392 были некурящими. Через 3.5 года от рака легкого умерли среди некурящих 4 человека, среди курящих – 81.
Через 3.5 года от рака легкого умерли среди некурящих 4 человека, среди курящих – 81.
Американские исследователи Хаммонд и Хорн приводят весьма убедительные показатели смертности от рака легкого на 100 тыс. населения: среди некурящих – 12.8; среди курящих сигареты: полпачки вдень – 95.2; от полпачки до 1 пачки – 107.8; 1-2 пачки – 229 и более 2 пачек – 264.2.
В странах, где широко распространено курение, смертность от рака легкого продолжает увеличиваться, в том числе и среди женщин, так как число курящих за последние несколько десятилетий увеличилось. Так, в Мексике, где женщины курят наравне с мужчинами, процент заболеваемости и смертности от рака легкого у мужчин и женщин, по статистическим данным, примерно одинаков.
При отказе от курения относительный риск развития рака легкого постепенно снижается и через 10 лет становится таким же, как у никогда не куривших. Проведенные в Великобритании наблюдения показали, что за 15 лет общее потребление сигарет не изменилось, однако за этот период смертность от рака легкого среди мужчин в возрасте 35-64 лет увеличилась на 7 %, а среди мужчин-врачей этого же возраста, прекративших курение, смертность снизилась на 38 %.
Многочисленными научными исследованиями установлена связь курения с развитием злокачественных опухолей губы, полости рта, гортани, пищевода. Это объясняется тем, что при курении сигареты или папиросы 1/3 табачного дегтя, а у курящих трубку или сигару – 2/3 его остаются в полости рта. Наряду с этим на развитие злокачественных опухолей влияют тепловые (горячий дым) и механические (держание во рту сигареты, трубки, сигары) факторы.
Заглатываемые со слюной частицы табачной копоти и содержащийся в них никотин способствуют развитию рака желудка.
Установлена связь рака мочевого пузыря с курением вследствие того, что вредные вещества табачного дыма выводятся через мочевые пути. Рак мочевого пузыря примерно в 2.7 раза чаще наблюдается у курильщиков по сравнению с некурящими.
По данным ВОЗ общая смертность среди курящих превышает смертность среди некурящих на 30-80%. Для тех, кто выкуривает 10 -19 сигарет, коэффициент смертности возрастает на 70%, а для выкуривающих 40 и более — на 130%.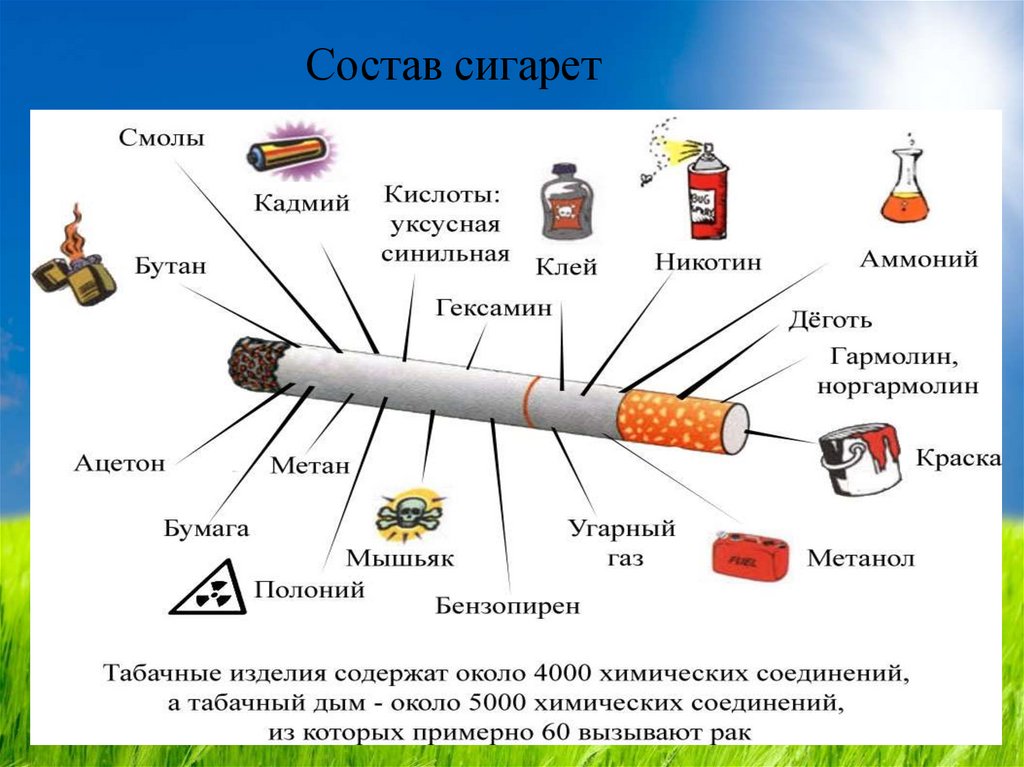
Вдыхание воздуха в накуренном помещении (пассивное курение) вызывает те же болезни, которыми страдают курильщики. В настоящее время курение глубоко вошло в быт многих девушек, молодых людей, стало повседневным явлением.
В среднем в мире курит около 50% мужчин и 25%о женщин. В нашей стране курение также распространено. Ряды курильщиков пополняются в основном за счет подростков и молодежи. По данным STEPS – исследования 2016 года в Республике Беларусь средний возраст начала курения в общей выборке составил 17,5 года (16,9 года у мужчин и 19,9 года у женщин), при этом наблюдается омоложение среднего возраста начала курения: так, в возрастной группе 18-29 лет средний возраст начала курения составил 16,4 года, в группе 60-69 лет – 19,3 года. В настоящее время курят 29,6 % респондентов: среди мужчин – 48.8 %, среди женщин – 12,6 %.
Желание казаться старше, стремление подражать взрослым, любопытство способствуют тому, что подростки начинают курить. Те, кто пробует закурить или курит, не всегда задумываются над тем, к чему в конечном итоге приведет курение. Эта привычка развивается как зависимость дыхательного центра от веществ, вызывающих дополнительную его стимуляцию.
Эта привычка развивается как зависимость дыхательного центра от веществ, вызывающих дополнительную его стимуляцию.
В мире от табака ежегодно умирают 3 млн. человек, то есть от курения погибает один человек каждые 13 секунд. Курение убивает в 50 раз больше людей, чем СПИД.
ПОМНИТЕ: закурить легко, а вот отвыкнуть от курения в дальнейшем очень трудно, и вы будете рабом курения, медленно и верно уничтожая свое здоровье. Задумайтесь, пока не поздно: стоит ли начинать курить?
Роля курэння ў канцерагенэзе — УАЗ «Гродзенская Універсітэцкая клініка»
Как ни странно, самый легкий и результативный путь, который может значительно снизить заболеваемость раком,- это отказ от вредных привычек, к которым относятся курение и злоупотребление алкоголем.
Проблема распространения табачной эпидемии продолжает оставаться актуальной как во всем мире, так и в нашей республике. Это подтверждают статистические данные. В Европе 38% мужчин и 23% женщин являются курильщиками. В нашей стране ситуация еще более сложная. Так, среди белорусов курящих мужчин около 64% и 20% женщин в возрасте старше 15 лет. Ущерб и смертные случаи, связанные с табаком,- это не только статистика, это трагедия. По данным Всемирной организации здравоохранения, ежегодно во всем мире табак убивает 5 миллионов людей (11 тысяч человек каждый день!). В Белоруссии от болезней, связанных с курением, ежегодно умирают около 15,5 тысяч человек.
В нашей стране ситуация еще более сложная. Так, среди белорусов курящих мужчин около 64% и 20% женщин в возрасте старше 15 лет. Ущерб и смертные случаи, связанные с табаком,- это не только статистика, это трагедия. По данным Всемирной организации здравоохранения, ежегодно во всем мире табак убивает 5 миллионов людей (11 тысяч человек каждый день!). В Белоруссии от болезней, связанных с курением, ежегодно умирают около 15,5 тысяч человек.
На сегодняшний день потребление табака является самой серьезной и предотвратимой причиной возникновения хронических болезней, преждевременной инвалидности и смертности.
Курение — широко распространенная вредная привычка. Убедительно доказана связь табакокурения с 12 формами рака у человека. В первую очередь это рак легкого, пищевода, гортани и полости рта, большое число случаев рака мочевого пузыря, поджелудочной железы и меньшее число случаев рака почки, желудка, молочной железы, шейки матки.
Онкогенный эффект курения находится вне сомнения. В серии докладов хирургического общества Соединенных Штатов показано, что риск развития рака легкого коррелируется с количеством курящих, подсчитанным за все время использования табака, количеством сигарет, потребляемых ежегодно, входящими в сигареты смолами и никотином, глубиной дыхания при курении. Риск уменьшается с прекращением курения, но приходит к уровню риска у некурящих лишь через 10-12 лет. Эти открытия показывают, что более раннее прекращение курения является наиболее важным среди курильщиков.
В серии докладов хирургического общества Соединенных Штатов показано, что риск развития рака легкого коррелируется с количеством курящих, подсчитанным за все время использования табака, количеством сигарет, потребляемых ежегодно, входящими в сигареты смолами и никотином, глубиной дыхания при курении. Риск уменьшается с прекращением курения, но приходит к уровню риска у некурящих лишь через 10-12 лет. Эти открытия показывают, что более раннее прекращение курения является наиболее важным среди курильщиков.
Табачный дым является непосредственной причиной рака. Дым состоит из газовой фракции, несгоревших частиц и смол. В газовой фракции содержатся бензол, винилхлорид, уретан, формальдегид и другие летучие вещества. Основная часть канцерогенов находится в смолах. Диаметр твердых частиц сигаретного дыма способствует их накоплению в периферических отделах трахеи, бронхах и альвеолах. Ментол, содержащийся в некоторых сортах сигарет, расширяет сосуды бронхов, поэтому у курильщика сигарет с ментолом всасывание вредных веществ табачного дыма усиливается. Курение сигарет более опасно, чем курение сигар или трубки, так как трубочный и сигарный дым меньше вдыхается.
Курение сигарет более опасно, чем курение сигар или трубки, так как трубочный и сигарный дым меньше вдыхается.
Многочисленные канцерогены табачного дыма повреждают генетический аппарат клетки, вызывают мутации в ДНК, что и приводит к возникновению злокачественной опухоли. Табачный дым усиливает выработку иммуноглобулина Е, который подавляет иммунный ответ, разрушает натуральные антиканцерогенные вещества, поступающие в организм с пищей, такие как витамин С, бета-каротин.
Канцерогенный эффект табачного дыма резко повышается при комбинации с другими канцерогенными факторами. Так, у шахтеров радоновых рудников совместное воздействие курения и ионизирующего излучения приводит 10-кратному увеличению частоты рака легкого.
Комбинирование воздействие курения и асбеста значительно увеличивает риск рака легкого, курения и профессиональных вредностей в типографиях, нефтяной, химической, газовой, текстильной, лакокрасочной, резиновой отраслях промышленности — рака мочевого пузыря.
Общепризнанно, что риск возникновения заболевания зависит напрямую от количества выкуриваемых сигарет в день, возраста начала курения, «стажа» курения. Мы должны с горечью признать, что все причины рака имеют тенденцию к росту.
Если вы курите — остановитесь. Если же вы не можете бросить курить, то не курите в присутствии некурящих.
В последнее время у многих сложилось мнение о том, что привычки, отрицательно влияющие на здоровье человека, являются его личным делом. В какой-то мере с этим можно было бы согласиться, если бы не следующие факторы. Появляется все больше сведений о том, что так называемое пассивное или принудительное курение способствует развитию у некурящих заболеваний, свойственных курильщикам. А кто же становится пассивным курильщиком? Да все те, кому приходится находиться в обществе курильщиков, чьи ряды ширятся день ото дня. Оглянитесь вокруг, когда стоите на остановке, когда просто идете по улице, сколько человек вы насчитаете с сигаретой? Поверьте, их будет немало. Нахождение же некурящего человека в течении 8 часов в закрытом помещении, где курят, равносильно для него 5 выкуренным сигаретам. Пассивные курильщики, находящиеся в одном помещении с курящим человеком, за один час поглощают примерно 2,3 мг золы.
Нахождение же некурящего человека в течении 8 часов в закрытом помещении, где курят, равносильно для него 5 выкуренным сигаретам. Пассивные курильщики, находящиеся в одном помещении с курящим человеком, за один час поглощают примерно 2,3 мг золы.
Действие вторичного дыма обуславливает разнообразные неблагоприятные воздействия на здоровье детей, включая бронхит и пневмонию, развитие и усиление астмы, инфекционных болезней уха, которые являются частой причиной глухоты у детей. У курящих отцов и матерей дети в 4 раза чаще болеют раком, чем у некурящих родителей.
Подверженность некурящих женщин вторичному дыму в период беременности задерживает рост плода, подверженность младенцев вторичному дыму существенно увеличивает риск синдрома внезапной смерти.
Интересно отметить, что в древние времена (табак появился в Европе в XVI веке) курящих преследовали очень жестоко. На старинных английских гравюрах изображены отрубленные головы с трубками во рту. В России XVII века за курение били кнутом и «драли ноздри».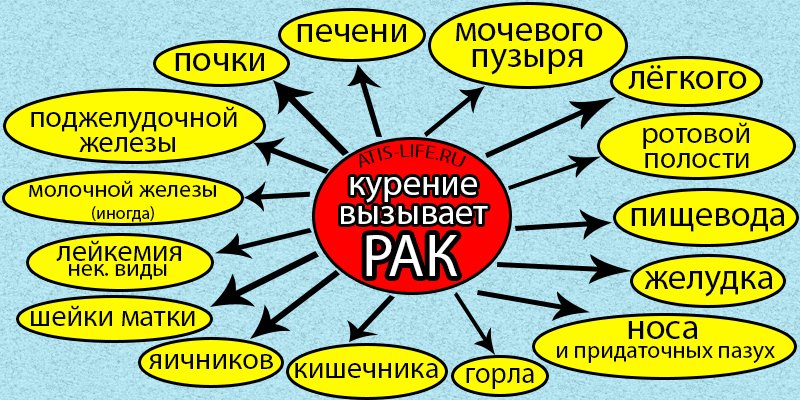 Даже сейчас в ряде стран курение в общественных местах преследуется в судебном порядке. Конечно, лучше сознательно отказаться от этой опасной привычки, но нередко определенные меры принуждения все же необходимы.
Даже сейчас в ряде стран курение в общественных местах преследуется в судебном порядке. Конечно, лучше сознательно отказаться от этой опасной привычки, но нередко определенные меры принуждения все же необходимы.
Существует индивидуальная предрасположенность к развитию рака легкого у курильщиков. У некоторых людей выявлены гены, которые определяют продукцию в повышенном количестве особых ферментов, активирующих некоторые канцерогены, содержащиеся в табачном дыме. Такие люди, начав курить, рискуют значительно быстрее заболеть раком легкого. У других людей, наоборот, имеются гены, обезвреживающие табачные канцерогены. Это объясняет, почему не все злостные курильщики заболевают раком. И рассказы о дедушке, который с детства курил крепкий самосад в огромных количествах, а умер в 100 лет от старости, могут быть правдой. Но вся проблема в том, что человек не знает, относится он к группе высокого или низкого риска.
Несомненно, существует принципиальная возможность предупредить рак.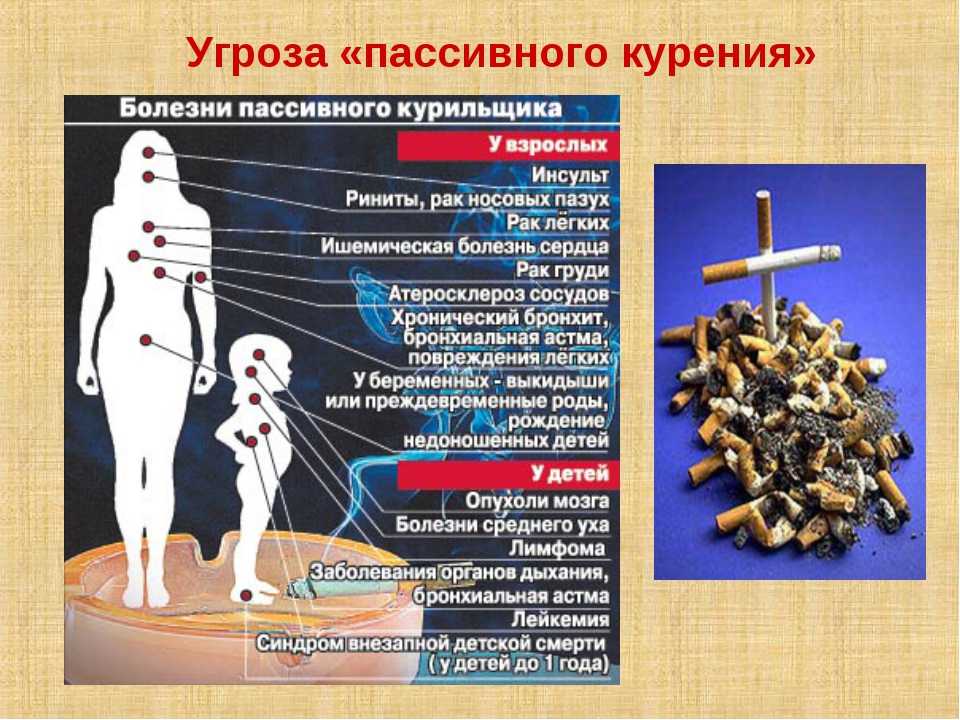 Многие показатели здоровья населения могут быть улучшены, а смертность от рака значительно снижена, если мы будем придерживаться здорового образа жизни. Борьба с курением — это борьба за здоровье не только людей, страдающих этой вредной привычкой, но и борьба за здоровье всего общества.
Многие показатели здоровья населения могут быть улучшены, а смертность от рака значительно снижена, если мы будем придерживаться здорового образа жизни. Борьба с курением — это борьба за здоровье не только людей, страдающих этой вредной привычкой, но и борьба за здоровье всего общества.
Кеда В.В. Заместитель главного врача по онкологической помощи учреждения здравоохранения «Гродненская университетская клиника»
Легочные заболевания – как табачный дым вызывает заболевания: биологическая и поведенческая основа заболеваний, связанных с курением
Аббас А.К., Лихтман А.Х., Побер Дж.С. Активация Т-лимфоцитов, клеточная и молекулярная иммунология. 4-е изд. Филадельфия: WB Сондерс; 2000а. стр. 161–81.
Аббас А.К., Лихтман А.Х., Побер Дж.С. Активация В-клеток и продукция антител, клеточная и молекулярная иммунология. 4-е изд. Филадельфия: WB Сондерс; 2000б. стр. 182–207.
Аббас А.К., Лихтман А.Х., Побер Дж.С. Врожденный иммунитет, клеточная и молекулярная иммунология. 4-е изд. Филадельфия: WB Сондерс; 2000с. стр. 270–90.
4-е изд. Филадельфия: WB Сондерс; 2000с. стр. 270–90.
Abboud RT, Fera T, Johal S, Richter A, Gibson N. Влияние курения на уровень эластазы нейтрофилов в плазме. Журнал лабораторной и клинической медицины. 1986;108(4):294–300. [PubMed: 3639117]
Abboud RT, Fera T, Richter A, Tabona MZ, Johal S. Острое влияние курения на функциональную активность ингибитора альфа-1-протеазы в бронхоальвеолярной лаважной жидкости. Американский обзор респираторных заболеваний. 1985;131(1):79–85. [PubMed: 3871315]
Abboud RT, Ofulue AF, Sansores RH, Muller NL. Связь активности активатора плазминогена и эластазы альвеолярных макрофагов с функцией легких и КТ-признаками эмфиземы. Грудь. 1998;113(5):1257–63. [PubMed: 9596303]
Адамс М.Р., Джессап В., Целермайер Д.С. Курение сигарет связано с повышенной адгезией моноцитов человека к эндотелиальным клеткам: обратимость при пероральном приеме L-аргинина, но не витамина С. Журнал Американского колледжа кардиологов. 1997;29(3):491–7. [PubMed:
1997;29(3):491–7. [PubMed:
Adams V, Nehrhoff B, Späte U, Linke A, Schulze PC, Baur A, Gielen S, Hambrecht R, Schuler G. Индукция экспрессии iNOS в скелетных мышцах путем активации IL-1β и NFκB : исследование in vitro и in vivo. Сердечно-сосудистые исследования. 2002;54(1):95–104. [PubMed: 12062366]
Adler KB, Holden-Stauffer WJ, Repine JE. Метаболиты кислорода стимулируют высвобождение высокомолекулярных гликоконъюгатов культурами клеток и органов респираторного эпителия грызунов по механизму, зависимому от арахидоновой кислоты. Журнал клинических исследований. 1990;85(1):75–85. [Бесплатная статья PMC: PMC296389] [PubMed: 2153154]
Агусти А., МакНи В., Дональдсон К., Косио М. Гипотеза: имеет ли ХОБЛ аутоиммунный компонент? грудная клетка. 2003;58(10):832–4. [Бесплатная статья PMC: PMC1746486] [PubMed: 14514931]
Alberg AJ. Влияние курения сигарет на циркулирующие концентрации антиоксидантных микронутриентов. Токсикология. 2002;180(2):121–37. [PubMed: 12324189]
Токсикология. 2002;180(2):121–37. [PubMed: 12324189]
Американский журнал респираторной и интенсивной терапии. Заявление Американского торакального общества/Европейского респираторного общества: стандарты диагностики и лечения лиц с дефицитом альфа-1-антитрипсина. Американский журнал респираторной и интенсивной терапии. 2003; 168(7):818–9.00. [PubMed: 14522813]
Американское торакальное общество. ATS публикует современный отчет по астме [пресс-релиз]. Нью-Йорк: Американское торакальное общество; Май 2000 г. [дата обращения: 13 апреля 2007 г.]. < http://www
Рабочая группа Американского торакального общества/Европейского респираторного общества. Стандарты диагностики и ведения больных ХОБЛ [Интернет]. Версия 1.2. Нью-Йорк: Американское торакальное общество; 2004. [дата обращения: 13 апреля 2007 г. ]. [обновлено 8 сентября 2005 г.]; < http://www
]. [обновлено 8 сентября 2005 г.]; < http://www
Anderson C, Kilty I, Marwick JA, MacNee W, Rahman I. Сигаретный дым и H. не за счет ингибирования киназы I-κB в клетках A549 [аннотация] Американский журнал респираторной и реаниматологической медицины. 2004;169:А424.
Andrade FH, Reid MB, Allen DG, Westerblad H. Влияние перекиси водорода и дитиотреитола на сократительную функцию отдельных волокон скелетных мышц мыши. Журнал физиологии. 1998; 509 (часть 2): 565–75. [Бесплатная статья PMC: PMC2230964] [PubMed: 9575304]
Антонисен Н.Р., Скинс М.А., Уайз Р.А., Манфреда Дж., Каннер Р.Е., Коннетт Д.Е. Исследовательская группа по изучению здоровья легких. Влияние вмешательства по прекращению курения на 14,5-летнюю смертность: рандомизированное клиническое исследование. Анналы внутренней медицины. 2005;142(4):233–9. [PubMed: 15710956]
Antonicelli F, Brown D, Parmentier M, Drost EM, Hirani N, Rahman I, Donaldson K, MacNee W. Регуляция воспаления, опосредованного LPS, in vivo и in vitro с помощью тиолового антиоксиданта Nacystelyn. Американский журнал физиологии — клеточная и молекулярная физиология легких. 2004;286(6):L1319–L1327. [PubMed: 15136298]
Регуляция воспаления, опосредованного LPS, in vivo и in vitro с помощью тиолового антиоксиданта Nacystelyn. Американский журнал физиологии — клеточная и молекулярная физиология легких. 2004;286(6):L1319–L1327. [PubMed: 15136298]
Anttila S, Hirvonen A, Vainio H, Husgafvel-Pursiainen K, Hayes JD, Ketterer B. Иммуногистохимическая локализация глутатион S -трансфераз в легких человека. Исследования рака. 1993; 53 (23): 5643–8. [PubMed: 8242618]
Aoshiba K, Koinuma M, Yokohori N, Nagai A. Иммуногистохимическая оценка окислительного стресса в легких мышей после воздействия сигаретного дыма. Ингаляционная токсикология. 2003а; 15(10):1029–38. [В паблике: 12
8]Аошиба К., Койнума М., Йокохори Н., Нагаи А. Группа по исследованию дыхательной недостаточности в Японии. Различия в распределении CD4+ и CD8+ Т-клеток в эмфизематозных легких. Дыхание. 2004;71(2):184–90. [PubMed: 15031576]
Аошиба К., Тамаоки Дж., Нагаи А. Острое воздействие сигаретного дыма вызывает апоптоз альвеолярных макрофагов. Американский журнал физиологии — клеточная и молекулярная физиология легких. 2001a; 281(6):L1392–L1401. [В паблике: 11704535]
Острое воздействие сигаретного дыма вызывает апоптоз альвеолярных макрофагов. Американский журнал физиологии — клеточная и молекулярная физиология легких. 2001a; 281(6):L1392–L1401. [В паблике: 11704535]
Аошиба К., Ясуда К., Ясуи С., Тамаоки Дж., Нагаи А. Сериновые протеазы усиливают окислительный стресс в клетках легких. Американский журнал физиологии — клеточная и молекулярная физиология легких. 2001b;281(3):L556–L564. [PubMed: 11504681]
Aoshiba K, Yokohori N, Nagai A. Апоптоз альвеолярной стенки вызывает разрушение легких и эмфизематозные изменения. Американский журнал респираторных клеток и молекулярной биологии. 2003b;28(5):555–62. [PubMed: 12707011]
Arnér ESJ, Holmgren A. Физиологические функции тиоредоксина и тиоредоксинредуктазы. Европейский журнал биохимии. 2000;267(20):6102–9. [PubMed: 11012661]
Арсалан К., Дюбуа С.М., Муанза Т., Бегин Р., Будро Ф., Асселин С., Кантин А.М. Трансформирующий фактор роста-β1 является мощным ингибитором синтеза глутатиона в эпителиальной клеточной линии легких A549: транскрипционное действие на ограничивающий скорость GSH фермент γ-глутамилцистеинсинтетазу. Американский журнал респираторных клеток и молекулярной биологии. 1997;17(5):599–607. [PubMed:
Американский журнал респираторных клеток и молекулярной биологии. 1997;17(5):599–607. [PubMed:
Astemborski JA, Beaty TH, Cohen BH. Анализ компонентов дисперсии форсированного выдоха в семьях. Американский журнал медицинской генетики. 1985;21(4):741–53. [PubMed: 4025399]
Аткинсон Дж. Дж., Холмбек К., Ямада С., Биркедал-Хансен Х., Parks WC, Senior RM. Матриксная металлопротеиназа мембранного типа 1 необходима для нормального развития альвеол. Динамика развития. 2005;232(4):1079–90. [PubMed: 15739229]
Баарендс Э.М., Шолс А.М., Мостерт Р., Воутерс Э.Ф. Пиковая реакция на физическую нагрузку в связи с истощением тканей у пациентов с хронической обструктивной болезнью легких. Европейский респираторный журнал. 1997;10(12):2807–13. [PubMed: 94
Балинт Б., Доннелли Л.Е., Ханадзава Т., Харитонов С.А., Барнс П.Дж. Увеличение метаболитов оксида азота в конденсате выдыхаемого воздуха после воздействия табачного дыма. грудная клетка. 2001;56(6):456–61. [Бесплатная статья PMC: PMC1746081] [PubMed: 11359961]
грудная клетка. 2001;56(6):456–61. [Бесплатная статья PMC: PMC1746081] [PubMed: 11359961]
Баранова Х., Перрио Ж., Альбюссон Э., Иващенко Т., Баранова В.С., Хемери Б., Мурэр П., Риоль Н., Мале П. Особенности генотипа GSTM1 0/0 у заядлых курильщиков Франции с различными типами хронического бронхита. Генетика человека. 1997; 99(6):822–6. [PubMed:
80]Barberà JA, Peinado VI, Santos S. Легочная гипертензия при хронической обструктивной болезни легких. Европейский респираторный журнал. 2003;21(5):892–905. [PubMed: 12765440]
Barclay JK, Hansel M. Свободные радикалы могут способствовать окислительной усталости скелетных мышц. Канадский журнал физиологии и фармакологии. 1991;69(2):279–84. [PubMed: 2054745]
Барнс П.Дж. Альвеолярные макрофаги как организаторы ХОБЛ. ХОБЛ. 2004а; 1(1):59–70. [PubMed: 16997739]
Барнс П.Дж. Медиаторы хронической обструктивной болезни легких. Фармакологические обзоры. 2004b;56(4):515–48. [PubMed: 15602009]
2004b;56(4):515–48. [PubMed: 15602009]
Барнс П.Дж., Шапиро С.Д., Пауэлс Р.А. Хроническая обструктивная болезнь легких: молекулярные и клеточные механизмы. Европейский респираторный журнал. 2003;22(4):672–88. [В паблике: 14582923]
Баст А., Хэнен Г.Р., Доелман С.Дж. Оксиданты и антиоксиданты: современное состояние. Американский журнал медицины. 1991;91(3C):2S–13S. [PubMed: 17]
Beatty K, Bieth J, Travis J. Кинетика ассоциации сериновых протеиназ с нативным и окисленным ингибитором α-1-протеиназы и α-1-антихимотрипсином. Журнал биологической химии. 1980;255(9):3931–4. [PubMed: 6989830]
Беккер К., Гуй М., Ширмер Р.Х. Ингибирование глутатионредуктазы человека S -нитрозоглутатион. Европейский журнал биохимии. 1995;234(2):472–8. [PubMed: 8536691]
Беккер С., Соукуп Дж.М., Гилмор М.И., Девлин Р.Б. Стимуляция альвеолярных макрофагов человека и крыс частицами городского воздуха: влияние на образование окислительных радикалов и продукцию цитокинов. Токсикология и прикладная фармакология. 1996;141(2):637–48. [PubMed: 8975789]
Токсикология и прикладная фармакология. 1996;141(2):637–48. [PubMed: 8975789]
Beckman JS, Koppenol WH. Оксид азота, супероксид и пероксинитрит: хорошие, плохие и уродливые. Американский журнал физиологии — клеточная физиология. 1996; 271 (5 ч. 1): C1424–C1437. [PubMed: 8944624]
Бехзад А.Р., Чу Ф., Уокер, округ Колумбия. Фибробласты способны предоставлять информацию о направлении миграции нейтрофилов во время пневмонии в легких кролика. Микрососудистые исследования. 1996;51(3):303–16. [PubMed: 89
Benetazzo MG, Gilè LS, Bombieri C, Malerba G, Massobrio M, Pignatti PF, Luisetti M. Полиморфизм α 1 -антитрипсин TAQ I и мутация α 1 -антихимотрипсин обструктивная болезнь легких. Респираторная медицина. 1999;93(9):648–54. [PubMed: 10542979]
Bernstein D. Обзор влияния размера частиц, объема затяжки и характера вдыхания на осаждение частиц сигаретного дыма в дыхательных путях. Ингаляционная токсикология. 2004;16(10):675–89. [PubMed: 15371056]
2004;16(10):675–89. [PubMed: 15371056]
Betsuyaku T, Nishimura M, Takeyabu K, Tanino M, Venge P, Xu S, Kawakami Y. Белки нейтрофильных гранул в жидкости бронхоальвеолярного лаважа у субъектов с субклинической эмфиземой. Американский журнал респираторной и интенсивной терапии. 1999;159(6):1985–91. [PubMed: 10351949]
Бетсуяку Т., Нисимура М., Йошиока А., Такеябу К., Миямото К., Каваками Ю. Пептиды, полученные из эластина, и нейтрофильная эластаза в жидкости бронхоальвеолярного лаважа. Американский журнал респираторной и интенсивной терапии. 1996; 154 (3 часть 1): 720–4. [PubMed: 8810611]
Betsuyaku T, Takeyabu K, Tanino M, Nishimura M. Роль ингибитора секреторной лейкоцитарной протеазы в развитии субклинической эмфиземы. Европейский респираторный журнал. 2002;19(6): 1051–107. [PubMed: 12108856]
Бетсуяку Т., Танино М., Нагаи К., Насухара Ю., Нисимура М., старший РМ. Уровень индуктора металлопротеиназы внеклеточного матрикса увеличивается в жидкости бронхоальвеолярного лаважа у курильщиков. Американский журнал респираторной и интенсивной терапии. 2003;168(2):222–7. [PubMed: 12714350]
Американский журнал респираторной и интенсивной терапии. 2003;168(2):222–7. [PubMed: 12714350]
Бетсуяку Т., Йошиока А., Нисимура М., Миямото К., Кондо Т., Каваками Ю. Нейтрофильная эластаза, связанная с альвеолярными макрофагами у пожилых добровольцев. Американский журнал респираторной и интенсивной терапии. 1995;151(2 ч. 1):436–42. [PubMed: 7842203]
Бит Дж.Г. Антиэластазный экран нижних дыхательных путей. Приложение к Европейскому журналу респираторных заболеваний. 1985; 139: 57–61. [PubMed: 3876235]
Bilimoria MH, Ecobichon DJ. Защитные антиоксидантные механизмы в тканях крыс и морских свинок при остром воздействии сигаретного дыма. Токсикология. 1992;72(2):131–44. [PubMed: 1566276]
Black LF, Kueppers F. Дефицит α1-антитрипсина у некурящих. Американский обзор респираторных заболеваний. 1978;117(3):421–8. [PubMed: 305219]
Boschetto P, Miniati M, Miotto D, Braccioni F, De Rosa E, Bononi I, Papi A, Saetta M, Fabbri LM, Mapp CE. Преобладающий фенотип эмфиземы у больных хронической обструктивной болезнью легких. Европейский респираторный журнал. 2003;21(3):450–4. [PubMed: 12662000]
Преобладающий фенотип эмфиземы у больных хронической обструктивной болезнью легких. Европейский респираторный журнал. 2003;21(3):450–4. [PubMed: 12662000]
Bosken CH, Hards J, Gatter K, Hogg JC. Характеристика воспалительной реакции в периферических дыхательных путях курильщиков с помощью иммуноцитохимии. Американский обзор респираторных заболеваний. 1992;145( 4 Пт 1):911–7. [PubMed: 1554220]
Боулер Р.П., Барнс П.Дж., Крапо Д.Д. Роль оксидативного стресса в развитии хронической обструктивной болезни легких. ХОБЛ. 2004;1(2):255–77. [PubMed: 17136992]
Брантли М., Нукива Т., Кристал Р.Г. Молекулярная основа дефицита альфа-1-антитрипсина. Американский журнал медицины. 1988; 84 (Приложение 6A): 13–31. [PubMed: 3289385]
Брейер Р., Кристенсен Т.Г., Люси Э.К., Болбочан Г., Стоун П.Дж., Снайдер Г.Л. Эластаза вызывает секреторное отделяемое в бронхах хомяков с индуцированной эластазой метаплазией секреторных клеток. Экспериментальное исследование легких.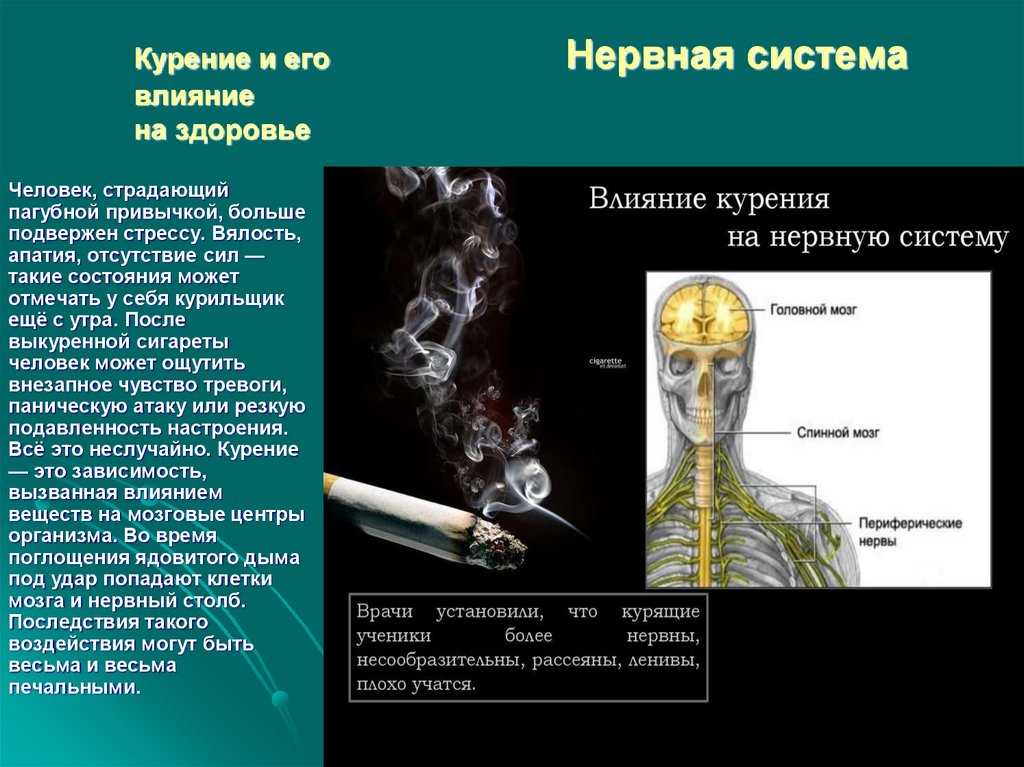 1993;19(2):273–82. [PubMed: 8467766]
1993;19(2):273–82. [PubMed: 8467766]
Bridgeman MME, Marsden M, Drost E, Selby C, Ryle AP, Donaldson K, MacNee W. Влияние сигаретного дыма на клетки легких [аннотация] American Review of Respiratory Disease. 1991;143:A737.
БМЖ. Стандартизированные анкеты [так в оригинале] по респираторным симптомам. BMJ (Британский медицинский журнал). 1965; 2(5213):1665.
Buck M, Chojkier M. Атрофию мышц и дедифференцировку, вызванную окислительным стрессом в мышиной модели кахексии, предотвращают ингибиторы синтеза оксида азота и антиоксиданты. Журнал ЭМБО. 1996;15(8):1753–65. [Бесплатная статья PMC: PMC450091] [PubMed: 8617220]
Burgel PR, Escudier E, Coste A, Dao-Pick T, Ueki IF, Takeyama K, Shim JJ, Murr AH, Nadel JA. Связь экспрессии рецептора эпидермального фактора роста с гиперплазией бокаловидных клеток в полипах носа. Журнал аллергии и клинической иммунологии. 2000;106(4):705–12. [PubMed: 11031341]
Бернс А. Р., Смит К.В., Уокер, округ Колумбия. Уникальные структурные особенности, влияющие на эмиграцию нейтрофилов в легкие. Физиологические обзоры. 2003;83(2):309–36. [PubMed: 12663861]
Р., Смит К.В., Уокер, округ Колумбия. Уникальные структурные особенности, влияющие на эмиграцию нейтрофилов в легкие. Физиологические обзоры. 2003;83(2):309–36. [PubMed: 12663861]
Бузату Л., Чу Ф., Джавадифард А., Эллиот В.М., Ли В., Черньяк Р.М., Роджерс Р.М., Шурба Ф.К., Коксон Х.О., Паре П.Д., Хогг Д.К. Накопление дендритных и натуральных киллеров в мелких дыхательных путях при различной степени тяжести ХОБЛ. Труды Американского торакального общества. 2005;2:А135.
Байт Британская Колумбия, Биллингсли Г.Д., Кокс Д.В. Физическое и генетическое картирование кластера генов серпина в 14q32.1: аллельная ассоциация и уникальный гаплотип, связанные с дефицитом альфа-1-антитрипсина. Американский журнал генетики человека. 1994;55(1):126–33. [Статья бесплатно PMC: PMC1
Calabrese F, Giacometti C, Beghe B, Rea F, Loy M, Zuin R, Marulli G, Baraldo S, Saetta M, Valente M. Выраженный альвеолярный апоптоз/ Дисбаланс пролиферации при терминальной стадии эмфиземы. Дыхательные исследования. 2005;6(1):14. [Бесплатная статья PMC: PMC549521] [PubMed: 15705190]
Дыхательные исследования. 2005;6(1):14. [Бесплатная статья PMC: PMC549521] [PubMed: 15705190]
Cantin A, Crystal RG. Оксиданты, антиоксиданты и патогенез эмфиземы легких. Приложение к Европейскому журналу респираторных заболеваний. 1985;139:7–17. [PubMed: 2995106]
Cantin AM, North SL, Hubbard RC, Crystal RG. Нормальная жидкость, выстилающая альвеолярный эпителий, содержит высокий уровень глутатиона. Журнал прикладной физиологии. 1987; 63 (1): 152–7. [PubMed: 3040659]
Кантрелл Э.Т., Уорр Г.А., Басби Д.Л., Мартин Р.Р. Индукция арилуглеводородгидроксилазы в легочных альвеолярных макрофагах человека при курении сигарет. Журнал клинических исследований. 1973; 52 (8): 1881–184. [Бесплатная статья PMC: PMC302469] [PubMed: 4124207]
Карневали С., Петруцелли С., Лонгони Б., Ванакор Р., Барале Р., Чиполлини М., Скатена Ф., Паджаро П., Чели А., Джунтини С. Экстракт сигаретного дыма вызывает окислительный стресс и апоптоз у человека фибробласты легких. Американский журнал физиологии — клеточная и молекулярная физиология легких. 2003; 284(6):L955–L963. [PubMed: 12547733]
Американский журнал физиологии — клеточная и молекулярная физиология легких. 2003; 284(6):L955–L963. [PubMed: 12547733]
Картер А.Б., Тефли Л.А., Венкатараман С., Оберли Л.В., Чжан И., Бюттнер Г.Р., Шпиц Д.Р., Ханнингхейк Г.В. Высокие уровни активности каталазы и глутатионпероксидазы ослабляют H 2 O 2 передача сигналов в альвеолярных макрофагах человека. Американский журнал респираторных клеток и молекулярной биологии. 2004;31(1):43–53. [PubMed: 14962975]
Cavarra E, Bartalesi B, Lucattelli M, Fineschi S, Lunghi B, Gambelli F, Ortiz LA, Martorana PA, Lungarella G. Влияние сигаретного дыма на мышей с различными уровнями α 1 -ингибитор протеиназ и чувствительность к оксидантам. Американский журнал респираторной и интенсивной терапии. 2001а; 164(5):886–9.0. [PubMed: 11549550]
Cavarra E, Lucattelli M, Gambelli F, Bartalesi B, Fineschi S, Szarka A, Giannerini F, Martorana PA, Lungarella G. Инактивация SLPI человека после воздействия сигаретного дыма в новом эксперименте in vivo Модель легочного окислительного стресса. Американский журнал физиологии — клеточная и молекулярная физиология легких. 2001b;281(2):L412–L417. [PubMed: 11435216]
Американский журнал физиологии — клеточная и молекулярная физиология легких. 2001b;281(2):L412–L417. [PubMed: 11435216]
Celedón JC, Lange C, Raby BA, Litonjua AA, Palmer LJ, DeMeo DL, Reilly JJ, Kwiatkowski DJ, Chapman HA, Laird N, et al. Ген трансформирующего фактора роста-β1 (TGFB1) связан с хронической обструктивной болезнью легких (ХОБЛ). Молекулярная генетика человека. 2004;13(15):1649–56. [PubMed: 15175276]
Центры по контролю и профилактике заболеваний. Годовая смертность, относимая на счет курения, потерянные годы потенциальной жизни и потери производительности — США, 1997–2001 гг. Еженедельный отчет о заболеваемости и смертности. 2005;54(25):625–8. [PubMed: 15988406]
Чемберс, округ Колумбия, Танниклифф В.С., Эйрес Дж.Г. Острое вдыхание сигаретного дыма увеличивает концентрацию оксида азота в нижних дыхательных путях. грудная клетка. 1998;53(8):677–9. [Бесплатная статья PMC: PMC1745302] [PubMed: 9828855]
Chance B, Sies H, Boveris A. Метаболизм гидроперекисей в органах млекопитающих. Физиологические обзоры. 1979; 59 (3): 527–605. [PubMed: 37532]
Метаболизм гидроперекисей в органах млекопитающих. Физиологические обзоры. 1979; 59 (3): 527–605. [PubMed: 37532]
Chan-Yeung M, Abboud R, Buncio AD, Vedal S. Количество лейкоцитов на периферии и продольное снижение функции легких. грудная клетка. 1988;43(6):462–6. [Статья бесплатно PMC: PMC461311] [PubMed: 3420557]
Чой А.М., Алам Дж. Гемоксигеназа-1: функция, регуляция и роль нового белка, индуцируемого стрессом, в окислительно-индуцированном повреждении легких. Американский журнал респираторных клеток и молекулярной биологии. 1996;15(1):9–19. [PubMed: 8679227]
Church DF, Pryor WA. Свободнорадикальная химия сигаретного дыма и ее токсикологические последствия. Перспективы гигиены окружающей среды. 1985; 64: 111–26. [Бесплатная статья PMC: PMC1568603] [PubMed: 3007083]
Чарг А., Дай Дж., Тай Х., Се С., Райт Дж.Л. Фактор некроза опухоли-α играет центральную роль в остром воспалении, вызванном сигаретным дымом, и разрушении соединительной ткани. Американский журнал респираторной и интенсивной терапии. 2002;166(6):849–54. [PubMed: 12231496]
Американский журнал респираторной и интенсивной терапии. 2002;166(6):849–54. [PubMed: 12231496]
Чарг А., Ван Р.Д., Тай Х., Ван Х., Се С., Райт Дж.Л. Фактор некроза опухоли-α вызывает 70% эмфиземы, вызванной сигаретным дымом, у мышей. Американский журнал респираторной и интенсивной терапии. 2004;170(5):492–8. [PubMed: 15184206]
Чарг А., Ван Р.Д., Се С., Райт Дж.Л. α1-антитрипсин облегчает эмфизему, вызванную сигаретным дымом, у мышей. Американский журнал респираторной и интенсивной терапии. 2003;168(2):199–207. [В паблике: 12689849]
Чарг А., Райт Д.Л. Протеазы и эмфизема. Современное мнение в области легочной медицины. 2005;11(2):153–9. [PubMed: 15699789]
Кларк РАФ. Ремонт раны. Молекулярная и клеточная биология заживления ран. 2-е изд. Кларк РАФ, редактор. Нью-Йорк: Пленум Пресс; 1996. С. 3–50.
Clark AG, Debnam P. Ингибирование глутатиона S -трансфераз из печени крыс с помощью S -нитрозо- L -глутатиона. Биохимическая фармакология. 1988;37(16):3199–201. [PubMed: 3401252]
Биохимическая фармакология. 1988;37(16):3199–201. [PubMed: 3401252]
Clark-Lewis I, Mattioli I, Gong JH, Loetscher P. Структурно-функциональные отношения между рецептором хемокинов человека CXCR3 и его лигандами. Журнал биологической химии. 2003;278(1):289–95. [PubMed: 12417585]
Clini E, Bianchi L, Pagani M, Ambrosino N. Эндогенный оксид азота у пациентов со стабильной ХОБЛ: коррелирует с тяжестью заболевания. грудная клетка. 1998;53(10):881–3. [Бесплатная статья PMC: PMC1745093] [PubMed: 101
- ]
Коэн Д., Араи С.Ф., Брэйн Д.Д. Курение ухудшает долговременную очистку легких от пыли. Наука. 1979; 204 (4392): 514–7. [PubMed: 432655]
Comhair SAA, Bhathena PR, Farver C, Thunnissen FBJM, Erzurum SC. Индукция внеклеточной глутатионпероксидазы в астматических легких: свидетельство окислительно-восстановительной регуляции экспрессии в эпителиальных клетках дыхательных путей человека. Журнал ФАСЭБ. 2001;15(1):70–8. [PubMed: 11149894]
Коннер Э. М., Гришам М.Б. Воспаление, свободные радикалы и антиоксиданты. Питание. 1996;12(4):274–7. [PubMed: 8862535]
М., Гришам М.Б. Воспаление, свободные радикалы и антиоксиданты. Питание. 1996;12(4):274–7. [PubMed: 8862535]
Conway EM, Collen D, Carmeliet P. Молекулярные механизмы роста кровеносных сосудов. Сердечно-сосудистые исследования. 2001;49(3):507–21. [PubMed: 11166264]
Кук CL. Инфекции верхних и нижних дыхательных путей. Учебник диагностической микробиологии. 2-е изд. Mahon CR, Manuselis G, редакторы. Филадельфия: WB Сондерс; 2000. стр. 878–917.
Корради М., Монтуши П., Доннелли Л.Е., Пеши А., Харитонов С.А., Барнс П.Дж. Повышение содержания нитрозотиолов в конденсате выдыхаемого воздуха при воспалительных заболеваниях дыхательных путей. Американский журнал респираторной и интенсивной терапии. 2001;163(4):854–8. [В паблике: 11282756]
Корради М., Рубинштейн И., Андреоли Р., Манини П., Кальери А., Поли Д., Алинови Р., Мутти А. Альдегиды в выдыхаемом конденсате пациентов с хронической обструктивной болезнью легких. Американский журнал респираторной и интенсивной терапии. 2003;167(10):1380–6. [PubMed: 12522029]
2003;167(10):1380–6. [PubMed: 12522029]
Cosio MG, Majo J, Cosio MG. Воспаление дыхательных путей и паренхимы легких при ХОБЛ: роль Т-клеток. Грудь. 2002; 121 (5 Дополнение): 160S–165S. [PubMed: 12010846]
Cotgreave IA, Johansson U, Moldeus P, Brattsand R. Влияние острого вдыхания сигаретного дыма на легочные и системные окислительно-восстановительные состояния цистеина и глутатиона у крыс. Токсикология. 1987;45(2):203–12. [PubMed: 3603585]
Couillard A, Koechlin C, Cristol JP, Varray A, Prefaut C. Доказательства местного системного окислительного стресса, вызванного физическими упражнениями, у пациентов с хронической обструктивной болезнью легких. Европейский респираторный журнал. 2002;20(5):1123–9. [В паблике: 12449164]
Couillard A, Maltais F, Saey D, Debigare R, Michaud A, Koechlin C, LeBlanc P, Prefant C. Вызванный физическими упражнениями окислительный стресс четырехглавой мышцы и дисфункция периферических мышц у пациентов с хронической обструктивной болезнью легких. Американский журнал респираторной и интенсивной терапии. 2003; 167 (12): 1664–9. [PubMed: 12672647]
Американский журнал респираторной и интенсивной терапии. 2003; 167 (12): 1664–9. [PubMed: 12672647]
Cross CE, Halliwell B, Allen A. Антиоксидантная защита: функция трахеобронхиальной и желудочно-кишечной слизи. Ланцет. 1984;323(8390):1328–30. [PubMed: 6145029]
Cross CE, van der Vliet A, Eiserich JP, Wong J, Halliwell B. Окислительный стресс и антиоксиданты в жидкостях, выстилающих дыхательные пути. Кислород, экспрессия генов и клеточная функция. Clerch LB, Massaro DJ, редакторы. Нью-Йорк: Марсель Деккер; 1997. С. 367–98.
Кросс К.Я., Мустой Т.А. Факторы роста при заживлении ран. Хирургические клиники Северной Америки. 2003;83(3):531–45. [PubMed: 12822724]
Кроутер А.Дж., Рахман И., Антоничелли Ф., Хименес Л.А., Солтер Д., МакНи В. Окислительный стресс и факторы транскрипции AP-1 и NF-κB в легочной ткани человека [аннотация] American Journal of Respiratory и реаниматология. 1999;159:А816.
Кертис Дж. Л., Фримен К.М., Хогг Дж.К. Иммунопатогенез хронической обструктивной болезни легких: выводы из недавних исследований. Труды Американского торакального общества. 2007;4(7):512–21. [Статья бесплатно PMC: PMC2365762] [PubMed: 17878463]
Л., Фримен К.М., Хогг Дж.К. Иммунопатогенез хронической обструктивной болезни легких: выводы из недавних исследований. Труды Американского торакального общества. 2007;4(7):512–21. [Статья бесплатно PMC: PMC2365762] [PubMed: 17878463]
Д’Армьенто Дж., Далал С.С., Окада Й., Берг Р.А., Чада К. Экспрессия коллагеназы в легких трансгенных мышей вызывает эмфизему легких. Клетка. 1992;71(6):955–61. [PubMed: 1458541]
Дэвис К.Дж. Окислительный стресс: парадокс аэробной жизни. Симпозиум биохимического общества. 1995; 61:1–31. [PubMed: 8660387]
де Серрес Ф.Дж. Расовое и этническое распространение дефицита α 1 -антитрипсина во всем мире: резюме анализа опубликованных генетических эпидемиологических исследований. Грудь. 2002; 122(5):1818–29. [PubMed: 12426287]
Dekhuijzen PN, Aben KK, Dekker I, Aarts LP, Wielders PL, van Herwaarden CL, Bast A. Повышенное выдыхание перекиси водорода у пациентов со стабильной и нестабильной хронической обструктивной болезнью легких. Американский журнал респираторной и интенсивной терапии. 1996; 154 (3 часть 1): 813–6. [PubMed: 8810624]
Американский журнал респираторной и интенсивной терапии. 1996; 154 (3 часть 1): 813–6. [PubMed: 8810624]
Делен Ф.М., Сиппель Дж.М., Осборн М.Л., Лоу С., Туккани Н., Холден В.Е. Повышение выдыхаемого оксида азота при хроническом бронхите: сравнение с астмой и ХОБЛ. Грудь. 2000;117(3):695–701. [PubMed: 10712993]
DeMeo DL, Celedon JC, Lange C, Reilly JJ, Chapman MA, Sylvia JS, Speizer FE, Weiss ST, Silverman EK. Полногеномная связь форсированного потока в середине выдоха при хронической обструктивной болезни легких. Американский журнал респираторной и интенсивной терапии. 2004;170(12):1294–301. [PubMed: 15347563]
Денеке С.М., Фанбург Б.Л. Регуляция клеточного глутатиона. Американский журнал физиологии. 1989; 257 (4 части 1): L163–L173. [PubMed: 2572174]
Di Francia M, Barbier D, Mege JL, Orehek J. Уровень фактора некроза опухоли-альфа и потеря веса при хронической обструктивной болезни легких. Американский журнал респираторной и интенсивной терапии. 1994; 150 (5 часть 1): 1453–1455. [PubMed: 7952575]
1994; 150 (5 часть 1): 1453–1455. [PubMed: 7952575]
Ди Стефано А., Карамори Г., Оутс Т., Капелли А., Лусуарди М., Гнемми И., Иоли Ф., Чанг К.Ф., Доннер С.Ф., Барнс П.Дж. и др. Повышенная экспрессия ядерного фактора-κB в биоптатах бронхов курильщиков и больных ХОБЛ. Европейский респираторный журнал. 2002;20(3):556–63. [В паблике: 12358328]
Ди Стефано А., Карамори Г., Риччардоло Флорида, Капелли А., Адкок И.М., Доннер С.Ф. Клеточные и молекулярные механизмы хронической обструктивной болезни легких: обзор. Клиническая и экспериментальная аллергия. 2004;34(8):1156–67. [PubMed: 15298554]
Di Stefano A, Turato G, Maestrelli P, Mapp CE, Ruggieri MP, Roggeri A, Boschetto P, Fabbri LM, Saetta M. Ограничение воздушного потока при хроническом бронхите связано с Т-лимфоцитами и макрофагами инфильтрация слизистой бронхов. Американский журнал респираторной и интенсивной терапии. 1996;153(2):629–32. [PubMed: 8564109]
Doelman CJ, Bast A. Кислородные радикалы в патологии легких. Свободнорадикальная биология и медицина. 1990;9(5):381–400. [PubMed: 1705530]
Кислородные радикалы в патологии легких. Свободнорадикальная биология и медицина. 1990;9(5):381–400. [PubMed: 1705530]
Дональдсон Г.К., Симунгал Т.А., Бховмик А., Ведзича Дж.А. Взаимосвязь между частотой обострений и снижением функции легких при хронической обструктивной болезни легких. грудная клетка. 2002;57(10):847–52. [Бесплатная статья PMC: PMC1746193] [PubMed: 12324669]
Дранник А.Г., Пулади М.А., Роббинс С.С., Гончарова С.И., Кианпур С., Стампфли М.Р. Влияние сигаретного дыма на клиренс и воспаление после 9 лет.0074 Инфекция Pseudomonas aeruginosa . Американский журнал респираторной и интенсивной терапии. 2004;170(11):1164–71. [PubMed: 15317669]
Drost EM, Selby C, Bridgeman MM, MacNee W. Снижение деформируемости лейкоцитов после острого курения сигарет у людей. Американский обзор респираторных заболеваний. 1993;148(5):1277–83. [PubMed: 8239165]
Drost EM, Selby C, Lannan S, Lowe GD, MacNee W. Изменения деформируемости нейтрофилов после воздействия дыма in vitro: механизм и защита. Американский журнал респираторных клеток и молекулярной биологии. 1992;6(3):287–95. [PubMed: 1311595]
Американский журнал респираторных клеток и молекулярной биологии. 1992;6(3):287–95. [PubMed: 1311595]
Dunnill MS. Эмфизема. Легочная патология. Даннилл М.С., редактор. Нью-Йорк: Черчилль Ливингстон; 1982. С. 81–112.
Ид А.А., Ионеску А.А., Никсон Л.С., Льюис-Дженкинс В., Мэтьюз С.Б., Гриффитс Т.Л., Шейл Д.Дж. Воспалительная реакция и состав тела при хронической обструктивной болезни легких. Американский журнал респираторной и интенсивной терапии. 2001; 164 (8 ч. 1): 1414–8. [PubMed: 11704588]
Эйзерих Дж. П., ван дер Влит А., Хандельман Г. Дж., Холливелл Б., Кросс К. Э. Пищевые антиоксиданты и биомолекулярные повреждения, вызванные сигаретным дымом: сложное взаимодействие. Американский журнал клинического питания. 1995;62(6 Дополнение):1490S–1500S. [PubMed: 7495250]
Экберг-Янссон А., Бэйк Б., Андерссон Б., Скух Б.Е., Лофдал К.Г. Респираторные симптомы связаны с физиологическими изменениями и воспалительными маркерами, отражающими центральные, но не периферические дыхательные пути: исследование 60-летних «здоровых» курильщиков и никогда не куривших. Респираторная медицина. 2001;95(1):40–7. [PubMed: 11207016]
Респираторная медицина. 2001;95(1):40–7. [PubMed: 11207016]
Engelen MP, Schols AM, Does JD, Deutz NE, Wouters EF. Измененный метаболизм глутамата связан со снижением уровня глутатиона в мышцах у пациентов с эмфиземой. Американский журнал респираторной и интенсивной терапии. 2000а; 161(1):98–103. [PubMed: 10619804]
Engelen MP, Schols AM, Does JD, Wouters EF. Слабость скелетных мышц связана с потерей безжировой массы конечностей, но не с обструкцией дыхательных путей у пациентов с хронической обструктивной болезнью легких. Американский журнал клинического питания. 2000b;71(3):733–8. [PubMed: 10702166]
Эрикссон С. Исследования дефицита α 1 -антитрипсина. Acta Medica Scandinavica Supplementum. 1965; 432:1–85. [В паблике: 4160491]
Evans MD, Pryor WA. Повреждение ингибитора α-1-протеиназы человека водными экстрактами сигаретной смолы и образованием метионинсульфоксида. Химические исследования в токсикологии. 1992;5(5):654–60. [PubMed: 1446005]
1992;5(5):654–60. [PubMed: 1446005]
Фарук М.О., Хан М.Р., Рахман М.М., Ахмед Ф. Связь между курением и антиоксидантным статусом питания. Британский журнал питания. 1995;73(4):625–32. [PubMed: 7794877]
Фельдман С., Андерсон Р., Кантакумар К., Варгас А., Коул П.Дж., Уилсон Р. Окислительно-опосредованная цилиарная дисфункция в респираторном эпителии человека. Свободнорадикальная биология и медицина. 1994;17(1):1–10. [PubMed: 7959161]
Ferrarotti I, Zorzetto M, Beccaria M, Gile LS, Porta R, Ambrosino N, Pignatti PF, Cerveri I, Pozzi E, Luisetti M. Гены семейства факторов некроза опухоли в фенотипе связанной с ХОБЛ с эмфиземой. Европейский респираторный журнал. 2003;21(3):444–9. [PubMed: 12661999]
Финкельштейн Р., Фрейзер Р.С., Геццо Х., Козио М.Г. Альвеолярное воспаление и его связь с эмфиземой у курильщиков. Американский журнал респираторной и интенсивной терапии. 1995; 152 (5 ч. 1): 1666–72. [PubMed: 7582312]
Finlay GA, O’Donnell MD, O’Connor CM, Hayes JP, FitzGerald MX. Ремоделирование эластина и коллагена при эмфиземе: исследование с помощью сканирующей электронной микроскопии. Американский журнал патологии. 1996;149(4):1405–15. [Бесплатная статья PMC: PMC1865175] [PubMed: 8863687]
Ремоделирование эластина и коллагена при эмфиземе: исследование с помощью сканирующей электронной микроскопии. Американский журнал патологии. 1996;149(4):1405–15. [Бесплатная статья PMC: PMC1865175] [PubMed: 8863687]
Финли Г.А., О’Дрисколл Л.Р., Рассел К.Дж., Д’Арси Э.М., Мастерсон Дж.Б., Фитцджеральд М.Х., О’Коннор К.М. Экспрессия и продукция матриксных металлопротеиназ альвеолярными макрофагами при эмфиземе. Американский журнал респираторной и интенсивной терапии. 1997а; 156(1):240–7. [PubMed:
Финлей Г.А., Рассел К.Дж., МакМахон К.Дж., Д’Арси Э.М., Мастерсон Д.Б., Фитцджеральд М.Х., О’Коннор К.М. Повышенные уровни матриксных металлопротеиназ в жидкости бронхоальвеолярного лаважа больных эмфизематозом. грудная клетка. 1997б;52(6):502–6. [Бесплатная статья PMC: PMC1758576] [PubMed:
14]
Флетчер К.М., Пето Р., Тинкер С., Спейзер Ф.Е.
Нью-Йорк:
Издательство Оксфордского университета; Естественная история хронического бронхита и эмфиземы: восьмилетнее исследование ранней хронической обструктивной болезни легких у рабочих в Лондоне. 1976
1976
Foronjy R, D’Armiento J. Роль коллагеназы в эмфиземе. Дыхательные исследования. 2001;2(6):348–52. [Бесплатная статья PMC: PMC64802] [PubMed: 11737934]
Форонжи Р.Ф., Мирочниченко О., Пропокенко О., Леметр В., Цзя И., Иноуе М., Окада Ю., Д’Армьенто Д.М. Экспрессия супероксиддисмутазы ослабляет эмфизему, вызванную сигаретным дымом или эластазой, у мышей. Американский журнал респираторной и интенсивной терапии. 2006;173(6):623–31. [Бесплатная статья PMC: PMC3982860] [PubMed: 16387805]
Foronjy RF, Okada Y, Cole R, D’Armiento J. Прогрессирующая эмфизема у взрослых у трансгенных мышей, экспрессирующих MMP-1 человека в легких. Американский журнал физиологии — клеточная и молекулярная физиология легких. 2003; 284(5):L727–L737. [PubMed: 12676763]
Франко А.А., Одом Р.С., Рандо Т.А. Регуляция экспрессии генов антиоксидантных ферментов в ответ на окислительный стресс и во время дифференцировки скелетных мышц мышей. Свободнорадикальная биология и медицина. 1999;27(9–10):1122–32. [PubMed: 10569645]
Свободнорадикальная биология и медицина. 1999;27(9–10):1122–32. [PubMed: 10569645]
Freedman ML, Reich D, Penney KL, McDonald GJ, Mignault AA, Patterson N, Gabriel SB, Topol EJ, Smoller JW, Pato CN, et al. Оценка влияния стратификации населения на исследования генетических ассоциаций. Генетика природы. 2004;36(4):388–93. [PubMed: 15052270]
Фридлендер А.Л., Линч Д., Дьяр Л.А., Боулер Р.П. Фенотипы хронической обструктивной болезни легких. ХОБЛ. 2007;4(4):301–2. [PubMed: 18027155]
Fujii T, Hayashi S, Hogg JC, Mukae H, Suwa T, Goto Y, Vincent R, van Eeden SF. Взаимодействие альвеолярных макрофагов и эпителиальных клеток дыхательных путей после воздействия твердых частиц приводит к образованию медиаторов, которые стимулируют костный мозг. Американский журнал респираторных клеток и молекулярной биологии. 2002;27(1):34–41. [PubMed: 120]
Fujii T, Hayashi S, Hogg JC, Vincent R, van Eeden SF. Твердые частицы индуцируют экспрессию цитокинов в бронхиальных эпителиальных клетках человека. Американский журнал респираторных клеток и молекулярной биологии. 2001;25(3):265–71. [В паблике: 11588002]
Американский журнал респираторных клеток и молекулярной биологии. 2001;25(3):265–71. [В паблике: 11588002]
Фуке С., Бетсуяку Т., Насухара Ю., Морикава Т., Като Х., Нисимура М. Хемокины в бронхиолярном эпителии при развитии хронической обструктивной болезни легких. Американский журнал респираторных клеток и молекулярной биологии. 2004;31(4):405–12. [PubMed: 15220136]
Фукуда Ю., Масуда Ю., Ишизаки М., Масуги Ю., Ферранс В.Дж. Морфогенез аномальных эластических волокон в легких больных панацинарной и центриацинарной эмфиземой. Патология человека. 1989; 20 (7): 652–9.. [PubMed: 2661409]
Гадек Дж. Э., Феллс Дж. А., Кристал Р. Г. Курение сигарет вызывает дефицит функциональной антипротеазы в нижних дыхательных путях человека. Наука. 1979; 206 (4424): 1315–6. [PubMed: 316188]
Gardner DE, Crapo JD, McClellan RO. Токсикология легких. 3-е изд. Филадельфия: Тейлор и Фрэнсис; 2000.
Гебель С., Герстмайер Б. , Босио А., Хаусманн Х.Дж., Ван Мирт Э., Мюллер Т. Профилирование экспрессии генов в дыхательных тканях крыс, подвергшихся воздействию основного потока сигаретного дыма. Канцерогенез. 2004;25(2):169–78. [PubMed: 14578158]
, Босио А., Хаусманн Х.Дж., Ван Мирт Э., Мюллер Т. Профилирование экспрессии генов в дыхательных тканях крыс, подвергшихся воздействию основного потока сигаретного дыма. Канцерогенез. 2004;25(2):169–78. [PubMed: 14578158]
Гил Э., Чен Б., Клируп Э., Уэббер М., Ташкин Д.П. Острые и хронические эффекты курения марихуаны на легочную альвеолярную проницаемость. Науки о жизни. 1995; 56 (23–24): 2193–9. [PubMed: 7776849]
Gilmour PS, Rahman I, Donaldson K, MacNee W. Ацетилирование гистонов регулирует высвобождение эпителиального IL-8, опосредованное окислительным стрессом от частиц окружающей среды. Американский журнал физиологии — клеточная и молекулярная физиология легких. 2003;284(3):L533–L540. [В паблике: 12573991]
Глобальная инициатива по хронической обструктивной болезни легких. Рекомендации: Глобальная стратегия диагностики, лечения и профилактики ХОБЛ. ноябрь 2006 г. [дата обращения: 9 апреля 2007 г.]. < http://www  goldcopd.org>.
goldcopd.org>.
Golpon HA, Coldren CD, Zamora MR, Cosgrove GP, Moore MD, Tuder RM, Geraci MW, Voelkel NF. Профилирование экспрессии генов легочной ткани эмфиземы. Американский журнал респираторных клеток и молекулярной биологии. 2004;31(6):595–600. [В паблике: 15284076]
Гонсалес С., Хардс Дж., Ван Иден С., Хогг Дж.С. Экспрессия молекул адгезии при обструкции дыхательных путей, вызванной сигаретным дымом. Европейский респираторный журнал. 1996;9(10):1995–2001. [PubMed: 8
Goto Y, Hogg JC, Shih CH, Ishii H, Vincent R, van Eeden SF. Воздействие частиц окружающей среды ускоряет высвобождение моноцитов из костного мозга у кроликов с атеросклерозом. Американский журнал физиологии — клеточная и молекулярная физиология легких. 2004;287(1):L79–L85. [PubMed: 15003928]
Gottlieb DJ, Stone PJ, Sparrow D, Gale ME, Weiss ST, Snider GL, O’Connor GT. Экскреция десмозина с мочой у курильщиков с быстрым снижением функции легких и без него: нормативное исследование старения. Американский журнал респираторной и интенсивной терапии. 1996;154(5):1290–5. [PubMed: 8
Американский журнал респираторной и интенсивной терапии. 1996;154(5):1290–5. [PubMed: 8
Грей-Дональд К., Гиббонс Л., Шапиро С.Х., Маклем П.Т., Мартин Дж.Г. Состояние питания и смертность при хронической обструктивной болезни легких. Американский журнал респираторной и интенсивной терапии. 1996;153(3):961–6. [PubMed: 8630580]
Greene CM, McElvaney NG. Экспрессия и функция Toll-подобных рецепторов в эпителиальных клетках дыхательных путей. Архив иммунологии и экспериментальной терапии. 2005;53(5):418–27. [PubMed: 16314825]
Громер С., Уриг С., Беккер К. Тиоредоксиновая система — от науки к клинике. Обзоры медицинских исследований. 2004;24(1):40–89. [PubMed: 14595672]
Гросс П., Бабяк М.А., Толкер Э., Кащак М. Эмфизема легких, вызванная ферментами: предварительный отчет. Журнал медицины труда. 1964;6:481–4. [PubMed: 14241128]
Gross P, Pfitzer EA, Tolker E, Babyak MA, Kaschak M. Экспериментальная эмфизема: ее производство папаином у нормальных и силикозных крыс. Архивы гигиены окружающей среды. 1965; 11:50–8. [PubMed: 14312390]
Архивы гигиены окружающей среды. 1965; 11:50–8. [PubMed: 14312390]
Грумелли С., Корри Д.Б., Сонг Л.З., Сонг Л., Грин Л., Ха Дж., Хакен Дж., Эспада Р., Бэг Р., Льюис Д.Е. и др. Иммунная основа деструкции паренхимы легких при хронической обструктивной болезни легких и эмфиземе легких. ПЛОС Медицина. 2004;1(1):e8. [Бесплатная статья PMC: PMC523885] [PubMed: 15526056] [CrossRef]
Guatura SB, Martinez JA, Santos Bueno PC, Santos ML. Повышенное выдыхание перекиси водорода у здоровых людей после курения сигарет. Медицинский журнал Сан-Паулу. 2000;118(4):93–8. [PubMed: 10887384]
Герассимов А., Хосино Ю., Такубо Ю., Туркотт А., Ямамото М., Геззо Х., Триантафиллопулос А., Уиттакер К., Хойдал Дж. Р., Косио М. Г. Развитие эмфиземы у мышей, подвергшихся воздействию сигаретного дыма, зависит от штамма. Американский журнал респираторной и интенсивной терапии. 2004;170(9): 974–80. [PubMed: 15282203]
Gum JR Jr. Муциновые гены и белки, которые они кодируют: структура, разнообразие и регуляция. Американский журнал респираторных клеток и молекулярной биологии. 1992;7(6):557–64. [PubMed: 1449803]
Американский журнал респираторных клеток и молекулярной биологии. 1992;7(6):557–64. [PubMed: 1449803]
Guo X, Lin H-M, Lin Z, Montaño M, Sansores R, Wang G, DiAngelo S, Pardo A, Selman M, Floros J. Маркерные аллели гена сурфактантного белка A, B и D при хронической обструктивной болезни легких у населения Мексики. Европейский респираторный журнал. 2001; 18(3):482–9.0. [PubMed: 11589345]
Гаттеридж Дж. М. Биологическое происхождение свободных радикалов и механизмы антиоксидантной защиты. Химико-биологические взаимодействия. 1994; 91 (2–3): 133–40. [PubMed: 8194129]
Хабиб, член парламента, Клементс, Северная Каролина, Гаревал, Х.С. Курение сигарет и выдыхание этана у человека. Американский журнал респираторной и интенсивной терапии. 1995;151(5):1368–72. [PubMed: 7735586]
Хейл К.А., Юинг С.Л., Гокснелл Б.А., Нивёнер Д.Э. Заболевания легких у курильщиков, длительно курящих сигареты, с хронической обструкцией дыхательных путей и без нее. Американский обзор респираторных заболеваний. 1984;130(5):716–21. [PubMed: 6497154]
Американский обзор респираторных заболеваний. 1984;130(5):716–21. [PubMed: 6497154]
Холливелл Б., Гаттеридж Дж. М. Роль свободных радикалов и каталитических ионов металлов в заболеваниях человека: обзор. Методы в энзимологии. 1990; 186:1–85. [PubMed: 2172697]
Halliwell B, JMC Gutteridge. Определение и измерение антиоксидантов в биологических системах [письмо] Free Radical Biology & Medicine. 1995;18(1):125–6. [PubMed: 7896166]
Хан Дж., Стамлер Дж.С., Ли Х., Гриффит О.В. Ингибирование γ-глутамилцистеинсинтетазы путем S-нитрозилирования. Биология оксида азота. Часть 5: Материалы 4-го Международного совещания по биологии оксида азота. Монкада С., Стамлер Дж., Гросс С., Хиггс Э.А., редакторы. Лондон: Портленд Пресс; 1996. с. 114.
Handelman GJ, Packer L, Cross CE. Разрушение токоферолов, каротиноидов и ретинола в плазме человека сигаретным дымом. Американский журнал клинического питания. 1996;63(4):559–65. [PubMed: 8599320]
Haniuda M, Kubo K, Fujimoto K, Honda T, Yamaguchi S, Yoshida K, Amano J. Влияние ремоделирования легочной артерии на легочный кровоток после операции по уменьшению объема легких. Торакальный и сердечно-сосудистый хирург. 2003;51(3):154–8. [В паблике: 12833205]
Влияние ремоделирования легочной артерии на легочный кровоток после операции по уменьшению объема легких. Торакальный и сердечно-сосудистый хирург. 2003;51(3):154–8. [В паблике: 12833205]
Harrison DJ, Cantlay AM, Rae F, Lamb D, Smith CA. Частота делеции глутатион-S-трансферазы М1 у курильщиков с эмфиземой и раком легких. Человеческая и экспериментальная токсикология. 1997;16(7):356–60. [PubMed:
Хаутамаки Р.Д., Кобаяши Д.К., Старший Р.М., Шапиро С.Д. Потребность в эластазе макрофагов при эмфиземе, вызванной сигаретным дымом, у мышей. Наука. 1997; 277(5334):2002–4. [PubMed:
Hayes JD, Flanagan JU, Jowsey IR. Глутатионтрансферазы. Ежегодный обзор фармакологии и токсикологии. 2005; 45:51–88. [В паблике: 15822171]
He J-Q, Connett JE, Anthonisen NR, Paré PD, Sandford AJ. Варианты глутатиона S -трансферазы и их влияние на функцию легких при курении. Американский журнал респираторной и интенсивной терапии. 2004;170(4):388–94. [PubMed: 15184197]
2004;170(4):388–94. [PubMed: 15184197]
Хеффнер Дж. Э., Репин Дж. Э. Легочные стратегии антиоксидантной защиты. Американский обзор респираторных заболеваний. 1989;140(2):531–54. [PubMed: 2669581]
Хеле Д. Первая Сиенская международная конференция по животным моделям хронической обструктивной болезни легких, Чертоза ди Понтиньяно, Сиенский университет, Италия, 30 сентября – 2 октября 2001 г. Исследования органов дыхания. 2002;3(1):12. [Бесплатная статья PMC: PMC64810] [PubMed: 11806847]
Heppleston AG, Leopold JG. Хроническая эмфизема легких: анатомия и патогенез. Американский журнал медицины. 1961; 31: 279–91. [PubMed: 13713495]
Hersh CP, Dahl M, Ly NP, Berkey CS, Nordestgaard BG, Silverman EK. Хроническая обструктивная болезнь легких у гетерозигот α 1 -антитрипсин PI MZ: метаанализ. грудная клетка. 2004;59(10):843–9. [Бесплатная статья PMC: PMC1746834] [PubMed: 15454649]
Hersh CP, DeMeo DL, Lange C, Litonjua AA, Reilly JJ, Kwiatkowski D, Laird N, Sylvia JS, Sparrow D, Speizer FE и др. Попытка репликации зарегистрированных ассоциаций генов-кандидатов на хроническую обструктивную болезнь легких. Американский журнал респираторных клеток и молекулярной биологии. 2005;33(1):71–8. [Бесплатная статья PMC: PMC2715305] [PubMed: 15817713]
Попытка репликации зарегистрированных ассоциаций генов-кандидатов на хроническую обструктивную болезнь легких. Американский журнал респираторных клеток и молекулярной биологии. 2005;33(1):71–8. [Бесплатная статья PMC: PMC2715305] [PubMed: 15817713]
Heunks LM, Dekhuizen PN. Функция дыхательных мышц и свободные радикалы: от клетки до ХОБЛ. грудная клетка. 2000;55(8):704–16. [Бесплатная статья PMC: PMC1745815] [PubMed: 10899251]
Хиггинс М., Келлер Дж. Семейное возникновение хронических респираторных заболеваний и семейное сходство вентиляционной способности. Журнал хронических заболеваний. 1975;28(4):239–51. [PubMed: 1127070]
Хайэм М.А., Прайд Н.Б., Алихан А., Моррелл Н.В. Полиморфизм промотора гена фактора некроза опухоли-α при хронической обструктивной болезни легких. Европейский респираторный журнал. 2000;15(2):281–4. [В паблике: 10706492]
Hill JM, Zalos G, Halcox JP, Schenke WH, Waclawiw MA, Quyyumi AA, Finkel T. Циркулирующие эндотелиальные клетки-предшественники, сосудистая функция и сердечно-сосудистый риск. Медицинский журнал Новой Англии. 2003;348(7):593–600. [PubMed: 12584367]
Циркулирующие эндотелиальные клетки-предшественники, сосудистая функция и сердечно-сосудистый риск. Медицинский журнал Новой Англии. 2003;348(7):593–600. [PubMed: 12584367]
Хобсон Дж., Райт Дж., Чарг А. Гистохимические доказательства образования активных форм кислорода на апикальной поверхности эксплантатов трахеи, подвергшихся воздействию сигаретного дыма. Американский журнал патологии. 1991;139(3):573–80. [Бесплатная статья PMC: PMC1886209] [PubMed: 1653519]
Hockertz S, Emmendorffer A, Scherer G, Ruppert T, Daube H, Tricker AR, Adlkofer F. Острое воздействие курения и сильного экспериментального воздействия табачного дыма из окружающей среды (ETS) на иммунную систему . Клеточная биология и токсикология. 1994;10(3):177–90. [PubMed: 7994635]
Hodge SJ, Hodge GL, Reynolds PN, Scicchitano R, Holmes M. Увеличение продукции TGF-β и апоптоз Т-лимфоцитов, выделенных из периферической крови при ХОБЛ. Американский журнал физиологии — клеточная и молекулярная физиология легких. 2003;285(2):L492–L499. [PubMed: 12851215]
2003;285(2):L492–L499. [PubMed: 12851215]
Хогг Дж.С. Патофизиология ограничения воздушного потока при хронической обструктивной болезни легких. Ланцет. 2004;364(9435):709–21. [PubMed: 15325838]
Хогг Дж.С. Связь курения табака с ХОБЛ: гистопатогенез. Клиническое лечение хронической обструктивной болезни легких. Биология легких в норме и болезни. 2-е изд. Реннард С.И., Родригес-Ройзен, Хушон Г., Рош Н., редакторы. Том. 222. Нью-Йорк: Informa Healthcare; 2007. С. 43–66.
Хогг Дж.С. Структура и функция легких при ХОБЛ. Международный журнал туберкулеза и болезней легких. 2008;12(5):467–79. [PubMed: 18419881]
Hogg JC, Chu F, Utokaparch S, Woods R, Elliott WM, Buzatu L, Cherniack RM, Rogers RM, Sciurba FC, Coxson HO и др. Характер обструкции мелких дыхательных путей при хронической обструктивной болезни легких. Медицинский журнал Новой Англии. 2004;350(26):2645–53. [PubMed: 15215480]
Hogg JC, Macklem PT, Thurlbeck WM. Локализация и характер обструкции дыхательных путей при хронической обструктивной болезни легких. Медицинский журнал Новой Англии. 1968;278(25):1355–1356. [PubMed: 5650164]
Локализация и характер обструкции дыхательных путей при хронической обструктивной болезни легких. Медицинский журнал Новой Англии. 1968;278(25):1355–1356. [PubMed: 5650164]
Hogg JC, Senior RM. Хроническая обструктивная болезнь легких с2: патология и биохимия эмфиземы легких. грудная клетка. 2002;57(9):830–4. [Бесплатная статья PMC: PMC1746435] [PubMed: 12200530]
Hoidal JR, Fox RB, LeMarbe PA, Perri R, Repine JE. Измененные окислительные метаболические реакции in vitro альвеолярных макрофагов бессимптомных курильщиков сигарет. Американский обзор респираторных заболеваний. 1981;123(1):85–9. [В паблике: 6257154]
Холмгрен А. Антиоксидантная функция систем тиоредоксина и глутаредоксина. Антиоксиданты и передача сигналов окислительно-восстановительного потенциала. 2000;2(4):811–20. [PubMed: 11213485]
Horne SL, Cockcroft DW, Dosman JA. Возможный защитный эффект аллеля GC2 против хронической обструктивной болезни дыхательных путей. Наследственность человека. 1990;40(3):173–176. [PubMed: 2365378]
Наследственность человека. 1990;40(3):173–176. [PubMed: 2365378]
Хорсфилд К., Сигел Н., Бишоп Дж.М. Легочное кровообращение при хроническом бронхите в покое и при физической нагрузке дышит воздухом и 80-процентным кислородом. Клиническая наука. 1968;34(3):473–83. [PubMed: 5666876]
Хойт Дж. К., Роббинс Р. А., Хабиб М., Спринголл Д. Р., Баттери Л. Д., Полак Дж. М., Барнс П. Дж. Сигаретный дым снижает уровень индуцибельной синтазы оксида азота в эпителиальных клетках легких. Экспериментальное исследование легких. 2003;29(1):17–28. [PubMed: 12652813]
Хуан С.Л., Су Ч.Х., Чанг С.К. Полиморфизм гена фактора некроза опухоли-α при хроническом бронхите. Американский журнал респираторной и интенсивной терапии. 1997;156(5):1436-9. [В паблике:
- 57]
Hubert HB, Fabsitz RR, Feinleib M, Gwinn C. Влияние генетики и окружающей среды на легочную функцию у взрослых близнецов. Американский обзор респираторных заболеваний. 1982;125(4):409–15. [PubMed: 7200340]
[PubMed: 7200340]
Hulbert WC, Walker DC, Jackson A, Hogg JC. Проницаемость дыхательных путей для пероксидазы хрена у морских свинок: фаза восстановления после повреждения сигаретным дымом. Американский обзор респираторных заболеваний. 1981;123(3):320–6. [PubMed: 7224343]
Ханнингхейк GW, Кристалл RG. Курение сигарет и разрушение легких: накопление нейтрофилов в легких курильщиков сигарет. Американский обзор респираторных заболеваний. 1983;128(5):833–8. [PubMed: 6556892]
Ханнингхейк Г.В., Гадек Дж.Э., Каванами О., Ферранс В.Дж., Кристал Р.Г. Воспалительные и иммунные процессы в легких человека в норме и при патологии: оценка методом бронхоальвеолярного лаважа. Американский журнал патологии. 1979; 97 (1): 149–206. [Бесплатная статья PMC: PMC2042387] [PubMed: 495693]
DCS Хатчисон. α 1 — Дефицит антитрипсина в Европе: географическое распространение Pi типов S и Z. Респираторная медицина. 1998;92(3):367–77. [PubMed: 96
[PubMed: 96
Ичиносе М., Сугиура Х., Ямагата С., Коараи А., Ширато К. Увеличение производства активных форм азота при хронической обструктивной болезни легких. Американский журнал респираторной и интенсивной терапии. 2000; 162 (2 часть 1): 701–6. [PubMed: 10
Имаи К., Далал С.С., Чен Э.С., Дауни Р., Шульман Л.Л., Гинзбург М., Д’Армиенто Дж. Экспрессия коллагеназы человека (матриксная металлопротеиназа-1) в легких пациентов с эмфиземой. Американский журнал респираторной и интенсивной терапии. 2001; 163 (3 часть 1): 786–91. [PubMed: 11254539]
Международное агентство по изучению рака. Монографии МАИР по оценке канцерогенных рисков для человека: табачный дым и непроизвольное курение. Том. 83. Лион (Франция): Международное агентство по изучению рака; 2004. [Бесплатная статья PMC: PMC4781536] [PubMed: 15285078]
Международная комиссия по радиологической защите. Модель респираторного тракта человека для радиологической защиты, отчет рабочей группы Международной комиссии по радиологической защите. Публикация МКРЗ. Том. 66. Тарритаун (Нью-Йорк): Elsevier Science; 1994.
Публикация МКРЗ. Том. 66. Тарритаун (Нью-Йорк): Elsevier Science; 1994.
Исии Т., Кейчо Н., Терамото С., Адзума А., Кудох С., Фукути Ю., Оучи Ю., Мацусэ Т. Связь вариации Gc-глобулина с предрасположенностью к ХОБЛ и диффузному панбронхиолиту. Европейский респираторный журнал. 2001;18(5):753–7. [В паблике: 11757623]
Исии Т., Мацусе Т., Терамото С., Мацуи Х., Хосой Т., Фукучи Ю., Оучи Ю. Связь между полиморфизмом альфа-1-антихимотрипсина и предрасположенностью к хронической обструктивной болезни легких. Европейский журнал клинических исследований. 2000а; 30(6):543–8. [PubMed: 10849024]
Исии Т., Мацусе Т., Терамото С., Мацуи Х., Мияо М., Хосой Т., Такахаши Х., Фукути Ю., Оучи Ю. Полиморфизм глутатиона S -трансферазы P1 (GSTP1) у пациентов с хроническое обструктивное заболевание легких. грудная клетка. 1999;54(8):693–6. [Бесплатная статья PMC: PMC1745535] [PubMed: 10413721]
Исии Т., Мацусэ Т., Терамото С. , Мацуи Х., Мияо М., Хосой Т., Такахаши Х., Фукути Ю., Оучи Ю. Ни IL-1 β, ни IL-1 β, IL -1 антагонист рецептора, ни полиморфизмы TNF-α не связаны с предрасположенностью к ХОБЛ. Респираторная медицина. 2000b;94(9):847–51. [PubMed: 11001075]
, Мацуи Х., Мияо М., Хосой Т., Такахаши Х., Фукути Ю., Оучи Ю. Ни IL-1 β, ни IL-1 β, IL -1 антагонист рецептора, ни полиморфизмы TNF-α не связаны с предрасположенностью к ХОБЛ. Респираторная медицина. 2000b;94(9):847–51. [PubMed: 11001075]
Ишизаки Т., Киши Ю., Сасаки Ф., Амешима С., Накаи Т., Миябо С. Влияние пробукола, перорального гипохолестеринемического средства, на острое вдыхание табачного дыма у крыс. Клиническая наука (Лондон). 1996;90(6):517–23. [PubMed: 8697723]
Ито К., Ханадзава Т., Томита К., Барнс П.Дж., Адкок И.М. Окислительный стресс снижает активность гистондеацетилазы 2 и усиливает экспрессию гена IL-8: роль нитрования тирозина. Коммуникации биохимических и биофизических исследований. 2004а; 315(1):240–5. [PubMed: 15013452]
Ito K, Ito M, Elliott WM, Cosio B, Caramori G, Kon OM, Barczyk A, Hayashi S, Adcock IM, Hogg JC, et al. Снижение активности гистондеацетилазы при хронической обструктивной болезни легких. Медицинский журнал Новой Англии. 2005;352(19): 1967–76. [PubMed: 15888697]
2005;352(19): 1967–76. [PubMed: 15888697]
Ито К., Лим С., Карамори Г., Чанг К.Ф., Барнс П.Дж., Адкок И.М. Курение сигарет снижает экспрессию гистондеацетилазы 2, усиливает экспрессию цитокинов и ингибирует действие глюкокортикоидов в альвеолярных макрофагах. Журнал ФАСЭБ. 2001;15(6):1110–2. [PubMed: 112
Ito I, Nagai S, Hoshino Y, Muro S, Hirai T, Tsukino M, Mishima M. Риск и тяжесть ХОБЛ связаны с групповым компонентом аллеля 1F глобулина сыворотки. Грудь. 2004б; 125(1):63–70. [В паблике: 14718422]
Янофф А. Эластазы и эмфизема: текущая оценка протеазно-антипротеазной гипотезы. Американский обзор респираторных заболеваний. 1985;132(2):417–33. [PubMed: 3896082]
Янофф А., Карп Х., Лоран П., Раджу Л. Роль окислительных процессов при эмфиземе. Американский обзор респираторных заболеваний. 1983а; 127(2):S31–S38. [PubMed: 6600889]
Janoff A, Raju L, Dearing R. Уровни активности эластазы в жидкостях бронхоальвеолярного лаважа здоровых курильщиков и некурящих. Американский обзор респираторных заболеваний. 1983б; 127(5):540–4. [PubMed: 6552150]
Американский обзор респираторных заболеваний. 1983б; 127(5):540–4. [PubMed: 6552150]
Янофф А., Шерер Дж. Медиаторы воспаления в лизосомах лейкоцитов. IX: эластинолитическая активность в гранулах полиморфноядерных лейкоцитов человека. Журнал экспериментальной медицины. 1968;128(5):1137–55. [Бесплатная статья PMC: PMC2138566] [PubMed: 5303065]
Janssen-Heininger YMW, Macara I, Mossman BT. Взаимодействие между оксидантами и фактором некроза опухоли при активации ядерного фактора (NF)-κB: потребность Ras/митоген-активируемых протеинкиназ в активации NF-κB оксидантами. Американский журнал респираторных клеток и молекулярной биологии. 1999;20(5):942–52. [PubMed: 10226064]
Janus ED, Phillips NT, Carrell RW. Курение, функция легких и дефицит альфа-1-антитрипсина. Ланцет. 1985;325(8421):152–4. [PubMed: 2857224]
Дженкинс Р.К., Росс Р.Дж. Терапия гормоном роста при катаболизме белков. Ежеквартальный медицинский журнал. 1996;89(11):813–9. [PubMed: 8977960]
1996;89(11):813–9. [PubMed: 8977960]
Jezek V, Schrijen F, Sadoul P. Функция правого желудочка и легочная гемодинамика при физической нагрузке у пациентов с хронической обструктивной бронхолегочной болезнью. Кардиология. 1973;58(1):20–31. [PubMed: 4710797]
Хименес Л.А., Томпсон Дж., Браун Д.А., Рахман И., Антоничелли Ф., Даффин Р., Дрост Э.М., Хэй Р.Т., Дональдсон К., Макни В. Активация NF-κB PM 10 происходит через механизм, опосредованный железом, в отсутствие деградации IκB. Токсикология и прикладная фармакология. 2000;166(2):101–10. [PubMed: 10896851]
Jones JG, Minty BD, Lawler P, Hulands G, Crawley JCW, Veall N. Повышенная проницаемость альвеолярного эпителия у курильщиков сигарет. Ланцет. 1980;315(8159):66–8. [PubMed: 6101416]
Joost O, Wilk JB, Cupples LA, Harmon M, Shearman AM, Baldwin CT, O’Connor GT, Myers RH, Gottlieb DJ. Генетические локусы, влияющие на функцию легких: сканирование всего генома в Framingham Study. Американский журнал респираторной и интенсивной терапии. 2002;165(6):795–9. [PubMed: 11897646]
Американский журнал респираторной и интенсивной терапии. 2002;165(6):795–9. [PubMed: 11897646]
Каннер Р.Э., Антонисен Н.Р., Коннетт Дж.Е. Исследовательская группа по изучению здоровья легких. Заболевания нижних дыхательных путей способствуют снижению ОФВ 1 у нынешних курильщиков, но не у бывших курильщиков с легким хроническим обструктивным заболеванием легких. Американский журнал респираторной и интенсивной терапии. 2001;164(3):358–64. [В паблике: 11500333]
Каплан Д.Д., Каландрино Ф.С., Шустер Д.П. Влияние курения на проницаемость легочных сосудов: исследование позитронно-эмиссионной томографии. Американский обзор респираторных заболеваний. 1992;145(3):712–5. [PubMed: 1546854]
Kasahara Y, Tuder RM, Cool CD, Lynch DA, Flores SC, Voelkel NF. Гибель эндотелиальных клеток и снижение экспрессии фактора роста эндотелия сосудов и рецептора фактора роста эндотелия сосудов 2 при эмфиземе. Американский журнал респираторной и интенсивной терапии. 2001; 163 (3 часть 1): 737–44. [В паблике: 11254533]
2001; 163 (3 часть 1): 737–44. [В паблике: 11254533]
Касахара Ю., Тудер Р.М., Тарасевичене-Стюарт Л., Ле Крас Т.Д., Абман С., Хирт П.К., Вальтенбергер Дж., Воелкель Н.Ф. Ингибирование рецепторов VEGF вызывает апоптоз клеток легких и эмфизему. Журнал клинических исследований. 2000;106(11):1311–9. [Бесплатная статья PMC: PMC387249] [PubMed: 11104784]
Касуга И., Паре, П.Д., Руан Дж., Коннетт Дж.Е., Антонисен Н.Р., Сэндфорд А.Дж. Отсутствие связи гаплотипов групповых компонентов с функцией легких у курильщиков. грудная клетка. 2003;58(9): 790–3. [Бесплатная статья PMC: PMC1746792] [PubMed: 12947140]
Kauffmann F, Kleisbauer JP, Cambon-DeMouzon A, Mercier P, Constans J, Blanc M, Rouch Y, Feingold N. Генетические маркеры при хроническом ограничении воздушного потока : генетическое эпидемиологическое исследование. Американский обзор респираторных заболеваний. 1983;127(3):263–9. [PubMed: 6572487]
Kayyali US, Budhiraja R, Pennella CM, Cooray S, Lanzillo JJ, Chalkley R, Hassoun PM. Активация ксантиноксидазы конденсатом табачного дыма в эндотелиальных клетках легких. Токсикология и прикладная фармакология. 2003;188(1):59–68. [PubMed: 12668123]
Активация ксантиноксидазы конденсатом табачного дыма в эндотелиальных клетках легких. Токсикология и прикладная фармакология. 2003;188(1):59–68. [PubMed: 12668123]
Китингс В.М., Коллинз П.Д., Скотт Д.М., Барнс П.Дж. Различия интерлейкина-8 и фактора некроза опухоли-альфа в индуцированной мокроте у пациентов с хронической обструктивной болезнью легких или астмой. Американский журнал респираторной и интенсивной терапии. 1996;153(2):530–4. [PubMed: 8564092]
Keicho N, Elliott WM, Hogg JC, Hayashi S. Ген аденовируса E1A нарушает регуляцию экспрессии ICAM-1 в трансформированных клетках легочного эпителия. Американский журнал респираторных клеток и молекулярной биологии. 1997;16(1):23–30. [PubMed: 8998075]
Келлерманн Г., Уолтер Х. Исследования популяционной генетики полиморфизма альфа-1-антитрипсина. Гуманогенетика. 1970;10(2):145–50. [PubMed: 5507048]
Kessler R, Faller M, Weitzenblum E, Chaouat A, Aykut A, Ducolone A, Ehrhart M, Oswald-Mammomosser M. «Естественная история» легочной гипертензии в серии из 131 пациента с хроническим обструктивная болезнь легких» Американский журнал респираторной и реаниматологической медицины. 2001;164(2):219–24. [PubMed: 11463591]
«Естественная история» легочной гипертензии в серии из 131 пациента с хроническим обструктивная болезнь легких» Американский журнал респираторной и реаниматологической медицины. 2001;164(2):219–24. [PubMed: 11463591]
Харитонов С.А., Роббинс Р.А., Йейтс Д., Китингс В., Барнс П.Дж. Острые и хронические эффекты курения сигарет на выдыхаемый оксид азота. Американский журнал респираторной и интенсивной терапии. 1995;152(2):609–12. [PubMed: 7543345]
Ким Х, Лю Х, Кохяма Т, Кобаяши Т, Коннер Х, Абэ С, Фан Кью, Вен Ф-Кью, Реннард С.И. Сигаретный дым стимулирует выработку MMP-1 фибробластами легких человека посредством пути ERK1/2. Хроническое обструктивное заболевание легких. 2004;1(1):13–23. [В паблике: 16997735]
Ким В., Роджерс Т.Дж., Крайнер Г.Дж. Новые представления в патобиологии хронической обструктивной болезни легких. Труды Американского торакального общества. 2008;5(4):478–85. [Бесплатная статья PMC: PMC2645323] [PubMed: 18453359]
Киннула В. Л., Крапо Д.Д. Супероксиддисмутазы в легких и легочных заболеваниях человека. Американский журнал респираторной и интенсивной терапии. 2003;167(12):1600–19. [PubMed: 12796054]
Л., Крапо Д.Д. Супероксиддисмутазы в легких и легочных заболеваниях человека. Американский журнал респираторной и интенсивной терапии. 2003;167(12):1600–19. [PubMed: 12796054]
Kinnula VL, Lehtonen S, Kaarteenaho-Wiik R, Lakari E, Paakko P, Kang SW, Rhee SG, Soini Y. Клеточная специфичная экспрессия пероксиредоксинов в легких человека и легочный саркоидоз. грудная клетка. 2002;57(2):157–64. [Бесплатная статья PMC: PMC1746258] [PubMed: 11828047]
Klaassen CD, редактор. Токсикология Казаретта и Доулла: фундаментальная наука о ядах. 6-е изд. Нью-Йорк: Макгроу-Хилл; 2001.
Knowles MR, Boucher RC. Очищение от слизи как первичный врожденный защитный механизм дыхательных путей млекопитающих. Журнал клинических исследований. 2002;109(5):571-7. [Бесплатная статья PMC: PMC150901] [PubMed: 11877463]
Kohri K, Ueki IF, Nadel JA. Эластаза нейтрофилов индуцирует продукцию муцина путем лиганд-зависимой активации рецептора эпидермального фактора роста. Американский журнал физиологии — клеточная и молекулярная физиология легких. 2002; 283(3):L531–L540. [В паблике: 12169572]
Американский журнал физиологии — клеточная и молекулярная физиология легких. 2002; 283(3):L531–L540. [В паблике: 12169572]
Koike E, Hirano S, Shimojo N, Kobayashi T. Анализ кДНК-микрочипов экспрессии генов в альвеолярных макрофагах крысы в ответ на органический экстракт частиц дизельного выхлопа. Токсикологические науки. 2002;67(2):241–6. [PubMed: 12011483]
Kreyling WG, Scheuch G. Очистка легких от частиц. Взаимодействие частиц с легкими. Биология легких в норме и болезни. Гер П., Хейдер Дж., редакторы. Том. 1143. Нью-Йорк: Марсель Деккер; 2000. С. 323–76.
Крух Г.Д., Белинский М.Г. Семейство насосов для оттока лекарств MRP. Онкоген. 2003;22(47):7537–52. [PubMed: 14576857]
Кубо Х, Алитало К. Кровавая судьба эндотелиальных стволовых клеток. Гены и развитие. 2003;17(3):322–9. [PubMed: 12569121]
Kubo K, Ge RL, Koizumi T, Fujimoto K, Yamanda T, Haniuda M, Honda T. Ремоделирование легочной артерии изменяет легочную гипертензию во время упражнений при тяжелой эмфиземе. Физиология дыхания. 2000;120(1):71–9.. [PubMed: 10786646]
Физиология дыхания. 2000;120(1):71–9.. [PubMed: 10786646]
Küçükaycan M, Van Krugten M, Pennings HJ, Huizinga TWJ, Buurman WA, Dentener MA, Wouters EFM. Полиморфизм гена фактора некроза опухоли-α +489G/A ассоциирован с хронической обструктивной болезнью легких. Дыхательные исследования. 2002;3(1):29. [Статья бесплатно PMC: PMC150514] [PubMed: 12537602]
Kueppers F, Miller RD, Gordon H, Hepper NG, Offord K. Семейная распространенность хронической обструктивной болезни легких в парном исследовании. Американский журнал медицины. 1977;63(3):336–42. [PubMed: 302643]
Кугельман А., Чой Х.А., Лю Р., Ши М.М., Гозал Э., Форман Х.Дж. Гамма-глутамилтранспептидаза увеличивается при окислительном стрессе в альвеолярных эпителиальных клетках L2 крысы. Американский журнал респираторных клеток и молекулярной биологии. 1994;11(5):586–92. [PubMed: 7946387]
Kuhn C, Yu SY, Chraplyvy M, Linder HE, Senior RM. Индукция эмфиземы эластазой. II: изменения в соединительной ткани. Лабораторные исследования. 1976;34(4):372–80. [В паблике: 177809]
II: изменения в соединительной ткани. Лабораторные исследования. 1976;34(4):372–80. [В паблике: 177809]
Кумар В., Аббас А.К., Фаусто Н. Обновление и восстановление тканей: регенерация, заживление и фиброз, Роббинс и Котран, патологическая основа заболевания. 7-е изд. Филадельфия: Эльзевир; 2005. С. 87–118.
Kuschner WG, D’Alessandro A, Wong H, Blanc PD. Дозозависимые воспалительные реакции, связанные с курением сигарет, у здоровых взрослых. Европейский респираторный журнал. 1996;9(10):1989–94. [PubMed: 8
Лаэннек РУТ. Трактат о болезнях грудной клетки и опосредованной аускультации. 4-е изд. Forbes J, редактор. Лондон: Лонгманс; 1834.
Лакари Э., Паакко П., Киннула В.Л. Супероксиддисмутаза марганца, но не супероксиддисмутаза CuZn, высоко экспрессируется в гранулемах легочного саркоидоза и внешнего аллергического альвеолита. Американский журнал респираторной и интенсивной терапии. 1998;158(2):589–96. [PubMed: 9700139]
Лакари Э. , Паакко П., Пьетаринен-Рунти П., Киннула В.Л. Марганцевая супероксиддисмутаза и каталаза согласованно экспрессируются в альвеолярной области при хронических интерстициальных пневмониях и гранулематозных заболеваниях легких. Американский журнал респираторной и интенсивной терапии. 2000; 161 (2 часть 1): 615–21. [В паблике: 10673208]
, Паакко П., Пьетаринен-Рунти П., Киннула В.Л. Марганцевая супероксиддисмутаза и каталаза согласованно экспрессируются в альвеолярной области при хронических интерстициальных пневмониях и гранулематозных заболеваниях легких. Американский журнал респираторной и интенсивной терапии. 2000; 161 (2 часть 1): 615–21. [В паблике: 10673208]
Ланцет. Определение и классификация хронического бронхита для клинико-эпидемиологических целей. Ланцет. 1965; 285 (7389): 775–9. [PubMed: 4165081]
Ландбо С., Прескотт Э., Ланге П., Вестбо Дж., Алмдал Т.П. Прогностическое значение нутритивного статуса при хронической обструктивной болезни легких. Американский журнал респираторной и интенсивной терапии. 1999; 160 (6): 1856–61. [PubMed: 10588597]
Lang MR, Fiaux GW, Gillooly M, Stewart JA, Hulmes DJ, Lamb D. Содержание коллагена в ткани альвеолярной стенки в эмфизематозных и неэмфизематозных легких. грудная клетка. 1994;49(4):319–26. [Бесплатная статья PMC: PMC475363] [PubMed: 8202900]
Langen RC, Korn SH, Wouters EF. АФК в местном и системном патогенезе ХОБЛ. Свободнорадикальная биология и медицина. 2003;35(3):226–35. [PubMed: 12885585]
АФК в местном и системном патогенезе ХОБЛ. Свободнорадикальная биология и медицина. 2003;35(3):226–35. [PubMed: 12885585]
Langen RCJ, Van Der Velden JLJ, Schols AMWJ, Kelders MCJM, Wouters EFM, Janssen-Heininger YMW. Фактор некроза опухоли-альфа ингибирует миогенную дифференцировку посредством дестабилизации белка MyoD. Журнал ФАСЭБ. 2004;18(2):227–37. [В паблике: 14769817]
Ланнан С., Дональдсон К., Браун Д., Макни В. Влияние сигаретного дыма и его конденсатов на повреждение клеток альвеолярного эпителия in vitro. Американский журнал физиологии. 1994; 266 (1 часть 1): L92–L100. [PubMed: 8304473]
Ларсон Р.К., Барман М.Л., Куэпперс Ф., Фуденберг Х.Х. Генетические и экологические детерминанты хронической обструктивной болезни легких. Анналы внутренней медицины. 1970;72(5):627–32. [PubMed: 5448092]
Ларссон С. Естественная история и ожидаемая продолжительность жизни при тяжелом дефиците альфа-1-антитрипсина, Pi Z. Acta Medica Scandinavica. 1978;204(5):345–51. [PubMed: 309708]
Acta Medica Scandinavica. 1978;204(5):345–51. [PubMed: 309708]
Laurell CB, Eriksson S. Электрофоретическая картина α 1 -глобулина сыворотки при дефиците α 1 -антитрипсина. Скандинавский журнал клинических и лабораторных исследований. 1963; 15 (2): 132–40.
Леко К.Дж., Уотерхаус П., Санчес О.Х., Гоуинг К.Л.М., Пул А.Р., Уэйкхэм А., Мак Т.В., Хоха Р. Спонтанное увеличение воздушного пространства в легких мышей, лишенных тканевого ингибитора металлопротеиназ-3 (ТИМП-3). Журнал клинических исследований. 2001; 108(6):817–29.. [Бесплатная статья PMC: PMC200926] [PubMed: 11560951]
Lee HM, Takeyama K, Dabbagh K, Lausier JA, Ueki IF, Nadel JA. Инстилляция агарозной пробки вызывает метаплазию бокаловидных клеток путем активации рецепторов EGF в дыхательных путях крыс. Американский журнал физиологии — клеточная и молекулярная физиология легких. 2000;278(1):L185–L192. [PubMed: 10645906]
Leonarduzzi G, Scavazza A, Biasi F, Chiarpotto E, Camandola S, Vogel S, Dargel R, Poli G. Конечный продукт перекисного окисления липидов 4-гидрокси-2,3-ноненаль повышает регуляцию экспрессия трансформирующего фактора роста β1 в линии макрофагов: связь между окислительным повреждением и фибросклерозом. Журнал ФАСЭБ. 1997;11(11):851–7. [PubMed: 83]
Конечный продукт перекисного окисления липидов 4-гидрокси-2,3-ноненаль повышает регуляцию экспрессия трансформирующего фактора роста β1 в линии макрофагов: связь между окислительным повреждением и фибросклерозом. Журнал ФАСЭБ. 1997;11(11):851–7. [PubMed: 83]
Леопольд Дж. Г., Гоф Дж. Центрилобулярная форма гипертрофической эмфиземы и ее связь с хроническим бронхитом. грудная клетка. 1957; 12 (3): 219–35. [Бесплатная статья PMC: PMC1019212] [PubMed: 13467881]
Левиттер Ф.И., Тагер И.Б., МакГью М., Тишлер П.В., Спейзер Ф.Е. Генетические и экологические детерминанты уровня легочной функции. Американский журнал эпидемиологии. 1984;120(4):518–30. [PubMed: 6475921]
Li XY, Donaldson K, Rahman I, MacNee W. Исследование роли глутатиона в повышении проницаемости эпителия, вызванном сигаретным дымом in vivo и in vitro. Американский журнал респираторной и интенсивной терапии. 1994;149(6):1518–25. [PubMed: 8004308]
Li XY, Rahman I, Donaldson K, MacNee W. Механизмы воздействия сигаретного дыма на повышенную проницаемость воздушного пространства. грудная клетка. 1996;51(5):465–71. [Бесплатная статья PMC: PMC473589] [PubMed: 8711672]
Механизмы воздействия сигаретного дыма на повышенную проницаемость воздушного пространства. грудная клетка. 1996;51(5):465–71. [Бесплатная статья PMC: PMC473589] [PubMed: 8711672]
Li YP, Atkins CM, Sweatt JD, Reid MB. Митохондрии опосредуют передачу сигналов фактора некроза опухоли-α/NF-κB в мышечных трубках скелетных мышц. Антиоксиданты и передача сигналов окислительно-восстановительного потенциала. 1999;1(1):97–104. [PubMed: 11225736]
Либерман Дж., Винтер Б., Састр А. Альфа 1 -антитрипсин Pi-типа у 965 больных ХОБЛ. Грудь. 1986;89(3):370–3. [PubMed: 3485034]
Linden M, Rasmussen JB, Piitulainen E, Tunek A, Larson M, Tegner H, Venge P, Laitinen LA, Brattsand R. Воспаление дыхательных путей у курильщиков с необструктивным и обструктивным хроническим бронхитом. Американский обзор респираторных заболеваний. 1993;148(5):1226–32. [PubMed: 8239158]
Лёфдаль Дж.М., Седерлунд К., Нателл Л., Эклунд А., Скольд К. М. Бронхоальвеолярный лаваж при ХОБЛ: восстановление жидкости коррелирует со степенью эмфиземы. Европейский респираторный журнал. 2005;25(2):275–81. [В паблике: 15684291]
М. Бронхоальвеолярный лаваж при ХОБЛ: восстановление жидкости коррелирует со степенью эмфиземы. Европейский респираторный журнал. 2005;25(2):275–81. [В паблике: 15684291]
Lowenstein CJ, Snyder SH. Оксид азота, новый биологический мессенджер. Клетка. 1992;70(5):705–7. [PubMed: 1381285]
Лукач Н.В., Хогабоам К.М., Кункель С.Л. Хемокины и их рецепторы при хронических заболеваниях легких. Текущие мишени для лекарств: воспаление и аллергия. 2005;4(3):313–7. [PubMed: 16101539]
Lykkesfeldt J, Loft S, Nielsen JB, Poulsen HE. Аскорбиновая кислота и дегидроаскорбиновая кислота как биомаркеры окислительного стресса, вызванного курением. Американский журнал клинического питания. 1997;65(4):959–63. [PubMed:
79] Ма С., Либерман С., Турино Г.М., Лин Ю.Ю. Обнаружение и количественное определение свободного десмозина и изодесмозина в моче человека и их форм, связанных с пептидами, в мокроте. Труды Национальной академии наук Соединенных Штатов Америки. 2003;100(22):12941–3. [Бесплатная статья PMC: PMC240723] [PubMed: 14563926]
2003;100(22):12941–3. [Бесплатная статья PMC: PMC240723] [PubMed: 14563926]
MacFarlane NG, Miller DJ. Депрессия пиковой силы без изменения чувствительности к кальцию анионом супероксида в сердечной мышце крысы с химически снятой кожей. Исследование кровообращения. 1992;70(6):1217–24. [PubMed: 1315636]
MacNee W. Оксиданты/антиоксиданты и ХОБЛ. Грудь. 2000;117(5 Приложение 1):303S–317S. [PubMed: 10843965]
MacNee W. Окислительный стресс и воспаление легких при заболеваниях дыхательных путей. Европейский журнал фармакологии. 2001;429(1–3):195–207. [PubMed: 11698041]
MacNee W. Оксиданты и ХОБЛ. Текущие мишени для лекарств: воспаление и аллергия. 2005а;4(6):627–41. [PubMed: 17305519]
MacNee W. Легочный и системный оксидант/антиоксидантный дисбаланс при хронической обструктивной болезни легких. Труды Американского торакального общества. 2005b;2(1):50–60. [В паблике: 16113469]
MacNee W, Rahman I. Является ли окислительный стресс центральным в патогенезе хронической обструктивной болезни легких? Тенденции молекулярной медицины. 2001;7(2):55–62. [PubMed: 11286755]
Является ли окислительный стресс центральным в патогенезе хронической обструктивной болезни легких? Тенденции молекулярной медицины. 2001;7(2):55–62. [PubMed: 11286755]
MacNee W, Wiggs B, Belzberg AS, Hogg JC. Влияние курения сигарет на кинетику нейтрофилов в легких человека. Медицинский журнал Новой Англии. 1989;321(14):924–8. [PubMed: 2779614]
Махадева Р., Ломас Д.А. Генетика и респираторные заболевания. 2: альфа 1 -дефицит антитрипсина, цирроз печени и эмфизема. грудная клетка. 1998;53(6):501–5. [Бесплатная статья PMC: PMC1745245] [PubMed: 9713452]
Махадева Р., Шапиро С.Д. Хроническое обструктивное заболевание легких. 3: экспериментальные модели эмфиземы легких на животных. грудная клетка. 2002;57(10):908–14. [Бесплатная статья PMC: PMC1746206] [PubMed: 12324680]
Majo J, Ghezzo H, Cosio MG. Популяция лимфоцитов и апоптоз в легких курильщиков и их связь с эмфиземой. Европейский респираторный журнал. 2001;17(5):946–53. [PubMed: 11488331]
2001;17(5):946–53. [PubMed: 11488331]
Малхотра А., Пайффер А.П., Рюджин Д.Т., Эльснер Т., Каннер Р.Е., Лепперт М.Ф., Хастедт С.Дж. Еще одно доказательство роли генов на хромосомах 2 и 5 в наследовании легочной функции. Американский журнал респираторной и интенсивной терапии. 2003;168(5):556–61. [PubMed: 127
]
Mall M, Grubb BR, Harkema JR, O’Neal WK, Boucher RC. Повышенное поглощение NA + эпителием дыхательных путей вызывает заболевание легких, подобное муковисцидозу, у мышей. Природная медицина. 2004; 10(5):487–9.3. [PubMed: 15077107]
Мао Дж.Т., Ташкин Д.П., Беллони П.Н., Бейлихили И., Барателли Ф., Рот М.Д. All- транс- ретиноевая кислота модулирует баланс матриксной металлопротеиназы-9 и тканевого ингибитора металлопротеиназы-1 у пациентов с эмфиземой. Грудь. 2003;124(5):1724–32. [PubMed: 14605041]
Marangon K, Herbeth B, Lecomte E, Paul-Dauphin A, Grolier P, Chancerelle Y, Artur Y, Siest G. Диета, антиоксидантный статус и привычки к курению у французских мужчин. Американский журнал клинического питания. 1998;67(2):231–9. [PubMed: 9459370]
Диета, антиоксидантный статус и привычки к курению у французских мужчин. Американский журнал клинического питания. 1998;67(2):231–9. [PubMed: 9459370]
Марклунд С.Л. Внеклеточная супероксиддисмутаза в тканях человека и линиях клеток человека. Журнал клинических исследований. 1984;74(4):1398–403. [Бесплатная статья PMC: PMC425307] [PubMed: 6541229]
Martin TR, Frevert CW. Врожденный иммунитет в легких. Труды Американского торакального общества. 2005;2(5):403–11. [Бесплатная статья PMC: PMC2713330] [PubMed: 16322590]
Martonen TB. Характер отложения сигаретного дыма в дыхательных путях человека. Журнал Американской ассоциации промышленной гигиены. 1992;53(1):6–18. [PubMed: 15
Marwick JA, Kirkham P, Gilmour PS, Donaldson K, Mac-Nee W, Rahman I. Вызванный сигаретным дымом окислительный стресс и TGF-β1 увеличивают экспрессию p21 waf1/cip1 в альвеолярном эпителии клетки. Анналы Нью-Йоркской академии наук. 2002; 973: 278–83. [PubMed: 12485877]
2002; 973: 278–83. [PubMed: 12485877]
Marwick JA, Kirkham PA, Stevenson CS, Danahay H, Giddings J, Butler K, Donaldson K, MacNee W, Rahman I. Сигаретный дым изменяет ремоделирование хроматина и индуцирует провоспалительные гены в легких крыс. Американский журнал респираторных клеток и молекулярной биологии. 2004;31(6):633–42. [В паблике: 15333327]
Мейсон Р.Дж., Броддус В.К., Мюррей Дж.Ф., Надель Дж.А. Учебник Мюррея и Наделя по респираторной медицине. 4-е изд. Сент-Луис: Эльзевир; 2005.
Массаро Д., Массаро Г.Д. Голодная болезнь и легочные альвеолы. Американский журнал респираторной и интенсивной терапии. 2004;170(7):723–4. [PubMed: 15447950]
Мацуба К., Терлбек В.М. Количество и размеры мелких дыхательных путей в эмфизематозных легких. Американский журнал патологии. 1972;67(2):265–75. [Бесплатная статья PMC: PMC2032597] [PubMed: 5021102]
Mattson JP, Sun J, Murray DM, Poole DC. Перекисное окисление липидов в скелетных мышцах хомяков с эмфиземой. Патофизиология. 2002;8(3):215–21. [PubMed: 12039654]
Патофизиология. 2002;8(3):215–21. [PubMed: 12039654]
Майер А.К., Дальпке А.Х. Регуляция местного иммунитета эпителиальными клетками дыхательных путей. Архив иммунологии и экспериментальной терапии. 2007;55(6):353–62. [PubMed: 18060372]
Майер А.С., Столлер Дж.К., Бартельсон Б.Б., Руттенбер А.Дж., Сандхаус Р.А., Ньюман Л.С. Риски профессионального облучения у лиц с PI*Z α 1 -дефицит антитрипсина. Американский журнал респираторной и интенсивной терапии. 2000; 162 (2 часть 1): 553–8. [PubMed: 10
Мазиак В., Лукидес С., Калпитт С., Салливан П., Харитонов С.А., Барнс П.Дж. Выдыхаемый оксид азота при хронической обструктивной болезни легких. Американский журнал респираторной и интенсивной терапии. 1998; 157 (3 часть 1): 998–1002. [PubMed: 9517624]
McCallum WG. Виды повреждений — непроходимость дыхательных путей. Учебник патологии. 7-е изд. MacCallum WG, редактор. Филадельфия: В. Б. Сондерс; 1940. С. 419–28.
С. 419–28.
Маккей П.Б. Витамин Е: взаимодействие со свободными радикалами и аскорбатом. Ежегодный обзор питания. 1985; 5: 323–40. [PubMed: 29]
McCloskey SC, Patel BD, Hinchliffe SJ, Reid ED, Wareham NJ, Lomas DA. Братья и сестры пациентов с тяжелой хронической обструктивной болезнью легких имеют значительный риск обструкции дыхательных путей. Американский журнал респираторной и интенсивной терапии. 2001; 164 (8 ч. 1): 1419–24. [PubMed: 11704589]
МакКорд Дж. М., Фридович И. Использование супероксиддисмутазы в изучении свободнорадикальных реакций. II: механизм опосредования восстановления цитохрома с различными переносчиками электронов. Журнал биологической химии. 1970; 245(6):1374–1377. [PubMed: 5462997]
Маклин К.Х. Макроскопическая анатомия эмфиземы легких. Австралийские анналы медицины. 1956; 5 (2): 73–88. [PubMed: 13355793]
Мид Дж., Тернер Дж.М., Маклем П.Т., Литтл Дж.Б. Значение взаимосвязи между отдачей легких и максимальным потоком выдоха. Журнал прикладной физиологии. 1967;22(1):95–108. [PubMed: 6017658]
Журнал прикладной физиологии. 1967;22(1):95–108. [PubMed: 6017658]
Мейстер А., Андерсон М.Э. Глутатион. Ежегодный обзор биохимии. 1983; 52: 711–60. [PubMed: 6137189]
Мерсер Б.А., Колесникова Н., Сонетт Дж., Д’Армьенто Дж. Внеклеточно регулируемая киназа/митоген-активируемая протеинкиназа активируется при эмфиземе легких и опосредует индукцию матриксной металлопротеиназы-1 сигаретным дымом . Журнал биологической химии. 2004;279(17):17690–6. [PubMed: 14764579]
Минемацу Н., Накамура Х., Татено Х., Накадзима Т., Ямагути К. Генетический полиморфизм матриксной металлопротеиназы-9 и эмфизема легких. Коммуникации биохимических и биофизических исследований. 2001; 289(1):116–9. [PubMed: 11708786]
Molet S, Belleguic C, Lena H, Germain N, Bertrand CP, Shapiro SD, Planquois J-M, Delaval P, Lagente V. Увеличение эластазы макрофагов (MMP-12) в легких у пациентов с хроническое обструктивное заболевание легких. Исследование воспаления. 2005;54(1):31–6. [В паблике: 15723202]
2005;54(1):31–6. [В паблике: 15723202]
Монто А.С., Хиггинс М.В., Росс Х.В. Исследование респираторных заболеваний Tecumseh. VIII: острая инфекция при хронических заболеваниях органов дыхания и группы сравнения. Американский обзор респираторных заболеваний. 1975;111(1):27–36. [PubMed: 163065]
Montuschi P, Collins JV, Ciabattoni G, Lazzeri N, Corradi M, Haritonov SA, Barnes PJ. Выдыхаемый 8-изопростан как биомаркер in vivo окислительного стресса легких у пациентов с ХОБЛ и здоровых курильщиков. Американский журнал респираторной и интенсивной терапии. 2000; 162 (3 части 1): 1175–7. [В паблике: 10988150]
Монтуши П., Харитонов С.А., Барнс П.Дж. Выдыхаемый угарный газ и оксид азота при ХОБЛ. Грудь. 2001;120(2):496–501. [PubMed: 11502649]
Morgan MDL. Буллезная болезнь легких. Хроническое обструктивное заболевание легких. Calverley PMA, Pride NB, редакторы. Лондон: Чепмен и Холл; 1995. стр. 547–60.
Моррисон Д. , Рахман И., Ланнан С., МакНи В. Проницаемость эпителия, воспаление и окислительный стресс в воздушных пространствах курильщиков. Американский журнал респираторной и интенсивной терапии. 1999;159(2):473–9. [PubMed: 9
, Рахман И., Ланнан С., МакНи В. Проницаемость эпителия, воспаление и окислительный стресс в воздушных пространствах курильщиков. Американский журнал респираторной и интенсивной терапии. 1999;159(2):473–9. [PubMed: 9
0]
Morrison D, Skwarski K, Millar AM, Adams W, MacNee W. Сравнение трех методов измерения 99m Tc-DTPA клиренса легких и их воспроизводимость. Европейский респираторный журнал. 1998а; 11(5):1141–6. [PubMed: 9648969]
Morrison D, Strieter RM, Donnelly SC, Burdick MD, Kunkel SL, MacNee W. Нейтрофильные хемокины в жидкости бронхоальвеолярного лаважа и кондиционированной лейкоцитами среде у некурящих и курильщиков. Европейский респираторный журнал. 1998б; 12(5):1067–72. [PubMed: 9863998]
Морроу Д.Д., Фрей Б., Лонгмайр А.В., Газиано Д.М., Линч С.М., Шир Ю., Штраус В.Е., Оутс Д.А., Робертс Л.Дж. II. Увеличение циркулирующих продуктов перекисного окисления липидов (F 2 -изопростаны) у курильщиков: курение как причина окислительного повреждения. Медицинский журнал Новой Англии. 1995;332(18):1198–203. [PubMed: 7700313]
Медицинский журнал Новой Англии. 1995;332(18):1198–203. [PubMed: 7700313]
Мотояма Т., Кавано Х., Кугияма К., Хирасима О., Огуши М., Йошимура М., Огава Х., Ясуэ Х. Эндотелий-зависимая вазодилатация плечевой артерии нарушена у курильщиков: влияние витамина С , Американский журнал физиологии. 1997;273(4 часть 2):h2644–h2650. [PubMed:
Mukae H, Hogg JC, English D, Vincent R, van Eeden SF. Фагоцитоз твердых загрязнителей воздуха альвеолярными макрофагами человека стимулирует костный мозг. Американский журнал физиологии — клеточная и молекулярная биология легких. 2000;279(5):L924–L931. [PubMed: 11053029]
Мукаэ Х., Винсент Р., Куинлан К., Инглиш Д., Хардс Дж., Хогг Дж.С., ван Иден С.Ф. Эффект многократного воздействия загрязнения воздуха твердыми частицами (PM 10 ) на костный мозг. Американский журнал респираторной и интенсивной терапии. 2001;163(1):201–9. [PubMed: 11208647]
Muley T, Wiebel M, Schulz V, Ebert W. Эластинолитическая активность альвеолярных макрофагов при эмфиземе легких, связанной с курением. Клинический исследователь. 1994;72(4):269–76. [PubMed: 8043973]
Эластинолитическая активность альвеолярных макрофагов при эмфиземе легких, связанной с курением. Клинический исследователь. 1994;72(4):269–76. [PubMed: 8043973]
Маллен Дж. Б., Райт Дж. Л., Виггс Б. Р., Паре П. Д., Хогг Д. К. Переоценка воспаления дыхательных путей при хроническом бронхите. BMJ (Британский медицинский журнал). 1985;291(6504):1235–9. [Бесплатная статья PMC: PMC1417096] [PubMed: 3
Munro LH, Burton G, Kelly FJ. Концентрации RRR-альфа-токоферола в плазме ниже у курильщиков, чем у некурящих, после приема аналогичной пероральной дозы этого витамина-антиоксиданта. Клиническая наука (Лондон). 1997;92(1):87–93. [PubMed:
Murphy TF, Brauer AL, Grant BJ, Sethi S. Moraxella catarrhalis при хронической обструктивной болезни легких: бремя болезни и иммунный ответ. Американский журнал респираторной и интенсивной терапии. 2005;172(2):195–9. [Бесплатная статья PMC: PMC2718466] [PubMed: 15805178]
Надель Дж. А. Роль активации рецептора эпидермального фактора роста в регуляции синтеза муцина. Дыхательные исследования. 2001;2(2):85–9. [Бесплатная статья PMC: PMC59573] [PubMed: 11686870]
А. Роль активации рецептора эпидермального фактора роста в регуляции синтеза муцина. Дыхательные исследования. 2001;2(2):85–9. [Бесплатная статья PMC: PMC59573] [PubMed: 11686870]
Нагаиши С. Лимфатическая система. Функциональная анатомия и гистология легких. Нагаиши С, редактор. Балтимор: University Park Press; 1972. стр. 102–79.
Накаяма Т., Черч, Д.Ф., Прайор, Вашингтон. Количественный анализ пероксида водорода, образующегося в водных экстрактах сигаретной смолы. Свободнорадикальная биология и медицина. 1989;7(1):9–15. [PubMed: 2753397]
Натан С., Се Q-W. Регуляция биосинтеза оксида азота. Журнал биологической химии. 1994;269(19):13725–8. [PubMed: 7514592]
Niewohner DE. Курение сигарет, воспаление легких и развитие эмфиземы легких. Журнал лабораторной и клинической медицины. 1988;111(1):15–27. [PubMed: 3275730]
Niewoehner DE, Kleinerman J, Rice DB. Патологические изменения периферических дыхательных путей у молодых курильщиков сигарет. Медицинский журнал Новой Англии. 1974;291(15):755–8. [PubMed: 4414996]
Медицинский журнал Новой Англии. 1974;291(15):755–8. [PubMed: 4414996]
Нин В., Ли Си-Джей, Камински Н., Фегали-Боствик К.А., Альбер С.М., Ди Ю.П., Оттербейн С.Л., Сонг Р., Хаяши С., Чжоу З. и др. Комплексные профили экспрессии генов раскрывают пути, связанные с патогенезом хронической обструктивной болезни легких. Труды Национальной академии наук Соединенных Штатов Америки. 2004;101(41):14895–900. [Бесплатная статья PMC: PMC522001] [PubMed: 15469929]
Нишикава М., Какемизу Н., Ито Т., Кудо М., Канеко Т., Сузуки М., Удауа Н., Икеда Х., Окубо Т. Супероксид опосредует инфильтрацию, вызванную сигаретным дымом. нейтрофилов в дыхательные пути посредством активации ядерного фактора-κB и экспрессии мРНК IL-8 у морских свинок in vivo. Американский журнал респираторных клеток и молекулярной биологии. 1999;20(2):189–98. [PubMed: 9
9] Noronha-Dutra AA, Epperlein MM, Woolf N. Влияние курения сигарет на культивируемые эндотелиальные клетки человека. Сердечно-сосудистые исследования. 1993;27(5):774–8. [PubMed: 8394208]
Сердечно-сосудистые исследования. 1993;27(5):774–8. [PubMed: 8394208]
Northrop-Clewes CA, Thurnham DI. Мониторинг микроэлементов у курильщиков сигарет. Клиника Химика Акта. 2007; 377(1–2):14–38. [PubMed: 17045981]
Nowak D, Kasielski M, Antczak A, Pietras T, Bialasiewicz P. Повышенное содержание тиобарбитурово-реактивных веществ и перекиси водорода в конденсате выдыхаемого воздуха у пациентов со стабильной хронической обструктивной болезнью легких: нет значительное влияние курения сигарет. Респираторная медицина. 1999;93(6):389–96. [PubMed: 10464820]
Nowak D, Kasielski M, Pietras T, Bialasiewicz P, Antczak A. Курение сигарет не увеличивает уровень перекиси водорода в конденсате выдыхаемого воздуха у пациентов со стабильной ХОБЛ. Архив Monaldi для заболеваний грудной клетки. 1998;53(3):268–73. [PubMed: 9785809]
Oberdörster G, Oberdörster E, Oberdörster J. Нанотоксикология: развивающаяся дисциплина, развивающаяся в результате изучения сверхтонких частиц. Перспективы гигиены окружающей среды. 2005; 113(7):823–39.. [Бесплатная статья PMC: PMC1257642] [PubMed: 16002369]
Перспективы гигиены окружающей среды. 2005; 113(7):823–39.. [Бесплатная статья PMC: PMC1257642] [PubMed: 16002369]
Огуши Ф., Феллс Г.А., Хаббард Р.К., Штраус С.Д., Кристал Р.Г. α1-антитрипсин Z-типа менее компетентен, чем α1-антитрипсин M1-типа, как ингибитор эластазы нейтрофилов. Журнал клинических исследований. 1987; 80 (5): 1366–74. [Бесплатная статья PMC: PMC442392] [PubMed: 3500183]
Охата М., Судзуки Х. Патогенез спонтанного пневмоторакса с особым упором на ультраструктуру эмфизематозных булл. Грудь. 1980;77(6):771-6. [PubMed: 7398388]
Охниси К., Такаги М., Курокава Ю., Сатоми С., Конттинен Ю.Т. Опосредованная металлопротеиназой матрикса деградация белка внеклеточного матрикса при эмфиземе легких человека. Лабораторные исследования. 1998;78(9):1077–87. [PubMed: 9759652]
О’Шонесси TC, Ансари TW, Барнс NC, Джеффри П.К. Воспаление в биоптатах бронхов у пациентов с хроническим бронхитом: обратная связь CD8+ Т-лимфоцитов с ОФВ 1 . Американский журнал респираторной и интенсивной терапии. 1997;155(3):852–7. [PubMed:
Американский журнал респираторной и интенсивной терапии. 1997;155(3):852–7. [PubMed:
Otis AB, McKerrow CB, Bartlett RA, Mead J, McIlRoy MB, Selverstone NJ, Radford EP. Механические факторы в распределении легочной вентиляции. Журнал прикладной физиологии. 1956; 8 (4): 427–443. [PubMed: 13286206]
Oury TD, Day BJ, Crapo JD. Внеклеточная супероксиддисмутаза: регулятор биодоступности оксида азота. Лабораторные исследования. 1996;75(5):617–36. [PubMed: 8941209]
Пабст Р., Герке И. Является ли лимфоидная ткань, связанная с бронхами (БАЛТ), неотъемлемой структурой легких нормальных млекопитающих, включая человека? Американский журнал респираторных клеток и молекулярной биологии. 1990;3(2):131–5. [PubMed: 2378747]
Паланж П., Форте С., Фелли А., Галассетти П., Серра П., Карлоне С. Состояние питания и толерантность к физической нагрузке у пациентов с ХОБЛ. Грудь. 1995;107(5):1206–12. [PubMed: 7750307]
Палмер Л. Дж., Целедон Дж. К., Чепмен Х.А., Спейзер Ф.Е., Вайс С.Т., Сильверман Э.К. Полногеномный анализ сцепления бронходилататоров и спирометрических фенотипов после бронхолитиков при хронической обструктивной болезни легких. Молекулярная генетика человека. 2003;12(10):1199–210. [PubMed: 12719384]
Дж., Целедон Дж. К., Чепмен Х.А., Спейзер Ф.Е., Вайс С.Т., Сильверман Э.К. Полногеномный анализ сцепления бронходилататоров и спирометрических фенотипов после бронхолитиков при хронической обструктивной болезни легких. Молекулярная генетика человека. 2003;12(10):1199–210. [PubMed: 12719384]
Палмер Л.Дж., Кнуиман М.В., Дивитини М.Л., Бертон П.Р., Джеймс А.Л., Варфоломей Х.К., Райан Г., Маск А.В. Семейная агрегация и наследственность функции легких у взрослых: результаты исследования здоровья Басселтона. Европейский респираторный журнал. 2001;17(4):696–702. [PubMed: 11401066]
Пардо А., Сельман М. Протеиназно-антипротеиназный дисбаланс в патогенезе эмфиземы: роль металлопротеиназ в повреждении легких. Гистология и гистопатология. 1999;14(1):227–33. [PubMed: 9987667]
Пареди П., Харитонов С., Барнс П.Дж. Анализ выдыхаемого воздуха на продукты окисления. Американский журнал респираторной и интенсивной терапии. 2002; 166 (12 ч. 2): S31–S37. [PubMed: 12471086]
[PubMed: 12471086]
Пареди П., Харитонов С.А., Барнс П.Дж. Повышение концентрации этана в выдыхаемом воздухе при астме. Американский журнал респираторной и интенсивной терапии. 2000a; 162 (4 части 1): 1450–4. [PubMed: 11029360]
Пареди П., Харитонов С.А., Утечка Д., Уорд С., Крамер Д., Барнс П.Дж. Этан в выдыхаемом воздухе, маркер перекисного окисления липидов, повышен при хронической обструктивной болезни легких. Американский журнал респираторной и интенсивной терапии. 2000b; 162 (2 часть 1): 369–73. [PubMed: 10
Паркс Нью-Джерси, Крон К.Дж., Матис К.А., Часко Дж.Х., Гейгер К.Р., Грегор М.Е., Пик Н.Ф. Нитриты и нитраты, меченные азотом-13: распределение и метаболизм после интратрахеального введения. Наука. 1981;212(4490):58–60. [PubMed: 7209517]
Parmentier M, Hirani N, Rahman I, Donaldson K, MacNee W, Antonicelli F. Регуляция опосредованного липополисахаридом высвобождения интерлейкина-1β с помощью N -ацетилцистеина в THP-1 клетки. Европейский респираторный журнал. 2000;16(5):933–9. [PubMed: 11153595]
Европейский респираторный журнал. 2000;16(5):933–9. [PubMed: 11153595]
Parr DG, Stoel BC, Stolk J, Stockley RA. Характер распространения эмфиземы при дефиците α1-антитрипсина влияет на нарушение функции легких. Американский журнал респираторной и интенсивной терапии. 2004;170(11):1172–1178. [PubMed: 15306534]
Патель Р.П., МакЭндрю Дж., Селлак Х., Уайт К.Р., Джо Х., Фриман Б.А., Дарли-Усмар В.М. Биологические аспекты активных форм азота. Биохимика и биофизика Acta. 1999;1411(2–3):385–400. [В паблике: 10320671]
Патиар С., Слэйд Д., Киркпатрик У., МакКоллум К.Н. Курение вызывает дозозависимое увеличение L-селектина, связанного с гранулоцитами. Исследование тромбоза. 2002;106(1):1–6. [PubMed: 12165281]
Patuzzo C, Gilè LS, Zorzetto M, Trabetti E, Malerba G, Pignatti PF, Luisetti M. Генный комплекс фактора некроза опухоли при ХОБЛ и диссеминированных бронхоэктазах. Грудь. 2000;117(5):1353–1358. [PubMed: 10807822]
Pauwels RA, Buist AS, Calverley PM, Jenkins CR, Hurd SS. ЗОЛОТОЙ научный комитет. Глобальная стратегия диагностики, лечения и профилактики хронической обструктивной болезни легких: Итоги семинара Глобальной инициативы NHLBI/ВОЗ по хронической обструктивной болезни легких (GOLD). Американский журнал респираторной и интенсивной терапии. 2001;163(5):1256–76. [В паблике: 11316667]
ЗОЛОТОЙ научный комитет. Глобальная стратегия диагностики, лечения и профилактики хронической обструктивной болезни легких: Итоги семинара Глобальной инициативы NHLBI/ВОЗ по хронической обструктивной болезни легких (GOLD). Американский журнал респираторной и интенсивной терапии. 2001;163(5):1256–76. [В паблике: 11316667]
Пембертон П.А., Кантвелл Дж.С., Ким К.М., Сундин Д.Дж., Кобаяши Д., Финк Дж.Б., Шапиро С.Д., Барр П.Дж. Ингаляционный ингибитор матриксной металлопротеиназы предотвращает эмфизему, вызванную сигаретным дымом, у мышей. Хроническое обструктивное заболевание легких. 2005;2(3):303–10. [PubMed: 17146995]
Petruzzelli S, Puntoni R, Mimotti P, Pulera N, Baliva F, Fornai E, Giuntini C. 3-нитротирозин плазмы у курильщиков сигарет. Американский журнал респираторной и интенсивной терапии. 1997; 156 (6): 1902–1907. [PubMed: 9412573]
Пьетаринен П., Райвио К., Девлин Р.Б., Крапо Д.Д., Чанг Л.И., Киннула В.Л. Каталаза и глутатионредуктаза защищают альвеолярные макрофаги человека при воздействии оксидантов in vitro. Американский журнал респираторных клеток и молекулярной биологии. 1995;13(4):434–41. [PubMed: 7546773]
Американский журнал респираторных клеток и молекулярной биологии. 1995;13(4):434–41. [PubMed: 7546773]
Piitulainen E, Tornling G, Eriksson S. Экологические корреляты нарушения функции легких у некурящих с тяжелым дефицитом α 1 -антитрипсина (PiZZ). грудная клетка. 1998;53(11):939–43. [Бесплатная статья PMC: PMC1745103] [PubMed: 101
Pinamonti S, Leis M, Barbieri A, Leoni D, Muzzoli M, Sostero S, Chicca MC, Carrieri A, Ravenna F, Fabbri LM, et al. Обнаружение продуктов активности ксантиноксидазы методами ЭПР и ВЭЖХ в жидкости бронхоальвеолярного лаважа у пациентов с хронической обструктивной болезнью легких. Свободнорадикальная биология и медицина. 1998;25(7):771–9. [PubMed: 9823542]
Pinamonti S, Muzzoli M, Chicca MC, Papi A, Ravenna F, Fabbri LM, Ciaccia A. Активность ксантиноксидазы в жидкости бронхоальвеолярного лаважа у пациентов с хронической обструктивной болезнью легких. Свободнорадикальная биология и медицина. 1996;21(2):147–55. [PubMed: 8818629]
1996;21(2):147–55. [PubMed: 8818629]
Пино Ф., Бачелет М., Франсуа Д., Полла Б.С., Валти Х. Модифицированный натуральный поверхностно-активный агент свиньи модулирует стрессовую реакцию моноцитов человека, вызванную табачным дымом. Науки о жизни. 1999;64(2):125–34. [PubMed: 10069490]
Поллер В., Фабер Дж. П., Вайдингер С., Тиф К., Шольц С., Фишер М., Олек К., Кирхгессер М., Хайдтманн Х.-Х. Замена лейцина на пролин вызывает дефектный аллель α 1 -антихимотрипсина, связанный с семейной обструктивной болезнью легких. Геномика. 1993;17(3):740–3. [PubMed: 8244391]
Postma DS, Timens W. Ремоделирование при астме и хронической обструктивной болезни легких. Труды Американского торакального общества. 2006;3(5):434–9. [PubMed: 16799088]
Пауэлл GM, Грин GM. Исследование влияния сигаретного дыма на альвеолярные макрофаги кролика. Биохимический журнал. 1971;124(2):26P–27P. [Статья бесплатно PMC: PMC1177198] [PubMed: 5158487]
Powis G, Mustacich D, Coon A. Роль окислительно-восстановительного белка тиоредоксина в росте клеток и раке. Свободнорадикальная биология и медицина. 2000;29(3–4): 312–22. [PubMed: 11035260]
Роль окислительно-восстановительного белка тиоредоксина в росте клеток и раке. Свободнорадикальная биология и медицина. 2000;29(3–4): 312–22. [PubMed: 11035260]
Praticò D, Basili S, Vieri M, Cordova C, Violi F, FitzGerald GA. Хроническая обструктивная болезнь легких связана с повышением уровня изопростана F 2 α-III в моче, что является показателем оксидантного стресса. Американский журнал респираторной и интенсивной терапии. 1998;158(6):1709–14. [PubMed: 9847257]
Profita M, Chiappara G, Mirabella F, Di Giorgi R, Chimenti L, Costanzo G, Riccobono L, Bellia V, Bousquet J, Vignola AM. Влияние циломиласта (Арифло) на высвобождение TNF-α, IL-8 и GM-CSF клетками дыхательных путей у пациентов с ХОБЛ. грудная клетка. 2003; 58 (7): 573–9.. [Бесплатная статья PMC: PMC1746747] [PubMed: 12832668]
Proudfoot AE. Хемокиновые рецепторы: многогранные терапевтические мишени. Обзоры природы Иммунология. 2002;2(2):106–15. [Статья бесплатно PMC: PMC7097668] [PubMed: 11
Прайор В. А., Стоун К. Окислители в сигаретном дыме: радикалы, перекись водорода, пероксинитрат и пероксинитрит. Анналы Нью-Йоркской академии наук. 1993; 686: 12–27. [PubMed: 8512242]
А., Стоун К. Окислители в сигаретном дыме: радикалы, перекись водорода, пероксинитрат и пероксинитрит. Анналы Нью-Йоркской академии наук. 1993; 686: 12–27. [PubMed: 8512242]
Набережная Дж.Л., Рид В., Самет Дж., Девлин Р.Б. Частицы загрязнения воздуха индуцируют экспрессию гена IL-6 в эпителиальных клетках дыхательных путей человека посредством активации NF-κB. Американский журнал респираторных клеток и молекулярной биологии. 1998;19(1):98–106. [PubMed: 9651185]
Rabe KF, Hurd S, Anzueto A, Barnes PJ, Buist SA, Calverley P, Fukuchi Y, Jenkins C, Rodriquez-Roisin R, van Weel C, et al. Глобальная стратегия диагностики, лечения и профилактики хронической обструктивной болезни легких: резюме GOLD. Американский журнал респираторной и интенсивной терапии. 2007;176(6):532–55. [PubMed: 17507545]
Rafii S, Meeus S, Dias S, Hattori K, Heissig B, Shmelkov S, Rafii D, Lyden D. Вклад предшественников костного мозга в регенерацию сосудов и сердца. Семинары по клеточной биологии и биологии развития. 2002;13(1):61–7. [В паблике: 11969372]
Семинары по клеточной биологии и биологии развития. 2002;13(1):61–7. [В паблике: 11969372]
Rahman I, Bel A, Mulier B, Donaldson K, MacNee W. Дифференциальная регуляция глутатиона оксидантами и дексаметазоном в клетках альвеолярного эпителия. Американский журнал физиологии. 1998; 275 (1 часть 1): L80–L86. [PubMed: 9688938]
Rahman I, MacNee W. Роль факторов транскрипции в воспалительных заболеваниях легких. грудная клетка. 1998;53(7):601–12. [Статья бесплатно PMC: PMC1745272] [PubMed: 9797762]
Rahman I, MacNee W. Глутатион легких и окислительный стресс: последствия для заболеваний дыхательных путей, вызванных сигаретным дымом. Американский журнал физиологии. 1999;277(6 ч. 1):L1067–L1088. [PubMed: 10600876]
Rahman I, MacNee W. Регуляция уровней окислительно-восстановительного глутатиона и транскрипция генов при воспалении легких: терапевтические подходы. Свободнорадикальная биология и медицина. 2000;28(9):1405–20. [PubMed: 109]
[PubMed: 109]
Рахман И., Моррисон Д., Дональдсон К., Макни В. Системный окислительный стресс при астме, ХОБЛ и курильщиках. Американский журнал респираторной и интенсивной терапии. 1996а; 154 (4 часть 1): 1055–60. [В паблике: 8887607]
Rahman I, Smith CAD, Lawson MF, Harrison DJ, MacNee W. Индукция γ-глутамилцистеинсинтетазы сигаретным дымом связана с AP-1 в клетках альвеолярного эпителия человека. Письма ФЭБС. 1996б; 396(1):21–5. [PubMed: 8
Рахман И., ван Шадевийк А.А., Кроутер А.Дж., Хиемстра П.С., Столк Дж., МакНи В., ДеБук В.И. 4-гидрокси-2-ноненаль, специфический продукт перекисного окисления липидов, повышен в легких у пациентов с хронической обструктивной болезнью легких. Американский журнал респираторной и интенсивной терапии. 2002;166(4):490–5. [PubMed: 12186826]
Ramezanian MS, Padmaja S, Koppenol WH. Нитрование и гидроксилирование фенольных соединений пероксинитритом. Химические исследования в токсикологии. 1996;9(1):232–40. [PubMed: 8
1996;9(1):232–40. [PubMed: 8
Rangasamy T, Cho CY, Thimmulappa RK, Zhen L, Srisuma SS, Kensler TW, Yamamoto M, Petrache I, Tuder RM, Biswal S. Генетическое удаление Nrf2 повышает восприимчивость к сигаретному дыму эмфизема у мышей. Журнал клинических исследований. 2004;114(9): 1248–59. [Бесплатная статья PMC: PMC524225] [PubMed: 15520857]
Redline S, Tishler PV, Lewitter FI, Tager IB, Munoz A, Speizer FE. Оценка генетических и негенетических влияний на легочную функцию: исследование близнецов. Американский обзор респираторных заболеваний. 1987;135(1):217–22. [PubMed: 3800147]
Рейд Л. Измерение слоя бронхиальной слизистой железы: диагностический критерий при хроническом бронхите. грудная клетка. 1960; 15: 132–41. [Бесплатная статья PMC: PMC1018549] [PubMed: 14437095]
Репин Дж. Э., Баст А., Ланкхорст И. Окислительный стресс при хронической обструктивной болезни легких. Группа изучения окислительного стресса. Американский журнал респираторной и интенсивной терапии. 1997; 156 (2 часть 1): 341–57. [PubMed: 09]
Американский журнал респираторной и интенсивной терапии. 1997; 156 (2 часть 1): 341–57. [PubMed: 09]
Retamales I, Elliott WM, Meshi B, Coxson HO, Paré PD, Sciurba FC, Rogers RM, Hayashi S, Hogg JC. Усиление воспаления при эмфиземе легких и его связь с латентной аденовирусной инфекцией. Американский журнал респираторной и интенсивной терапии. 2001;164(3):469–73. [PubMed: 11500352]
Рейес М., Дудек А., Джахагирдар Б., Куди Л., Маркер П.Х., Верфайли К.М. Происхождение эндотелиальных предшественников в постнатальном костном мозге человека. Журнал клинических исследований. 2002;109(3):337–46. [Бесплатная статья PMC: PMC150857] [PubMed: 11827993]
Reynolds HY. Бронхоальвеолярный лаваж. Американский обзор респираторных заболеваний. 1987;135(1):250–63. [PubMed: 3541717]
Ри С.Г., Кан С.В., Нетто Л.Е., Сео М.С., Штадтман Э.Р. Семейство новых пероксидаз, пероксиредоксинов. Биофакторы. 1999;10(2–3):207–9. [PubMed: 10609884]
Ричмонд I, Причард Г. Э., Эшкрофт Т., Эйвери А., Коррис П.А., Уолтерс Э.Х. Бронх-ассоциированная лимфоидная ткань (БАЛТ) в легких человека: ее распределение у курильщиков и некурящих. грудная клетка. 1993;48(11):1130–4. [Бесплатная статья PMC: PMC464898] [PubMed: 8296257]
Э., Эшкрофт Т., Эйвери А., Коррис П.А., Уолтерс Э.Х. Бронх-ассоциированная лимфоидная ткань (БАЛТ) в легких человека: ее распределение у курильщиков и некурящих. грудная клетка. 1993;48(11):1130–4. [Бесплатная статья PMC: PMC464898] [PubMed: 8296257]
Рошель Л.Г., Фишер Б.М., Адлер К.Б. Одновременное производство активных форм кислорода и азота эпителиальными клетками дыхательных путей in vitro. Свободнорадикальная биология и медицина. 1998;24(5):863–8. [PubMed: 9586818]
Роули Д.А., Холливелл Б. Формирование гидроксильных радикалов из перекиси водорода и солей железа с помощью механизмов, зависящих от супероксида и аскорбата: отношение к патологии ревматоидного заболевания. Клиническая наука (Лондон). 1983;64(6):649–53. [PubMed: 6301745]
Rubio ML, Martin-Mosquero MC, Ortega M, Peces-Barba G, Gonzalez-Mangado N. Пероральный N-ацетилцистеин ослабляет индуцированную эластазой эмфизему легких у крыс. Грудь. 2004;125(4):1500–6. [В паблике: 15078764]
Рассел Р. К., Калпитт С.В., ДеМатос С., Доннелли Л., Смит М., Уиггинс Дж., Барнс П.Дж. Высвобождение и активность матриксной металлопротеиназы-9 и тканевого ингибитора металлопротеиназы-1 альвеолярными макрофагами у пациентов с хронической обструктивной болезнью легких. Американский журнал респираторных клеток и молекулярной биологии. 2002а; 26(5):602–9. [PubMed: 11970913]
К., Калпитт С.В., ДеМатос С., Доннелли Л., Смит М., Уиггинс Дж., Барнс П.Дж. Высвобождение и активность матриксной металлопротеиназы-9 и тканевого ингибитора металлопротеиназы-1 альвеолярными макрофагами у пациентов с хронической обструктивной болезнью легких. Американский журнал респираторных клеток и молекулярной биологии. 2002а; 26(5):602–9. [PubMed: 11970913]
Рассел Р.К., Торли А., Калпитт С.В., Додд С., Доннелли Л.Е., Дематтос С., Фитцджеральд М., Барнс П.Дж. Эластолиз, опосредованный альвеолярными макрофагами: роль матриксных металлопротеиназ, цистеиновых и сериновых протеаз. Американский журнал физиологии — клеточная и молекулярная физиология легких. 2002b; 283(4):L867–L873. [В паблике: 12225964]
Rutgers SR, Postma DS, ten Hacken NH, Kauffman HF, van der Mark TW, Koëter GH, Timens W. Текущее воспаление дыхательных путей у пациентов с ХОБЛ, которые в настоящее время не курят. Грудь. 2000; 117 (5 Приложение 1): 262S. [PubMed: 10843943]
Рутгерс С. Р., ван дер Марк Т.В., Курс В., Мошаге Х., Тайменс В., Кауфман Х.Ф., Коэтер Г.Х., Постма Д.С. Маркеры метаболизма оксида азота в мокроте и выдыхаемом воздухе не повышены при хронической обструктивной болезни легких. грудная клетка. 1999;54(7):576–80. [Бесплатная статья PMC: PMC1745531] [PubMed: 10377200]
Р., ван дер Марк Т.В., Курс В., Мошаге Х., Тайменс В., Кауфман Х.Ф., Коэтер Г.Х., Постма Д.С. Маркеры метаболизма оксида азота в мокроте и выдыхаемом воздухе не повышены при хронической обструктивной болезни легких. грудная клетка. 1999;54(7):576–80. [Бесплатная статья PMC: PMC1745531] [PubMed: 10377200]
Ryder RC, Dunnill MS, Anderson JA. Количественное исследование объема бронхиальной слизи, эмфиземы и курения в популяции вскрытий. Журнал патологии. 1971; 104 (1): 59–71. [PubMed: 5568351]
Sabatini F, Petecchia L, Tavian M, Jodon de Villeroche V, Rossi GA, Brouty-Boye D. Бронхиальные фибробласты человека демонстрируют фенотип мезенхимальных стволовых клеток и многолинейные дифференцирующие возможности. Лабораторные исследования. 2005;85(8):962–71. [PubMed: 15
Sabroe I, Parker LC, Dockrell DH, Davies DE, Dower SK, Whyte MKB. Ориентация на сети, лежащие в основе смежного иммунитета при астме и хронической обструктивной болезни легких. Американский журнал респираторной и интенсивной терапии. 2007;175(4):306–11. [PubMed: 17138954]
Американский журнал респираторной и интенсивной терапии. 2007;175(4):306–11. [PubMed: 17138954]
Саэтта М., Мариани М., Панина-Бординьон П., Турато Г., Буонсанти С., Баральдо С., Беллеттато С.М., Папи А., Корбетта Л., Зуин Р. и др. Повышенная экспрессия хемокинового рецептора CXCR3 и его лиганда CXCL10 в периферических дыхательных путях курильщиков с хронической обструктивной болезнью легких. Американский журнал респираторной и интенсивной терапии. 2002; 165(10):1404–9.. [PubMed: 12016104]
Saetta M, Turato G, Facchini FM, Corbino L, Lucchini RE, Casoni G, Maestrelli P, Mapp CE, Ciaccia A, Fabbri LM. Воспалительные клетки в бронхиальных железах курильщиков с хроническим бронхитом. Американский журнал респираторной и интенсивной терапии. 1997; 156 (5): 1633–9. [PubMed:
- 87]
Сакао С., Тацуми К., Игара Х., Шино Ю., Ширасава Х., Курияма Т. Ассоциация полиморфизма промотора гена фактора некроза опухоли α с наличием хронической обструктивной болезни легких. Американский журнал респираторной и интенсивной терапии. 2001;163(2):420–2. [В паблике: 11179116]
Американский журнал респираторной и интенсивной терапии. 2001;163(2):420–2. [В паблике: 11179116]
Сэндфорд А.Дж., Чагани Т., Вейр Т.Д., Коннетт Дж.Е., Антонисен Н.Р., Паре Д.Д. Гены предрасположенности к быстрому снижению функции легких в исследовании здоровья легких. Американский журнал респираторной и интенсивной терапии. 2001;163(2):469–73. [PubMed: 11179124]
Sandford AJ, Chagani T, Weir TD, Paré PD. α 1 — Мутации антихимотрипсина у пациентов с хронической обструктивной болезнью легких. Маркеры заболеваний. 1998;13(4):257–60. [В паблике: 9553741]
Sastre J, Asensi M, Gasco E, Pallardo FV, Ferrero JA, Furukawa T, Vina J. Изнурительные физические упражнения вызывают окисление статуса глутатиона в крови: профилактика путем введения антиоксидантов. Американский журнал физиологии. 1992; 263 (5 часть 2): R992–R995. [PubMed: 1443237]
Шаберг Т., Халлер Х., Рау М., Кайзер Д., Фассбендер М., Лоде Х. Высвобождение супероксидного аниона, индуцированное фактором активации тромбоцитов, увеличивается в альвеолярных макрофагах человека у курильщиков. Европейский респираторный журнал. 1992;5(4):387–93. [PubMed: 1314191]
Европейский респираторный журнал. 1992;5(4):387–93. [PubMed: 1314191]
Шаберг Т., Кляйн У., Рау М., Эллер Дж., Лоде Х. Субпопуляции альвеолярных макрофагов у курильщиков и некурящих: связь с экспрессией молекул CD11/CD18 и выработкой супероксидных анионов. Американский журнал респираторной и интенсивной терапии. 1995; 151 (5): 1551–8. [PubMed: 7735614]
Шелленберг Д., Паре П.Д., Вейр Т.Д., Спинелли Дж.Дж., Уокер Б.А., Сэндфорд А.Дж. Варианты белка, связывающего витамин D, и риск ХОБЛ. Американский журнал респираторной и интенсивной терапии. 1998; 157 (3 ч. 1): 957–61. [PubMed: 9517617]
Scholz H, Yndestad A, Damås JK, Wæhre T, Tonstad S, Aukrust P, Halvorsen B. 8-изопростан увеличивает экспрессию интерлейкина-8 в макрофагах человека посредством активации митоген-активируемых протеинкиназ . Сердечно-сосудистые исследования. 2003;59(4):945–54. [PubMed: 14553834]
Schulz H, Brand P, Heyder J. Отложение частиц в дыхательных путях. Взаимодействие частиц с легкими. Биология легких в норме и болезни. Гер П., Хейдер Дж., редакторы. Том. 143. Нью-Йорк: Марсель Деккер; 2000. стр. 229.–90.
Взаимодействие частиц с легкими. Биология легких в норме и болезни. Гер П., Хейдер Дж., редакторы. Том. 143. Нью-Йорк: Марсель Деккер; 2000. стр. 229.–90.
Скотт Д.А., Постон Р.Н., Уилсон Р.Ф., Кауард П.Ю., Палмер Р.М. Влияние витамина С на системные маркеры активации эндотелиальных и воспалительных клеток у курильщиков и некурящих. Исследование воспаления. 2005;54(3):138–44. [PubMed: 15883748]
Seemungal T, Harper-Owen R, Bhowmik A, Moric I, Sanderson G, Message S, Maccallum P, Meade TW, Jeffries DJ, Johnston SL, et al. Респираторные вирусы, симптомы и маркеры воспаления при обострениях и стабильной хронической обструктивной болезни легких. Американский журнал респираторной и интенсивной терапии. 2001;164(9): 1618–23. [PubMed: 11719299]
Seersholm N, Kok-Jensen A, Dirksen A. Выживаемость пациентов с тяжелым дефицитом альфа-1-антитрипсина с особым упором на неиндексные случаи. грудная клетка. 1994;49(7):695–8. [Статья бесплатно PMC: PMC475060] [PubMed: 8066566]
Seersholm N, Kok-Jensen A, Dirksen A. Снижение ОФВ1 среди пациентов с тяжелой наследственной недостаточностью альфа-1-антитрипсина типа PiZ. Американский журнал респираторной и интенсивной терапии. 1995;152(6 часть 1):1922–5. [PubMed: 8520756]
Снижение ОФВ1 среди пациентов с тяжелой наследственной недостаточностью альфа-1-антитрипсина типа PiZ. Американский журнал респираторной и интенсивной терапии. 1995;152(6 часть 1):1922–5. [PubMed: 8520756]
Segura-Valdez L, Pardo A, Gaxiola M, Uhal BD, Becerril C, Selman M. Активация желатиназ A и B, коллагеназ 1 и 2 и повышенная гибель паренхиматозных клеток при ХОБЛ. Грудь. 2000;117(3):684–94. [PubMed: 10712992]
Seifart C, Plagens A, Brodje D, Muller B, von Wichert P, Floros J. Вариант интрона 4 сурфактантного белка B у немецких пациентов с ХОБЛ и острой дыхательной недостаточностью. Маркеры заболеваний. 2002;18(3):129–36. [Бесплатная статья PMC: PMC3851100] [PubMed: 12515908]
Selman M, Cisneros-Lira J, Gaxiola M, Ramirez R, Kudlacz EM, Mitchell PG, Pardo A. Ингибирование матриксных металлопротеиназ ослабляет индуцированную табачным дымом эмфизему у морских свинок. Грудь. 2003;123(5):1633–41. [PubMed: 12740284]
Selman M, Montaño M, Ramos C, Vanda B, Becerril C, Delgado J, Sansores R, Barrios R, Pardo A. Вызванная табачным дымом эмфизема легких у морских свинок связана с увеличением интерстициальной коллагеназа. Американский журнал физиологии — клеточная и молекулярная физиология легких. 1996 нояб.; 271 (5 ч. 1): L734–L743. [PubMed: 8944716]
Вызванная табачным дымом эмфизема легких у морских свинок связана с увеличением интерстициальной коллагеназа. Американский журнал физиологии — клеточная и молекулярная физиология легких. 1996 нояб.; 271 (5 ч. 1): L734–L743. [PubMed: 8944716]
Сети С., Эванс Н., Грант Б.Дж.Б., Мерфи Т.Ф. Новые штаммы бактерий и обострения хронической обструктивной болезни легких. Медицинский журнал Новой Англии. 2002;347(7):465–71. [PubMed: 12181400]
Шапиро С.Д. Терминальная стадия хронической обструктивной болезни легких: сигарета догорела, но воспаление бушует в [редакционном] Американском журнале респираторной и реаниматологической медицины. 2001;164(3):339–40. [В паблике: 11500330]
Шапиро С.Д. ХОБЛ раскручена. Медицинский журнал Новой Англии. 2005;352(19):2016–9. [PubMed: 15888704]
Шапиро С.Д., ДеМео Д.Л., Сильверман Э.К. Дым и зеркала: мышиные модели как отражение хронической обструктивной болезни легких человека. Американский журнал респираторной и интенсивной терапии. 2004;170(9):929–31. [PubMed: 15504815]
2004;170(9):929–31. [PubMed: 15504815]
Шапиро С.Д., Гольдштейн Н.М., Хоутон А.М., Кобаяши Д.К., Келли Д., Белаауай А. Эластаза нейтрофилов способствует развитию эмфиземы, вызванной сигаретным дымом, у мышей. Американский журнал патологии. 2003;163(6):2329–35. [Бесплатная статья PMC: PMC18
] [PubMed: 14633606]
Сильверман Э.К., Чепмен Х.А., Дрейзен Дж.М., Вайс С.Т., Рознер Б., Кэмпбелл Э.Дж., О’Доннелл В.Дж., Рейли Дж.Дж., Джиннс Л., Ментцер С. и др. . Генетическая эпидемиология тяжелой хронической обструктивной болезни легких с ранним началом: риск обструкции дыхательных путей и хронического бронхита для родственников. Американский журнал респираторной и интенсивной терапии. 1998; 157 (6 ч. 1): 1770–8. [PubMed: 9620904]
Silverman EK, Mosley JD, Palmer LJ, Barth M, Senter JM, Brown A, Drazen JM, Kwiatkowski DJ, Chapman HA, Campbell EJ и др. Полногеномный анализ сцепления тяжелой хронической обструктивной болезни легких с ранним началом: обструкция дыхательных путей и фенотипы хронического бронхита. Молекулярная генетика человека. 2002а; 11(6):623–32. [В паблике: 11
Молекулярная генетика человека. 2002а; 11(6):623–32. [В паблике: 11
7]. Полногеномный анализ сцепления количественных спирометрических фенотипов при тяжелой хронической обструктивной болезни легких с ранним началом. Американский журнал генетики человека. 2002b;70(5):1229–39. [Бесплатная статья PMC: PMC447597] [PubMed: 11
Сильверман Э.К., Пирс Дж.А., Провинция Массачусетс, Рао, округ Колумбия, Кэмпбелл Э.Дж. Вариабельность легочной функции при дефиците альфа-1-антитрипсина: клинические корреляты. Анналы внутренней медицины. 1989;111(12):982–91. [PubMed: 2596778]
Сильверман Э.К., Провинция М.А., Кэмпбелл Э.Дж., Пирс Дж.А., Рао Д.К., Бурвинкль Э. Семейное исследование дефицита α1-антитрипсина: влияние курения сигарет, измеренный генотип и их взаимодействие на функцию легких и биохимические признаки. Генетическая эпидемиология. 1992;9(5):317–31. [PubMed: 1427021]
Сингх С., Эванс Т.В. Оксид азота, биологический медиатор десятилетия: правда или вымысел? Европейский респираторный журнал. 1997;10(3):699–707. [PubMed:
1997;10(3):699–707. [PubMed:
Skwarski KM, Gorecka D, Sliwinski P, Hogg JC, MacNee W. Влияние курения сигарет на легочную гемодинамику. Грудь. 1993;103(4):1166–72. [PubMed: 8131459]
Слот JW, Geuze HJ, Freeman BA, Crapo JD. Внутриклеточная локализация медно-цинковой и марганцевой супероксиддисмутаз в паренхиматозных клетках печени крысы. Лабораторные исследования. 1986;55(3):363–71. [PubMed: 3747450]
Smith CA, Harrison DJ. Ассоциация между полиморфизмом гена микросомальной эпоксидгидролазы и предрасположенностью к эмфиземе. Ланцет. 1997;350(9078):630–3. [PubMed: 46]
Smith CB, Golden CA, Kanner RE, Renzetti AD Jr. Ассоциация вирусных и Mycoplasma pneumoniae инфекций с острыми респираторными заболеваниями у пациентов с хроническими обструктивными заболеваниями легких. Американский обзор респираторных заболеваний. 1980;121(2):225–32. [PubMed: 6244766]
Снайдер Г.Л., Кляйнерман Дж. , Терлбек В.М., Бенгали З.Х. Определение эмфиземы: отчет Национального института сердца, легких и крови, Отдел семинара по заболеваниям легких. Американский обзор респираторных заболеваний. 1985;132(1):182–5. [PubMed: 4014865]
, Терлбек В.М., Бенгали З.Х. Определение эмфиземы: отчет Национального института сердца, легких и крови, Отдел семинара по заболеваниям легких. Американский обзор респираторных заболеваний. 1985;132(1):182–5. [PubMed: 4014865]
Соэдзима К., Ямагути К., Кода Э., Такэсита К., Ито Ю., Мастубара Х., Огума Т., Иноуэ Т., Окубо Ю., Амакава К. и др. Продольное последующее исследование изменений плотности легких, вызванных курением, с помощью компьютерной томографии высокого разрешения. Американский журнал респираторной и интенсивной терапии. 2000; 161 (4 часть 1): 1264–73. [PubMed: 10764322]
Soini Y, Näpänkangas U, Jarvinen K, Kaarteenaho-Wiik R, Pääkkö P, Kinnula VL. Экспрессия γ-глутамилцистеинсинтетазы при немелкоклеточном раке легкого. Рак. 2001;92(11):2911–9. [PubMed: 11753966]
Солер Н., Эвиг С., Торрес А., Филелла X, Гонсалес Дж., Заубет А. Воспаление дыхательных путей и бронхиальные микробные паттерны у пациентов со стабильной хронической обструктивной болезнью легких. Европейский респираторный журнал. 1999;14(5):1015–22. [PubMed: 10596683]
Европейский респираторный журнал. 1999;14(5):1015–22. [PubMed: 10596683]
Speizer FE, Rosner B, Tager I. Семейная агрегация хронических респираторных заболеваний: использование данных опроса National Health Interview Survey для проверки конкретной гипотезы. Международный журнал эпидемиологии. 1976;5(2):167–72. [PubMed: 955766]
Спира А., Бин Дж., Пинто-Плата В., Кадар А., Лю Г., Шах В., Челли Б., Броди Дж.С. Профилирование экспрессии генов в легочной ткани человека от курильщиков с тяжелой эмфиземой. Американский журнал респираторных клеток и молекулярной биологии. 2004;31(6):601–10. [PubMed: 15374838]
Stangel M, Zettl UK, Mix E, Zielasek J, Toyka KV, Hartung HP, Gold R. h3O2 и окислительный стресс, опосредованный оксидом азота, вызывают апоптоз в миобластах скелетных мышц крыс. Журнал невропатологии и экспериментальной неврологии. 1996;55(1):36–43. [PubMed: 8558170]
Стокли Р.А. Протеазы и антипротеазы. Симпозиум Фонда Novartis. 2001; 234:189–99. [PubMed: 11199096]
2001; 234:189–99. [PubMed: 11199096]
Стокли Р.А., Кэмпбелл Э.Дж. Генотипирование альфа-1-антитрипсина с помощью образцов жидкости для полоскания рта. Европейский респираторный журнал. 2001;17(3):356–9. [PubMed: 11405511]
Stolk J, Nieuwenhuizen W, Stoller JK, Aboussouan L. Высокие дозы внутривенного AAT и фрагменты фибриногена, полученные из нейтрофилов плазмы. грудная клетка. 2005;60(1):84. [Бесплатная статья PMC: PMC1747165] [PubMed: 15618590]
Столлер Дж.К., Абуссуан Л.С. α 1 — Дефицит антитрипсина. 5: внутривенная аугментационная терапия: текущее понимание. грудная клетка. 2004;59(8):708–12. [Бесплатная статья PMC: PMC1747086] [PubMed: 15282394]
Stone PJ, Gottlieb DJ, O’Connor GT, Ciccolella DE, Breuer R, Bryan-Rhadfi J, Shaw HA, Franzblau C, Snider GL. Продукты деградации эластина и коллагена в моче курильщиков с хронической обструктивной болезнью легких и без нее. Американский журнал респираторной и интенсивной терапии. 1995;151(4):952–9. [PubMed: 7697272]
1995;151(4):952–9. [PubMed: 7697272]
Szulakowski P, Crowther AJL, Jimenez LA, Donaldson K, Mayer R, Leonard TB, MacNee W, Drost E. Влияние курения на транскрипционную регуляцию воспаления легких у пациентов с хронической обструктивной болезнью легких болезнь. Американский журнал респираторной и интенсивной терапии. 2006;174(1):41–50. [PubMed: 16574938]
Tager I, Tishler PV, Rosner B, Speizer FE, Litt M. Исследования семейной агрегации хронического бронхита и обструктивных заболеваний дыхательных путей. Международный журнал эпидемиологии. 1978;7(1):55–62. [PubMed: 659050]
Takeyabu K, Betsuyaku T, Nishimura M, Yoshioka A, Tanino M, Miyamoto K, Kawakami Y. Цистеиновые протеиназы и цистатин C в жидкости бронхоальвеолярного лаважа у субъектов с субклинической эмфиземой. Европейский респираторный журнал. 1998;12(5):1033–9. [PubMed: 9863993]
Takeyabu K, Yamaguchi E, Suzuki I, Nishimura M, Hizawa N, Kamakami Y. Полиморфизм гена микросомальной эпоксидгидролазы и восприимчивость к эмфиземе у населения Японии. Европейский респираторный журнал. 2000;15(5):891–4. [PubMed: 10853854]
Европейский респираторный журнал. 2000;15(5):891–4. [PubMed: 10853854]
Такеяма К., Даббаг К., Чон Шим Дж., Дао-Пик Т., Уэки И.Ф., Надель Дж.А. Окислительный стресс вызывает синтез муцина посредством трансактивации рецептора эпидермального фактора роста: роль нейтрофилов. Журнал иммунологии. 2000;164(3):1546–52. [PubMed: 10640773]
Такеяма К., Даббаг К., Ли Х.М., Агусти С., Лаузье Дж.А., Уэки И.Ф., Граттан К.М., Надель Дж.А. Система эпидермального фактора роста регулирует выработку муцина в дыхательных путях. Труды Национальной академии наук Соединенных Штатов Америки. 1999;96(6):3081–6. [Бесплатная статья PMC: PMC15898] [PubMed: 10077640]
Takeyama K, Fahy JV, Nadel JA. Связь рецепторов эпидермального фактора роста с продукцией бокаловидных клеток в бронхах человека. Американский журнал респираторной и интенсивной терапии. 2001а; 163(2):511–6. [PubMed: 11179132]
Такеяма К., Юнг Б., Шим Дж.Дж., Бургель П.Р., Дао-Пик Т. , Уэки И.Ф., Протин Ю., Крошель П., Надель Дж.А. Активация рецепторов эпидермального фактора роста отвечает за синтез муцина, индуцированный сигаретным дымом. Американский журнал физиологии — клеточная и молекулярная физиология легких. 2001b; 280(1):L165–L172. [В паблике: 11133506]
, Уэки И.Ф., Протин Ю., Крошель П., Надель Дж.А. Активация рецепторов эпидермального фактора роста отвечает за синтез муцина, индуцированный сигаретным дымом. Американский журнал физиологии — клеточная и молекулярная физиология легких. 2001b; 280(1):L165–L172. [В паблике: 11133506]
Tan WC, Qui D, Liam BL, Ng TP, Lee SH, Van Eeden SF, D’Yachkova Y, Hogg JC. Реакция костного мозга человека на острое загрязнение воздуха, вызванное лесными пожарами. Американский журнал респираторной и интенсивной терапии. 2000;161(4):1213–7. [PubMed: 10764314]
Тан К., Росситер Х.Б., Вагнер П.Д., Брин ЕС. Направленная на легкие инактивация VEGF приводит к фенотипу эмфиземы у мышей. Журнал прикладной физиологии. 2004;97(4):1559–66. [PubMed: 15208295]
Терлбек ВМ. Заболеваемость эмфиземой легких с наблюдениями за относительной заболеваемостью и пространственным распределением различных типов эмфиземы. Американский обзор респираторных заболеваний. 1963; 87: 207–15. [PubMed: 13981312]
[PubMed: 13981312]
Тиитто Л., Каартинахо-Вийк Р., Сормунен Р., Холмгрен А., Пяяккё П., Сойни Ю., Киннула В.Л. Экспрессия тиоредоксиновой системы при интерстициальном заболевании легких. Журнал патологии. 2003;201(3):363–70. [PubMed: 14595747]
Тишлер П.В., Кэри В.Дж., Рид Т., Фабсиц Р.Р. Роль генотипа в определении влияния курения сигарет на легочную функцию. Генетическая эпидемиология. 2002;22(3):272–82. [PubMed: 11
7]Тобин М.Дж., Кук П.Дж.Л., Hutchison DCS. Alpha 1 Дефицит антитрипсина: клинические и физиологические особенности эмфиземы легких у субъектов, гомозиготных по Pi типа Z: обзор Британской торакальной ассоциации. Британский журнал болезней грудной клетки. 1983;77(1):14–27. [В паблике: 6602621]
Томасек Дж.Дж., Габбиани Г., Хинц Б., Шапонье С., Браун Р.А. Миофибробласты и механорегуляция ремоделирования соединительной ткани. Nature Reviews Молекулярно-клеточная биология. 2002;3(5):349–63. [PubMed: 11988769]
[PubMed: 11988769]
Томита К., Барнс П.Дж., Адкок И.М. Влияние окислительного стресса на ацетилирование гистонов и высвобождение IL-8. Коммуникации биохимических и биофизических исследований. 2003;301(2):572–7. [PubMed: 12565901]
Торреллес Дж. Б., Азад А. К., Хеннинг Л. Н., Карлсон Т. К., Шлезингер Л. С. Роль лектинов С-типа в микобактериальных инфекциях. Текущие цели по наркотикам. 2008;9(2): 102–12. [PubMed: 18288961]
Traves SL, Culpitt SV, Russell REK, Barnes PJ, Donnelly LE. Повышение уровня хемокинов GRO-альфа и МСР-1 в образцах мокроты больных ХОБЛ. грудная клетка. 2002;57(7):590–5. [Бесплатная статья PMC: PMC1746378] [PubMed: 12096201]
Трэвис Дж., Салвесен Г.С. Ингибиторы протеиназы плазмы человека. Ежегодный обзор биохимии. 1983; 52: 655–709. [PubMed: 61
Tribble DL, Giuliano LJ, Fortmann SP. Снижение концентрации аскорбиновой кислоты в плазме у некурящих, регулярно подвергающихся воздействию табачного дыма в окружающей среде. Американский журнал клинического питания. 1993;58(6):886–90. [PubMed: 8249873]
Американский журнал клинического питания. 1993;58(6):886–90. [PubMed: 8249873]
Tsuchiya M, Asada A, Kasahara E, Sato EF, Shindo M, Inoue M. Выкуривание одной сигареты быстро снижает комбинированные концентрации нитратов и нитритов и концентрации антиоксидантов в плазме. Тираж. 2002;105(10):1155–1157. [PubMed: 11889006]
Tsuchiya M, Thompson DF, Suzuki YJ, Cross CE, Packer L. Супероксид, образованный из сигаретного дыма, ухудшает активность генерации активного кислорода полиморфноядерными лейкоцитами. Архив биохимии и биофизики. 1992;299(1):30–7. [PubMed: 1332616]
Tsukagoshi H, Shimizu Y, Iwamae S, Hisada T, Ishizuka T, Iizuka K, Dobashi K, Mori M. Доказательства окислительного стресса при астме и ХОБЛ: потенциальное ингибирующее действие теофиллина. Респираторная медицина. 2000;94(6):584–8. [PubMed: 10
4] Tuder RM, McGrath S, Neptune E. Патобиологические механизмы моделей эмфиземы: что у них общего? Легочная фармакология и терапия. 2003а; 16(2):67–78. [В паблике: 12670776]
2003а; 16(2):67–78. [В паблике: 12670776]
Тудер Р.М., Петраче И., Элиас Дж.А., Воелкель Н.Ф., Хенсон П.М. Апоптоз и эмфизема: недостающее звено. Американский журнал респираторных клеток и молекулярной биологии. 2003б; 28(5):551–4. [PubMed: 12707010]
Tuder RM, Wood K, Taraseviciene L, Flores SC, Voelkel NF. Экстракт сигаретного дыма снижает экспрессию сосудистого эндотелиального фактора роста культивируемыми клетками и запускает апоптоз легочных эндотелиальных клеток. Грудь. 2000;117(5 Приложение 1):241S–242S. [В паблике: 10843927]
Тудер Р.М., Жень Л., Чо С.И., Тарасевичене-Стюарт Л., Касахара Ю., Сальвемини Д., Воелкель Н.Ф., Флорес СК. Окислительный стресс и апоптоз взаимодействуют и вызывают эмфизему из-за блокады рецепторов фактора роста эндотелия сосудов. Американский журнал респираторных клеток и молекулярной биологии. 2003с; 29(1):88–97. [PubMed: 12600822]
Уотила П. Влияние сигаретного дыма на конъюгацию глюкуронида в изолированных легких хомяка. Научные коммуникации в области химической патологии и фармакологии. 1982;38(1):173–6. [PubMed: 7146617]
Научные коммуникации в области химической патологии и фармакологии. 1982;38(1):173–6. [PubMed: 7146617]
Министерство здравоохранения и социальных служб США. Последствия курения для здоровья: хроническая обструктивная болезнь легких. Отчет главного хирурга. Rockville (MD): Министерство здравоохранения и социальных служб США, Служба общественного здравоохранения, Управление по вопросам курения и здоровья; 1984. Публикация DHHS № (PHS) 84-50205.
Министерство здравоохранения и социальных служб США. Польза для здоровья от отказа от курения Доклад главного хирурга. Атланта: Министерство здравоохранения и социальных служб США, Служба общественного здравоохранения, Центры контроля заболеваний, Национальный центр профилактики хронических заболеваний и укрепления здоровья, Управление по вопросам курения и здоровья; 1990. Публикация DHHS № (CDC) 90-8416. [PubMed: 32255575]
Министерство здравоохранения и социальных служб США. 9-й отчет о канцерогенах. Research Triangle Park (Северная Каролина): Министерство здравоохранения и социальных служб США, Служба общественного здравоохранения, Национальная программа по токсикологии; 2000. [PubMed: 20669515]
Research Triangle Park (Северная Каролина): Министерство здравоохранения и социальных служб США, Служба общественного здравоохранения, Национальная программа по токсикологии; 2000. [PubMed: 20669515]
Министерство здравоохранения и социальных служб США. Последствия курения для здоровья: отчет главного хирурга. Атланта: Министерство здравоохранения и социальных служб США, Центры по контролю и профилактике заболеваний, Национальный центр по профилактике хронических заболеваний и укреплению здоровья, Управление по вопросам курения и здоровья; 2004.
Министерство здравоохранения и социальных служб США. Последствия для здоровья непреднамеренного воздействия табачного дыма: отчет главного хирурга. Атланта: Министерство здравоохранения и социальных служб США, Центры по контролю и профилактике заболеваний, Координационный центр по укреплению здоровья, Национальный центр по профилактике хронических заболеваний и укреплению здоровья, Управление по вопросам курения и здоровья; 2006. [PubMed: 20669524]
[PubMed: 20669524]
Министерство здравоохранения, образования и социального обеспечения США. Курение и здоровье: отчет Консультативного комитета главному хирургу службы общественного здравоохранения. Вашингтон: Министерство здравоохранения, образования и социального обеспечения США, Служба общественного здравоохранения, Центр по контролю за заболеваниями; 1964. Публикация PHS № 1103.
Агентство по охране окружающей среды США. Критерии качества воздуха по оксидам азота. Вашингтон: Агентство по охране окружающей среды США; 1993. Публикация № EPA/600/8-91/049AF.
Агентство по охране окружающей среды США. Критерии качества воздуха для угарного газа. Вашингтон: Агентство по охране окружающей среды США, Управление исследований и разработок; 2000. Публикация № EPA 600/P-99/001F.
ван Акер С.А., Койманс Л.М., Баст А. Молекулярная фармакология витамина Е: структурные аспекты антиоксидантной активности. Свободнорадикальная биология и медицина. 1993;15(3):311–28. [PubMed: 8406131]
1993;15(3):311–28. [PubMed: 8406131]
ван Брабандт Х., Каубергс М., Вербекен Э., Моэрман П., Лауверинс Дж.М., Ван де Войстин К.П. Разделение легочного импеданса в иссеченных легких человека и собаки. Журнал прикладной физиологии. 1983; 55 (6): 1733–42. [PubMed: 6662764]
Ван дер Ваарт Х., Постма Д.С., Тайменс В., Тен Хакен НХТ. Острые эффекты сигаретного дыма на воспаление и окислительный стресс: обзор. грудная клетка. 2004;59(8):713–21. [Бесплатная статья PMC: PMC1747102] [PubMed: 15282395]
ван дер Влит А., Эйзерих Дж.П., Шигенага М.К., Кросс CE. Активные формы азота и нитрование тирозина в дыхательных путях: эпифеномены или патобиологический механизм заболевания? Американский журнал респираторной и интенсивной терапии. 1999;160(1):1–9. [PubMed: 103]
ван Иден С.Ф., Хогг Дж.К. Реакция костного мозга человека на хроническое курение сигарет. Европейский респираторный журнал. 2000;15(5):915–21. [PubMed: 10853859]
ван Иден С. Ф., Тан В.К., Сува Т., Мукаэ Х., Терашима Т., Фуджи Т., Куи Д., Винсент Р., Хогг Д.С. Цитокины, участвующие в системной воспалительной реакции, вызванной воздействием твердых частиц загрязнителей воздуха (PM 10 ). Американский журнал респираторной и интенсивной терапии. 2001;164(5):826–30. [PubMed: 11549540]
Ф., Тан В.К., Сува Т., Мукаэ Х., Терашима Т., Фуджи Т., Куи Д., Винсент Р., Хогг Д.С. Цитокины, участвующие в системной воспалительной реакции, вызванной воздействием твердых частиц загрязнителей воздуха (PM 10 ). Американский журнал респираторной и интенсивной терапии. 2001;164(5):826–30. [PubMed: 11549540]
Вестбо Дж., Ланге П. Может ли GOLD Стадия 0 предоставить информацию прогностического значения при хронической обструктивной болезни легких? Американский журнал респираторной и интенсивной терапии. 2002;166(3):329–32. [PubMed: 12153965]
Вестбо Дж., Прескотт Э., Ланге П. Связь хронической гиперсекреции слизи со снижением ОФВ 1 и заболеваемостью хронической обструктивной болезнью легких. Копенгагенская городская группа по изучению сердца. Американский журнал респираторной и интенсивной терапии. 1996; 153(5):1530–5. [PubMed: 8630597]
Винья Дж., Сервера Э., Асенси М., Састре Дж., Паллардо Ф.В., Ферреро Дж. А., Гарсия-Де-Ла-Асунсьон Дж., Антон В., Марин Дж. Упражнения вызывают окисление глутатиона в крови при хронической обструктивной легочные заболевания: профилактика с помощью O 2 терапия. Журнал прикладной физиологии. 1996;81(5):2199–202. [PubMed: 8941545]
А., Гарсия-Де-Ла-Асунсьон Дж., Антон В., Марин Дж. Упражнения вызывают окисление глутатиона в крови при хронической обструктивной легочные заболевания: профилактика с помощью O 2 терапия. Журнал прикладной физиологии. 1996;81(5):2199–202. [PubMed: 8941545]
Влахович Г., Рассел М.Л., Мерсер Р.Р., Крапо Д.Д. Клеточные и соединительнотканные изменения стенок альвеолярных перегородок при эмфиземе легких. Американский журнал респираторной и интенсивной терапии. 1999;160(6):2086–92. [PubMed: 10588633]
Voelkel NF. Отчет о конференции: вторая Сиенская международная конференция по животным моделям хронической обструктивной болезни легких. Легочная фармакология и терапия. 2004;17(2):61–3. [В паблике: 15125496]
Voelkel N, Taraseviciene-Stewart L. Эмфизема: аутоиммунное сосудистое заболевание? Труды Американского торакального общества. 2005;2(1):23–5. [PubMed: 16113465]
von Ahsen N, Oellerich M, Schütz E. Использование двух репортерных красителей без вмешательства в ПЦР с быстрым циклом в одной пробирке: α 1 -генотипирование антитрипсина с помощью мультиплексной флуоресцентной ПЦР в реальном времени с LightCycler. Клиническая химия. 2000;46(2):156–61. [PubMed: 10657370]
Клиническая химия. 2000;46(2):156–61. [PubMed: 10657370]
Уокер Д.К., Бехзад А., Чу Ф. Миграция нейтрофилов через ранее существовавшие отверстия в базальных пластинках альвеолярных капилляров и эпителия во время стрептококковой пневмонии. Микрососудистые исследования. 1995;50(3):397–416. [PubMed: 8583953]
Валлаерт Б., Грессье Б., Маркетт Ч., Госсет П., Реми-Жарден М., Мизон Дж., Тоннель АБ. Инактивация ингибитора альфа-1-протеиназы альвеолярными воспалительными клетками у курящих пациентов с эмфиземой или без нее. Американский обзор респираторных заболеваний. 1993; 147 (6 ч. 1): 1537–43. [PubMed: 8389110]
Уолтер С., Нэнси Н.Р. Базопения после курения сигарет. Индийский журнал медицинских исследований. 1980; 72: 422–5. [PubMed: 7461773]
Уолтер С., Уолтер А. Дегрануляция базофилов, вызванная курением сигарет у человека. грудная клетка. 1982; 37 (10): 756–9. [Бесплатная статья PMC: PMC459421] [PubMed: 7157215]
Wang Z, Zheng T, Zhu Z, Homer RJ, Riese RJ, Chapman HA Jr, Shapiro SD, Elias JA. Индукция гамма-интерфероном легочной эмфиземы в легком взрослой мыши. Журнал экспериментальной медицины. 2000;192(11):1587–99. [Бесплатная статья PMC: PMC21] [PubMed: 11104801]
Индукция гамма-интерфероном легочной эмфиземы в легком взрослой мыши. Журнал экспериментальной медицины. 2000;192(11):1587–99. [Бесплатная статья PMC: PMC21] [PubMed: 11104801]
Уорд С., Тьен Ф., Секомб Дж., Голлант С., Уолтерс Э.Х. Мочевина в жидкости бронхоальвеолярного лаважа как показатель легочной проницаемости у здоровых курильщиков. Европейский респираторный журнал. 2000;15(2):285–90. [PubMed: 10706493]
Weiss SJ, Test ST, Eckmann CM, Roos D, Regiani S. Бромирующие оксиданты, генерируемые эозинофилами человека. Наука. 1986; 234 (4773): 200–3. [PubMed: 3018933]
Weiss ST, Segal MR, Sparrow D, Wager C. Отношение FEV 1 и количества лейкоцитов периферической крови к общей смертности: нормативное исследование старения. Американский журнал эпидемиологии. 1995;142(5):493–8. [PubMed: 7677128]
Weitzenblum E, Hirth C, Ducolone A, Mirhom R, Rasahol-injanahary J, Ehrhart M. Прогностическое значение давления в легочной артерии при хронической обструктивной болезни легких. грудная клетка. 1981;36(10):752–8. [Бесплатная статья PMC: PMC471749] [PubMed: 7330793]
грудная клетка. 1981;36(10):752–8. [Бесплатная статья PMC: PMC471749] [PubMed: 7330793]
Вернер С., Гроуз Р. Регуляция заживления ран факторами роста и цитокинами. Физиологические обзоры. 2003;83(3):835–70. [PubMed: 12843410]
Wert SE, Yoshida M, LeVine AM, Ikegami M, Jones T, Ross GF, Fisher JH, Korfhagen TR, Whitsett JA. Повышенная активность металлопротеиназы, продукция оксидантов и эмфизема у мышей с инактивированным геном сурфактантного протеина D. Труды Национальной академии наук Соединенных Штатов Америки. 2000;97(11):5972–7. [Статья бесплатно PMC: PMC18543] [PubMed: 10801980]
Wickenden JA, Clarke MC, Rossi AG, Rahman I, Faux SP, Donaldson K, MacNee W. Сигаретный дым предотвращает апоптоз за счет ингибирования активации каспазы и вызывает некроз. Американский журнал респираторных клеток и молекулярной биологии. 2003;29(5):562–70. [PubMed: 12748058]
Wilk JB, DeStefano AL, Arnett DK, Rich SS, Djousse L, Crapo RO, Leppert MF, Province MA, Cupples LA, Gottlieb DJ и др. Полногеномное сканирование показателей функции легких в исследовании семейного сердца Национального института сердца, легких и крови. Американский журнал респираторной и интенсивной терапии. 2003а; 167(11):1528–33. [В паблике: 12637344]
Полногеномное сканирование показателей функции легких в исследовании семейного сердца Национального института сердца, легких и крови. Американский журнал респираторной и интенсивной терапии. 2003а; 167(11):1528–33. [В паблике: 12637344]
Wilk JB, DeStefano AL, Joost O, Myers RH, Cupples LA, Slater K, Atwood LD, Heard-Costa NL, Herbert A, O’Connor GT, et al. Сцепление и ассоциация с мерами легочной функции на хромосоме 6q27 в Framingham Heart Study. Молекулярная генетика человека. 2003b;12(21):2745–51. [PubMed: 12966033]
Wilkinson TMA, Patel IS, Wilks M, Donaldson GC, Wedzicha JA. Бактериальная нагрузка дыхательных путей и ОФВ 1 снижаются у пациентов с хронической обструктивной болезнью легких. Американский журнал респираторной и интенсивной терапии. 2003;167(8):1090–5. [PubMed: 12684248]
Wink DA, Hanbauer I, Grisham MB, Laval F, Nims RW, Laval J, Cook J, Pacelli R, Liebmann J, Krishna M, et al. Химическая биология оксида азота: регуляторно-защитно-токсические механизмы. Актуальные темы клеточной регуляции. 1996; 34: 159–87. [PubMed: 8646847]
Актуальные темы клеточной регуляции. 1996; 34: 159–87. [PubMed: 8646847]
Winkel P, Statland BE. Острое влияние курения сигарет на концентрацию типов лейкоцитов крови у здоровых молодых женщин. Американский журнал клинической патологии. 1981;75(6):781–5. [PubMed: 7258139]
Winklhofer-Roob BM, Ellmunter H, Frühwirth M, Schlegel-Haueter SE, Khoschsorur G, van’t Hof MA, Shmerling DH. Концентрация витамина С в плазме у пациентов с муковисцидозом: свидетельство связи с воспалением легких. Американский журнал питания. 1997; 65 (6): 1858–66. [PubMed:
Wouters EF, Creutzberg EC, Schols AM. Системные эффекты при ХОБЛ. Грудь. 2002; 121 (5 Дополнение): 127S–130S. [В паблике: 12010840]
Райт Д.Т., Фишер Б.М., Ли С., Рошель Л.Г., Экли Н.Дж., Адлер К.Б. Оксидантный стресс стимулирует секрецию муцина и PLC в эпителии дыхательных путей через механизм, зависящий от оксида азота. Американский журнал физиологии. 1996; 271 (5 ч. 1): L854–L861. [PubMed: 8944730]
1): L854–L861. [PubMed: 8944730]
Wright JL, Churg A. Вызванная дымом эмфизема у морских свинок связана с морфометрическими признаками разрушения и восстановления коллагена. Американский журнал физиологии. 1995; 268 (1 часть 1): L17–L20. [В паблике: 7840223]
Райт Дж.Л., Дай Дж., Зай К., Прайс К., Гилкс С.Б., Чарг А. Влияние сигаретного дыма на экспрессию синтазы оксида азота в легких крыс. Лабораторные исследования. 1999;79(8):975–83. [PubMed: 10462035]
Райт Дж.Л., Фармер С.Г., Чарг А. Синтетический ингибитор сериновой эластазы уменьшает эмфизему, вызванную сигаретным дымом, у морских свинок. Американский журнал респираторной и интенсивной терапии. 2002;166(7):954–60. [PubMed: 12359653]
Райт Дж.Л., Лоусон Л., Паре П.Д., Хупер Р.О., Перец Д.И., Нелемс Дж.М., Шульцер М., Хогг Дж.К. Структура и функция легочной сосудистой сети при легкой форме хронической обструктивной болезни легких: влияние кислорода и физической нагрузки. Американский обзор респираторных заболеваний. 1983а; 128(4):702–7. [PubMed: 6625346]
Американский обзор респираторных заболеваний. 1983а; 128(4):702–7. [PubMed: 6625346]
Райт Дж. Л., Лоусон Л. М., Паре П. Д., Виггс Б. Дж., Кеннеди С., Хогг Дж. К. Морфология периферических дыхательных путей у нынешних курильщиков и бывших курильщиков. Американский обзор респираторных заболеваний. 1983б; 127(4):474–7. [PubMed: 6838053]
Райт Дж.Л., Петти Т., Терлбек В.М. Анализ структуры мышечных легочных артерий у пациентов с легочной гипертензией и ХОБЛ: Испытание ночной оксигенотерапии Национального института здравоохранения. Легкое. 1992;170(2):109–24. [PubMed: 1501507]
Wu HM, Jin M, Marsh CB. К функциональной протеомике альвеолярных макрофагов. Американский журнал физиологии — клеточная и молекулярная физиология легких. 2005; 288(4):L585–L595. [PubMed: 15757951]
Ву Л., Чау Дж., Янг Р.П., Покорный В., Миллс Г.Д., Хопкинс Р., Маклин Л., Блэк П.Н. Трансформирующий фактор роста-β 1 генотип и предрасположенность к хронической обструктивной болезни легких. грудная клетка. 2004;59(2):126–9. [Бесплатная статья PMC: PMC1746926] [PubMed: 14760152]
грудная клетка. 2004;59(2):126–9. [Бесплатная статья PMC: PMC1746926] [PubMed: 14760152]
Wyatt JP, Fischer VW, Sweet HC. Панлобулярная эмфизема: анатомия и патодинамика. Заболевания грудной клетки. 1962; 41 (3): 239–59. [PubMed: 14008600]
Вятт Т.А., Хейрес А.Дж., Сандерсон С.Д., Флореани А.А. Активация протеинкиназы С необходима для опосредованного сигаретным дымом C5a-опосредованного высвобождения интерлейкина-8 в клетках бронхиального эпителия человека. Американский журнал респираторных клеток и молекулярной биологии. 1999;21(2):283–8. [В паблике: 10423413]
Yamamoto C, Yoneda T, Yoshikawa M, Fu A, Tokuyama T, Tsukaguchi K, Narita N. Воспаление дыхательных путей при ХОБЛ, оцениваемое по уровню интерлейкина-8 в мокроте. Грудь. 1997;112(2):505–10. [PubMed:
Yanai M, Sekizawa K, Ohrui T, Sasaki H, Takishima T. Место обструкции дыхательных путей при заболеваниях легких: прямое измерение внутрибронхиального давления. Журнал прикладной физиологии. 1992;72(3):1016–23. [PubMed: 1568955]
Журнал прикладной физиологии. 1992;72(3):1016–23. [PubMed: 1568955]
Йим Дж.Дж., Пак Г.Ю., Ли К.Т., Ким Ю.В., Хан С.К., Шим И.С., Ю К.Г. Генетическая предрасположенность к хронической обструктивной болезни легких у корейцев: комбинированный анализ полиморфных генотипов микросомальной эпоксидгидролазы и глутатиона S -трансферазы М1 и Т1. грудная клетка. 2000;55(2):121–5. [Бесплатная статья PMC: PMC1745681] [PubMed: 10639528]
Yim JJ, Yoo CG, Lee CT, Kim YW, Han SK, Shim YS. Отсутствие связи между полиморфизмом глутатион S -трансферазы P1 и ХОБЛ у корейцев. Легкое. 2002;180(2):119–25. [PubMed: 12172904]
Йошикава М., Хияма К., Исиока С., Маэда Х., Маэда А., Ямакидо М. Генотипы микросомальной эпоксидгидролазы и хроническая обструктивная болезнь легких у японцев. Международный журнал молекулярной медицины. 2000;5(1):49–53. [PubMed: 10601573]
Йошиока А., Бецуяку Т., Нисимура М., Миямото К., Кондо Т. , Каваками Ю. Чрезмерная эластаза нейтрофилов в жидкости бронхоальвеолярного лаважа при субклинической эмфиземе. Американский журнал респираторной и интенсивной терапии. 1995; 152 (6 ч. 1): 2127–32. [PubMed: 8520785]
, Каваками Ю. Чрезмерная эластаза нейтрофилов в жидкости бронхоальвеолярного лаважа при субклинической эмфиземе. Американский журнал респираторной и интенсивной терапии. 1995; 152 (6 ч. 1): 2127–32. [PubMed: 8520785]
Занг Л.И., Стоун К., Прайор В.А. Обнаружение свободных радикалов в водных экстрактах сигаретной смолы методом электронного спинового резонанса. Свободнорадикальная биология и медицина. 1995;19(2):161–7. [PubMed: 7649487]
Чжэн Т., Чжу З., Ван З., Гомер Р.Дж., Ма Б., Ризе Р.Дж. младший, Чепмен Х.А. младший, Шапиро С.Д., Элиас Дж.А. Индуцируемое нацеливание IL-13 на взрослое легкое вызывает матрикс-металлопротеиназу- и катепсин-зависимую эмфизему. Журнал клинических исследований. 2000;106(9):1081–93. [Бесплатная статья PMC: PMC301418] [PubMed: 11067861]
Держите воздух чистым: как табак может нанести вред вашим легким
Каждый орган в человеческом теле служит важной цели, поддерживая его в рабочем состоянии и в отличном состоянии. Большинство здоровых людей не знают о своих органах, таких как легкие, каждый день, потому что они могут дышать без затруднений и выполнять свои повседневные задачи без особых усилий. Но повреждение этих жизненно важных органов может привести к серьезным заболеваниям, а иногда и к летальному исходу. Сигареты могут нанести вред ткани легких, препятствуя их нормальному функционированию, и могут увеличить риск таких состояний, как эмфизема легких, рак легких и хроническая обструктивная болезнь легких (ХОБЛ).
Большинство здоровых людей не знают о своих органах, таких как легкие, каждый день, потому что они могут дышать без затруднений и выполнять свои повседневные задачи без особых усилий. Но повреждение этих жизненно важных органов может привести к серьезным заболеваниям, а иногда и к летальному исходу. Сигареты могут нанести вред ткани легких, препятствуя их нормальному функционированию, и могут увеличить риск таких состояний, как эмфизема легких, рак легких и хроническая обструктивная болезнь легких (ХОБЛ).
Основная функция легких — доставлять богатую кислородом кровь к остальным частям тела из вдыхаемого воздуха и выводить углекислый газ в виде отходов при выдохе. Хотя ни один табачный продукт не является безопасным, горючие продукты — или те, которые вы должны поджечь, чтобы использовать, например сигареты — особенно вредны для легких.
Курение и ваши легкие
Курение сигарет может нанести непоправимый вред вашему здоровью. Каждая затяжка сигаретного дыма содержит смесь более 7000 химических веществ. 1 Когда вы вдыхаете это, дым очень быстро попадает в ваши легкие, и кровь, которая затем разносится по всему телу, содержит эти токсичные химические вещества. Поскольку табачный дым содержит окись углерода, этот смертельный газ вытесняет кислород из вашей крови, лишая ваши органы кислорода, в котором они нуждаются. 1,2
1 Когда вы вдыхаете это, дым очень быстро попадает в ваши легкие, и кровь, которая затем разносится по всему телу, содержит эти токсичные химические вещества. Поскольку табачный дым содержит окись углерода, этот смертельный газ вытесняет кислород из вашей крови, лишая ваши органы кислорода, в котором они нуждаются. 1,2
Другие химические вещества, обнаруженные в сигаретном дыме, включают акролеин, который может вызвать необратимое повреждение легких, и даже в небольших количествах он может вызвать боль в горле через 10 минут. 3 Сигареты могут также содержать бронходилататоры или химические вещества, которые предназначены для открытия дыхательных путей легких и могут увеличить количество опасных химических веществ, поглощаемых легкими. 4
Курение сигарет может иметь серьезные последствия для легких в любом возрасте. У младенцев, матери которых курили во время беременности, легкие могут развиваться ненормально, 5 , а у подростков, курящих сигареты, могут развиться меньшие по размеру и более слабые легкие, которые никогда не вырастут до полного размера и никогда не будут работать на пике своих возможностей. 6 Кроме того, курение может разрушить реснички или крошечные волоски в дыхательных путях, которые удерживают грязь и слизь от попадания в легкие. Когда эти реснички разрушаются, у вас развивается так называемый «кашель курильщика», хронический кашель, который часто наблюдается у заядлых или ежедневных курильщиков. 1
6 Кроме того, курение может разрушить реснички или крошечные волоски в дыхательных путях, которые удерживают грязь и слизь от попадания в легкие. Когда эти реснички разрушаются, у вас развивается так называемый «кашель курильщика», хронический кашель, который часто наблюдается у заядлых или ежедневных курильщиков. 1
На этом повреждение легких из-за курения не заканчивается. 8 из 10 случаев хронической обструктивной болезни легких (или ХОБЛ) вызваны курением. 7 Люди с ХОБЛ испытывают трудности с дыханием и в конечном итоге умирают из-за нехватки воздуха. Лекарства от ХОБЛ не существует. Кроме того, почти все виды рака легких — основная причина смерти от рака у мужчин и женщин — вызваны курением, а вероятность развития рака легких у курильщиков в 20 раз выше, чем у некурящих. 8 Курение может привести не только к раку легких, но и к другим видам рака органов дыхания, таким как:
- Ротоглотка (задняя часть рта, включая части языка, мягкое небо, боковые и задние отделы глотки, и миндалины)
- Гортань («голосовой аппарат»)
- Трахея («трахея»)
- Бронх (один из двух крупных дыхательных путей, соединяющих трахею с легкими) 9
Не только сигареты: другие табачные изделия и здоровье легких
FDA Tobacco
Библиотека образовательных ресурсов
Бесплатно встраивайте материалы FDA о табаке на свой веб-сайт. Благодаря библиотеке образовательных ресурсов FDA Tobacco Education Resource Library при обновлении контента на нашем сайте он будет автоматически обновляться и на вашем сайте.
Благодаря библиотеке образовательных ресурсов FDA Tobacco Education Resource Library при обновлении контента на нашем сайте он будет автоматически обновляться и на вашем сайте.
Вставить этот контент
Несмотря на то, что сигареты — с учетом их высокой скорости курения, вызывающего привыкание и токсичной смеси химических веществ — являются наиболее опасным табачным изделием, любой табачный продукт, который вы вдыхаете, может вызвать повреждение легких. Курение сигар может увеличить риск ХОБЛ и привести к раку легких, полости рта и гортани, среди других видов рака. 10,11
Электронные системы доставки никотина (ЭСДН), как и электронные сигареты, все еще являются относительно новыми табачными изделиями, и их воздействие на здоровье все еще изучается. Но использование электронных сигарет или «вейпинг» может нанести вред вашим легким. Было обнаружено, что некоторые аэрозоли для электронных сигарет содержат некоторые из тех же химических веществ, что и сигареты, в том числе акролеин, вызывающий раздражение легких, и формальдегид, которые могут неблагоприятно воздействовать на горло. 12,13,14,15 Ароматизаторы считаются безопасными для употребления в пищу, но могут нанести вред при вдыхании. Маслянистые вкусы, такие как карамель, ириска и шоколад, содержат химические вещества диацетил и ацетоин, которые могут быть вредны для ваших легких. 16 Кроме того, электронные сигареты со вкусом фруктов могут иметь более высокие концентрации химического вещества, называемого акрилонитрилом, которое является известным раздражителем дыхательных путей. 17
12,13,14,15 Ароматизаторы считаются безопасными для употребления в пищу, но могут нанести вред при вдыхании. Маслянистые вкусы, такие как карамель, ириска и шоколад, содержат химические вещества диацетил и ацетоин, которые могут быть вредны для ваших легких. 16 Кроме того, электронные сигареты со вкусом фруктов могут иметь более высокие концентрации химического вещества, называемого акрилонитрилом, которое является известным раздражителем дыхательных путей. 17
Как защитить легкие от табака
Легкие — это одна из систем фильтрации вашего организма, которая забирает воздух из атмосферы, насыщает кровь кислородом для циркуляции по всему телу и удаляет избыток углекислого газа. Когда табак вдыхается, он нарушает этот тонкий баланс. Лучший способ сохранить здоровье легких — никогда не начинать курить, но если вы заядлый курильщик, чем раньше вы бросите курить, тем быстрее начнут заживать ваши легкие. Отказ от курения может снизить риск заболеть раком. На самом деле, когда вы бросите курить, ваш риск:
На самом деле, когда вы бросите курить, ваш риск:
- Рак гортани уменьшается сразу;
- Рак легких снижается на 50 процентов через 10 лет после отказа от курения;
- Заболеваемость раком полости рта и горла снижается на 50% через пять лет после отказа от курения. 8
Любой, кто бросит курить, улучшит общее состояние здоровья. Всего через 12 часов после отказа от курения уровень угарного газа в крови падает до нормы, позволяя большему количеству кислорода циркулировать в ваших органах. 2
Дополнительные ресурсы
Найдите информацию о том, как бросить курить, и другие ресурсы о табачных изделиях и их влиянии на здоровье:
- Кампания FDA «Каждая попытка имеет значение»
- Кампании FDA по профилактике табакокурения среди молодежи
- Выход из ресурсов Smokefree.gov
- «Знай риски»: факты об электронных сигаретах от главного хирурга
Ссылки
1. Министерство здравоохранения и социальных служб США (USDHHS). Отчет главного хирурга: как табачный дым вызывает болезни: что это значит для вас (буклет для потребителей). Атланта, Джорджия: Министерство здравоохранения и социальных служб США, Центры по контролю и профилактике заболеваний, Национальный центр по профилактике хронических заболеваний и укреплению здоровья, Управление по вопросам курения и здоровья; 2010.
Министерство здравоохранения и социальных служб США (USDHHS). Отчет главного хирурга: как табачный дым вызывает болезни: что это значит для вас (буклет для потребителей). Атланта, Джорджия: Министерство здравоохранения и социальных служб США, Центры по контролю и профилактике заболеваний, Национальный центр по профилактике хронических заболеваний и укреплению здоровья, Управление по вопросам курения и здоровья; 2010.
2. Министерство здравоохранения и социальных служб США (USDHHS). Последствия курения для здоровья: что это значит для вас (буклет для потребителей). Атланта, Джорджия: Министерство здравоохранения и социальных служб США, Центры по контролю и профилактике заболеваний, Национальный центр по профилактике хронических заболеваний и укреплению здоровья, Управление по вопросам курения и здоровья; 2004.
3. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Вредные и потенциально вредные вещества в табачных изделиях и табачном дыме; Установленный список. https://www.fda.gov/TobaccoProducts/Labeling/RulesRegulationsGuidance/ucm297786.htm По состоянию на 8 января 2019 г.
https://www.fda.gov/TobaccoProducts/Labeling/RulesRegulationsGuidance/ucm297786.htm По состоянию на 8 января 2019 г.
4. Министерство здравоохранения и социальных служб США (USDHHS). Как табачный дым вызывает заболевание: биологическая и поведенческая основа болезней, связанных с курением: отчет главного хирурга. Атланта, Джорджия: Министерство здравоохранения и социальных служб США, Центры по контролю и профилактике заболеваний, Национальный центр по профилактике хронических заболеваний и укреплению здоровья, Управление по вопросам курения и здоровья; 2010.
5. Министерство здравоохранения и социальных служб США (USDHHS). Женщины и курение. Доклад главного хирурга. Атланта, Джорджия: Министерство здравоохранения и социальных служб США, Центры по контролю и профилактике заболеваний, Координационный центр по укреплению здоровья, Национальный центр по профилактике хронических заболеваний и укреплению здоровья, Управление по вопросам курения и здоровья; 2001.
6. Министерство здравоохранения и социальных служб США (USDHHS). Отчет главного хирурга: Профилактика употребления табака среди молодежи и молодых людей. Мы можем сделать следующее поколение без табака (буклет для потребителей). Атланта, Джорджия: Министерство здравоохранения и социальных служб США, Центры по контролю и профилактике заболеваний, Национальный центр по профилактике хронических заболеваний и укреплению здоровья, Управление по вопросам курения и здоровья; 2012.
Отчет главного хирурга: Профилактика употребления табака среди молодежи и молодых людей. Мы можем сделать следующее поколение без табака (буклет для потребителей). Атланта, Джорджия: Министерство здравоохранения и социальных служб США, Центры по контролю и профилактике заболеваний, Национальный центр по профилактике хронических заболеваний и укреплению здоровья, Управление по вопросам курения и здоровья; 2012.
7. Министерство здравоохранения и социальных служб США (USDHHS). Последствия курения для здоровья — 50 лет прогресса: отчет главного хирурга (информационный бюллетень). Атланта, Джорджия: Министерство здравоохранения и социальных служб США, Центры по контролю и профилактике заболеваний, Национальный центр по профилактике хронических заболеваний и укреплению здоровья, Управление по вопросам курения и здоровья; 2014.
8. Министерство здравоохранения и социальных служб США (USDHHS). Последствия курения для здоровья: отчет главного хирурга. Атланта, Джорджия: Министерство здравоохранения и социальных служб США, Центр контроля и профилактики заболеваний, Национальный центр профилактики хронических заболеваний и укрепления здоровья, Управление по вопросам курения и здоровья, 2004 г.
9. Национальный институт рака. Словарь терминов рака NCI. https://www.cancer.gov/syndication/widgets. По состоянию на 10 сентября 2018 г.
10. Шанкс Т.Г., Бернс Д.М. Болезненные последствия курения сигар. В: Монография о курении и борьбе против табака 9: Сигары – влияние на здоровье и тенденции. Bethesda, MD: Национальный институт рака; 1998.
11. Международное агентство по изучению рака (IARC). Табачный дым и непроизвольное курение. В: Монографии IARC по оценке канцерогенных рисков для человека. Том. 83. Лион, Франция: Международное агентство по изучению рака; 2004.
12. Goniewicz ML, Knysak J, Gawron M, et al. Уровни отдельных канцерогенов и токсикантов в парах электронных сигарет. Табачный контроль. 2014; 23(2):133-139.
13. Ченг Т. Химическая оценка электронных сигарет. Табачный контроль. 2014; 23:ii11–ii17.
14. Бейн К., Лейкауф Г.Д. Акролеин — легочная опасность. Молекулярное питание и исследования продуктов питания. 2011;55(9):1342-1360.
15. Управление по безопасности и гигиене труда (OSHA). Стандарты безопасности и гигиены труда. Медицинское наблюдение – Формальдегид. Вашингтон, округ Колумбия: Министерство труда США, Управление по охране труда. https://www.osha.gov/pls/oshaweb/owadisp.show_document?p_table=STANDARDS&p_id=10078. По состоянию на 8 мая 2018 г.
Стандарты безопасности и гигиены труда. Медицинское наблюдение – Формальдегид. Вашингтон, округ Колумбия: Министерство труда США, Управление по охране труда. https://www.osha.gov/pls/oshaweb/owadisp.show_document?p_table=STANDARDS&p_id=10078. По состоянию на 8 мая 2018 г.
16. Allen J, Flanigan SS, LeBlanc M, et al. Ароматизирующие химические вещества в электронных сигаретах: диацетил, 2,3-пентандион и ацетоин в образце из 51 продукта, включая электронные сигареты со вкусом фруктов, конфет и коктейлей. Перспектива охраны окружающей среды. 2016;124. https://ehp.niehs.nih.gov/15-10185/. По состоянию на 27 марта 2018 г.
17. Рубинштейн М., Делукки К., Беновиц Н., Рамо Д. Воздействие токсичных летучих органических химикатов из электронных сигарет на подростков. Педиатрия. 2018; 141(4):e20173557.
Курение – воздействие на организм
Действия для этой страницы
Резюме
Читать полный информационный бюллетень- Табачный дым содержит более 70 известных канцерогенных химических веществ.

- Курение наносит вред почти каждому органу вашего тела.
- Курение во время беременности наносит вред вашему будущему ребенку.
- Дети, подвергающиеся пассивному курению в первый год жизни, имеют более высокий риск заболевания и внезапной неожиданной смерти в младенчестве (SUDI).
Никотин – это наркотик, вызывающий привыкание в табачном дыме, который заставляет курильщиков продолжать курить.
Наряду с никотином курильщики вдыхают с сигаретным дымом около 7000 других химических веществ. Многие из этих химических веществ образуются при сжигании табачного листа. Некоторые из этих соединений химически активны и вызывают глубокие и разрушительные изменения в организме.
Табачный дым содержит более 70 известных канцерогенных химических веществ. Курение наносит вред почти каждому органу тела, вызывая множество заболеваний и ухудшая общее состояние здоровья.
Опасные химические вещества в табачном дыме
Сильно вредные компоненты табачного дыма включают:
- смолы – так называются твердые частицы, взвешенные в табачном дыме.
 Частицы содержат химические вещества, в том числе вызывающие рак вещества (канцерогены). Деготь липкий и коричневый, окрашивает зубы, ногти и легочную ткань
Частицы содержат химические вещества, в том числе вызывающие рак вещества (канцерогены). Деготь липкий и коричневый, окрашивает зубы, ногти и легочную ткань - окись углерода – ядовитый газ. Он не имеет запаха и цвета и в больших дозах быстро вызывает смерть, поскольку заменяет кислород в крови. У курящих людей угарный газ в крови затрудняет доступ кислорода к их органам и мышцам
- окисляющие химические вещества – это высокореактивные химические вещества, которые могут повредить сердечную мышцу и кровеносные сосуды курящих людей. Они вступают в реакцию с холестерином, что приводит к накоплению жирового материала на стенках артерий. Их действия приводят к сердечным заболеваниям, инсульту и заболеваниям сосудов
- металлы – табачный дым содержит несколько металлов, вызывающих рак, включая мышьяк, бериллий, кадмий, хром, кобальт, свинец и никель
- радиоактивные соединения – Табачный дым содержит радиоактивные соединения, известные как канцерогены.

Воздействие курения табака на организм
Вдыхание табачного дыма вызывает поражение многих органов и систем организма.
Воздействие курения на дыхательную систему
Воздействие табачного дыма на дыхательную систему включает:
- раздражение трахеи (трахеи) и гортани (голосовой ящик)
- снижение функции легких и одышка из-за отека и сужения легочных дыхательных путей и избыток слизи в легочных путях
- нарушение системы очистки легких, ведущее к накоплению ядовитых веществ, что приводит к раздражению и повреждению легких
- повышенный риск инфекции легких и такие симптомы, как кашель и хрипы легкие.
Влияние курения на систему кровообращения
Влияние табачного дыма на систему кровообращения включает:
- повышение артериального давления и частоты сердечных сокращений
- сужение (уплотнение) кровеносных сосудов в коже, приводящее к падению температуры кожи
- меньше кислорода, переносимого кровью во время физической нагрузки
- более «липкая» кровь, которая более склонна к свертыванию артерий, что считается фактором, способствующим атеросклерозу (накопление жировых отложений на стенках артерий)
- уменьшение притока крови к конечностям (пальцы рук и ног)
- повышенный риск инсульта и сердечного приступа из-за закупорки кровоснабжения.

Влияние курения на иммунную систему
Влияние табачного дыма на иммунную систему включает:
- повышенную восприимчивость к таким инфекциям, как пневмония и грипп
- более тяжелые и продолжительные заболевания
- более низкие уровни защиты антиоксиданты (например, витамин С) в крови.
Воздействие курения на опорно-двигательный аппарат
Воздействие табачного дыма на опорно-двигательный аппарат включает:
- напряжение некоторых мышц
- снижение плотности костей.
Воздействие курения на половые органы
Воздействие табачного дыма на мужской организм включает повышенный риск: что может быть связано с влиянием курения на кровоток и повреждением кровеносных сосудов полового члена.
Влияние табачного дыма на женский организм включает:
- снижение фертильности, нарушения менструального цикла или отсутствие менструаций
- менопауза, наступившая на один или два года раньше
- повышенный риск рака шейки матки
- значительно повышенный риск инсульта и сердечного приступа, если курильщик старше 35 лет и принимает оральные противозачаточные таблетки.

Другие эффекты курения на организм
Другие эффекты табачного дыма на организм включают:
- раздражение и воспаление желудка и кишечника
- повышенный риск болезненных язв вдоль пищеварительного тракта
- снижение обоняния и вкуса
- преждевременное образование морщин на коже
- повышенный риск слепоты
- заболевание десен (пародонтит) .
Воздействие курения на младенцев
Последствия курения матери для будущего ребенка включают:
- повышенный риск выкидыша, мертворождения и преждевременных родов
- более слабые легкие
- низкая масса тела при рождении, которая может оказывать длительное влияние на рост и развитие детей. Низкий вес при рождении связан с повышенным риском сердечно-сосудистых заболеваний, высокого кровяного давления и диабета во взрослом возрасте
- повышенный риск расщелины неба и губы
- повышенный риск синдрома дефицита внимания и гиперактивности (СДВГ).

Пассивное курение (подвержение некурящей матери пассивному курению) также может нанести вред плоду.
Если родитель продолжает курить в течение первого года жизни ребенка, у ребенка повышается риск ушных инфекций, респираторных заболеваний, таких как пневмония и бронхит, внезапная неожиданная смерть в младенчестве (SUDI) и менингококковая инфекция.
Болезни, вызванные длительным курением
Человек, курящий на протяжении всей жизни, подвержен высокому риску развития ряда потенциально смертельных заболеваний, в том числе:
- рак легких, рта, носа, гортани, языка, носа синус, пищевод, горло, поджелудочная железа, костный мозг (миелоидный лейкоз), почки, шейка матки, яичник, мочеточник, печень, мочевой пузырь, кишечник и желудок
- болезни легких, такие как хронический бронхит и хроническая обструктивная болезнь легких, включая обструктивный бронхиолит и эмфизему
- болезни сердца и инсульт
- язвы пищеварительной системы может привести к боли и, в тяжелых случаях, к гангрене и ампутации
- сахарный диабет 2 типа
- ревматоидный артрит.

Где получить помощь
- Ваш терапевт (врач)
- Ваш фармацевт
- Quitline Тел. 13 QUIT (13 7848)
- Winstanley M, et al., 2015, « Глава 3. Влияние активного курения на здоровье », Табак в Австралии: факты и проблемы, Cancer Council Victoria.
- Уинстенли М., Форд С., Кэмпбелл М., 2017 г., « Глава 4. Влияние пассивного курения на здоровье », Табак в Австралии: факты и проблемы, Совет по раку Виктории.
- Чемберлен С., О Мара-Ивс А., Оливер С. и др. 2013, Психосоциальные вмешательства для поддержки женщин в отказе от курения во время беременности , Кокрановские резюме.
- Влияние курения сигарет на здоровье , 2017 г., Управление по вопросам курения и здоровья, Национальный центр профилактики хронических заболеваний и укрепления здоровья, Центры по контролю и профилактике заболеваний, США.
- Отчет главного хирурга, 2010 г. – Как табачный дым вызывает болезни: биологическая и поведенческая основа заболеваний, связанных с курением , Центры по контролю и профилактике заболеваний, США.

- Обзор канцерогенов человека. Часть E: Личные привычки и сжигание в помещениях , 2012 г., Рабочая группа IARC по оценке канцерогенных рисков для человека, Международное агентство по изучению рака, Лион, Франция.
- Последствия курения для здоровья – 50 лет прогресса: отчет главного хирурга , 2014 г., Министерство здравоохранения и социальных служб США.
- Что содержится в сигаретах и самокрутках? , 2017, Уйти из Виктории.
Эта страница была подготовлена в консультации с и одобрена по:
Эта страница была подготовлена в консультации с и одобрена по:
Оставить отзыв об этой странице
Была ли эта страница полезной?
Дополнительная информация
Заявление об отказе от ответственности
Содержание этого веб-сайта предоставляется только в информационных целях. Информация о терапии, услуге, продукте или лечении никоим образом не одобряет и не поддерживает такую терапию, услугу, продукт или лечение и не предназначена для замены рекомендаций вашего врача или другого зарегистрированного медицинского работника. Информация и материалы, содержащиеся на этом веб-сайте, не предназначены для использования в качестве исчерпывающего руководства по всем аспектам терапии, продукта или лечения, описанным на веб-сайте. Всем пользователям настоятельно рекомендуется всегда обращаться за советом к зарегистрированному специалисту в области здравоохранения для диагностики и ответов на свои медицинские вопросы, а также для выяснения того, подходит ли конкретная терапия, услуга, продукт или лечение, описанные на веб-сайте, в их обстоятельствах. Штат Виктория и Министерство здравоохранения не несут никакой ответственности за использование любым пользователем материалов, содержащихся на этом веб-сайте.
Информация и материалы, содержащиеся на этом веб-сайте, не предназначены для использования в качестве исчерпывающего руководства по всем аспектам терапии, продукта или лечения, описанным на веб-сайте. Всем пользователям настоятельно рекомендуется всегда обращаться за советом к зарегистрированному специалисту в области здравоохранения для диагностики и ответов на свои медицинские вопросы, а также для выяснения того, подходит ли конкретная терапия, услуга, продукт или лечение, описанные на веб-сайте, в их обстоятельствах. Штат Виктория и Министерство здравоохранения не несут никакой ответственности за использование любым пользователем материалов, содержащихся на этом веб-сайте.
Пересмотрено: 12-02-2019
3.2 Респираторные заболевания (кроме рака легких)
Последнее обновление: декабрь 2020 г. Рекомендуемое цитирование: Winnall, WR, Peters, M, Greenhalgh, EM & Winstanley, MH. 3.2 Респираторные заболевания. |
3.2.1 Поражение легких, вызванное курением
Основной функцией дыхательных путей человека является газообмен. Вдыхание воздуха осуществляется через верхние дыхательные пути (полость носа, глотка и гортань) в легкие, которые вместе с трахеей и бронхами составляют нижние дыхательные пути. Между альвеолами и легочными капиллярами происходит газообмен, где кислород переходит в кровь, а углекислый газ из крови в легкие для выдоха. Этот газообмен происходит через очень тонкую мембрану на очень большой площади поверхности легких. Газообмен происходит за счет неравновесия концентраций газов в крови и воздухе. Могут происходить обмены и с другими газами, находящимися в неравновесном состоянии, в том числе присутствующими в табачном дыме. 1
1
Частицы и газы вдыхаются при каждом вдохе. К ним относятся безвредная пыль, химические вещества, которые могут быть вредными, аллергены, такие как пыльца, и патогены (вирусы, бактерии, грибковые споры и крошечные паразиты). Газы проходят непосредственно в легкие. Крупные и очень мелкие частицы в основном задерживаются в носу и верхних дыхательных путях и выводятся, не достигая легких. Частицы среднего размера, примерно от 0,005 до 2,5 микрометров в диаметре, могут проникать глубоко в легкие. 1 Легкие защищены антимикробной системой защиты органов дыхания и системой мукоцилиарной очистки, которая физически выводит частицы из легких.
Дыхательная система, являясь путем воздействия табачного дыма, подвергается воздействию более высоких концентраций токсичных компонентов дыма, чем любая другая система организма. Дым вдыхается через рот и нос, попадает в легкие через верхние и нижние дыхательные пути. В каждой части дыхательной системы дым вызывает повреждения и приводит к таким заболеваниям, как рак и хроническая обструктивная болезнь легких (ХОБЛ). 1 2 В этом разделе описываются основные нераковые респираторные заболевания, вызванные или связанные с курением.
1 2 В этом разделе описываются основные нераковые респираторные заболевания, вызванные или связанные с курением.
3.2.1.1 Нарушение иммунных и защитных реакций легких
Около 60% частиц основного потока сигаретного дыма оседает в легких. Эти частицы вызывают структурные и иммунологические повреждения легких. Частицы дыма также попадают в кровоток через легкие и циркулируют по всему телу. Чтобы избежать вредных последствий этих потенциальных повреждений, дыхательная система использует набор защитных механизмов. Сигаретный дым может ослабить или подавить защитные силы легких, что приведет к острому или хроническому заболеванию. 1
Мукоцилиарный клиренс
Частицы сигаретного дыма и других источников захватываются слизистым слоем на поверхности клеток, выстилающих дыхательные пути. Они удаляются с помощью таких механизмов, как мукоцилиарный клиренс, кашель и альвеолярный клиренс. Во время мукоцилиарного клиренса частицы слизистой удаляются из дыхательных путей синхронизированным движением ресничек, которые представляют собой крошечные волосовидные структуры на поверхности клеток дыхательных путей. 3
3
Воздействие сигаретного дыма снижает скорость выведения частиц из легких. 1 Это частично связано с укорочением, потерей или нарушением координации ресничек, но также может быть связано с изменениями толщины слизи, что снижает эффективное продвижение слизи ресничками. 3 4 5 6 Предполагается, что акролеин и формальдегид в сигаретном дыме вызывают повреждение дыхательных ресничек. 1
Поражение мукоцилиарной системы также увеличивает риск инфицирования. 1 Курильщики все больше полагаются на кашель для удаления слизи, а не на обычный процесс очистки, который является более эффективным и менее раздражающим. 7 Заядлые курильщики сохраняют значительное количество частиц в легких. 1 Отказ от курения улучшает мукоцилярный клиренс в носу через две недели и в легких через три месяца. 4 8
Врожденный иммунитет в дыхательной системе
Врожденные иммунные респираторные реакции состоят из быстродействующих пептидов, белков и лейкоцитов, направленных на блокирование и уничтожение инфекционных патогенов, попадающих в дыхательные пути. Врожденная иммунная система также направляет адаптивную иммунную систему, что приводит к выработке антител и цитотоксическим клеточным ответам, которые защищают от инфекционных агентов, таких как вирус гриппа. 9
Врожденная иммунная система также направляет адаптивную иммунную систему, что приводит к выработке антител и цитотоксическим клеточным ответам, которые защищают от инфекционных агентов, таких как вирус гриппа. 9
Курение нарушает способность иммунной системы легких обнаруживать и уничтожать вирусы и бактерии. 10 11 Курение подрывает врожденную иммунную систему, провоцируя воспалительную реакцию и повышая вероятность инфекции. 1 12 13 Воспаление — это один из типов врожденного иммунного ответа на патогены. Это должен быть быстрый и временный ответ, разрешающийся после устранения угрозы, поскольку хроническое воспаление наносит ущерб. Из-за регулярного вредного воздействия табака у курильщиков обычно возникают хронические воспалительные процессы в легких. 1 14 В отчете Главного хирурга США по прекращению курения за 2020 г. указано, что доказательства были наводящими на размышления, но недостаточными для вывода о том, что это воспаление дыхательных путей сохраняется в течение месяцев или лет после прекращения курения. 15
15
Согласно экспериментальным данным, некоторые определенные химические вещества из табачного дыма могут повредить иммунные реакции легких. В экспериментах на мышах акролеин из сигаретного дыма нарушал способность белков сурфактанта ингибировать рост бактерий и активировать защитные функции альвеолярных макрофагов (лейкоцитов, которые поглощают и уничтожают бактерии). 16 Кадмий из сигаретного дыма может изменить регуляцию врожденного иммунитета и воспаления. Повышенный уровень кадмия в тканях связан с ХОБЛ, которая обычно вызывается курением. 17
3.2.1.2 Нарушение функции легких
Располагаясь под мукоцилиарной системой в легких, наружный слой легочных клеток, выстилающих дыхательные пути, образует физический барьер между легочной тканью и воздушным пространством. Хроническое воздействие сигаретного дыма повреждает этот защитный барьер, вызывая воспаление и увеличивая его проницаемость. 1 12 11
Сигаретный дым вызывает воспалительную реакцию, приводящую к разрушению легочной паренхимы (функциональной ткани, участвующей в газообмене). Этому способствует высвобождение клеточных протеиназ, которые повреждают внеклеточный матрикс легких, запрограммированная гибель клеток из-за окислительного стресса, потеря связи между матриксом и клетками и неэффективное восстановление эластина и других компонентов внеклеточного матрикса, которые увеличивают воздушное пространство. 1, 13
Этому способствует высвобождение клеточных протеиназ, которые повреждают внеклеточный матрикс легких, запрограммированная гибель клеток из-за окислительного стресса, потеря связи между матриксом и клетками и неэффективное восстановление эластина и других компонентов внеклеточного матрикса, которые увеличивают воздушное пространство. 1, 13
Активные курильщики в детстве и подростковом возрасте имеют как снижение функции легких, так и нарушение роста легких. 18 Курение вызывает раннее начало снижения функции легких в позднем подростковом и раннем взрослом возрасте. Все взрослые с возрастом испытывают потерю функции легких, но у курильщиков этот процесс происходит раньше и чаще, чем у некурящих. 10 Среди курильщиков существует скользящая шкала предрасположенности к потере функции легких. 19 20 Некоторые курильщики могут терять функцию легких почти так же медленно, как и некурящие. . У значительного меньшинства курильщиков быстрая потеря функции легких становится инвалидизирующей или смертельной. 1 12 19 Большинство курильщиков попадает в эти группы. 20 Диагноз хронической обструктивной болезни легких (ХОБЛ) может быть поставлен после значительной и необратимой потери функции легких. В популяции курильщиков без ХОБЛ возрастная скорость снижения функции легких замедляется до уровня, наблюдаемого у людей, которые никогда не курили в течение пяти лет после отказа от курения. Однако они не восстанавливают функцию легких, которую они уже потеряли. 14 Отказ от курения является единственным признанным вмешательством, которое со временем снижает потерю функции легких у людей с ХОБЛ. 15
1 12 19 Большинство курильщиков попадает в эти группы. 20 Диагноз хронической обструктивной болезни легких (ХОБЛ) может быть поставлен после значительной и необратимой потери функции легких. В популяции курильщиков без ХОБЛ возрастная скорость снижения функции легких замедляется до уровня, наблюдаемого у людей, которые никогда не курили в течение пяти лет после отказа от курения. Однако они не восстанавливают функцию легких, которую они уже потеряли. 14 Отказ от курения является единственным признанным вмешательством, которое со временем снижает потерю функции легких у людей с ХОБЛ. 15
3.2.2 Курение и респираторные симптомы
Активное курение вызывает респираторные симптомы у взрослых, подростков и детей, включая кашель, выделение мокроты, свистящее дыхание и одышку (затрудненное дыхание и одышку). Эти симптомы связаны с рядом острых и хронических респираторных заболеваний. Они также могут указывать на основное повреждение легких и заболевание. Распространенность этих симптомов среди населения снижается с отказом от курения. 10
Распространенность этих симптомов среди населения снижается с отказом от курения. 10
3.2.3 Влияние курения на острые респираторные инфекции
У курящих взрослых вероятность развития острых респираторных инфекций, таких как пневмония, выше, чем у некурящих. Подробнее см. в разделе 3.9.
3.2.4 Основные хронические респираторные заболевания, вызванные курением
3.2.4.1 Хроническая обструктивная болезнь легких (ХОБЛ)
Хроническая обструктивная болезнь легких (ХОБЛ) характеризуется стойкими респираторными симптомами и ограничением воздушного потока, которое обычно прогрессирует. 21 Хроническое ограничение воздушного потока вызвано сочетанием заболевания мелких дыхательных путей (обструктивный бронхит) и разрушения газообменных поверхностей легких из-за хронического воспаления (так называемая эмфизема). Относительный вклад обеих патологий варьируется от человека к человеку. Изменения не всегда происходят одновременно, и они развиваются с разной скоростью с течением времени. Хронические респираторные симптомы могут предшествовать обструкции дыхательных путей, которая характерна для ХОБЛ. 21
Хронические респираторные симптомы могут предшествовать обструкции дыхательных путей, которая характерна для ХОБЛ. 21
На основе данных, предоставленных самими исследователями из Национального обследования состояния здоровья ABS за 2017–2018 годы, распространенность ХОБЛ среди австралийцев в возрасте 45 лет и старше оценивается в 4,8%. 22 В 2018 г. в Австралии было зарегистрировано 7 113 случаев смерти от ХОБЛ, что делает ее пятой по значимости причиной смерти. 23
Показатели смертности от ХОБЛ со временем снижаются. 23 ХОБЛ более распространена среди людей среднего и пожилого возраста, на этой стадии она имеет важные взаимодействия со многими другими острыми и хроническими заболеваниями. 23 24 Данные также свидетельствуют о том, что женщины могут быть более восприимчивы к развитию тяжелой ХОБЛ в более молодом возрасте. 13 Помимо влияния на смертность, хронический характер ХОБЛ означает, что те, у кого развилась ХОБЛ, могут жить в течение многих лет с различными степенями дискомфорта и инвалидности. 24 Даже у лиц с легким течением ХОБЛ снижается качество жизни, которое ухудшается по мере того, как болезнь становится более тяжелой. 25
24 Даже у лиц с легким течением ХОБЛ снижается качество жизни, которое ухудшается по мере того, как болезнь становится более тяжелой. 25
Курение как причина ХОБЛ
По данным Глобальной инициативы по хронической обструктивной болезни легких (GOLD), причины ХОБЛ включают курение табака, воздействие пассивного курения, генетические факторы, факторы развития легких, воздействие некоторых химических веществ и загрязнителей, а также другие хронические заболевания, которые увеличивают риск ХОБЛ. 21
Курение является основной причиной ХОБЛ. Подсчитано, что у 15-20% постоянных курильщиков в течение длительного времени развивается ХОБЛ, и что курение вызывает большинство случаев ХОБЛ. 14 Метаанализ 133 исследований показал, что у нынешних курильщиков риск развития ХОБЛ в 3,5 раза выше, чем у некурящих. 26 В отчете Главного хирурга США за 2004 г. содержится достаточно доказательств того, что активное курение вызывает заболеваемость и смертность от ХОБЛ. 10 В отчете главного хирурга США за 2014 г. сделан вывод о том, что курение является основной причиной ХОБЛ в Соединенных Штатах. Курение вызывает все элементы фенотипа ХОБЛ, включая эмфизему и поражение дыхательных путей легких. 13
10 В отчете главного хирурга США за 2014 г. сделан вывод о том, что курение является основной причиной ХОБЛ в Соединенных Штатах. Курение вызывает все элементы фенотипа ХОБЛ, включая эмфизему и поражение дыхательных путей легких. 13
Курение является основной причиной ХОБЛ в Австралии. В 2015 г. 68,3% бремени ХОБЛ было связано с употреблением табака у мужчин и 76,5% у женщин в Австралии. 27
Люди с ХОБЛ, которые продолжают курить, могут иметь более тяжелые симптомы и больше обострений. Нынешние курильщики с ХОБЛ могут иметь значительно более низкое качество жизни, связанное со здоровьем, чем бывшие курильщики. 28 29 Однако некоторые исследования выявили одинаковую частоту обострений ХОБЛ у нынешних и бывших курильщиков. 30 31 Курение также может увеличить риск острых респираторных инфекций у людей с ранее существовавшей ХОБЛ. 10
Патофизиология ХОБЛ
ХОБЛ возникает в результате прогрессирующего необратимого повреждения дыхательных путей и дыхательных мешков (альвеол) легких. Основными процессами, которые считаются важными в развитии ХОБЛ, вызванной курением, являются воспаление, окислительный стресс и дисбаланс протеаз (ферментов, расщепляющих определенные белки) и антипротеаз в легких. 1 10 Окислительный стресс возникает в результате высокореактивных свободных радикалов и окисляющих химических веществ в табачном дыме, что создает дисбаланс между окислителями и антиоксидантами в легких. Окислительный стресс может напрямую повреждать клетки легких, способствовать воспалению и способствовать дисбалансу протеаз-антипротеаз.
Основными процессами, которые считаются важными в развитии ХОБЛ, вызванной курением, являются воспаление, окислительный стресс и дисбаланс протеаз (ферментов, расщепляющих определенные белки) и антипротеаз в легких. 1 10 Окислительный стресс возникает в результате высокореактивных свободных радикалов и окисляющих химических веществ в табачном дыме, что создает дисбаланс между окислителями и антиоксидантами в легких. Окислительный стресс может напрямую повреждать клетки легких, способствовать воспалению и способствовать дисбалансу протеаз-антипротеаз.
Хотя у всех курильщиков есть воспаление легких, не у всех развивается ХОБЛ. Считается, что у людей, у которых развивается ХОБЛ, наблюдается усиленная или аномальная воспалительная реакция на вредные частицы или газы (обычно от сигаретного дыма). 1 14 Известны некоторые генетические причины ХОБЛ. Люди с дефицитом альфа-1-антитрипсина, распространенным наследственным заболеванием, 1, 13 21 , или люди с редким наследственным заболеванием, называемым кожной недостаточностью, подвержены большему риску ХОБЛ. 13
13
Различные болезненные процессы приводят к ограничению скорости воздушного потока, характерному для ХОБЛ. Основными заболеваниями являются обструктивный бронхиолит и эмфизема легких. 1 14 Хронический бронхит часто сочетается с ХОБЛ (как описано ниже). Курильщики по-разному восприимчивы к каждому заболеванию, и это влияет на их симптомы.
Обструктивный бронхиолит
Воспаление мелких дыхательных путей в той или иной степени наблюдается у всех курильщиков, у некоторых наблюдается хронический бронхит (описано ниже). 10 32 Обструкция мелких дыхательных путей (обструктивный бронхит) возникает, когда в мелких бронхах и бронхиолах легких происходит аномально усиленное воспаление и ремоделирование. Термин «ремоделирование» описывает цикл повреждения и восстановления при наличии воспаления, что приводит к утолщению стенки дыхательных путей и сужению просвета дыхательных путей. Основная причина может быть связана с перепроизводством и гиперсекрецией слизи бокаловидными клетками. 12 21 33 Этот процесс препятствует потоку воздуха через мелкие дыхательные пути в воздушные мешочки легких (альвеолы), где происходит газообмен. Пока курение продолжается, состояние прогрессирует. Основным симптомом является одышка, потому что постепенно изменяющаяся структура легких не позволяет увеличить поток воздуха, необходимый для комфортных упражнений. 12 Отказ от курения замедляет снижение функции легких, и устойчивый отказ от курения необходим, чтобы вернуть снижение функции легких к состоянию некурящего. 10
12 21 33 Этот процесс препятствует потоку воздуха через мелкие дыхательные пути в воздушные мешочки легких (альвеолы), где происходит газообмен. Пока курение продолжается, состояние прогрессирует. Основным симптомом является одышка, потому что постепенно изменяющаяся структура легких не позволяет увеличить поток воздуха, необходимый для комфортных упражнений. 12 Отказ от курения замедляет снижение функции легких, и устойчивый отказ от курения необходим, чтобы вернуть снижение функции легких к состоянию некурящего. 10
Эмфизема
Эмфизема представляет собой необратимое разрушение стенок альвеол — небольших воздушных мешочков, в которых происходит газообмен. Поскольку этот каркас утрачен, стенки альвеол не могут регенерировать, а воздушные полости увеличиваются. В результате потеря площади поверхности, на которой происходит газообмен, снижает способность легких переносить кислород к эритроцитам и удалять углекислый газ из кровотока — его основные функции. 4 34 Легкие становятся менее эластичными, что ограничивает их способность сокращаться и расширяться. Потеря упругой отдачи уменьшает силу, выталкивающую воздух из легких, поэтому выдох занимает больше времени. 1 12 При запущенной эмфиземе неэластичные легкие увеличиваются, что приводит к большой бочкообразной форме грудной клетки.
4 34 Легкие становятся менее эластичными, что ограничивает их способность сокращаться и расширяться. Потеря упругой отдачи уменьшает силу, выталкивающую воздух из легких, поэтому выдох занимает больше времени. 1 12 При запущенной эмфиземе неэластичные легкие увеличиваются, что приводит к большой бочкообразной форме грудной клетки.
Курение приводит к сдвигу протеазно-антипротеазного баланса в сторону протеаз. 1 Протеазы — это ферменты, расщепляющие определенные белки. Эмфизема связана с избыточной активностью протеаз, которые разрушают белки внеклеточного матрикса, такие как эластин и коллаген, в дыхательных путях и альвеолах. 10 Против этой деградации белка действуют антипротеазы, такие как альфа-1-антитрипсин. Считается, что люди с более низкой антипротеазной активностью по наследству более подвержены ХОБЛ. Однако протеазно-антипротеазный баланс не полностью объясняет повреждение, лежащее в основе ХОБЛ, указывая на то, что в основе этого болезненного процесса лежат и другие механизмы. 35
35
Течение ХОБЛ после отказа от курения
Отказ от курения является единственным установленным вмешательством, уменьшающим потерю функции легких у людей с ХОБЛ. 15 36 Отказ от курения также снижает риск развития ХОБЛ у курильщиков сигарет. 15 У людей с ХОБЛ наблюдается небольшое среднее улучшение функции легких в течение года после отказа от курения. После этого возрастное снижение функции легких составляет менее половины того, что наблюдается у продолжающих курить. 14 Уменьшение количества выкуриваемых сигарет не влияет на потерю функции легких. 37 Бывшие курильщики имеют меньший риск госпитализации в связи с ХОБЛ и смерти от ХОБЛ по сравнению с теми, кто продолжает курить. 14 38
3.2.4.2 Хронический бронхит
Хронический бронхит характеризуется симптомами кашля в сочетании с частым и повышенным выделением мокроты или мокроты. Диагноз ставится, когда эти симптомы присутствуют в течение трех месяцев в течение каждого из двух лет подряд. 1 Хронический бронхит связан с воспалением крупных и мелких бронхов, что приводит к увеличению слизеобразующих желез и ремоделированию (утолщению) стенок дыхательных путей. Люди с хроническим бронхитом чаще болеют респираторными инфекциями. 1 39 У лиц с хронической обструктивной болезнью легких (ХОБЛ) симптомы хронического бронхита повышают риск смерти от респираторных инфекций. 40
1 Хронический бронхит связан с воспалением крупных и мелких бронхов, что приводит к увеличению слизеобразующих желез и ремоделированию (утолщению) стенок дыхательных путей. Люди с хроническим бронхитом чаще болеют респираторными инфекциями. 1 39 У лиц с хронической обструктивной болезнью легких (ХОБЛ) симптомы хронического бронхита повышают риск смерти от респираторных инфекций. 40
Хронический бронхит часто сочетается с ХОБЛ, но не влияет на ограничение скорости воздушного потока, если только воспаление не распространяется на мелкие дыхательные пути. 1 Наличие симптомов хронического бронхита связано с ускоренным ухудшением функции легких, наблюдаемым при ХОБЛ. 1 10 Ранее считалось, что хронический бронхит является необходимым первым шагом в развитии ХОБЛ. Однако с тех пор исследования показали, что ограничение воздушного потока может развиться без симптомов хронического бронхита. 1 Также у людей с нормальной функцией легких наличие хронического бронхита не увеличивает вероятность развития ХОБЛ. 1 14
1 14
Курение является давно известной причиной хронического бронхита. 41 1 26 Метаанализ 101 исследования 2011 года показал, что у нынешних курильщиков риск развития хронического бронхита в 3,4 раза выше, чем у некурящих. 26 Симптомы хронического бронхита уменьшаются через один-два месяца после отказа от курения, а распространенность кашля и мокроты у населения возвращается к уровню никогда не куривших в течение пяти лет. 14 У людей с тяжелой формой ХОБЛ хронический кашель, связанный с хроническим бронхитом, с большей вероятностью сохраняется после прекращения курения. 39
3.2.5 Другие респираторные заболевания, связанные с курением
3.2.5.1 Астма
Астма является распространенным хроническим респираторным заболеванием, которым страдает примерно каждый девятый человек в Австралии. 42 У больных астмой наблюдается обструкция (сужение) дыхательных путей, что приводит к свистящему дыханию, одышке, кашлю, стеснению в груди и/или усталости. Тяжелая астма может быть опасной для жизни: в 2018 г. в Австралии погибло 389 человек. 43 Триггерами симптомов астмы являются табачный дым, аллергены, респираторные инфекции и воздействие некоторых химических веществ.
Тяжелая астма может быть опасной для жизни: в 2018 г. в Австралии погибло 389 человек. 43 Триггерами симптомов астмы являются табачный дым, аллергены, респираторные инфекции и воздействие некоторых химических веществ.
Астма обычно начинается в детстве и со временем часто становится реже. Однако у некоторых людей это может продолжаться, повторяться или начинаться позже в жизни. Эти временные периоды могут означать, что трудно быть уверенным в том, что воздействие табачного дыма предшествовало возникновению заболевания, что усложняет изучение причинно-следственной связи.
В отчете главного хирурга США за 2014 г. были рассмотрены 12 исследований риска астмы среди курящих подростков. Многие из этих исследований показали повышенный риск астмы среди курящих подростков, но было проведено ограниченное количество исследований высокого качества. В отчете сделан вывод о том, что имеющиеся данные предполагают, но недостаточны для вывода о том, что активное курение является причиной астмы у подростков. Точно так же в этом отчете также сделан вывод о том, что доказательства предполагают, но недостаточны для вывода о том, что курение увеличивает заболеваемость астмой у взрослых.
Точно так же в этом отчете также сделан вывод о том, что доказательства предполагают, но недостаточны для вывода о том, что курение увеличивает заболеваемость астмой у взрослых.
Курение обостряет астму у взрослых и приводит к плохому контролю астмы. 10 13 44 Три рандомизированных контрольных группы определили, что ингаляционные кортикостероиды приносят меньше пользы курильщикам с астмой по сравнению с некурящими. 13 45 46 47 В одном из этих исследований у курильщиков частота обострений при приеме кортикостероидов для контроля астмы была в 6 раз выше, чем у некурящих. 47 Курящие люди с астмой чаще страдают от ускоренной потери функции легких. 13 48 49 В исследовании Copenhagen City Heart Study у взрослых курильщиков с астмой наблюдалось более выраженное ухудшение функции легких с течением времени, чем у некурящих. 50 У курильщиков повышен риск тяжелых приступов астмы, таких как госпитализация, обращение в службу неотложной помощи и смерть. 13 49 51
13 49 51
В отчете главного хирурга США за 2014 г. сделан вывод о том, что доказательства предполагают, но недостаточны для демонстрации причинно-следственной связи курения с обострением астмы у детей и подростков. 13
Отказ от курения может улучшить контроль над астмой. 52 53 15 Однако в отчете главного хирурга США за 2020 г. сделан вывод о том, что, хотя фактические данные свидетельствуют о том, что отказ от курения уменьшает симптомы астмы, улучшает результаты лечения и показатели качества жизни, характерные для астмы, а также улучшает функцию легких у курильщики, этого в настоящее время недостаточно, чтобы сделать вывод о причинно-следственной связи. 15
Дополнительную информацию о влиянии курения родителей, бабушек и дедушек и перинатального курения на астму у детей см. в разделе 3.8.
3.2.5.2 Интерстициальные заболевания легких (IDL)
Интерстициальные заболевания легких представляют собой группу заболеваний, которые в основном характеризуются прогрессирующим рубцеванием интерстициальной альвеолярной ткани. Патофизиология часто представляет собой фиброз (образование рубцовой ткани) и воспаление. Некоторые из этих нарушений вызваны или спровоцированы воздействием токсичных материалов или связаны с аутоиммунными заболеваниями, заболеваниями соединительной ткани или применением определенных лекарств. 54 В отчете «Болезни легких в Австралии» за 2014 г. указано, что интерстициальные заболевания легких привели к 4050 госпитализациям и 1161 смерти в 2011–2012 гг. 55
Патофизиология часто представляет собой фиброз (образование рубцовой ткани) и воспаление. Некоторые из этих нарушений вызваны или спровоцированы воздействием токсичных материалов или связаны с аутоиммунными заболеваниями, заболеваниями соединительной ткани или применением определенных лекарств. 54 В отчете «Болезни легких в Австралии» за 2014 г. указано, что интерстициальные заболевания легких привели к 4050 госпитализациям и 1161 смерти в 2011–2012 гг. 55
Идиопатический легочный фиброз — это прогрессирующее фатальное фиброзное интерстициальное заболевание легких. Это одно из самых распространенных и тяжелых интерстициальных заболеваний легких. Он имеет наихудший прогноз из всех идиопатических интерстициальных заболеваний легких со средним временем выживания от трех до четырех лет. 56 Хотя его причины неизвестны, данные свидетельствуют о том, что в его развитии участвуют как генетические факторы, так и факторы окружающей среды. 57 Заболеваемость и распространенность идиопатического легочного фиброза в Австралии в настоящее время трудно оценить. 55
55
В отчете Главного хирурга США за 2014 г. проанализировано 12 исследований риска идиопатического легочного фиброза у курильщиков. 13 Все, кроме одного, обнаружили повышенный риск этого заболевания у курильщиков. В двух крупнейших исследованиях сообщалось об отношении шансов 1,59 и 1,57 для идиопатического легочного фиброза у когда-либо куривших по сравнению с никогда не курившими. Тем не менее, есть некоторые проблемы с качеством эпидемиологических исследований, такие как непоследовательная корректировка с учетом потенциальных искажающих факторов. В отчете за 2014 г. сделан вывод о том, что доказательства предполагают, но недостаточны для вывода о том, что курение является причиной идиопатического легочного фиброза. 13
Респираторный бронхиолит-интерстициальное заболевание легких (RB-ILD) наблюдается у очень заядлых курильщиков, обычно у тех, кто выкуривает более 30 сигарет в день. В отличие от типичной ХОБЛ, ее можно наблюдать у молодых курильщиков. 58 59 RB-ILD — это сильно преувеличенная форма бронхиолита, которая распространяется, вызывая воспаление в близлежащих альвеолах. RB-ILD ухудшает функцию легких и имеет ненормальный вид на рентгенограммах грудной клетки. Рекомендуется прекращение курения. 58
58 59 RB-ILD — это сильно преувеличенная форма бронхиолита, которая распространяется, вызывая воспаление в близлежащих альвеолах. RB-ILD ухудшает функцию легких и имеет ненормальный вид на рентгенограммах грудной клетки. Рекомендуется прекращение курения. 58
3.2.5.3 Легочный гистиоцитоз X (легочный лангергансоклеточный гистиоцитоз)
Гистиоцитоз X — редкий вид рака, вызывающий поражение различных областей тела. Легочный гистиоцитоз X включает развитие воспалительных узелков в легких наряду с кистозной дегенерацией самих легких. Он имеет отчетливый вид на рентгеновских снимках. Пациенты обычно молодые люди, и подавляющее большинство из них в анамнезе курили. 58 Настоятельно рекомендуется отказ от курения, поскольку в отчетах о случаях заболевания после прекращения курения отмечается улучшение и даже восстановление нормальной или почти нормальной структуры легких. 58 60 61 Таким образом, курение может быть причиной этого заболевания, но текущих исследований недостаточно, чтобы сделать такой вывод.
3.2.5.4 Обоняние
См. раздел 3.22.6.
3.2.5.5 Храп
См. раздел 3.22.4.
Соответствующие новости и исследования
Чтобы ознакомиться с последними новостями и исследованиями по этой теме, нажмите здесь. ( Последнее обновление: август 2022 г.)
Ссылки
1. Министерство здравоохранения и социальных служб США. Как табачный дым вызывает болезни: биологическая и поведенческая основа заболеваний, связанных с курением. Отчет главного хирурга США, Атланта, Джорджия: Министерство здравоохранения и социальных служб США, Центры по контролю и профилактике заболеваний, Национальный центр профилактики хронических заболеваний и укрепления здоровья, Управление по вопросам курения и здоровья, 2010 г. Доступно по адресу: https: //www.ncbi.nlm.nih.gov/books/NBK53017/.
2. Чарг А., Косио М. и Райт Дж.Л. Механизмы ХОБЛ, вызванной сигаретным дымом: выводы из моделей на животных. Американский журнал физиологии. Клеточная и молекулярная физиология легких, 2008 г.; 294(4):L612-31. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/18223159
Клеточная и молекулярная физиология легких, 2008 г.; 294(4):L612-31. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/18223159
3. Leopold PL, O’Mahony MJ, Lian XJ, Tilley AE, Harvey BG, et al. Курение связано с укорочением ресничек дыхательных путей. ПЛОС ОДИН, 2009; 4(12):e8157. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/20016779
4. Министерство здравоохранения и социальных служб США. Последствия курения для здоровья: хроническая обструктивная болезнь легких. Доклад главного хирурга. Роквилл, Мэриленд: Министерство здравоохранения и социальных служб США, Служба общественного здравоохранения, Управление по вопросам курения и здоровья, 19.84. Доступно по адресу: https://profiles.nlm.nih.gov/spotlight/nn/catalog/nlm:nlmuid-101584932X476-doc.
5. Стэнли П.Дж., Уилсон Р., Гринстоун М.А., МакВильям Л. и Коул П.Дж. Влияние курения сигарет на назальный мукоцилиарный клиренс и частоту цилиарных сокращений. Торакс, 1986; 41(7):519-23. Доступно по адресу: https://www. ncbi.nlm.nih.gov/pubmed/3787531
ncbi.nlm.nih.gov/pubmed/3787531
6. Kreindler JL, Jackson AD, Kemp PA, Bridges RJ, and Danahay H. экстракт сигаретного дыма. Американский журнал физиологии. Клеточная и молекулярная физиология легких, 2005; 288(5):L894-902. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/15626749
7. Houtmeyers E, Gosselink R, Gayan-Ramirez G и Decramer M. Регуляция мукоцилиарного клиренса в норме и при патологии. Европейский респираторный журнал, 1999 г.; 13(5):1177-88. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/10414423
8. Ramos EM, De Toledo AC, Xavier RF, Fosco LC, Vieira RP, et al. Обратимость нарушения назального мукоцилиарного клиренса у курильщиков после программы отказа от курения. Респирология, 2011; 16(5):849-55. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/21545372
9. Riches DWH и Martin TR. Обзор врожденного иммунитета легких и воспаления. Методы молекулярной биологии, 2018; 1809:17-30. Доступно по адресу: https://www.ncbi.nlm. nih.gov/pubmed/29987779
nih.gov/pubmed/29987779
10. Министерство здравоохранения и социальных служб США. Последствия курения для здоровья: доклад главного хирурга. Атланта, Джорджия: Министерство здравоохранения и социальных служб США, Служба общественного здравоохранения, Центры по контролю и профилактике заболеваний, Национальный центр по профилактике хронических заболеваний и укреплению здоровья, Управление по вопросам курения и здоровья, 2004 г. Доступно по адресу: https://www. cdc.gov/tobacco/data_statistics/sgr/2004/index.htm.
11. Stampfli MR и Anderson GP. Как сигаретный дым искажает иммунный ответ, способствуя инфекции, заболеваниям легких и раку. Обзоры природы. Иммунология, 2009; 9(5):377-84. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/116
12. Hogg JC. Патофизиология ограничения воздушного потока при хронической обструктивной болезни легких. Ланцет, 2004; 364 (9435): 709-21. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/15325838
13. Министерство здравоохранения и социальных служб США. Последствия курения для здоровья — 50 лет прогресса. Атланта, Джорджия: Министерство здравоохранения и социальных служб США, Центры по контролю и профилактике заболеваний, Национальный центр по профилактике хронических заболеваний и укреплению здоровья, Управление по вопросам курения и здоровья, 2014 г. Доступно по адресу: https://www.ncbi.nlm. nih.gov/books/NBK179276/
Последствия курения для здоровья — 50 лет прогресса. Атланта, Джорджия: Министерство здравоохранения и социальных служб США, Центры по контролю и профилактике заболеваний, Национальный центр по профилактике хронических заболеваний и укреплению здоровья, Управление по вопросам курения и здоровья, 2014 г. Доступно по адресу: https://www.ncbi.nlm. nih.gov/books/NBK179276/
14. Международное агентство по изучению рака. Уменьшение риска после отказа от курения. Справочники IARC по профилактике рака и борьбе против табака, 11 Vol. 11. Лион, Франция: IARC, 2007. Доступно по ссылке: https://publications.iarc.fr/Book-And-Report-Series/Iarc-Handbooks-Of-Cancer-Prevention/Tobacco-Control-Reversal-Of-Risk. -После отказа от курения-2007.
15. Министерство здравоохранения и социальных служб США. Отказ от курения. Доклад главного хирурга. Атланта, Джорджия, Министерство здравоохранения и социальных служб США, Центры по контролю и профилактике заболеваний, Национальный центр по профилактике хронических заболеваний и укреплению здоровья, Управление по вопросам курения и здоровья, 2020 г. Доступно по адресу: https://www.cdc.gov/tobacco/ data_statistics/sgr/2020-прекращение курения/.
Доступно по адресу: https://www.cdc.gov/tobacco/ data_statistics/sgr/2020-прекращение курения/.
16. Takamiya R, Takahashi M, Maeno T, Saito A, Kato M, et al. Акролеин в сигаретном дыме ослабляет врожденные иммунные реакции, опосредованные поверхностно-активным белком D. Biochimica et Biophysica Acta — General Subjects, 2020; 1864 (11): 129699. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/32738274
17. Knoell DL и Wyatt TA. Неблагоприятное влияние кадмия на иммунную функцию и защиту легких хозяина. Семинары по биологии клетки и развития, 2020 г. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/33158728
18. Министерство здравоохранения и социальных служб США. Профилактика употребления табака среди молодежи: отчет главного хирурга. Атланта, Джорджия: Министерство здравоохранения и социальных служб США, Центры по контролю и профилактике заболеваний, Национальный центр по профилактике хронических заболеваний и укреплению здоровья, Управление по вопросам курения и здоровья, 2012 г. Доступно по адресу: http://www.cdc.gov/ табак/data_statistics/sgr/2012/.
Доступно по адресу: http://www.cdc.gov/ табак/data_statistics/sgr/2012/.
19. Fletcher C и Peto R. Естественное течение хронической обструкции дыхательных путей. Британский медицинский журнал, 1977; 1(6077):1645-8. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/871704
20. Реннард С.И. и Вестбо Дж. ХОБЛ: опасная недооценка на 15%. Ланцет, 2006; 367 (9518): 1216-9. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/16631861
21. Глобальная инициатива по хронической обструктивной болезни легких. Глобальная стратегия диагностики, лечения и профилактики хронической обстриктивной болезни легких. отчет за 2018 год. 2018. Доступно по адресу: https://goldcopd.org/wp-content/uploads/2017/11/GOLD-2018-v6.0-FINAL-revised-20-Nov_WMS.pdf.
22. Австралийское бюро статистики. Национальное обследование состояния здоровья: первые результаты, 2017–2018 годы. Кат № 4364.0.55.001 Канберра, Австралия: ABS, 2018 г. Доступно по адресу: https://www.abs.gov.au/statistics/health/health-conditions-and-risks/national-health-survey-first-results/latest- выпускать.
23. Австралийский институт здравоохранения и социального обеспечения. Хроническая обструктивная болезнь легких (ХОБЛ). Канберра, Австралия: AIHW, 2020 г. Доступно по адресу: https://www.aihw.gov.au/reports/chronic-respiratory-conditions/copd/contents/copd.
24. Австралийский институт здравоохранения и социального обеспечения, Здоровье Австралии, 2010 г. Серия сообщений о здоровье Австралии №. 12. АИЗС кат. нет. AUS 122. Канберра: AIHW; 2010. Доступно по адресу: https://www.aihw.gov.au/reports/australias-health/australias-health-2010/contents/table-of-contents.
25. Деверо Г. Азбука хронической обструктивной болезни легких. Определение, эпидемиология и факторы риска. Британский медицинский журнал, 2006 г.; 332 (7550): 1142-4. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/1669.0673
26. Фори Б.А., Торнтон А.Дж. и Ли П.Н. Систематический обзор с метаанализом эпидемиологических данных о связи курения с ХОБЛ, хроническим бронхитом и эмфиземой. BMC пульмонология, 2011; 11:36. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/21672193
Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/21672193
27. Австралийский институт здравоохранения и социального обеспечения. Бремя употребления табака в Австралии: Австралийское исследование бремени болезней, 2015 г. Канберра, 2019 г. Доступно по адресу: https://www.aihw.gov.au/getmedia/953dcb20-b369-4c6b-b20f-526bdead14cb/aihw-bod-20. pdf.aspx?inline=true.
28. Черуву В.К., Одиамбо Л.А., Маулс Д.С., Зулло М.Д., Гудина А.Т. Качество жизни, связанное со здоровьем, у нынешних курильщиков с ХОБЛ: факторы, связанные с нынешним курением, и новое понимание половых различий. Международный журнал хронической обструктивной болезни легких, 2016 г.; 11:2211-9. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/27695308
29. Riesco JA, Alcazar B, Trigueros JA, Campuzano A, Perez J, et al. Активное курение и фенотип ХОБЛ: распространение и влияние на прогностические факторы. Международный журнал хронической обструктивной болезни легких, 2017 г.; 12:1989-99. Доступно по адресу: https://www. ncbi.nlm.nih.gov/pubmed/28740378
ncbi.nlm.nih.gov/pubmed/28740378
30. Baris SA, Onyilmaz T, Basyigit I, Boyaci H, and Yildiz F. Частота обострений и госпитализаций у пациентов с продолжающейся ХОБЛ. курить. Акта Медика Окаяма, 2017 г.; 71(1):11-7. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/28238005
31. Tal S, Adir Y, Stein N, Shalom H, Lache O, et al. Фенотип обострения ХОБЛ обратно связан с текущим курением, но не с фенотипом гаптоглобина. Журнал Израильской медицинской ассоциации, 2019 г.; 21(1):19-23. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/30685900
32. Hogg JC, Wright JL, Wiggs BR, Coxson HO, Opazo Saez A, et al. Строение и функция легких у курильщиков сигарет. Торакс, 1994; 49(5):473-8. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/8016769
33. Ким В. и Крайнер Г.Дж. Хронический бронхит и хроническая обструктивная болезнь легких. Американский журнал респираторной и интенсивной терапии, 2013 г.; 187(3):228-37. Доступно по адресу: https://www. ncbi.nlm.nih.gov/pubmed/23204254
ncbi.nlm.nih.gov/pubmed/23204254
34. Австралийский институт здравоохранения и социального обеспечения. Хронические заболевания и связанные с ними факторы риска в Австралии, 2001. Кат. нет. PHE 33, Канберра, Австралия: AIHW, 2002 г. Доступно по адресу: https://www.aihw.gov.au/reports/chronic-disease/associated-risk-factors-australia-2001/contents/table-of-contents.
35. Ломас Д.А. Объясняет ли протеазно-антипротеазный дисбаланс хроническую обструктивную болезнь легких? Анналы Американского торакального общества, 2016 г.; 13 Приложение 2:S130-7. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/271159.47
36. Барнс П.Дж. Хроническое обструктивное заболевание легких. Медицинский журнал Новой Англии, 2000 г.; 343(4):269-80. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/100
37. Godtfredsen NS, Vestbo J, Osler M, and Prescott E. Риск госпитализации по поводу ХОБЛ после прекращения и сокращения курения: a Изучение населения Дании. Торакс, 2002; 57(11):967-72. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/12403880
Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/12403880
38. Godtfredsen NS, Lam TH, Hansel TT, Leon ME, Gray N, et al. Заболеваемость и смертность, связанные с ХОБЛ, после отказа от курения: состояние доказательств. Европейский респираторный журнал, 2008 г.; 32(4):844-53. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/18827152
39. Браман С.С. Хронический кашель из-за хронического бронхита: рекомендации ACCP по клинической практике, основанные на фактических данных. Сундук, 2006; 129 (1 Дополнение): 104S-15S. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/16428699
40. Прескотт Э., Ланге П. и Вестбо Дж. Хроническая гиперсекреция слизи при ХОБЛ и смерть от легочной инфекции. Европейский респираторный журнал, 1995 г.; 8(8):1333-8. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/7489800
41. Министерство здравоохранения, образования и социального обеспечения, курение и здоровье: отчет Консультативного комитета главному хирургу общественного здравоохранения. Обслуживание. Публикация № (PHS) 1103 Вашингтон: Министерство здравоохранения, образования и социального обеспечения США, Служба общественного здравоохранения, Центр по контролю за заболеваниями; 1964. Доступно по адресу: https://profiles.nlm.nih.gov/spotlight/nn/catalog/nlm:nlmuid-101584932X202-doc.
Обслуживание. Публикация № (PHS) 1103 Вашингтон: Министерство здравоохранения, образования и социального обеспечения США, Служба общественного здравоохранения, Центр по контролю за заболеваниями; 1964. Доступно по адресу: https://profiles.nlm.nih.gov/spotlight/nn/catalog/nlm:nlmuid-101584932X202-doc.
42. Австралийский институт здравоохранения и социального обеспечения. Астма. Канберра, Австралия: AIHW, 2020. Доступно по адресу: https://www.aihw.gov.au/reports/chronic-respiratory-conditions/asthma/contents/asthma.
43. Австралийский институт здравоохранения и социального обеспечения. Книги общего учета смертности (GRIM). Канберра, Австралия: AIHW, 2020. Доступно по адресу: https://www.aihw.gov.au/reports/life-expectancy-deaths/grim-books/contents/grim-excel-workbooks.
44. Австралийский центр мониторинга астмы. Астма в Австралии, 2011 г.: с акцентом на хроническую обструктивную болезнь легких. Серия AIHW по астме №. 4, кот. нет. ACM 22, Канберра, Австралия: AIHW, доступно по адресу: https://www. aihw.gov.au/reports/chronic-respiratory-conditions/asthma-in-australia-2011-with-chapter-on-copd/contents/ оглавление.
aihw.gov.au/reports/chronic-respiratory-conditions/asthma-in-australia-2011-with-chapter-on-copd/contents/ оглавление.
45. Chalmers GW, Macleod KJ, Little SA, Thomson LJ, McSharry CP, et al. Влияние курения сигарет на лечение ингаляционными кортикостероидами при легкой форме астмы. Торакс, 2002; 57(3):226-30. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/11867826
46. Lazarus SC, Chinchilli VM, Rollings NJ, Boushey HA, Cherniack R, et al. Курение влияет на реакцию на ингаляционные кортикостероиды или антагонисты лейкотриеновых рецепторов при астме. Американский журнал респираторной и интенсивной терапии, 2007 г.; 175(8):783-90. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/17204725
47. Tomlinson JE, McMahon AD, Chaudhuri R, Thompson JM, Wood SF, et al. Эффективность низких и высоких доз ингаляционных кортикостероидов у курильщиков по сравнению с некурящими с легкой астмой. Торакс, 2005; 60(4):282-7. Доступно по адресу: https://www.ncbi.nlm.nih. gov/pubmed/1579.0982
gov/pubmed/1579.0982
48. Джеймс А.Л., Палмер Л.Дж., Кичич Э., Максвелл П.С., Лаган С.Е. и др. Снижение функции легких в исследовании здоровья Басселтона: последствия астмы и курения сигарет. Американский журнал респираторной и интенсивной терапии, 2005 г.; 171(2):109-14. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/15486340
49. Thomson NC и Spears M. Влияние курения сигарет на стойкую обструкцию дыхательных путей при астме. Анналы респираторной медицины, 2011 г.; 2(1):47. Доступно по адресу: https://www.researchgate.net/publication/22847129.9_The_Role_of_Cigarette_Smoking_on_Persistent_Airflow_Obstruction_in_Asthma
50. Lange P, Parner J, Vestbo J, Schnohr P, and Jensen G. 15-летнее последующее исследование вентиляционной функции у взрослых с астмой. Медицинский журнал Новой Англии, 1998 г.; 339(17):1194-200. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/9780339
51. Ulrik CS и Frederiksen J. Смертность и маркеры риска смерти от астмы среди 1075 амбулаторных пациентов с астмой. Грудь, 1995; 108(1):10-5. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/76069.41
Грудь, 1995; 108(1):10-5. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/76069.41
52. Chaudhuri R, Livingston E, McMahon AD, Lafferty J, Fraser I, et al. Влияние отказа от курения на функцию легких и воспаление дыхательных путей у курильщиков с астмой. Американский журнал респираторной и интенсивной терапии, 2006 г.; 174(2):127-33. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/16645173
53. Tonnesen P, Pisinger C, Hvidberg S, Wennike P, Bremann L, et al. Последствия отказа от курения и снижения заболеваемости астмой. Исследование никотина и табака, 2005 г.; 7(1):139-48. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/15804686
54. Зибрак Дж. Д. и Прайс Д. Интерстициальное заболевание легких: повышение индекса подозрения в первичной медико-санитарной помощи. Респираторная медицина первичной медико-санитарной помощи NPJ, 2014 г.; 24:14054. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/25208940
55. Prasad J, Holland AE, Glaspole I и Westall G. Идиопатический легочный фиброз: взгляд Австралии. Журнал внутренних болезней, 2016; 46(6):663-8. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/27257148
Идиопатический легочный фиброз: взгляд Австралии. Журнал внутренних болезней, 2016; 46(6):663-8. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/27257148
56. Бер Дж. Диагностика и лечение идиопатического легочного фиброза. Deutsches Ärzteblatt International, 2013 г.; 110(51-52):875-81. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/24529303
57. Уолтерс Г.И. Профессиональные облучения и идиопатический легочный фиброз. Текущее мнение в области аллергии и клинической иммунологии, 2020 г .; 20(2):103-11. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/31895128
58. Caminati A и Harari S. Интерстициальные пневмонии, связанные с курением, и легочный лангергансоклеточный гистиоцитоз. Труды Американского торакального общества, 2006 г .; 3(4):299-306. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/16738193
59. Portnoy J, Veraldi KL, Schwarz MI, Cool CD, Curran-Everett D, et al. Респираторный бронхиолит-интерстициальное заболевание легких: отдаленные результаты. Сундук, 2007; 131(3):664-71. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/17356078
Сундук, 2007; 131(3):664-71. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/17356078
60. Negrin-Dastis S, Butenda D, Dorzee J, Fastrez J, and d’Odemont JP. Полное исчезновение аномалий легких на компьютерной томографии высокого разрешения: случай гистиоцитоза X. Canadian Respiratory Journal, 2007; 14(4):235-7. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/17551600
61. Kinoshita Y, Watanabe K, Sakamoto A и Hidaka K. Легочная легочная гипертензия, связанная с гистиоцитозом клеток Лангерганса, демонстрирующая резкое улучшение после прекращения курения. Терапия, 2016; 55(5):491-5. Доступно по адресу: https://www.ncbi.nlm.nih.gov/pubmed/269
Заявление ВОЗ: Употребление табака и COVID-19
Заявление ВОЗ: Употребление табака и COVID-19- Все темы »
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- Q
- R
- Q
- R
- P
- Q
- .

- U
- V
- W
- X
- Y
- Z
- Ресурсы »
- Бюллетени
- Факты в картинках
- Мультимедиа
- Публикации
- Вопросы и Ответы
- Инструменты и наборы инструментов
- Популярный »
- Загрязнение воздуха
- Коронавирусная болезнь (COVID-19)
- Гепатит
- оспа обезьян
- Все страны »
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- J
- K
- M
- K
- M
- K 9000 2
- M
- K
- I
- K
- I
- K
- M
- 0005
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- x
- Y
- Z
- Африка
- Америка
- Юго-Восточная Азия
- Европа
- Восточное Средиземноморье
- Западная часть Тихого океана
- ВОЗ в странах »
- Статистика
- Стратегии сотрудничества
- Украина ЧП
- все новости »
- Выпуски новостей
- Заявления
- Кампании
- Комментарии
- События
- Тематические истории
- Выступления
- Прожекторы
- Информационные бюллетени
- Библиотека фотографий
- Список рассылки СМИ
- Заголовки »
- Сконцентрируйся »
- Афганистан кризис
- COVID-19 пандемия
- Кризис в Северной Эфиопии
- Сирийский кризис
- Украина ЧП
- Вспышка оспы обезьян
- Кризис Большого Африканского Рога
- Последний »
- Новости о вспышках болезней
- Советы путешественникам
- Отчеты о ситуации
- Еженедельный эпидемиологический отчет
- ВОЗ в чрезвычайных ситуациях »
- Наблюдение
- Исследовательская работа
- Финансирование
- Партнеры
- Операции
- Независимый надзорный и консультативный комитет
- Данные ВОЗ »
- Глобальные оценки здоровья
- ЦУР в области здравоохранения
- База данных о смертности
- Сборы данных
- Панели инструментов »
- COVID-19Приборная доска
- Приборная панель «Три миллиарда»
- Монитор неравенства в отношении здоровья
- Особенности »
- Глобальная обсерватория здравоохранения
- СЧЕТ
- Инсайты и визуализации
- Инструменты сбора данных
- Отчеты »
- Мировая статистика здравоохранения 2022 г.

- избыточная смертность от COVID
- DDI В ФОКУСЕ: 2022 г.
- Мировая статистика здравоохранения 2022 г.
- О ком »
- Люди
- Команды
- Структура
- Партнерство и сотрудничество
- Сотрудничающие центры
- Сети, комитеты и консультативные группы
- Трансформация
- Наша работа »
- Общая программа работы
- Академия ВОЗ
- мероприятия
- Инициативы
- Финансирование »
- Инвестиционный кейс
- Фонд ВОЗ
- Подотчетность »
- Аудит
- Бюджет
- Финансовые отчеты
- Портал программного бюджета
- Отчет о результатах
- Управление »
- Всемирная ассамблея здравоохранения
- Исполнительный совет
- Выборы Генерального директора
- Веб-сайт руководящих органов
- Дом/
- Новости/
- шт/
- Заявление ВОЗ: Употребление табака и COVID-19
Табак ежегодно убивает более 8 миллионов человек во всем мире. Более 7 миллионов из этих смертей связаны с непосредственным употреблением табака, а около 1,2 миллиона — с тем, что некурящие подвергаются пассивному курению.
Более 7 миллионов из этих смертей связаны с непосредственным употреблением табака, а около 1,2 миллиона — с тем, что некурящие подвергаются пассивному курению.
Табакокурение является известным фактором риска многих респираторных инфекций и увеличивает тяжесть респираторных заболеваний. Обзор исследований экспертов в области общественного здравоохранения, созванных ВОЗ 29В апреле 2020 года было установлено, что у курильщиков вероятность развития тяжелого заболевания COVID-19 выше, чем у некурящих.
COVID-19 — это инфекционное заболевание, которое в первую очередь поражает легкие. Курение ухудшает функцию легких, из-за чего организму становится сложнее бороться с коронавирусом и другими заболеваниями. Табак также является основным фактором риска неинфекционных заболеваний, таких как сердечно-сосудистые заболевания, рак, респираторные заболевания и диабет, которые подвергают людей с этими заболеваниями более высокому риску развития тяжелых заболеваний при воздействии COVID-19. . Имеющиеся исследования показывают, что курильщики подвергаются более высокому риску развития тяжелых заболеваний и смерти.
. Имеющиеся исследования показывают, что курильщики подвергаются более высокому риску развития тяжелых заболеваний и смерти.
ВОЗ постоянно оценивает новые исследования, в том числе исследования, в которых изучается связь между употреблением табака, употреблением никотина и COVID-19. ВОЗ призывает исследователей, ученых и средства массовой информации быть осторожными в распространении бездоказательных заявлений о том, что табак или никотин могут снизить риск заражения COVID-19. В настоящее время недостаточно информации для подтверждения какой-либо связи между табаком или никотином в профилактике или лечении COVID-19..
Заместительные никотиновые препараты, такие как жевательная резинка и пластыри, предназначены для того, чтобы помочь курильщикам бросить курить. ВОЗ рекомендует курильщикам принять незамедлительные меры, чтобы бросить курить, используя проверенные методы, такие как бесплатные телефонные линии для бросающих курить, программы обмена текстовыми сообщениями по мобильным телефонам и никотинозамещающая терапия.
В течение 20 минут после отказа от курения учащается сердцебиение и снижается артериальное давление. Через 12 часов уровень угарного газа в крови падает до нормы. В течение 2-12 недель улучшается кровообращение и повышается функция легких. После 1-9месяцев кашель и одышка уменьшаются.
ВОЗ подчеркивает важность одобренных с этической точки зрения высококачественных систематических исследований, которые будут способствовать укреплению индивидуального и общественного здоровья, подчеркивая, что продвижение непроверенных вмешательств может оказать негативное влияние на здоровье.
Подпишитесь на наши новости →
COVID-19
Симптомы, причины и домашние средства
У курящих людей часто возникает кашель. Этот кашель вызван тем, что организм выводит химические вещества, которые попадают в дыхательные пути и легкие при употреблении табака.
Если кашель постоянный, длящийся более 3 недель, он известен как кашель курильщика. Хотя кашель может начинаться как сухой кашель, в конечном итоге он может вызвать выделение мокроты. Другие симптомы включают боль в горле и груди.
Другие симптомы включают боль в горле и груди.
Несколько домашних средств могут помочь справиться с симптомами кашля курильщика.
Краткие факты о кашле курильщика:
- Не у всех курильщиков есть кашель курильщика.
- Курение вызывает кашель курильщика.
- Это может привести к целому ряду других заболеваний, таких как бронхит.
- Наиболее эффективным методом лечения кашля курильщика является отказ от курения.
Кашель курильщика является распространенной жалобой среди курильщиков.
Исследование молодых военнослужащих показало, что более 40 процентов участников, которые курили ежедневно, и 27 процентов, которые курили время от времени, испытывали хронический кашель и выделение мокроты.
Поскольку возраст участников исследования был от 18 до 21 года, а кашель курильщика более распространен среди заядлых курильщиков, вполне вероятно, что истинный процент курильщиков, пострадавших от кашля курильщика, выше.
Не у всех курильщиков развивается кашель курильщика, но он более вероятен среди тех, кто постоянно употребляет табак в течение длительного времени.
Поделиться на PinterestОдышка и боль в груди могут быть симптомами, сопровождающими кашель курильщика.
На ранних стадиях кашля курильщика кашель, как правило, сухой. На более поздних стадиях кашель выделяет мокроту, которая может быть:
- бесцветной
- кровянистой
- желто-зеленой
- белой
Другие симптомы, сопровождающие кашель, включают:
- хрипящий звук при дыхании
- боль в груди
- одышка
- боль в горле
- свистящее дыхание
Кашель курильщика обычно усиливается с утра и постепенно улучшается в течение дня. Симптомы кашля курильщика со временем ухудшаются, если только человек не бросит курить.
Кашель курильщика по сравнению с другими видами кашля
Кашель курильщика можно отличить от других видов кашля по таким симптомам, как выделение мокроты, хрипы в груди и хрипы.
Однако трудно отличить кашель, связанный с заболеваниями легких, такими как рак или ХОБЛ, от кашля курильщика. Этот факт подчеркивает важность регулярных медицинских осмотров, особенно для курильщиков.
Этот факт подчеркивает важность регулярных медицинских осмотров, особенно для курильщиков.
По данным Американского онкологического общества, из тысяч химических веществ, содержащихся в табаке, как минимум 70 вызывают рак.
При попадании в организм многие из этих химических веществ нарушают функцию ресничек, крошечных волосовидных структур, которые помогают фильтровать токсины из дыхательных путей. Исследования показывают, что формальдегид и другие химические вещества замедляют движение ресничек и даже сокращают их длину, позволяя большему количеству токсинов попадать в легкие.
Этот процесс, вызванный курением, приводит к воспалению. В результате организм пытается удалить вещества через кашель. Кашель курильщика может усиливаться после пробуждения, потому что табачный дым не влияет на реснички во время сна, и поэтому они лучше улавливают и выделяют химические вещества.
Есть некоторые вещи, которые человек может сделать, чтобы облегчить кашель курильщика, а также некоторые методы лечения, чтобы облегчить симптомы.
Отказ от курения
Несомненно, наиболее эффективным методом лечения кашля курильщика является отказ от курения. Однако первоначально кашель может сохраняться или усиливаться после отказа от курения – обычно до 3 месяцев, но в некоторых случаях и намного дольше – по мере того, как организм очищает дыхательные пути от накопившихся токсинов.
Другие методы лечения и средства
Поделиться на PinterestОтказ от курения — лучшее средство от кашля курильщика.
Следующие советы могут помочь уменьшить раздражение и другие симптомы, связанные с кашлем курильщика:
- пить воду
- полоскать горло
- мед с теплой водой или чаем попробуйте увлажнитель воздуха
- зарядка
- здоровое питание
- приподнимать голову ночью
Кашель способствует удалению токсинов из легких, поэтому подавление кашля обычно не помогает. Всегда консультируйтесь с врачом, прежде чем принимать средства от кашля при кашле курильщика.
Существует множество осложнений, связанных с курением и кашлем курильщика, многие из которых связаны с повреждением ресничек. Вероятность развития одного или нескольких осложнений зависит от того, как часто кто-то курит, тяжести кашля и общего состояния здоровья.
Осложнения включают:
- повышенный риск бактериальных и вирусных респираторных инфекций
- поражение горла
- изменения голоса, такие как охриплость
- продолжительный кашель и раздражение
накопление химических веществ в легких и дыхательных путях, которые могут играть роль в развитии:
Бронхит
Бронхит – это воспаление слизистой оболочки бронхов – трубок, соединяющих легкие с носом и ртом. Симптомы включают затрудненное дыхание из-за снижения способности переносить воздух и мокроту в дыхательных путях.
Если бронхит сохраняется в течение 3 месяцев и более или рецидивирует в течение как минимум 2 лет, он называется хроническим бронхитом. В 2015 году у 9,3 миллиона человек в США был диагностирован хронический бронхит. Курение является наиболее распространенной причиной этого состояния.
В 2015 году у 9,3 миллиона человек в США был диагностирован хронический бронхит. Курение является наиболее распространенной причиной этого состояния.
Хроническая обструктивная болезнь легких (ХОБЛ)
ХОБЛ — прогрессирующее заболевание, характеризующееся затрудненным дыханием. Термин ХОБЛ включает как эмфизему, так и хронический бронхит. Симптомы включают кашель, мокроту, хрипы и стеснение в груди.
По данным Национального института сердца, легких и крови, ХОБЛ, вызываемая главным образом курением, является третьей по значимости причиной смерти в США.
Эмфизема
воздушные мешки в легких. В результате организм с трудом получает необходимый ему кислород. Симптомы включают затрудненное дыхание и хронический кашель.
Недержание мочи
У женщин кашель курильщика может вызвать стрессовое недержание мочи. Некоторые исследования показывают, что женщины, которые много курят, гораздо чаще испытывают внезапные и сильные позывы к мочеиспусканию, чем некурящие женщины.
Рак легких
Рак легких является основной причиной смерти от рака в Америке, а курение сигарет является основной причиной рака легких. По данным Центров по контролю и профилактике заболеваний (CDC), до 90 процентов случаев рака легких в Соединенных Штатах связаны с курением, причем даже эпизодическое курение увеличивает риск развития рака.
Пневмония
Употребление табака повышает восприимчивость к бактериальным инфекциям легких, таким как пневмония. Симптомы пневмонии включают кашель, лихорадку и затрудненное дыхание.
Некоторым людям, особенно с сопутствующими проблемами со здоровьем, требуется госпитализация по поводу пневмонии. Эмфизема и некоторые другие состояния могут усугубляться этой инфекцией.
Социальное и эмоциональное воздействие
Помимо физического воздействия, хронический кашель курильщика может повлиять на эмоциональное и социальное функционирование.
Например, постоянный кашель может мешать сну и беспокоить окружающих. Это может мешать общению и может быть разрушительным для семьи, друзей и коллег.
Это может мешать общению и может быть разрушительным для семьи, друзей и коллег.
Кашель курильщика, скорее всего, будет сохраняться, пока человек курит. Хотя существуют некоторые домашние средства для облегчения симптомов кашля курильщика, они не улучшают состояние.
Даже после прекращения курения кашель может сохраняться в течение нескольких месяцев.
Когда обращаться к врачу
Важно обратиться к врачу, если:
- Кашель сохраняется более 2-3 недель. Хронический кашель является одним из наиболее распространенных симптомов рака легких.
- Симптомы мешают повседневной жизни. Симптомы могут включать
- Проблема со сном
- Постоянная боль в горле или в груди
- Экстремальная потеря веса
- головные боли
- Желто-зеленая мокрота
Ищите немедленное лечение:
9000 Также рекомендуется проконсультироваться с врачом, чтобы получить информацию о том, как бросить курить, и при рассмотрении вопроса об использовании средств от кашля при кашле курильщика.
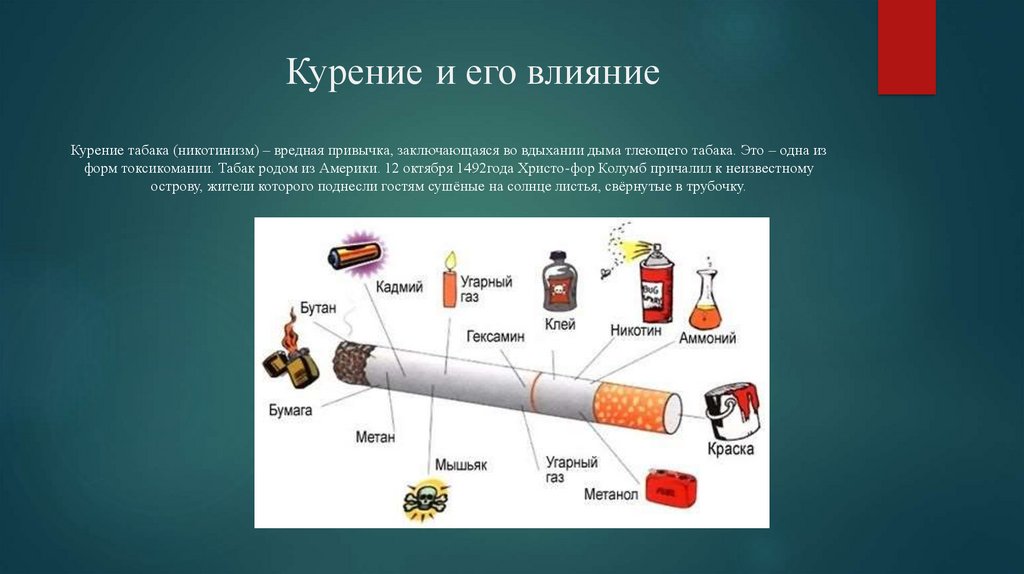


 В первые годы заболевания изменения на рентгенограмме лёгких могут отсутствовать. Позднее визуализируются рентгенологические признаки эмфиземы и пневмосклероза. КТ грудной полости выявляет бронхоэктазы, наличие интерстициальных изменений. В стадии ХОБЛ определяется саблевидная деформация трахеи.
В первые годы заболевания изменения на рентгенограмме лёгких могут отсутствовать. Позднее визуализируются рентгенологические признаки эмфиземы и пневмосклероза. КТ грудной полости выявляет бронхоэктазы, наличие интерстициальных изменений. В стадии ХОБЛ определяется саблевидная деформация трахеи.
 Препаратами первой линии являются антихолинергические средства в качестве монотерапии или в комбинации с бета-2-агонистами. Также можно использовать метилксантины.
Препаратами первой линии являются антихолинергические средства в качестве монотерапии или в комбинации с бета-2-агонистами. Также можно использовать метилксантины.


 Вызывает лейкозы и другие формы онкологии.
Вызывает лейкозы и другие формы онкологии.
