8. Органические вещества. Углеводы. Белки. Биология. Общая биология. 10 класс. Базовый уровень
8. Органические вещества. Углеводы. Белки
Вспомните!
Какие вещества называют биологическими полимерами?
Каково значение углеводов в природе?
Назовите известные вам белки. Какие функции они выполняют?
Углеводы (сахара). Это обширная группа природных органических соединений. В животных клетках углеводы составляют не более 5 % сухой массы, а в некоторых растительных (например, клуб ни картофеля) их содержание достигает 90 % сухого остатка. Углеводы подразделяют на три основных класса: моносахариды, дисахариды и полисахариды.
Моносахариды рибоза и дезоксирибоза входят в состав нуклеиновых кислот (рис. 15). Глюкоза присутствует в клетках всех организмов и является одним из основных источников энергии для животных. Широко распространена в природе фруктоза – фруктовый сахар, который значительно слаще других сахаров. Этот моносахарид придаёт сладкий вкус плодам растений и мёду.
Этот моносахарид придаёт сладкий вкус плодам растений и мёду.
Если в одной молекуле объединяются два моносахарида, такое соединение называют дисахаридом. Самый распространённый в природе дисахарид – сахароза, или тростниковый сахар, – состоит из глюкозы и фруктозы (рис. 16). Её получают из сахарного тростника или сахарной свёклы. Именно она и есть тот самый сахар, который мы покупаем в магазине.
Сложные углеводы – полисахариды, состоящие из простых сахаров, выполняют в организме несколько важных функций (рис. 17). Крахмал для растений и гликоген для животных и грибов являются резервом питательных веществ и энергии.
Рис. 15. Структурные формулы моносахаридов
Рис. 16. Структурная формула сахарозы (дисахарида)
Рис. 17. Строение полисахаридов
Крахмал запасается в растительных клетках в виде так называемых крахмальных зёрен. Больше всего его откладывается в клубнях картофеля и в семенах бобовых и злаков.
Целлюлоза и хитин выполняют в организмах структурную и защитную функции. Целлюлоза, или клетчатка, образует стенки растительных клеток. По общей массе она занимает первое место на Земле среди всех органических соединений. По своему строению очень близок к целлюлозе хитин, который составляет основу наружного скелета членистоногих и входит в состав клеточной стенки грибов.
Белки (полипептиды). Одними из наиболее важных органических соединений в живой природе являются белки. В каждой живой клетке присутствует одновременно более тысячи видов белковых молекул. И у каждого белка своя особая, только ему свойственная функция. О первостепенной роли этих сложных веществ догадывались ещё в начале XX в., именно поэтому им дали название 
Строение белков. Длинные белковые цепи построены всего из 20 различных типов аминокислот, имеющих общий план строения, но отличающихся друг от друга по строению радикала (R) (рис. 18). Соединяясь, молекулы аминокислот образуют так называемые пептидные связи (рис. 19).
Рис. 18. Общая структурная формула аминокислот, входящих в состав белков
Рис. 19. Образование пептидной связи между двумя аминокислотами
Две полипептидные цепи, из которых состоит гормон поджелудочной железы – инсулин, содержат 21 и 30 аминокислотных остатков. Это одни из самых коротких «слов» в белковом «языке». Миоглобин – белок, связывающий кислород в мышечной ткани, состоит из 153 аминокислот. Белок коллаген, составляющий основу коллагеновых волокон соединительной ткани и обеспечивающий её прочность, состоит из трёх полипептидных цепей, каждая из которых содержит около 1000 аминокислотных остатков.
Последовательное расположение аминокислотных остатков, соединённых пептидными связями, является первичной структурой белка и представляет собой линейную молекулу (рис. 20). Закручиваясь в виде спирали, белковая нить приобретает более высокий уровень организации – вторичную структуру. И наконец, спираль полипептида сворачивается, образуя клубок (глобулу). Именно такая третичная структура белка и является его биологически активной формой, обладающей индивидуальной специфичностью. Однако для ряда белков третичная структура не является окончательной.
20). Закручиваясь в виде спирали, белковая нить приобретает более высокий уровень организации – вторичную структуру. И наконец, спираль полипептида сворачивается, образуя клубок (глобулу). Именно такая третичная структура белка и является его биологически активной формой, обладающей индивидуальной специфичностью. Однако для ряда белков третичная структура не является окончательной.
Может существовать четвертичная структура – объединение нескольких белковых глобул в единый рабочий комплекс. Так, например, сложная молекула гемоглобина состоит из четырёх полипептидов, и только в таком виде она может выполнять свою функцию.
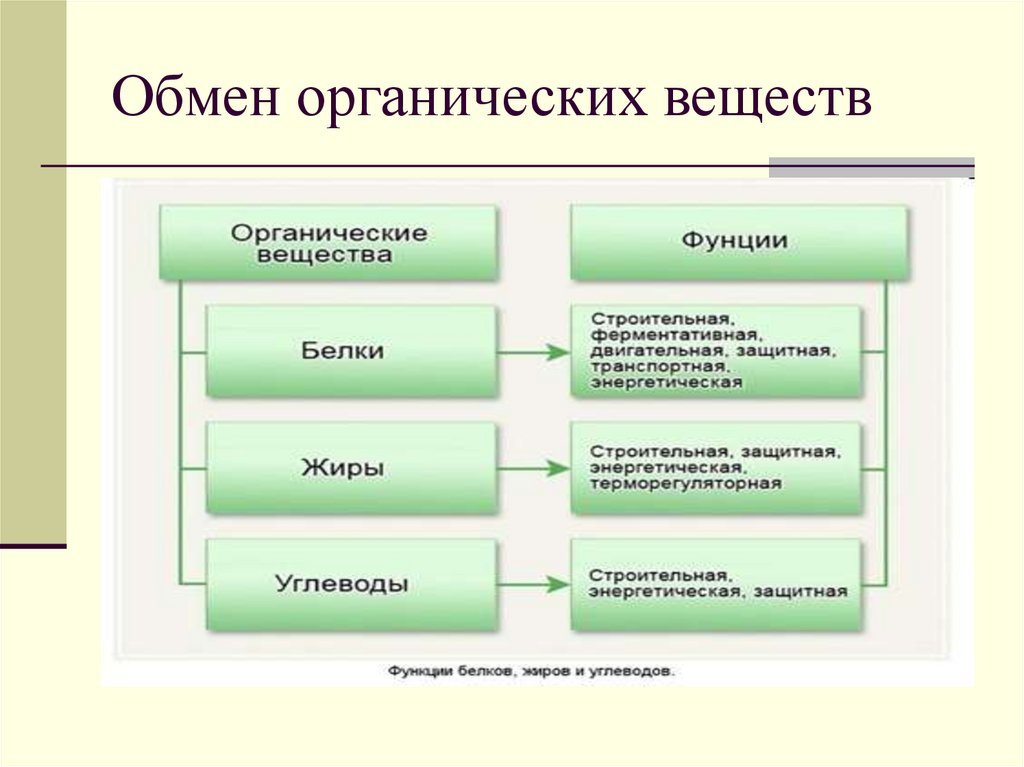
Функции белков. Огромное разнообразие белковых молекул подразумевает столь же широкое разнообразие их функций (рис. 21, 22). Около 10 тыс. белков-ферментов служат катализаторами химических реакций. Они обеспечивают слаженную работу биохимического ансамбля клеток живых организмов, ускоряя во много раз скорость химических реакций.
Рис. 20. Строение белковой молекулы: А – первичная; Б – вторичная; В – третичная; Г – четвертичная структуры
Вторая по величине группа белков выполняет структурную и двигательную функции. Белки участвуют в образовании всех мембран и органоидов клетки. Коллаген входит в состав межклеточного вещества соединительной и костной ткани, а основным компонентом волос, рогов и перьев, ногтей и копыт является белок кератин. Сократительную функцию мышц обеспечивают актин и миозин.
Транспортные белки связывают и переносят различные вещества и внутри клетки, и по всему организму.
Белки-гормоны обеспечивают регуляторную функцию.
Например, соматотропный гормон, вырабатываемый гипофизом, регулирует общий обмен веществ и влияет на рост. Недостаток или избыток этого гормона в детском возрасте приводит соответственно к развитию карликовости или гигантизма.
Рис. 21. Основные группы белков
Чрезвычайно важна защитная функция белков. При попадании в организм человека чужеродных белков, вирусов или бактерий на защиту встают иммуноглобулины – защитные белки. Фибриноген и протромбин обеспечивают свёртываемость крови, предохраняя организм от кровопотери. Есть у белков и защитная функция несколько иного рода. Многие членистоногие, рыбы, змеи и другие животные выделяют токсины – сильные яды белковой природы. Белками являются и самые сильные микробные токсины, например ботулиновый, дифтерийный, холерный.
При попадании в организм человека чужеродных белков, вирусов или бактерий на защиту встают иммуноглобулины – защитные белки. Фибриноген и протромбин обеспечивают свёртываемость крови, предохраняя организм от кровопотери. Есть у белков и защитная функция несколько иного рода. Многие членистоногие, рыбы, змеи и другие животные выделяют токсины – сильные яды белковой природы. Белками являются и самые сильные микробные токсины, например ботулиновый, дифтерийный, холерный.
При нехватке пищи в организме животных начинается активный распад белков до конечных продуктов, и тем самым реализуется энергетическая функция этих полимеров. При полном расщеплении 1 г белка выделяется 17,6 кДж энергии.
Рис. 22. Синтезированные белки или остаются в клетке для внутриклеточного применения, или выводятся наружу для использования на уровне организма
Рис. 23. Денатурация белка
Денатурация и ренатурация белков. Денатурация – это утрата белковой молекулой своей структурной организации: четвертичной, третичной, вторичной, а при более жёстких условиях – и первичной структуры (рис.
Дезинфицирующее свойство этилового спирта основано на его способности вызывать денатурацию бактериальных белков, что приводит к гибели микроорганизмов.
Денатурация может быть обратимой и необратимой, частичной и полной. Иногда, если воздействие денатурирующих факторов оказалось не слишком сильным и разрушение первичной структуры молекулы не произошло, при наступлении благоприятных условий денатурированный белок может вновь восстановить свою трёхмерную форму. Этот процесс называют ренатурацией, и он убедительно доказывает зависимость третичной структуры белка от последовательности аминокислотных остатков, т. е. от его первичной структуры.
Вопросы для повторения и задания
1. Какие химические соединения называют углеводами?
2. Что такое моно– и дисахариды? Приведите примеры.
Что такое моно– и дисахариды? Приведите примеры.
3. Какой простой углевод служит мономером крахмала, гликогена, целлюлозы?
4. Из каких органических соединений состоят белки?
5. Как образуются вторичная и третичная структуры белка?
6. Назовите известные вам функции белков. Чем вы можете объяснить существующее многообразие функций белков?
7. Что такое денатурация белка? Что может явиться причиной денатурации?
Подумайте! Выполните!
1. Используя знания, полученные при изучении биологии растений, объясните, почему в растительных организмах углеводов значительно больше, чем в животных.
2. К каким заболеваниям может привести нарушение превращения углеводов в организме человека?
3. Известно, что, если в рационе отсутствует белок, даже несмотря на достаточную калорийность пищи, у животных останавливается рост, изменяется состав крови и возникают другие патологические явления. Какова причина подобных нарушений?
Какова причина подобных нарушений?
4. Объясните трудности, возникающие при пересадке органов, опираясь на знания специфичности белковых молекул в каждом организме.
5. Оцените содержание белков, жиров и углеводов в продуктах питания (на основании данных, представленных на этикетках).
Работа с компьютером
Обратитесь к электронному приложению. Изучите материал и выполните задания.
Узнайте больше
К настоящему времени выделено и изучено более тысячи ферментов, каждый из которых способен влиять на скорость той или иной биохимической реакции.
Молекулы одних ферментов состоят только из белков, другие включают белок и небелковое соединение, или кофермент. В качестве коферментов выступают различные вещества, как правило, витамины и неорганические – ионы различных металлов.
Как правило, ферменты строго специфичны, т. е. ускоряют только определённые реакции, хотя встречаются ферменты, которые катализируют несколько реакций. Такая избирательность действия ферментов связана с их строением. Активность фермента определяется не всей его молекулой, а определённым участком, который называют активным центром фермента. Форма и химическое строение активного центра таковы, что с ним могут связываться только определённые молекулы, которые подходят ферменту, как ключ замку. Вещество, с которым связывается фермент, называют субстратом. Иногда одна молекула фермента имеет несколько активных центров, что, естественно, ещё более ускоряет скорость катализируемого биохимического процесса.
Такая избирательность действия ферментов связана с их строением. Активность фермента определяется не всей его молекулой, а определённым участком, который называют активным центром фермента. Форма и химическое строение активного центра таковы, что с ним могут связываться только определённые молекулы, которые подходят ферменту, как ключ замку. Вещество, с которым связывается фермент, называют субстратом. Иногда одна молекула фермента имеет несколько активных центров, что, естественно, ещё более ускоряет скорость катализируемого биохимического процесса.
На заключительном этапе химической реакции комплекс «фермент – субстрат» распадается на конечные продукты и свободный фермент. Освободившийся при этом активный центр фермента может снова принимать новые молекулы вещества-субстрата (рис. 24).
Рис. 24. Схема образования комплекса «фермент – субстрат»
Повторите и вспомните!
Человек
Обмен углеводов. В организм углеводы попадают в виде различных соединений: крахмал, гликоген, сахароза, фруктоза, глюкоза. Сложные углеводы начинают перевариваться уже в ротовой полости. В двенадцатиперстной кишке они расщепляются окончательно – до глюкозы и других простых углеводов. В тонком кишечнике простые углеводы всасываются в кровь и направляются в печень. Здесь избыток углеводов задерживается и превращается в гликоген, а оставшаяся часть глюкозы распределяется между всеми клетками тела. В организме глюкоза, прежде всего, является источником энергии. Расщепление 1 г глюкозы сопровождается выделением 17,6 кДж (4,2 ккал) энергии. Продукты распада углеводов (углекислый газ и вода) выводятся через лёгкие или с мочой. Главная роль в регуляции концентрации глюкозы в крови принадлежит гормонам поджелудочной железы и надпочечников.
Сложные углеводы начинают перевариваться уже в ротовой полости. В двенадцатиперстной кишке они расщепляются окончательно – до глюкозы и других простых углеводов. В тонком кишечнике простые углеводы всасываются в кровь и направляются в печень. Здесь избыток углеводов задерживается и превращается в гликоген, а оставшаяся часть глюкозы распределяется между всеми клетками тела. В организме глюкоза, прежде всего, является источником энергии. Расщепление 1 г глюкозы сопровождается выделением 17,6 кДж (4,2 ккал) энергии. Продукты распада углеводов (углекислый газ и вода) выводятся через лёгкие или с мочой. Главная роль в регуляции концентрации глюкозы в крови принадлежит гормонам поджелудочной железы и надпочечников.
Больше всего углеводов содержится в продуктах растительного происхождения. Обычно в пище человека встречаются такие углеводы, как крахмал, свекловичный сахар (сахароза) и фруктовый сахар. Особенно богаты крахмалом различные крупы, хлеб, картофель. Очень полезен фруктовый сахар, он легко усваивается организмом. Этого сахара много в мёде, фруктах и ягодах. Взрослому человеку необходимо получать с пищей не менее 150 г углеводов в сутки. При выполнении физически тяжёлых работ это количество необходимо увеличить в 1,5–2 раза. С точки зрения процессов обмена веществ введение в организм полисахаридов более рационально, чем моно– и дисахаридов. Действительно, относительно медленный распад крахмала в пищеварительной системе приводит к постепенному поступлению глюкозы в кровь. В случае же переедания сладкого концентрация глюкозы в крови растёт резко, скачкообразно, что негативно влияет на работу многих органов (в том числе поджелудочной железы).
Этого сахара много в мёде, фруктах и ягодах. Взрослому человеку необходимо получать с пищей не менее 150 г углеводов в сутки. При выполнении физически тяжёлых работ это количество необходимо увеличить в 1,5–2 раза. С точки зрения процессов обмена веществ введение в организм полисахаридов более рационально, чем моно– и дисахаридов. Действительно, относительно медленный распад крахмала в пищеварительной системе приводит к постепенному поступлению глюкозы в кровь. В случае же переедания сладкого концентрация глюкозы в крови растёт резко, скачкообразно, что негативно влияет на работу многих органов (в том числе поджелудочной железы).
Обмен белков. Попадая в организм, пищевые белки под действием ферментов расщепляются в желудочно-кишечном тракте до отдельных аминокислот и в таком виде всасываются в кровь. Главная функция этих аминокислот – пластическая, т. е. из них строятся все белки нашего организма. Реже белки используются как источники энергии: при распаде 1 г выделяется 17,6 кДж (4,2 ккал). Аминокислоты, входящие в состав белков нашего организма, подразделяют на заменимые и незаменимые. Заменимые аминокислоты могут синтезироваться в нашем организме из других аминокислот, поступающих с пищей. К ним относятся глицин, серин и другие. Однако многие необходимые нам аминокислоты не синтезируются в нашем организме и поэтому должны постоянно поступать в организм в составе белков пищи. Такие аминокислоты называют незаменимыми. Среди них, например, валин, метионин, лейцин, лизин и некоторые другие. В случае дефицита незаменимых аминокислот возникает состояние «белкового голодания», приводящее к замедлению роста организма, ухудшению процессов самовозобновления клеток и тканей. Пищевые белки, содержащие все необходимые человеку аминокислоты, называют полноценными. К ним относят животные и некоторые растительные белки (бобовых растений). Пищевые белки, в составе которых отсутствуют какие-либо незаменимые аминокислоты, называют неполноценными (например, белки кукурузы, ячменя, пшеницы).
Аминокислоты, входящие в состав белков нашего организма, подразделяют на заменимые и незаменимые. Заменимые аминокислоты могут синтезироваться в нашем организме из других аминокислот, поступающих с пищей. К ним относятся глицин, серин и другие. Однако многие необходимые нам аминокислоты не синтезируются в нашем организме и поэтому должны постоянно поступать в организм в составе белков пищи. Такие аминокислоты называют незаменимыми. Среди них, например, валин, метионин, лейцин, лизин и некоторые другие. В случае дефицита незаменимых аминокислот возникает состояние «белкового голодания», приводящее к замедлению роста организма, ухудшению процессов самовозобновления клеток и тканей. Пищевые белки, содержащие все необходимые человеку аминокислоты, называют полноценными. К ним относят животные и некоторые растительные белки (бобовых растений). Пищевые белки, в составе которых отсутствуют какие-либо незаменимые аминокислоты, называют неполноценными (например, белки кукурузы, ячменя, пшеницы).
Большинство продуктов питания содержит белок. Богаты белком мясо, рыба, сыр, творог, яйца, горох, орехи. Особенно важны животные белки молодому растущему организму. Недостаток полноценных белков в пище приводит к замедлению роста. В сутки человеку необходимо съедать с пищей 100–120 г белка.
Распадаясь, аминокислоты образуют воду, углекислый газ и ядовитый аммиак, который в печени превращается в мочевину. Конечные продукты обмена белков выводятся из организма с мочой, по?том и в составе выдыхаемого воздуха.
Данный текст является ознакомительным фрагментом.
ГМ растения с заданным химическим составом и структурой молекул (аминокислоты, белки, углеводы)
ГМ растения с заданным химическим составом и структурой молекул (аминокислоты, белки, углеводы)
Основной закон рационального питания диктует необходимость соответствия уровней поступления и расхода энергии. Уменьшение энерготрат современного человека ведет к
Уменьшение энерготрат современного человека ведет к
2. Белки хроматина
2. Белки хроматина Мы уже знаем, что хроматин состоит из ДНК и гистонов в равном весовом количестве и негистоновых белков (НГБ), которых в неактивных районах хромосомы всего 0,2 веса ДНК, а в активных — более чем 1,2 (в среднем НГБ мепьше, чем ДНК). Мы знаем также, что гистоны
О природе родства, связывающего органические существа.
О природе родства, связывающего органические существа. Так как модифицированные потомки доминирующих видов, принадлежащих к обширным родам, склонны унаследовать преимущества, делавшие группы, к которым они принадлежат, обширными и их прародителей доминирующими, то тем
Белки
Белки
Пищевая ценность белка обеспечивается наличием незаменимых аминокислот, углеводородные скелеты которых не могут синтезироваться в организме человека, и они соответственно должны поступать с пищей. Они также являются основными источниками азота. Суточная
Они также являются основными источниками азота. Суточная
Углеводы
Углеводы Основными углеводами пищи являются моносахариды, олигосахариды и полисахариды, которые должны поступать в количестве 400–500 г в сутки. Углеводы пищи являются основным энергетическим материалом клетки, обеспечивают 60–70% суточного энергопотребления. Для обмена
Глава 16. Углеводы тканей и пищи – обмен и функции
Глава 16. Углеводы тканей и пищи – обмен и функции Углеводы входят в состав живых организмов и вместе с белками, липидами и нуклеиновыми кислотами определяют специфичность их строения и функционирования. Углеводы участвуют во многих метаболических процессах, но прежде
Что такое углеводы, зачем они нужны организму и в каких продуктах содержатся?
Что такое углеводы, зачем они нужны организму и в каких продуктах содержатся?
Углеводы (сахара) – обширная группа природных соединений, химическая структура которых часто отвечает общей формуле Cm(h3O)n (то есть углерод плюс вода, отсюда название). Углеводы являются
Углеводы являются
2.1. Органические соединения в составе живых организмов
2.1. Органические соединения в составе живых организмов Органические соединения характерны только для живых организмов. Можно сказать, что жизнь на Земле построена на основе углерода, который обладает рядом уникальных свойств. Основное значение для выполнения роли
Углеводы
Углеводы Углеводы – это наиболее распространенная в природе группа органических веществ. Основная их функция – энергетическая. Все углеводы содержат гидроксильные группы (—ОН) вместе с альдегидной или кетогруппой. Выделяют три группы углеводов (табл. 2.1).Наибольшее
Белки
Белки
Белки имеют первостепенное значение в жизни организмов. Огромное разнообразие живых существ в значительной степени определяется различиями в составе имеющихся в их организме белков. Например, в организме человека их известно более 5 млн.Белки – это полимеры,
Например, в организме человека их известно более 5 млн.Белки – это полимеры,
3.1. Органические поражения ЦНС
3.1. Органические поражения ЦНС В рамках онтогенетического подхода к причинам возникновения поведенческих расстройств следует отметить, что органические поражения ЦНС могут быть вызваны неправильно протекавшей беременностью, сложными родами, осложненным послеродовым
7. Органические вещества. Общая характеристика. Липиды
7. Органические вещества. Общая характеристика. Липиды Вспомните!В чём особенность строения атома углерода?Какую связь называют ковалентной?Какие вещества называют органическими?Какие продукты питания содержат большое количество жира?Общая характеристика
9. Органические вещества. Нуклеиновые кислоты
9. Органические вещества. Нуклеиновые кислоты
Вспомните!Почему нуклеиновые кислоты относят к гетерополимерам?Что является мономером нуклеиновых кислот?Какие функции нуклеиновых кислот вам известны?Какие свойства живого определяются непосредственно строением и
Органические вещества. Нуклеиновые кислоты
Вспомните!Почему нуклеиновые кислоты относят к гетерополимерам?Что является мономером нуклеиновых кислот?Какие функции нуклеиновых кислот вам известны?Какие свойства живого определяются непосредственно строением и
Ну а белки?
Ну а белки? В шестидесятых годах я неоднократно пытался завести в доме и белок, но каждая такая попытка кончалась самым печальным образом. Через некоторое время белки слабели, задние конечности у них отнимались и несчастные животные в судорогах погибали. Поначалу я
Тема 2.5 Органические вещества. Углеводы. Белки.
1. Дайте определения понятий.
Углеводы – органические вещества, содержащие карбонильную группу и несколько гидроксильных групп.
Моносахарид – простой углевод, при гидролизе не расщепляющийся на более простые соединения.
Дисахарид – углевод, представляющий собой соединений из двух моносахаридов.
2. Дополните схему «Разнообразие углеводов в клетке».
3. Рассмотрите рисунок 11 учебника и приведите примеры моносахаридов, в состав которых входит:
пять атомов углерода: рибоза, дезоксирибоза;
шесть атомов углерода: глюкоза, фруктоза.
4. Заполните таблицу.
Биологические функции моно- и дисахаридов
5. Назовите растворимые в воде углеводы. Какие особенности строения их молекул обеспечивают свойство растворимости?
Моносахариды (глюкоза, фруктоза) и дисахариды (сахароза). Их молекулы небольшого размера и полярные, поэтому растворимы в воде. Полисахариды образуют длинные цепи, которые в воде не растворяются
6. Заполните таблицу.
БИОЛОГИЧЕСКИЕ ФУНКЦИИ ПОЛИСАХАРИДОВ
7. Полисахарид хитин входит в структуру клеточных стенок грибов и составляет основу наружного скелета членистоногих. С каким из известных вам полисахаридов он проявляет функциональное сходство? Ответ обоснуйте.
Полисахарид хитин входит в структуру клеточных стенок грибов и составляет основу наружного скелета членистоногих. С каким из известных вам полисахаридов он проявляет функциональное сходство? Ответ обоснуйте.
Хитин является веществом, очень близким по строению, физико-химическим свойствам и биологической роли к целлюлозе. Он выполняет защитную и опорную функции, содержится в клеточных стенках грибов, некоторых водорослей, бактерий.
8. Дайте определения понятий.
Полипептид — химическое вещество, состоящее из длинной цепи аминокислот, связанных пептидными связями.
Денатурация — потеря белками или нуклеиновыми кислотами их естественных свойств вследствие нарушения пространственной структуры их молекул.
Ренатурация — восстановление (после денатурации) биологически активной пространственной структуры биополимера (белка или нуклеиновой кислоты).
9. Объясните утверждение: «Белки — носители и организаторы жизни».
По Энгельсу «Всюду, где есть встречаем жизнь, она связана с каким-либо белковым телом, и повсюду, где мы встречаем какое-либо белковое тело, которое не находится в процессе разложения, мы без исключения встречаем и явления жизни…». «Жизнь есть способ существования белковых тел…».
10. Напишите общую структурную формулу аминокислоты. Объясните, почему мономер белка носит такое название.
RCH(Nh3)COOH. Аминокислоты объединяют в себе свойства кислот и аминов, т. е. содержат наряду с карбоксильной группой -COOH аминогруппу -Nh3.
11. Чем отличаются друг от друга различные аминокислоты?
Аминокислоты отличаются друг т друга по строению радикала.
12. Заполните кластер «Многообразие белков и их функции».
Белки: гормоны, транспортные белки, ферменты, токсины, антибиотики, запасные белки, защитные белки, двигательные белки, структурные белки.
13. Закончите заполнение таблицы.
14. Пользуясь учебником, объясните суть высказывания: «Биохимические реакции, протекающие в присутствии ферментов, — основа жизнедеятельности клеток».
Белки-ферменты катализируют множество реакций, обеспечивают слаженность ансамбля клеток живых организмов, ускоряя во много раз скорость химических реакций.
15. Приведите примеры белков, участвующих в перечисленных процессах.
Бег, ходьба, прыжки – актин и миозин.
Рост – соматотропин.
Транспорт кислорода и углекислого газа в крови – гемоглобин.
Рост ногтей и волос – кератин.
Свертывание крови – протромбин, фибриноген.
Связывание кислорода в мышцах – миоглобин.
16. Установите соответствие между конкретными белками и их функциями.
1. Протромбин
2. Коллаген
3. Актин
4. Соматотропин
5. Гемоглобин
6. Инсулин
Роль в организме
A. Сократительный белок мышц
Б.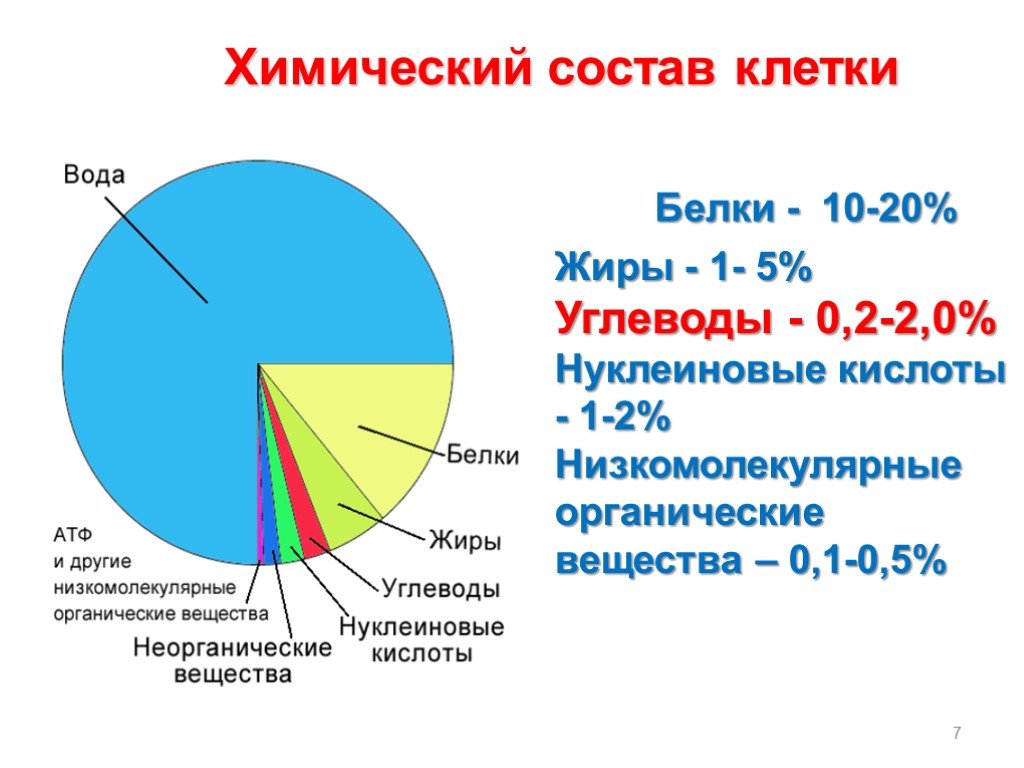 Гормон гипофиза
Гормон гипофиза
B. Обеспечивает свертываемость крови
Г. Входит в состав волокон соединительной ткани
Д. Гормон поджелудочной железы
Е. Переносит кислород
17. На чем основано дезинфицирующее свойство этилового спирта?
Он разрушает белки (в т. ч. токсины) бактерий, приводит к их денатурации.
18. Почему вареное яйцо, погруженное в холодную воду, не возвращается к исходному состоянию?
Происходит необратимая денатурация белка куриного яйца под воздействием высокой температуры.
19. При окислении 1 г белков выделяется столько же энергии, сколько при окислении 1 г углеводов. Почему организм использует белки как источник энергии только в крайних случаях?
Функции белков – это, во-первых, строительная, ферментативная, транспортная функции, и только в крайних случаях организм использует или тратит белки на получение энергии, только тогда, когда в организм не поступают углеводы и жиры, когда организм голодает.
20. Выберите правильный ответ.
Тест 1.
Белки, увеличивающие скорость химических реакций в клетке:
2) ферменты;
Тест 2.
Мономер сложных углеводов — это:
4) глюкоза.
Тест 3.
Углеводы в клетке не выполняют функцию:
3) хранения наследственной информации.
Тест 4.
Полимер, мономеры которого располагаются в одну линию:
2) неразветвленный полимер;
Тест 5.
В состав аминокислот не входит:
3) фосфор;
Тест 6.
У животных гликоген, а у растений:
3) крахмал;
Тест 7.
У гемоглобина есть, а у лизоцима нет:
4) четвертичной структуры.
21. Объясните происхождение и общее значение слова (термина), опираясь на значение корней, его составляющих.
22. Выберите термин и объясните, насколько его современное значение соответствует первоначальному значению его корней.
Выбранный термин: дезоксирибоза.
Соответствие: термин соответствует значению. Это дезоксисахар — производное рибозы, где гидроксильная группа у второго атома углерода замещена водородом с потерей атома кислорода (дезокси — отсутствие атома кислорода).
23. Сформулируйте и запишите основные идеи § 2.5.
Углеводы и белки относятся к органическим веществам клетки. К углеводам относятся: моносахариды (рибоза, дезоксирибоза, глюкоза), дисахариды (сахароза), полисахариды (крахмал, гликоген, целлюлоза, хитин). В организме они выполняют функции: энергетическую, запасающую, структурная.
Белки, мономерами которых являются аминокислоты, имеют первичную, вторичную, третичную и часто четвертичную структуры. Выполняют в организме важные функции: являются гормонами, ферментами, токсинами, антибиотиками, запасными, защитными, транспортными, двигательными и структурными белками.
Органические соединения
Химические соединения живых существ известны как органические соединения из-за их связи с организмами и потому, что они являются углеродсодержащими соединениями. Органические соединения, которые представляют собой соединения, связанные с жизненными процессами, являются предметом органической химии. Среди многочисленных типов органических соединений во всех живых существах встречаются четыре основные категории: углеводы, липиды, белки и нуклеиновые кислоты.Углеводы
Почти все организмы используют углеводов в качестве источников энергии. Кроме того, некоторые углеводы служат структурными материалами. Углеводы — это молекулы, состоящие из углерода, водорода и кислорода; отношение атомов водорода к атомам кислорода и углерода составляет 2:1.
Простые углеводы, обычно называемые сахарами, могут быть моносахаридами , если они состоят из одиночных молекул, или дисахаридами , если они состоят из двух молекул. Самый важный моносахарид – глюкоза, углевод с молекулярной формулой C 6 H 12 O 6 . Глюкоза является основной формой топлива в живых существах. В многоклеточных организмах он растворим и транспортируется жидкостями организма во все клетки, где метаболизируется с высвобождением энергии. Глюкоза является исходным материалом для клеточного дыхания и основным продуктом фотосинтеза (см. главы 5 и 6).
Самый важный моносахарид – глюкоза, углевод с молекулярной формулой C 6 H 12 O 6 . Глюкоза является основной формой топлива в живых существах. В многоклеточных организмах он растворим и транспортируется жидкостями организма во все клетки, где метаболизируется с высвобождением энергии. Глюкоза является исходным материалом для клеточного дыхания и основным продуктом фотосинтеза (см. главы 5 и 6).
В живых организмах также содержатся три важных дисахарида: мальтоза, сахароза и лактоза. Мальтоза представляет собой комбинацию двух единиц глюкозы, ковалентно связанных. Столовый сахар сахароза образуется путем связывания глюкозы с другим моносахаридом, называемым 9.0002 фруктоза. (На рис. 2-2 показано, что при синтезе сахарозы образуется молекула воды. Поэтому этот процесс называется реакцией дегидратации. добавляется вода.) Лактоза состоит из единиц глюкозы и галактозы.
Рисунок 2-2 Молекулы глюкозы и фруктозы объединяются, образуя дисахарид сахарозу.
Сложные углеводы известны как полисахариды. Полисахариды образуются путем связывания бесчисленных моносахаридов. Одним из наиболее важных полисахаридов является крахмал, который состоит из сотен или тысяч звеньев глюкозы, связанных друг с другом. Крахмал служит формой хранения углеводов. Большая часть населения мира удовлетворяет свои потребности в энергии за счет крахмала в виде риса, пшеницы, кукурузы и картофеля.
Двумя другими важными полисахаридами являются гликоген и целлюлоза. Гликоген также состоит из тысяч звеньев глюкозы, но эти звенья связаны иначе, чем в крахмале. Гликоген – это форма, в которой глюкоза хранится в печени человека. Целлюлоза используется главным образом как структурный углевод. Он также состоит из единиц глюкозы, но эти единицы не могут высвобождаться друг из друга, за исключением нескольких видов организмов. Древесина состоит в основном из целлюлозы, как и клеточные стенки растений. Хлопчатобумажная ткань и бумага являются товарными целлюлозными продуктами.
Хлопчатобумажная ткань и бумага являются товарными целлюлозными продуктами.
Липиды
Липиды представляют собой органические молекулы, состоящие из атомов углерода, водорода и кислорода. Отношение атомов водорода к атомам кислорода в липидах значительно выше, чем в углеводах. К липидам относятся стероиды (материал, из которого состоят многие гормоны), воски и жиров.
Молекулы жира состоят из молекулы глицерина и одной, двух или трех молекул жирных кислот (см. рис. 2-3). Молекула глицерина содержит три гидроксильных (–ОН) группы. А жирная кислота представляет собой длинную цепь атомов углерода (от 4 до 24) с карбоксильной (–COOH) группой на одном конце. Жирные кислоты в жире могут быть как одинаковыми, так и разными. Они связаны с молекулой глицерина в процессе, который включает удаление воды.
Некоторые жирные кислоты имеют в своих молекулах одну или несколько двойных связей. Жиры, в состав которых входят эти молекулы, являются ненасыщенными жирами. Другие жирные кислоты не имеют двойных связей. Жиры, в состав которых входят эти жирные кислоты, составляют насыщенные жиры. В большинстве ситуаций, связанных со здоровьем человека, потребление ненасыщенных жиров предпочтительнее потребления насыщенных жиров.
Другие жирные кислоты не имеют двойных связей. Жиры, в состав которых входят эти жирные кислоты, составляют насыщенные жиры. В большинстве ситуаций, связанных со здоровьем человека, потребление ненасыщенных жиров предпочтительнее потребления насыщенных жиров.
Жиры, хранящиеся в клетках, обычно образуют прозрачные капли масла, называемые глобулами , поскольку жиры не растворяются в воде. Растения часто хранят жиры в своих семенах, а животные запасают жиры в виде крупных прозрачных глобул в клетках жировой ткани. Жиры в жировой ткани содержат много концентрированной энергии. Следовательно, они служат резервным источником энергии для организма. Фермент липаза расщепляет жиры на жирные кислоты и глицерин в пищеварительной системе человека.
Рисунок 2-3 Молекула жира состоит из соединения молекулы глицерина с тремя молекулами жирных кислот. (Для сравнения показаны две насыщенные жирные кислоты и одна ненасыщенная жирная кислота. ) Сконструированная молекула находится внизу.
) Сконструированная молекула находится внизу.
Белки
Белки, одни из самых сложных органических соединений, состоят из аминокислот (см. рис. 2-4), которые содержат атомы углерода, водорода, кислорода и азота. Некоторые аминокислоты также содержат атомы серы, фосфора или других микроэлементов, таких как железо или медь.
Рисунок 2-4 Структура и химический состав аминокислот. Когда две аминокислоты соединяются в дипептид, -OH одной аминокислоты удаляется, а -H второй удаляется. Итак, вода удалена. Дипептидная связь (справа) образуется для соединения аминокислот.
Многие белки огромны и чрезвычайно сложны. Однако все белки состоят из длинных цепочек относительно простых аминокислот. Существует 20 видов аминокислот. Каждая аминокислота (см. иллюстрацию слева на рис. 2-4) имеет аминогруппу (–NH 2 ), карбоксильную группу (–COOH) и группу атомов, называемую группой –R (где R означает радикал ). Аминокислоты различаются в зависимости от природы группы –R, как показано на средней иллюстрации рисунка 2-4. Примерами аминокислот являются аланин, валин, глутаминовая кислота, триптофан, тирозин и гистидин.
Аминокислоты различаются в зависимости от природы группы –R, как показано на средней иллюстрации рисунка 2-4. Примерами аминокислот являются аланин, валин, глутаминовая кислота, триптофан, тирозин и гистидин.
Удаление молекул воды связывает аминокислоты с образованием белка. Процесс называется дегидратационным синтезом, и побочным продуктом синтеза является вода. Связей между аминокислотами 9.Пептидные связи 0002, и малые белки часто называют пептидами .
Все живые существа зависят от белков в своем существовании. Белки являются основными молекулами, из которых построены живые существа. Одни белки растворены или взвешены в водном веществе клеток, другие включены в различные структуры клеток. Белки также используются в качестве поддерживающих и укрепляющих материалов в тканях вне клеток. Кости, хрящи, сухожилия и связки состоят из белков.
Одной из основных функций белков является фермент. Ферменты катализируют химические реакции, происходящие внутри клеток.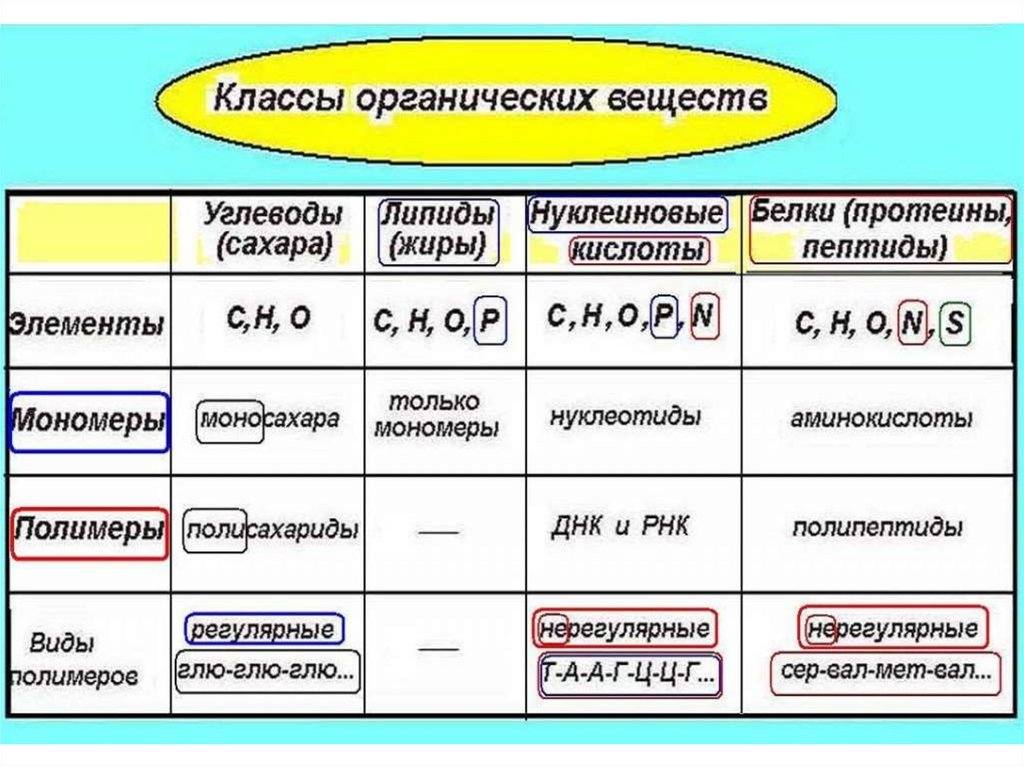 Они не расходуются в реакции; скорее, они остаются доступными для катализа последующих реакций.
Они не расходуются в реакции; скорее, они остаются доступными для катализа последующих реакций.
Каждый вид производит белки, уникальные для этого вида. Информация для синтеза уникальных белков находится в ядре клетки. Так называемый генетический код определяет последовательность аминокислот в белках. Следовательно, генетический код регулирует химию, происходящую внутри клетки. Белки также могут служить резервным источником энергии для клетки. Когда аминогруппа удаляется из аминокислоты, полученное соединение становится богатым энергией.
Нуклеиновые кислоты
Как и белки, нуклеиновые кислоты представляют собой очень большие молекулы. Нуклеиновые кислоты состоят из более мелких единиц, называемых нуклеотидов. Каждый нуклеотид содержит молекулу углевода (сахара), фосфатную группу и азотсодержащую молекулу, которая по своим свойствам является азотистым основанием .
Живые организмы содержат две важные нуклеиновые кислоты.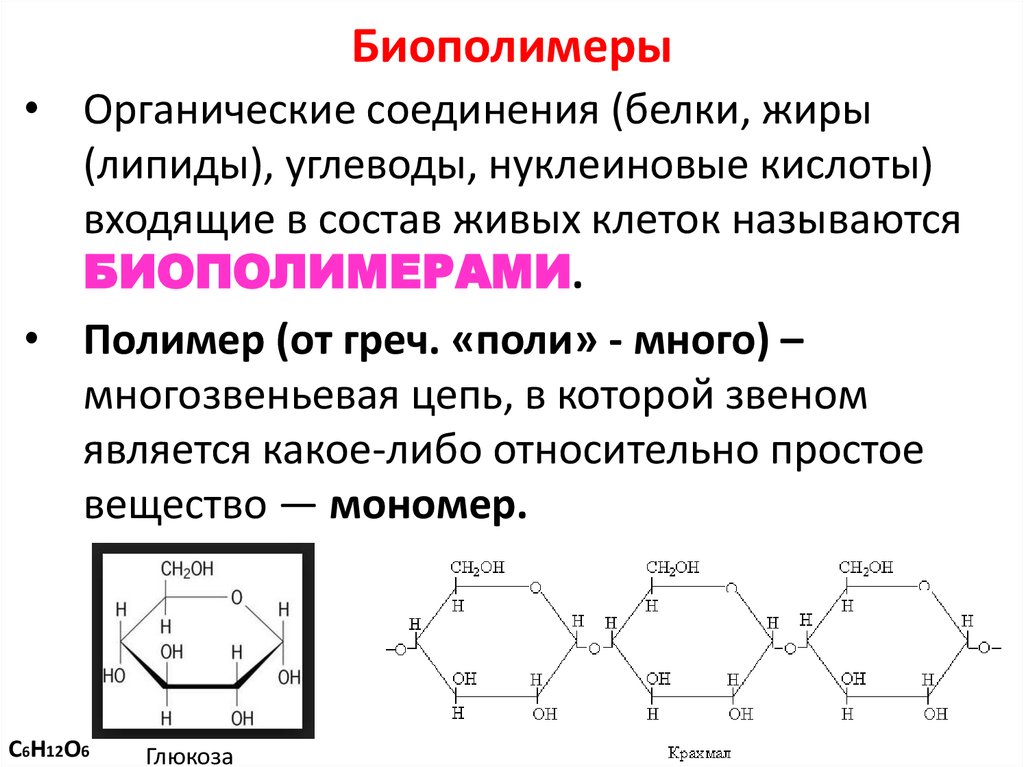 Один тип — дезоксирибонуклеиновая кислота, или ДНК. Другой — рибонуклеиновая кислота, или РНК. ДНК находится в основном в ядре клетки, тогда как РНК находится как в ядре, так и в цитоплазме, полужидком веществе, составляющем объем клетки (см. главу 3).
Один тип — дезоксирибонуклеиновая кислота, или ДНК. Другой — рибонуклеиновая кислота, или РНК. ДНК находится в основном в ядре клетки, тогда как РНК находится как в ядре, так и в цитоплазме, полужидком веществе, составляющем объем клетки (см. главу 3).
ДНК и РНК отличаются друг от друга своими компонентами. ДНК содержит углевод дезоксирибозу, а РНК — рибозу. Кроме того, ДНК содержит основание тимин, а РНК — урацил. Структура ДНК и ее значение для клеточной жизни исследуются в главе 10.
Лабораторные заметки для BIO 1003© Мэри Джин Холланд, 30 августа 1999 г.ОРГАНИЧЕСКИЕ МОЛЕКУЛЫСПРАВОЧНАЯ ЛИТЕРАТУРА Органические соединения содержат атомы углерода, связанные друг с другом в цепи или кольца. I. Липиды Липиды представляют собой органические молекулы, нерастворимые в воде и других полярных растворителях . Жиры и масла имеют сходную структуру, и оба служат молекулами для накопления энергии. При комнатной температуре масла жидкие, а жиры твердые. Оба являются триглицеридами , образованными путем объединения молекулы глицерина с тремя молекулами жирной кислоты. Свойства триглицеридов зависят от структуры содержащихся в них жирных кислот. Жирные кислоты представляют собой длинные цепи, содержащие углерод и водород с 90–155 карбоксильной группой 90–156 (COOH) на одном конце, что делает молекулу кислотой. Карбоксильная группа участвует в связывании каждой жирной кислоты с молекулой глицерина. Существует три простых теста для определения липидов. (1) Поскольку липиды (неполярные молекулы) и вода (полярные молекулы) не смешиваются, их комбинация разделится на два слоя. (2) краситель Суданский красный растворяется в липидах; при добавлении к смеси липидов и воды он окрашивает только липидный слой. (3) липиды оставляют жирные пятна на бумаге; воды и растворов, растворяющихся в воде, нет. II. Углеводы Углеводы являются основными молекулами-аккумуляторами энергии в большинстве организмов. Они также являются важными структурными компонентами для многих организмов. Строительные блоки углеводов представляют собой небольшие молекулы, называемые сахарами , состоящие из углерода, водорода и кислорода. Углеводы классифицируют по количеству молекул сахара, которые они содержат. Моносахариды, , такие как глюкоза, фруктоза, рибоза и галактоза, содержат только одну молекулу сахара. Моносахариды имеют молекулярную формулу (CH 2 O) n , где n может быть любым целым числом от 3 до 8. Моносахариды содержат гидроксильные группы и либо кетоновую, либо альдегидную группу. Эти полярные функциональные группы делают сахара очень хорошо растворимыми в воде. Глюкоза, сахар, содержащийся в крови большинства позвоночных, включая человека, имеет молекулярную формулу C9.0019 6 Н 12 О 6 . Фруктоза, сахар, содержащийся во многих фруктах, имеет ту же молекулярную формулу, что и глюкоза, но атомы углерода, водорода и кислорода расположены в этих двух моносахаридах немного по-разному. Глюкоза имеет альдегидную группу; фруктоза имеет кетоновую группу. Эта разница в структуре придает двум моносахаридам немного разные химические свойства. Дисахариды образуются путем соединения двух моносахаридов вместе реакция синтеза дегидратации . В процессе образуется молекула воды. Мальтоза (солодовый сахар) образуется путем соединения двух молекул глюкозы вместе. Сахароза (тростниковый сахар) образуется путем соединения глюкозы и фруктозы. Лактоза (молочный сахар) образуется путем соединения глюкозы и галактозы. Мальтоза, сахароза и лактоза имеют одинаковую молекулярную формулу C 12 H 22 O 11 , но немного разные структурные формулы и немного разные химические свойства.
Простой тест на восстанавливающие сахара состоит в том, чтобы смешать их с равным количеством реагента Бенедикта (синего цвета) в пробирке и нагреть его в кипящей воде. Полисахариды образуются путем связывания многих моносахаридов вместе в ходе ряда реакций синтеза дегидратации. На каждый моносахарид, присоединенный к полисахаридной цепи, образуется молекула воды. Крахмал можно быстро определить, добавив йод Люголя. Наблюдается немедленное изменение цвета с коричневого цвета йода на иссиня-черный. Реакция происходит только с крахмалом. III. Белки Белки представляют собой сложные специализированные молекулы, состоящие из углерода,
водород, кислород и азот. Белки состоят из одного или нескольких полипептидов . Полипептиды
образуются путем соединения аминокислот в длинную неразветвленную цепь.
Аминокислоты связаны между собой пептидными связями, которых образуются при
карбоксильная группа одной аминокислоты взаимодействует с аминогруппой другой
следующая аминокислота в реакции синтеза дегидратации. Белки выполняют множество важных функций в живых организмах. Структурный
белки, такие как эластин и коллаген, обеспечивают поддержку. нормативный
белки контролируют клеточные процессы. Запасные белки, вырабатываемые в репродуктивных
структуры являются источником аминокислот для развивающихся организмов, например,
казеин в молоке, альбумин в яичном белке, различные белки в семенах растений. |
 Четыре класса органических соединений — углеводы, липиды, белки и нуклеиновые кислоты — в больших количествах обнаруживаются в живых организмах. Химические свойства различных классов зависят от присутствия конкретных функциональных групп. Как правило, более крупные молекулы в каждом классе образуются путем соединения одной или нескольких молекул строительного блока вместе в реакции синтеза дегидратации, во время которой на каждый добавленный строительный блок образуется молекула воды. Большие молекулы расщепляются на более мелкие молекулы строительных блоков посредством обратной реакции, называемой гидролизом , во время которой добавляется вода. В этом упражнении вы узнаете о структуре и свойствах углеводов, липидов и белков, а также о том, как проверить наличие этих органических молекул.
Четыре класса органических соединений — углеводы, липиды, белки и нуклеиновые кислоты — в больших количествах обнаруживаются в живых организмах. Химические свойства различных классов зависят от присутствия конкретных функциональных групп. Как правило, более крупные молекулы в каждом классе образуются путем соединения одной или нескольких молекул строительного блока вместе в реакции синтеза дегидратации, во время которой на каждый добавленный строительный блок образуется молекула воды. Большие молекулы расщепляются на более мелкие молекулы строительных блоков посредством обратной реакции, называемой гидролизом , во время которой добавляется вода. В этом упражнении вы узнаете о структуре и свойствах углеводов, липидов и белков, а также о том, как проверить наличие этих органических молекул. Липиды легко растворимы в неполярных растворителях , таких как хлороформ, бензол и эфир. К липидам относятся жиры и масла (важные в качестве соединений для накопления энергии), фосфолипиды и гликолипиды (часть структуры клеточных мембран), воски (защитные поверхностные покрытия на многих растениях и животных) и стероиды (находятся в некоторых клеточных мембранах и многих гормонах). .
Липиды легко растворимы в неполярных растворителях , таких как хлороформ, бензол и эфир. К липидам относятся жиры и масла (важные в качестве соединений для накопления энергии), фосфолипиды и гликолипиды (часть структуры клеточных мембран), воски (защитные поверхностные покрытия на многих растениях и животных) и стероиды (находятся в некоторых клеточных мембранах и многих гормонах). . Жирные кислоты различаются длиной цепи и количеством двойных связей между соседними атомами углерода. Если все атомы углерода в цепи жирной кислоты связаны с четырьмя различными атомами (двойные связи между атомами углерода отсутствуют), то жирная кислота имеет прямую цепь без изгибов или перегибов. Двойные связи между атомами углерода заставляют цепи жирных кислот изгибаться или перекручиваться. Жирные кислоты насыщенные жиры (например, сало, беконный жир или сливочное масло) не содержат двойных связей, содержат максимум атомов водорода, а прямые цепи жирных кислот плотно прилегают друг к другу. Жирные кислоты ненасыщенных жиров содержат по крайней мере одну двойную связь, меньше атомов водорода, и цепи жирных кислот не могут упаковываться так плотно друг к другу, потому что по крайней мере одна из цепей имеет излом или изгиб. Мононенасыщенные жиры , такие как оливковое масло, имеют одну двойную связь. Полиненасыщенные жиры , такие как кукурузное масло, имеют две или более двойных связи.
Жирные кислоты различаются длиной цепи и количеством двойных связей между соседними атомами углерода. Если все атомы углерода в цепи жирной кислоты связаны с четырьмя различными атомами (двойные связи между атомами углерода отсутствуют), то жирная кислота имеет прямую цепь без изгибов или перегибов. Двойные связи между атомами углерода заставляют цепи жирных кислот изгибаться или перекручиваться. Жирные кислоты насыщенные жиры (например, сало, беконный жир или сливочное масло) не содержат двойных связей, содержат максимум атомов водорода, а прямые цепи жирных кислот плотно прилегают друг к другу. Жирные кислоты ненасыщенных жиров содержат по крайней мере одну двойную связь, меньше атомов водорода, и цепи жирных кислот не могут упаковываться так плотно друг к другу, потому что по крайней мере одна из цепей имеет излом или изгиб. Мононенасыщенные жиры , такие как оливковое масло, имеют одну двойную связь. Полиненасыщенные жиры , такие как кукурузное масло, имеют две или более двойных связи.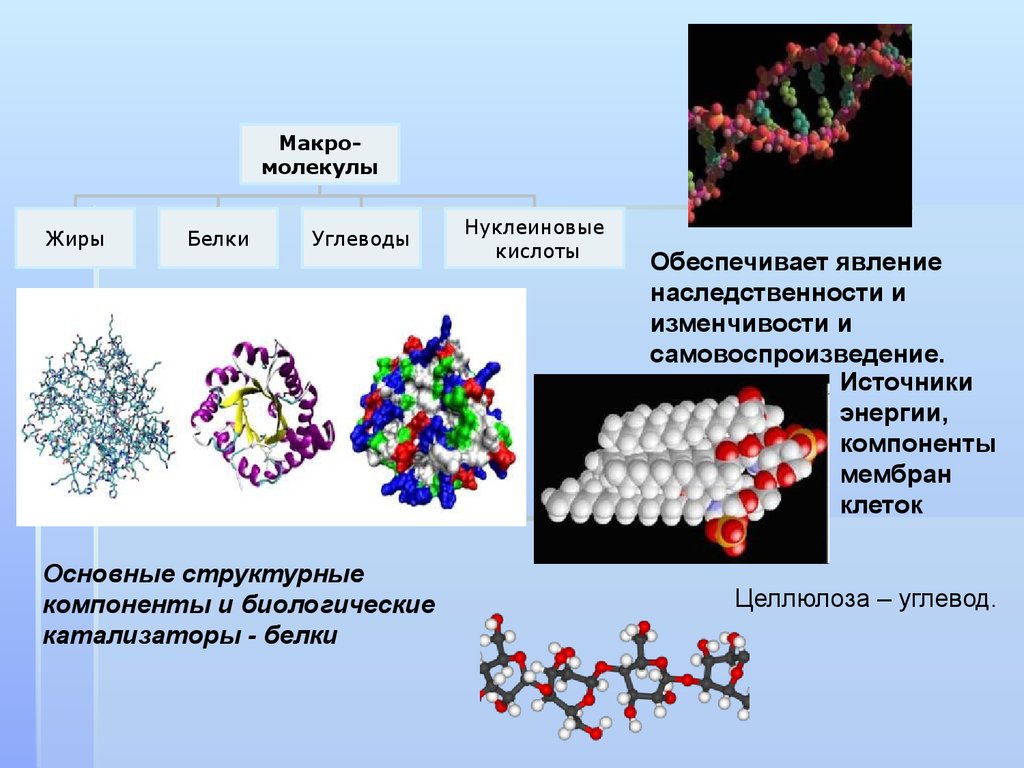 Менее «упорядоченная» структура ненасыщенных жиров является причиной их более низкой температуры плавления.
Менее «упорядоченная» структура ненасыщенных жиров является причиной их более низкой температуры плавления.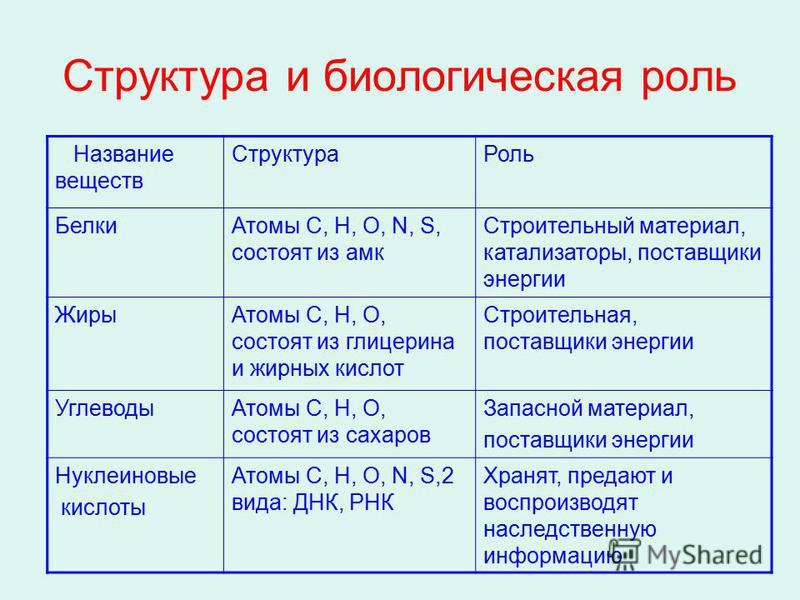 Дисахариды, , такие как сахароза, мальтоза и лактоза, содержат две молекулы сахара, связанные вместе. Полисахариды, , такие как крахмал, гликоген, целлюлоза и хитин, содержат много молекул сахара, связанных вместе.
Дисахариды, , такие как сахароза, мальтоза и лактоза, содержат две молекулы сахара, связанные вместе. Полисахариды, , такие как крахмал, гликоген, целлюлоза и хитин, содержат много молекул сахара, связанных вместе.
 Если присутствует редуцирующий сахар, образуется оранжевый осадок. Положительный тест Бенедикта требует, чтобы альдегидная или кетоновая группа находилась рядом с гидроксильной группой. Все моносахариды являются редуцирующими сахарами. Некоторые дисахариды являются восстанавливающими сахарами, а некоторые нет. Если реакционноспособные альдегидные или кетоновые группы обоих моносахаридов вовлечены в связь, удерживающую две единицы вместе, эти группы не могут свободно реагировать с ионами меди в растворе Бенедикта, и образующийся дисахарид не является восстанавливающим сахаром. Полисахариды не дают положительного результата на восстанавливающие сахара, если они не подвергаются реакции гидролиза (путем нагревания или вываривания), во время которой полисахариды расщепляются с образованием моносахаридов.
Если присутствует редуцирующий сахар, образуется оранжевый осадок. Положительный тест Бенедикта требует, чтобы альдегидная или кетоновая группа находилась рядом с гидроксильной группой. Все моносахариды являются редуцирующими сахарами. Некоторые дисахариды являются восстанавливающими сахарами, а некоторые нет. Если реакционноспособные альдегидные или кетоновые группы обоих моносахаридов вовлечены в связь, удерживающую две единицы вместе, эти группы не могут свободно реагировать с ионами меди в растворе Бенедикта, и образующийся дисахарид не является восстанавливающим сахаром. Полисахариды не дают положительного результата на восстанавливающие сахара, если они не подвергаются реакции гидролиза (путем нагревания или вываривания), во время которой полисахариды расщепляются с образованием моносахаридов. Полисахариды используются в качестве соединений для хранения энергии как растениями, так и животными. Растения производят полисахарид под названием крахмал . Позвоночные животные, включая человека, вырабатывают полисахарид, называемый гликогеном , , который хранится в клетках печени и мышц. Гликоген иногда называют животным крахмалом. Полисахариды также важны как структурные компоненты многих организмов. Клеточные стенки растений содержат полисахарид под названием 9.0155 целлюлоза . Клеточные стенки грибов и экзоскелеты членистоногих содержат хитин , полисахарид с азотом.
Полисахариды используются в качестве соединений для хранения энергии как растениями, так и животными. Растения производят полисахарид под названием крахмал . Позвоночные животные, включая человека, вырабатывают полисахарид, называемый гликогеном , , который хранится в клетках печени и мышц. Гликоген иногда называют животным крахмалом. Полисахариды также важны как структурные компоненты многих организмов. Клеточные стенки растений содержат полисахарид под названием 9.0155 целлюлоза . Клеточные стенки грибов и экзоскелеты членистоногих содержат хитин , полисахарид с азотом. Многие белки также содержат серу.
строительными блоками белков являются аминокислот . Есть двадцать
различные аминокислоты, обычно встречающиеся в белках. Все эти амино
кислоты имеют сходное строение. В центре молекулы находится альфа-углерод , который связан с четырьмя различными группами: (1) аминогруппа (NH 2 ), (2) карбоксильная группа (COOH),
(3) атом водорода и (4) группа R (также называемая боковой цепь ). Разные аминокислоты имеют разные группы R; в противном случае
двадцать аминокислот имеют идентичную структуру.
Многие белки также содержат серу.
строительными блоками белков являются аминокислот . Есть двадцать
различные аминокислоты, обычно встречающиеся в белках. Все эти амино
кислоты имеют сходное строение. В центре молекулы находится альфа-углерод , который связан с четырьмя различными группами: (1) аминогруппа (NH 2 ), (2) карбоксильная группа (COOH),
(3) атом водорода и (4) группа R (также называемая боковой цепь ). Разные аминокислоты имеют разные группы R; в противном случае
двадцать аминокислот имеют идентичную структуру.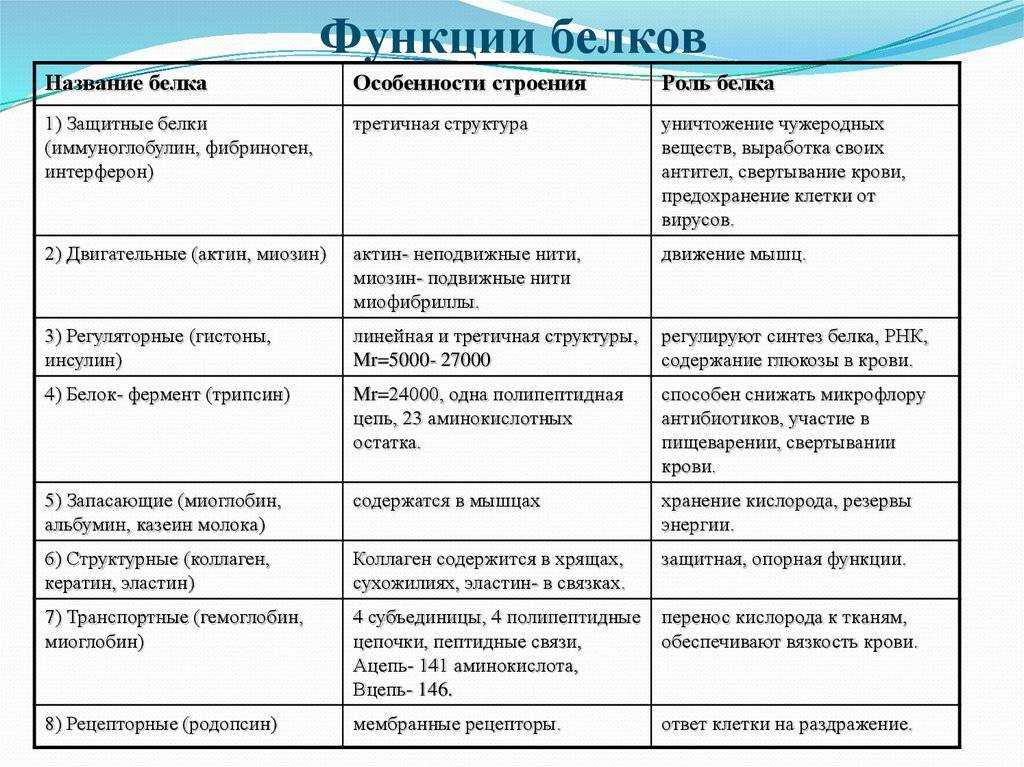 Как каждое амино
к растущей полипептидной цепи добавляется кислота, молекула воды
сформирован. Полипептиды имеют свободную (непрореагировавшую) аминогруппу, расположенную
на одном конце молекулы, называемом N-конец и свободный (непрореагировавший)
карбоксильная группа на другом конце молекулы называется C-концом .
Биохимики описывают структуру определенного полипептида, написав
вниз по последовательности аминокислот, начиная с N-конца и продолжая
по цепи до С-конца.
Как каждое амино
к растущей полипептидной цепи добавляется кислота, молекула воды
сформирован. Полипептиды имеют свободную (непрореагировавшую) аминогруппу, расположенную
на одном конце молекулы, называемом N-конец и свободный (непрореагировавший)
карбоксильная группа на другом конце молекулы называется C-концом .
Биохимики описывают структуру определенного полипептида, написав
вниз по последовательности аминокислот, начиная с N-конца и продолжая
по цепи до С-конца.