Метформин и сердечно–сосудистые осложнения сахарного диабета: «размышления у парадного подъезда» | Александров А.А.
В настоящее время метформин позиционируется, как один из основных препаратов выбора при лечении сахарного диабета (СД) 2 типа. По крайней мере, таково мнение авторов многих статей, опирающихся на рекомендации IFD и ADA. Складывается впечатление, что метформин – это своего рода «парадный подъезд» сахарного диабета 2 типа, через который рекомендуется пройти практически каждому больному при лечении этого заболевания.
Дело даже не в том, что сахароснижающая способность монотерапии метформина вполне сопоставима с эффективностью других групп гипогликемических средств (рис. 1). И, пожалуй, даже не в том, что комбинация метформина с большинством других сахароснижающих препаратов значительно расширяет возможности достижения целевых уровней компенсации углеводного обмена у больных сахарным диабетом 2 типа.
Представляется, что мнение о метформине, как о препарате первого выбора прежде всего основано на данных исследования UKPDS об уникальном для сахароснижающих препаратов свойстве метформина (Глюкофаж®), достоверно снижать частоту развития инфаркта миокарда и нарушений мозгового кровообращения у больных сахарным диабетом 2 типа (табл.
Представления об уникальных сердечно–сосудистых свойствах метформина особенно впечатляющи на фоне данных об особой безопасности применения метформина. Это проявляется, с одной стороны, в практически полном отсутствии опасных гипогликемий при его использовании, а с другой – в том, что такое тяжелое осложнение, как лактат–ацидоз, развивающийся у ряда больных при приеме препаратов группы бигуанидов, встречается исключительно редко при применении метформина. Все это неопровержимо свидетельствует о необходимости максимально широкого внедрения этого препарата в терапевтическую практику больных сахарным диабетом 2 типа.
Однако медицинская практика каждый раз сталкивает врача с индивидуальным, конкретным больным. И поэтому, планируя использовать рекомендации, основанные на опыте проведенных исследований, всякий раз пытаешься еще раз вспомнить, у каких же больных были получены столь привлекательные результаты. И, конечно, сопоставить больного, который сейчас, сегодня обратился к тебе за помощью, с теми больными из цитируемого исследования.

По сути, сталкиваешься с необходимостью ответить на несколько простых вопросов. В первую очередь: действительно ли применение метформина приводит к желаемым результатам у всех без исключения больных? Все ли ожидающие перед этим «парадным подъездом» получат обещанное благо? Или некоторым из них в этот «подъезд» входить все–таки не стоит? Много ли таких? Как их распознать? И можем ли мы ответить на эти вопросы сейчас?
В опубликованных в январе 2007 года Европейских рекомендациях по лечению сахарного диабета, предиабета и сердечно–сосудистых осложнений, разработанных специальной объединенной группой Европейского общества кардиологов и Европейского общества по изучению сахарного диабета, метформин представляется, как препарат первого выбора при избыточном весе у больных диабетом 2 типа.
 Правда, отнюдь не противопоказано. Просто нормальный и тем более пониженный вес у больных СД 2 типа часто свидетельствует о наличии у них уже достаточно выраженной инсулиновой недостаточности. У таких больных, конечно, целесообразнее начинать терапию с назначения препаратов сульфанилмочевины.
Правда, отнюдь не противопоказано. Просто нормальный и тем более пониженный вес у больных СД 2 типа часто свидетельствует о наличии у них уже достаточно выраженной инсулиновой недостаточности. У таких больных, конечно, целесообразнее начинать терапию с назначения препаратов сульфанилмочевины. Существует мнение, что дополнительными показаниями к использованию метформина у больных СД 2 типа может служить наличие гиперинсулинемии или гиперлипидемии. Пока это отдельные, частные мнения, не нашедшие отражения в официальных рекомендациях.
При назначении метформина лицам с повышенным весом из их числа должны быть исключены те, у кого имеются серьезные противопоказания к приему метформина. Вот как об этом говорится в уже упоминавшихся последних Европейских рекомендациях: «Метформин является важным компонентом как моно–, так и комбинированной терапии, при условии, что противопоказания для его применения отсутствуют».
Наиболее серьезным противопоказанием для применения метформина является высокий риск развития лактат–ацидоза.

С точки зрения клиники наиболее важными диагностическими критериями вышеперечисленных ситуаций являются следующие показатели:
• У каждого больного сахарным диабетом, получающим метформин, перед в/в введением йод–содержащих контрастных веществ необходимо определять концентрацию креатинина в сыворотке.

• При нормальном уровне креатинина исследование может быть проведено, а прием метформина приостанавливается на 48 часов и может быть возобновлен, если функция почек/концентрация креатинина остаются нормальными.
• Если функция почек нарушена, прием метформина приостанавливается и контрастные исследования могут быть проведены не ранее, чем через 48 часов. Возобновление приема метформина возможно только при отсутствии изменений в функции почек/концентрации креатинина (ESUR, 2006).
Учитывая, что в 80–90% случаев лактат–ацидоз развивается при почечной недостаточности – это одно из самых важных противопоказаний.
– Хроническое нарушение функции легких. Считается, что метформин противопоказан, если имеются симптомы, подтверждающие нарушение функции внешнего дыхания, выраженные рентгенологические признаки патологии бронхолегочной системы, постоянная медикаментозная терапия, кроме ингаляционных бронхолитиков.

– Хроническое нарушение функции печени. Повышение более чем в 2 раза уровня трансаминаз и щелочной фосфатазы.
– Алкоголизм.
– Острые инфекции, травмы, операции под общей анестезией.
Таким образом, строго говоря, абсолютно безопасно применять метформин можно в первую очередь у больных без явных сердечно–сосудистых и почечных осложнений сахарного диабета 2 типа.
В то же время, по данным многих Европейских исследований, на практике метформин применяется гораздо шире. Так, более чем у половины амбулаторных больных, получающих метформин, на самом деле имеется одно или даже несколько противопоказаний к его приему. Среди госпитализированных больных, принимающих метформин, доля пациентов хотя бы с одним противопоказанием к его применению достигает почти 75%. Реально каждый десятый амбулаторный и каждый второй стационарный больной, принимающий метформин, имеет несколько противопоказаний.
Ситуация объясняется довольно просто. Дело в том, что хотя вышеуказанные состояния действительно резко повышают риск развития лактат–ацидоза, сам по себе лактат–ацидоз при приеме метформина развивается весьма редко (в 0,03 случаях/1000 пациенто–лет).
 Таким образом, на практике лечащий врач сталкивается с подобной ситуацией крайне редко. Несомненно, это создает ощущение «мнимой» безопасности. «Мнимой» в связи с тем, что в руках у врача нет точных критериев, позволяющих вычислить, какого же конкретно больного с высоким риском лактат–ацидоза «пронесет», а у какого он вдруг разовьется. Летальность, связанная с лактат–ацидозом, составляет 0–0,039 на 1000 пациенто–лет. То есть если лактат–ацидоз вдруг «неожиданно» развивается, то вероятность летального исхода составляет для подобного конкретного «неудачника» 40–50%. Своего рода «русская рулетка» с большим количеством холостых зарядов.
Таким образом, на практике лечащий врач сталкивается с подобной ситуацией крайне редко. Несомненно, это создает ощущение «мнимой» безопасности. «Мнимой» в связи с тем, что в руках у врача нет точных критериев, позволяющих вычислить, какого же конкретно больного с высоким риском лактат–ацидоза «пронесет», а у какого он вдруг разовьется. Летальность, связанная с лактат–ацидозом, составляет 0–0,039 на 1000 пациенто–лет. То есть если лактат–ацидоз вдруг «неожиданно» развивается, то вероятность летального исхода составляет для подобного конкретного «неудачника» 40–50%. Своего рода «русская рулетка» с большим количеством холостых зарядов.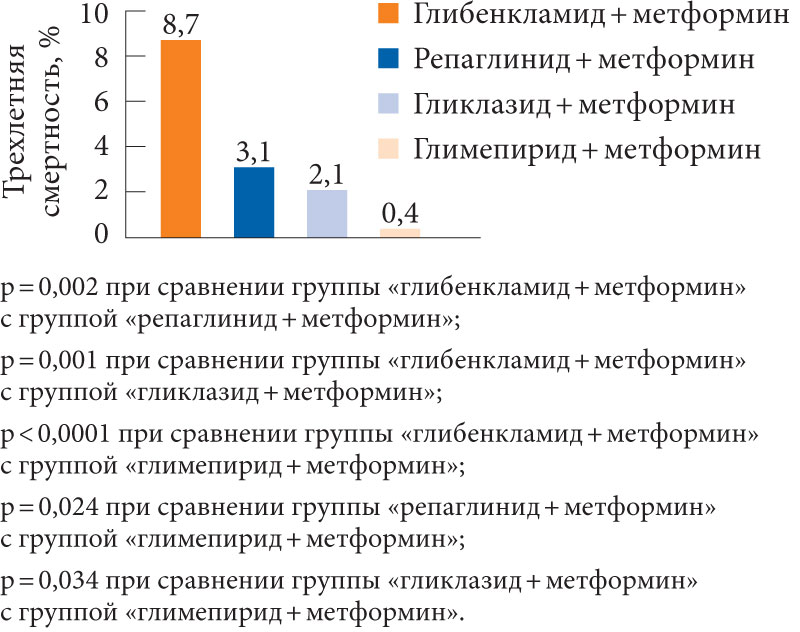 Во–вторых, необходимо безусловно отменять прием метформина при таких наиболее часто встречающихся в повседневной практике ситуациях, как предстоящая общая анестезия (метформин отменяется не менее чем за 72 часа), периоперационный период, острые инфекционные заболевания и обострения хронических, предстоящие рентгеноконтрастные исследования, острый коронарный синдром. Следует знать, что прием ряда кардиологических препаратов (дигоксин, прокаинамид, хинин, амилорид, триамтерен, фуросемид) может замедлить выведение метформина и способствовать повышению уровня лактата в крови.
Во–вторых, необходимо безусловно отменять прием метформина при таких наиболее часто встречающихся в повседневной практике ситуациях, как предстоящая общая анестезия (метформин отменяется не менее чем за 72 часа), периоперационный период, острые инфекционные заболевания и обострения хронических, предстоящие рентгеноконтрастные исследования, острый коронарный синдром. Следует знать, что прием ряда кардиологических препаратов (дигоксин, прокаинамид, хинин, амилорид, триамтерен, фуросемид) может замедлить выведение метформина и способствовать повышению уровня лактата в крови. Кроме того, при терапии метформином необходим регулярный лабораторный контроль гемоглобина (один раз в полгода) и не реже одного раза в год – мочевины, креатинина, печеночных ферментов. Если есть возможность, то планово, два раза в год определять содержание лактата в крови, а также проводить данное исследование при появлении жалоб на боли в мышцах (!). Больного следует также строго предупредить об опасности злоупотребления алкоголем, который может при одновременном приеме с метформином усилить продукцию лактата, а также способствовать развитию при этом гипогликемий.
Следуя этим достаточно простым правилам, можно в полной мере реализовать потенциальную безопасность метформина.
Игра безусловно стоит свеч! Ни один сахароснижающий препарат не снижает сердечно–сосудистую смертность и смертность от инфаркта миокарда столь мощно, как это способен сделать метформин. Надо только помнить, что подобных впечатляющих результатов врачи вправе ожидать в первую очередь при применении метформина в качестве монотерапии у больных с избыточным весом с впервые выявленным сахарным диабетом 2 типа.
С 2000 до 2010 года в мире число больных сахарным диабетом вырастет с 151 до 221 млн., а затем – до 300 млн. к 2025 году (прирост примерно в 6 млн. больных в год). Именно этим больным прежде всего должна проводиться монотерапия метформином. И больше, чем у половины из них ее эффективность сохранится до 6 лет, а у 25% – до 9 лет. И каждый следующий год будет прибавляться еще и еще 6 млн. больных. Огромный, постоянно растущий, с трудом осознаваемый ареал метформина, который уже сейчас составляет 25% от всех таблетированных сахароснижающих средств.

Именно с этим огромным ростом прогнозируемого применения метформина связан, по моему мнению, призыв международных экспертов к более настойчивому распространению среди практикующих врачей знаний о противопоказаниях к метформину и к тщательному соблюдению ими условий его безопасного применения. При подобной массовости использования метформина его ничтожная способность к стимуляции лактат–ацидоза может оказаться клинически значимой.
Применение метформина в 65% случаев связано с его использованием в комбинациях с другими сахароснижающими препаратами, в первую очередь с препаратами сульфанилмочевины. И здесь существует одна проблема, возникшая после публикации результатов UKPDS. Она не связана с сахароснижающими возможностями подобных комбинаций. Сульфаниламиды + метформин – это сахароснижающая классика. Ее эффективность в достижении целевых уровней глюкозы в крови сделала подобное сочетание наиболее используемым у больных сахарным диабетом 2 типа
Проблема в другом.
 С 1998 года широко обсуждаются следующие данные UKPDS: «У больных сахарным диабетом, интенсивно леченных комбинацией сульфаниламидов и метформина, общая смертность и смертность, связанная с диабетом, соответственно на 96% и 60% выше аналогичных показателей больных, находящихся на лечении только сульфаниламидами». Группа таких больных в UKPDS была немногочисленной – 480 больных. Это служило одним из объяснений полученных шокирующих результатов.
С 1998 года широко обсуждаются следующие данные UKPDS: «У больных сахарным диабетом, интенсивно леченных комбинацией сульфаниламидов и метформина, общая смертность и смертность, связанная с диабетом, соответственно на 96% и 60% выше аналогичных показателей больных, находящихся на лечении только сульфаниламидами». Группа таких больных в UKPDS была немногочисленной – 480 больных. Это служило одним из объяснений полученных шокирующих результатов. Возможно, критика в адрес UKPDS вполне обоснована. Однако можно привести и другие, менее известные работы, в которых смертность среди больных сахарным диабетом 2 типа, леченных комбинацией препаратов сульфанилмочевины и метформина, была выше, чем среди лиц на монотерапии сульфаниламидами. Там тоже можно высказать ряд критических замечаний. Плодотворней усомниться в абсолютной правоте критики и поискать возможную причину подобных совпадений.
Сейчас, в 2008 году, возможное объяснение найти достаточно просто. В литературе вполне доступны результаты нескольких хорошо организованных исследований по применению комбинированных препаратов, одновременно содержащих сульфанилмочевину и метформин.
 В подавляющем большинстве этих работ обнаружено, что при приеме определенных дозовых сочетаний глибенкламида и метформина количество фиксируемых гипогликемических осложнений не намного, но все же достоверно превышает подобный показатель при приеме аналогичных доз при монотерапии глибенкламидом.
В подавляющем большинстве этих работ обнаружено, что при приеме определенных дозовых сочетаний глибенкламида и метформина количество фиксируемых гипогликемических осложнений не намного, но все же достоверно превышает подобный показатель при приеме аналогичных доз при монотерапии глибенкламидом. Несомненно, рост числа гипогликемий – это рост риска сердечно–сосудистой смертности среди больных диабетом. Не знаю, можно ли данные об определенном росте риска гипогликемий при использовании комбинированной терапии препаратами сульфанилмочевины и метформина использовать для объяснения вышеописанных результатов UKPDS? Важно другое. Теперь, когда доказано, что опасность гипогликемий у подобных больных реально повышена, информированность о ней врачей и больных поможет минимизировать ее последствия. Еще раз подтверждено: сахароснижающая эффективность и эффективность в предотвращении сердечно–сосудистых осложнений – это не одно и то же.
Тем не менее рост риска гипогликемий при комбинированной терапии метфармина и препаратов сульфанилмочевины, по–видимому, если и представляет реальную сердечно–сосудистую опасность, то только для какой–то небольшой группы больных сахарным диабетом 2 типа.
 Об этом свидетельствуют результаты Канадского ретроспективного исследования, проанализировавшего 5–летний прием сахароснижающих средств у 12 тыс. больных СД 2 типа. Было обнаружено, что в целом среди больных сахарным диабетом 2 типа, получавших метформин в виде монотерапии или в виде его комбинации с другими сахароснижающими препаратами, общая и сердечно–сосудистая смертность была примерно на 40% ниже, чем у лиц, находящихся на терапии препаратами сульфанилмочевины. Европейские рекомендации 2007 года, подчеркивающие пользу применения метформина в комбинации с другими сахароснижающими средствами для контроля за развитием сердечно–сосудистых осложнений у больных сахарным диабетом 2 типа, таким образом, вполне объективно отражают уровень сегодняшних знаний по этой проблеме.
Об этом свидетельствуют результаты Канадского ретроспективного исследования, проанализировавшего 5–летний прием сахароснижающих средств у 12 тыс. больных СД 2 типа. Было обнаружено, что в целом среди больных сахарным диабетом 2 типа, получавших метформин в виде монотерапии или в виде его комбинации с другими сахароснижающими препаратами, общая и сердечно–сосудистая смертность была примерно на 40% ниже, чем у лиц, находящихся на терапии препаратами сульфанилмочевины. Европейские рекомендации 2007 года, подчеркивающие пользу применения метформина в комбинации с другими сахароснижающими средствами для контроля за развитием сердечно–сосудистых осложнений у больных сахарным диабетом 2 типа, таким образом, вполне объективно отражают уровень сегодняшних знаний по этой проблеме.Существует, однако, еще одна весьма заманчивая перспектива использования метформина. Это перспектива целенаправленного применения метформина при решении проблем интервенционного лечения ишемической болезни сердца у больных сахарным диабетом.
Как известно, результаты реваскуляризации коронарных сосудов сердца у больных сахарным диабетом достоверно хуже, чем у лиц без нарушения углеводного обмена. Даже при полном восстановлении просвета пораженных коронарных сосудов, возобновление клинических признаков ишемической болезни сердца у больных сахарным диабетом происходит чаще и через более короткий промежуток времени после произведенного вмешательства. Во многом это связано с тем, что у больных сахарным диабетом в большом проценте случаев (до 40%) восстановление кровотока в крупных коронарных сосудах не сопровождается полноценным улучшением тканевой микрососудистой циркуляции крови.
Исходное, не связанное с процессом реваскуляризации нарушение микрососудистого кровотока является характерной чертой поражения коронарного бассейна при сахарном диабете. Значительное – на 30–40% снижение микрососудистого коронарного резерва отмечается у больных диабетом задолго до появления гемодинамически значимых сужений просвета крупных коронарных артерий. Во многом именно поэтому после удачного восстановления просвета крупных коронарных сосудов у больных сахарным диабетом более часто сохраняются или через более короткое время вновь появляются клинические признаки ишемической болезни сердца: стенокардия, нарушения ритма сердца, признаки застойной сердечной недостаточности.
К сожалению, до настоящего времени не существует единых общепризнанных эффективных методов, позволяющих положительно решить данную проблему. Вот почему опубликованные в 2004 году результаты исследования PRESTO (Prevention of Restenosis with Tranilast and its Outcomes), проведенного в Калифорнии, привлекают к себе пристальное внимание.
PRESTO является крупнейшим проспективным рандомизированным исследованием, в котором проводилось длительное тщательное наблюдение за больными, перенесшими чрескожное интервенционное вмешательство на коронарных сосудах сердца. В исследование было включено 11484 больных. При анализе их историй болезни было обнаружено, что 2772 из этих больных страдают сахарным диабетом. Специфическая терапия больных диабетом включала в себя прием препаратов сульфанилмочевины, метформина (Глюкофаж®), тиазолидиндионов или инъекции инсулина. При этом 1110 больных получали метформин или его комбинацию с другими сахароснижающими препаратами, а у 887 больных в их сахароснижающей терапии метформин и тиазолидиндионы отсутствовали.
Мультивариантное сравнение результатов чрескожной интервенционной реваскуляризации у больных на инсулиносинсетайзерах (метформин + его комбинация с другими препаратами) и больных без инсулиносинсетайзеров обнаружил их существенные достоверные отличия. Оказалось, что терапия метформином (Глюкофаж®) сопровождается достоверно более редким наступлением у больных сахарным диабетом летального исхода в отдаленном постреваскуляризационном периоде и достоверно более редким развитием у них в последующем инфаркта миокарда. Интересно, что достоверной разницы в повторных реваскуляризациях заинтересованных сосудов между этими группами больных отмечено не было.
Полученные данные наводят на мысль, что механизм действия метформина у этих больных не связан с его воздействием на постреваскуляризационную пролиферацию интимы в коронарном сосуде, подвергшемся воздействию. Скорее, благоприятный эффект метформина можно связать с его абсолютно уникальной недавно обнаруженной способностью резко уменьшать гемодинамические нарушения на уровне микроциркуляторного русла, особенно развивающейся при постишемической реперфузии. Учитывая, что данная способность метформина (Глюкофажа) проявляется как при наличии сахарного диабета, так и в его отсутствие, возможный потенциал его применения при интервенционных вмешательствах может оказаться необычайно широк.
Однако для того, чтобы это стало явью, необходимо, конечно, еще не одно исследование, подтверждающее результаты PRESTO. Но если это произойдет, то к многомиллионному сообществу больных сахарным диабетом 2 типа, безусловно нуждающихся в приеме Глюкофажа, присоединятся миллионы больных, подвергающиеся интервенционной реваскуляризации коронарных сосудов и, возможно, еще и многие другие пациенты, у которых возникновение нарушений микроциркуляторного русла вносит существенный вклад в прогрессирование их заболевания.
.
Клинико-фармакологические аспекты титирования дозировки метформина | Карпов
Метформин относится к числу базовых средств для лечения сахарного диабета 2 типа (СД 2), а также, совместно с препаратами других групп применяется при метаболическом синдроме, ожирении, дислипидемиях, дизовариальных нарушениях и некоторых других состояниях. Фармакодинамические эффекты препарата, имеющие отношение к лечению СД 2, известные к настоящему времени, включают в себя [1]:
усиление утилизации глюкозы;
увеличение числа рецепторов к инсулину на клеточной мембране и активизацию транспорта глюкозы в тканях.
уменьшение продукции глюкозы печенью;
уменьшение всасывания углеводов в желудочно-кишечном тракте;
увеличение потребления глюкозы мышечной и жировой тканями.
Метформин, таким образом, оказывает влияние на ключевой момент инсулинорезистентности – повышает чувствительность тканей к инсулину, скорее всего, за счет увеличения количества рецепторов инсулина на мембранах. На мембранах эритроцитов показано, что через 1 нед лечения число рецепторов увеличивается на 16%, а через 4 нед – на 84% [2]. К тому же метформин вызывает увеличение активности тирозинкиназы, гликогенсинтетазы, стимулирует синтез фосфатидилинозитол-3-киназы, ферментов, ответственных за переносчики глюкозы, и, таким образом, увеличивает ее утилизацию [3]. Предполагается, что и на пострецепторном уровне, наряду с потенцированием действия инсулина, он может оказывать непосредственное влияние на ферментные системы, участвующие в метаболизме глюкозы [4].
Метформин – единственное из пероральных сахаропонижающих средств, угнетающее продукцию глюкозы в печени, которая у больных СД 2 значительно увеличена. Это может быть обусловлено подавлением основных ферментов глюконеогенеза, повышением чувстительности гепатоцитов к инсулину и подавлением липолиза в висцеральной жировой ткани, что приводит к снижению поступления свободных жирных кислот (СЖК) в печень [5]. Снижение инсулинорезистентности в гепатоцитах под влиянием метформина стимулирует действие инсулина на ферменты обмена гликогена – фосфорилазу и гликогенсинтетазу, что активирует синтез гликогена, на который расходуется в том числе имеющаяся в печени глюкоза. Эти основные механизмы действия метформина приводят к снижению уровня глюкозы натощак и повышению чувствительности тканей к инсулину. Благодаря замедлению всасывания углеводов метформин практически не дает гликемических пиков после еды, чем отличается от производных сульфонилмочевины. Опасности гипогликемии при его применении нет. С фармакологической точки зрения будет правильно называть его антигипергликемическим, а не гипогликемизирующим средством. Уменьшение инсулинорезистентности метформином по иному, чем сульфонилмочевинными препаратами, механизму, препятствует гиперинсулинемии – мощному фактору дислипидемий, сердечно-сосудистых осложнений, абдоминального ожирения, повышенной агрегации тромбоцитов и угнетения фибринолитической активности плазмы [6]. Под влиянием метформина снижается окисление свободных жирных кислот [7], высокие концентрации которых способствуют инсулинорезистентности и синтезу атерогенных классов липопротеидов. Повышенный уровень свободных жирных кислот наблюдается при ожирении и СД 2. Метформин способен стабилизировать и даже снижать вес, особенно у лиц с ожирением, за счет уменьшения массы жировой ткани. Значительное уменьшение количества общего и висцерального жира при лечении метформином наблюдали у женщин с абдоминальным ожирением [8]. Учитывая роль абдоминального ожирения в патогенезе МС, снижение веса рассматривается у больных с ИР как способ профилактики сердечно-сосудистых осложнений [9].
Все вышеприведенные сведения не представляют особой новости для специалистов, поскольку препарат применяется несколько десятилетий, и фармакоэпидемиологические данные по его фармакодинамике и клинической эффективности убедительно доказывают целесообразность применения при СД 2. Вместе с тем клинико-фармакологические особенности метформина, особенно то, что касается его фармакокинетики, повлекшие необходимость внесения технологических новшеств в современные лекарственные формы, требуют внимания.
Абсорбция метформина медленная и может составлять до 6 ч. Период полуэлиминации из плазмы крови до 6 ч. Не метаболизируется и выводится с мочой в неизмененном виде. Важно заметить, что метформин не влияет на скорость печеночного кровотока и, с учетом, что и поступление его по портальной вене имеет константные характеристики, можно ожидать стабильных фармакокинетических параметров его в крови [10]. Среднетерапевтические плазменные концентрации 1–2 мкг/мл и не должны превышать 5 мкг/мл. Имеется дозозависимый характер установления максимальных концентраций в плазме от 1,03 мкг/мл при приеме 500 мг до 2,01 мкг/мл при приеме по 850 мг 3 раза в сутки. Концентрации метформина в стенке кишечника, слюнных железах, почках и печени превышают его уровень в плазме крови, тогда как в скелетных мышцах и мышце сердца содержание метформина практически соответствует таковому в плазме крови [7].
Особое внимание должно быть привлечено к существенному возрастанию максимальной концентрации и снижению почечного клиренса препарата у пожилых больных и пациентов с нарушением функции почек (рис. 1, 2). Согласно клинико-фармакологическому закону, равновесная концентрация любого препарата в крови, а следовательно, максимально возможный терапевтический эффект при выбранной дозе, устанавливается через 5 периодов его полуэлиминации. С учетом среднего значения этого периода для метформина следует полагать, что равновесная концентрация при нормальной функции почек устанавливается в течение 2 сут, что позволяет достаточно быстро оценить клиническую эффективность препарата. Вместе с тем короткий период полуэлиминации требует и пристального к себе внимания – необходимости постепенного повышения дозировки, так называемого титрования. Иными словами, лечебные дозировки метформина, диапазон которых 1,7–2 г в сутки [22], достигаются постепенно, начиная с 500 мг в сутки.
Опасность назначения всей суточной дозы сразу, при первом приеме, без титрования, к тому же без учета клиренсовой функции почек чревата развитием лактоацидоза, послужившего причиной запрета применения бигуанидов ранних поколений. Угнетая глюконеогенез, бигуаниды способствуют увеличению содержания лактата, пирувата, аланина, т.е. предшественников глюкозы в процессе глюконеогенеза. Поступающий при этом в повышенном количестве в печень лактат используется для образования глюкозы как глюконеогенный субстрат, что препятствует развитию гипогликемии [11]. Однако при действии препаратов этого класса количество нарастающего лактата превышает образование пирувата, и создаются условия для развития молочнокислого ацидоза. В случае постепенного прибавления лечебной дозировки метформина до оптимальной это осложнение практически не встречается. Тщательный фармакоэпидемиологический метаанализ клинических исследований препарата у больных СД 2 показывает, что частота лактацидоза при его использовании составляет 8,4 случая на 100 тыс. человеко-лет, а в контроле (плацебо или другие сахаропонижающие средства) – 9 на 100 тыс. [12]. Таким образом, при правильной тактике титрования метформин не повышает риск лактоацидоза. Риск этого осложнения при лечении метформином в 20 раз ниже, чем при лечении фенформином, а смертность от него не выше таковой при гипогликемической коме, возникающей при неправильном применении препаратов сульфонилмочевины [13].
Существенной причиной для титрования дозировки метформина является также недостаточно хорошая переносимость полной суточной дозировки, данной одномоментно сразу при старте фармакотерапии. В качестве основных нежелательных эффектов метформина выступают желудочно-кишечные нарушения: диарея, вздутие живота, тошнота (табл. 1) [14]. Механизмы уменьшения всасывания углеводов в кишечнике под влиянием метформина еще не до конца выяснены. Известно, что распределение препарата в кишечнике меньше, чем в печени или почках, тем не менее концентрации вполне достаточны для эффективного вмешательства в процессы абсорбции и транспортировки углеводов (рис. 3) [15]. При использовании малых дозировок метформина в эксперименте транспорт глюкозы через слизистую тонкого кишечника изменялся незначительно – на 6,5%, при повышении концентрации бигуанида (соответствует приему 850 мг) уменьшение всасывания глюкозы происходило на 53,8% (p<0,001) [16]. Экстраполируя экспериментальные данные по концентрации метформина на фармакотерапевтические, принятые у человека, можно сделать вывод о том, что при использовании препарата в дозе 250–500 мг всасывание глюкозы страдает незначительно, а при назначении его в дозировке 2 г – уменьшается наполовину. При этом толерантности к антиабсорбционному эффекту метформина не прослеживается, т.е. он постоянен как во временном, так и количественном отношении [17].
Всасывание углеводов зависит от наличия дисахаридаз в щеточной кайме ворсинок тонкой кишки. Имеется детерминированная предельная срочная (одномоментная) энзиматическая активность, которая не может полноценно обработать весь объем остающихся в полости кишечника углеводов. Экспериментальные данные свидетельствуют о том, что при сахарном диабете дисахаридазы итак менее активны [18], что может усугубляться единовременным применения метформина в большой дозировке. Относительный дефицит активности хотя бы одного энзима или более приводит к осмотической задержке воды неабсорбированными дисахаридами в просвете кишки. При синдроме нарушенного всасывания повышение осмолярности является следствием нарушения пищеварительно-транспортного конвейера и накопления в кишечном содержимом гидролизованных нутриентов. Поскольку слизистая оболочка тонкой кишки свободно проницаема для воды и электролитов, устанавливается осмотическое равновесие между содержимым тонкой кишки и плазмой, что и ведет к диарейному синдрому. Осмотическая диарея характеризуется жидким стулом, полифекалией, высокой осмолярностью химуса и фекалий, возрастанием фекальной концентрации короткоцепочечных жирных кислот и молочной кислоты, незначительными фекальными потерями электролитов, низким значением рН кала. Еще одним механизмом диареи в патогенезе ятрогенного воздействия высокодозной одномоментной терапии метформином можно считать возникающую гиперсекрецию со стороны слизистой оболочки кишечника. При начале терапии метформином с больших дозировок и высоком остаточном объеме углеводного содержимого в кишечнике неминуемо возникает бактериальное обсеменение тонкой кишки и связанные с жизнедеятельностью микроорганизмов биохимические процессы избыточного брожения и гниения в кишечнике.
Постепенное титрование дозировки метформина существенно снижает частоту диареи, вздутия живота и других неприятных ощущений, что повышает приверженность больных проводимой фармакотерапии. Казалось бы парадоксально – выше упоминалось, что эффект препарата по уменьшению всасывания углеводов остается относительно постоянным, неугасающим. Следовательно, углеводная масса остается той же, и нарушения ферментации и следующие за ними нежелательные эффекты – такими же в количественном и качественном выражении. За счет чего же достигается лучший комплаенс при титровании метформина?
По нашему мнению, есть две составляющие. Во-первых, больной в процессе лечения в случае появления дискомфорта начинает более тщательно следить за диетой. Говоря образно, метформин к тому же еще является дисциплинирующим фармакологическим фактором комплаентности диеты и его своеобразным индикатором. Во-вторых, активность ферментов подвержена определенным законам: если компенсаторно не могут значимо – по механизму отрицательной обратной связи – возрасти энзиматические возможности дисахаридаз, снижаемые метформином, увеличивается амилолитическая составляющая (количество, активность) панкреатического сока. Давно известно, что при СД 2 экзокринная функция поджелудочной железы практически не страдает [19]. При отсутствии у таких пациентов генетически детерминированных нарушений образования амилазы ее активность возрастает в десятки раз, что приводит к нормализации процесса внутрикишечного превращения углеводов без последующего их всасывания, поскольку функция дисахаридаз, как уже неоднократно отмечалось выше, снижена [20].
Таким образом, нивелировка возможного отрицательного эффекта метформина на функции органов пищеварения, кислотно-основное состояние лежит в плоскости постепенного увеличения его дозировки и полностью находится под контролем врача и пациента. Врачебная составляющая контроля зависит не только от понимания специалистом важности инициации и последующей консолидации фармакотерапии, но и от тех возможностей, которые предоставляет фармацевтическая промышленность для ее обеспечения. С этой точки зрения несомненно преимущество тех лекарственных форм метформина, которые могут применяться как в начальных невысоких дозировках, так и в дальнейшем – при наращивании дозы. К тому же имеется абсолютно четко прослеживаемая приверженность больных выбранной «марке» (торговому наименованию препарата, упаковке, даже виду таблеток). Больные в массе своей далеко не всегда ориентируются в том аспекте самолечения, который предусматривает прием даже одного и того же средства, но выпускаемого в разных дозировках. Нами это ранее было показано на примере антибиотиков, когда на основании опроса больных мы пришли к заключению, что более чем в половине случаев, когда больной сталкивается с тем что ему надо принимать одновременно 2–3 таблетки или для обеспечения разовой дозы, имеются нарушения в приеме [21]. Поэтому лучше всего использовать препараты, выпускаемые в лекарственных формах со среднетерапевтическими дозировками, при условии, что таблетки, как в случае с метформином, в целях титрования легко можно делить на части. В дальнейшем постепенное наращивание дозы пройдет для больного менее сложно. С этой точки зрения перспективы комплаенса лучше при использовании таблеток метформина по 1000 мг, которые можно было бы как разделить на 2 равные части для инициации лечения, так и использовать для дальнейшего постепенного повышения дозировки до оптимальной суточной.
Титрование Метформина (Консенсус Американской Диабетической Ассоциации и Европейской Ассоциации по изучению диабета, ADA/EASD, 2006 г.) [22]
Начальная доза составляет 500 мг 1 или 2 раза в день во время еды (завтрак или ужин).
Через 5–7 дней, при отсутствии побочных явлений со стороны органов пищеварения, доза увеличивается до 850–1000 мг перед завтраком и ужином.
В случае появления побочных эффектов, дозу препарата следует уменьшить до первоначальной и попытаться увеличить ее позже.
Максимально эффективная доза препарата обычно составляет 850 мг 2 раза в сутки. Увеличение дозы препарата до 3,0 г в сутки лишь немного улучшает показатели гликемии. Основным ограничением к увеличению дозы препарата обычно является развитие побочных эффектов со стороны органов пищеварения.
***
Сиофор® 1000 (Берлин-Хеми /Менарини) – новая форма метформина, хорошо зарекомендовавшего себя в России на протяжении 10 лет. Таблетка Сиофор® 1000, в отличие от препаратов метформина других производителей, единственная легко делящаяся на части благодаря широко нанесенной на нее риске. Простое деление таблетки Сиофора® 1000 позволяет с легкостью подобрать дозу препарата и обеспечить максимальную индивидуализацию лечения.
1. Campbell A. Glycaemic control in type 2 diabetes // Clin Evid. — 2005;14:474-490.
2. Lord J.M., White S.I., Bailey C.J. et al. Effect of metformin on insulin receptor binding and glycaemic control in type II diabetes // Br.Med.J. — 1983;286(6368):830-831.
3. Musi N., Goodyear L.J. Insulin resistance and improvements in signal transduction // Endocrine. — 2006;29(1):73-80.
4. Musi N. AMP-activated protein kinase and type 2 diabetes // Curr Med Chem. — 2006;13(5):583-589.
5. Guigas B., Bertrand L., Taleux N. et al. 5-Aminoimidazole-4-carboxamide- 1-beta-D-ribofuranoside and metformin inhibit hepatic glucose phosphorylation by an AMP-activated protein kinase-independent effect on glucokinase translocation // Diabetes. — 2006;55(4):865-74.
6. Schumm-Draeger P.M. Current treatment with oral antidiabetic agents // MMW Fortschr Med. — 2006;148(9):33-35.
7. Bailey C.J, Turner R.C. Metformin // N.Engl. J. Med. — 1996;334:574-579.
8. Phillips S.A., Ciaraldi T.P., Kong A.P.S. et al. Modulation of circulating and adipose tissue adiponectin levels by antidiabetic therapy // Diabetes. — 2002;52:667-674. 9. McFarlane SI, Banerji M, Sowers JR. Insulin resistance and cardiovascular disease. J Clin Endocrinol Metab 2001;86:713-18.
9. Signore A., Fiore V., Chianelli M. et al. The effect of metformin on liver blood flow in vivo in normal subjects and patients with non insulin dependent diabetes // Diabetes Res Clin Pract. — 1996;33(2):83-7.
10. Khan J.K., Pallaki M., Tolbert S.R., Hornick TR. Lactic acidemia associated with met-formin // Ann Pharmacother. — 2003;37(1):66-9.
11. Salpeter S.R., Greyber E., Pasternak G.A., et al. Risk of fatal and nonfatal lactic acidosis with metformin use in type 2 diabetes mellitus: systematic review and meta-analysis. Arch Intern Med. 2003;163(21):2594-602.
12. Chan N.N., Brain H.P., Feher M.D. Metformin-associated lactic acidosis: a rare or very rare clinical entity? Diabet Med 1999;16(4):273-81.
13. http://www.mosbysdrugconsult.com/DrugConsult/ Top_200/Drugs/e3204.html#t003204-cp-1
14. De-Sheng Wang D-S., Jonker J.W, Kato Y. et al. Involvement of organic cation trans-porter 1 in hepatic and intestinal distribution of metformin // Prarmacol. Exp. Ther. — 2002;302(2):510-5
15. Ikeda T., Iwata K., Murakami H. Inhibitory effect of metformin on intestinal glucose absorption in the perfused rat intestine // Biochem Pharmacol. — 2000;59(7):887-90.
16. Cheng A., George Fantus G. Oral antihyperglycemic therapy for type 2 diabetes melli-tus // CMAJ — 2005;172(2):213-26
17. McAnuff-Harding M.A., Omoruyi F.O., Asemota H.N. Intestinal disaccharidases and some renal enzymes in streptozotocin-induced diabetic rats // Life Sci. — 2006;78(22):2595-600.
18. Bretzke G. Diabetes mellitus and exocrine pancreas function // Z Gesamte Inn Med. — 1984;39(16):388-90.
19. Guarna M.M., Borowsky R.L. Genetically controlled food preference: biochemical mechanisms // Proc Natl Acad Sci USA. — 1993;90(11):5257-61.
20. Karpov O., Zaytsev A. Utilization of antimicrobials in CAP // Abstr. 5-th Annual In-tern. Meeting ISPOR, 2000, Arlington, USA. In:Value in Health.- 2000;3(2):124-125.
21. Nathan DM, Buse JB, Davidson MB, et al. Management of hyperglycemia in type 2 diabetes: a consensus algorithm for the initiation and adjustment of therapy. Diabetes Care 2006; 29 (8): 1963-1972.
Роль метформина в профилактике диабетической нефропатии при экспериментальном сахарном диабете 2 типа | Байрашева
1. Бабенко А.Ю., Байрашева В.К. Диабетическая нефропатия: зависит ли ренопротекция от выбора сахароснижающей терапии? // Медицинский совет. 2015. № 7. С. 32-43.
2. Байрашева В.К. Моделирование сахарного диабета и диабетической нефропатии в эксперименте // Современные проблемы науки и образования. 2015. Т. 4. С. 460(11). doi: 10.17513/spno.127-21024.
3. Байрашева В.К., Бабенко А.Ю., Дмитриев Ю.В. и др. Новая модель сахарного диабета 2 типа и диабетической нефропатии у крыс // Трансляционная медицина. 2016. № 3(4). С. 44-55.
4. Бондарь И.А., Климонтов В.В. Ранние маркеры диабетической нефропатии // Клиническая нефрология. 2010. № 2. С. 60-65.
5. Кравчук Е.Н., Галагудза М.М. Применение метформина при сочетании ишемической болезни сердца и сахарного диабета 2 типа: механизмы действия и клиническая эффективность // Сахарный диабет. 2013. № 1. С. 5-14.
6. Моргунов Л. Ю. Плейотропные эффекты метформина // Исследования и практика в медицине. 2014. Т. 1. № 1. С. 62-68.
7. Попова П.В., Рязанцева Е.М., Зазерская И.Е. и др. Восстановление менструальной функции в результате терапии метформином у женщин с синдромом поликистозных яичников // Проблемы женского здоровья. 2010. Т. 5. № 3. С. 11-17.
8. Попова П.В., Рязанцева Е.М., Зазерская И.Е. и др. Роль снижения массы тела и приема метформина в восстановлении менструальной функции у женщин с синдромом поликистозных яичников и избыточной массой тела // Проблемы эндокринологии. 2011. Т. 57. № 2. С. 14-18.
9. Спасов А.А, Воронкова М.П., Снигур Г.Л, и др. Экспериментальная модель сахарного диабета типа 2 // Биомедицина. 2011. Т. 3. С. 12-18.
10. Шестакова М.В, Дедов И.И. Сахарный диабет и хроническая болезнь почек. Москва: Медицинское информационное агентство, 2009. 482 с.
11. Alhaider A.A., Korashy H.M., Sayed-Ahmed M.M., et al. Metformin attenuates streptozotocin-induced diabetic nephropathy in rats through modulation of oxidative stress genes expression // Chem. Biol. Interact. 2011. Vol. 192. № 3. P. 233-242.
12. Bakoush O., Tencer J., Tapia J., et al. Higher urinary IgM excretion in type 2 diabetic nephropathy compared to type 1 diabetic nephropathy // Kidney Int. 2002. Vol. 61. № 1. P. 203-208.
13. Bayrasheva V.K., Grineva E.N., Babenko A.Y. et al. Nicotinamide-streptozotocin-induced type 2 diabetes in uninephrectomized high-fat-fed rats: a novel non-genetic rat model of diabetic nephropathy // Eumpean Heart Journal. 2015. Vol. 36 (suppl 1): P. 5236.
14. Ekstrom N., Schioler L., Svensson A.M., et al. Effectiveness and safety of metformin in 51 675 patients with type 2 diabetes and different levels of renal function: a cohort study from the Swedish National Diabetes Register // B. M. J. Open. 2012. Vol. 2. № 4. pii: e001076. doi: 10.1136/bmjopen-2012-001076.
15. Fox C.S., Matsushita K., Woodward M., et al. Associations of kidney disease measures with mortality and end-stage renal disease in individuals with and without diabetes: a meta-analysis // Lancet. 2012. Vol. 380. № 9854. P. 1662-1673.
16. Fu W.J., Xiong S.L., Fang Y.G., et al. Urinary tubular biomarkers in short-term type 2 diabetes mellitus patients: a cross-sectional study // Endocrine. 2012. Vol. 41. № 1. P. 82-88.
17. Giunti S., Barit D., Cooper M. E. Mechanisms of diabetic nephropathy. Role of hypertension // Hypertension. Vol. 48. № 4. P. 519-526.
18. Gunaratnam L., Bonventre J.V. HIF in kidney disease and development // J. Am. Soc. Nephrol. 2009. Vol. 20. № 9. P. 1877-1887.
19. Holman R.R., Paul S.K., Bethel M.A., et al. 10-year follow-up of intensive glucose control in type 2 diabetes // N. Engl. J. Med. 2008. Vol. 359. № 15. P. 1577-1589.
20. Hosohata K., Ando H., Takeshita Y., et al. Urinary TIM-1 is a sensitive biomarker for the early stage of diabetic nephropathy in Otsuka Long-Evans Tokushima Fatty rats // Diab. Vasc. Dis. Res. 2014. Vol. 11. № 4. P. 243-250.
21. Ishibashi Y., Matsui T., Takeuchi M., et al. Metformin inhibits advanced glycation end products (A GEs)-induced renal tubular cell injury by suppressing reactive oxygen species generation via reducing receptor for AGEs (RAGE) expression // Horm. Metab. Res. 2012. Vol. 44. № 12. P. 891-895.
22. Jefferson J.A., Shankland S.J., Pichler R.H. Proteinuria in diabetic kidney disease: a mechanistic viewpoint // Kidney Int. 2008. Vol. 74. № 1. P. 22-36.
23. Jin Q., Cheng J., Liu Y., et al. Improvement of functional recovery by chronic metformin treatment is associated with enhanced alternative activation of microglia/ macrophages and increased angiogenesis and neurogenesis following experimental stroke // Brain Behav. Immun. 2014. Vol. 40. P. 131-142.
24. Kim J., Shon E., Kim C.S., et al. Renalpodocyte injury in a rat model of type 2 diabetes is prevented by metformin // Exp. Diabetes Res. 2012. 2012:210821.
25. Klachko D., Whaley-Connell A. Use of metformin in patients with kidney and cardiovascular diseases // Cardiorenal Med. 2011. Vol. 1. № 2. P. 87-95.
26. Kravchuk E., Grineva E., Bairamov A., et al. The effect of metformin on the myocardial tolerance to ischemia-reperfusion injury in the rat model of diabetes mellitus type II // Exp. Diabetes Res. 2011. 2011:907496.
27. Kunika K., Yamaoka T., Itakura M. Damage of charge-dependent renal tubular reabsorption causes diabetic microproteinuria // Diabetes Res. Clin. Pract. 1997. Vol. 36. № 1. P. 1-9.
28. Lachin J. M., Viberti G., Zinman B., et al. Renal function in type 2 diabetes with rosiglitazone, metformin, and glyburide monotherapy // Clin. J. Am. Soc. Nephrol. 2011. Vol. 6. № 5. P. 1032-1040.
29. Lemley K.V., Blouch K., Abdullah I., et al. Glomerular permselectivity at the onset of nephropathy in type 2 diabetes mellitus // J. Am. Soc. Nephrol. 2000. Vol. 11. P. 2095-2105.
30. Mann J.F., Gerstein H.C., Yi Q.L., et al. Progression of renal insufficiency in type 2 diabetes with and without microalbuminuria: results of the Heart Outcomes and Prevention Evaluation (HOPE) randomized study // Am. J. Kidney Dis. 2003. Vol. 42. № 5. P. 936-942.
31. Manotham K., Tanaka T., Matsumoto M., et al. Transdifferentiation of cultured tubular cells induced by hypoxia // Kidney Int. 2004. Vol. 65. № 3. P. 871-880.
32. Nakagawa S., Nishihara K., Miyata H., et al. Molecular markers of tubulointerstitial fibrosis and tubular cell damage in patients with chronic kidney disease // PLoS One. 2015. Vol. 10. № 8. e0136994. doi: 10.1371/journal.pone.0136994. eCollection 2015.
33. Peterson R.G, Jackson C.V., Zimmerman K., et al. Characterization of the ZDSD rat: a translational model for the study of metabolic syndrome and type 2 diabetes // J. Diabetes Res. 2015. 2015:487816.
34. Effect of intensive blood-glucose control with metformin on complications in overweight patients with type 2 diabetes (UKPDS 34). UK Prospective Diabetes Study (UKPDS) Group // Lancet. 1998. Vol. 352. No 9131. P. 854-865.
35. Schainuck L., Striker G.E., Cutler R.E., et al. Structural-functional correlations in renal disease: II. The correlations //Hum. Pathol. 1970. Vol. 1. P. 631-641.
36. Sowers K.M, Habibi J., Hayden M.R. Diabetic nephropathy and tubulointerstitial fibrosis in cardiometabolic syndrome and type 2 diabetes mellitus // J. Cardiometab. Syndr. 2007. Vol. 2. № 2. P. 143-148.
37. Takiyama Y., Harumi T., Watanabe J., et al. Tubular injury in a rat model of type 2 diabetes is prevented by metformin a possible role of HIF-1a expression and oxygen metabolism // Diabetes. 2011. Vol. 60. № 3. P. 981-992.
38. Takiyama Y., Haneda M. Hypoxia in diabetic kidneys // Biomed. Res. Int. 2014. 2014:837421. doi: 10.1155/2014/837421.
39. Vallon V., Thomson S.C. Renal function in diabetic disease models: the tubular system in the pathophysiology of the diabetic kidney // Annu. Rev. Physiol. 2012. Vol. 74. P. 351375.
40. Zuurbier C.J., Demirci C., Koeman A., et al. Short-term hyperglycemia increases endothelial glycocalyx permeability and acutely decreases lineal density of capillaries with flowing red blood cells // J. Appl. Physiol. 2005. Vol. 99. P. 1471-1476.
Современные аспекты клиники, диагностики и лечения предиабета | Пырикова
1. Barbarash O.L., Voevoda M.I., Galstyan G.R. Prediabetes as an interdisciplinary problem: definition, risks, approaches to the diagnosis and prevention of type 2 diabetes and cardiovascular complications. Russian Journal of Cardiology. 2019; 24(4): 83-91. doi: 10.15829/1560-4071-2019-4-83-91 [in Russian].
2. Cho N.H., Shaw J.E., Karuranga S. et al. IDF diabetes atlas: global estimates of diabetes prevalence for 2017 and projections for 2045. Diabetes Res Clin Pract. 2018; 138: 271-281.
3. International diabetes federation. Diabetes Atlas 7th edition. [Electronic resource]. URL: https://www.idf.org/elibrary/epidemiology-research/diabetes-atlas/13diabetes-atlasseventh-edition.html. (date of the application: 17.06.2020).
4. Gujral U.P., Mohan V., Pradeepa R. et al. Ethnic variations in diabetes and prediabetes prevalence and the roles of insulin resistance and cell function: the CARRS and NHANES studies. J ClinTransl Endocrinol. 2016; 4: 19-27. doi: 10.1016/j.jcte.2016.02.004.
5. Мenke A., Casagrande S., Geiss L. et al. Prevalence of and trends in diabetes among adults in the United States, 1988–2012. J Am Med Assoc. 2015; 314: 1021-1029. doi: 10.1001/jama.2015.10029.
6. Andes L.J., Cheng Y.J., Rolka D.B. et al. Prevalence of Prediabetes Among Adolescents and Young Adults in the United States, 2005-2016. JAMA Pediatr. 2019:e194498. doi: 10.1001/jamapediatrics.2019.4498.
7. Konnov M.V., Deev A.D. Own and parental predictors of prediabetes in children of individuals with early coronary heart disease. Cardiology. 2017; 57(6): 16-21. doi: 10.18087/cardio.2019.7.10266 [in Russian].
8. Lyu Y.S., Kim S.Y., Bae H.Y. et al. Prevalence and Risk Factors for Undiagnosed Glucose Intolerance Status in Apparently Healthy Young Adults Aged <40 Years: The Korean National Health and Nutrition Examination Survey 2014-2017. Int J Environ Res Public Health. 2019; 16(13). pii: E2393. doi: 10.3390/ijerph26132393.
9. Wang L., Gao P., Zhang M. et al. Prevalence and Ethnic Pattern of Diabetes and Prediabetes in China in 2013. JAMA. 2017; 27:2515-2523. doi: 10.1001/jama.2017.7596.
10. Younes N., Atallah M., Alam R. et al. HbA1c and blood pressure measurements: relation with gender, body mass index, study field and lifestyle in Lebanese students. Endocr Pract. 2019; 25(11): 1101-1108. doi: 10.4158/EP-2019-0163.
11. Fazli G.S., Moineddin R., Bierman A.S. et al. Ethnic differences in prediabetes incidence among immigrants to Canada: a populationbased cohort study. BMC Med. 2019; 17(1): 100. doi: 10.1186/s12916-019-1337-2.
12. Dedov I., Shestakova M., Galstyan G. The prevalence of type 2 diabetes mellitus in the adult population of Russia (NATION study). Diabetes. 2016; 19(2): 104-112. doi:10.1016/j.diabres.2016.02.010 [in Russian].
13. Breyer M.K., Ofenheimer A., Altziebler J. et al. Marked differences in prediabetes and diabetes associated comorbidities between men and women — epidemiological results from a general population-based cohort aged 6-80 years — the LEAD (Lung, hEart, sociAl, boDy) study. Eur J Clin Invest. 2020:e13207. doi: 10.1111/eci.13207.
14. Al Amri T., Bahijri S., Al-Raddadi R. et al. The Association Between Prediabetes and Dyslipidemia Among Attendants of Primary Care Health Centers in Jeddah, Saudi Arabia. Diabetes Metab Syndr Obes. 2019; 12: 2735-2743. doi: 10.2147/DMSO.S233717.
15. Мainous A.G., Tanner R.J., Baker R. et al. Prevalence of prediabetes in England from 2003 to 2011: population-based, cross-sectional study. BMJ Open. 2014; 4:e005002. doi: 10.1136/bmjopen-2014-005002.
16. American Diabetes Association. 2. Classification and Diagnosis of Diabetes: Standards of Medical Care in Diabetes — 2018. Diabetes Care. 2018; 41(Suppl 1):S13-S27. doi: 10.2337/dc18-S002.
17. Standards of specialized diabetes care. Edited by Dedov II, Shestakova MV, Mayorov AY. 8th edition. 2017; 20,1S:1-121. doi: 10.14341/DM20171S8.
18. Нuang Y., Cai X., Mai W. et al. Association between prediabetes and risk of cardiovascular disease and all cause mortality: systematic review and meta-analysis. BMJ. 2016; 355:i5953. doi: 10.1136/bmj.i5953
19. Zhang Z., Monro J., Venn B.J. Development and Evaluation of an Internet-Based Diabetes Nutrition Education Resource. Nutrients. 2019 May 28;11(6). pii: E1217. doi: 10.3390/nu11061217.
20. Nedogoda S.V., Barykina I.N., Salasyuk A.S. Prediabetes: the main causes, symptoms, prevention and treatment. Medicinal Bulletin. 2018; 12, 70(2): 3-13 [in Russian].
21. Lee M., Saver J.L., Hong K.S. et al. Effect of pre-diabetes on future risk of stroke: meta-analysis. Br Med J. 2012; 344:e3564. doi: 10.1136/bmj.e3564.
22. Huo X., Gao L., Guo L. et al. Risk of non-fatal cardiovascular diseases in early-onset versus late-onset type 2 diabetes in China: A crosssectional study. Lancet. Diabetes Endocrinol. 2016; 4: 115-124. doi: 10.1016/S2213-8587(15)00508-2.
23. Hui Y., Wang J., An Y. et al. Premature death and risk of cardiovascular disease in young-onset diabetes: A 23-year follow-up of the Da Qing Diabetes Study. Endocrine. 2019; 65: 46-52. doi: 10.1007/s12020-019-01928-7.
24. Lee G., Kim S.M., Choi S. et al. The effect of change in fasting glucose on the risk of myocardial infarction, stroke, and all-cause mortality: a nationwide cohort study. Cardiovasc Diabetol. 2018; 17: 51. doi: 10.1186/s12933-018-0694-z.
25. Warren B., Pankow J.S., Matsushita K. et al. Comparative prognostic performance of definitions of prediabetes: a prospective cohort analysis of the Atherosclerosis Risk in Communities (ARIC) study. Lancet Diabetes Endocrinol. 2017 Jan; 5(1): 34-42. doi: 10.1016/S2213-8587(16)30321-7.
26. Kristensen S.L., Preiss D., Jhund P.S. et al. Risk Related to Pre-Diabetes Mellitus and Diabetes Mellitus in Heart Failure With Reduced Ejection Fraction: Insights From Prospective Comparison of ARNI With ACEI to Determine Impact on Global Mortality and Morbidity in Heart Failure Trial. Circ Heart Fail. 2016; 9(1). pii: e002560. doi: 10.1161/CIRCHEARTFAILURE.115.002560.
27. Saleem S.M., Jan S.S., Haq I. et al. Identification of risk factors affecting impaired glucose metabolism among the adult population of district Srinagar. Diabetes Metab Syndr. 2019; 13(2): 1047-1051. doi: 10.1016/j.dsx.2019.01.023.
28. Rodriguez-Segade S., Rodriguez J., Camiña F. et al. Prediabetes defined by HbA1c and by fasting glucose: differences in risk factors and prevalence. Acta Diabetol. 2019; 56(9): 1023-1030. doi: 10.1007/s00592-019-01342-5.
29. Cuschieri S., Grech S. Closing the gap — Is type 2 diabetes awareness enough to prevent the growing epidemic? Diabetes Metab Syndr. 2019; 13(3): 1739-1744. doi: 10.1016/j.dsx.2019.03.044.
30. Man REK, Charumathi S., Gan ATL. et al. Cumulative incidence and risk factors of prediabetes and type 2 diabetes in a Singaporean Malay cohort. Diabetes Res Clin Pract. 2017; 127: 163-171. doi: 10.1016/j.diabres.2017.03.007.
31. Ligthart S., van Herpt TTW., Leening MJG. et al. Lifetime risk of developing impaired glucose metabolism and eventual progression from prediabetes to type 2 diabetes: a prospective cohort study. Lancet Diabetes Endocrinol. 2016; 4: 44-51. doi: 10.1016/S2213-8587(15)00362-9.
32. Sánchez E., Betriu À., López-Cano C. et al. ILERVAS project collaborators. Characteristics of atheromatosis in the prediabetes stage: a cross-sectional investigation of the ILERVAS project. Cardiovasc Diabetol. 2019; 18(1): 154. doi: 10.1186/s12933-019-0962-6.
33. Helck A., Bianda N., Canton G. et al. Intra-individual comparison of carotid and femoral atherosclerotic plaque features with in vivo MR plaque imaging. Int J Cardiovasc Imaging. 2015; 31: 1611-1618. doi: 10.1007/s10554-015-0737-4.
34. Altin C., Sade L.E., Gezmis E. et al. Assessment of epicardial adipose tissue and carotid/femoral intima media thickness in insulin resistance. J Cardiol. 2017; 69: 843-850. doi: 10.1016/j.jjcc.2016.08.006.
35. Acar B., Ozeke O., Karakurt M. et al. Association of Prediabetes With Higher Coronary Atherosclerotic Burden Among Patients With First Diagnosed Acute Coronary Syndrome. Angiology. 2019; 70(2): 174-180. doi: 10.1177/0003319718772420.
36. Sumin A.N., Bezdenezhnykh N.A., Bezdenezhnykh A.V. Pre-surgery status and in-hospital complications of coronary bypass grafting in prediabetes and type 2 diabetes patients. Russian Journal of Cardiology. 2018; (5): 40-48. doi: 10.15829/1560-4071-2018-5-40-48 [in Russian].
37. Ferrannini E. Definition of intervention points in prediabetes. Lancet Diabetes Endocrinol. 2014; 2: 667-675. doi: 10.1016/S2213-8587(13)70175-X.
38. Buysschaert M., Medina J.L., Bergman M. et al. Prediabetes and associated disorders. Endocrine. 2015; 48: 371-393. doi: 10.1007/s12020-014-0436-2.
39. Wasserman D.H., Wang T.J., Brown N.J. The vasculature in prediabetes. Circ Res. 2018; 122: 1135-1150. doi: 10.1161/CIRCRESAHA.118.311912.
40. Park G.M., Cho Y.R., Lee S.W. et al. Prediabetes is not a risk factor for subclinical coronary atherosclerosis. Int J Cardiol. 2017; 243: 479-484. doi: 10.1016/j.ijcard.2017.05.073.
41. Reis J.P., Allen N.B., Bancks M.P. et al. Duration of diabetes and prediabetes during adulthood and subclinical atherosclerosis and cardiac dysfunction in middle age: the CARDIA study. Diabetes Care. 2018; 41: 731-738. doi: 10.2337/dc17-2233.
42. Krysiak R., Szkróbka W., Okopień B. Sexual functioning and depressive symptoms in men with various types of prediabetes: a pilot study. Int J Impot Res. 2018; 30(6): 327-334. doi: 10.1038/s41443-018-0050-6.
43. Krysiak R., Drosdzol-Cop A., Skrzypulec-Plinta V. et al. Sexual functioning and depressive symptoms in women with various types of prediabetes — a pilot study. Endokrynol Pol. 2018; 69(2): 175-181. doi: 10.5603/EP.2018.0021.
44. Serlachius A., Elovainio M., Juonala M. et al. The Association Between Social Support, Body Mass Index and Increased Risk of Prediabetes: the Cardiovascular Risk in Young Finns Study. Int J Behav Med. 2017; 24(2): 161-170. doi: 10.1007/s12529-016-9597-0.
45. Hilding A., Shen C., Östenson C.G. Social network and development of prediabetes and type 2 diabetes in middle-aged Swedish women and men. Diabetes Res Clin Pract. 2015; 107(1): 166-177. doi: 10.1016/j.diabres.2014.09.057.
46. 2017 IDF clinical practice recommendations for managing type 2 diabetes in primary care. [Electronic resource]. URL: https://www.idf.org/e-library/guidelines/128-idf-clinical-practice-recommendationsformanaging-type-2-diabetes-in-primary-care.html. (date of the application: 17.06.2020).
47. NICE 2017 Type 2 diabetes: prevention in people at high risk. [Electronic resource]. URL: nice. org.uk/guidance/ph48. (date of the application: 17.06.2020).
48. Diabetes Canada Clinical Practice Guidelines Expert Committee, Ekoe JM, Goldenberg R, Katz P. Screening for Diabetes in Adults. Can J Diabetes. 2018; 42 Suppl 1:S16-S19. doi:10.1016/j.jcjd.2017.10.004.
49. Wang G., Radovick S., Xu X. et al. Strategy for early identification of prediabetes in lean populations: New insight from a prospective Chinese twin cohort of children and young adults. Diabetes Res Clin Pract. 2018; 146: 101-110. doi: 10.1016/j.diabres.2018.10.003.
50. Davis P.J., Liu M., Sherman S. et al. HbA1c, lipid profiles and risk of incident type 2 Diabetes in United States Veterans. PLoS One. 2018 Sep 13; 13(9):e0203484. doi:10.1371/journal.pone.0203484.
51. Vistisen D., Witte D.R., Brunner E.J. et al. Risk of Cardiovascular Disease and Death in Individuals With Prediabetes Defined by Different Criteria: The Whitehall II Study. Diabetes Care. 2018 Apr; 41(4): 899-906. doi:10.2337/dc17-2530.
52. Paprott R., Scheidt-Nave C., Heidemann C. Determinants of Change in Glycemic Status in Individuals with Prediabetes: Results from a Nationwide Cohort Study in Germany. J Diabetes Res. 2018; 2018: 5703652. doi: 10.1155/2018/5703652.
53. Fares S., Said MSM., Ibrahim W. et al. Accuracy of salivary glucose assessment in diagnosis of diabetes and prediabestes. Diabetes Metab Syndr. 2019; 13(2): 1543-1547. doi: 10.1016/j.dsx.2019.03.010.
54. Mahat R.K., Singh N., Rathore V. Association of myeloperoxidase with cardiovascular disease risk factors in prediabetic subjects. Diabetes Metab Syndr. 2019; 13(1): 396-400. doi: 10.1016/j. dsx.2018.10.016.
55. Mahat R.K., Singh N., Rathore V. et al. Cross-sectional correlates of oxidative stress and inflammation with glucose intolerance in prediabetes. Diabetes Metab Syndr. 2019; 13(1): 616-621. doi: 10.1016/j.dsx.2018.11.045.
56. Yoshida N., Miyake T., Yamamoto S. et al. The Serum Creatinine Level Might Be Associated with the Onset of Impaired Fasting Glucose: A Community-based Longitudinal Cohort Health Checkup Study. Intern Med. 2019; 58(4): 505-510. doi: 10.2169/internalmedicine.0760-18.
57. Jiménez-Lucena R., Camargo A., Alcalá-Diaz J.F. et al. A plasma circulating miRNAs profile predicts type 2 diabetes mellitus and prediabetes: from the CORDIOPREV study. Exp Mol Med. 2018; 50(12): 168. doi: 10.1038/s12276-018-0194-y.
58. Al-Hamdan R., Avery A., Salter A. et al. Identification of Education Models to Improve Health Outcomes in Arab Women with Pre-Diabetes. Nutrients. 2019; 11(5). pii: E1113. doi: 10.3390/nu11051113.
59. Li G., Zhang P., Wang J. et al. Cardiovascular mortality, all-cause mortality, and diabetes incidence after lifestyle intervention for people with impaired glucose tolerance in the Da Qing diabetes prevention study: a 23-year follow-up study. Lancet Diabetes Endocrinol. 2014; 2(6): 474-480. doi: 10.1016/S2213-8587(14)70057-9.
60. Saslow L.R., Daubenmier J.J., Moskowitz J.T. et al. Twelve-month outcomes of a randomized trial of a moderate-carbohydrate versus very low-carbohydrate diet in overweight adults with type 2 diabetes mellitus or prediabetes. Nutr Diabetes. 2017; 7(12): 304. doi: 10.1038/s41387-017-0006-9.
61. Sluik D., Brouwer-Brolsma E.M., Berendsen AAM. et al. Protein intake and the incidence of pre-diabetes and diabetes in 4 populationbased studies: the PREVIEW project. Am J Clin Nutr. 2019; 109(5): 1310-1318. doi: 10.1093/ajcn/nqy388.
62. Muscogiuri G., Barrea L., Di Somma C. et al. Patient empowerment and the Mediterranean diet as a possible tool to tackle prediabetes associated with overweight or obesity: a pilot study. Hormones (Athens). 2019; 18(1): 75-84. doi: 10.1007/s42000-018-0090-9.
63. Mirmiran P., Carlström M., Bahadoran Z. et al. Long-term effects of coffee and caffeine intake on the risk of pre-diabetes and type 2 diabetes: Findings from a population with low coffee consumption. Nutr Metab Cardiovasc Dis. 2018; 28(12): 1261-1266. doi: 10.1016/j.numecd.2018.09.001.
64. RezkAllah S.S., Takla M.K. Effects of Different Dosages of Interval Training on Glycemic Control in People With Prediabetes: A Randomized Controlled Trial. Diabetes Spectr. 2019; 32(2): 125-131. doi: 10.2337/ds18-0024.
65. Bock B.C., Dunsiger S.I., Wu W.C. et al. Reduction in HbA1c with Exercise videogames among participants with elevated HbA1c: Secondary analysis of the Wii Heart Fitness trial. Diabetes Res Clin Pract. 2019; 154: 35-42. doi: 10.1016/j.diabres.2019.06.011.
66. Strauss S.M., McCarthy M. Arthritis-Related Limitations Predict Insufficient Physical Activity in Adults With Prediabetes Identified in the NHANES 2011-2014. Diabetes Educ. 2017; 43(2): 163-170. doi: 10.1177/0145721717691849.
67. Sandoval-Rosario M., Nayeri B.M., Rascon A. et al. Prevalence of Arthritis Among Adults with Prediabetes and Arthritis-Specific Barriers to Important Interventions for Prediabetes — United States, 2009-2016. MMWR Morb Mortal Wkly Rep. 2018; 67(44): 1238-1241. doi: 10.15585/mmwr.mm6744a4.
68. Dunbar J.A., Hernan A.L., Janus E.D. on behalf of the Melbourne Diabetes Prevention Study (MDPS) research group, et al. Challenges of diabetes prevention in the real world: results and lessons from the Melbourne Diabetes Prevention Study. BMJ Open Diabetes Res Care. 2015; 3:e000131. doi: 10.1136/bmjdrc-2015-000131.
69. DPPOS. Lancet Diabetes Endocrinol. Published online September 14, 2015. [Electronic resource]. URL: http://dx.doi.org/10.1016/S2213-8587(15)00291-0 (date of the application: 17.06.2020).
70. Garber A.J., Abrahamson M.J., Barzilay J.I. et al. AACE/ACE Comprehensive type 2 diabetes management algorithm 2017. Endocrine Practice. 2017; 23(2): 207-227. doi:10.4158/CS-2018-0535.
71. Goldberg R.B., Temprosa M.G., Mather K.J. et al. Lifestyle and metformin interventions have a durable effect to lower CRP and tPA levels in the Diabetes Prevention Program except in those who develop diabetes. Diabetes Care. 2014; 37(8): 2253-2260. doi: 10.2337/dc13-2471.
72. Mohan M., Al-Talabany S., McKinnie A. et al. Metformin regresses left ventricular hypertrophy in normotensive patients with coronary artery disease without type 2 diabetes mellitus — the met-remodel trial. Heart 2018; 104:A6. doi: 10.1136/heartjnl-2018-BCS.6.
73. Zhou L., Liu H., Wen X. et al. Effects of metformin on blood pressure in nondiabetic patients. J Hypertens. 2017; 35(1): 18-26. doi: 10.1097/HJH.0000000000001119.
74. Goldberg R.B., Aroda V.R., Bluemke D.A. et al. Effect of Long-Term Metformin and Lifestyle in the Diabetes Prevention Program and Its Outcome Study on Coronary Artery Calcium. Circulation. 2017; 136(1): 52-64. doi: 10.1161/CIRCULATIONAHA.116.025483.
75. Ming J., Xu S., Liu C. et al. Effectiveness and safety of bifidobacteria and berberine in people with hyperglycemia: study protocol for a randomized controlled trial. Trials. 2018; 19(1): 72. doi: 10.1186/s13063-018-2438-5.
76. Barthow C., Hood F., McKinlay E. et al. Food 4 Health — He Oranga Kai: Assessing the efficacy, acceptability and economic implications of Lactobacillus rhamnosus HN001 and β-glucan to improve glycated haemoglobin, metabolic health, and general well-being in adults with pre-diabetes: study protocol for a 2 × 2 factorial design, parallel group, placebo-controlled randomized controlled trial, with embedded qualitative study and economic analysis. Trials. 2019; 20(1): 464. doi: 10.1186/s13063-019-3553-7.
77. Atkinson F.S., Villar A., Mulà A. et al. Abscisic Acid Standardized Fig (Ficus carica) Extracts Ameliorate Postprandial Glycemic and Insulinemic Responses in Healthy Adults. Nutrients. 2019; 11(8). pii: E1757. doi: 10.3390/nu11081757.
78. Yoo J.Y., Yum K.S. Effect of Coenzyme Q10 on Insulin Resistance in Korean Patients with Prediabetes: A Pilot Single-Center, Randomized, Double-Blind, Placebo-Controlled Study. Biomed Res Int. 2018; 2018:1613247. eCollection 2018. doi: 10.1155/2018/1613247.
Метформин способен предупреждать развитие полипоза толстой кишки
Новости онкологии
21.04.2016
Метформин способен предупреждать развитие полипоза толстой кишки
Тюляндин Сергей Алексеевич
Заслуженный деятель науки РФ, главный научный сотрудник
ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России,
председатель Российского общества клинической онкологии (RUSSCO),
профессор, доктор медицинских наук,
Москва
Колоректальный рак – одна их наиболее часто диагностируемых опухолей. Известно, что предшествующий полипоз толстой кишки является фактором, повышающим риск развития рака. Не все полипы и аденомы перерождаются в злокачественные опухоли, но большинство случаев колоректального рака возникло из предшествующей аденомы на фоне полипоза толстой кишки. Эндоскопическое удаление полипов приводит к уменьшению заболеваемости раком толстой кишки. Поэтому такой важной представляется профилактика возникновения полипов и последующего рака. Проведены многочисленные исследования по использованию различных агентов для профилактики полипоза и рака толстой кишки, включая нестероидные противовоспалительные препараты (аспирин) и COX-2 ингибиторы. Последние показали свою способность уменьшать частоту возникновения рака толстой кишки, но их прием сочетался с высокой частотой сердечно-сосудистых осложнений.
Метформин – препарат, используемый для лечения сахарного диабета. Метформин уменьшает содержание глюкозы в крови за счет подавления ее образования в печени и повышения потребления мышечной тканью. Поскольку он не стимулирует продукцию инсулина, прием метформина не сопровождается гипогликемическими состояниями. В эпидемиологических исследованиях было показано, что больные сахарным диабетом 2 типа, принимающие метформин, демонстрируют меньшую частоту развития колоректального рака по сравнению с общей популяцией. Поскольку диабет является одним из факторов риска возникновения рака, остается неясным, за счет чего реализуется превентивный эффект метформина: за счет успешного лечения диабета или за счет прямого действия препарата на клетки эпителия толстой кишки. В связи с этим огромный интерес вызывает исследование по оценке способности приема метформина снижать частоту образования полипов в толстой кишке, проведенное в Японии.
Это было многоцентровое рандомизированное, двойное слепое, плацебо контролируемое исследование, в котором пациенты без наличия диабета и с наличием удаленных полипов или аденом толстой кишки рандомизировались в группу плацебо или группу метформина. Пациенты последней группы получали препарат в дозе 250 мг (1 таблетка) ежедневно в течение года. На момент включения в исследование участники не должны были иметь полипы или аденомы. Через год выполнялась колоноскопия с оценкой частоты полипов и аденом и их последующим удалением. Основным критерием эффективности было наличие и число вновь образованных полипов и аденом в группе плацебо и метформина после одного года наблюдения. Вторичными критериями были частота побочных эффектов, концентрация глюкозы и инсулина в крови после утреннего приема пищи, масса тела и индекс массы тела. Статистическая гипотеза строилась на предположении, что прием метформина снизит частоту вновь образованных полипов и аденом на 40%, для чего предполагалось включить по 75 пациентов в каждую группу.
За период 2011-2014 гг. в исследование был включен 151 пациент: в группу метформина – 79 и в группу плацебо – 72. Колоноскопия через один год после включения была проведена у 71 и 62 пациентов соответственно. В группе метформина вновь образованные гиперпластические полипы и аденомы диагностированы у 27 (38%) пациентов, а в группе плацебо – у 32 (51,5%), что соответствует снижению риска на 40% (HR=0,60 p=0,016). При эндоскопии через 1 год было обнаружено 110 полипов: 96 аденом и 14 гиперпластических полипов. В группе метформина было 44 полипа (37 аденом и 7 гиперпластических полипов), в группе плацебо – 66 полипов (59 аденом и 7 гиперпластических полипов). Локализация и гистологическое строение полипов были одинаковыми в обеих группах. Исследователи не выявили ни одного случая рака толстой кишки. Побочные эффекты были отмечены у 15 (11%) пациентов, включая боли в брюшной полости, диарею, кожную сыпь, запоры. Все побочные эффекты имели 1 степень выраженности. Один пациент, получавший плацебо, прекратил прием досрочно в связи с диареей.
Таким образом, это первое исследование, продемонстрировавшее способность метформина предотвращать развитие полипов толстой кишки у пациентов без наличия диабета. Возможно, период наблюдения в один год является слишком коротким для определения истинного превентивного эффекта метформина. Небольшое число больных требует проведения более масштабного проверочного исследования, без которого рекомендовать метформин пациентам с наличием полипоза толстой кишки было бы опрометчиво.
Ключевые слова: рак толстой кишки, полипы толстой кишки, метформин.
Литература:
- Higurashi T, Hosono K, Takahashi H, et al. Metformin for chemoprevention of mechronous colorectal adenoma or polyps in post-polypectomy patients without diabetes: a multicenter double-blind, placebo-controlled, randomized phase 3 trial. Lancet Oncol. 2016, 17: 475-83.
Таблетированные препараты в лечении сахарного диабета II типа
Таблетированные препараты в лечении сахарного диабета II типа
Сахарный диабет (СД) – группа обменных заболеваний, характеризующихся гипергликемией, возникающих в результате нарушения секреции инсулина, его действия или обоих факторов. На сегодняшний день заболеваемость СД катастрофически растет во всех без исключения странах мира, приобретая масштабы всемирной эпидемии. В 2000 г . в мире насчитывалось более 160 млн больных, и предполагается, что к 2010 г . их число превысит 215 млн. В России в 2001 г . было более 2 млн больных СД, из них около 1, 775 млн страдали СД II типа.
В основе СД II типа лежит как наличие резистентности к инсулину, так и нарушение его секреции. СД II типа (прежде всего инсулинорезистентность) является составной частью так называемого метаболического синдрома, представляющего собой висцеральное ожирение, дислипидемию (повышение ТГ, хс-ЛПНП, снижение хс-ЛПВП), артериальную гипертензию. Метаболический синдром и СД II типа, как одно из его проявлений, являются ведущими причинами смертности в развитых странах Европы и Северной Америки. Более того, в 90-е гг. прошлого века смертность от СД II типа неуклонно возрастала. Одной из особенностей СД II типа является длительное малосимптомное течение. На ранних стадиях заболевания гипергликемия способствует как развитию выраженных нарушений секреции инсулина, так и быстрому прогрессированию атеросклероза и поражению нервной системы. Отсутствие клинических симптомов умеренного (до 7-10 ммоль/л и выше) повышения гликемии приводит к низкой обращаемости пациентов в медицинские учреждения, создает иллюзию видимого благополучия. Все это приводит к тому, что на момент выявления СД II типа (обычно случайному) у пациентов уже присутствуют осложнения заболевания в виде нарушения зрения (ретинопатия), почек (микро-, макропротеинурия), поражения сосудов сердца, мозга, нижних конечностей. Вышеуказанные осложнения являются основной причиной смерти и высокой инвалидизации больных СД II типа.
В настоящее время патогенез осложнений СД 2 типа определен в рамках международных многоцентровых проспективных клинических исследований (DECODE, UKPDS, Helsinki Policemen Study, Kumamoto Study и др.) и на лабораторных моделях. В основе развития осложнений СД лежат инсулинорезистентность, компенсаторная гиперинсулинемия и гипергликемия, в первую очередь развивающаяся после приема пищи. Развитие СД II типа претерпевает ряд последовательных этапов, финалом которых является стойкое снижение секреции инсулина (рис.). В этой связи одной из основных задач терапии СД II типа является поддержание не только нормогликемии, но и сохранение резервных возможностей бета-клеток поджелудочной железы (ПЖ). Поскольку нарушения углеводного обмена не являются единственными проявлениями СД, а гипергликемия и инсулинорезистентность приводят к нарушению всех видов обмена веществ, компенсация СД осуществляется в нескольких направлениях.
Первоочередной и важнейшей задачей лечения СД II типа является нормализация гликемии. Крупнейшее проспективное клиническое исследование UKPDS (United Kingdom Prospective Diabetes Study) убедительно показало, что нормализация (снижение) гликемии предупреждает или задерживает развитие всех осложнений СД II типа. Снижение уровня HbA1c на 1% приводит к уменьшению общей смертности на 21, сердечно-сосудистой заболеваемости на 14, нарушений микроциркуляторного русла на 37%. Вместе с этим риск смерти при СД II типа уменьшается на 42 и 63% при снижении HbA1c на 2 и 3% соответственно. Другое крупнейшее исследование – DECODE (Diabetes Epidemiology: Collaborative Analysis of Diagnostic Criteria in Europe) показало, что наличие гликемии после еды на уровне 11 моль/л (10,0 ммоль/л в цельной венозной крови) увеличивает риск сердечно-сосудистой смертности в 2 и более раза вне зависимости от уровня гликемии натощак.
На сегодняшний день в арсенале врача есть все возможности воздействия на механизмы развития гипергликемии при СД II типа.
Питание и физическая нагрузка являются важными компонентами в лечении. Роль диеты и увеличения физической нагрузки доказали свою эффективность в профилактике СД II типа. По данным DPP (Diabetes Prevention Program), активное изменение образа жизни у лиц с нарушением толерантности к глюкозе (НТГ) привело к снижению развития СД II типа на 58%. Вместе с этим на более поздних стадиях СД II типа модификация образа жизни не приводит к полному устранению гипергликемии. Так, в вышеуказанном исследовании UKPDS лишь 6% пациентов на диетотерапии смогли достичь приемлемых показателей HbA1c (7%) за 8-летний период наблюдения. Более того, имеющиеся сегодня эпидемиологические, клинические и лабораторные наблюдения показывают, что достижение целевых показателей гликемии при СД II типа должно начинаться максимально быстро с момента выявления СД II типа. В подавляющем большинстве случаев для этого требуется медикаментозная терапия.
Вся сахароснижающая терапия при СД II типа условно может быть разделена на четыре группы:
- Препараты, оказывающие выраженное действие на устранение инулинорезистентности (метформин, тиазолидиндионы (глитазоны).
- Препараты, преимущественно оказывающие прямое действие на бета-клетки ПЖ (секретогоги), что приводит к усилению секреции инсулина. Препараты данной группы обычно используются для нормализации уровня глюкозы после еды.
- Препараты, уменьшающие поступление углеводов из кишечника в кровь (акарбоза, гуаровая смола и отчасти метформин). Препараты этой группы оказывают действие на гликемию после еды, однако в отличие от секретогогов не вызывают увеличения секреции инсулина.
- Инсулин и инсулиноподобные препараты (аналоги).
Препараты, устраняющие инсулинорезистентность
Наиболее известным, давно использующимся в клинической практике представителем данной группы является метформин, относящийся к группе бигуанидов. В последние несколько лет в арсенале врача появилась новая группа препаратов – тиазолидиндионы.
Бигуаниды. После прекращения использования в клинических целях буформина и фенформина метформин остался единственным препаратом данной группы в лечении СД II типа. Безопасность метформина в сравнении с другими бигуанидами объясняется иной химической структурой, снижающей блокирование переноса электронов через мембраны клеток и уменьшающей риск развития лактатацидоза.
Метформин используется в лечении СД II типа с 1957 г ., в настоящее время накоплен колоссальный клинический опыт и научный материал, связанный с его применением. Основное действие метформина можно определить как антигипергликемическое, а не сахароснижающее. В настоящее время доказано, что препарат снижает продукцию глюкозы клетками печени, увеличивает утилизацию глюкозы периферическими тканями (прежде всего мышцами) и уменьшает гликемию после приема пищи за счет активации анаэробного гликолиза в тонком кишечнике и замедления кишечной абсорбции.
Препарат не влияет на бета-клетки ПЖ, не усиливает секрецию инсулина, следовательно, не вызывает гипогликемии.
Одним из важнейших механизмов развития гипергликемии при СД II типа является повышение продукции глюкозы печенью в ночные и ранние утренние часы, что приводит к повышению уровня глюкозы в крови натощак. Метформин эффективно устраняет этот дефект.
До появления глитазонов бигуаниды являлись основными препаратами, воздействующими на инсулинорезистентность. Основу инсулинорезистентности при СД II типа составляют нарушения механизмов пострецепторного действия инсулина, т.е. уменьшается чувствительность различных органов и тканей к воздействию инсулина. Метформин оказывает влияние на этот процесс, что в свою очередь приводит к снижению периферической инсулинорезистентности, нормализации метаболизма и поглощению глюкозы мышцами, печенью и жировой тканью, предотвращает развитие гипергликемии и поздних осложнений СД II типа.
К другим благоприятным эффектам относят снижение всасывания углеводов в кишечнике, снижение аппетита на фоне приема метформина, что способствует уменьшению массы тела у пациентов с диабетом и ожирением.
Метформин активно влияет на процесс метаболизма жиров, он снижает уровень ТГ (до 30-45%), СЖК (на 10-17%), замедляет процессы липолиза.
Клинические и метаболические действия метформина нашли выраженное подтверждение в период проведения UKPDS и других исследований (табл. 1).
Более того, проводимое исследование DPP по профилактике СД II типа выявило снижение развития заболевания на 31% в группе лиц, получавших метформин в дозе 850 мг/сутки.
Метформин является препаратом выбора при СД II типа у лиц с избыточной массой тела или абдоминальным ожирением. Лечение препаратом начинают с приема 500 мг в ужин или на ночь, максимальная доза может составлять 2,5-3 г/сутки (в несколько приемов). В исследовании UKPDS, проводимом на оригинальном препарате метформина – глюкофаже, было достоверно доказано, что наибольшая эффективность препарата по предотвращению развития осложнений СД II типа достигается на среднесуточной дозе в 2500 мг. В настоящий момент на рынке появляется глюкофаж в дозировке 1000 мг. Это поможет врачам оптимизировать лечение, а пациентам – упростить прием препарата.
В связи с накоплением лактата на фоне приема метформина препарат не рекомендуют назначать при тяжелой сердечно-сосудистой патологии, у лиц с гипоксией любой этиологии и при нарушениях функции печени. Следование этим рекомендациям привело к тому, что в последние годы случаи фатального лактатацидоза не отмечались. Частота лактатацидоза при приеме метформина составляет в среднем 0,03 случая на 1 тыс. пациенто-лет. Все случаи лактатацидоза за последние 10 лет при терапии метформином связаны с нарушением правил приема препарата. Следует помнить, что у пожилых пациентов возможно уменьшение терапевтической дозы препарата в связи со снижением функции почек.
Итак, метформин является препаратом выбора для нормализации гликемии натощак. При отсутствии его эффективности или наличии противопоказаний (гипоксия любой этиологии, болезни печени, беременность) для поддержания гликемии натощак назначаются инсулины средней продолжительности действия на ночь в дозе 0,1-0,15 ЕД/кг с последующей коррекцией. Монотерапию метформином можно с хорошей эффективностью использовать и при незначительном (до 7,5-9,0 ммоль/л) превышении постпрандиальной (2-часовой) гликемии у пациентов при диетотерапии. При больших значениях гликемии целевые показатели, как правило, не достигаются и целесообразно использование препаратов, повышающих секрецию инсулина (секретогогов).
Тиазолидиндионы (глитазоны) – группа препаратов, представляющих собой агонисты гамма-рецепторов, активируемых пролифератором пероксисом (PPAR-гамма). Действие глитазонов основано на активации метаболизма глюкозы и липидов преимущественно в мышечной и жировой ткани, что приводит к повышению активности эндогенного инсулина, т.е. устранению инсулинорезистентности (сенситайзеры инсулина). Препараты данной группы являются наиболее активными в отношении коррекции дислипидемии при СД II типа за счет действия в печени и жировой ткани. На сегодняшний день за счет вышеуказанных свойств глитазоны являются одними из наиболее многообещающих препаратов в лечении СД II типа. Вместе с тем данная группа препаратов имеет очень незначительный период клинических наблюдений (с 1998 г. в США и с 2000 г . в Европе), пока нет ни одного крупномасштабного долговременного законченного проспективного клинического исследования в рамках доказательной медицины, подтвердившего длительный клинический и хороший прогностический эффект. Подавляющее большинство препаратов данной группы используется в странах Северной Америки, их распространенность в Европе не достигает 5% от общего числа.
В России зарегистрированы оба основных представителя данной группы – розиглитазон и пиоглитазон. Оба препарата принимаются, как правило, в первой половине дня однократно (розиглитазон может применяться дважды в день). Препараты практически не выводятся через почки, в связи с чем могут назначаться при нарушенной почечной функции, фармакокинетика стабильна и не требует коррекции дозы у пожилых. Противопоказанием к назначению являются повышенные (в 2,5 и более раз) печеночные трансаминазы.
Препараты, стимулирующие секрецию инсулина
В данную группу препаратов входят производные сульфонилмочевины и глиниды.
Глиниды – группа препаратов, вошедшая в практическое здравоохранение с середины 90-х гг. В нашей стране зарегистрировано два препарата – репаглинид (производное бензоевой кислоты) и натеглинид (производное D-фенилаланина). По своим фармакокинетическим свойствам оба препарата сходны, их отличает быстрое и обратимое взаимодействие с рецептором сульфонилмочевины. Это приводит к быстрому и недлительному эффекту, имитирующему первую фазу секреции инсулина при приеме пищи. Особенности фармакокинетики требуют назначения препаратов данной группы перед основными приемами пищи за 5-10 мин. При приеме препарата во время еды снижается скорость его всасывания, что проявляется более слабым гипогликемизирующим эффектом.
Производные сульфонилмочевины применяются в лечении СД II типа с конца 50-х гг., в настоящее время используются препараты 2-го поколения.
Препараты, входящие в данную группу, имеют разную аффинность к рецептору, различное время действия. После клонирования АТФ-зависимых К+-каналов в середине 90-х гг. прошлого века активно обсуждается вопрос о селективности ряда препаратов данной группы в отношении бета-клеток ПЖ. Время взаимодействия с рецептором, селективность определяют их фармакокинетику.
По основным свойствам препараты можно разделить на следующие группы: имеющие суточный спектр действия (глимепирид, гликлазид МВ), низкие риск гипогликемии и кардиотоксический эффект (гликлазид, глимепирид), максимальный гипогликемизирующий эффект (глибенкламид, глимепирид), а также препараты, применение которых возможно при хронической почечной недостаточности (гликвидон, гликлазид).
Различные представители этой группы анализировались с позиций доказательной медицины в рамках крупномасштабных проспективных исследований. Из всех препаратов наибольший опыт накоплен в отношении глибенкламида (табл. 2).
Назначение секретогогов при СД II типа имеет основной целью нормализацию усвоения постабсорбционной глюкозы. В подавляющем большинстве случаев при СД II типа на фоне диетотерапии и применения секретогогов возможно достижение гликемии после еды до 7,5-8,0 ммоль/л. При отсутствии достижения целевых показателей гликемии после еды к лечению можно добавить метформин, тиазолидиндионы или акарбозу. При неэффективности комбинации целесообразно добавление инсулинотерапии.
Больные СД II типа вынуждены получать большое количество медикаметов для достижения целевых показателей лечения, профилактики или лечения поздних осложнений. Прием большого количества лекарственных препаратов приводит к низкой комплаентности больных. Пациенты неохотно выполняют рекомендации, пропускают прием препаратов. Одной из тенденций в лечении таких больных является внедрение на рынок комбинированных препаратов, позволяющих воздействовать на разные звенья патогенеза, например сочетание глибенкламида с метформином. Использование комбинированных препаратов позволяет воздействовать как на гликемию натощак, так и на прандиальную. Интересным представляется тот факт, что комбинированная терапия глибенкламидом и метформином в одном препарате достоверно улучшала эффективность лечения не только по сравнению с монотерапией, но и с раздельным приемом этих препаратов в эквивалентных дозах.
Блокаторы альфа-глюкозидазы
Представителем данной группы препаратов в России является акарбоза. Препарат конкурентно ингибирует альфа-глюкозидазу, замедляет всасывание углеводов и снижает уровень гликемии после еды. Доля назначений, приходящихся на акарбозу, в лечении СД II типа и ее эффективность относительно невелики в сравнении с секретогогами. Вместе с тем препарат показал хорошую эффективность в профилактике развития СД II типа у лиц с НТГ. Назначение акарбозы пациентам с НТГ за 3 года снизило риск развития СД II типа на 25%, также почти у 1/3 пациентов нормализовалась толератность к углеводам (STOP-NIDDM Trial).
Суммируя вышеизложенное, следует отметить, что в арсенале практического врача сегодня есть все возможности эффективно воздействовать на гипергликемию при СД II типа; лечение следует начинать максимально быстро для достижения целевых показателей как по углеводному обмену (HbA1c-гликемия), так и АД и липидному спектру. Только комбинированное воздействие на механизмы развития осложнений СД II типа позволит улучшить прогноз пациентов, снизить смертность и осложнения.
Инсулин и препараты сульфонилмочевины, назначаемые в качестве препаратов второй линии для лечения сахарного диабета 2 типа, ассоциируются с бóльшим риском сердечно-сосудистых осложнений по сравнению с более новыми сахароснижающими препаратами
В качестве препарата первой линии при лечении сахарного диабета 2 типа рекомендуется использовать метформин. Выбор препарата второй линии может повлиять на риск развития сердечно-сосудистых осложнений.
В журнале JAMA Network Open опубликованы результаты крупного когортного исследования (N=132737), посвященного оценке риска развития сердечно-сосудистых осложнений у пациентов в реальной клинической практике, получающих разные сахароснижающие препараты в качестве терапии второй линии. Препаратом первой линии в большинстве случаев был метформин. В качестве препарата второй линии в 47.6% случаев назначались препараты сульфонилмочевины, 21.8% — ингибиторы DPP-4, 12.2% — базальный инсулин, 8.6% — агонисты глюкагоноподобного пептида — 1, 5.6% — тиазолидиндионы, 4.3% — ингибиторы натрийзависимого переносчика глюкозы типа 2.
В качестве препаратов сравнения были выбраны тиазолидиндионы, поскольку ранее было показано, что они обладают нейтральным эффектом на риск сердечно-сосудистых осложнений.
В исследование включались пациенты с 2011 по 2016гг. За время наблюдения во всей когорте пациентов было зарегистрировано 3480 событий, удовлетворяющих критериям комбинированной конечной точки (развитие ИБС, инсульта, атеросклеротической болезни периферических артерий, госпитализации в связи с декомпенсацией НК).
В сравнении с тиазолидиндионами, частота сердечно-сосудистых осложнений была достоверно выше у пациентов, получающих препараты сульфонилмочевины (ОШ 1.36; 95% ДИ 1.23-1.49) и базальный инсулин (ОШ 2.03; 95% ДИ 1.81-2.27). Возможными общими механизмами неблагоприятного влияния этих препаратов является развитие гиперинсулинемии, нарастание массы тела, эпизоды гипогликемии.
Остальные препараты (в том числе, ингибиторы ГПП-1 и ингибиторы натрийзависимого переносчика глюкозы типа 2) не продемонстрировали протективного эффекта в отношении ССО при сравнении с тиазолидиндионами. Напомним, что прямого сравнения между новыми классами сахароснижающих препаратов с точки зрения развития ССО в рамках рандомизированных клинических исследований не проводилось.
По материалам:
O’Brien MJ, Karam SL, Wallia A, et al. Association of Second-line Antidiabetic Medications With Cardiovascular Events Among Insured Adults With Type 2 Diabetes. JAMA Netw Open. 2018;1(8):e186125. doi:10.1001/jamanetworkopen.2018.6125
Источник
Текст: к.м.н. Шахматова О.О.
Management and Who’s Risk
ИСТОЧНИКИ:
Diabetologia : «Метформин: исторический обзор», «Метформин и желудочно-кишечный тракт», «Метформин для профилактики диабета: выводы, полученные в результате исследования результатов Программы профилактики диабета / Программы профилактики диабета. . »
Уход за диабетом : «Стандарты медицинской помощи при диабете — 2019», «Долгосрочная безопасность, переносимость и потеря веса, связанные с метформином, в исследовании результатов программы профилактики диабета.»
Cell Reports :« Гиперглюкагонемия снижает влияние метформина на выработку глюкозы при предиабете ».
Клиника Мэйо: новый взгляд на метформин.
Американская диабетическая ассоциация: какие у меня варианты?
Канадский журнал диабета : «Влияние существующих и появляющихся сахароснижающих препаратов на массу тела при диабете 2 типа».
Frontiers in Physiology : «Молекулярные механизмы метформина для лечения диабета и рака.«
Экспертный обзор гастроэнтерологии и гепатологии : новые взгляды на антидиабетическое действие метформина: от печени до кишечника».
Aging Research Reviews : «Плейотропные эффекты метформина: формирование микробиома для управления диабетом 2 типа и замедления старения».
Медицинские гипотезы : «Метформин оказывает эффект против ожирения за счет модуляции кишечного микробиома у предиабетиков: гипотеза».
Журнал клинических исследований : «Роль AMP-активированной протеинкиназы в механизме действия метформина.
Медицина : «Генетические полиморфизмы переносчика органических катионов 1 (OCT1) и ответы на терапию метформином у лиц с диабетом 2 типа: систематический обзор».
Национальная медицинская библиотека: DailyMed: глюкофаг (метформин гидрохлорид), метформина гидрохлорид с расширенным высвобождением.
Journal of Diabetes & Metabolic Disorders : «Дефицит витамина B12 у пациентов с сахарным диабетом: оправдан ли рутинный скрининг и прием добавок?»
Диабет и метаболический синдром : «Наблюдательное исследование уровней витамина b12 и профиля периферической нейропатии у пациентов с сахарным диабетом, получающих терапию метформином.»
Диабет и метаболизм :« Связь между метформином и дефицитом витамина B12 у пациентов с диабетом 2 типа: систематический обзор и метаанализ ».
PLoS One : «Связь приема метформина с дефицитом витамина B12 и периферической невропатией у саудовских людей с сахарным диабетом 2 типа».
Национальный институт диабета, болезней органов пищеварения и почек: «Периферическая невропатия».
Национальные институты здравоохранения: «Витамин B12.»
Диабет, ожирение и метаболизм :« Метформин-ассоциированный лактоацидоз (МАЛА): движение к новой парадигме ».
Метаболизм : «Метформин-ассоциированный лактоацидоз: современные взгляды на причины и риск».
Американский колледж кардиологов: «Метформин».
UpToDate: «Метформин в лечении взрослых с сахарным диабетом 2 типа».
Уход за диабетом : «Метформин, сульфонилмочевины или другие противодиабетические препараты и риск молочнокислого ацидоза или гипогликемии», «Стандарты медицинской помощи при диабете — 2017», «Количественная оценка влияния лечения и доз метформина на гликемический контроль. .«
Национальная служба здравоохранения (Великобритания):« Метформин ».
FDA: «Информация о метформине», «FDA пересматривает предупреждения относительно использования лекарственного средства от диабета метформина у некоторых пациентов с нарушенной функцией почек».
Центр диабета Джослина: «Сводная таблица оральных лекарств от диабета».
Университет здравоохранения Висконсина: «Метформин».
Medscape: «Использование метформина связано с усилением деменции, риском болезни Паркинсона у пациентов с диабетом».
Побочные эффекты и взаимодействия метформина, и как их избежать
Метформин — это антидиабетический препарат (технически классифицируемый как бигуанид), который врачи обычно назначают для лечения диабета 2 типа и преддиабета.Он помогает контролировать уровень глюкозы в крови и восстанавливать реакцию организма на инсулин. Метформин также может лечить синдром поликистозных яичников (СПКЯ). Популярные торговые марки метформина включают Glucophage, Fortamet, Glumetza и Riomet.
И диабет 2 типа, и СПКЯ являются распространенными заболеваниями, каждый год в США регистрируется более 200 000 новых случаев. Согласно уведомлению общественного здравоохранения CDC, миллионы взрослых подвержены риску развития диабета 2 типа.
Если вам поставили какой-либо диагноз, скорее всего, метформин — это вариант лечения для вас.Информация о побочных эффектах, предупреждениях и взаимодействиях метформина является полезным первым шагом к лучшему пониманию препарата.
Что такое метформин?
Метформин чаще всего назначают людям с диабетом 2 типа. Диабет 2 типа вызван инсулинорезистентностью или пониженной чувствительностью к инсулину, что означает, что организм не реагирует на инсулин должным образом. Люди с диабетом 2 типа или преддиабетом страдают гипергликемией (высоким уровнем сахара в крови). Метформин работает, замедляя высвобождение глюкозы из печени и замедляя абсорбцию глюкозы организмом, что помогает снизить уровень сахара в крови.Также считается, что метформин повышает чувствительность к инсулину, что помогает снизить уровень глюкозы.
Метформин также может быть прописан не по назначению для лечения синдрома поликистозных яичников (СПКЯ), состояния, которое может вызвать повышенный уровень инсулина, что увеличивает риск диабета. Это лекарство помогает нормализовать уровень инсулина и может улучшить фертильность.
Общие побочные эффекты метформина
Узнать о потенциальных побочных эффектах метформина так же важно, как и узнать о его преимуществах.Как и с любым лекарством, всегда есть возможные риски. Вот некоторые из наиболее распространенных побочных эффектов метформина:
- Диарея
- Тошнота
- Расстройство желудка
- Металлический привкус во рту
- Рвота
- Метеоризм
- Похудание
- Потеря аппетита
- Изжога
- Вздутие живота
- Кашель
- Сонливость
- Запор
- Головная боль
- Болезненное или затрудненное мочеиспускание
- Астения
- Пониженный уровень витамина B12
Метформин вызывает потерю веса?
Метформин часто беспокоит то, что он вызывает потерю веса.Хотя он может вызвать потерю веса, изменяя способ накопления жира в организме, это не означает, что все, кто принимает препарат, похудеют или что вам следует использовать его для похудения.
Как долго длятся побочные эффекты метформина?
Побочные эффекты могут начаться, когда вы впервые начнете принимать метформин. У некоторых людей побочные эффекты проходят вскоре после того, как их организм привыкает к лекарствам. Для других побочные эффекты могут сохраняться или ухудшаться. Большинство людей принимают метформин в течение длительных периодов времени, поэтому, если побочные эффекты не исчезнут, они потенциально могут вызвать долгосрочный ущерб.Некоторые побочные эффекты метформина могут остаться незамеченными, поэтому необходимы регулярные осмотры.
Серьезные побочные эффекты метформина
Метформин связан с некоторыми серьезными долгосрочными побочными эффектами. Некоторые серьезные побочные эффекты, вызываемые метформином, опасны и требуют немедленной медицинской помощи. Если вы испытываете что-либо из следующего, немедленно обратитесь к врачу:
- Усталость
- Необычная сонливость
- Проблемы с дыханием
- Медленный или нерегулярный пульс
- Дремота или головокружение
Прием метформина в течение длительного времени может вызвать долгосрочные побочные эффекты.Метформин может влиять на способность организма усваивать витамин B12 и вызывать дефицит витамина B12. Людям, принимающим метформин, часто необходимо регулярно сдавать анализы крови для проверки уровня витамина B12.
Метформин, хотя и встречается редко, может вызывать аллергические реакции. Признаки аллергической реакции включают затрудненное дыхание, отек лица или рук и кожную сыпь. Вам следует немедленно обратиться за медицинской помощью, если вы считаете, что испытываете аллергическую реакцию.
Лактоацидоз
Прием метформина может вызвать серьезное заболевание, называемое лактоацидозом, которое представляет собой накопление молочной кислоты в кровотоке.Лактоацидоз может вызывать серьезные побочные эффекты и почти всегда требует госпитализации. Употребление чрезмерного количества алкоголя во время приема метформина может значительно увеличить риск развития лактоацидоза. Признаки лактоацидоза включают:
- Головокружение или дурноту
- Мышечные боли
- Сильная слабость или усталость
- Проблемы с дыханием
- Быстрый или медленный пульс
- Промывание кожи
- Пониженный аппетит
- Сильная боль в животе
Если вы испытываете серьезные побочные эффекты от приема метформина, лучше немедленно позвонить своему врачу.Он посоветует, что делать дальше, и может посоветовать прекратить прием метформина.
Предупреждения о метформине
Метформин не подходит для людей с диабетом 1 типа. Обычно это считается приемлемым для детей и взрослых с диабетом 2 типа или преддиабетом, если это одобряет врач, но дозировки могут варьироваться. Взрослым старше 80 лет метформин назначают с осторожностью в индивидуальном порядке.
Люди с определенными заболеваниями имеют повышенный риск возникновения побочных эффектов от приема метформина.Людям с застойной сердечной недостаточностью, нарушением функции почек, плохой функцией печени или диабетическим кетоацидозом не следует принимать метформин.
Людям с проблемами крови, с проблемами почек, с заболеваниями почек, с заболеваниями печени или с проблемами дыхания следует с осторожностью принимать метформин. Наличие любого из этих состояний и прием метформина могут снизить эффективность метформина или вызвать дополнительные осложнения для здоровья, такие как лактоацидоз. Это состояние вызывает накопление молочной кислоты в крови и может быть смертельным.
Некоторые исследования показывают, что метформин может иметь факторы риска, выходящие за рамки обычных побочных эффектов. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) изучает, содержит ли метформин канцерогены, и исследование 2018 года показывает, что метформин может снизить некоторые положительные преимущества аэробных упражнений для пожилых людей.
Между тем, некоторые мифы о метформине были развенчаны. Некоторые предположили, что метформин вызывает деменцию, но исследование, опубликованное в феврале 2019 года, показало, что «использование метформина связано со снижением риска деменции.”
Хотя метформин не работает для некоторых людей, эти предупреждения не должны отрицать того факта, что он по-прежнему помогает многим людям во всем мире управлять своим состоянием здоровья.
Метформин взаимодействия
Некоторые лекарства могут снизить эффективность метформина или усугубить побочные эффекты.
Например, по данным Центра обучения диабету Калифорнийского университета, прием метформина с таблетками, высвобождающими инсулин, или инсулином может вызвать гипогликемию (низкий уровень сахара в крови).Многим людям, принимающим метформин, необходимо внимательно следить за уровнем в крови. Признаки гипогликемии включают головокружение, дрожь, спутанность сознания, усталость и обмороки.
«Метформин может взаимодействовать с другими лекарствами, включая мочегонные препараты, стероидные препараты, некоторые препараты для щитовидной железы, оральные контрацептивы и препараты, блокирующие кальциевые каналы, такие как нифедипин», — говорит Чираг Шах, доктор медицины и соучредитель Push Health, онлайн-платформы здравоохранения. . «В связи с широким спектром лекарственных взаимодействий, перед назначением метформина важно пересмотреть текущие лекарства пациента.”
Составьте список всех добавок и рецептурных препаратов, которые вы принимаете, и поделитесь им со своим врачом, чтобы избежать побочных эффектов, которые могут возникнуть при приеме метформина с другими препаратами.
Следующие препараты могут отрицательно взаимодействовать с метформином:
- Хинолоновые антибиотики
- Тиазидные диуретики
- Верапамил
- Лекарства, вводимые перед МРТ, рентгеном или компьютерной томографией
- Этанол
- Нестероидные противовоспалительные средства (НПВП)
- Стероидные препараты
- Препараты для щитовидной железы
Врач или другой медицинский работник может дать вам полный список лекарств, которые отрицательно взаимодействуют с метформином.
Как избежать побочных эффектов метформина
1. Принимайте постоянные дозы
Лучше всего следовать инструкциям производителя о том, как использовать препарат, чтобы снизить вероятность возникновения побочных эффектов метформина. Большинство пациентов принимают метформин каждые 12 часов. Последовательный прием соответствующей дозы в нужное время может помочь уменьшить побочные эффекты.
Стандартная дозировка метформина для взрослых составляет 1000 мг два раза в день во время еды. Прием метформина с пищей может помочь устранить или уменьшить побочные эффекты, связанные с желудком.Пропуск или пропуск дозы метформина может усугубить побочные эффекты.
2. Внесите изменения в образ жизни и диету
Изменение образа жизни — еще один ключевой компонент лечения диабета 2 типа или преддиабета. Регулярные упражнения могут положительно повлиять на артериальное давление и уровень глюкозы в крови у людей с диабетом 2 типа. Некоторые продукты, такие как рафинированный сахар, алкоголь и гидрогенизированные масла, могут вызывать повышенный уровень сахара в крови, поэтому их исключение может быть очень полезным.
Диета и физические упражнения не могут служить полноценной альтернативой метформину, но они все же могут улучшить качество жизни.Лучший способ снизить вероятность возникновения побочных эффектов при приеме метформина — это поговорить с врачом.
3. Искать альтернативы
Существуют альтернативные варианты метформина для людей с заболеваниями, которые не позволяют им принимать метформин, или для тех, кто не может принимать метформин из-за его побочных эффектов. Пациентам с диабетом 2 типа могут быть полезны ингибиторы SGLT2, препараты GLP1, ингибиторы альфа-глюкозидазы, глиптины или пиоглитазон.
Поговорите со своим врачом — лучший способ узнать о других лекарствах, которые могут вам подойти, исходя из вашей истории болезни и индивидуальных симптомов.
Сравнение метформина и метформина ER
Метформин и метформин расширенного высвобождения (ER) — это, по сути, одно и то же лекарство, но пациенты не принимают метформин ER так часто. ER означает расширенный выпуск, что означает, что организм поглощает метформин ER медленнее, чем обычный метформин. Оба препарата помогают людям с диабетом 2 типа и преддиабетом контролировать уровень сахара в крови.
Метформин, иногда называемый метформином немедленного высвобождения (IR), часто принимают два раза в день. Метформин ER принимают реже, обычно один раз в день.Стандартная дозировка метформина ER для взрослых с диабетом 2 типа составляет 1000–2000 мг. Некоторым людям может потребоваться прием метформина ER два раза в день. Медицинский работник может определить это в каждом конкретном случае.
Метформин ER — это общая версия торговой марки Glucophage XR. Пациенты, у которых расстройство желудка при приеме обычного метформина, могут перейти на метформин ER, который лучше переносится. Примите метформин ER в соответствии с указаниями врача. Некоторые врачи могут рекомендовать прием метформина ER один раз утром во время завтрака или вечером во время ужина.Прием метформина ER с пищей может помочь снизить риск побочных эффектов, таких как расстройство желудка и диарея.
Метформин против побочных эффектов метформина ER
Подобно метформину побочные эффекты метформина ER могут включать:
- Тошнота
- Диарея
- Изжога
- Головная боль
- Металлический привкус во рту
- Усталость
- Легкомысленность
- Мышечные боли
- Медленное или нерегулярное сердцебиение
Подобно метформину, метформин ER может увеличивать риск лактоацидоза.
Медицинский работник может дать полный список побочных эффектов. Лучший способ узнать больше о побочных эффектах метформина и метформина ER — это поговорить со своим врачом.
Побочные эффекты метформина
Сахарный диабет 2 типа (СД2) необходимо лечить с помощью лекарств и вести здоровый образ жизни для стабилизации уровня глюкозы в крови. Метформин представляет собой пероральный бигуанид и препарат первого выбора при сахарном диабете 2 типа.Он снижает уровень глюкозы в крови за счет подавления выработки глюкозы в печени. Метформин помогает организму восстановить способность реагировать на инсулин и, как правило, является безопасным и эффективным средством лечения. Помимо контроля гликемии, метформин также улучшает инсулинорезистентность, дисфункцию эндотелия, окислительный стресс, гемостаз и липидный профиль.
Метформин может помочь избежать осложнений в результате высокого уровня глюкозы в крови, таких как диабетическая нефропатия, нейропатия и ретинопатия.Метформин может отрицательно влиять на функцию почек у пациентов с СД2 и может развиваться хроническая болезнь почек. Серьезный побочный эффект лактоацидоза встречается редко, но может развиться из-за накопления метформина. В этом обзоре обсуждаются возможные побочные эффекты метформина, однако пациенты, принимающие метформин, могут испытывать или не испытывать некоторые или все из них. Метформин следует с осторожностью применять пожилым людям и пациентам с травмами, лихорадкой, хирургическим вмешательством, сердечной недостаточностью, нарушением функции почек или печени. Перед хирургическим вмешательством следует прекратить лечение метформином.
Желудочно-кишечные расстройства; Лактоацидоз, метформин, побочные эффекты, диабет 2 типа
Сахарный диабет связан с различными метаболическими состояниями, и его растущая распространенность во всем мире является поводом для беспокойства. В 2016 году диабет стал причиной 1,6 миллиона смертей, а в 2014 году диабет развился примерно у 8,5% людей в возрасте 18 лет и старше [1]. Высокий уровень глюкозы в крови стал причиной смерти еще 2,2 миллиона человек в 2012 году [1]. Это экономическое бремя во всем мире, поскольку оно вызывает широкий спектр осложнений и является основной причиной как смертности, так и заболеваемости.Такие заболевания, как невропатия, нефропатия и ретинопатия, являются результатом их долгосрочных осложнений [2]. Гормон инсулин вырабатывается поджелудочной железой и регулирует уровень глюкозы в крови. Большинство (90% людей), страдающих диабетом, страдают сахарным диабетом 2 типа (СД2) [3]. СД2 возникает из-за нарушения действия или секреции инсулина или их сочетания и является хроническим и постепенным [4].
При T2DM поджелудочная железа вырабатывает недостаточное количество инсулина или вырабатываемый инсулин не может использоваться эффективно [1].Это вызывает повышенную концентрацию глюкозы в плазме или гипергликемию. Развитию гипергликемии предшествуют годы резистентности к инсулину (ИР) и гиперинсулинемии. Некоторые из симптомов гипергликемии включают полиурию, полидипсию, учащенное дыхание, фруктовый запах изо рта, спутанность сознания и сонливость. Гипергликемия со временем может серьезно повредить нервы, кровеносные сосуды и многие системы организма [1]. Следовательно, поддержание гликемического контроля имеет важное значение при лечении СД2 [5]. Некоторые люди с СД2 могут достичь целевого уровня сахара в крови только с помощью вмешательства в образ жизни, однако другим могут потребоваться лекарства, чтобы контролировать свой уровень глюкозы в крови.
Самым распространенным лекарством, используемым для лечения СД2, является метформин (диметилбигуанид), пероральное антигипергликемическое средство [6]. Это фармакологическое лечение первой линии при СД2 [7]. Примерно 380 миллионов пациентов во всем мире страдают диабетом, из которых метформин употребляют около 120 миллионов [8, 9]. Метформин является производным гуанидина, содержащегося в Galega officinalis [10], и уже более сорока лет он используется в клинических условиях [4]. Метформин получил одобрение Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) в 1994 году как препарат, назначаемый для лечения диабета.Американские и европейские руководства рекомендуют терапию метформином при СД2 в дополнение к изменению образа жизни [11]. Профиль безопасности метформина хороший, и он рекомендуется из-за его низкой стоимости и связанной с этим безопасности [12].
Метформин является бигуанидом и подавляет выработку глюкозы в печени, снижая таким образом уровень глюкозы в крови [11]. У взрослых с СД2 метформин используется либо отдельно, либо вместе с инсулином или другими противодиабетическими препаратами и модификациями образа жизни. Систематический обзор показал, что метформин снижает уровень глюкозы в крови после приема пищи, а также снижает уровень глюкозы в плазме натощак (ГПН) у пациентов с СД2 [13].Метформин быстро всасывается из тонкого кишечника, и самые высокие уровни концентрации в плазме наблюдаются примерно через два часа [14, 15]. Было обнаружено, что введение метформина за 30 минут до еды лучше всего снижает постпрандиальную гипергликемию [16]. Метформин улучшает углеводный и липидный обмен и значительно снижает гликемические показатели [17]. Мета-анализ показал, что метформин снижает уровень ГПН на 2,8 ммоль / л — 3,9 ммоль / л (50 мг / дл — 70 мг / дл) и уровень гликированного гемоглобина (HbA1c) примерно на 1.5% — 2,0% [15]. Он подавляет глюконеогенез, подавляет гликогенолиз и стимулирует гликолиз [18]. Метформин также снижает концентрацию свободных жирных кислот в сыворотке [19], улучшает ИР и корректирует дислипидемию.
Метформин может оказывать защитное действие на клетки островков поджелудочной железы [20]. Программа профилактики диабета (DPP) [21] обнаружила, что в течение 3 лет метформин уменьшал прогрессирование диабета на 31% у взрослых с нарушенной толерантностью к глюкозе (IGT), а также улучшал функционирование бета-клеток [21, 22].Однако метформин работает только при наличии эндогенного инсулина и, следовательно, действует, когда еще остаются некоторые функциональные островковые клетки поджелудочной железы [23]. Секреция инсулина не стимулируется непосредственно метформином [24], однако чувствительность к инсулину улучшается метформином, поскольку он увеличивает поглощение глюкозы периферическими тканями и использование глюкозы в мышечных тканях [23,25]. В результате количество лактата в энтероцитах увеличивается [26]. Было обнаружено, что действие метформина меньше на дипептидилпептидазу-4, но уровни глюкагоноподобного пептида-1 (GLP-1) в плазме повышаются им [26].
Метформин (родовое название) доступен в различных формах, таких как таблетки, капсулы, пероральные суспензии, пероральные растворы или таблетки с модифицированным высвобождением [23]. Метформин доступен под различными торговыми марками, включая диагемет, боламин, глюкофаг, метабет, глюциент [27], глюкофагXR, фортамет и глюмеца [28]. Riomet — торговая марка жидкого метформина [27]. Таблетка с немедленным высвобождением доступна под торговой маркой глюкофага. Метформин для приема внутрь — это лекарственные средства с немедленным высвобождением или лекарственные средства с модифицированным высвобождением [21].Вначале доза метформина с немедленным высвобождением составляет 500 мг два раза в день перорально или 850 мг один раз в день перорально, поддерживающая доза составляет 2000 мг в день в разделенных дозах, а максимальная доза составляет 2550 мг в день [29]. Для пролонгированного высвобождения начальная доза составляет от 500 до 1000 мг перорально один раз в день, а максимальная доза составляет 2000 мг [29]. Взрослые пациенты, которые получают метформин стандартного высвобождения в дозе до 2 г в день, могут начинать с той же суточной дозы метформина с модифицированным высвобождением, однако это не подходит, если доза для таблеток стандартного высвобождения превышает 2 г в день [23 ].
Метформин не имеет лицензии на применение у детей младше 10 лет [23]. Для детей (только для специального применения) в возрасте от 10 до 17 лет сначала рекомендуется принимать внутрь 500 мг лекарств немедленного действия один раз в день. Дозу лекарственного средства с модифицированным высвобождением можно увеличить до 2 г в день перорально, что при необходимости является максимальным значением [23]. Взрослым сначала рекомендуется 500 мг один раз в день, при необходимости можно увеличить до 2 г один раз в день [23], за исключением синдрома поликистозных яичников (СПКЯ).Хотя метформин не имеет официальной лицензии на лечение СПКЯ, он иногда используется для лечения этого состояния [23,27]. При СПКЯ метформин можно вводить перорально с помощью лекарств с немедленным высвобождением, затем 1,5–1,7 г в день в два-три приема [23]. У пациенток с СПКЯ в пременопаузе и ановуляторной стадии метформин может вызывать овуляцию. Однако максимальная дозировка метформина с немедленным высвобождением в публикациях и в Британском национальном формуляре (BNF) отличается от лицензии на продукт, поскольку могут существовать различия в лицензиях на разные составы, содержащие одно и то же лекарство [23].
Метформин оказался безопасным и эффективным и обычно хорошо переносится. Однако многие пациенты не переносят лекарство из-за его побочных эффектов. Следовательно, оптимальное использование метформина требует четкого понимания его побочных эффектов и безопасности [30]. Таблетки для приема внутрь метформина могут вызывать побочные эффекты, которые могут быть легкими или серьезными [23]. Обычные побочные эффекты включают тошноту, вздутие живота, метеоризм, рвоту, диарею / запор, изжогу, головную боль, возбуждение, озноб, головокружение, усталость, спазмы или боль в животе, потерю аппетита, астению, миалгию, инфекцию верхних дыхательных путей и другие изменения. или металлический привкус [23,27].Однако данные показывают, что симптомы желудочно-кишечного тракта (ЖКТ) [11,31] и симптомы пищеварительного тракта [32] в основном наблюдаются при лечении метформином. Было подтверждено, что симптомы со стороны желудочно-кишечного тракта были больше у участников, принимавших метформин, по сравнению с участниками, принимавшими плацебо (в среднем 28% против 16%, p = 0,01) [33]. Причина этого может быть в том, что микробиом кишечника изменяется под действием метформина [26]. Одним из основных участков действия метформина является печень, однако текущие исследования показывают, что метформин также влияет на кишечник из-за связи с осью кишечник-мозг-печень.Содержание желчных кислот в кишечнике увеличивается с метформином, что может повлиять на микробиом и, как следствие, нарушить секрецию GLP-1, уровень холестерина и консистенцию стула [26].
В одном исследовании сообщалось, что побочные эффекты со стороны желудочно-кишечного тракта были связаны с метформином примерно у 25% пациентов, и около 5% пациентов не могли переносить метформин [34]. Напротив, другое исследование показало, что, хотя симптомы со стороны желудочно-кишечного тракта наблюдались примерно у 20-30% пациентов, принимавших метформин, менее 5% пациентов нуждались в прекращении приема препарата [4].Побочные эффекты со стороны желудочно-кишечного тракта обычно наблюдаются при приеме метформина вначале, а у некоторых пациентов они могут продолжаться, особенно у тех, кто принимает очень высокие дозы [23]. Однако было обнаружено, что со временем симптомы со стороны ЖКТ уменьшаются [35]. Поглощение метформина во многом зависит от дозировки и транспортера [26]. Некоторые исследования утверждают, что поглощение метформина и генетическая наследственность и вариации переносчиков могут влиять на его переносимость [36]. Переносимость можно улучшить, медленно увеличивая дозу [23].Если взрослый с СД2 испытывает побочные эффекты со стороны желудочно-кишечного тракта при стандартном начальном лечении, ему следует предложить метформин стандартного высвобождения в качестве начального лекарственного лечения с постоянным увеличением дозы в течение нескольких недель [7].
В отличие от сульфонилмочевины, гипогликемия обычно не вызывается метформином [6]. Однако, если метформин используется вместе с инсулином или другими антидиабетическими препаратами, может возникнуть низкий уровень глюкозы в крови. Кроме того, гипогликемия может возникать при повышенных физических нагрузках, употреблении алкоголя или недостаточном потреблении пищи.Некоторые из симптомов гипогликемии включают голод, сердцебиение, дрожь, беспокойство, потоотделение, нервозность, раздражительность, капризность, головокружение, головную боль и помутнение зрения. Метформин может ухудшать потребление / всасывание кальция [35], вызывать потерю веса или астению [37]. Метформин вызывает редкие побочные эффекты, в том числе гепатит, кожные реакции, такие как сыпь, зуд или покраснение, снижение всасывания витамина B12 или лактоацидоз (ЛА), когда его следует немедленно прекратить [23]. Использование метформина в долгосрочной перспективе было связано с дефицитом витамина B12 и анемией, как сообщалось в Программе профилактики диабета (DPP), а также в исследовании результатов DPP (DPPOS) [35].Риски, связанные с дефицитом витамина B12 из-за метформина, были оценены DPPOS. Они обнаружили, что средний уровень гемоглобина и гематокрита был немного ниже у пациентов, получавших метформин, по сравнению с пациентами, получавшими плацебо [35]. Около 30% людей, принимающих метформин, в долгосрочной перспективе испытывают дефицит витамина B-12 [38]. Следовательно, необходимо периодически контролировать сывороточные концентрации витамина B12 при длительной терапии у пациентов, принимающих метформин. Метформин использовался в течение многих лет, особенно у пациентов с избыточным весом или ожирением с СД2.У этой категории субъектов может быть трудно контролировать уровень глюкозы в крови с помощью нефармакологических методов. Метформин был первым противодиабетическим препаратом, который снизил количество осложнений, связанных с диабетом, и общую смертность у пациентов с СД2, страдающих избыточным весом или ожирением [39]. Улучшение контроля глюкозы за счет метформина достигается без увеличения веса, поскольку метформин нейтрален в весе или обладает эффектом снижения веса [11]. Систематический обзор показал, что лечение метформином вызывает потерю веса [13].Однако, как метформин связан с весом, не очень ясно, и поэтому существуют различные причины и объяснения колебаний веса. Одна из причин может быть связана с побочными эффектами препарата, общими симптомами со стороны желудочно-кишечного тракта, частым расстройством желудка или диареей, которые могут отрицательно повлиять на прием пищи. Другая причина может заключаться в том, что из-за сильного дискомфорта люди уменьшают чувство голода и едят меньше, что приводит к снижению потребления калорий. Однако Федеральное управление по лекарствам (FDA) не одобрило метформин для похудания, и он доступен только по рецепту.
Метформин ассоциирован с редким метаболическим заболеванием, называемым лактоацидозом (ЛА), которое очень опасно, часто со смертельным исходом и опасно для жизни [40,41]. Симптомы LA не очень специфичны, и пациенты могут иметь усталость, вялость, слабость, диарею, рвоту, тошноту, боль в животе, анорексию, посинение или холодную кожу, озноб, мышечные боли, гипотензию, учащенное или затрудненное дыхание, головокружение, гипервентиляцию, тяжелую форму. сонливость, металлический привкус во рту или медленное или нерегулярное сердцебиение [31].Исследования показали, что ЛА возникает из-за значительной гипоперфузии тканей и гипоксии [42,43]. При ЛА концентрация лактата в крови увеличивается (более 45 мг / дл или 5,0 мэкв / л), pH крови снижается (ниже 7,35), а электролиты нарушаются с увеличением разрыва в анионах [13].
Болезнь метформин-ассоциированной ЛА до конца не изучена. Данные свидетельствуют о том, что метформин предотвращает клиренс лактата в печени, останавливая комплекс I дыхательной цепи митохондрий [44].С повышением уровня метформина окислительное фосфорилирование снижается, и аэробный метаболизм превращается в анаэробный метаболизм [45]. Почки обычно выводят метформин, однако метформин может накапливаться при почечной недостаточности. Это приводит к увеличению концентрации метформина и может привести к ЛА [46]. Повышенное производство молочной кислоты также может быть вызвано гемодинамической нестабильностью и / или гипоксией тканей, что может быть связано с тяжелой передозировкой метформина или с какими-либо основными сердечно-сосудистыми или респираторными заболеваниями.ЛА также может быть вызвана недостаточным клиренсом лактата, а не увеличением его производства. При остром метаболическом ацидозе (который включает ЛА и диабетический кетоацидоз) метформин противопоказан [23].
В 1970-х годах в США более ранний бигуанид, известный как фенформин, был исключен из формуляра, поскольку он показал риски, связанные с ЛА [47]. Приблизительно 40–64 случая ЛП были зарегистрированы на 100 000 пациенто-лет, и было обнаружено, что они были связаны с фенформином [4,48].Однако, в отличие от фенформина, метформин наблюдал повышенное окисление глюкозы без каких-либо значительных изменений в продукции лактата натощак в периферических тканях [49]. Более того, в другом исследовании сообщалось, что метформин отличается от фенформина в отношении его молекулярной структуры и фармакокинетики [50]. Кроме того, было обнаружено, что заболеваемость ЛА очень низкой у пациентов, принимающих метформин, в отличие от фенформина [51]. Метформин был снят с рынка США из-за опасений по поводу ЛА, но был повторно введен в продажу в 1995 году после того, как было доказано, что он эффективен и безопасен для снижения уровня глюкозы в крови [30].Однако сообщения об истинной частоте индуцированного метформином ЛА противоречивы. Однако у пользователей метформина общая заболеваемость ЛА, по-видимому, различается в разных исследованиях от примерно трех на сто тысяч человеко-лет до десяти на сто тысяч человеко-лет воздействия [41]. Двухлетний обзор 11 800 участников, принимавших метформин, показал, что только у двух участников развился ЛА (частота: девять пациентов на сто тысяч человеко-лет) [13], в то время как другие исследования пришли к выводу, что использование метформина не имело связи с ЛА [ 39,40,51].Исследование, проведенное в Дании, показало, что пациенты, которые были госпитализированы с острой госпитализацией с LA, имели pH менее 7,35 и уровень лактата ≥2,0 ммоль / л, а отношение шансов после корректировки составляло 0,79 с 95% доверительным интервалом 0,54–1,17 [ 40]. В другом исследовании подчеркивалось, что ЛА обычно возникает из-за передозировки наркотиков, обезвоживания, сердечного приступа или инсульта, чрезмерного употребления алкоголя, застойной сердечной недостаточности, серьезных инфекций, недавней операции, рентгеновских лучей или других механизмов сканирования, которые требуют инъекционного йодсодержащего контрастного препарата и у людей старше 80 лет [31].Метформин имеет противопоказания при различных гипоксических хронических состояниях, которые связаны с ЛП, таких как болезни почек [41,52], болезни печени или легких и болезни сердца [13]. Нарушение функции почек может вызвать накопление метформина. Систематический обзор показал, что уровень лактата не увеличивался значительно у пациентов с ХБП от легкой до умеренной степени, при этом расчетная скорость клубочковой фильтрации (рСКФ) составляла 30 мл / мин на 1,73 м 2 -60 мл / мин на 1,73 м 2 [41]. Однако данные о ЛП при ХБП ограничены.Более того, не проводилось рандомизированных контролируемых исследований применения метформина у людей с нарушением функции почек [41]. Таким образом, остается дискуссионным вопрос о том, повышаются ли риски развития ЛА из-за лечения метформином у пациентов с СД2 по сравнению с другими видами терапии, снижающими уровень глюкозы. Другие утверждают, что большинство случаев LA наблюдается у пациентов с серьезными заболеваниями, такими как почечная недостаточность, которая может вызывать LA, а не метформин [53,54]. Соблюдение безопасной практики назначения лекарств может снизить риск развития ЛА, а также риски могут быть уменьшены, если принять во внимание меры предосторожности и противопоказания, чтобы избежать накопления метформина или лактата в организме [6].Пациенты и лица, осуществляющие уход за ними, должны быть проинформированы о риске ЛП, и следует немедленно обратиться за медицинской помощью при появлении таких симптомов, как одышка, боль в животе, мышечные спазмы, переохлаждение или астения [23]. Крайняя нехватка энергии, мышечная слабость, сильная усталость, медленное сердцебиение, желтая кожа, быстрое / поверхностное дыхание, общее чувство дискомфорта, ощущение холода, булавок и игл, болезненный язык, язвы во рту и нарушение зрения — вот некоторые из предупреждающих знаков. [26]. Пациентам с хронической сердечной недостаточностью или при одновременном применении с метформином других препаратов, которые могут нарушить функцию почек, следует осторожно назначать лечение.Лечение следует прервать, если у пациента наблюдается обезвоживание, и следует избегать приема метформина при состояниях, которые могут вызвать ухудшение функции почек или вызвать гипоксию тканей [23]. При печеночной недостаточности на фоне тканевой гипоксии метформин следует полностью отменить [23].
При СД2 диабетическая нефропатия (ДН) является микрососудистым осложнением [12,55], и накопление метформина из-за почечной недостаточности вызывает опасения. Некоторые пациенты, принимающие метформин, также могут иметь риск повреждения почек.Однако в одном исследовании было обнаружено, что метформин улучшает альбуминурию у пациентов с ДН по сравнению с глибенкламидом [56]. Кроме того, в исследовании на животных было обнаружено, что метформин останавливает потерю подоцитов, вызванную диабетом, предотвращая окислительное повреждение [57]. Однако недавнее исследование показало, что у пациентов, получавших метформин, риск острого повреждения почек не увеличивался при исходной рСКФ по сравнению с пациентами, не принимавшими метформин [58]. Что касается использования метформина, нарушение функции почек является одним из основных противопоказаний.Рекомендации FDA в начале 2016 г. противопоказали использование метформина мужчинам с уровнем креатинина в сыворотке 1,5 мг / дл (133 мкмоль / л) или выше и женщинам с уровнем креатинина в сыворотке 1,4 мг / дл (124 мкмоль / л) или выше [7 , 12]. Однако другие утверждали, что сывороточный креатинин сам по себе не позволяет точно измерить функцию почек у пожилых пациентов или у других пациентов, у которых наблюдается снижение мышечной массы, и поэтому необходимо определять рСКФ [7]. Использование метформина следует прекратить при значении рСКФ менее 60 мл / мин [7].Метформин следует назначать с осторожностью, а дозу следует пересматривать при внезапном ухудшении функции почек и у пациентов с риском рСКФ ниже 45 мл / мин / 1,73 м 2 [7]. Лечение метформином необходимо прекратить, если рСКФ ниже 30 мл / мин / 1,73 м 2 [7,59]. У взрослых со сниженной функцией почек следует избегать приема метформина, если значение рСКФ падает ниже 30 мл / мин / 1,73 м 2 [23]. Для пациентов с СД2, принимающих метформин, значение рСКФ более 30 мл / мин / л.73m 2 отображается в настоящее время [23]. Метформин не следует продолжать у пациентов, которым требуется внутривенное введение йодсодержащего контрастного вещества, или у пациентов, которым необходимо хирургическое вмешательство, до тех пор, пока почечная функция не станет стабильной, с нормальным уровнем креатинина в сыворотке крови и диурезом, без нарушения кровообращения или перегрузки жидкостью [7]. У детей с нарушением функции почек прием метформина следует прекратить, если установлено, что рСКФ ниже 30 мл / мин / 1,73 м 2 [23]. Однако дозы могут быть скорректированы, и у детей с умеренными нарушениями рекомендуется рассмотреть возможность снижения дозы.У взрослых с умеренными нарушениями доза должна быть уменьшена [23]. Параметры пациента следует контролировать ежегодно. Дважды в год необходимо оценивать почечную функцию у пациентов, у которых начинается ухудшение или у которых есть другие факторы риска почечной недостаточности [23].
Пациентам с диагнозом «Хроническая болезнь почек (ХБП)», а также СД2, следует соблюдать осторожность при назначении метформина, поскольку он может снижать функцию почек, и поэтому необходим тщательный мониторинг почечной функции [12].Исследование, проведенное на Тайване, показало, что рСКФ снизилась больше у пациентов с СД2, принимавших метформин не менее 6 месяцев, по сравнению с участниками, которые прекратили прием метформина примерно на сто дней [12]. Ретроспективное когортное исследование показало, что лечение метформином у пациентов с СД2 значительно ухудшало почечную функцию у пациентов с СД2 и умеренной ХБП [12]. Однако это исследование имело некоторые ограничения, потому что, во-первых, нельзя было сделать вывод о причинно-следственной связи по результатам, потому что исследователи не включили рандомизацию, поскольку это не было клиническим испытанием.Во-вторых, все сопутствующие факторы, например, продолжительность СД2 или заболевания печени, не были включены в это одноцентровое исследование. Предыдущее исследование показало, что использование метформина у пациентов с СД2 и поздней стадией ХБП имело значительную связь с повышенным риском общей смертности по сравнению с участниками, которые имели СД2, но не принимали метформин [60]. Это вызывало беспокойство, потому что снижение функции почек у пациентов с умеренной ХБП, также принимавших метформин, могло увеличивать риск развития токсических реакций с метформином.Однако в апреле 2016 г. FDA пересмотрело свои предупреждения относительно лечения метформином у пациентов с нарушением функции почек и пересмотрело измерения почечной недостаточности в соответствии с рСКФ [61]. В пересмотренных рекомендациях указано, что только у пациентов с тяжелой формой ХБП и рСКФ ниже 30 мл / мин / 1,73 м 2 использование метформина полностью противопоказано. Таким образом, лечение метформином разрешено пациентам с ХБП средней степени тяжести, у которых значение рСКФ составляет 30-59 мл / мин / л.73m 2 [61].
Клинически значимые лекарственные взаимодействия с участием метформина встречаются нечасто [62]. Однако некоторые лекарства могут влиять на действие метформина. Концентрация метформина может увеличиваться, если одновременно вводить циметидин, фуросемид или нифедипин [62]. Дозировка должна быть скорректирована, если пациент принимает фуросемид, преднизолон, эстроген, прогестерон, тестостерон, противозачаточные таблетки или другие лекарства от диабета, а уровень глюкозы в крови, возможно, необходимо проверять чаще [26].Некоторые лекарства, выделяемые с секрецией почечных канальцев, такие как морфин, хинин, ранитидин, дигоксин, хинидин, амилорид, прокаинамид, триамтерен, ванкомицин и триметоприм, могут конкурировать с метформином за выведение [62]. Поэтому пациенты, принимающие метформин одновременно с этими препаратами, нуждаются в тщательном наблюдении за какими-либо токсическими реакциями [63].
Было обнаружено, что некоторые препараты, такие как контрастные вещества (йодированные), этанол и иоверсол, серьезно взаимодействуют с метформином, однако все возможные взаимодействия не были включены в этот обзор.Противопоказания включают хроническую сердечную недостаточность, диабетический кетоацидоз (DKA), гиперчувствительность, метаболический ацидоз с комой или без нее, инфаркт миокарда, аномальный клиренс креатинина из-за шока, сепсиса или тяжелой почечной недостаточности. Однако, хотя ИМ является важным событием по сравнению с препаратами сульфонилмочевины, при применении метформина он наблюдается реже. Серьезные аллергические реакции на метформин не очень распространены, однако некоторые присутствующие неактивные ингредиенты могут вызывать аллергические реакции [31]. Также возможна анафилаксия — серьезная аллергическая реакция на метформин [26].
Метформин можно применять во время беременности как при уже существующем, так и при гестационном диабете [23]. Во время беременности обычно безопасно принимать метформин отдельно или в сочетании с инсулином. Исследования показали отсутствие или незначительный риск использования метформина во время беременности [23]. Однако лечение метформином не следует продолжать у женщин с гестационным диабетом после родов [23]. У женщин с ранее существовавшим диабетом метформин можно применять во время кормления грудью [23].Хотя метформин попадает в грудное молоко, его количество очень мало. Отсутствуют достаточные данные о метформине с травяными добавками и лечебными средствами. Однако этот обзор не охватывает обширного списка побочных эффектов, которые могут возникнуть. Кроме того, люди, принимающие метформин, могут или не могут испытывать какие-либо или все из вышеперечисленных побочных эффектов [64].
В заключение, стабилизация уровня глюкозы в крови является конечной целью для лечения диабета, которая может быть достигнута с помощью правильных лекарств по отдельности или в комбинации, наряду со здоровым образом жизни.Метформин является терапией первой линии для лечения СД2 и, как правило, безопасным и эффективным методом лечения. Метформин может помочь организму избежать осложнений, связанных с высоким уровнем глюкозы в крови, таких как повреждение почек, диабетическая невропатия или ретинопатия. Он правильно усваивает пищу и восстанавливает способность организма реагировать на инсулин. Существует возможный повышенный риск смерти от сердечно-сосудистых заболеваний, и, хотя и редко, серьезные побочные эффекты LA могут возникать из-за того, что метформин может накапливаться в организме. В этом обзоре обсуждаются возможные побочные эффекты метформина, но каждый, принимающий метформин, может испытывать или не испытывать некоторые или все из них.У пациентов с СД2 метформин может оказывать неблагоприятное воздействие на функцию почек и может развиться умеренная ХБП. Метформин следует применять с осторожностью у пациентов с травмами, лихорадкой, застойной сердечной недостаточностью, хирургическим вмешательством, почечной или печеночной недостаточностью или у пожилых людей, а лечение метформином следует прекратить перед любым типом хирургического вмешательства.
Никаких грантов ни от каких финансирующих агентств в каком-либо секторе для этого обзора получено не было.
Метформин: определение, применение, побочные эффекты
Что такое метформин?
Популярный пероральный препарат для лечения диабета 2 типа.Метформин (торговая марка Glucophage, Glucophage XR, Glumetza, Riomet) является членом класса препаратов, называемых бигуанидами, которые помогают снизить уровень глюкозы в крови, улучшая то, как организм обрабатывает инсулин, а именно предотвращая выработку печенью избытка глюкозы и делает мышечные и жировые клетки более чувствительными к доступному инсулину.
Метформин не только снижает уровень глюкозы в крови, что в долгосрочной перспективе снижает риск диабетических осложнений, но также снижает уровень холестерина и триглицеридов в крови и не вызывает увеличения веса в отличие от инсулина и некоторых других пероральных сахароснижающих препаратов. .Избыточный вес, высокий уровень холестерина и высокий уровень триглицеридов увеличивают риск развития сердечных заболеваний, что является основной причиной смерти людей с диабетом 2 типа. Еще одно преимущество метформина заключается в том, что он не вызывает гипогликемии (низкого уровня глюкозы в крови), когда это единственное лекарство от диабета, которое принимается. Метформин обычно принимают два-три раза в день во время еды. Формула с пролонгированным высвобождением (Glucophage XR) принимается один раз в день во время ужина.
Совместное руководство, выпущенное Американской диабетической ассоциацией (ADA) и Европейской ассоциацией по изучению диабета (EASD) для лечения людей с диабетом 2 типа, призывает использовать метформин в качестве лекарственной терапии первой линии наряду с образом жизни. вмешательства (здоровая диета и упражнения).Обширные обзоры многочисленных исследований показали снижение HbA1c (показатель контроля уровня глюкозы в крови за предыдущие 2–3 месяца) с 1% до 2% у людей, принимающих метформин. В большом проспективном исследовании диабета в Соединенном Королевстве (UKPDS) метформин был связан с лучшими результатами для здоровья, чем различные другие методы лечения, включая хлорпропамид (торговая марка Diabinese), глибенкламид, также известный как глибурид (DiaBeta и другие) или инсулин, и был дополнительно связано с меньшим набором веса и меньшим количеством эпизодов гипогликемии.Фактически, UKPDS — одно из основных исследований, которое привело к тому, что ADA и EASD выбрали метформин в качестве терапии первой линии.
Чтобы получать самые свежие новости о диабете, стратегии контроля уровня глюкозы в крови, советы по питанию, рецепты здорового питания и многое другое прямо на ваш почтовый ящик, подпишитесь на нашу бесплатную рассылку!
Побочные эффекты метформина
Наиболее частыми побочными эффектами метформина являются тошнота и диарея, которые обычно проходят со временем. Более серьезным побочным эффектом является редкое, но потенциально смертельное заболевание, называемое лактоацидозом, при котором в кровотоке накапливается опасно высокий уровень молочной кислоты.Лактоацидоз чаще всего возникает у людей с заболеваниями почек, печени или застойной сердечной недостаточностью или у тех, кто регулярно употребляет алкоголь. (Если вы употребляете более четырех алкогольных напитков в неделю, метформин может быть не лучшим лекарством для вас.) К сожалению, многие врачи игнорируют эти противопоказания (состояния, делающие нецелесообразным конкретное лечение) и прописывают метформин людям с повышенным риском лактоацидоза. . Ранние симптомы лактоацидоза включают необычную усталость, тошноту, рвоту, потерю аппетита, боли в мышцах и затрудненное дыхание.Если вы испытываете какие-либо из этих симптомов при приеме метформина, обязательно сразу же обратитесь к врачу. Терапию метформином следует прекратить как минимум за 48 часов до операции и возобновить только после того, как вы снова начнете нормально есть.
Незначительные побочные эффекты этого лекарства включают металлический привкус и снижение всасывания витамина B12. Как упоминалось выше, развитие лактоацидоза при приеме этого лекарства встречается редко и оценивается примерно в 4–9 случаев на 100 000 человек. Чтобы предотвратить возникновение лактоацидоза, использование метформина не рекомендуется лицам старше 80 лет, а также людям с легкой дисфункцией почек, застойной сердечной недостаточностью или ацидозом в анамнезе, среди ряда других состояний.
Метформин изменил ландшафт лечения диабета, когда Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило его для продажи в 1994 году. В то время в Соединенных Штатах было только два других типа лекарств, доступных для лечения диабета 2 типа: сульфонлюмочевины, класс пероральных препаратов, которые снижают уровень глюкозы в крови, стимулируя поджелудочную железу выделять больше инсулина. С тех пор, как метформин был одобрен в Соединенных Штатах, на рынке появился ряд других классов лекарств от диабета, которые снижают уровень глюкозы в крови с помощью различных механизмов.К ним относятся ингибиторы альфа-глюкозидазы, которые замедляют всасывание углеводов в тонком кишечнике, вызывая более медленное повышение уровня глюкозы в крови после еды; тиазолидиндионы, повышающие чувствительность к инсулину; меглитиниды, которые стимулируют быструю секрецию инсулина поджелудочной железой после еды по другому механизму, чем более старые препараты сульфонилмочевины; Агонисты GLP-1, которые задерживают опорожнение желудка и стимулируют секрецию инсулина; Ингибиторы ДПП-4, усиливающие секрецию инсулина и задерживающие опорожнение желудка; аналоги амилина, которые замедляют опорожнение желудка, подавляют глюкагон и подавляют аппетит; Агонисты рецептора GLP-1, которые увеличивают чувство насыщения (чувство сытости), замедляют опорожнение желудка, увеличивают высвобождение инсулина и уменьшают высвобождение глюкагона; и ингибиторы SGLT2, которые блокируют реабсорбцию глюкозы почками.Поскольку эти лекарства имеют разные механизмы действия, врачи часто комбинируют лекарства разных классов для более сильного снижения уровня глюкозы в крови.
Поскольку метформин часто назначают вместе с другими лекарствами от диабета, некоторые производители начали комбинировать два препарата в одной таблетке для более удобного лечения. К ним относятся Kazano, Invokamet, Invokamet XR, Xigduo XR, Synjardy, Synjardy XR, Metaglip, Glucovance, Jentadueto, Jentadueto XR, PrandiMet, Avandamet, Kombiglyze XR, Janumet и Janumet XR.Любой, кто принимает одну из этих таблеток, должен помнить о симптомах лактоацидоза.
Хотите узнать больше об этом популярном лекарстве от диабета? Прочтите «Диабетическая медицина: метформин», «Метформин: несанкционированная биография» и «Метформин с рыбным запахом? Что вы можете сделать », затем пройдите нашу викторину« Как много вы знаете о метформине? »
Первоначально опубликовано 17 мая 2006 г.
Метформин :: Диабетическое образование онлайн
Метформин — наиболее часто назначаемое лекарство от диабета 2 типа во всем мире.
Бигуанид (метформин)
Метформин в основном действует на печень и снижает чрезмерное высвобождение сахара, наблюдаемое при диабете 2 типа. Метформин не вызывает увеличения веса и обычно является препаратом первого выбора для лечения диабета 2 типа. Однако, если у вас проблемы с почками или печенью, сердечная недостаточность или вы очень больны, метформин нельзя использовать.
Основными побочными эффектами метформина являются диарея, расстройство желудка или спазмы. Важно принимать метформин во время еды, чтобы уменьшить побочные эффекты со стороны желудка.Очень редкий побочный эффект (менее 1 человека на 100 000 пациентов, принимающих метформин) — это лактоацидоз (накопление молочной кислоты в крови). Лактоацидоз очень опасен и обычно приводит к летальному исходу. Как правило, люди, у которых развивается этот редкий побочный эффект, — это те, кому вообще не следовало принимать метформин (люди с проблемами почек, сердечной недостаточностью или алкоголизмом).
Метформин также называют эугликемическим , что означает, что он может восстанавливать уровень сахара в крови до нормального или недиабетического уровня.Если вы лечитесь только метформином, у вас не должно наблюдаться низкого уровня сахара в крови. И если вы лечитесь метформином и другими нормализующими уровень сахара в крови («эугликемическими») агентами (такими как тиазолидиндионы, блокаторы крахмала или инкретины), у вас также не должно быть низкого уровня сахара в крови. Однако при приеме метформина вместе с таблетками, высвобождающими инсулин, и инсулином могут развиться гипогликемия или низкий уровень сахара в крови, поскольку они повышают уровень инсулина и повышают риск развития депрессии.
Короче говоря, метформин снижает выработку глюкозы печенью
Наиболее частые побочные эффекты:
- Диарея и спазмы желудка
- Низкий уровень сахара в крови при применении в сочетании с таблетками, высвобождающими инсулин (стимуляторы секреции) и инсулином
A Редкий побочный эффект метформина — накопление молочной кислоты.
Для получения дополнительной информации о дозировке (формах) таблеток метформина, начальной и конечной дозах, побочных эффектах и различных имеющихся на рынке препаратах, содержащих метформин, см. Нашу Таблицу лекарств.
Тест для самооценки
Тесты для самооценки доступны по темам, затронутым на этом веб-сайте. Чтобы узнать, сколько вы узнали о Лечение диабета 2 типа , пройдите нашу викторину для самооценки, когда вы заполнили этот раздел. Викторина с множественным выбором.Пожалуйста, выберите лучший ответ на каждый вопрос. В конце викторины отобразится ваш счет. Если ваша оценка верна более чем на 70%, у вас все хорошо. Если ваша оценка меньше 70%, вы можете вернуться в этот раздел и просмотреть информацию.
60 лет использования метформина: взгляд в прошлое и взгляд в будущее
В этом году исполняется 60 лет со дня первого клинического применения метформина при диабете.С самого начала (и несмотря на несколько неоднозначную историю) метформин в настоящее время рекомендуется в качестве перорального глюкозоснижающего средства первой линии в большинстве, если не во всех, клинических руководствах по ведению диабета 2 типа. Возможно, как отражение этого, метформин был прописан 83,6% людей с диабетом 2 типа в Великобритании в 2013 году [1]. Между тем, в США с 2008 по 2012 год метформин занимал восьмое место среди наиболее часто назначаемых лекарств [2], количество назначений выросло с 51.С 6 миллионов в 2008 году до 61,6 миллиона в 2012 году. Метформин и гликлазид — единственные два пероральных глюкозоснижающих средства в Примерном списке основных лекарственных средств ВОЗ [3]. Как этот препарат занял такое доминирующее положение и оправдано ли такое широкое применение?
Если фармакологическая терапия действительно необходима в дополнение к мерам, связанным с образом жизни, специалисты по диабету и люди с диабетом 2 типа нуждаются в лекарствах, эффективных для снижения уровня глюкозы в крови, легко принимаемых, желательно с дозированием один раз в день, без коротких или длительных с краткосрочными побочными эффектами, не несет риска гипогликемии, не вызывает увеличения веса и доступен во всем мире.Кроме того, идеальное лекарство могло бы воздействовать на основную патофизиологию диабета 2 типа и иметь дополнительную ценность с точки зрения снижения негликемических факторов риска и частоты микро- и макрососудистых осложнений диабета. Как метформин соответствует этим требованиям?
Лекарство, безусловно, является эффективным средством для снижения уровня глюкозы, обычно снижая уровень HbA 1c примерно на 10–15 ммоль / моль (1,0–1,5%) при диабете 2 типа [4]. Однако мы начинаем понимать, что не все реагируют на препарат одинаково и что генетические вариации могут влиять на индивидуальный ответ [5].Кроме того, многие люди с диабетом будут утверждать, что его нелегко принимать, считая большие таблетки отталкивающими и необходимость употребления более одного раза в день неудобными. За 60 лет клинического применения мы хорошо понимаем краткосрочные и долгосрочные побочные эффекты метформина. Общие побочные эффекты со стороны желудочно-кишечного тракта можно свести к минимуму, медленно повышая дозу, принимая лекарство во время / после еды и, при необходимости, переходя на препараты с пролонгированным высвобождением. При длительном применении из-за страха перед метформин-ассоциированным лактоацидозом использование метформина в некоторых странах изначально затруднялось.Однако недавний систематический обзор проспективных сравнительных исследований и наблюдательных когорт показывает, что лактоацидоз встречается крайне редко, с аналогичной частотой у людей с диабетом, принимающих метформин или другие сахароснижающие препараты [6]. Действительно, многие люди предположили, что противопоказания к применению метформина при хронической болезни почек 3 стадии и выше (расчетная СКФ [рСКФ] <60 мл мин –1 [1,73 м] –2 ) являются слишком строгими. Однако дальнейший метаанализ подтверждает осторожное использование метформина у лиц с хроническим заболеванием почек с рСКФ не более 30 мл мин -1 [1.73 m] −2 , с соответствующим снижением дозы и тщательным постоянным измерением функции почек [7]. Однако существует очень небольшой, но реальный риск лактоацидоза, особенно у лиц, принимающих метформин, у которых развивается острое повреждение почек [8]. Таким образом, люди, принимающие метформин, и их медицинские работники должны помнить о том, чтобы временно исключить метформин во время заболеваний, которые могут увеличить риск острого повреждения почек.
А как насчет метформина и массы тела? Клиницисты часто подчеркивают влияние метформина на потерю веса, но систематический обзор и метаанализ плацебо-контролируемых рандомизированных исследований показывают, что средняя потеря веса с помощью метформина составляет 1.1 кг [9]. Метформин имеет явное преимущество перед препаратами сульфонилмочевины, которые приводят к увеличению веса на 2–3 кг. Однако по сравнению с глюкозоснижающим и снижающим вес эффектами аналогов глюкагоноподобного пептида-1 (GLP-1) и ингибиторов натрий-глюкозного котранспортера 2 (SGLT2), метформин, по-видимому, не обеспечивает никакого дополнительного улучшения веса [10].
Итак, в целом, метформин — это проверенный и проверенный препарат, который, по крайней мере, в некоторой степени соответствует некоторым нашим критериям хорошего лекарства от диабета.Это особенно верно по сравнению с другим классом хорошо зарекомендовавших себя средств, снижающих уровень глюкозы, сульфонилмочевиной. Однако удастся ли новым классам глюкозоснижающих средств сбить метформин с его высокого пьедестала? В настоящее время эти препараты намного дороже метформина, и их долгосрочная безопасность еще не ясна, поэтому их обычно рекомендуют в качестве препаратов второго или третьего ряда для лечения диабета 2 типа. Однако есть вероятность, что по мере накопления данных и клинического опыта они вытеснят метформин и станут терапией первой линии, по крайней мере, для некоторых людей с диабетом 2 типа.
Центральная роль метформина в лечении диабета 2 типа тем более примечательна, что даже по прошествии 60 лет мы все еще не полностью понимаем механизм его действия. То, что он подавляет глюконеогенез в печени, вероятно, не вызывает сомнений, но как именно он это делает, неясно. Горячо обсуждается вопрос о том, являются ли другие действия на желудочно-кишечный тракт и, возможно, даже на ось кишечник-мозг-печень более важными [11]. Кроме того, отсутствуют доказательства того, что метформин на самом деле влияет на основной процесс диабета.В основном на основании рандомизированного исследования UKPDS (UKPDS) и открытых результатов последующего наблюдения, мы считаем, что метформин снижает частоту макрососудистых заболеваний, по крайней мере, у лиц с ожирением [12, 13], но не уверены в том, является ли это чистым эффект снижения уровня глюкозы или наличие у метформина других плеоморфных эффектов. Для аналогов GLP-1 и ингибиторов SGLT2 есть предварительные доказательства положительного воздействия на сердечно-сосудистую систему отдельных агентов каждого класса [14,15,16]. Ожидаются дополнительные данные от других агентов в обоих классах.
Метформин не является исключением из нынешней моды на перепрофилирование старых лекарств для новых применений. Он широко используется при лечении синдрома поликистозных яичников (СПКЯ), но оправдано ли это использование? Кроме того, после признания того, что риск некоторых видов рака повышается при диабете 2 типа, внимание было обращено на влияние глюкозоснижающих агентов на рак. Наблюдательные исследования показали, что смертность от рака была ниже у лиц, которым прописан метформин, по сравнению с теми, кто принимал инсулин или сульфонилмочевину [17].Несмотря на несколько метаанализов, свидетельствующих об обратном (что метформин не снижает риск рака или смертность [18, 19]), в настоящее время прилагаются большие усилия для исследований in vitro и in vivo, изучающих потенциальные механизмы действия и биологические эффекты этого препарата на профилактика и лечение рака. Метформин также все чаще продвигается как средство против старения [20]. Насколько существенна эта шумиха?
В ознаменование 60-летия первого клинического применения метформина при диабете, Diabetologia заказала серию статей по многим из этих спорных и развивающихся аспектов метформина.Помимо критического обзора имеющихся данных, наших авторов попросили заглянуть в будущее и порассуждать о том, куда нас может завести метформин.
Наша серия начинается с введения в препарат Клиффорда Бейли [21], который описывает его травяную историю, прослеживая его до Galega officinalis , который впервые был показан для лечения симптомов, связанных с диабетом, в 1772 году. только в 1957 году врач по имени Жан Стерн вновь пробудил интерес к метформину.Он отметил тот факт, что флумамин (гидрохлорид метформина) способен снижать уровень глюкозы в крови у больных гриппом (у которых этот препарат использовался в качестве противогриппозного средства). Задавшись целью исследовать фармакодинамику соединений на основе гуанидина, Стерн «воплотил потенциал метформина в снижении уровня глюкозы в крови в терапевтическую реальность». На основании этих результатов исследования, проведенные между 1960 и 1980 годами, подтвердили эффективность этого препарата для снижения уровня глюкозы в крови, с небольшими доказательствами серьезных последствий для безопасности, в результате чего этот препарат в конечном итоге был назван «оптимальным» средством лечения диабета 2 типа.
Несмотря на то, что метформин занимает первое место в иерархии глюкозоснижающих средств, остается много вопросов относительно механизмов действия метформина. Широко сообщается о влиянии метформина на печень, снижая глюконеогенез в печени и улучшая чувствительность к инсулину. В своем обзоре Рена и его коллеги [22] обсуждают влияние метформина на функцию митохондрий и активность AMPK в печени, а также независимые от AMPK эффекты. Кроме того, авторы подчеркивают недавно установленную критическую роль кишечника в действиях метформина, когда метформин изменяет метаболизм глюкозы в кишечнике, подавляет выработку глюкозы в печени через перекрестные помехи между печенью, кишечником и мозгом и изменяет микробиом кишечника.
Sanchez-Rangel и Inzucchi [23] рассматривают иерархическое место метформина в клинической терапии. Они представляют данные, указывающие на эффективность метформина для снижения уровня глюкозы при диабете 2 типа как в виде монотерапии, так и в комбинации с другими агентами. В этой когорте препарат также, по-видимому, не увеличивает риск гипогликемии и не влияет на вес, но при этом имеет потенциальную пользу для сердечно-сосудистой системы. Авторы не игнорируют побочные эффекты, связанные с этим препаратом, обсуждая клинические подходы, принятые для предотвращения побочных эффектов.Наконец, они признают, что, хотя многие испытания лекарств проводились на фоне терапии метформином, некоторые новые методы лечения не тестировались напрямую против метформина. Таким образом, они задаются вопросом, как этот бигуанид будет действовать против новых препаратов, снижающих уровень глюкозы в крови, при лечении диабета 2 типа.
При диабете 1 типа инсулин является терапией первой линии. Однако, несмотря на успехи в составах и способах введения инсулина, использование инсулина связано с повышенным риском гипогликемии и увеличения веса, последнее приводит к инсулинорезистентности и увеличению потребности в дозах инсулина, более высокому АД и повышению холестерина ЛПНП.Поэтому диабетологи и люди с диабетом 1 типа ищут дополнение к терапии инсулином, которое могло бы улучшить гликемический контроль при диабете 1 типа без увеличения веса и его неблагоприятных последствий. Может ли метформин быть такой терапией? В своем обзоре Ливингстон и др. [24] приводят доказательства использования метформина при диабете 1 типа. В целом, исследования показывают, что использование метформина не приводит к устойчивому улучшению гликемического контроля, но снижает требуемую дозу инсулина, вес и, возможно, холестерин ЛПНП.Авторы также представляют новые данные из исследования «Уменьшение с помощью метформина» сосудистых побочных эффектов (REMOVAL), показывающие, что прогрессирование атеросклероза также может быть уменьшено при использовании метформина, в то время как наблюдалось только временное снижение HbA 1c . Следовательно, у этого препарата есть потенциал, чтобы оказывать независимое от глюкозы действие, что может быть полезно для людей с диабетом 1 типа.
Наряду с ведением болезней одной из основных целей терапии является предотвращение начала болезни.Программа профилактики диабета (DPP) — это крупнейшее и самое продолжительное клиническое испытание метформина для профилактики диабета, и в этой серии обзоров Aroda et al [25] представляют основные связанные с метформином результаты исследования DPP и его последующего исследования. , исследование результатов DPP (DPPOS). В частности, метформин снизил заболеваемость диабетом на 31% по сравнению с плацебо после 2,8 лет наблюдения, при этом снижение риска (18%) все еще наблюдалось в течение 10 и 15 лет после рандомизации. Более того, наблюдались благоприятные эффекты метформина на несколько факторов риска сердечно-сосудистых заболеваний.Таким образом, результаты DPP / DPPOS показывают многообещающие перспективы использования метформина для профилактики диабета 2 типа с дополнительными преимуществами, распространяющимися на его сердечно-сосудистые осложнения.
Griffin et al [26] углубились в связь между метформином и риском сердечно-сосудистых заболеваний. Эти авторы провели метаанализ рандомизированных исследований, сообщающих о сердечно-сосудистых исходах, в которых эффект метформина был «изолирован» путем сравнения с диетой, образом жизни или плацебо. Был проанализирован риск общей смертности, смерти от сердечно-сосудистых заболеваний, инфаркта миокарда, инсульта и заболеваний периферических сосудов, и все исходы, кроме инсульта, отдавали предпочтение метформину; Результаты показали, что метформин снижает риск смерти от всех причин на 16%, но может также увеличить риск инсульта на 48%.Однако авторы отмечают, что при интерпретации этих результатов следует учитывать несколько важных ограничений (включая систематическую ошибку исследования и небольшой размер выборки) и что необходимы хорошо спланированные рандомизированные исследования терапии метформином, чтобы можно было проводить сравнение с более новыми сахароснижающими препаратами (например, эмпаглифлозином). и лираглутид), для которых доступны строгие данные о конечных показателях сердечно-сосудистой системы.
При некоторых состояниях метформин представляет собой относительно новый терапевтический подход. В своем обзоре Сэм и Эрманн [27] обсуждают использование метформина при СПКЯ.Помимо репродуктивных проявлений, СПКЯ также имеет метаболические последствия, включая инсулинорезистентность, нарушение толерантности к глюкозе и диабет 2 типа. Впервые метформин уменьшил гиперандрогенизм у женщин с СПКЯ в 1990-х годах, и, хотя точный механизм действия полностью не изучен, его использование при СПКЯ является обычным явлением. Сэм и Эрманн используют небольшой пул имеющихся данных, чтобы обрисовать, как метформин действует на ткани, имеющие отношение к СПКЯ, снижая выработку глюкозы в печени, увеличивая поглощение глюкозы мышцами и регулируя выработку андрогенов яичниками.Эти индуцированные метформином эффекты в основном предотвращают метаболические последствия заболевания, в то же время оказывая лишь ограниченное влияние на репродуктивные осложнения. Однако, чтобы установить истинный потенциал метформина при СПКЯ, авторы заявляют о необходимости крупных хорошо спланированных проспективных исследований.
Важное понимание использования метформина во время беременности было получено в результате исследований его использования при СПКЯ. Метформин используется при беременности более 40 лет. Препарат проникает через плацентарный барьер, и предполагаемый повышенный риск лактоацидоза и относительно гипоксическая среда плода вызывают опасения по поводу его использования во время беременности.Однако исследования СПКЯ показали, что метформин не увеличивает врожденные пороки развития или выкидыши. В своем обзоре Lindsay и Loeken [28] обсуждают использование метформина при гестационном диабете, представляя доказательства того, что метформин имеет хороший профиль безопасности и эффективен для снижения показателей тяжелой гипогликемии и увеличения веса у беременных. В отличие от этого, при прегестационном диабете 2 типа доказательная база для использования метформина невелика, но данные наблюдений указывают на повышенный риск преэклампсии и перинатальной смертности.Доказательства долгосрочных эффектов использования метформина у потомков матерей с гестационным диабетом неоднозначны для изменений в составе тела, в то время как никаких различий в АД, моторном, социальном и языковом развитии не наблюдалось. Таким образом, хотя метформин потенциально может выступать в качестве подходящей терапии при гестационном диабете (но не прегестационном диабете), его использование вызывает опасения из-за нехватки надежных данных.
Исследования также показали, что метформин может снизить риск диабета у людей в возрасте 60 лет и старше, а также что его применение улучшает такие исходы старения, как слабость и нарушение физических и когнитивных функций.В своем обзоре Валенсия и др. [29] описывают потенциальные механизмы, с помощью которых метформин вмешивается в процесс старения, независимо от регуляции уровня глюкозы в крови. Например, считается, что влияние метформина на воспаление и активные формы кислорода снижает повреждение ДНК, в то время как его влияние на церамиды (которые способствуют снижению количества миобластов у пожилых людей) также может помочь улучшить здоровье и функцию тканей. Кроме того, кардио- и нейропротекторная роль метформина и влияние метформина на психологическое здоровье и когнитивные функции также могут способствовать здоровому старению и увеличению продолжительности жизни.В заключение Валенсия и соавторы рассказали о нескольких предстоящих клинических испытаниях метформина при старении, которые предлагают захватывающую возможность раскрыть истинный потенциал метформина у стареющего населения, с диабетом или без него.
В своем обзоре Майкл Поллак [30] также обсуждает негликемические эффекты метформина. Он предполагает, что функция метформина может быть частично объяснена его влиянием на микробиоту человека (например, снижение уровня Intestinibacter , увеличение продолжительности жизни Caenorhabditis elegans ) и метаболом кишечника (например.грамм. повышенный синтез бутирата), хотя точные механизмы этих изменений еще предстоит определить. Например, определенные профили микробиоты связаны с непереносимостью глюкозы, в то время как кишечные метаболиты могут изменять резистентность к инсулину и гликемический контроль. Альтернативно, метформин может изменять желудочно-кишечные механизмы, которые влияют на системный метаболизм углеводов, например, изменяя физиологию желчных кислот, уровни GLP-1 и передачу сигналов дуоденального AMPK. Метформин также обладает иммуномодулирующим действием, влияя на энергетический метаболизм в иммунных клетках, что может влиять на иммунную функцию.Считается, что это приводит к противоопухолевой активности или уменьшению воспаления. Эти эффекты метформина могут иметь значение при других состояниях, помимо диабета, включая рак.
В соответствии с этим, эпидемиологические исследования предоставили доказательства связи между метформином и снижением заболеваемости и смертности от рака. В этой серии обзоров Heckman-Stoddard et al [31] обсуждают потенциальное использование метформина для профилактики и лечения рака. Предлагаются два основных пути, способствующих противоопухолевой активности метформина: (1) непрямой путь через снижение уровня инсулина, что может замедлять пролиферацию опухоли у людей с гиперинсулинемией; и (2) снижение потребления энергии в предопухолевых и неопластических клетках за счет прямого воздействия на респираторный комплекс I транспортной цепи электронов.Хекман-Стоддард и его коллеги продолжают обсуждение результатов клинических испытаний метформина при раке. Они демонстрируют, что, в зависимости от типа исследуемого рака, метформин по-разному влияет на биомаркеры, связанные с раком, показывая многообещающие результаты с некоторыми видами рака, но оказывая минимальное влияние на другие. В этой области исследований ведется много испытаний, и мы терпеливо ждем результатов испытаний фазы III, которые предоставят важные доказательства за или против противоопухолевой роли метформина.
Независимо от состояния, для лечения которого он используется, ответ на терапию метформином варьируется от человека к человеку. В своем обзоре Хосе Флорес [32] обсуждает, почему возникает неоднородность реакции и как мы можем ее предсказать. При этом есть надежда, что может быть возможен индивидуальный подход к терапии метформином. Однако отсутствие у нас сведений о точной молекулярной мишени и механизме действия метформина затрудняет стратификацию пациентов. Тем не менее Флорес предлагает потенциальное решение: генетический подход.Исследования генов-кандидатов показали, что мутации в гене, кодирующем переносчик органических катионов 1 (OCT1), с большей вероятностью влияют на ответ на метформин по сравнению с другими белками-переносчиками метформина. Результаты полногеномных ассоциативных исследований указывают на роль мутаций в ATM и SLC2A2 (последний кодирует GLUT2) в гликемическом ответе на метформин. Тем не менее, индивидуальный подход к терапии метформином пока что не обсуждается, поскольку необходимо гораздо больше данных генетических исследований, прежде чем эта надежда станет реальностью.
Таким образом, эта серия обзоров демонстрирует, как лекарство, которое можно было легко потерять и забыть после бурного старта, не только стало играть ведущую роль в лечении диабета 2 типа, но и показало многообещающие возможности для лечения диабета второго типа. 1 диабет, диабет при беременности, СПКЯ, старение и рак. Тем не менее, общая тема всей этой серии заключается в том, что отсутствуют убедительные доказательства использования метформина во многих из этих состояний, что угрожает шансам этого препарата остаться на первом месте, в то время как на рынке быстро появляются другие новые глюкозоснижающие препараты.Тем не менее, в настоящее время метформин остается одним из «наиболее эффективных, безопасных и рентабельных лекарств от приоритетных состояний» [3], и есть большая вероятность, что через следующие 60 лет убедительные доказательства подтвердят его использование при заболеваниях. кроме диабета.
Надеюсь, вы согласитесь с тем, что наши авторы приняли вызов, который мы им поставили, и что вы найдете эту серию информативной, стимулирующей и заставляющей задуматься как с клинической, так и с научной точки зрения.
Сокращения
- DPP:
Программа профилактики диабета
- DPPOS:
Исследование результатов программы профилактики диабета
- рСКФ:
Расчетная СКФ
- GLP-1:
Глюкагоноподобный пептид-1
- PCOS:
Синдром поликистозных яичников
- SGLT2:
Котранспортер натрия и глюкозы 2
- УКПДС:
Проспективное исследование диабета в Великобритании
Ссылки
- 1.
Шарма М., Назарет I, Петерсен I (2016) Тенденции в заболеваемости, распространенности и назначении при сахарном диабете 2 типа в период с 2000 по 2013 год в системе первичной медико-санитарной помощи: ретроспективное когортное исследование. BMJ Open 6: e010210
Статья PubMed PubMed Central Google Scholar
- 2.
Институт медицинской информатики IMS. Национальный аудит рецептов, декабрь 2012 г. Доступно на сайте www.imshealth.com. По состоянию на 3 мая 2017 г.
- 3.
Всемирная организация здравоохранения. Примерный перечень основных лекарственных средств ВОЗ. 19-й список. 2015. Доступно на сайте www.who.int/medicines/publications/essentialmedicines/EML_2015_FINAL_amended_NOV2015.pdf?ua=1. По состоянию на 3 мая 2017 г.
- 4.
DeFronzo RA, Stonehouse AH, Han J, Wintle ME (2010) Взаимосвязь исходного уровня HbA1c и эффективности текущих сахароснижающих терапий: метаанализ рандомизированных клинических испытаний. Diabet Med 27: 309–317
CAS Статья PubMed Google Scholar
- 5.
Zhou K, Yee SW, Seiser EL et al (2016) Вариация гена транспортера глюкозы SLC2A2 связана с гликемическим ответом на метформин. Нат Генет 48: 1055–1059
CAS Статья PubMed PubMed Central Google Scholar
- 6.
Солпитер С.Р., Грейбер Э., Пастернак Г.А., Солпитер Э.Е. (2010). Риск смертельного и нефатального лактоацидоза при использовании метформина при сахарном диабете 2 типа. Кокрановская база данных Syst Rev, выпуск 4, ст.№: CD002967. DOI: 10.1002 / 14651858.CD002967.pub4
- 7.
Inzucchi SE, Lipska KJ, Mayo H, Bailey CJ, McGuire DK (2014) Метформин у пациентов с диабетом 2 типа и заболеванием почек: систематический обзор. JAMA 312: 2668–2675
Статья PubMed Central Google Scholar
- 8.
Connelly PJ, Lonergan M, Soto-Pedre E, Donnelly L, Zhou K, Pearson ER (2017) Острое повреждение почек, концентрация лактата в плазме и лактоацидоз у пользователей метформина: исследование GoDarts.Диабет, ожирение, метаболизм: 10.1111 / dom.12978
- 9.
Домек Дж. П., Пруцкий Г., Леппин А. и др. (2015) Лекарства, обычно связанные с изменением веса: систематический обзор и метаанализ. J Clin Endocrinol Metab 100: 363–370
CAS Статья PubMed PubMed Central Google Scholar
- 10.
Wilding JP, Rajeev SP, DeFronzo RA (2016) Позиционирование ингибиторов SGLT2 / терапии на основе инкретина в алгоритме лечения.Уход за диабетом 39 (Приложение 2): S154 – S164
Статья PubMed Google Scholar
- 11.
McCreight LJ, Bailey CJ, Pearson ER (2016) Метформин и желудочно-кишечный тракт. Диабетология 59: 426–435
CAS Статья PubMed PubMed Central Google Scholar
- 12.
Группа перспективного исследования диабета Великобритании (UKPDS) (1998) Влияние интенсивного контроля уровня глюкозы в крови с помощью метформина на осложнения у пациентов с избыточной массой тела и диабетом 2 типа (UKPDS 34).Ланцет 352: 854–865
Артикул Google Scholar
- 13.
Holman RR, Paul SK, Bethel MA, Matthews DR, Neil HA (2008) 10-летнее наблюдение за интенсивным контролем уровня глюкозы при диабете 2 типа. N Engl J Med 359: 1577–1589
CAS Статья PubMed Google Scholar
- 14.
Zinman B, Wanner C, Lachin JM et al (2015) Эмпаглифлозин, сердечно-сосудистые исходы и смертность при диабете 2 типа.N Engl J Med 373: 2117–2128
CAS Статья PubMed Google Scholar
- 15.
Ваннер C, Inzucchi SE, Lachin JM et al (2016) Эмпаглифлозин и прогрессирование заболевания почек при диабете 2 типа. N Engl J Med 375: 323–334
CAS Статья PubMed Google Scholar
- 16.
Марсо С.П., Дэниэлс Г.Х., Браун-Франдсен К. и др. (2016) Лираглутид и сердечно-сосудистые исходы при диабете 2 типа.N Engl J Med 375: 311–322
CAS Статья PubMed PubMed Central Google Scholar
- 17.
Bowker SL, Majumdar SR, Veugelers P, Johnson JA (2006) Повышенная смертность от рака у пациентов с диабетом 2 типа, принимающих сульфонилмочевину или инсулин. Уход за диабетом 29: 254–258
Статья PubMed Google Scholar
- 18.
Стивенс Р.Дж., Али Р., Бэнкхед К.Р. и др. (2012) Исходы рака и общая смертность у взрослых, принимавших метформин: систематический обзор и совместный метаанализ рандомизированных клинических испытаний.Диабетология 55: 2593–2603
CAS Статья PubMed Google Scholar
- 19.
Farmer RE, Ford D, Forbes HJ et al (2016) Метформин и рак при диабете 2 типа: систематический обзор и всесторонняя оценка систематической ошибки. Int J Epidemiol 46: 728–744
- 20.
Анисимов В.Н. (2013) Метформин: наконец-то появился антивозрастной препарат? Клеточный цикл 12: 3483–3489
CAS Статья PubMed PubMed Central Google Scholar
- 21.
Bailey CJ (2017) Метформин: исторический обзор. Diabetologia doi: 10.1007 / s00125-017-4318-z
- 22.
Рена Г., Харди Д.Г., Пирсон Э.Р. (2017) Механизмы действия метформина. Diabetologia doi: 10.1007 / s00125-017-4342-z
- 23.
Sanchez-Rangel E, Inzucchi SE (2017) Метформин: клиническое применение при диабете 2 типа. Diabetologia doi: 10.1007 / s00125-017-4336-x
- 24.
Ливингстон Р., Бойл Дж. Г., Петри Дж. Р., Исследовательская группа REMOVAL (2017).Новый взгляд на метформин при диабете 1 типа. Diabetologia doi: 10.1007 / s00125-017-4364-6
- 25.
Aroda VR, Knowler WC, Crandall JP et al (2017). Метформин для профилактики диабета: выводы, полученные в результате исследования результатов Программы профилактики диабета / Программы профилактики диабета. Diabetologia doi: 10.1007 / s00125-017-4361-9
- 26.
Griffin SJ, Leaver JK, Irving GJ (2017) Влияние метформина на сердечно-сосудистые заболевания: метаанализ рандомизированных исследований среди людей с диабетом 2 типа.Diabetologia doi: 10.1007 / s00125-017-4337-9
- 27.
Сэм С., Эрманн Д.А. (2017) Метформиновая терапия репродуктивных и метаболических последствий синдрома поликистозных яичников. Diabetologia doi: 10.1007 / s00125-017-4306-3
- 28.
Линдси Р.С., Локен М.Р. (2017). Применение метформина при беременности: обещания и неуверенность. Diabetologia doi: 10.1007 / s00125-017-4351-y
- 29.
Валенсия, WM, Palacio A, Tamariz L, Florez H (2017).Метформин и старение: улучшение результатов старения, выходящих за рамки контроля гликемии. Diabetologia doi: 10.1007 / s00125-017-4349-5
- 30.
Pollack M (2017). Влияние метформина на микробиоту кишечника и иммунную систему как границы исследований. Diabetologia doi: 10.1007 / s00125-017-4352-x
- 31.
Heckman-Stoddard BM, Decensi A, Sahasrabuddhe VV, Ford L (2017). Использование метформина для профилактики рака и рецидивов рака.Diabetologia doi: 10.1007 / s00125-017-4372-6
- 32.
Florez JC (2017) Фармакогенетика метформина. Diabetologia doi: 10.1007 / s00125-017-4335-y
Скачать ссылки
Информация об авторе
Принадлежности
Группа исследований диабета, Институт клеточной медицины, Факультет клинических медицинских наук, Университет Ньюкасла, 4-й этаж здания Уильяма Лич, Фрамлингтон-плейс, Ньюкасл-апон-Тайн, NE2 4HH , Великобритания
Салли М.Маршалл
Автор, ответственный за переписку
Переписка на Салли М. Маршалл.
Об этой статье
Цитируйте эту статью
Marshall, S.M. 60 лет использования метформина: взгляд в прошлое и взгляд в будущее. Диабетология 60, 1561–1565 (2017). https://doi.org/10.1007/s00125-017-4343-y
Ссылка для скачивания
Метформин (глюкофаг) Побочные эффекты и осложнения
Удивительное соединение под названием метформин было открыто почти столетие назад.Ученые поняли, что он может снизить уровень сахара в крови на модели животных (кролики) еще в 1929 году, но только в конце 1950-х годов французский исследователь придумал название Glucophage (примерно переводится как глюкоза или поедатель сахара). . FDA дало метформину (глюкофагу) зеленый свет для лечения диабета 2 типа в 1994 году, через 36 лет после того, как он был одобрен для этого использования в Великобритании. Теперь исследователи обнаруживают, что метформин обладает противораковой активностью, особенно у мужчин с раком простаты ( Canadian Journal of Urology , Oct.2018).
Использование дженерика метформина:
Глюкофаг потерял патентную защиту в США в 2002 году, и теперь большинство рецептов содержат генерический метформин. Этот препарат признан препаратом первой линии для контроля уровня сахара в крови за счет улучшения реакции клеток на инсулин и снижения количества сахара, производимого печенью. В отличие от некоторых других пероральных лекарств от диабета, он не приводит к увеличению веса и может даже помочь людям контролировать свой вес ( Current Obesity Reports , июнь 2019).
С начала 2000 года продажи метформина (глюкофага) столкнулись с проблемой нового класса лекарств от диабета. Сначала Avandia , а затем Actos бросили вызов метформину за лидерство в лечении диабета. Позже Avandia потеряла свой блеск, потому что была связана с сердечными приступами и инсультами. Продажи этого препарата сейчас минимальны из-за жестких правил FDA.
Actos также находится под пристальным вниманием. Препарат был запрещен во Франции и Германии из-за связи с раком мочевого пузыря.FDA также потребовало, чтобы Actos несли строжайшее предупреждение в виде черного ящика о повышенном риске застойной сердечной недостаточности, вызванной приемом препарата. Новые лекарства от диабета, такие как лираглутид ( Victoza ), саксаглиптин ( Onglyza ) и ситаглиптин ( Januvia ), стали очень успешными. Но метформин остается основой лечения диабета. Его назначают отдельно или иногда в сочетании с новыми лекарствами от диабета.
Метформин как средство первой линии для лечения диабета 2 типа:
Все это означает, что метформин (глюкофаж) вернул себе репутацию лучшего средства для лечения диабета 2 типа.Американский колледж врачей рекомендовал метформин в качестве первой линии лечения, когда изменения образа жизни (диета, физические упражнения и потеря веса) не привели к адекватному контролю уровня глюкозы в крови. Возможно, именно поэтому в 2014 году было выписано почти 60 миллионов рецептов на метформин. Несмотря на большое количество новых лекарств от диабета 2 типа, метформин по-прежнему является наиболее выгодным.
Несмотря на все теплые и туманные чувства по поводу использования этого лекарства от диабета 2 типа, есть некоторые предостережения.Этот препарат может вызвать ряд побочных эффектов, особенно если речь идет о желудочно-кишечном тракте. Они могут быть особенно надоедливыми в течение первых нескольких недель лечения. Однако через несколько недель симптомы со стороны пищеварения часто проходят. Если они повторяются, немедленно сообщите своему врачу, так как это могут быть симптомы лактоацидоза (см. Ниже). Вот список побочных реакций, на которые следует обратить внимание:
Метформин Побочные эффекты:
- Изжога
- Боль в животе
- Диарея
- Газ
- Головная боль
- Тошнота
- Слабость Слабость Слабость Слабость
- Лактоацидоз (симптомы могут включать нерегулярную частоту сердечных сокращений, тошноту, боль в животе, летаргию, беспокойство, низкое кровяное давление и учащенное сердцебиение) Немедленно сообщите своему врачу, если вы заметили любой из этих симптомов!
Эти побочные эффекты могут показаться пугающими, но большинство людей переносят это лекарство довольно хорошо.Однако препарат может быть опасен для людей с заболеванием почек. Им не следует принимать препарат, и у всех, кто принимает метформин, следует регулярно (не реже одного раза в год) контролировать функцию почек. Также нельзя принимать метформин людям с застойной сердечной недостаточностью.
Истощение запасов витамина B12:
Однако последнее слово предостережения. Метформин имеет некоторые последствия для питания. Основное беспокойство вызывает дефицит витамина B12, особенно в дозах 1500 мг или выше ( Medicine , ноябрь.2019).
Абигейл спросила:
Q. Я читал, что метформин может вызывать дефицит витамина B12. Мне не удалось снова найти источник этой информации, и я хотел бы получить ваш отзыв.
A. Это из информации о назначении на DailyMed, идентичной тому, что опубликовано в PDR:«Уровни витамина B12: в контролируемых клинических испытаниях метформина продолжительностью 29 недель, снижение до субнормальных уровней, которые были ранее. Нормальный уровень витамина B12 в сыворотке крови без клинических проявлений наблюдался примерно у 7% пациентов.Такое снижение, возможно, из-за нарушения абсорбции B12 комплексом B12-внутренний фактор, однако, очень редко связано с анемией и, по-видимому, быстро обратимо при прекращении приема метформина или витамина B12. Пациентам, принимающим метформин, рекомендуется ежегодно измерять гематологические параметры, и любые явные отклонения должны быть соответствующим образом исследованы и устранены (см. МЕРЫ ПРЕДОСТОРОЖНОСТИ: Лабораторные исследования). Некоторые люди (с недостаточным потреблением или всасыванием витамина B12 или кальция), по-видимому, предрасположены к развитию субнормальных уровней витамина B12.У этих пациентов могут быть полезны рутинные измерения уровня витамина B12 в сыворотке крови с интервалом в два-три года ».
Дефицит витамина B12 может способствовать онемению, покалыванию или боли в пальцах ног, стоп или пальцев, затруднениям при ходьбе, проблемам с памятью, депрессии, спутанности сознания и жжению языка. Любой, кто испытывает такие симптомы во время приема метформина, должен попросить врача, выписывающего рецепт, проверить статус витамина B12.
Другая читательница написала о болезни ее мужа метформином и нарушении функции почек:
Q. Мой муж много лет принимал метформин без каких-либо побочных эффектов. Затем его функция почек начала ухудшаться, поэтому его осмотрел специалист, который немедленно отменил метформин. Он сказал, что это лекарство очень сильно влияет на почки, и всем, у кого есть какие-либо изменения в функциях почек, не следует его принимать.
A. Как упоминалось выше, функцию почек необходимо регулярно контролировать, чтобы предотвратить именно такое осложнение.
Расстройство пищеварения, связанное с метформином (глюкофагом), обычно со временем уменьшается, но иногда сохраняется:
Q. У меня такой сильный понос, что иногда я боюсь выходить из дома. Еще у меня сильные газы и приступы болей в животе. Я подозреваю, что метформин принимаю от диабета, но мой врач говорит, что мои симптомы не связаны с моим лекарством.
Превацида, который я принимаю от изжоги, недостаточно, чтобы оправдать затраты. Я также испытываю боль и покалывание в пальцах ног.
A. Метформин (глюкофаг) может вызывать диарею, тошноту, изжогу, метеоризм и боль в животе.Кислотоподавляющие препараты, такие как лансопразол ( Prevacid ), омепразол ( Prilosec ) или эзомепразол ( Nexium ), не решат проблему полностью и могут помешать всасыванию витамина B12.
Чудо метформина против рака:
Прежде чем вы откажетесь от метформина из-за побочных эффектов и страшных историй, мы хотим рассказать вам о некоторых удивительных преимуществах этого препарата. Появляется все больше свидетельств того, что он может обладать впечатляющей противораковой активностью.В частности, есть данные, свидетельствующие о том, что метформин может снизить риск развития рака груди, рака печени, рака поджелудочной железы и колоректального рака у людей с диабетом и что общий риск развития рака у таких пациентов значительно ниже. Препарат не только снижает риск развития ряда распространенных видов рака, но и может уменьшить распространение рака после его диагностики.
Исследователи начинают выяснять один из предложенных механизмов противоопухолевого действия метформина, особенно при раке простаты.В исследовании, опубликованном в журнале Prostate Cancer and Prostatic Diseases (28 июля 2015 г.), сообщается, что эффективное лечение агрессивного или запущенного заболевания является сложной задачей.
Примечание исследователей:
Одна из потенциальных мишеней — раковые стволовые клетки (CSC). РСК описаны в нескольких солидных опухолях, включая рак простаты, и вносят вклад в терапевтическую резистентность и рецидив опухоли. Метформин, распространенный пероральный бигуанид, используемый для лечения диабета 2 типа, обладает противоопухолевым действием.В частности, метформин нацелен на ОСК при раке груди, раке поджелудочной железы, глиобластоме и раке толстой кишки ».
Используя метаболическую слабость раковых стволовых клеток, метформин теоретически делает эти проблемные клетки более уязвимыми для традиционных методов лечения рака и может снизить вероятность резистентности к раку и рецидива. Одно исследование показало, что у женщин с раком эндометрия вероятность рецидива была ниже, если они принимали метформин ( International Journal of Gynecological Cancer , Feb.2016).
Последние исследования метформина против рака простаты очень обнадеживают. Мужчины, получавшие лучевую терапию (дистанционное облучение или брахитерапию), чувствовали себя намного лучше, чем мужчины, не принимавшие метформин ( Canadian Journal of Urology , октябрь 2018 г.).
Последняя глава — Anti-Aging Activity:
Это звучит слишком хорошо, чтобы быть правдой. Может ли это старое лекарство от диабета замедлить биологическое старение?
В обзорной статье в журнале
Postepy Higieny i Medycyny Doswiadczainej (онлайн, 3 марта 2017 г.) авторы отмечают:«Интересно, что быстро растет количество литературы, демонстрирующей ее потенциал в терапии множественных болезней. другие расстройства, кроме диабета.Многие эпидемиологические анализы сообщают, что метформин может улучшить прогноз у онкологических больных, а также может предотвратить возникновение опухоли. Более того, есть данные, свидетельствующие о том, что метформин действует как фактор против старения и модулирует микробиоту, способствуя укреплению здоровья. Таким образом, метформин в настоящее время исследуется для новых применений ».
Авторы описывают потенциальные механизмы антивозрастного действия этого лекарства, а также способы борьбы с раком. Они характеризуют потенциал метформина на обоих фронтах как «многообещающий».”
Совсем недавно канадские ученые изучили влияние метформина на фиброз яичников ( Clinical Cancer Research , 9 октября 2019 г.). Исследование проводилось на мышах, а не на женщинах.
Однако исследователи пришли к выводу, что это
«предполагает потенциальное использование метформина в профилактике рака яичников».
Итог по метформину (глюкофагу):
Метформин — это старое лекарство от диабета, которое заново открывается из-за его потенциальной роли в борьбе с раком.Только время покажет, оправдает ли он ожидания.