Что такое плацента
Она связывает между собой два организма — матери и плода, обеспечивая его необходимыми питательными веществами.
Где находится и как выглядит плацента?
При нормально протекающей беременности плацента располагается в теле матки по ее задней (чаще) или передней стенке. Она полностью формируется к 15 16-й неделе беременности, после 20-й неделиначинается активный обмен через плацентарные сосуды. С 22 по 36 неделюбеременности происходит увеличение массы плаценты, и к 36 неделе она достигает полной функциональной зрелости.
Рисунок 1. Схематичное изображение места расположения плаценты в матке беременной женщины. Фото: Wikipedia (Public Domain)По внешнему виду плацента похожа на круглый плоский диск. К моменту родов масса плаценты составляет 500-600 г, диаметр — 15-18 см и толщину — 2-3 см. В плаценте различают две поверхности: материнскую, прилегающую к стенке матки, и противоположную — плодовую.
Функции плаценты
Фото: zffoto / freepik. com
com- Во-первых, через плаценту осуществляется газообмен: кислород проникает из материнской крови к плоду, а углекислый газ транспортируется в обратном направлении.
- Во-вторых, плод получает через плаценту питательные вещества, необходимые для его роста и развития. Необходимо помнить, что многие вещества (алкоголь, никотин, наркотические средства, многие лекарственные препараты, вирусы) легко проникают через нее и могут оказывать повреждающее действие на плод. Кроме того, с ее помощью плод избавляется от продуктов своей жизнедеятельности.
- В-третьих, плацента обеспечивает иммунологическую защиту плода, задерживая клетки иммунной системы матери, которые, проникнув к плоду и распознав в нем чужеродный объект, могли бы запустить реакции его отторжения. В тоже время плацента пропускает материнские антитела, защищающие плод от инфекций.
- В-четвертых, плацента играет роль железы внутренней секреции и синтезирует гормоны (хорионический гонадотропин человека (ХГЧ), плацентарный лактоген, пролактин и т.

В норме плацента вместе с оболочками (послед) рождается через 10-15 минут после рождения плода. Ее внимательно осматривают и отправляют на морфологическое исследование. Во-первых, очень важно убедиться в том, что плацента родилась целиком (то есть на ее поверхности отсутствуют повреждения и нет оснований считать, что кусочки плаценты остались в полости матки). Во-вторых, по состоянию плаценты можно судить о течении беременности (не было ли отслойки, инфекционных процессов и т.п.).
Что хотят знать о плаценте врачи?
Во время беременности важно выявить признаки нарушения функции плаценты — плацентарной недостаточности. Для этого во время ультразвукового исследования изучают структуру плаценты, ее расположение в полости матки, толщину, соответствие размеров плода сроку беременности. Кроме того, изучается кровоток в плацентарных сосудах.
Степень зрелости
Фото: wavebreakmedia-micro / freepik. com
comЭтот параметр, как говорят врачи, «ультразвуковой», то есть он зависит от плотности определяемых при ультразвуковом исследовании структур плаценты.
Различают четыре степени зрелости плаценты:
- В норме до 30 недель беременности должна определяться нулевая степень зрелости плаценты.
- Первая степень считается допустимой с 27 по 34 неделю.
- Вторая — с 34 по 39.
- Начиная с 37 недели может определяться третья степень зрелости плаценты.
В конце беременности наступает так называемое физиологическое старение плаценты, сопровождающееся уменьшением площади ее обменной поверхности, появлением участков отложения солей.
Место прикрепления
Фото: kuprevich / freepik.comОпределяется с помощью УЗИ. Как было сказано выше, при нормальной беременности плацента располагается в теле матки. Иногда при ультразвуковом исследовании в первой половине беременности обнаруживается, что плацента располагается в нижних отделах матки, доходя или даже перекрывая область внутреннего зева шейки матки.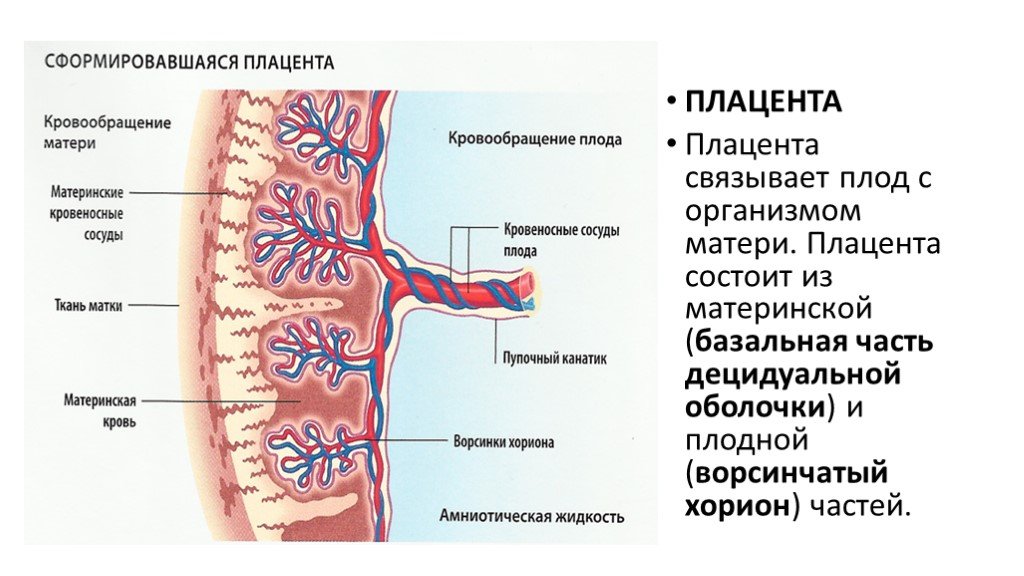 В дальнейшем, по мере прогрессирования беременности, плацента чаще всего смещается из нижних отделов матки верх. Однако, если после срока 32 недели плацента по-прежнему перекрывает область внутреннего зева, такое состояние называется * предлежанием плаценты**, что является серьезным осложнением беременности.
В дальнейшем, по мере прогрессирования беременности, плацента чаще всего смещается из нижних отделов матки верх. Однако, если после срока 32 недели плацента по-прежнему перекрывает область внутреннего зева, такое состояние называется * предлежанием плаценты**, что является серьезным осложнением беременности.
Предлежание плаценты может привести к развитию кровотечения, которое может возникать во II-III триместре беременности или во время родов.
Ультразвуковой снимок с предлежанием плаценты. Turk J Obstet Gynecol / ResearchGate (Creative Commons Attribution 2.5 Generic license)Толщина
Тоже определяется посредством ультразвукового исследования— плацентометрии: после установления места прикрепления плаценты отыскивается участок, где она имеет наибольший размер, который и определяется. Толщина плаценты, как уже было сказано, непрерывно увеличивается до 36-37 недель беременности (к этому сроку она составляет от 20 до 40 мм). Затем ее рост прекращается, и в дальнейшем толщина плаценты либо уменьшается, либо остается на том же уровне.
Отклонение от нормы хотя бы одного из этих показателей может свидетельствовать о неблагополучии в течение беременности.
Источники
- Tiwari D., Das CR., Sultana R., Kashyap N., Islam M., Bose PD., Saikia AK., Bose S. Increased homocysteine mediated oxidative stress as key determinant of hepatitis E virus (HEV) infected pregnancy complication and outcome: A study from Northeast India. // Infect Genet Evol — 2021 — Vol — NNULL — p.104882; PMID:33905889
- Salmanian B., Belfort MA., Shamshirsaz AA. The risk of placenta accreta spectrum in women with in vitro fertilization in different populations. // Am J Obstet Gynecol — 2021 — Vol — NNULL — p.; PMID:33905744
- Olmos-Ortiz A., Olivares-Huerta A., García-Quiroz J., Zariñán T., Chavira R., Zaga-Clavellina V., Avila E., Halhali A., Durand M., Larrea F., Díaz L. Placentas associated with female neonates from pregnancies complicated by urinary-tract infections have higher cAMP content and cytokines expression than males.
 // Am J Reprod Immunol — 2021 — Vol — NNULL — p.e13434; PMID:33905581
// Am J Reprod Immunol — 2021 — Vol — NNULL — p.e13434; PMID:33905581 - Tandl V., Hoch D., Bandres-Meriz J., Nikodijevic S., Desoye G., Majali-Martinez A. Different regulation of IRE1α and eIF2α pathways by oxygen and insulin in ACH-3P trophoblast model. // Reproduction — 2021 — Vol — NNULL — p.; PMID:33904834
- Ji S., Gumina D., McPeak K., Moldovan R., Post MD., Su EJ. Human placental villous stromal extracellular matrix regulates fetoplacental angiogenesis in severe fetal growth restriction. // Clin Sci (Lond) — 2021 — Vol — NNULL — p.; PMID:33904582
- Shmeleva EV., Colucci F. Maternal natural killer cells at the intersection between reproduction and mucosal immunity. // Mucosal Immunol — 2021 — Vol — NNULL — p.; PMID:33903735
- Moreno-Sepulveda J., Espinós JJ., Checa MA. Lower risk of adverse perinatal outcomes in natural versus artificial frozen-thawed embryo transfer cycles: a systematic review and meta-analysis. // Reprod Biomed Online — 2021 — Vol — NNULL — p.
 ; PMID:33903031
; PMID:33903031 - Owen MD., Cassidy AL., Weeks AD. Why are women still dying from obstetric hemorrhage? A narrative review of perspectives from high and low resource settings. // Int J Obstet Anesth — 2021 — Vol — NNULL — p.102982; PMID:33903002
- Liu CN., Yu FB., Xu YZ., Li JS., Guan ZH., Sun MN., Liu CA., He F., Chen DJ. Prevalence and risk factors of severe postpartum hemorrhage: a retrospective cohort study. // BMC Pregnancy Childbirth — 2021 — Vol21 — N1 — p.332; PMID:33902475
- Munoz JL., Kimura AM., Xenakis E., Jenkins DH., Braverman MA., Ramsey PS., Ireland KE. Whole blood transfusion reduces overall component transfusion in cases of placenta accreta spectrum: a pilot program. // J Matern Fetal Neonatal Med — 2021 — Vol — NNULL — p.1-6; PMID:33902384
Плацентарная недостаточность — что это и как лечить
- Виды и причины плацентарной недостаточности
- Диагностика плацентарной недостаточности
- Лечение плацентарной недостаточности
Большинство женщин знают, что плацента связывает маму и малыша во время беременности и при помощи нее к малышу поступают питательные вещества и кислород.
Бывают ли такие ситуации, когда плацента перестает правильно и полноценно выполнять свою функцию? Можно ли как то предотвратить это?
Какую функцию выполняет плацента
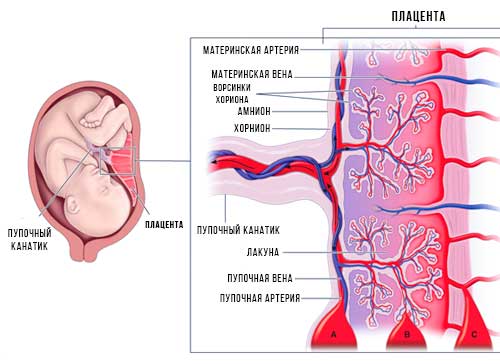
Итак, плацента – это важный орган, который образуется только во время беременности. Образуется плацента из хориона — зародышевых оболочек плода. В самом начале беременности ворсины хориона – выросты оболочки — равномерно покрывают всю поверхность плодного яйца, начиная со второго месяца беременности с одной стороны плодного яйца ворсины начинают удлиняться, увеличиваться в размерах и формируют плаценту.
Внутри ворсин течет кровь малыша, а снаружи они омываются кровью матери. Между кровотоком мамы и малыша расположен всего один слой клеток, который и играет роль барьера между организмом матери и ребенка. Благодаря этой мембране кровь матери и плода не смешивается.
Однако в последние годы стало известно, что клетки крови плода все-таки проникают через плацентарный барьер в кровоток матери и благодаря этому стало возможным проведение генетических анализов и определение хромосомных аномалий, резуса фактора и пола плода по крови беременной женщины (неинвазивный пренатальный тест).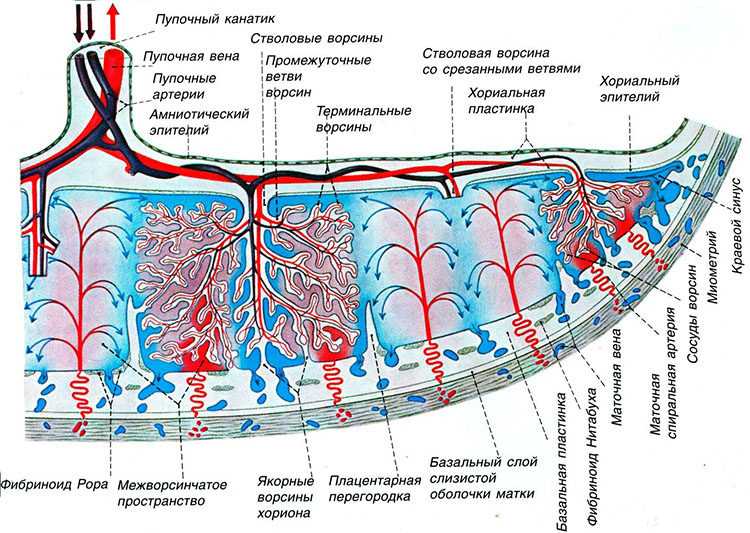
В плаценте происходит постоянный обмен веществ между мамой и ребенком. Из материнской крови к плоду поступает кислород и питательные вещества, от плода обратно к матери углекислый газ и продукты обмена, подлежащие выведению из организма.
Плацентарный барьер выполняет иммунологическую функцию, поскольку пропускает некоторые защитные антитела – клетки крови, обеспечивающие борьбу с инфекционными агентами, кроме того он является непроницаемым для некоторых вредных веществ, вирусов и бактерий. К сожалению, плацентарный барьер легко преодолевают наркотические вещества, алкоголь, никотин, компоненты многих лекарств и некоторые вирусы.
Важной функцией плаценты является выработка гормонов и биологически активных веществ. В первую очередь это гормоны, важные для успешного вынашивания беременности, например хорионический гонадотропин, плацентарный лактоген, эстрогены и др.
К сожалению, не всегда все складывается вполне благополучно. В силу самых различных причин на разных сроках беременности могут происходить отклонения в развитии и функционировании плаценты.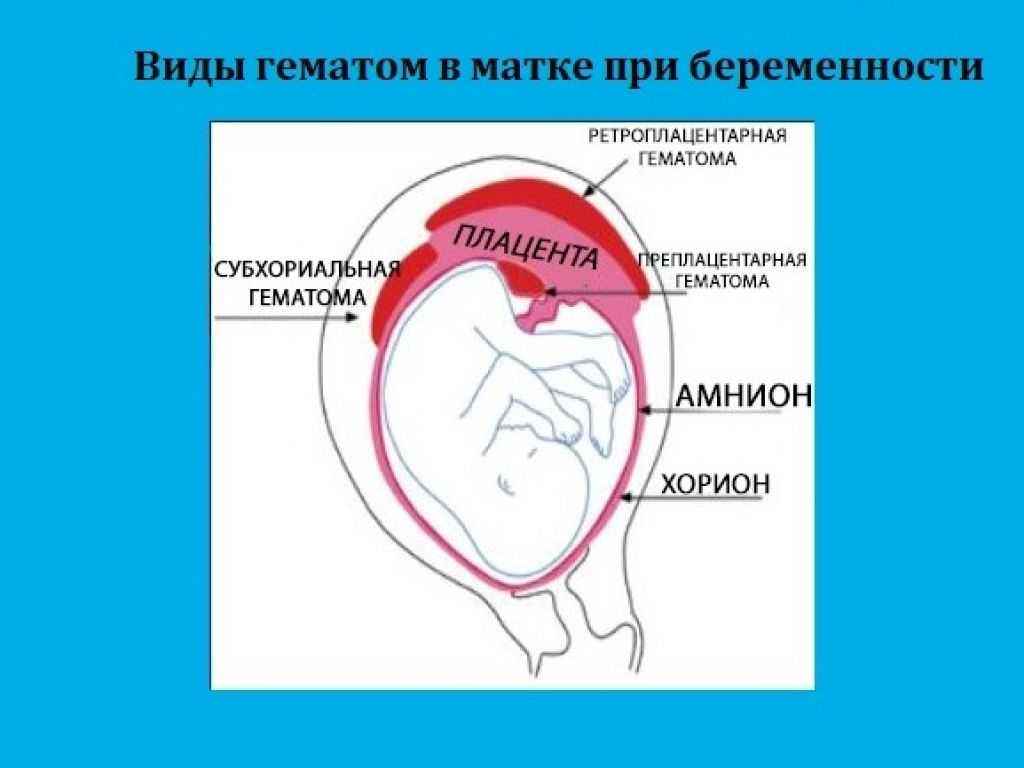 Изменения эти никогда не проходят бесследно для мамы и малыша, а зачастую имеют грозные последствия.
Изменения эти никогда не проходят бесследно для мамы и малыша, а зачастую имеют грозные последствия.
Если плацента перестает выполнять свои функции в полной мере, развивается так называемая плацентарная недостаточность. По сути, она заключается в ухудшении кровообращения в системе мать-плацента-плод.
Виды и причины плацентарной недостаточности
Врачи различают острую и хроническую плацентарную недостаточность:
Острая плацентарная недостаточность
Это состояние, требующее экстренного вмешательства врачей. Она характеризуется стремительным ухудшением плацентарного кровотока. Острая плацентарная недостаточность возникает в основном в результате отслойки плаценты или гибели отдельных участков ткани плаценты например при образовании тромбов в сосудах. Причиной отслойки может послужить травма живота, антифосфолипидный синдром.
Фосфолипиды – это сложные жиры, которые входят в состав оболочек всех клеток организма. В ряде случаев иммунная система организма вырабатывает большое количество антител к некоторым собственным фосфолипидам и белкам, связывающим эти липиды.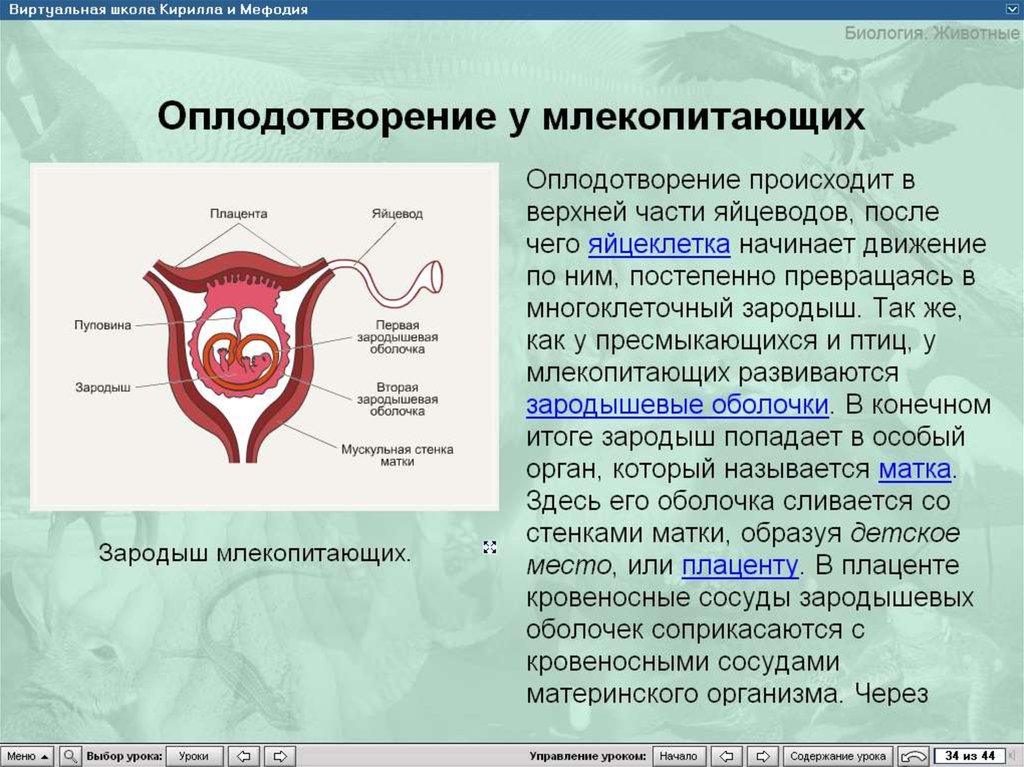
Антифосфолипидный синдром является самой частой причиной тромботических осложнений при беременности, в том числе причиной отслойки плаценты и острой плацентаной недостаточности.
Вызвать отслойку плаценты может также тяжелое течение гестоза – грозного осложнения второй половины беременности, проявляющееся отеками, повышением давления и появлением белка в моче.
Острая плацентарная недостаточность развивается при отслойке более 2/3 поверхности плаценты.
В случае развития острой плацентарной недостаточности необходимо максимально быстро провести операцию кесарева сечения для сохранения жизни малыша и мамы.
Хроническая плацентарная недостаточность
Значительно чаще у беременных женщин встречается хроническая плацентарная недостаточность. В этом случае происходит нарушение формирования и созревания плаценты, уменьшается маточно-плацентарный и плодово-плацентарный кровотоки, ограничивается газообмен и обмен веществ в плаценте, снижается синтез плацентарных гормонов.
Причинами плацентарной недостаточности чаще всего являются перенесенные аборты, особенно хирургический аборт при первой беременности, курение, при этом количество и крепость выкуриваемых сигарет значения не имеют, поскольку на формировании неполноценных сосудов плаценты негативное действие оказывает табачный дым, а не никотин.
В группу риска по развитию плацентарной недостаточности входят также женщины с хроническими заболеваниями, такими как артериальная гипертензия, железодефицитная анемия, пиелонефрит, сахарный диабет, заболевания щитовидной железы.
Немаловажное значение в формировании хронической плацентарной недостаточности играет патология матки: эндометриоз, пороки развития матки (седловидная, двурогая). Фактором риска врачи считают также миому матки. Безусловно, целый ряд лекарственных средств оказывает неблагоприятное влияние на формирование плаценты и развитие плода. В настоящее время определен список препаратов, не разрешенных к применению во время беременности.
Также большое значение в развитии плацентарной недостаточности имеет тромбофилия – повышенная склонность организма к образованию сгустков крови — тромбов в сосудах.
В некоторых случаях плацентарная недостаточность может быть обусловлена наличием хромосомных нарушений у плода, в частности при синдромах Дауна (наличие дополнительной 21 хромосомы у плода) или синдроме Эдвардса (дополнительная 18 хромосома у плода) уже в ранние сроки беременности диагностируется нарушение функции плаценты.
Следует отметить, что среди осложнений беременности, наиболее часто приводящих к развитию хронической плацентарной недостаточности, существенным фактором является преэклампсия (или поздний гестоз) – это осложнения второй половины беременности, проявляющееся отеками, повышением давления и появлением белка в моче.
Независимо от факторов, способствующих развитию плацентарной недостаточности, в основе ее лежат нарушения кровообращения в маточно-плацентарном комплексе, приводящие к нарушению всех функций плаценты. Следовательно, симптомы хронической плацентарной недостаточности будут обусловлены недостатком поступления кислорода и питательных веществ к плоду.
Это прежде всего, задержка внутриутробного развития плода – отставание размеров плода и замедление темпов его роста. Часто имеют место изменение двигательной активности плода. Сначала может быть некоторое усиление движений, а затем уменьшение. Нарушение защитной функции плаценты приводит к внутриутробному инфицированию плода под действием проникающих через плаценту патогенных (болезнетворных) микроорганизмов. Плод, развитие которого происходит в условиях плацентарной недостаточности, в значительно большей степени подвержен риску травматизации в родах, у них отмечается нарушение адаптации к внеутробной жизни, повышенная заболеваемость в первый год жизни.
По времени возникновения врачи разделяют плацентарную недостаточность на раннюю и позднюю.
Ранняя (или первичная) плацентарная недостаточность
Развивается до 16 недель беременности. Она возникает уже на этапе формирования плаценты и связана с заболеваниями беременной женщины, имеющимися до беременности, к примеру с патологией матки, хронической артериальной гипертензией, эндокринологическими заболеваниями. При этом происходит формированием неполноценных сосудов в плаценте.
Поздняя (или вторичная) плацентарная недостаточность
Возникает после 16 недель беременности и чаще всего связана с заболеваниями, возникшими уже во время беременности. Чаще всего это железодефицитная анемия (то есть снижение концентрации гемоглобина и железа в крови), гестационный сахарный диабет (то есть нарушение усвоения организмом глюкозы, возникшее на фоне беременности), перенесенные вирусные и бактериальные инфекции.
Важным является подразделение плацентарной недостаточности на компенсированную и декомпенсированные формы.
Компенсированная плацентарная недостаточность
Развивается, к примеру, при угрозе прерывания беременности и нетяжелых формах позднего гестоза, в случае, если эти осложнения успешно поддаются медикаментозной коррекции.
Декомпенсированная плацентарная недостаточность
Вызывает развитие задержки развития плода, хронической внутриутробной гипоксии, вплоть до гибели плода.
Ознакомьтесь подробнее с услугами:
- Узи беременным
- Узи 1 триместра беременности
- Узи сосудов при беременности
- Консультация гинеколога
Диагностика плацентарной недостаточности
Лечить уже развившуюся плацентарную недостаточность практически невозможно, поэтому врачи активно стремятся выявлять беременных женщин, угрожаемых в отношении формирования нарушений функции плаценты. Если плацентарная недостаточность выявляется в 3 триместре беременности, эффективного лечения, к сожалению, не существует. Поэтому очень активно в настоящее время применяются все способы выявления в ранние сроки беременности тех женщин, в формировании плаценты которых произошли нарушения.
В первую очередь, при постановке на учет по беременности выявляют максимально значимые факторы риска – курение, перенесенные аборты, отягощенную наследственность (низкий вес при рождении, склонность к тромбозам), наличие хронических заболеваний сердца, сосудов, сахарного диабета.
Профилактические мероприятия против развития плацентарной недостаточности особенно актуальны и необходимы до 16-17 недель беременности, когда происходит формирование структур плаценты.
Значимую помощь в оценке риска развития плацентарной недостаточности оказывает пренатальный скрининг, который проводится в 11-14 недель беременности. Он проводится для выявления синдромов Дауна, Эдвардса и др. хромосомных болезней у плода. В настоящее время самым актуальным является проведение комплексного ранний скрининг беременной на прогнозирование риска развития плацентарной недостаточности, преэклампсии и внутриутробной задержки развития плода. Поскольку данный вид диагностики относится к самым современным и передовым, к сожалению, он пока не включен в перечень услуг, предоставляемых в женской консультации в рамках ОМС, но доступен всем желающим в центрах пренатальной диагностики.
Определение белков, вырабатываемых плацентой
В первую очередь проводят определение белка РАРР-А, он является также маркером хромосомных аномалий плода. Снижение концентрации РАРР-А в крови в 11-14 недель беременности встречается у беременных женщин, имеющих высокий риск плацентарной недостаточности и задержки развития плода.
Второй гормон плаценты, который помогает в оценке рисков плацентарной недостаточности – PIGF (плацентарный фактор роста). Его концентрация в крови снижается задолго до первых проявлений плацентарной недостаточности. Его определение применяют не настолько широко, как PAPP-A, но тем не менее многие лаборатории уже включили данный белок в пренатальный скрининг 1 триместра. Крайне важное значение при проведении скрининга 1 триместра имеет измерение кровотоков в сосудах матки. Однозначно доказано, что сужение сосудов матки, определяемое при исследовании, свидетельствует о неполноценности формирования плаценты, которое будет ухудшаться с увеличением срока беременности и приведет к снижению питания малыша и снабжения его кислородов, то есть к развитию плацентарной недостаточности и задержки развития плода. При нормальных размерах маточных сосудов в 11-14 недель беременности риск тяжелой плацентарной недостаточности ничтожно мал.
При нормальных размерах маточных сосудов в 11-14 недель беременности риск тяжелой плацентарной недостаточности ничтожно мал.
Следующее обязательное скрининговое ультразвуковое исследование проводится в 20-21 неделю беременности. При этом обязательно проводят измерения плода, чтобы оценить, нет ли отставания в росте. Ведь при кислородном голодании замедляются темпы роста плода и размеры его начинают отставать от нормы для каждого срока беременности. Кроме того врач обязательно оценивает состояние и зрелость плаценты. Во время УЗИ проводится также допплерометрия сосудов матки для выявления ранних изменений, предшествующих клиническим проявлениям плацентарной недостаточности.
У пациенток, относящихся к группе высокого риска кроме УЗИ и допплерометрии проводят также суточное мониторирование колебаний артериального давления, определение количества белка в анализе мочи, собранном за сутки, оценивают показатели системы свертывания крови.
Третье УЗИ проводится всем будущим мамам в 30–34 недели беременности. Врач измеряет окружность головы и живота крохи, длину костей его ручек и ножек, и вычисляет предполагаемый вес плода. Эти измерения позволяют доктору убедиться в том, что малыш развивается нормально. Также имеет значение строение плаценты, наличие в ней признаков старения, вследствие чего она обычно перестает полноценно снабжать малыша кровью, а, значит, ему перестает хватать кислорода и питательных веществ и развитие ребенка нарушается. Во время УЗИ оценивается количество и вид околоплодных вод, которые также могут изменяться при внутриутробном страдании плода.
Врач измеряет окружность головы и живота крохи, длину костей его ручек и ножек, и вычисляет предполагаемый вес плода. Эти измерения позволяют доктору убедиться в том, что малыш развивается нормально. Также имеет значение строение плаценты, наличие в ней признаков старения, вследствие чего она обычно перестает полноценно снабжать малыша кровью, а, значит, ему перестает хватать кислорода и питательных веществ и развитие ребенка нарушается. Во время УЗИ оценивается количество и вид околоплодных вод, которые также могут изменяться при внутриутробном страдании плода.
Допплерометрия
Допплерометрия сосудов плаценты и пуповины (метод исследования скоростей кровотоков в этих сосудах) так же позволяет оценить самочувствие малыша. Доктор исследует кровоток в артериях матки, пуповины, сердца и мозга ребенка. Это исследование позволяет определить, хорошо ли работает плацента, нет ли признаков нехватки кислорода у малыша, или развития гестоза у мамы. При снижении скорости кровотока в каком-либо сосуде можно говорить о нарушениях питания плода различной степени тяжести.
Вовремя проведенное обследование позволяет выявить начальные стадии дефицита кровоснабжения. В таких случаях лечение сможет предотвратить грозные осложнения, такие как гипоксия и внутриутробная задержка развития малыша. Допперометрию проводят в 20–21 неделю и в 30-32 недели беременности, при наличии изменений, контроль осуществляют минимум каждые две недели.
Кардиотокография
Это важный метод оценки состояния плода. Проводится КТГ при сроке беременности 33 недели и более, поскольку только на этом этапе внутриутробного развития малыша устанавливается полноценная регуляция деятельности сердечно-сосудистой системы плода центрами спинного и головного мозга. Запись сердцебиений плода проводят в течение 20–40 минут, а при необходимости исследование может быть продлено до 1,5 часов.
Аппарат регистрирует и записывает частоту сердцебиений малыша. Врач акушер-гинеколог оценивает кривую записи сердцебиений, эпизоды урежения и резкого учащения частоты сердечных сокращений плода и на основании этих данных делает заключение о том, насколько комфортно малыш чувствует себя в животе у мамы. К примеру, при снижении концентрации кислорода в крови плода, уменьшается и его поступление к клеткам нервной системы, что в свою очередь отражается на частоте сердечных сокращений. При нормальном течении беременности КТГ проводят после 33 недели 1 раз в 10–14 дней, иногда чаще. В некоторых клиниках в настоящее время предлагается услуга постоянного КТГ-мониторирования, что приобретает актуальность при наличии признаков плацентарной недостаточности. Беременной женщине выдается мониторчик, который регистрирует изменения сердечной деятельности малыша и эти данные по интернету передаются лечащему врачу.
К примеру, при снижении концентрации кислорода в крови плода, уменьшается и его поступление к клеткам нервной системы, что в свою очередь отражается на частоте сердечных сокращений. При нормальном течении беременности КТГ проводят после 33 недели 1 раз в 10–14 дней, иногда чаще. В некоторых клиниках в настоящее время предлагается услуга постоянного КТГ-мониторирования, что приобретает актуальность при наличии признаков плацентарной недостаточности. Беременной женщине выдается мониторчик, который регистрирует изменения сердечной деятельности малыша и эти данные по интернету передаются лечащему врачу.
Лечение плацентарной недостаточности
Специфических способов лечения плацентарной недостаточности в настоящее время не существует, поскольку нет лекарственных препаратов, которые избирательно улучшают маточно-плацентарный кровоток. Именно поэтому все меры борьбы с плацентарной недостаточностью направлены на профилактику. Если пациентка относится к группе высокого риска по развитию плацентарной недостаточности, с раннего срока беременности ей назначают лекарственные препараты, эффективность которых хорошо доказана и которые предупреждают раннее развитие выраженных нарушений функции плаценты.
Если во время проведения дополнительных методов оценки состояния плода выявляются начальные нарушения поступления кислорода к малышу, проводится медикаментозное лечение, направленное на увеличение притока крови и кислорода через плаценту и обязательные контрольные обследования на фоне проводимой терапии. Если изменения серьезные и малыш испытывает выраженный дефицит кислорода и питательных веществ, состояние его страдает, то в таких случаях проводится экстренное родоразрешение.
Эмбриология, плацента — StatPearls — NCBI Bookshelf
Введение
Плацента — жизненно важный орган, выполняющий множество функций, таких как эндокринная, иммунная и физиологическая. Плацента формируется постепенно в течение первых трех месяцев беременности, а после четвертого месяца растет параллельно развитию матки. После завершения он напоминает губчатый диск диаметром 20 см и толщиной 3 см. Это временный орган, генетические характеристики которого идентичны характеристикам развивающегося ребенка.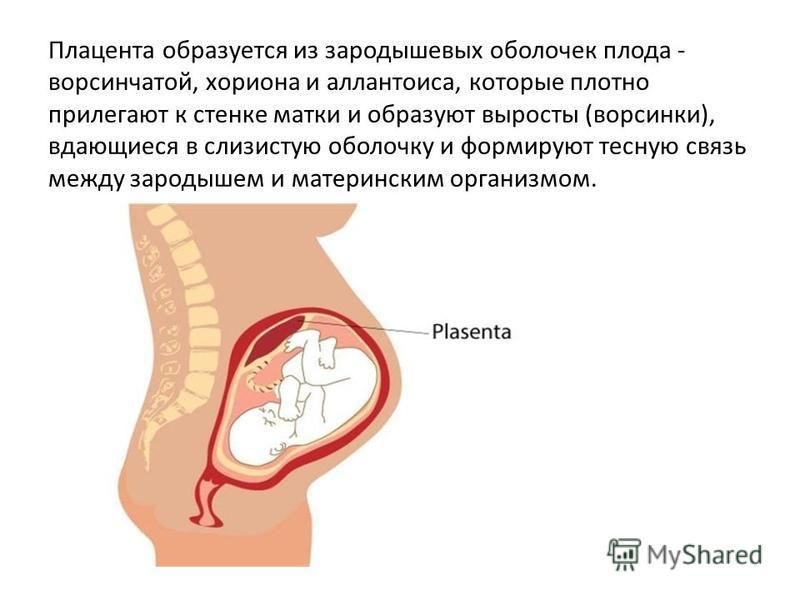 Плацента взаимодействует с окружающей средой, в которой она находится, и наоборот. Правильное развитие плаценты необходимо для успешной беременности. Этот тонкий орган состоит из нескольких слоев ткани, которые должны нормально развиваться для правильного функционирования во время беременности. Без надлежащего функционирования могут быть разрушительные последствия для беременности.
Плацента взаимодействует с окружающей средой, в которой она находится, и наоборот. Правильное развитие плаценты необходимо для успешной беременности. Этот тонкий орган состоит из нескольких слоев ткани, которые должны нормально развиваться для правильного функционирования во время беременности. Без надлежащего функционирования могут быть разрушительные последствия для беременности.
Развитие
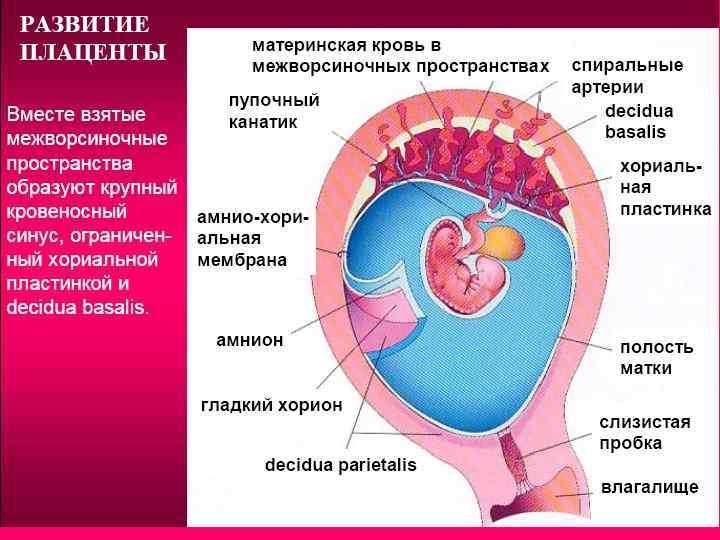
Плацента представляет собой орган плода, состоящий из паренхимы, хориона, амниона и пуповины. Структуры плода формируются из зиготы и поэтому отделяют плод от эндометрия. Ткани плода формируются из хорионического мешка, в который входят амнион, хорион, желточный мешок и аллантоис. Эти ткани доставляются после рождения. Материнская часть происходит из эндометрия и называется децидуальной оболочкой. Децидуальная оболочка состоит из трех частей: базальная децидуальная оболочка (глубоко в месте имплантации), капсульная децидуальная оболочка (покрывает место имплантации) и париетальная децидуальная оболочка (все остальное) [1].
После оплодотворения оплодотворенная яйцеклетка превращается в морулу, которая разовьется в эмбрион и плодную плаценту. Внутренняя клеточная масса развивается в эмбриобласт, а наружная клеточная масса — в трофобласт. Затем морула поглощает жидкость и образует бластоцисту с трофобластом, окружающим внутреннюю клеточную массу и жидкость. Бластоциста имплантируется в матку примерно через шесть дней после оплодотворения. Контакт трофобласта с эндометрием вызывает развитие синцитиотрофобласта, который секретирует хорионический гонадотропный гормон человека (ХГЧ), и цитотрофобласта, который секретирует ферменты, разрушающие связь между клетками эндометрия, поэтому синцитиотрофобласт может проникнуть в стенку эндометрия. И цитотрофобласт, и синцитиотрофобласт являются частью хориона, который развивается в плаценту вместе с экстраэмбриональной мезодермой.
Хорион образует плаценту и состоит из синцитиотрофобласта, цитотрофобласта и экстраэмбриональной мезодермы. Цитотрофобласт врастает в синцитиотрофобласт в виде пальцевидных отростков, которые называются первичными ворсинками хориона. Внезародышевая мезодерма разделяется на соматическую и внутренностную мезодерму, а соматическая мезодерма прорастает в первичные ворсинки, образуя вторичные ворсинки. Мезенхима дает начало клеткам крови и сосудам, которые при формировании обозначают третичные ворсинки. От ворсинок отрастают капиллярные русла, которые соединяются с сердцем зародыша. Материнская кровь, текущая по эмбриональным капиллярам, обеспечивает плод кислородом и питательными веществами. Ворсинки продолжают расти и разветвляются на хорион ворсинок, который представляет собой плаценту плода.[5]
Внезародышевая мезодерма разделяется на соматическую и внутренностную мезодерму, а соматическая мезодерма прорастает в первичные ворсинки, образуя вторичные ворсинки. Мезенхима дает начало клеткам крови и сосудам, которые при формировании обозначают третичные ворсинки. От ворсинок отрастают капиллярные русла, которые соединяются с сердцем зародыша. Материнская кровь, текущая по эмбриональным капиллярам, обеспечивает плод кислородом и питательными веществами. Ворсинки продолжают расти и разветвляются на хорион ворсинок, который представляет собой плаценту плода.[5]
По мере развития клетки цитотрофобласта продолжают расширяться через синцитиотрофобласт, чтобы в конечном итоге сформировать цитотрофобластическую оболочку. По мере повышения уровня прогестерона соединительная ткань децидуальной оболочки превращается в «клетки децидуальной оболочки», которые помогают защитить матку от инвазии синцитиотрофобласта. По мере роста мешка капсульная децидуальная оболочка ворсинок дегенерирует и в конечном итоге исчезает, сливаясь с париетальной децидуальной оболочкой.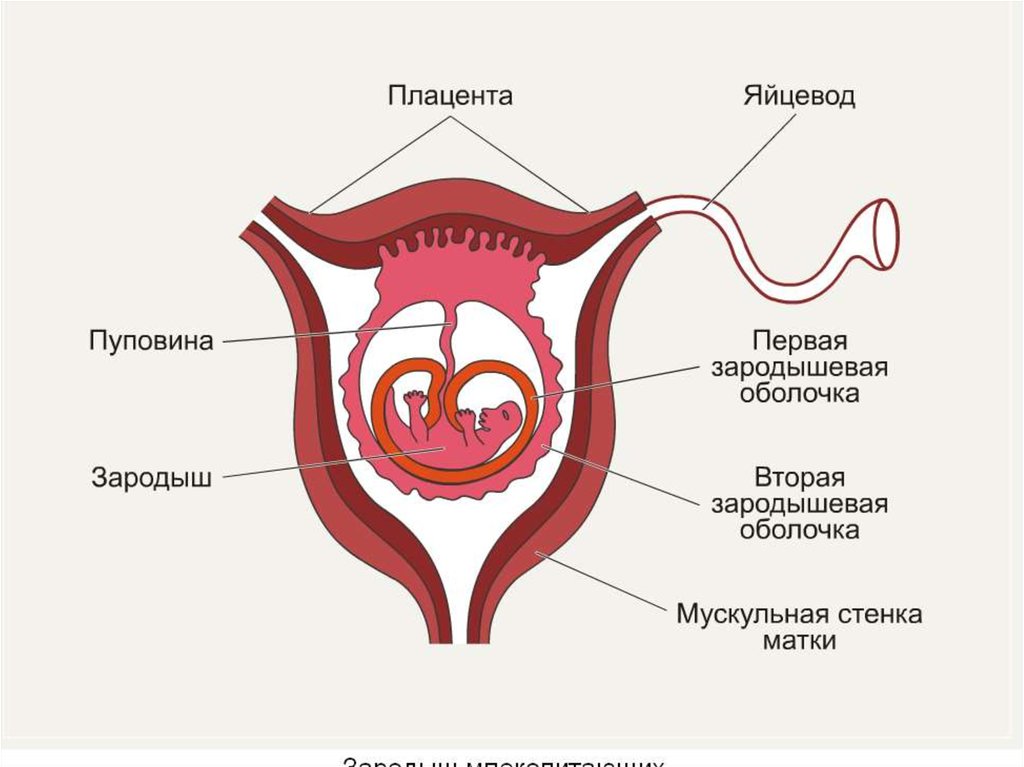
Амниотический мешок увеличивается быстрее, чем хорионический мешок, что приводит к тому, что они в конечном итоге соприкасаются и сливаются в амниохориальную мембрану. Затем амниохориальная мембрана сливается с капсульной децидуальной оболочкой и, в конечном счете, с париетальной децидуальной оболочкой для обеспечения стабильности. Амниохориальная оболочка разрывается во время родов. Амниохориальная оболочка с сосудами плода составляет хорионическую пластинку. Части базальной децидуальной оболочки врастают в пластинку хориона, разделяя ее на отдельные перегородки, называемые семядолями, каждая из которых содержит стволовые ворсинки.
Плодо-материнское соединение обеспечивает стабильность хориона. Ворсинки хориона, прикрепляющиеся к базальной децидуальной оболочке, служат якорем хорионического мешка плода к эндометрию. Сосуды эндометрия, называемые спиральными артериями, проходят через отверстия в цитотрофобластической оболочке и располагаются внутри ворсинок, где они выпускают материнскую кровь для омывания ворсинок хориона в каждой семядоле; это позволяет материнской крови снабжать плод кислородом и питательными веществами через плацентарную мембрану. Вены эндометрия затем дренируют кровь. Хотя сосуды плода омываются материнской кровью, в норме эритроциты матери и плода не смешиваются [7].
Вены эндометрия затем дренируют кровь. Хотя сосуды плода омываются материнской кровью, в норме эритроциты матери и плода не смешиваются [7].
Плацентарная оболочка — это место, где мать и плод обмениваются газами, питательными веществами и т. д. Мембрана образуется из синцитиотрофобласта, цитотрофобласта, эмбриональной соединительной ткани (вартоново желе) и эндотелия кровеносных сосудов плода.
Пуповина служит для прикрепления плода к плаценте и состоит из двух пупочных артерий и одной пупочной вены.
Клеточная
Плацента имеет несколько клеточных структур для защиты здоровья плода. Мы можем найти вещества, которые являются частью суперсемейства АТФ-связывающих кассет (ABC), такие как белок множественной лекарственной устойчивости типа 1, белок устойчивости к раку молочной железы, белок множественной лекарственной устойчивости, подобный белкам типа 2 и 5.
Плаценту можно рассматривать как иммунный и эндокринный орган. Он продуцирует многие гормоны и факторы роста в аутокринном и паракринном режимах, такие как прогестерон, кортикотропин-рилизинг-гормон, хорионический гонадотропин человека, плацентарный лактоген человека, фактор роста фибробластов и многие другие.
Биохимический
Плацента выполняет несколько метаболических функций, жизненно важных для здорового роста плода. Плацента может производить собственный гликоген и холестерин из материнской глюкозы и жирных кислот соответственно. Гликоген запасается в качестве энергии для плода, а холестерин используется для производства гормонов, таких как прогестерон, эстроген и глюкокортикоиды. Он также синтезирует пептидные гормоны, такие как хорионический гонадотропин человека (ХГЧ) и плацентарный лактоген человека (hPL), гормон роста (GH), фактор роста эндотелия сосудов (VEGF), кортикотропин-рилизинг-гормон (CRH), инсулиноподобный фактор роста (IGF). ), плацентарный фактор роста (PIGF) и цитокины.]
Молекулярный
Несколько молекул взаимодействуют с плацентой. Например, лептин обеспечивает здоровье плаценты благодаря своему действию в качестве гомеостатического агента, пролиферации и синтеза белка в качестве антиапоптотической молекулы. В свою очередь лептин находится под контролем других веществ, таких как инсулин, многие факторы роста, хорионический гонадотропин человека, стероиды и гипоксия.
Функция
Плацента является средством связи между мамой и плодом. В плацентарной оболочке происходит обмен веществ между матерью и плодом. Этот обмен необходим для переноса газов, электролитов, гормонов, материнских антител, отходов плода и питательных веществ, таких как вода, аминокислоты, глюкоза, витамины и свободные жирные кислоты. Отходы плода включают мочевину, мочевую кислоту и билирубин. Также происходит обмен альфа-фетопротеина и других белков. Эти переносы полезны для плода, но многие вредные вещества могут проникать через плацентарную мембрану, например, некоторые лекарства, живые вакцины, угарный газ, анти-Rh-антитела и некоторые инфекционные агенты (инфекции ToRCHEs).[10][11] ] Сопротивление растворителя — это объемный поток воды, который приносит питательные вещества через плацентарную мембрану в каждую семядолю для поглощения. Чем выше давление, тем больше питательных веществ будет поглощено.[12] Растворенные вещества и газы поглощаются путем простой диффузии в зависимости от их молекулярного состава и свойств. Кислород и углекислый газ хорошо проникают через ткани плаценты из-за их липофильности. Их обмен ограничен перфузией, что может вызвать ограничение роста плода при тканевой гипоксии.[13] Плацента также использует каналы для транспорта ионов по их электрохимическому градиенту, облегченную диффузию глюкозы с использованием белков-носителей и активный транспорт некоторых растворенных веществ.
Кислород и углекислый газ хорошо проникают через ткани плаценты из-за их липофильности. Их обмен ограничен перфузией, что может вызвать ограничение роста плода при тканевой гипоксии.[13] Плацента также использует каналы для транспорта ионов по их электрохимическому градиенту, облегченную диффузию глюкозы с использованием белков-носителей и активный транспорт некоторых растворенных веществ.
Из-за многочисленных питательных свойств многие млекопитающие, помимо человека, имеют привычку поедать извергнутую плаценту после родов.
Механизм
Кровообращение плода течет от плода к двум пупочным артериям (деоксигенированным), затем к хорионическим артериям в семядолях, через капиллярные русла для обмена газами с материнской кровью, затем обратно к плоду через единственную пупочную вену ( кислородом).
Тестирование
Биопсия ворсин хориона (CVS) — это либо трансабдоминальная, либо трансцервикальная процедура, при которой врачи берут образцы плаценты на сроке от 10 до 13 недель беременности для генетического тестирования. Этот тест выгоден тем, что его можно сделать намного раньше, чем амниоцентез, и, следовательно, получить результаты скрининга раньше. Если результаты приводят к прерыванию беременности, существует меньше рисков, чем позднее прерывание. Более ранняя беременность также приводит к менее точным результатам. Осложнения процедуры могут включать инфекцию, кровотечение, повреждение плода и гибель плода.[15][16]
Этот тест выгоден тем, что его можно сделать намного раньше, чем амниоцентез, и, следовательно, получить результаты скрининга раньше. Если результаты приводят к прерыванию беременности, существует меньше рисков, чем позднее прерывание. Более ранняя беременность также приводит к менее точным результатам. Осложнения процедуры могут включать инфекцию, кровотечение, повреждение плода и гибель плода.[15][16]
Амниоцентез — аналогичная трансабдоминальная процедура, при которой берутся амниотические жидкости для генетического анализа. Эту процедуру можно проводить в любое время после 15 недель. Амниотическая жидкость содержит клетки и вещества, созданные плодом, которые можно измерять для оценки таких заболеваний, как синдром Дауна, инфекции, дефекты нервной трубки, определение группы крови плода и развитие легких. Риски аналогичны CVS, включая инфекцию, повреждение плода или гибель плода, а также подтекание амниотической жидкости.[17]
Патофизиология
В норме смешение крови плода и матери не происходит. Хотя это возможно при специфических инфекционных агентах или небольших разрывах плацентарной оболочки, которые могут случиться во время родов. Если в мембране есть разрывы, материнские эритроциты могут попасть в кровоток плода и наоборот. Бледная трепонема (сифилитическая инфекция) может преодолевать барьер без разрывов мембраны. Toxoplasma gondii (токсоплазменная инфекция) может создавать собственные разрывы в мембране, проникать в кровоток плода и заражать его.
Хотя это возможно при специфических инфекционных агентах или небольших разрывах плацентарной оболочки, которые могут случиться во время родов. Если в мембране есть разрывы, материнские эритроциты могут попасть в кровоток плода и наоборот. Бледная трепонема (сифилитическая инфекция) может преодолевать барьер без разрывов мембраны. Toxoplasma gondii (токсоплазменная инфекция) может создавать собственные разрывы в мембране, проникать в кровоток плода и заражать его.
Эритробластоз плода, также называемый гемолитической болезнью новорожденных, возникает, когда мать вырабатывает антитела к резус-фактору плода после контакта резус-отрицательной матери с резус-положительной кровью плода. Мать вырабатывает антитела IgG к резус-фактору, которые могут проникать через плаценту. Первая беременность не является проблемой, потому что маме требуется время, чтобы вызвать эту реакцию, но это может вызвать проблемы при будущих беременностях резус-положительным плодом. Антитела могут проникать через плаценту и атаковать эритроциты плода, вызывая водянку плода (анемию и отек). [18]
[18]
Приращение плаценты — это когда плацента прорастает слишком далеко в миометрий из-за отсутствия децидуальной оболочки, что позволяет ворсинкам прикрепляться к миометрию. У placenta increta ворсинки погружаются еще глубже в миометрий. Placenta percreta — это когда плацента прорастает всю толщину миометрия и достигает серозной оболочки матки. Это вторжение в миометрий может вызвать кровотечение во время беременности и послеродовые кровотечения.
Здоровая пуповина должна содержать две пупочные артерии и одну пупочную вену. Если есть только одна артерия, у плода могут быть и другие дефекты, такие как задержка роста или генетические аномалии.[21] Также может быть несколько артерий, которые также могут быть связаны с генетическими аномалиями или врожденными дефектами. Также могут быть кисты в пуповине, заполненные жидкостью. Они видны на УЗИ на протяжении всей беременности.[23] Кисты могут рассасываться сами по себе, или, если кист несколько, могут быть и хромосомные аномалии. [24] Редким осложнением кисты может быть перекрут или гематома, которые потенциально могут вызвать гибель плода.[25] Истинные и ложные узлы также являются аномалией пуповины. Ложный узел – это когда сосуды внутри пуповины становятся извилистыми, но в самом пуповине узла нет. Нет никакого неблагоприятного результата, связанного с этим типом узла. Однако настоящий узел может быть опасен для плода. Настоящий узел — это когда пуповина фактически скручивается в узел, который потенциально может привести к гибели плода, если он слишком тугой.
[24] Редким осложнением кисты может быть перекрут или гематома, которые потенциально могут вызвать гибель плода.[25] Истинные и ложные узлы также являются аномалией пуповины. Ложный узел – это когда сосуды внутри пуповины становятся извилистыми, но в самом пуповине узла нет. Нет никакого неблагоприятного результата, связанного с этим типом узла. Однако настоящий узел может быть опасен для плода. Настоящий узел — это когда пуповина фактически скручивается в узел, который потенциально может привести к гибели плода, если он слишком тугой.
В норме пуповина прикрепляется к центру плаценты. Пуповина может аномально имплантироваться как в плод, так и в плаценту. В плаценте может быть оболочечное или краевое прикрепление. Оболочечная вставка — это когда сосуды разделяются по мере их развития между амнионом и хорионом по мере их роста к плаценте. По мере приближения к плаценте они обнажаются и не защищены вартоновым студнем; это может быть опасно, особенно при предлежании сосудов, когда сосуды особенно склонны к разрыву. [28] Краевое прикрепление — это место, где пуповина прикрепляется к краю плаценты. По-прежнему существует повышенный риск предлежания и отслойки плаценты, но не такой высокий, как при прикреплении оболочки [29].][30]
[28] Краевое прикрепление — это место, где пуповина прикрепляется к краю плаценты. По-прежнему существует повышенный риск предлежания и отслойки плаценты, но не такой высокий, как при прикреплении оболочки [29].][30]
Многие патологии плаценты видны при гистологическом исследовании, но некоторые патологии видны макроскопически.[31] Макроскопические патологии включают зеленое обесцвечивание мионекроза мекония, желто-зеленое обесцвечивание при васкулите, абсцессы, оранжевое обесцвечивание при инфаркте плаценты, массы, кисты, тромбы и неполное скопление тканей, указывающее на задержку плаценты. Плаценту можно хранить в холодильнике в свежем виде или помещать в фиксатор, если это необходимо для дальнейшего исследования после родов.
Отслойка плаценты является очень опасным обстоятельством: если это происходит, то на самом деле происходит отслоение плаценты от матки, вызывая сильное кровотечение, ставя под угрозу не только жизнь плода, который недополучает больше кислорода и питательных веществ необходимо, чтобы выжить, но и будущей матери.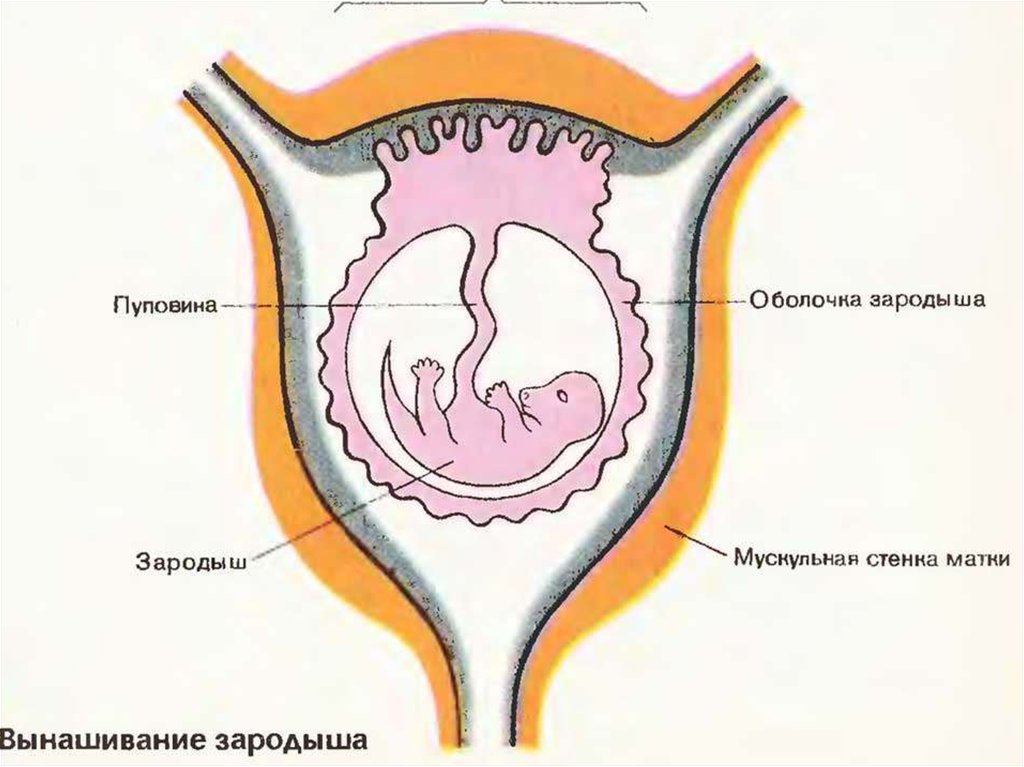 Отслойка плаценты может быть обусловлена: артериальной гипертензией, перерастяжением стенок матки из-за избытка околоплодных вод (многоводием), многоплодной беременностью, сахарным диабетом, употреблением наркотиков.
Отслойка плаценты может быть обусловлена: артериальной гипертензией, перерастяжением стенок матки из-за избытка околоплодных вод (многоводием), многоплодной беременностью, сахарным диабетом, употреблением наркотиков.
Клиническая значимость
Плацента является жизненно важным органом плода, необходимым для здоровой беременности как матери, так и плода. Неполное или нарушенное развитие плаценты также может вызвать аномалии развития плода или нежелательные явления у матери. На ранних сроках гестации можно провести забор плаценты для выявления аномалий развития плода, но эти процедуры сопряжены с риском для здоровья плода. В случае аномального родоразрешения или пороков развития плода плацента может пройти обследование на макроскопический и гистологический анализы.
Большинство заболеваний плаценты можно лечить, предохраняя беременную и плод от тяжелых последствий. Предлежание плаценты: часто низкая плацента возвращается в свое нормальное положение через несколько недель благодаря толчку матки. Если состояние низкой плаценты сохраняется на протяжении всей беременности, настоятельно рекомендуется кесарево сечение. Placenta accreta: для предотвращения риска кровотечения рекомендуется раннее кесарево сечение в течение нескольких недель. В этих случаях нельзя исключать гистерэктомию или удаление матки без исключения будущих беременностей. Возрастная плацента: диета, основанная на витаминах и кальции, и хорошие привычки (например, отказ от курения) предотвращает кальцификацию плаценты. Плацентарная недостаточность: специфического лечения этого типа проблемы не существует. Хорошо проходить периодические проверки рядом друг с другом, чтобы следить за развитием плода, а также, где это возможно, лечить поведение или патологию беременной. Отслойка плаценты: в зависимости от типа отслойки будет оцениваться гипотеза наблюдения за пациенткой с просьбой о полном покое или, как в большинстве случаев, продолжения кесарева сечения, в зависимости от срока беременности.
Если состояние низкой плаценты сохраняется на протяжении всей беременности, настоятельно рекомендуется кесарево сечение. Placenta accreta: для предотвращения риска кровотечения рекомендуется раннее кесарево сечение в течение нескольких недель. В этих случаях нельзя исключать гистерэктомию или удаление матки без исключения будущих беременностей. Возрастная плацента: диета, основанная на витаминах и кальции, и хорошие привычки (например, отказ от курения) предотвращает кальцификацию плаценты. Плацентарная недостаточность: специфического лечения этого типа проблемы не существует. Хорошо проходить периодические проверки рядом друг с другом, чтобы следить за развитием плода, а также, где это возможно, лечить поведение или патологию беременной. Отслойка плаценты: в зависимости от типа отслойки будет оцениваться гипотеза наблюдения за пациенткой с просьбой о полном покое или, как в большинстве случаев, продолжения кесарева сечения, в зависимости от срока беременности.
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.

Комментарий к этой статье.
Рисунок
Развитие плодной оболочки и плаценты, Диаграмма, показывающая расширение амниона и разграничение пупка, Сердце, Передняя кишка, Эмбрион, Амниотическая полость, Плацентарные ворсинки. Предоставлено Gray’s Anatomy Plates
Рисунок
Развитие плодной оболочки и плаценты. Схема поперечного сечения, показывающая способ формирования амниона у цыпленка. Амниотические складки почти слились по средней линии, эктодерма синего цвета — мезодерма; красный – энтодерма (подробнее…)
Рисунок
Развитие оболочек плода и плаценты, Модель человеческого эмбриона длиной 1,3 мм, Нервный канал, Нервная борозда, Амнион, Стебель тела, Желточные вены, Энтодерма, Спланхническая мезодерма, Желточный мешок, Соматическая мезодерма. Предоставлено Gray’s Anatomy Plates (подробнее…)
Рисунок
Развитие оболочек плода и плаценты, схема плацентарного кровообращения, маргинальный синус, хорион, амнион, трофобласт, пупочные артерии и вены пуповины. Предоставлено Grey’s Anatomy Plates
Предоставлено Grey’s Anatomy Plates
Рисунок
На рисунке показана человеческая плацента. Предоставлено Бруно Бордони, доктором философии.
Ссылки
- 1.
Burton GJ, Jauniaux E. Что такое плацента? Am J Obstet Gynecol. 2015 окт; 213 (4 Дополнение): S6.e1, S6-8. [PubMed: 26428504]
- 2.
Гуттмахер А.Е., Мэддокс Ю.Т., Спонг С.Ю. Проект «Человеческая плацента»: структура, развитие и функция плаценты в режиме реального времени. Плацента. 2014 май; 35(5):303-4. [Бесплатная статья PMC: PMC3999347] [PubMed: 24661567]
- 3.
Wamaitha SE, Niakan KK. Предгаструляционное развитие человека. Curr Top Dev Biol. 2018;128:295-338. [PubMed: 29477167]
- 4.
Мэтр JL. Механика морфогенеза бластоцисты. Биол Клетка. 2017 сен; 109 (9): 323-338. [PubMed: 28681376]
- 5.
Солница-Крезель Л., Сепич Д.С. Гаструляция: создание и формирование зародышевых листков.
 Annu Rev Cell Dev Biol. 2012;28:687-717. [В паблике: 22804578]
Annu Rev Cell Dev Biol. 2012;28:687-717. [В паблике: 22804578]- 6.
Favaron PO, Carvalho RC, Borghesi J, Anunciação AR, Miglino MA. Амниотическая мембрана: разработка и возможные применения — обзор. Репрод Дом Аним. 2015 декабрь; 50 (6): 881-92. [PubMed: 26510939]
- 7.
Labarrere CA, DiCarlo HL, Bammerlin E, Hardin JW, Kim YM, Chaemsaithong P, Haas DM, Kassab GS, Romero R. Отказ физиологической трансформации спиральных артерий, эндотелиальных и активация клеток трофобласта и острый атероз базальной пластинки плаценты. Am J Obstet Gynecol. 2017 март; 216(3):287.e1-287.e16. [Бесплатная статья PMC: PMC5881902] [PubMed: 28034657]
- 8.
Hahn D, Blaschitz A, Korgun ET, Lang I, Desoye G, Skofitsch G, Dohr G. От глюкозы матери к гликогену плода: экспрессия ключевых регуляторов в организме человека плацента. Мол Хум Репрод. 2001 г., декабрь 7(12):1173-8. [PubMed: 11719595]
- 9.
Herrera E, Amusquivar E, López-Soldado I, Ortega H.
 Метаболизм липидов у матери и перенос липидов через плаценту. Горм Рез. 2006; 65 Дополнение 3:59-64. [PubMed: 16612115]
Метаболизм липидов у матери и перенос липидов через плаценту. Горм Рез. 2006; 65 Дополнение 3:59-64. [PubMed: 16612115]- 10.
Neu N, Duchon J, Zachariah P. Инфекции TORCH. Клин Перинатол. 2015 март;42(1):77-103, viii. [PubMed: 25677998]
- 11.
Каплан К. Гросс Исследование плаценты. Сург Патол Клин. 2013 март;6(1):1-26. [PubMed: 26838700]
- 12.
Браунбилл П., Махендран Д., Оуэн Д., Суонсон П., Торнбург К.Л., Нельсон Д.М., Сибли К.П. Денудации как парацеллюлярные пути альфафетопротеина и креатинина через синцитиотрофобласт человека. Am J Physiol Regul Integr Comp Physiol. 2000 март; 278(3):R677-83. [В паблике: 10712288]
- 13.
Картер А.М. Факторы, влияющие на транспорт газов через плаценту и снабжение плода кислородом. Дж Дев Физиол. 1989 Декабрь; 12 (6): 305-22. [PubMed: 2701106]
- 14.
Сибли С.П., Браунбилл П., Глейзер Д.Д., Гринвуд С.Л. Необходимы знания об обменной физиологии плаценты.
 Плацента. 2018 Апрель;64 Дополнение 1:S9-S15. [PubMed: 29370939]
Плацента. 2018 Апрель;64 Дополнение 1:S9-S15. [PubMed: 29370939]- 15.
Вапнер Р.Дж. Биопсия хориона. Obstet Gynecol Clin North Am. 1997 марта; 24(1):83-110. [PubMed: 9086520]
- 16.
Sileo FG, Curado J, Bhide A. Обзор современной клинической практики взятия проб ворсин хориона. Пренат Диагн. 2019 март; 39(4):299-302. [PubMed: 30682214]
- 17.
Baird PA, Yee IM, Sadovnick AD. Популяционное исследование отдаленных результатов после амниоцентеза. Ланцет. 1994 г., 22 октября; 344 (8930): 1134-6. [PubMed: 7934498]
- 18.
ALLEN FH, DIAMOND LK. Эритробластоз плода. N Engl J Med. 1957 10 октября; 257(15):705-12 продолжение. [PubMed: 13477375]
- 19.
Khong TY. Патология приращения плаценты, всемирная эпидемия. Джей Клин Патол. 2008 декабрь; 61 (12): 1243-6. [PubMed: 18641410]
- 20.
Piñas Carrillo A, Chandraharan E. Спектр приращения плаценты: факторы риска, диагностика и лечение с особым вниманием к процедуре Triple P.
 Женское здоровье (Лондон). 2019 янв-декабрь;15:1745506519878081. [Бесплатная статья PMC: PMC6777059] [PubMed: 31578123]
Женское здоровье (Лондон). 2019 янв-декабрь;15:1745506519878081. [Бесплатная статья PMC: PMC6777059] [PubMed: 31578123]- 21.
Ghezzi F, Raio L, Di Naro E, Franchi M, Cromi A, Dürig P. Одиночные и множественные кисты пуповины на ранних сроках беременности: два разных образования. УЗИ Акушерство Гинекол. 2003 март; 21(3):215-9. [PubMed: 12666213]
- 22.
Бек Р., Наулти СМ. Пуповина человека с четырьмя артериями. Клин Педиатр (Фила). 1985 февраля; 24 (2): 118-9. [PubMed: 3967448]
- 23.
Аоки С., Хата Т., Ариюки Ю., Макихара К., Хата К., Китао М. Антенатальная диагностика аберрантных пупочных сосудов. Гинеколь Обстет Инвест. 1997;43(4):232-5. [PubMed: 9194620]
- 24.
Сепульведа В., Рейес М., Гонсалвеш Л.Ф. Две необычные аномалии пупочных сосудов у плода с трисомией 18. Prenat Diagn. 1998 октября; 18 (10): 1098-9. [PubMed: 9826906]
- 25.
Sepulveda W, Wong AE, Gonzalez R, Vasquez P, Gutierrez J.
 Смерть плода из-за гематомы пуповины: редкое осложнение кисты пуповины. J Matern Fetal Neonatal Med. 2005 Декабрь; 18 (6): 387-90. [PubMed: 16390804]
Смерть плода из-за гематомы пуповины: редкое осложнение кисты пуповины. J Matern Fetal Neonatal Med. 2005 Декабрь; 18 (6): 387-90. [PubMed: 16390804]- 26.
Гембрух Ю, Башат АА. Истинный узел пуповины: транзиторный констриктивный эффект на кровоток в пупочной вене, продемонстрированный с помощью допплерографии. УЗИ Акушерство Гинекол. 1996 г., июль; 8 (1): 53-6. [PubMed: 8843621]
- 27.
Hertzberg BS, Bowie JD, Bradford WD, Bolick D. Ложный узел пуповины: сонографический вид и дифференциальный диагноз. Дж. Клин Ультразвук. 1988 окт; 16 (8): 599-602. [PubMed: 3152409]
- 28.
Rocha J, Carvalho J, Costa F, Meireles I, do Carmo O. Вставка пуповины при одноплодной беременности: невыясненная причина экстренного кесарева сечения — клинический случай. Деловой представитель Акушер-гинеколог. 2012;2012:308206. [Бесплатная статья PMC: PMC3517836] [PubMed: 23243528]
- 29.
Nkwabong E, Njikam F, Kalla G.
 Исходы беременностей с маргинальной вставкой пуповины. J Matern Fetal Neonatal Med. 2021 апр;34(7):1133-1137. [PubMed: 31164018]
Исходы беременностей с маргинальной вставкой пуповины. J Matern Fetal Neonatal Med. 2021 апр;34(7):1133-1137. [PubMed: 31164018]- 30.
Эббинг С., Кисеруд Т., Джонсен С.Л., Альбрехтсен С., Расмуссен С. Распространенность, факторы риска и исходы прикрепления оболочечной и маргинальной пуповины: популяционное исследование 634 741 беременности. ПЛОС Один. 2013;8(7):e70380. [Бесплатная статья PMC: PMC3728211] [PubMed: 23936197]
- 31.
Kaplan CG. Макроскопическая патология плаценты: масса, форма, размер, цвет. Джей Клин Патол. 2008 г., декабрь 61(12):1285-95. [PubMed: 18708423]
- 32.
Робертс Диджей. Плацентарная патология, руководство по выживанию. Arch Pathol Lab Med. 2008 г., апрель; 132(4):641-51. [PubMed: 18384216]
Плацента и плацента.
Плацента является жизненно важным соединительным органом между материнской маткой и плодом.
Поддерживает развивающийся плод внутриутробно, снабжая его питательными веществами, удаляя продукты жизнедеятельности плода и обеспечивая газообмен через кровоснабжение матери.
В этой статье мы рассмотрим развитие плаценты.
Автор BruceBlaus [CC BY-SA 4.0], с Викисклада
Рисунок 1. Плацента поддерживает развивающийся плод в утробе матери.
До имплантацииРазвитие плаценты начинается во время имплантации бластоцисты .
Бластоциста из 32-64 клеток содержит два различных дифференцированных типа эмбриональных клеток: внешние клетки трофобласта и внутреннюю клеточную массу. Клетки трофобласта образуют плаценту. Внутренняя клеточная масса образует плод и плодные оболочки.
Имплантация На 6 -й -й день, когда распадается блестящая оболочка, бластоциста «вылупляется», что позволяет осуществить имплантацию. Клетки трофобласта взаимодействуют с децидуальным эпителием эндометрия, обеспечивая инвазию в клетки материнской матки.
Затем эмбрион секретирует протеазы, обеспечивающие глубокую инвазию в строму матки. Имплантация интерстициальная. В норме имплантация происходит на передней или задней стенке тела матки. Наиболее частым местом эктопической имплантации является ампула фаллопиевой трубы.
На 8 -й -й день развития клетки трофобласта дифференцируются в наружный многоядерный синцитиотрофобласт , разрушающий материнские ткани путем выброса отростков, и внутренний одноядерный цитотрофобласт, активно пролиферирующий.
Синцитиотрофобласт отвечает за выработку гормонов, таких как Хорионический гонадотропин человека (ХГЧ), ко второй неделе беременности, который используется при тестировании на беременность.
После имплантации На 9-й день внутри синцитиотрофобласта образуются лакуны или пространства. Синцитиотрофобласт также разрушает материнские ткани, позволяя материнской крови из маточных спиральных артерий попадать в лакунарную сеть. Таким образом, к концу 2-й недели устанавливается ранняя маточно-плацентарная циркуляция.
Таким образом, к концу 2-й недели устанавливается ранняя маточно-плацентарная циркуляция.
Тем временем цитотрофобласт начинает формировать первичные хорионические ворсинки (пальцеобразные выросты), которые проникают и расширяются в окружающий синцитиотрофобласт. В 3 rd неделя в эти ворсинки врастает экстраэмбриональная мезодерма, образуя ядро из рыхлой соединительной ткани, после чего эти структуры называются вторичными ворсинками хориона.
К концу третьей недели в эмбриональной мезодерме вторичных ворсин хориона начинают формироваться эмбриональные сосуды, превращая их в третичные ворсины хориона.
Клетки цитотрофобласта из третичных ворсинок растут по направлению к базальной децидуальной оболочке материнской матки и распространяются по ней, образуя цитотрофобластическую оболочку. Ворсинки, соединенные с базальной децидуальной оболочкой через цитотрофобластическую оболочку, известны как анкерные ворсинки .
Ворсинки, растущие наружу в межворсинчатом пространстве от стволовых (закрепляющих) ворсин, называются ветвящимися ворсинками и обеспечивают площадь поверхности для обмена метаболитами между матерью и плодом. Представление ворсинок в виде древовидных выступов может помочь визуализировать их структуру.
Налаживание кровообращенияСпиральные артерии матери подвергаются ремоделированию для создания условий с низким сопротивлением и высоким кровотоком для удовлетворения потребностей плода. Клетки цитотрофобласта проникают в спиральные артерии матери и замещают эндотелий матери. Они подвергаются эпителиально-эндотелиальной дифференцировке, что увеличивает диаметр и снижает резистентность сосудов.
Преэклампсия – это трофобластическое заболевание, связанное с неудачной или неполной дифференцировкой цитотрофобластических клеток во время трансформации эпителия в эндотелий.
Генри Вандайк Картер — Генри Грей (1918) Анатомия человеческого тела (см. Раздел «Книга» ниже) Bartleby.com: Анатомия Грея, табличка 39, Public Domain, https://commons.wikimedia.org/w/index.php?curid=792233
Раздел «Книга» ниже) Bartleby.com: Анатомия Грея, табличка 39, Public Domain, https://commons.wikimedia.org/w/index.php?curid=792233
-13 нед) поверхность ворсин хориона образована синцитиотрофобластом. Эти клетки лежат на слое цитотрофобластических клеток, которые, в свою очередь, покрывают сердцевину сосудистой мезодермы. Поэтому плацентарный барьер относительно толстый.
Площадь обменной поверхности резко увеличивается к доношенным (27-40 недель). Плацентарный барьер намного тоньше, и слой цитотрофобласта под синцитиотрофобластом утрачен.
Плацентарный барьер не является истинным барьером, поскольку он позволяет многим веществам проходить между кровотоком матери и плода. К сожалению, это означает, что различные наркотики (например, героин, кокаин) и вирусы (например, ЦМВ, краснуха, корь) могут попасть в кровоток плода. Поскольку материнская кровь в межворсинчатых пространствах отделена от крови плода хорионическими производными, человеческая плацента известна как гемохориальный тип .
Второй и третий триместры
По мере развития беременности лобный хорион («густой» хорион) формируется по мере развития большего количества ворсинок на эмбриональном полюсе. На поверхности плода плацента покрыта хорионической пластиной ; с материнской стороны она граничит с базальной децидуальной оболочкой, децидуальная пластинка которой наиболее тесно прилегает к плаценте.
В течение четвертого и пятого месяцев децидуальная оболочка образует децидуальные перегородки , которые выступают в межворсинчатое пространство, но не соединяются с пластинкой хориона. Эти перегородки имеют сердцевину из материнской ткани, но покрыты слоем синцитиальных клеток. Во все времена имеется синцитиальный слой, отделяющий материнскую кровь в межворсинчатых озерах от фетальной ткани ворсинок. Перегородки делят плаценту на отсеки, называемые семядолями. Семядоли получают кровоснабжение через 80-100 спиральных артерий, которые пронизывают децидуальную пластинку.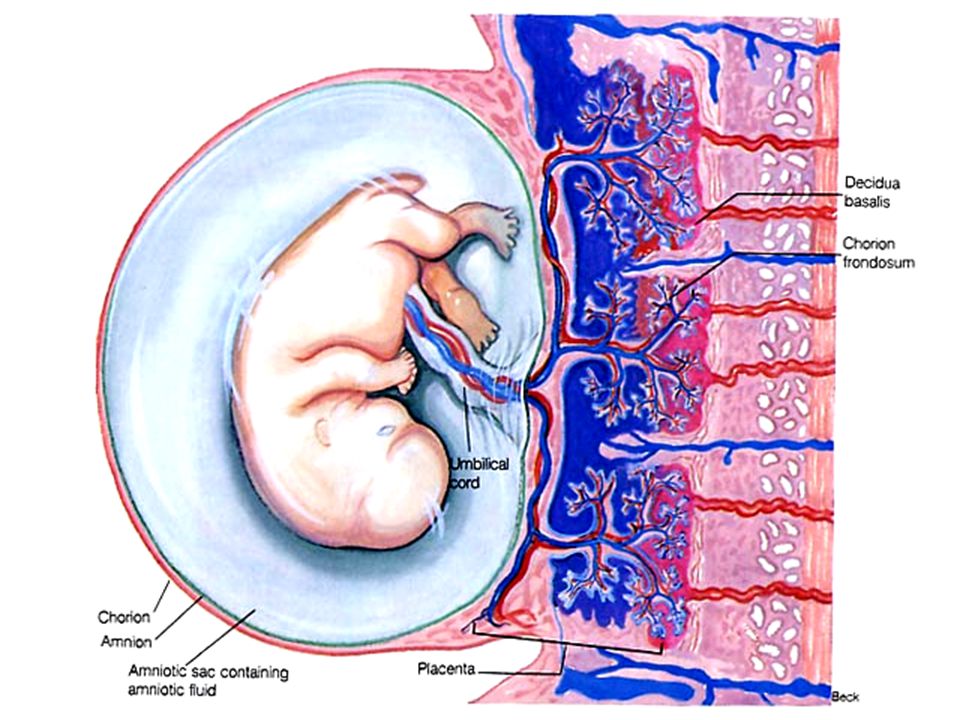
Авторы: Habj и Ravedave (в сочетании с Hairy Dude) — простая комбинация: изображение: человеческая плацента, детская сторона.jpg и: изображение: человеческая плацента, маточная сторона.jpg., Public Domain, https://commons.wikimedia.org/ ж/index.php?curid=6454988
Рисунок 3. Плацента человека, материнская сторона (внизу) и сторона плода (вверху)
Доношенная плацентаВ доношенном состоянии плацента имеет дисковидную форму диаметром 15-25 см, приблизительно Толщина 3 см, вес около 500-600 г. При рождении он отрывается от стенки матки и примерно через 30 минут после рождения ребенка выталкивается из полости матки.
Материнская сторона будет иметь 15-20 выпуклых областей, которые представляют собой семядоли, покрытые тонким слоем базальной децидуальной оболочки. Полностью сформировавшаяся плацента содержит межворсинчатые озера. Эти структуры вмещают около 150 мл материнской крови. Это обновляется 3-4 раза в минуту.
Пластинка хориона покрывает поверхность плода. Сосуды хориона сходятся к пуповине . Это ряд крупных артерий и вен. Амнион покрывает слой хориона. Пуповина обычно прикрепляется посередине плаценты, перпендикулярно ей. оболочечное прикрепление может возникнуть, если пуповина прикрепляется вне плаценты, но это бывает редко.
Конец беременности
Целью изменений, происходящих в плаценте в конце беременности, является снижение обмена между кровообращением матери и плода. Эти изменения заключаются в следующем:
- Увеличение фиброзной ткани в ядре ворсинки
- Утолщение базальных мембран капилляров плода
- Облитерирующие изменения мелких капилляров ворсинок
- Отложение фибриноида на поверхности ворсин в зоне перехода и в пластинке хориона.
Отложение фибриноидов приводит к инфаркту межворсинчатого озера или иногда всей семядоли, которая впоследствии становится беловатой.
 // Am J Reprod Immunol — 2021 — Vol — NNULL — p.e13434; PMID:33905581
// Am J Reprod Immunol — 2021 — Vol — NNULL — p.e13434; PMID:33905581 ; PMID:33903031
; PMID:33903031
 Annu Rev Cell Dev Biol. 2012;28:687-717. [В паблике: 22804578]
Annu Rev Cell Dev Biol. 2012;28:687-717. [В паблике: 22804578]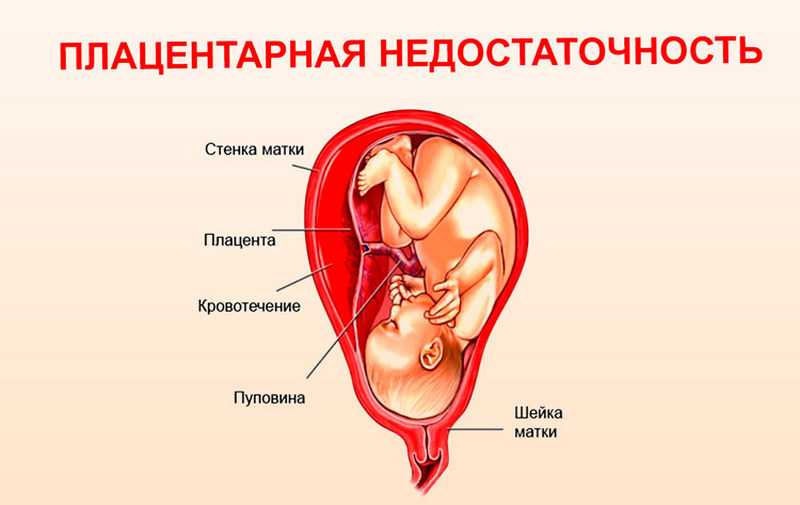 Метаболизм липидов у матери и перенос липидов через плаценту. Горм Рез. 2006; 65 Дополнение 3:59-64. [PubMed: 16612115]
Метаболизм липидов у матери и перенос липидов через плаценту. Горм Рез. 2006; 65 Дополнение 3:59-64. [PubMed: 16612115] Плацента. 2018 Апрель;64 Дополнение 1:S9-S15. [PubMed: 29370939]
Плацента. 2018 Апрель;64 Дополнение 1:S9-S15. [PubMed: 29370939] Женское здоровье (Лондон). 2019 янв-декабрь;15:1745506519878081. [Бесплатная статья PMC: PMC6777059] [PubMed: 31578123]
Женское здоровье (Лондон). 2019 янв-декабрь;15:1745506519878081. [Бесплатная статья PMC: PMC6777059] [PubMed: 31578123]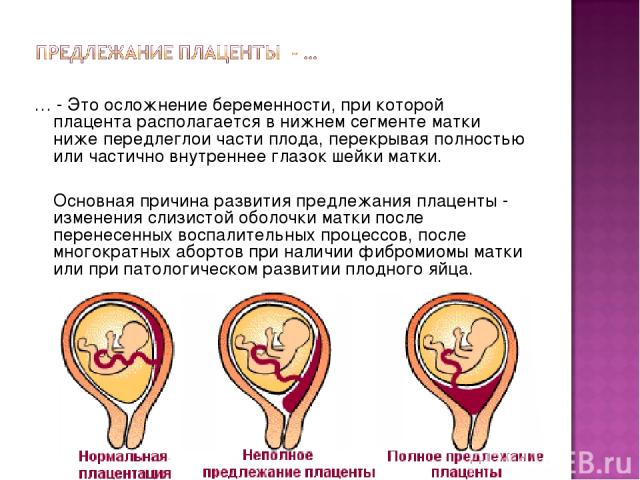 Смерть плода из-за гематомы пуповины: редкое осложнение кисты пуповины. J Matern Fetal Neonatal Med. 2005 Декабрь; 18 (6): 387-90. [PubMed: 16390804]
Смерть плода из-за гематомы пуповины: редкое осложнение кисты пуповины. J Matern Fetal Neonatal Med. 2005 Декабрь; 18 (6): 387-90. [PubMed: 16390804] Исходы беременностей с маргинальной вставкой пуповины. J Matern Fetal Neonatal Med. 2021 апр;34(7):1133-1137. [PubMed: 31164018]
Исходы беременностей с маргинальной вставкой пуповины. J Matern Fetal Neonatal Med. 2021 апр;34(7):1133-1137. [PubMed: 31164018]